一种微胶囊及其制备方法和应用与流程
1.本发明属于微胶囊技术领域,涉及一种微胶囊及其制备方法和应用。
背景技术:
2.火麻仁是桑科大麻属植物大麻的干燥成熟种子,其药用始见于《神农本草经》,具有滑肠、涧燥、活血、通淋之功效。火麻仁中含丰富的脂肪酸、单不饱和脂肪酸以及多元不饱和脂肪酸等,据统计,不饱和脂肪酸组分占总脂肪酸含量90%以上,而亚油酸占不饱和脂肪酸的50%~60%,亚麻酸(能够转化成epa和dha)占不饱和脂肪酸的20%~30%,火麻籽仁中ω-6型与ω-3型不饱和脂肪酸的比例为(2.29~3.68):1.00,与世界卫生组织和联合国粮农组织推荐比例接近,该比例与人体正常代谢所需比例一致,对人体健康最佳。火麻仁油是火麻仁经过物理冷榨或亚临界低温萃取制出的一种植物油。
3.维生素e是人体必需的一类营养成分,能保护机体细胞膜及生命大分子免遭自由基的攻击,是一类高效安全的天然抗氧化剂,在延缓衰老、防治心血管疾病、抗肿瘤方面具有良好的效果。随着营养学与病理学研究的深入,维生素e更多新功能被不断发现和得到证实,其作用越来越受到人们的重视。
4.火麻仁油和维生素e均属于油溶性的热敏物质,难以均匀的添加到水溶性产品中,且结构易被紫外线、碱以及氧化等因素破坏,需要封闭、避光保存,因此二者的广泛应用受到了一定的限制。
5.cn103054045a公开了具有降血脂功能的保健植物油脂组合物,所述组合物包括:火麻仁油40~50%、亚麻籽油40~50%、核桃油5~6%、红花籽油3.5~6%和维生素e 0.45~0.55%,具备一定的降低血脂效果,但稳定性较差。
6.综上所述,提供一种富含火麻仁油和维生素e的微胶囊,具备高稳定性和优良降血脂效果,对于火麻仁油和维生素e的广泛应用具有重要意义。
技术实现要素:
7.针对现有技术的不足和实际需求,本发明提供一种微胶囊及其制备方法和应用,所述微胶囊富含火麻仁油和维生素e两种营养物质,稳定性高,且具备降血脂、增强心血管、提高免疫力以及延缓人体衰老等多种功效。
8.为达上述目的,本发明采用以下技术方案:
9.第一方面,本发明提供一种微胶囊,所述微胶囊包括芯材和壁材,所述芯材包括火麻仁油和维生素e。
10.本发明的微胶囊中,火麻仁油含有丰富的不饱和脂肪酸,具有降血脂、调节心脏功能、降低血液粘稠度、改善血液微循环、提高脑细胞的活性以及增强人体防御系统等功效;维生素e中含有丰富的生育酚,有效阻止胞内氧化应激,抑制胆固醇的合成;维生素e作为高活性的抗氧化剂可以有效地捕获氧化自由基或过氧化自由基,而火麻仁油作为低活性抗氧化剂能够为其供给氢原子,使维生素e再生,火麻仁油和维生素e相互配合,降低了微胶囊的
氧化变性水平,提高了微胶囊的稳定性,具有降血脂、提高免疫力以及延缓人体衰老的功效。
11.优选地,所述火麻仁油和维生素e的质量比为(1~13):1,包括但不限于2:1、2.5:1、3:1、3.5:1、4:1、5.5:1、6:1、7:1、8:1、9:1、10:1、11:1或12:1。
12.本发明中,通过控制火麻仁油和维生素e的质量比为(1~13):1,能够显著增强微胶囊的降血脂功效。
13.优选地,所述芯材和壁材的质量比为1:(1.5~6),包括但不限于1:1.6、1:1.8、1:2、1:3、1:4.5、1:5、1:5.4、1:5.6或1:5.8。
14.优选地,所述火麻仁油中多不饱和脂肪酸含量为75%~100%,包括但不限于78%、80%、85%、88%、90%、92%、94%、96%或98%。
15.优选地,所述维生素e为天然维生素e。
16.优选地,所述维生素e中生育酚含量不低于90%,包括但不限于91%、92%、95%、96%或98%。
17.优选地,所述壁材包括碳水化合物类物质。
18.优选地,所述碳水化合物类物质包括变性淀粉、壳聚糖、麦芽糊精、阿拉伯胶或菊糖中的任意一种或至少两种的组合,其中典型但非限制性的组合包括壳聚糖和麦芽糊精的组合、阿拉伯胶和菊糖的组合或壳聚糖和菊糖的组合。
19.优选地,所述变性淀粉包括辛烯基琥珀酸淀粉酯(osa淀粉)、改性木薯淀粉或改性糯玉米淀粉中的任意一种或至少两种的组合,其中典型但非限制性的组合包括辛烯基琥珀酸酯淀粉和改性木薯淀粉的组合或改性木薯淀粉和改性糯玉米淀粉的组合。
20.本发明中,通过使用天然或人工合成的高分子壁材物质将火麻仁油和维生素e进行封存而形成微胶囊,可保护囊内火麻仁油和维生素e的物理状态、化学活性成分,并且能控制其缓释。
21.第二方面,本发明提供一种第一方面所述的微胶囊的制备方法,所述制备方法包括:
22.制备壁材溶液,按比例将火麻仁油、维生素e和壁材溶液混合,进行高压均质和干燥处理,获得所述微胶囊。
23.优选地,所述制备壁材溶液包括将壁材与水混合,加热并搅拌均匀,获得壁材溶液。
24.优选地,所述加热的温度为50~60℃,包括但不限于51℃、52℃、55℃、56℃或58℃。
25.优选地,所述高压均质包括使用高压均质机以180~250bar的压力均质2~3次,所述压力包括但不限于190bar、200bar、210bar、220bar或240bar,再以400~550bar的压力均质3~5次,所述压力包括但不限于410bar、450bar、480bar、500bar或540bar。
26.优选地,所述干燥处理包括喷雾干燥。
27.优选地,所述喷雾干燥的进风温度为170~220℃,包括但不限于171℃、175℃、178℃、180℃、190℃、200℃、210℃或215℃。
28.优选地,所述喷雾干燥的出风温度为70~80℃,包括但不限于71℃、72℃、74℃、76℃或78℃。
29.优选地,所述喷雾干燥的进料速度为0.5~1l/h,包括但不限于0.6l/h、0.7l/h、0.8l/h或0.9l/h。
30.作为优选的技术方案,所述微胶囊的制备方法包括以下步骤:
31.(1)将壁材与水混合,加热至50~60℃,搅拌均匀,得到壁材溶液;
32.(2)按比例将火麻仁油、维生素e和所述壁材溶液混合,搅拌均混匀;以180~250bar的压力均质2~3次,再以400~550bar的压力均质3~5次,得到乳浊液;
33.(3)将所述乳浊液保持温度在50~60℃进行喷雾干燥,进风温度为170~220℃,出风温度为70~80℃,进料速度为0.5~1l/h,得到所述微胶囊。
34.第三方面,本发明提供第一方面所述的微胶囊在制备降血脂药物中的应用。
35.与现有技术相比,本发明具有以下有益效果:
36.(1)本发明的微胶囊中,火麻仁油和维生素e相互配合,降低了微胶囊的氧化变性水平,提高了微胶囊的稳定性,且增强了微胶囊的降血脂、提高免疫力以及延缓人体衰老的功效;
37.(2)本发明控制微胶囊中火麻仁油和维生素e的质量比为(1~13):1,能够进一步增强微胶囊降血脂的能力;
38.(3)本发明的微胶囊能够有效抵抗氧化变性,并降低血脂三项指标(tc、tg和ldl)。
附图说明
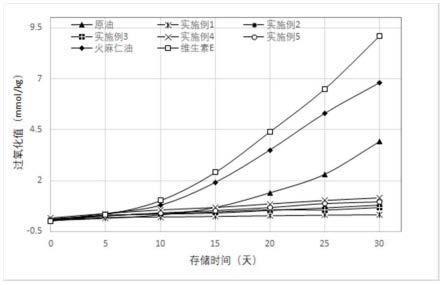
39.图1为各样品过氧化值变化趋势图。
具体实施方式
40.为进一步阐述本发明所采取的技术手段及其效果,以下结合实施例和附图对本发明作进一步地说明。可以理解的是,此处所描述的具体实施方式仅仅用于解释本发明,而非对本发明的限定。
41.实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
42.本发明中,相关指标检测方法如下所示:
43.含水量:采用美国分析化学家协会(association of official analytical chemists)标准测定微胶囊的水分含量,将样品置于105℃烘箱内干燥至恒重,根据其质量损失计算水分含量(%);
44.表面油:含火麻仁油和维生素e的微胶囊表面游离的油量占该微胶囊的总质量的百分数,含火麻仁油和维生素e的微胶囊的表面油易溶于30~60℃石油醚,而微胶囊其他成分不溶于30~60℃石油醚,采用30~60℃石油醚即可分离表面油和微胶囊,从而获得表面油质量;
45.包埋率:是指微胶囊内火麻仁油和维生素e的质量占所加入的火麻仁油和维生素e总量的百分数,计算公式如式(1)所示;
46.包埋率(%)=(总油质量-表面油质量)/总油质量
×
100%
ꢀꢀꢀꢀꢀꢀꢀ
(1)
47.过氧化值:过氧化值测定方法参照gb 5009.227-2016动植物油脂过氧化值测定方
法。
48.本发明实施例中,火麻仁油(多不饱和脂肪酸含量95%,云南汉盟制药有限公司),维生素e(生育酚含量96%,宁波大红鹰生物工程股份有限公司),osa淀粉购买于西安拉维亚生物科技有限公司,改性木薯淀粉、改性糯玉米淀粉购、菊糖、麦芽糊精、壳聚糖和阿拉伯胶均购买于四川华堂聚瑞生物科技有限。
49.实施例1
50.本实施例提供一种微胶囊,所述微胶囊的配方如表1所示。
51.表1
52.名称质量百分比osa淀粉50%菊糖10%火麻仁油20%维生素e20%
53.所述微胶囊的制备方法包括以下步骤:
54.(1)按比例将osa淀粉、菊糖与水混合(固形物含量约20%),加热至50℃,搅拌均匀,得到壁材溶液;
55.(2)按比例将火麻仁油、维生素e和所述壁材溶液混合,搅拌均混匀;以180bar的压力均质3次,再以550bar的压力均质3次,得到乳浊液;
56.(3)将所述乳浊液保持温度在50℃进行喷雾干燥,进风温度为170℃,出风温度为80℃,进料速度为0.5l/h,得到所述微胶囊。
57.测得所述微胶囊含水量为1.98%,表面油为3.51(g/100g微胶囊粉末),包埋率为88.1%,过氧化值为0.03mmol/kg。
58.实施例2
59.本实施例提供一种微胶囊,所述微胶囊的配方如表2所示。
60.表2
61.名称质量百分比osa淀粉34%麦芽糊精33%火麻仁油30%维生素e3%
62.所述微胶囊的制备方法包括以下步骤:
63.(1)按比例将osa淀粉、麦芽糊精与水混合(固形物含量约20%),加热至60℃,搅拌均匀,得到壁材溶液;
64.(2)按比例将火麻仁油、维生素e和所述壁材溶液混合,搅拌均混匀;以250bar的压力均质2次,再以400bar的压力均质5次,得到乳浊液;
65.(3)将所述乳浊液保持温度在60℃进行喷雾干燥(sd-1500喷雾仪干燥机,上海沃迪智能装配股份有限公司),进风温度为220℃,出风温度为70℃,进料速度为1l/h,得到所述微胶囊。
66.测得所述微胶囊含水量为1.67%,表面油为1.12(g/100g微胶囊粉末),包埋率为
95.8%,过氧化值为0.10mmol/kg。
67.实施例3
68.本实施例提供一种微胶囊,所述微胶囊的配方如表3所示。
69.表3
70.名称比例改性木薯淀粉40%壳聚糖40%火麻仁油16%维生素e4%
71.所述微胶囊的制备方法包括以下步骤:
72.(1)按比例将改性木薯淀粉、壳聚糖与水混合(固形物含量约20%),加热至60℃,搅拌均匀,得到壁材溶液;
73.(2)按比例将火麻仁油、维生素e和所述壁材溶液混合,搅拌均混匀;以220bar的压力均质3次,再以400bar的压力均质5次,得到乳浊液;
74.(3)将所述乳浊液保持温度在55℃进行喷雾干燥(sd-1500喷雾仪干燥机,上海沃迪智能装配股份有限公司),进风温度为220℃,出风温度为80℃,进料速度为1l/h,得到所述微胶囊。
75.测得所述微胶囊含水量为1.52%,表面油为2.07(g/100g微胶囊粉末),包埋率为91.8%,过氧化值为0.14mmol/kg。
76.实施例4
77.本实施例提供一种微胶囊,所述微胶囊的配方如表4所示。
78.表4
79.名称质量百分比阿拉伯胶60%麦芽糊精26%火麻仁油13%维生素e1%
80.所述微胶囊的制备方法包括以下步骤:
81.(1)按比例将阿拉伯胶、麦芽糊精与水混合(固形物含量约20%),加热至60℃,搅拌均匀,得到壁材溶液;
82.(2)按比例将火麻仁油、维生素e和所述壁材溶液混合,搅拌均混匀;以200bar的压力均质3次,再以450bar的压力均质5次,得到乳浊液;
83.(3)将所述乳浊液保持温度在55℃进行喷雾干燥(sd-1500喷雾仪干燥机,上海沃迪智能装配股份有限公司),进风温度为210℃,出风温度为75℃,进料速度为0.8l/h,得到所述微胶囊。
84.测得所述微胶囊含水量为1.52%,表面油为1.86(g/100g微胶囊粉末),包埋率为93.5%,过氧化值为0.15mmol/kg。
85.实施例5
86.本实施例提供一种微胶囊,所述微胶囊的配方如表5所示。
87.表5
[0088][0089][0090]
所述微胶囊的制备方法包括以下步骤:
[0091]
(1)按比例将改性糯玉米淀粉、壳聚糖、麦芽糊精与水混合(固形物含量约20%),加热至60℃,搅拌均匀,得到壁材溶液;
[0092]
(2)按比例将火麻仁油、维生素e和所述壁材溶液混合,搅拌均混匀;以210bar的压力均质3次,再以480bar的压力均质5次,得到乳浊液;
[0093]
(3)将所述乳浊液保持温度在55℃进行喷雾干燥(sd-1500喷雾仪干燥机,上海沃迪智能装配股份有限公司),进风温度为200℃,出风温度为75℃,进料速度为0.7l/h,得到所述微胶囊。
[0094]
测得所述微胶囊含水量为1.73%,表面油为1.18(g/100g微胶囊粉末),包埋率为96.2%,过氧化值为0.08mmol/kg。
[0095]
实施例6
[0096]
本实施例提供一种微胶囊,所述微胶囊的配方如表6所示。
[0097]
表6
[0098]
名称质量百分比osa淀粉47%菊糖9%火麻仁油20%维生素e24%
[0099]
所述微胶囊的制备方法与实施例1相同。
[0100]
测得所述微胶囊含水量为2.28%,表面油为4.41(g/100g微胶囊粉末),包埋率为86.5%,过氧化值为0.02mmol/kg。
[0101]
实施例7
[0102]
本实施例提供一种微胶囊,所述微胶囊的配方如表7所示。
[0103]
表7
[0104]
名称质量百分比阿拉伯胶59%
麦芽糊精25%火麻仁油15%维生素e1%
[0105]
所述微胶囊的制备方法与实施例4相同。
[0106]
测得该微胶囊含水量为1.94%,表面油为2.06(g/100g微胶囊粉末),包埋率为91.5%,过氧化值为0.17mmol/kg。
[0107]
试验例1储存过程微胶囊过氧化值变化
[0108]
过氧化值表示油脂和脂肪酸等被氧化程度的一种指标,过氧化值越高,被氧化程度越高,氧化变性水平越高。将实施例1-5制备的微胶囊、火麻仁油、维生素e以及火麻仁油和维生素e按质量比为13:1配制成的原油置于60℃的烘箱中储存30d,每5d取样测定一次样品的过氧化值,考察微胶囊样品在加速氧化条件下过氧化值的变化,即氧化变性的程度,结果如图1所示。
[0109]
由图1可知,在加速氧化条件下,实施例1-5制备的微胶囊具有壁材以及火麻仁油和维生素e混合的芯材,其过氧化值增幅较小,氧化变性程度较低,而原油、火麻仁油和维生素e的过氧化值均明显增加,且与原油相比,火麻仁油和维生素e的过氧化值的增幅更大,综合上述表明,本发明中火麻仁油和维生素e相互配合,降低了微胶囊的氧化变性水平,提高了微胶囊的稳定性,且微胶囊中的壁材能够进一步增强微胶囊的稳定性。
[0110]
试验例2高脂血症模型降脂试验
[0111]
将80只sd大鼠随机分为两组:空白组(10只)、模型组(70只),空白组喂养正常维持饲料,模型组给予定制高脂饲料(配方参照国家2012年版“保健食品评价标准”混合型高脂血症动物模型),整个实验期间大鼠饮水和进食不受人为干预。每天定时更换大鼠笼具内的垫料及饮水,确保大鼠的生活环境满足室内温度在22
±
2℃,相对湿度维持在40%~60%之间,光照和黑暗各12h。两周后,通过颈静脉抽血的方式取各组大鼠的血液,将取出的血液迅速置于ep管中,室温下静置30min,然后于4℃、600
×
g离心15min,移取上清液至0.5ml的ep管中,采用自动生化仪检测大鼠的血脂四项,即总胆固醇(tc)、甘油三酯(tg)、低密度脂蛋白胆固醇(ldl-c)和高密度脂蛋白胆固醇(hdl-c),并使用spss软件对结果进行统计分析,模型组的tc、tg、和ldl-c水平显著高于空白组,并且模型组的hdl水平没有显著低于空白组,视为造模成功,在统计学分析确定造模成功后,根据大鼠的tg水平将模型组大鼠分为7组:模型对照组(10只)、火麻仁油组(10只)、维生素e组(10只)、实施例1微胶囊组(10只)、实施例4微胶囊组(10只)、实施例6微胶囊组(10只)和实施例7微胶囊组(10只)。
[0112]
各组药物剂量与配制方法如下:
[0113]
(1)火麻仁油组:取3.33g火麻仁油,加入1g聚山梨酯80,搅拌,搅拌的过程中加入纯化水使其形成均匀的溶液,转移至100ml的容量瓶中进行定容,使得最终溶液中火麻仁油含量为0.0333g/ml;
[0114]
(2)维生素e组:取3.33g维生素e,加入1g聚山梨酯80,搅拌,搅拌的过程中加入纯化水使其形成均匀的溶液,玻璃棒转移至100ml的容量瓶中进行定容,使得最终溶液中维生素e含量为0.0333g/ml;
[0115]
(3)实施例1微胶囊组:取实施例1制备的微胶囊8.35g,然后加入1g聚山梨酯80,搅拌,搅拌的过程中加入纯化水使其形成均匀的溶液,玻璃棒转移至100ml的容量瓶中进行定
容,使得最终溶液中火麻仁油和维生素e总含量为0.0333g/ml;
[0116]
(4)实施例4微胶囊组:取23.8g实施例4制备的微胶囊,加入1g聚山梨酯80,搅拌,搅拌的过程中加入纯化水使其形成均匀的溶液,转移至100ml的容量瓶中进行定容,使得最终溶液中火麻仁油和维生素e总含量为0.0333g/ml;
[0117]
(5)实施例6微胶囊组:取7.6g实施例6制备的微胶囊,加入1g聚山梨酯80,搅拌,搅拌的过程中加入纯化水使其形成均匀的溶液,转移至100ml的容量瓶中进行定容,使得最终溶液中火麻仁油和维生素e总含量为0.0333g/ml;
[0118]
(6)实施例7微胶囊组:取20.8g实施例7制备的微胶囊,加入1g聚山梨酯80,搅拌,搅拌的过程中加入纯化水使其形成均匀的溶液,转移至100ml的容量瓶中进行定容,使得最终溶液中火麻仁油和维生素e总含量为0.0333g/ml。
[0119]
按照国家2012年版“保健食品评价标准”混合型高脂血症动物实验方法和保健品药效评价要求,参照市售相关产品的人体的日用量,再换算成动物的日用量,本实验采用1ml/100g(在配置时确保配置的药物浓度准确)的剂量进行换算,每天定时采用电子秤对大鼠的体重进行测量,然后换算成相应的给药体积,采用2.5ml注射器+灌胃针进行给药,在火麻仁油组、维生素e组、实施例1微胶囊组、实施例4微胶囊组、实施例6微胶囊组及实施例7微胶囊组给药的同时,对空白组和模型对照组的大鼠采用同样的灌胃处理,每天定时称量体重并换算成相应的灌胃体积,灌胃等体积的生理盐水,以此来消除灌胃这项操作对大鼠的各项检测指标的影响。连续、定时给药45天。
[0120]
给药45天后,将大鼠笼具内的饲料撤走,保持饮水不变,24h后,用10%水合氯醛腹腔注射使大鼠进入麻醉状态,等待10min左右,待大鼠完全被麻醉之后,采用静脉取血针从大鼠的心脏尖端取血,然后迅速将血液注入1ml ep管内,放置在ep管架子上静置30min,并于4℃、600
×
g离心15min,待ep管中的血液分为两层,小心地转移上层清液至0.5ml的ep管中,液氮冷冻,储存于-80℃超低温冰箱中,以待后续检测。
[0121]
取出储存在-80℃超低温冰箱里的血清,常温下解除冷冻状态,采用自动生化仪检测大鼠的血脂四项,各组大鼠的tc、tg、ldl及hdl水平的结果如表8所示。
[0122]
表8
[0123]
[0124][0125]
由表8可知,模型对照组血脂三项指标(tc、tg和ldl)显著高于空白组(p《0.05),实施例1和实施例4微胶囊组血脂三项指标(tc、tg和ldl)显著低于模型对照组(p《0.05),火麻仁油组和维生素e组血脂三项指标(tc、tg和ldl)和模型对照组无显著性差异(p》0.05),实施例6和实施例7微胶囊组血脂三项指标(tc、tg和ldl)中tc指标和tg指标与模型对照组无显著性差异(p》0.05),各个分组的hdl-c水平没有显示出显著的统计学差异(p》0.05)。
[0126]
上述结果表明,高脂喂养的模型对照组大鼠血脂水平(tc、tg、ldl-c)均明显的高于食用普通饲料的空白组大鼠,在45d的药物作用下,各组药物展现出了不同程度的降血脂的能力,其中,实施例1、4、6和7制备的微胶囊组的降血脂效果优于火麻仁组和维生素e组,表明本发明中火麻仁油和维生素e能够协同增效,增强微胶囊降血脂作用,实施例1和4制备的微胶囊组的降血脂效果优于实施例6和7制备的微胶囊组,表明本发明控制火麻仁油和维生素e的质量比为(1~13):1,能够进一步增强微胶囊的降血脂能力。
[0127]
综上所述,本发明的微胶囊中,火麻仁油和维生素e协同增效,能够提高微胶囊的抗氧化破坏的能力,增强微胶囊的降血脂的能力。
[0128]
申请人声明,本发明通过上述实施例来说明本发明的详细方法,但本发明并不局限于上述详细方法,即不意味着本发明必须依赖上述详细方法才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1