用于肠道成熟的营养组合物的制作方法
1.本发明属于婴儿营养领域,特别是婴儿配方产品。
背景技术:
2.人类母乳被普遍认为是婴儿出生后最初几个月的最佳营养。母乳可能在塑造婴儿肠道微生物群和免疫系统方面发挥若干补充作用。这些包括益生菌作用,通过这种作用,牛乳的营养成分对特定类型细菌的生长具有选择性,以及细菌和免疫成分的直接转移。然而,在某些情况下,由于医疗原因或由于选择不母乳喂养,母乳喂养不足或不成功。针对这种情况,开发出婴儿配方产品或后续(follow on)配方产品。如今,商业婴儿配方产品被普遍用作出生后早期的补充或唯一的营养来源。这些配方产品包括一系列营养素,以满足成长中的婴儿的营养需求,通常包括脂肪、碳水化合物、蛋白质、维生素、矿物质和其他有助于婴儿最佳生长和发育的营养素。商业婴儿配方产品是为了尽可能地模仿母乳的成分和功能而设计的。
3.新生儿的肠道在出生时功能不成熟,免疫力低下。胃肠道(gi)在出生后经历了快速的生长和成熟,其中充分的消化功能发展,功能性肠道屏障建立,肠道微生物群发展和免疫功能发展。这意味着在出生后的最初几周,所有哺乳动物都有一个未成熟的肠道。
4.已知出生后早期的营养可以直接通过提供构成要素来影响婴儿的发育轨迹包括肠道的发育,但也可以通过分子机制调节信号通路(jimenez-chillaron jc et al.2012,biochemie 94:2242-2263)。与母乳相比,配方产品的概念在临床和临床前研究中已经证明可以改变肠道成熟的时间和结果(catassi c et al.1995,j pediatr groustenterol nutr 21(4):383-386)。
5.在本领域中,需要调节肠道成熟和伴随的配方产品喂养的婴儿的肠道的免疫成熟,以实现/支持适当的时机和结果,其失败可能导致自身免疫性或特应性疾病的发生。
技术实现要素:
6.本发明旨在应本领域的需求提供婴儿配方产品用于调节肠道成熟和改善配方产品喂养的婴儿的肠道免疫系统以使其更类似于母乳喂养婴儿的肠道成熟模式。
7.发明人比较了三组健康小鼠的出生后基因表达模式,这三组小鼠被随机分为一组接受母乳喂养(母乳喂养),一组接受实验婴儿配方产品,其包含包衣磷脂的大脂质球形式的脂质成分(活性),一组接受对照婴儿配方产品,其不具有包衣磷脂的大脂质球形式的脂质成分,而是包衣蛋白质的标准小脂质球形式(对照)。两种配方产品均在出生后14.5天至18.5天施用。准备对照和实验乳配方以便在这两种制剂中达到相同的蛋白质含量,并且脂肪和碳水化合物含量以及热量含量非常相似。
8.发明人在分析不同饮食组小肠中的基因表达时惊奇地发现,喂养实验婴儿配方产品的小鼠的基因表达比喂养对照配方产品的小鼠的基因表达更类似于母乳喂养的小鼠的基因表达。喂养实验婴儿配方产品的小鼠在与调节作为免疫反应一部分的上皮屏障功能和
上皮防御有关的单个基因(包括再生胰岛衍生3β(reg3b)、再生胰岛衍生3g(reg3g)、酪氨酸蛋白激酶6(ptk6)、具有叉头相关结构域的traf相互作用蛋白(tifa))的基因表达与母乳喂养的小鼠更相似。此外,相比于对照组,喂养实验婴儿配方产品的小鼠在与免疫信号和细胞周期信号有关的功能基因组(典型通路)的基因表达模式(图4b)与母乳喂养组差异较小,因此更相似。
9.总的来说,这些发现表明,喂养热量含量和常量成分(macro-ingredient)含量相似但脂质球结构不同的婴儿配方产品,对出生后早期肠道成熟和肠道免疫系统有有益的影响,使其与接受对照配方产品的婴儿肠道成熟的时间和结果相比更具优势,更接近母乳喂养的婴儿肠道成熟的时间和结果。
附图说明
10.图1显示了从出生后14.5天起小鼠的体重增加,以克为单位,这些小鼠或为母乳喂养组(黑色三角形),或暴露在活性组(浅灰色圆圈)或对照组(深灰色方形)组合物中。所示为平均值
±
sem。两方差分析,然后是tukey多重比较检验。
11.图2a显示了不同饮食条件下的基因组交集和差异,这是通过使用文氏图比较活性组与母乳喂养组(n=351)和对照组与母乳喂养组(n=322)的fdr校正后差异表达基因(q≤0.05)得出的。
12.图2b显示了活性组与母乳喂养组(浅灰色)和对照组与母乳喂养组(黑色)的差异表达基因(q≤0.05)的差异倍数(fc)图(总计n=580),显示了不同组比较中基因变化的方向性和负荷。
13.图3a显示了对照组与母乳喂养组(n=322)的差异表达基因(q≤0.05)的fc图,表明了对照组与母乳喂养组和活性组与对照组比较中基因变化的方向性和负荷。浅灰色显示了活性组与对照组的差异表达基因的fc,黑色显示了对照组与母乳喂养组的差异表达基因的fc。
14.图3b显示了所有3组中对照组与母乳喂养组(n=322)的差异表达基因的pca;母乳喂养组(黑色三角形),活性组(浅灰色圆圈),对照组(深灰色方形)。对行应用单位方差缩放;主成分的计算采用带归因的奇异值分解(svd)。x轴和y轴表示主成分1和主成分2,分别解释了总方差的62.7%和5.4%。预测椭圆是这样的:当概率为0.95时,来自同一组的新观测值将落在椭圆内。n=23个数据点。
15.图3c显示了仅在对照组与母乳喂养组(n=229)中差异表达基因的pca,排除了所有3组的重叠;母乳喂养组(黑色三角形),活性组(浅灰色圆圈),对照组(深灰色方形)。对行应用单位方差缩放;主成分的计算采用带归因的svd。x轴和y轴表示主成分1和主成分2,分别解释了总方差的62%和6.3%。预测椭圆是这样的:当概率为0.95时,来自同一组的新观测值将落在椭圆内。n=23个数据点。
16.图4a显示了与调节作为免疫反应一部分的上皮屏障功能和上皮防御相关的单个基因的基因表达(包括reg3b、reg3g、ptk6、tifa),其与母乳喂养组(黑色条)相比受对照组(深灰色条)的影响,但不受活性组(浅灰色条)的影响。
17.图4b显示了使用n=322个差异表达基因,对照组与母乳喂养组的前10个显著调节的典型途径。以下是对照组与母乳喂养组的前10个调节的典型途径:th:t辅助细胞分化、
il-10:il-10信号通路、th1-th2:th1和th2激活通路、t1dm:i型糖尿病信号通路、icos-icosl:t辅助细胞的icos-icosl信号通路、dc-nk:树突状细胞与自然杀伤细胞间的串扰、tnfr2:tnfr2信号通路、th1:th1信号通路、铁:铁稳态信号通路、阿片:阿片信号通路。
具体实施方式
18.因此,本发明涉及一种用于调节婴儿肠道成熟的时间和结果的方法,该方法与施用包括基于体积计的模式直径为约0.5μm且没有磷脂包衣的脂质球的对照组婴儿配方产品或后续配方产品的婴儿肠道成熟的时间和结果相比,更类似于在母乳喂养的婴儿中观察到的肠道成熟的时间和结果,
19.所述方法包括给所述婴儿喂食选自婴儿配方产品和后续配方产品的营养组合物,其中所述婴儿配方产品或后续配方产品不是母乳,并且其中所述婴儿配方产品或后续配方产品包括脂质、蛋白质和可消化碳水化合物,其中所述脂质为脂质球的形式,并且其中,
20.a.所述脂质球基于体积计的模式直径(mode diameter)为至少1μm,和/或
21.b.至少45体积%的脂质球直径为2至12μm,以及
22.c.所述脂质包含基于总脂质的至少0.5重量%的磷脂,
23.并且所述脂质球具有包含磷脂包衣。
24.本发明还可表述为一种非治疗性方法,用于通过施用选自婴儿配方产品和后续配方产品的营养组合物来调节婴儿肠道成熟的时间和结果,其中所述婴儿配方产品或后续配方产品不是母乳,并且其中所述婴儿配方产品或后续配方产品包括脂质、蛋白质和可消化碳水化合物,其中所述脂质为脂质球的形式,并且其中,
25.a.所述脂质球基于体积计的模式直径为至少1至少,和/或
26.b.至少45体积%的脂质球直径为2至12μm,以及
27.c.所述脂质包含基于总脂质的至少0.5重量%的磷脂,并且所述脂质球具有包含磷脂包衣,
28.其中所述婴儿的肠道成熟的时间和结果与施用包括基于体积计的模式直径为约0.5μm且没有磷脂包衣的脂质球的对照组婴儿配方产品或后续配方产品的婴儿肠道成熟的时间和结果相比,更类似于在母乳喂养的婴儿中观察到的肠道成熟的时间和结果。
29.换言之,本发明涉及一种选自婴儿配方产品和后续配方产品的营养组合物,其中所述婴儿配方产品或后续配方产品不是母乳,并且其中所述婴儿配方产品或后续配方产品包括碳水化合物、蛋白质和脂质,其中所述脂质是脂质球的形式,并且其中,
30.a.所述脂质球基于体积计的模式直径为至少1μm,和/或
31.b.至少45体积%的脂质球直径为2至12μm,以及
32.c.所述脂质包含基于总脂质的至少0.5重量%的磷脂,
33.并且所述脂质球具有包含磷脂的包衣,
34.所述营养组合物用于调节婴儿肠道成熟的时间和结果,其与施用包括基于体积计的模式直径为约0.5μμm且没有磷脂包衣的脂质球的对照组婴儿配方产品或后续配方产品的婴儿肠道成熟的时间和结果相比,更类似于在母乳喂养的婴儿中观察到的肠道成熟的时间和结果。
35.本发明还可以被表述为脂质球在制造用于调节婴儿肠道成熟的时间和结果的营
养组合物中的用途,其中所述婴儿肠道成熟的时间和结果与施用包括基于体积计的模式直径为约0.5μμm且没有磷脂包衣的脂质球的对照组婴儿配方产品或后续配方产品的婴儿肠道成熟的时间和结果相比,更类似于在母乳喂养的婴儿中观察到的肠道成熟的时间和结果,
36.其中所述营养组合物选自婴儿配方产品和后续配方产品,其中所述婴儿配方产品或后续配方产品不是母乳,并且所述婴儿配方产品或后续配方产品包括碳水化合物、蛋白质和脂质,其中所述脂质是脂质球的形式,并且其中,
37.a.所述脂质球基于体积计的模式直径为至少1μm,和/或
38.b.至少45体积%的脂质球直径为2至12μμm,以及
39.c.所述脂质包含基于总脂质的至少0.5重量%的磷脂,
40.并且所述脂质球具有包含磷脂的包衣。
41.这里所用的术语“母乳喂养的婴儿”是指从出生到至少4个月大仅食用人类母乳的婴儿,无论是直接来自乳房还是来自含有挤出的母乳的瓶子。
42.这里所用的术语“对照组婴儿配方产品和或后续配方产品”是指以下婴儿配方产品或后续配方产品,其:
[0043]-符合婴儿配方产品或后续配方产品的法律要求(例如欧盟第609/2013号和第2016/127号法规);
[0044]-包括基于体积计的模式直径为约0.5μm的脂质球;以及
[0045]-所述脂质球没有磷脂包衣。
[0046]
在本发明的优选实施方案中,在婴儿出生后的前12个月,更优选在婴儿出生后的前6个月,肠道成熟的时间和结果与在母乳喂养的婴儿出生后的同一时期观察到的肠道成熟的时间和结果更相似。
[0047]
在本发明的优选实施方案中,所述营养组合物对婴儿施用,其中施用所述营养组合物的婴儿的年龄为0至12个月,优选为0至6个月,更优选为0至4个月。
[0048]
在本发明的优选实施方案中,婴儿肠道成熟的时间和结果是婴儿出生后的前12个月肠道成熟的时间和结果。
[0049]
在本发明的上下文中,婴儿优选为足月出生婴儿。优选地,所述营养组合物施用于或使用于足月婴儿。足月婴儿是指胎龄为37至42周的婴儿。优选地,所述营养组合物施用于或使用于健康婴儿。
[0050]
在本发明的上下文中,调节婴儿肠道成熟的时间和结果优选地包括调节作为肠道免疫应答的一部分的上皮屏障功能和上皮防御的时间和结果,使其更类似于在母乳喂养的婴儿中观察到的作为肠道免疫应答的一部分的上皮屏障功能和上皮防御。
[0051]
在本发明的上下文中,调节肠道成熟的时间和结果优选地包括调节肠道免疫状态和/或功能,使其更类似于在母乳喂养的婴儿中观察到的肠道免疫状态和/或功能。换言之,在一个实施方案中,调节肠道成熟的时间和结果是调节肠道免疫系统成熟的时间和结果,优选地调节肠道免疫系统成熟的时间。
[0052]
在本发明的上下文中,调节肠道免疫系统成熟的时间和结果优选地包括诱导耐受性免疫状态以刺激食物耐受。
[0053]
肠道免疫系统成熟优选地包括调节参与调节作为肠道免疫应答的一部分的上皮
屏障功能和上皮防御的基因的表达(包括但不限于人类基因reg3b、reg3g、ptk6、tifa)和/或参与肠道免疫信号传导的典型途径,以使其与喂养含有约0.5μm且没有磷脂包衣的脂质球的对照(或标准)配方产品的婴儿相比,更类似于母乳喂养的婴儿的方式。
[0054]
参与肠道免疫信号传导的典型途径包括但不限于以下生物功能牵涉的路径:t辅助细胞(th)分化、白细胞介素-10(il-10)信号传导、th1和th2激活通路、th细胞icos-icos配体信号传导、树突状细胞与自然杀伤细胞间的串扰、肿瘤坏死因子受体2(tnfr-2)信号传导、th1通路和铁稳态信号通路。与母乳喂养的婴儿更相似的参与肠道免疫信号传导的典型途径为显著不同地被调节的典型途径。特别被调节或表达得更像母乳喂养婴儿中观察到的模式的与肠道免疫信号传导相关的基因是以下基因:骨形态发生蛋白受体1a(bmpr1a)、braf、钙/钙调素依赖性蛋白激酶iiδ(camk2d)、hck、组蛋白去乙酰化酶9(hdac9)、人类白细胞抗原a(hla-a)、hla-dqb1、dna结合抑制剂4(id4)、干扰素γ受体1(ifngr1)、白细胞介素18(il18)、白细胞介素2受体2b(il2rb)、白细胞介素4受体(il4r)、丝裂原活化蛋白激酶激酶3(map2k3)、b细胞抑制剂中kappa轻链多肽基因增强子alpha(nfkbia)、蛋白酪氨酸磷酸酶非受体型22(ptpn22)、母亲抗dpp同源物4(mothers against decapentaplegic homolog 4;smad4)、鞘氨醇激酶1(sphk1)、信号传导子和转录激活子3(stat3)、traf家族成员相关nfkb激活子(tank)、具有叉头相关结构域的traf相互作用蛋白(tifa)、tnf受体超家族成员1a(tnfrsf1a)和vav1。
[0055]
在本发明的背景下,调节肠道成熟的时间和结果优选地包括调节参与免疫发育、免疫功能、免疫激活和免疫信号传导的基因的表达。
[0056]
脂质球大小
[0057]
根据本发明,营养组合物包括脂质球。当为液体形式时,这些脂质球在水相中乳化。或者,所述脂质球以粉末存在,所述粉末适合与水或另一种食品级水相重组,优选地提供即饮配方产品。
[0058]
脂质球包括核和表面。所述核优选包括植物脂质,优选包括至少90重量%的甘油三酯,更优选基本上由甘油三酯组成。并非存在于组合物中的所有植物脂质都必须包含在脂质球的核中,但优选主要部分是,优选大于50重量%,更优选大于70重量%,甚至更优选大于85重量%,甚至更优选大于95重量%,最优选大于98重量%的存在于组合物中的植物脂质包含在脂质球的核中。在一个实施方案中,脂质球的核包含至少40重量%的植物源甘油三酯,更优选至少50重量%,甚至更优选至少70重量%的植物源甘油三酯,更优选脂质球的核包含至少85重量%,更优选至少95重量%的植物源甘油三酯。
[0059]
本发明方法或用途中的营养组合物中的脂质球的体积加权模式直径大于1.0μm,优选大于3.0μm,更优选4.0μm或以上,优选1.0-10μm,更优选2.0-8.0μm,甚至更优选3.0-8.0μm,最优选4.0-8.0μm。优选地,作为补充或替代,所述尺寸分布的方式为至少45体积%,优选至少55体积%,甚至更优选至少65体积%,甚至更优选至少75体积%具有2至12μm之间的直径。更优选至少45体积%,优选至少55体积%,甚至更优选至少65体积%,甚至更优选至少75体积%的直径介于2至10μm之间。甚至更优选至少45体积%,优选至少55体积%,甚至更优选至少65体积%,甚至更优选至少75体积%的直径介于4和10μm之间。优选小于5体积%具有大于12μm的直径。
[0060]
脂质球的百分比基于总脂质体积计。模式直径涉及基于总脂质体积的存在最多的
直径,或在具有x轴为直径和y轴为体积(%)的图形表示中的峰值。
[0061]
脂质球的体积及其大小分布可适当地使用粒度分析仪如mastersizer(malvern instruments,malvern,uk)来确定,例如通过michalski et al,2001,lait81:787-796中描述的方法来确定。
[0062]
磷脂
[0063]
在根据本发明的方法或用途中施用的营养组合物包括磷脂,更优选该营养组合物包括来源于非人类动物的磷脂,最优选该营养组合物包括来源于非人类哺乳动物乳的磷脂。来源于非人类哺乳动物乳的磷脂包括从乳脂、奶油脂、奶油血清脂、黄油血清脂、β血清脂、乳清脂、奶酪脂和/或酪乳脂中分离的磷脂。酪乳脂通常是在酪乳生产过程中获得的。奶油血清脂或β血清脂通常是在从奶油或黄油生产无水乳脂的过程中获得的。优选地,磷脂是从乳油(milk cream)中获得的。磷脂优选来源于奶牛、母马、绵羊、山羊、水牛、马和骆驼的乳,最优选来源于牛乳。最优选使用从牛乳中分离的脂质提取物。从非人类哺乳动物乳中提取磷脂的合适来源是可以从奶中分离出来的部分,称为乳脂球膜(mfgm)。因此,在一个实施方案中,根据本发明的方法或用途中要用于营养组合物的磷脂作为mfgm提供。合适的市售牛乳磷脂脂质来源是corman的baef、sm2、sm3和sm4粉,glanbia的salibra和arla的lacprodan mfgm-10或pl20。
[0064]
所述营养组合物包含基于总脂质的至少0.5重量%的磷脂,优选基于总脂质的0.5至20重量%的磷脂,更优选基于总脂质的0.75至10重量%,更优选基于总脂质的1至10重量%,甚至更优选基于总脂质的1.5至10重量%,甚至更优选基于总脂质的2至8重量%的磷脂。
[0065]
存在于根据本发明使用的营养组合物中的脂质球至少部分地在表面包衣磷脂。所谓“包衣”是指脂质球的外表面层包含磷脂,而这些磷脂在脂质球的核中几乎没有。激光扫描显微镜是确定磷脂是否位于脂质球表面的一种合适的方法。
[0066]
已发现磷脂作为脂质球的包衣或外层存在于所给的饮食中有利于调节肠道成熟,更类似于母乳喂养的婴儿。并非所有存在于组合物中的磷脂都必须包含在包衣中,但优选主要部分是。优选大于30重量%、更优选大于50重量%、更优选大于70重量%、甚至更优选大于85重量%、最优选大于95重量%的存在于组合物中的磷脂包含在脂质球包衣中。
[0067]
根据本发明,营养组合物优选包括甘油磷脂。甘油磷脂是由脂肪酸在骨架甘油部分的碳-1和碳-2上的羟基酯化,并通过酯键连接到甘油的碳-3上的带负电荷的磷酸基团,以及任选地连接到磷酸基团上的胆碱基团(如磷脂酰胆碱,pc)、丝氨酸基团(如磷脂酰丝氨酸,ps)、乙醇胺基团(如磷脂酰乙醇胺,pe)、肌醇基团(如磷脂酰肌醇,pi)或甘油基团(如磷脂酰甘油,pg)形成的一种脂类。溶血磷脂是一类具有一个脂肪酰基链的磷脂。优选地,本发明的组合物包含pc、ps、pi和/或pe,更优选地至少包含pc。
[0068]
优选地,所述营养组合物包括鞘磷脂。鞘磷脂有一个磷酰胆碱或磷酰乙醇胺分子酯化到神经酰胺的1-羟基。它们被分类为磷脂和鞘脂,但不被分类为甘油磷脂或鞘糖脂。优选所述营养组合物包含基于总脂质的0.05至10重量%的鞘磷脂,更优选0.1至5重量%,甚至更优选0.2至2重量%。优选所述磷脂包含基于总磷脂的至少2重量%的鞘磷脂,更优选5-40重量%的鞘磷脂,最优选10-30重量%的鞘磷脂。
[0069]
根据本发明,营养组合物优选包括胆固醇。所述营养组合物优选包含基于总脂质
的至少0.005重量%的胆固醇,更优选至少0.01重量%,更优选至少0.02重量%,更优选至少0.05重量%,甚至更优选至少0.1重量%。优选胆固醇的量不超过总脂质的10重量%,更优选不超过总脂质的5重量%,甚至更优选不超过总脂质的1重量%。
[0070]
优选磷脂与蛋白质的重量比高于0.10,更优选高于0.20,甚至更优选高于0.3。
[0071]
同时使用来自非人类动物来源的磷脂和来自植物脂质的甘油三酯,可以制造具有更类似于母乳结构的脂质球,同时提供最佳的脂肪酸分布。
[0072]
在wo 2010/0027258、wo 2010/0027259和wo2013/135738中公开了获得更大尺寸和包衣磷脂的脂质球的方法。
[0073]
婴儿配方产品及后续配方产品
[0074]
在根据本发明的方法或用途中施用的营养组合物选自婴儿配方产品和后续配方产品。这意味着本营养组合物不是人乳。另外,“配方”一词意味着它涉及人工合成的组合物,或者换句话说,它是合成的。因此,在一个实施方案中,营养组合物选自人工婴儿配方产品和人工后续配方产品或合成婴儿配方产品和合成后续配方产品。在本文中,婴儿配方产品是指人工制造的营养成分,用于0至约4至6个月大的婴儿,并用作母乳的替代品。通常,婴儿配方产品适合作为唯一的营养来源。这样的配方产品也称为起始配方产品。婴儿配方产品从出生后4至6个月到12个月,旨在为开始断奶的婴儿提供补充营养。这样的配方产品也称为后续配方产品。婴儿配方产品和后续配方产品受到严格的监管,例如欧盟第609/2013和2016/127号规定。这些配方产品优选包括本领域推荐和已知的其它成分,如矿物质、微量元素、维生素和其它微量营养素。
[0075]
优选至少在婴儿出生后的前2个月期间,优选至少在婴儿出生后的前3个月期间,更优选至少在婴儿出生后的前4个月期间使用营养组合物。优选对小于12个月、优选小于6个月、更优选小于4个月的婴儿施用营养组合物。
[0076]
营养组合物优选包括3至7克脂质/100千卡,优选4至6克脂质/100千卡,更优选4.5至5.5克脂质/100千卡,优选1.2至5克蛋白质/100千卡,优选1.4至4克蛋白质/100千卡,更优选1.6至3克蛋白质/100千卡,更优选1.8至2.5克蛋白质/100千卡,优选6至18克可消化碳水化合物/100千卡,优选8至16克可消化碳水化合物/100千卡,更优选10至15克可消化碳水化合物/100千卡。
[0077]
在一个实施方案中,营养组合物为粉末形式,适合在与水溶液(优选与水)重组后制备即饮配方产品。优选地,所述营养组合物是可与水重组的粉末。
[0078]
优选婴儿配方产品或后续配方产品在即饮时能量密度为60千卡至75千卡/100毫升,更优选为60至70千卡/100毫升。这种密度保证了水合作用和热量摄入之间的最佳平衡。
[0079]
在本发明的上下文中,婴儿配方产品或后续配方产品不是原生牛乳或人乳。在本发明的上下文中,对照婴儿配方产品或后续配方产品也不是原生牛乳或人乳。
[0080]
脂质
[0081]
此处la指亚油酸和/或酰基链(18:2 n6);ala指α-亚麻酸和/或酰基链(18:3 n3);pufa是指多不饱和脂肪酸和/或酰基链;mufa是指单不饱和脂肪酸和/或酰基链;lc-pufa是指长链多不饱和脂肪酸和/或酰基链,在脂肪酰基链中包含至少20个碳原子并具有2个或更多不饱和键;dha是指二十二碳六烯酸和/或酰基链(22:6,n3);epa指二十碳五烯酸和/或酰基链(20:5 n3);ara指花生四烯酸和/或酰基链(20:4 n6);dpa是指二十二碳五烯酸和/或
酰基链(22:5 n3)。中链脂肪酸(mcfas)是指链长为6、8或10个碳原子的脂肪酸和/或酰基链。
[0082]
存在于根据本发明的营养组合物中的脂质优选包括pufas,更优选lc-pufas,因为lc-pufas进一步改善追赶生长期间的生长模式和身体组成,以及大脑和视网膜发育。所述营养组合物优选包含基于总脂质的5-35重量%的pufa,更优选10-30重量%的pufa,最优选15-20重量%的pufa。还优选本营养组合物包含mufas,基于总脂质计,优选10-80重量%的mufa,更优选20-70重量%的mufa,最优选35-55重量%的mufa。
[0083]
la优选以足够的量存在,以促进健康的生长和发育,但以尽可能低的量存在,以防止不必要的发育。因此,所述营养组合物优选包含基于总脂质的低于20重量%、优选5至16重量%、更优选10至14.5重量%的la。优选地,所述营养组合物包含基于总脂质的至少5重量%的la。每100千卡,营养组合物优选包含350-1400毫克la。优选地,ala的存在量足以促进婴儿的健康生长和发育。因此,本发明的组合物优选包含基于总脂质的至少1.0重量%的ala。优选地,该组合物包含基于总脂质的至少1.5重量%的ala,更优选至少2.0重量%。优选该组合物包含小于12.5重量%、更优选小于10.0重量%、最优选小于5.0重量%的ala。所述营养组合物优选包括la/ala的重量比为2~20,更优选为3~16,更优选为4~14,更优选为5~12。
[0084]
为了适当的生长和发育,本发明的组合物优选包含基于总脂质的至少3重量%的mcfa,更优选至少9重量%,甚至更优选15重量%。本发明的组合物有利地包含基于总脂质的小于50重量%、更优选小于40重量%、甚至更优选小于25重量%的mcfa。
[0085]
根据本发明,营养组合物优选包括lc-pufa,更优选n-3 lc-pufa,因为n-3 lc-pufa促进肠道成熟。更优选地,所述营养组合物包括epa、dpa和/或dha,甚至更优选dha。由于低浓度的dha、dpa和/或epa已经有效,营养组合物中n-3 lc-pufa的含量,更优选dha,优选不超过总脂肪酸含量的15重量%,优选不超过10重量%,甚至更优选不超过5重量%。优选所述营养组合物包含总脂肪酸含量的至少0.15重量%、优选至少0.35重量%、更优选至少0.75重量%的n-3 lc-pufa,更优选dha。在一个实施方案中,本组合物包含基于总脂肪酸的至少0.15重量%的n-3 lc-pufa,所述总脂肪酸选自dha、epa和dpa,更优选dha。
[0086]
由于n-6脂肪酸族,特别是花生四烯酸(ara)和作为其前体的la,与n-3脂肪酸族,特别是dha和epa和作为其前体的ala相抵消,所以营养组合物中的ara含量相对较低。n-6 lc-pufa,更优选ara,含量优选不超过5重量%,更优选不超过2.0重量%,更优选不超过0.75重量%,甚至更优选不超过0.5重量%,基于总脂肪酸计。
[0087]
优选地,所述营养组合物包括至少一种选自葵花籽油、菜籽油、椰子油和棕榈油的植物脂质来源。此外,优选除了植物脂质外,还存在至少一种选自鱼油(优选金枪鱼鱼油)、单细胞油(如藻类油、微生物油和真菌油)、mct油和鸡蛋脂的脂质来源。这些油源适合作为lc-pufa油源。优选地,作为n-3 lc-pufa的来源,使用单细胞油,包括藻类油和微生物油。在优选实施方案中,营养组合物包含至少一种选自葵花籽油、菜籽油、椰子油、棕榈油、mct油、鸡蛋脂、大豆卵磷脂、葵花籽卵磷脂、乳脂、酪乳脂、黄油血清脂、鱼油、海洋油、藻类油、真菌油和微生物油的脂质。
[0088]
蛋白质
[0089]
所述营养组合物包括蛋白质,优选以上述规定的量。蛋白质来源的选择应满足对
必需氨基酸含量的最低要求,并确保令人满意的生长。因此,优选蛋白质来源基于奶牛乳蛋白如乳清、酪蛋白及其混合物,以及基于大豆、马铃薯或豌豆的蛋白质。在使用乳清蛋白的情况下,蛋白质来源优选基于酸乳清或甜乳清、乳清分离蛋白或其混合物,并可包括α-乳白蛋白和β-乳球蛋白。更优选的是,所述蛋白质来源基于已去除酪蛋白糖巨肽(cgmp)的酸乳清或甜乳清。优选地,所述组合物包含基于干重的至少3重量%的酪蛋白。优选酪蛋白是完整的和/或非水解的。对于本发明,蛋白质包括肽和游离氨基酸。
[0090]
可消化碳水化合物
[0091]
营养组合物包括可消化碳水化合物,优选按上述规定的量。优选可消化碳水化合物来源是乳糖、葡萄糖、蔗糖、果糖、半乳糖、麦芽糖、淀粉和麦芽糊精。乳糖是人乳中主要的可消化碳水化合物。乳糖有利地具有低血糖指数。该营养组合物优选包括乳糖。该营养组合物优选包括可消化碳水化合物,其中至少35重量%、更优选至少50重量%、更优选至少75重量%、甚至更优选至少90重量%、最优选至少95重量%的可消化碳水化合物是乳糖。基于干重计,本组合物优选包含至少25重量%、优选至少40重量%的乳糖。
[0092]
非消化性碳水化合物
[0093]
在一个实施方案中,营养组合物包括非消化性寡糖。优选所述营养组合物包括聚合度(dp)在2至250、更优选3至60之间的非消化性寡糖。
[0094]
所述非消化性寡糖优选包括果寡糖、菊糖和/或半乳寡糖,更优选半乳寡糖,最优选反式半乳寡糖。在优选的实施方案中,非消化性寡糖包括反式半乳寡糖和果寡糖或菊糖的混合物。合适的非消化性寡糖例如gos(frieslandcampina domo)、或(orafti)。
[0095]
优选地,所述营养组合物包括每100毫升80毫克至2克非消化性寡糖,更优选150毫克至1.50克,甚至更优选每100毫升300毫克至1克。基于干重计,营养组合物优选包括0.25重量%至20重量%,更优选0.5重量%至10重量%,甚至更优选1.5重量%至7.5重量%。
[0096]
在本文件及其权利要求中,动词“包含”及其变体在其非限制性意义上使用,意指包括该词后面的项目,但不排除未具体提及的项目。此外,不定冠词“一个/种(a)”或“一个/种(an)”所指的要素并不排除存在一个以上要素的可能性,除非上下文明确要求存在一个且仅一个要素。因此,不定冠词“一个/种(a)”或“一个/种(an)”通常表示“至少一个/种”。
[0097]
实施例
[0098]
实施例1:制备具有较大脂质球大小的imf的方法
[0099]
如wo 2013/135738的实施例1所述制备婴儿配方产品。特别地,制备粉末形式的婴儿配方产品,其包含每千克最终产品约4800千卡、约247克脂质、约540克可消化碳水化合物、约41克非消化性寡糖和约97克蛋白质。该组合物是用富含牛乳磷脂的黄油乳血清粉、植物油混合物(脂质)、脱盐乳清粉(蛋白质)、乳糖和非消化性寡糖制备的。还使用了本领域已知的维生素、矿物质、微量元素。
[0100]
黄油乳血清粉的量是以基于总脂质的1.62重量%的磷脂存在于最终组合物中。制备包含黄油乳粉、蛋白质和可消化碳水化合物以及除脂质和脂溶性维生素以外的其他成分的水相,并通过本领域已知的方法制备,通过本领域已知的超高温(uht)处理进行热处理以防止细菌污染,然后进行蒸发步骤。蒸发步骤后,水相的干物质含量在30-48重量%之间。混合物被加热到50℃。
[0101]
按照本领域已知的方法制备脂质相。植物油混合物也被加热到50℃,并通过注射和离心增压泵以15至30的重量比加入到水相中。所述脂质和水相混合物的总固含量在40-60重量%之间。因此,将水相和脂质相进料到包括一个混合头的直列式混合器(ystral z80)中。直列式混合器的转子定子设计有3排齿。将水相和脂质相以20-50m/s的端速混合(产生50000至100000s-1
的剪切率),以便将脂质相乳化到水相中,然后用正排量泵,即单泵,以大约8bar的压力泵送到加热器。
[0102]
水包油混合物随后通过浓缩加热器被送入喷雾干燥器,由直列式混合器下游使用的泵驱动。
[0103]
乳液采用schlick(0/2-0/5系列)双流体喷嘴的低剪切雾化系统进行雾化,其中用于喷雾干燥的压力低于8bar,并在干燥气体入口温度为195℃下进行干燥。用mastersizer2000(malvern instruments,malvern uk)测量最终粉末中脂质球的大小。
[0104]
实施例2含有大脂质球和乳磷脂的早期饮食改善小鼠的肠道成熟。
[0105]
进行了体内动物实验,其中评估了含有大脂质球的早期饮食对小肠基因表达的影响,所述脂质球包括含磷脂的包衣。
[0106]
将小鼠c57bl/6幼仔随机分为三个不同的饮食处理组:在出生后第14.5天,小鼠维持母乳喂养(n=8);或开始口服喂养4天包括磷脂包衣的大脂质球的配方产品(活性组,n=8),所述脂质球基于体积计的模式直径为约4μm,并且其中模式直径在2至12μm之间的脂质球的体积%为高于45体积%;或开始口服喂养4天对照组配方产品(对照组,n=7),其中脂肪成分以蛋白质包衣的脂质球的形式存在,且所述脂质球基于体积计的模式直径小于约0.5μm,并且模式直径在2至12μm之间的脂质球的体积%为低于10体积%。
[0107]
幼仔自己吃食物。将活性组配方产品和对照组配方产品以液体形式放在笼内的器皿中提供给小鼠。每天给小鼠称重。在处理期间,母乳喂养的幼仔体重显著高于活动组和对照组。喂养活性组配方产品或对照组配方的幼仔在最初几天体重增加没有差异,但在pn17.5和pn18.5时,喂养活性组配方的幼仔体重增加比对照组显著增加,因此显示出与母乳喂养的小鼠一样的增长趋势(图1)。
[0108]
在18.5天龄时,处死小鼠,获得小鼠小肠,在-80℃下保存直至使用。
[0109]
活性组和对照组的配方产品组成相同,只是脂质球的大小和其上的包衣不同。配方组合物包括脂肪、蛋白质、可消化碳水化合物、非消化性寡糖、维生素、微量元素和矿物质,其比例如本领域人类婴儿配方产品中已知。
[0110]
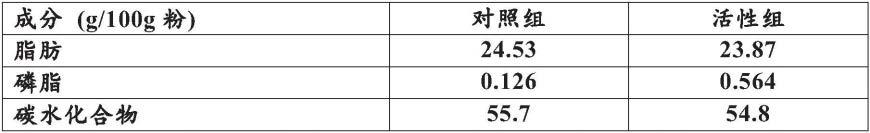
对照组和活性组组合物的组成如表1所示。
[0111]
表1:对照组和活性组组合物
[0112]
[0113][0114]
rna分离与微阵列分析
[0115]
根据制造商的说明,使用rneasy迷你试剂盒(qiagen,courtaboeuf,france)制备总rna,包括dna酶处理的附加步骤。总rna产量和质量在agilent 2100生物分析仪(agilent technologies,massy,france)上进行评估。采用单色全鼠(074809_d_f_20171030 slides)60mer寡核苷酸8
×
60k微阵列(agilent technologies)分析基因表达。根据供应商的说明(agilent technologies)进行crna标记、杂交和检测。对于每个微阵列,用低输入quickamp标记试剂盒从50ng总rna中合成花青3标记的crna。在所有试管中加入rna spike-in,作为标记和扩增步骤的阳性对照。将标记的crna纯化,然后600ng的各crna按照制造商的说明进行杂交并洗涤。在agilent g2505c扫描仪上扫描微阵列,并使用agilent特征提取(fe版10.7.3.1)提取数据。
[0116]
探针使用agilent的注释074809_d_genelist_sureprint g3 mouse v2进行注释,得到45973个注释特征,包括重复的基因符号。为了实现每个基因符号1个特征,通过对每个基因符号上不同探针的原始信号值进行算术平均来去除重复,得到26850个独特基因。利用clc工作台(qiagen bioinformatics)对数据进行质量控制,并对数据进行归一化和转换。
[0117]
生物信息学分析
[0118]
使用clc main workbench 8.1版,对各组独特基因的分位数归一化和log2转换的信号强度进行平均,并用单因素方差分析(anova)对三组进行统计分析,在适当的情况下进行配对t检验,以确定不同组比较活性组与对照组、活性组与母乳喂养组、对照组与母乳喂养组的差异表达基因及变化的相关意义(p值)。相应的差异倍数(fcs)表示一组的平均表达值相对于另一组的平均表达值大多少倍。为了控制假阳性结果,用benjamini和hochberg的方法(benjamini和hochberg1995)对p值进行错误发现率(fdr)的校正,得到q值(fdr校正的p值)。预计在q值低于0.05的fdr校正的特征中,有5%是假阳性。应用分位数归一化和log2转换信号强度、fcs和q值对数据进行描述性生物信息学分析,使用工具文氏图识别不同组比较的差异表达基因组的基因组交集和差异,graphpad prism version7.03for windows(graphpad software,la jolla california usa)用于fc图,clustvis(metsalu和vilo 2015)用于主成分分析(pca)。ingenuity pathway analysis(ipa,ingenuity systems,www.ingenuity.com)和ncbi基因数据库(https://www.ncbi.nlm.nih.gov/gene)将微阵列数据与典型途径和生物学功能联系起来。
[0119]
在数据集中所有独特注释基因(n=26849)中,在活性喂养与对照喂养的幼仔之间共有1127个显著差异表达基因(p≤0.05),在活性喂养与母乳喂养的组之间共有4509个显著差异表达基因(p≤0.05),在对照喂养与母乳喂养的组之间共有5417个显著差异表达基
因(p≤0.05)(表2)。经fdr校正后,显然可见活性组与母乳喂养组(n=351)和对照组与母乳喂养组(n=322)的小肠中差异表达基因的数量相似(q≤0.05)。fc范围则显示了两个相比较的组之间表达水平的变化程度,此处显示总体上对小肠基因表达的影响相对较小。
[0120]
表2:差异表达基因数量概览。
[0121][0122]
*q值=fdr校正后的p值
[0123]
总体而言,微阵列数据表明,对于对照喂养组与母乳喂养组中差异表达的基因组,活性喂养组的小肠基因表达更接近母乳喂养组,其中这种效果特别可以归结于免疫功能和增殖。
[0124]
差异表达基因的重叠
[0125]
通过比较活性组与母乳喂养组(n=351)和对照组与母乳喂养组(n=322)在fdr校正(q≤0.05)后的差异表达基因,所产生的不同饮食条件下基因组的交集和差异藉由文氏图(图2a)确定。文氏图显示,有93个基因重叠,反映了配方产品喂养(活性组和对照组两者)与母乳喂养的显著影响。
[0126]
为了验证基因表达变化是否遵循相同的方向性,将活性组与母乳喂养组和对照组与母乳喂养组的小肠中所有差异表达基因(q≤0.05)的倍数表达变化绘成图(图2b)。大多数累积的差异表达基因(n=580)在两个比较中显示出相似的变化方向,只有6个基因变化方向相反:转铁蛋白受体2(trf2)、荷电多囊体蛋白4b(chmp4b)、蛋白磷酸酶2调节亚基bγ(ppp2r3c)、编码riken的9330133o14rik和a730063m14rik、膜蛋白棕榈酰化7(mpp7)和er相关降解中的泛素识别因子1(ufd1)。
[0127]
当进一步分析活性组在对照组幼仔与母乳喂养组幼仔相比差异表达的322个基因中的影响时,有25个基因对于活性组与对照组而言具有相同的变化方向性,有297个基因对于对照组与母乳喂养组而言具有相反的方向性(图3a)。总的来说,这表明对这个基因组而言,活性喂养组的基因表达模式更接近于母乳喂养组,正如322个基因在3个不同组中的平均表达值的热图中所显示的那样(未示出)。对322个在对照组与母乳喂养组中差异表达的基因进行主坐标分析(pca),表明三个组主要沿着主成分(pc)1分开,母乳喂养组和对照组彼此分开,活性组位于两者之间趋向母乳喂养组,可见该活性配方产品影响在对照组和母乳喂养组之间差异表达的基因的表达,使其趋于更类似母乳喂养组中见到的表达(图3b)。仅对在对照组与仅母乳喂养组中特异性差异表达(不包括跟活性组与仅母乳喂养组相重叠的n=93个基因)的n=229个基因进行pca分析,显示类似的分离和聚类,活性组甚至更接近于母乳喂养组的集群(图3c)。后者发现,活性喂养组聚类更接近母乳喂养组,这并不受基因选择的影响;当对在活性组与母乳喂养组中差异表达的n=351个基因进行pca分析时,对照组的聚类不会更接近母乳喂养组(数据未显示)。
[0128]
为了深入了解不同组中观察到的基因表达模式的功能含义,我们首先考虑了在对
照组相较于母乳喂养组中(q≤0.05)、而不是活性组相较于母乳喂养组中(q≥0.05)显著性差异表达的、并且在活性组与对照组中和在对照组与母乳喂养组中相反调节的单个基因,并按代表基因表达在三组中的变异性的四分位距范围对它们进行排序。在符合这些标准的前20个基因中,有涉及调节作为免疫反应的一部分的上皮屏障功能和上皮防御的基因,包括reg3b(前2)、reg3g(前4)、ptk6(前9)和tifa(前20),对照组相较于母乳喂养组的q值分别为reg3b q=0.025、reg3g q=0.017、ptk6 q=0.007和tifa q=0.005(图4a)。
[0129]
除了单个基因外,我们还考虑了基因的功能组,因为普遍认为的是,在同一功能群中表明的各种单个基因的相当小的影响都可能具有生物学相关性。为了研究对照组与母乳喂养组的n=322个差异表达基因在哪些典型途径和生物学功能中隐含,以及这些途径和功能如何受喂养活性配方产品的影响,我们进行了独创性途径分析(ipa)。在ipa中,典型途径的调控意义由-log(p值)表示,该值是根据调控基因的数量与归属于该途径的总基因数量的关系计算的,因此,~1.3的-log(p值)与0.05的p值有关,如果有足够的信息,活性模式就表示为z-分数(正z-score=上调,负z-score=下调)。通过ipa,发现43个显著受调控的、-log(p值)》1.3的典型途径,其中前10个途径主要参与免疫信号传导(t辅助细胞分化、il-10信号传导、th1和th2激活通路、i型糖尿病信号传导、t辅助细胞icos-icosl信号传导、树突状细胞与自然杀伤细胞间的串扰、th1通路)和细胞周期与生存信号传导(tnfr2信号传导、阿片信号传导通路)(图4b)。43个受调控的通路由46个基因驱动。利用基因本体生物学过程(gene ontology biological processes)描述,我们发现49个基因中有18个(bcl2l1,bmpr1a,braf,hck,hdac9,id4,il18,il2rb,map2k3,nfkbia,ptpn22,smad4,sphk1,stat3,tank,tifa,tnfrsf1b,vav1)包含以下一个或多个术语:炎症(n=6)和/或免疫(n=6)和/或t细胞(n=8)和/或细胞因子(n=4)和/或nf-kappa(n=5)。在热图(图3b)中可视化46个基因在调控途径中的平均组表达,在此还发现活性组与母乳喂养组差异较小,而母乳喂养组和对照组之间确实存在差异。总的来说,数据表明,活性配方产品提供的基因表达模式与在母乳喂养组观察到的更相似,特别是在肠道免疫功能方面,考虑到研究的断奶前环境,这表明了肠道和免疫成熟的影响。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1