一种可即食的高活性益生菌冻干粉的制备方法与流程
1.本发明涉及一种可即食的高活性益生菌冻干粉的制备方法,属于食品微生物技术领域。
背景技术:
2.近年来,益生菌食品在基础研究领域和技术应用方面均得到快速发展,益生菌食品市场也成为了世界功能性食品的主要市场。科学研究表明,益生菌除了在维持肠道微生态平衡、改善肠道功能和调节机体免疫等方面具有益生作用以外,在诸如肥胖等代谢疾病以及抑郁症等神经系统相关疾病中也表现出一定积极作用。然而,益生菌的益生功能的实现,很大程度上依赖于所服用的益生菌产品达到足够的活菌含量和数量。
3.为了提高益生菌产品的活菌含量和数量,本领域技术人员尝试在益生菌生产工艺上进行改进,更为具体地来说,基于现有的基础理论以及本领域技术人员的普遍性思维,通常认为,“发酵生产”和“冷冻干燥”是影响益生菌高活菌数量的关键技术环节,因此,在实际应用中也重点聚焦于这两个技术环节。
4.在发酵生产环节,发酵培养基的配方原料选择是关键因素。为提高益生菌发酵生产的生物量,现有的发酵培养基一方面需要添加大量的无机盐,尤其是钠、钾无机盐作为调节ph的缓冲成分,导致发酵产物中残留高浓度离子;另一方面采用诸如酵母膏、蛋白胨、牛肉浸粉的碳源和氮源作为基础组分,发酵后产生诸多不良风味。即使经过后续的离心操作去除了绝大部分的发酵上清液,但菌体的胞内物质以及菌体表面粘附的代谢产物所携带的离子和不良风味物质仍会进入到后续的冷冻干燥环节,留在最终的益生菌冻干粉中。因此,采用现有工艺制得的益生菌冻干粉通常带有咸味、苦味和酸涩味,并且含有较高含量的钠钾离子,服用量大时存在健康风险,冻干生产后无法即食(直接食用),需要添加大量的辅料进行稀释和调味改良后才可食用。
5.因此,目前市面上销售的益生菌产品,均为益生菌冻干粉复配大比例的辅料(例如,辅料比例占90-95%wt)进行稀释调味后的制品,并非纯的益生菌冻干粉。然而,添加辅料必然会大大降低益生菌产品的活菌含量,也正因为如此,目前市售的益生菌产品的有效活菌含量一般较低(例如在100-500亿cfu/克),从而限制了服用者的活菌摄入量,影响益生菌菌株的功效发挥,也增加了不必要的辅料摄入。
6.另一方面,鉴于冷冻干燥的过程中,细胞膜上的脂肪酸、蛋白结构发生变化,导致细胞膜的完整性被破坏,以及细胞内外的冰晶生长导致细胞机械损伤,冻干引发的溶质效应等造成的细胞代谢损伤等,对于益生菌冻干产品的活菌存活率有很大影响。因此,现有技术对益生菌进行冷冻干燥前一般会用冻干保护剂对菌体进行包埋,减小冷冻干燥对益生菌造成的损伤,提高存活率。目前在提高益生菌冷冻干燥存活率的研究中,主要着眼于保护剂种类的筛选和复配,例如,冻干保护剂的配方中,一般会复配表面活性剂(诸如甘油、聚乙二醇等),蛋白类保护剂(诸如脱脂奶粉、乳清蛋白粉等),糖类保护剂(诸如蔗糖、麦芽糊精、乳糖、海藻糖等),维生素c,以及谷氨酸钠等。此外,有机酸是益生菌的主要代谢产物,在发酵
生产后的离心环节、以及离心后与冻干保护剂的乳化混合环节,有机酸会持续累积,因此,在冻干保护剂中或者在乳化混合环节需要加入酸性调节剂,例如磷酸盐缓冲液(磷酸氢二钠/钾-磷酸二氢钠/钾缓冲液)和半胱氨酸盐酸盐等。然而,冻干保护过程中所必须添加的表面活性剂、酸性调节剂等,会进一步增加所获得的益生菌冻干产物中的不良风味、口感,以及钠钾离子含量,会增加潜在的健康风险。
技术实现要素:
7.为了解决上述技术问题,本发明一方面提供了一种益生菌冻干粉的制备方法,其中,
8.所述制备方法包括以下依次进行的步骤:
9.步骤1)发酵生产:益生菌发酵生产获得发酵菌液;
10.步骤2)浓缩离心:对步骤1)获得的发酵菌液进行膜过滤浓缩和离心分离获得菌泥,且控制所述菌泥的含水量落入80~90%wt的范围;
11.步骤3)菌泥洗脱:将步骤2)获得的菌泥与洗脱液以1:5~1:20的重量比混合,搅拌直至获得均匀的菌悬液;静置所述菌悬液,并实时监测所述菌悬液的ph和电导率,直至ph达到平衡且电导率上升速率不高于0.5ms/cm.min;再将所述菌悬液搅拌均匀并进行离心分离,获得洗脱后的菌泥,并控制所述洗脱后菌泥的含水量落入70~80%wt的范围;
12.上述菌泥洗脱操作中,搅拌速度控制在300~500rpm的范围;
13.重复上述的菌泥洗脱操作,直至静置后的所述菌悬液的ph值不低于6.00,电导率不高于10.00ms/cm;
14.所述洗脱液为含有1~5%wt葡萄糖、0.1~2%wt岩藻多糖、0.2~2%wt小苏打和0.1~0.5%wt甘油的纯水溶液;
15.步骤4)冻干保护:将步骤3)获得的洗脱后菌泥与冻干保护剂混合,搅拌获得均匀的乳化菌悬液;
16.步骤5)真空冷冻干燥:将步骤4)获得的所述乳化菌悬液进行真空冷冻干燥制得所述益生菌冻干粉。
17.优选的,所述步骤4)中采用的冻干保护剂,其为含有5~15%wt麦芽糊精、1.5~5%wt海藻多糖、1.5~5%wt岩藻多糖、0.5~2%wt低聚糖、1.0~1.5%wt天然果胶和10~20%wt浓缩果蔬汁的纯水溶液;
18.所述低聚糖选自低聚果糖、低聚半乳糖、低聚木糖、低聚异麦芽糖、水苏糖中的任意一种或任意几种的组合;
19.所述浓缩果蔬汁选自蔓越莓浓缩汁、蓝莓浓缩汁、番茄浓缩汁、芒果浓缩汁、西兰花浓缩汁、柳橙浓缩汁、石榴浓缩汁、苹果浓缩汁中的任意一种或任意几种的组合。
20.优选的,所述步骤4)中,所述步骤3)获得的洗脱后菌泥与所述冻干保护剂以1:1~1:5的重量比混合。
21.优选的,所述发酵生产包括种子富集培养阶段和高密度发酵培养阶段;
22.所述种子富集培养阶段所采用的培养基的碳氮源基础组分选自蛋白胨、酵母膏和牛肉粉中的一种或几种;
23.所述高密度发酵培养阶段所采用的培养基含有0.3~0.8%wt柑橘纤维、0.8~
1.2%wt大豆低聚肽、0.18~0.22%wt大豆分离蛋白、1.8~2.2%wt甜乳清粉、0.5~1.2%wt葡萄糖、3~5%wt白砂糖、0.8~1.2%wt低聚半乳糖、0.3~0.7%wt西兰花汁、0.18~0.22%wt番茄汁、0.18~0.22%wt低聚果糖、0.18~0.22%wt低聚异麦芽糖、0.5~1.0%wt柠檬酸钠以及0.1~0.5%wt甘油;且其起始ph值为7.0-7.5。
24.优选的,所述高密度发酵培养阶段所采用的培养基含有0.5%wt柑橘纤维、1%wt大豆低聚肽、0.2%wt大豆分离蛋白、2%wt甜乳清粉、0.8%wt葡萄糖、4%wt白砂糖、1%wt低聚半乳糖、0.5%wt西兰花汁、0.2%wt番茄汁、0.2%wt低聚果糖、0.2%wt低聚异麦芽糖、0.75%wt柠檬酸钠以及0.2%wt甘油。
25.优选的,所述种子富集培养阶段包括一级富集培养和二级富集培养,所述一级富集培养的ph控制在4.5~5.0,所述二级富集培养的ph控制在3.5~4.0;
26.所述高密度发酵培养阶段的ph控制在3.8~4.2。
27.优选的,所述步骤3)重复1-3次的菌泥洗脱操作。
28.优选的,在所述步骤2)中,所述膜过滤浓缩将所述发酵菌液的体积浓缩4-6倍,所述离心分离采用的离心转速为10000-12000rpm。
29.优选的,所述膜过滤浓缩采用孔径为100~200nm的陶瓷膜,在跨膜压力100-150kpa下进行处理;所述离心分离采用碟片式离心机,进料量为10~20kg/min,出料间隔为3~5min。
30.本发明另一方面提供了一种益生菌冻干粉,其中,所述益生菌冻干粉采用如上述的制备方法直接制得,且所述益生菌冻干粉的含水量为2~8%wt。
31.本发明涉及一种益生菌冻干粉的制备方法;本发明方法所获得的益生菌冻干粉具有更高的活菌含量和更低的钠离子含量,并且口感风味优良,无需稀释,也无需添加辅料进行调味改良;本发明方法所获得的益生菌冻干粉可以直接食用,可以直接作为“即食”、高活菌含量的益生菌终产品;此外,本发明方法所采用的冻干保护剂不需要添加表面活性剂和酸性调节剂,因此获得的益生菌冻干粉更为健康,口感更优。
具体实施方式
32.关于术语的解释说明如下:
33.术语“益生菌”,是指一类对宿主有益的活性微生物,是定植于人体肠道系统内,能产生确切健康功效从而改善宿主微生态平衡、发挥对肠道有益作用的活性有益微生物的总称,大致分为乳杆菌类、双歧杆菌类和链球菌类等;本技术文件中所提及的益生菌,包括但不限于:诸如鼠李糖乳杆菌、副干酪乳杆菌、干酪乳杆菌、嗜酸乳杆菌、卷曲乳杆菌、格氏乳杆菌、植物乳杆菌、瑞士乳杆菌、罗伊氏乳杆菌、唾液乳杆菌、约氏乳杆菌、发酵乳杆菌、保加利亚乳杆菌的乳杆菌类益生菌;诸如乳双歧杆菌、动物双歧杆菌、长双歧杆菌、短双歧杆菌、青春双歧杆菌、两歧双歧杆菌、婴儿双歧杆菌的双歧杆菌类益生菌,以及诸如嗜热链球菌、唾液链球菌的链球菌类益生菌。
34.在本发明的一个具体实施方案中,提供了一种益生菌冻干粉的制备方法,其中,所述制备方法包括以下依次进行的步骤:
35.步骤1)发酵生产:益生菌发酵生产获得发酵菌液;
36.步骤2)浓缩离心:对步骤1)获得的发酵菌液进行膜过滤浓缩和离心分离获得菌
泥,且控制所述菌泥的含水量落入80~90%wt的范围;
37.步骤3)菌泥洗脱:将步骤2)获得的菌泥与洗脱液以1:5~1:20的重量比混合,搅拌直至获得均匀的菌悬液;静置所述菌悬液,并实时监测所述菌悬液的ph和电导率,直至ph达到平衡且电导率上升速率不高于0.5ms/cm.min;再将所述菌悬液搅拌均匀并进行离心分离,获得洗脱后的菌泥,并控制所述洗脱后菌泥的含水量落入70~80%wt的范围;
38.上述菌泥洗脱操作中,搅拌速度控制在300~500rpm的范围;
39.重复上述的菌泥洗脱操作,直至静置后的所述菌悬液的ph值不低于6.00,电导率不高于10.00ms/cm;
40.所述洗脱液为含有1~5%wt葡萄糖、0.1~2%wt岩藻多糖、0.2~2%wt小苏打和0.1~0.5%wt甘油的纯水溶液;
41.步骤4)冻干保护:将步骤3)获得的洗脱后菌泥与冻干保护剂混合,搅拌获得均匀的乳化菌悬液;
42.步骤5)真空冷冻干燥:将步骤4)获得的所述乳化菌悬液进行真空冷冻干燥制得所述益生菌冻干粉。
43.本技术背景技术中阐述了,为了提高益生菌产品的活菌含量和数量,本领域技术人员因受限于基础理论和普遍性思维,通常聚焦于“发酵生产”和“冷冻干燥”这两个技术环节进行改进。现有技术中为提高发酵生物量所采用的发酵培养基一方面添加大量的钠钾无机盐,另一方面所选择的碳源氮源基础组分以及微量元素会产生大量不良风味物质,即使经过后续的离心操作,但菌体的胞内物质以及菌体表面粘附的代谢产物所携带的离子和不良风味物质仍会进入到后续的冷冻干燥环节,留在最终的益生菌冻干粉中。现有技术为提高益生菌冷冻干燥存活率,主要着眼于冻干保护剂种类的筛选和复配,冻干保护剂所必须添加的表面活性剂、酸性调节剂等,会进一步增加所获得的益生菌冻干产物中的不良风味、口感,以及钠钾离子含量;冻干操作后制得的益生菌冻干产物无法直接食用。
44.因此,现有市售的益生菌产品都需要在冻干产物的基础上添加大量辅料进行稀释和调味改良,必然会大大降低益生菌产品的活菌含量,以及益生菌冻干产物中高钠钾离子含量所带来的健康风险,限制了服用者的摄入量,影响益生菌菌株功效发挥。
45.为解决上述的问题,本技术的发明人在已有研究中所公开的“发酵培养基的配方”和“冷冻保护剂的配方”改进方案基础上做进一步改良,但发现始终无法兼顾到发酵生物量/冷冻存活率与冻干产品中离子和不良风味物质残留问题。发明人也曾尝试对后续的浓缩离心的操作参数进行改进,但进一步去除不良风味物质的同时也严重影响到了益生菌的活力。
46.此外,现有技术中也有公开采用柠檬酸钠或磷酸钠溶液对发酵生产获得的发酵菌液先进行“蛋白洗脱”、再进行“浓缩离心”的方案(即在浓缩离心之前进行蛋白洗脱的操作)。发明人在研发中也尝试重复该操作方案,并做了进一步改良研究,但发现仍无法解决离子残留的问题。
47.由此,发明人转向从其他技术环节寻找突破。
48.发明人在研究中发现,离心后获得的菌泥与冻干保护剂混合时,带入未利用完的培养基组分以及发酵代谢产物,并且胞内的高浓度离子(钠钾离子)以及有机酸会持续地释放到乳化液中,导致了乳化液的高盐和酸性环境;为避免高盐酸性环境在冻干操作中对菌
体的损伤,冻干保护剂中就必须添加表面活性剂和酸性调节剂。
49.然而,基于现有技术的常规操作,以及长期以来本领域技术人员所形成的思维定势,经过“浓缩离心”后获得的菌泥,一直以来都是直接与冻干保护剂混合;原因是,按照现有理论,若对“浓缩离心”后的菌泥进行洗脱处理一般会导致菌量的损失和菌活力的严重下降。
50.发明人放弃了本领域技术人员基于常规思维通常会选择的两个关键工艺,转而尝试在“浓缩离心”之后、“冻干保护”之前进行“菌泥洗脱”的操作,同时对“菌泥洗脱”的操作参数进行了大量的实验研究。研究后发现,在将浓缩离心后的菌泥含水量控制在一定范围的基础上,采用特定配方的洗脱液在特定的搅拌速度下进行混悬,特别是,将形成的菌悬液静置一段时间,直至ph达到平衡且电导率上升速率不高于0.5ms/cm.min时,再进行离心脱除洗脱液,并控制洗脱后菌泥的含水量落入一定范围;这样的操作能够很大程度上避免菌体衰亡的产生、菌活力的降低,与此同时确保了菌体的胞内外物质获得充分交换(盐离子、有机酸和其他不良风味物质进入到洗脱液中,通过后续的离心操作进行脱除)。经过本技术特定的“菌泥洗脱”操作后,菌泥恢复到中性或微酸性,菌泥中的盐离子以及其他加剧冻干损伤的物质大大减少,后续与之混合乳化的冻干保护剂不需要再添加表面活性剂和酸性调节剂。
51.在本发明的一个优选实施方案中,所述步骤4)中采用的冻干保护剂,其为含有5~15%wt麦芽糊精、1.5~5%wt海藻多糖、1.5~5%wt岩藻多糖、0.5~2%wt低聚糖、1.0~1.5%wt天然果胶和10~20%wt浓缩果蔬汁的纯水溶液;
52.所述低聚糖选自低聚果糖、低聚半乳糖、低聚木糖、低聚异麦芽糖、水苏糖中的任意一种或任意几种的组合;
53.所述浓缩果蔬汁选自蔓越莓浓缩汁、蓝莓浓缩汁、番茄浓缩汁、芒果浓缩汁、西兰花浓缩汁、柳橙浓缩汁、石榴浓缩汁、苹果浓缩汁中的任意一种或任意几种的组合。
54.经过本技术发明人的试验研究发现,上述优选方案中的冻干保护剂配方,无需添加酸性调节剂,无需添加常规的表面活性剂,只需要在调整常规的糖类保护剂配比的基础上,再添加特定量的天然果胶和天然果蔬浓缩汁作为抗氧化剂就能够保证冻干存活率以及冻干产品的长期保存稳定性(货架稳定性)。
55.在本技术的一个优选实施方案中,所述发酵生产包括种子富集培养阶段和高密度发酵培养阶段;所述种子富集培养阶段所采用的培养基的碳氮源基础组分选自蛋白胨、酵母膏和牛肉粉中的一种或几种;
56.所述高密度发酵培养阶段所采用的培养基含有0.3~0.8%wt柑橘纤维、0.8~1.2%wt大豆低聚肽、0.18~0.22%wt大豆分离蛋白、1.8~2.2%wt甜乳清粉、0.5~1.2%wt葡萄糖、3~5%wt白砂糖、0.8~1.2%wt低聚半乳糖、0.3~0.7%wt西兰花汁、0.18~0.22%wt番茄汁、0.18~0.22%wt低聚果糖、0.18~0.22%wt低聚异麦芽糖、0.5~1.0%wt柠檬酸钠以及0.1~0.5%wt甘油;且其起始ph值为7.0-7.5。
57.经过本技术发明人的试验研究发现,仅在种子富集培养阶段采用常规的以蛋白胨、酵母膏和牛肉粉为基础碳氮源的培养基,而在高密度发酵培养阶段放弃了常规的碳氮源基础原料,采用上述特定组分复配的培养基,能够进一步减少发酵培养阶段的不良风味物质(酸涩味风味物质)和钠钾离子产生,进一步去除了酸涩味和咸腥味,获得的益生菌冻
干粉的风味口感更优良,与此同时能够在保证发酵生物量的同时,还进一步提高了益生菌冻干粉的活菌含量。
58.以下通过实施例对本发明作进一步的说明,但本发明并不限于这些具体实施方式。
59.实施例1——鼠李糖乳杆菌冻干粉的制备方法
60.实施例1的制备方法包括发酵生产、浓缩离心、菌泥洗脱、冻干保护和冷冻干燥五个步骤,具体如下:
61.步骤1)发酵生产:益生菌发酵生产获得发酵菌液;
62.在本技术的一个具体实施方案中,益生菌的发酵生产可以采用常规的发酵培养基以及生产工艺。例如,鼠李糖乳杆菌的发酵生产可以参考文献《鼠李糖乳杆菌yyjp-2高密度发酵的初步研究》或《鼠李糖乳杆菌(attc53103)高密度生产工艺研究》中发酵培养基及其生产工艺。
63.具体在本实施例中,采用的鼠李糖乳杆菌的菌种为鼠李糖乳杆菌rs01(cgmccno.24082);发明人重复文献《鼠李糖乳杆菌yyjp-2高密度发酵的初步研究》的工艺,获得了鼠李糖乳杆菌的发酵菌液2000kg,其活菌含量为8.2
×
109cfu/ml。
64.步骤2)浓缩离心:对步骤1)获得的发酵菌液进行膜过滤浓缩和离心分离获得菌泥;
65.在本技术的一个具体实施方案中,在步骤2)中,膜过滤浓缩将发酵菌液浓缩4-6倍,离心分离采用的离心转速为10000-12000rpm。
66.在本技术的一个优选实施方案中,所述膜过滤浓缩采用孔径为100~200nm的陶瓷膜,在跨膜压力100-150kpa下进行处理;所述离心分离采用碟片式离心机,进料量为10~20kg/min,出料间隔为3~5min。
67.具体在本实施例中,采用购自南京翃翌纳滤膜有限公司的型号为njyh-3的陶瓷膜装置(孔径100nm,面积3m2),在跨膜压力130kpa下,对步骤1)获得的发酵菌液进行膜浓缩处理,将发酵菌液浓缩5倍;再送入碟片式离心机(购自德国gea公司,型号为mse230-777)进料量约为20kg/min,出料间隔为3min,离心转速约为10000rpm。
68.在本技术的一个具体实施方案中,将步骤2)所获得的菌泥的含水量控制在80%~90%。具体在本实施例中,浓缩离心后获得的菌泥的含水量约为87%,质量约为48kg。
69.步骤3)菌泥洗脱
70.在本发明的一个具体实施方案中,将步骤2)获得的菌泥与洗脱液以1:5~1:20的重量比混合,搅拌直至获得均匀的菌悬液;静置所述菌悬液,并实时监测所述菌悬液的ph和电导率,直至ph达到平衡且电导率上升速率不高于0.5ms/cm.min;再将所述菌悬液搅拌均匀并进行离心分离,获得洗脱后的菌泥,并控制所述洗脱后菌泥的含水量落入70~80%wt的范围;上述菌泥洗脱操作中,搅拌速度控制在300~500rpm的范围;重复上述的菌泥洗脱操作,直至静置后的所述菌悬液的ph值不低于6.00,电导率不高于10.00ms/cm;所述洗脱液为含有1~5%wt葡萄糖、0.1~2%wt岩藻多糖、0.2~2%wt小苏打和0.1~0.5%wt甘油的纯水溶液;
71.在本技术的一个优选实施方案中,所述步骤3)在5~25摄氏度的温度下进行,并且所述步骤2)获得的菌泥与所述洗脱液以1:8~1:15的重量比混合。
72.在本技术的一个优选实施方案中,所述步骤3)重复0-3次,即菌泥洗脱1-4次。多次洗脱便于梯度稀释,更好地实现菌体的胞内外物质充分交换和平衡,但多次洗脱必然也会带来活菌量和菌活力的损失。本领域技术人员基于本技术的方案和精神实质,根据实际情况和具体需求来权衡调整菌泥洗脱的次数。
73.具体在本实施例中,所采用的洗脱液为含有约1.5%wt葡萄糖、0.8%wt岩藻多糖、0.7%wt小苏打和0.16%wt甘油的纯水溶液,配制后110度灭菌20min,再降温至15摄氏度。
74.具体在本实施例中,在约15摄氏度的温度下,将步骤2)获得的48kg菌泥与480kg洗脱液(以约1:10的质量比)在搅拌罐中混合,以300-500rpm的搅拌速度,搅拌约10-15min,获得均匀的菌悬液;再静置该菌悬液,并监控菌悬液中的ph和电导率,直至达到ph达到平衡(例如,具体在本实施例中,3min内ph值上升不超过5%),并且,电导率上升速率不高于0.5ms/cm.min;再立刻开启搅拌,在300~500rpm搅拌下搅拌均匀,再将该菌悬液转移至高速离心机以12000-14000rpm的转速进行离心分离,并控制洗脱后菌泥的含水量约为76%wt。
75.具体在本实施例中,重复上述洗脱操作2次(即洗脱3次),具体来说,经过两次上述的洗脱操作之后,经第三次静置后的菌悬液(待ph达到平衡且电导率上升速率不高于0.5ms/cm.min),测得其ph值约为6.1(达到ph不低于6的标准),其电导率约为9.6ms/cm(电导率达到不高于10ms/cm的标准),再将其搅拌均匀,并进行离心分离,获得最终洗脱后的菌泥,其含水量约为73%,重量约为31kg。
76.步骤4)冻干保护:将步骤3)获得的洗脱后菌泥与冻干保护剂混合,搅拌获得均匀的乳化菌悬液。
77.在本技术的一个优选实施方案中,所述步骤4)中采用的冻干保护剂,其为含有5~15%wt麦芽糊精、1.5~5%wt海藻多糖、1.5~5%wt岩藻多糖、0.5~2%wt低聚糖、1.0~1.5%wt天然果胶和10~20%wt浓缩果蔬汁的纯水溶液;
78.所述低聚糖选自低聚果糖、低聚半乳糖、低聚木糖、低聚异麦芽糖、水苏糖中的任意一种或任意几种的组合;
79.所述浓缩果蔬汁选自蔓越莓浓缩汁、蓝莓浓缩汁、番茄浓缩汁、芒果浓缩汁、西兰花浓缩汁、柳橙浓缩汁、石榴浓缩汁、苹果浓缩汁中的任意一种或任意几种的组合。
80.在本技术的一个具体实施方案中,步骤4)中,步骤3)获得的洗脱后菌泥与冻干保护剂以1:1~1:5的重量比混合。
81.具体在本实施例中,冻干保护剂为含有10%wt麦芽糊精、2.5%wt海藻多糖、2.5%wt岩藻多糖、1%wt低聚果糖、1.2%wt柑橘纤维和15%wt蔓越莓汁的纯水溶液。
82.具体在本实施例中,洗脱后菌泥31kg与该冻干保护剂93kg(以约1:3的重量比)在搅拌罐中混合,搅拌速度300-500rpm,搅拌约10-15min,直至获得均匀(无结块)的乳化菌悬液。
83.步骤5)真空冷冻干燥:将步骤4)获得的所述乳化菌悬液进行真空冷冻干燥制得所述益生菌冻干粉。
84.在本技术的具体实施方案中,真空冷冻干燥的操作可以采用现有技术中的常规工艺。
85.具体在本实施例中,真空冷冻干燥操作过程具体如下:
86.冷冻阶段:将乳化菌悬液以2℃/min的降温速率降至-45~-50℃,保持约60min;
87.一步干燥阶段:以1℃/min的升温速率升温至-25℃,维持此温度直至真空度达到约0.10mpa;
88.解析干燥阶段:以4℃/min的升温速率至15℃,维持此温度直至真空度达到约0.02mpa;
89.完成上述操作后,用粉碎机粉碎过筛、包装(例如采用铝箔袋),置于10℃以下保存。
90.实施例2——鼠李糖乳杆菌冻干产品的制备方法
91.实施例2的制备方法与实施例1的不同仅在于:a)步骤1)的发酵生产过程不同;b)步骤3)的洗脱操作只需要重复一次(即洗脱2次)即可。
92.在本技术的一个具体实施方案中,所述发酵生产包括种子富集培养阶段和高密度发酵培养阶段;
93.所述种子富集培养阶段所采用的培养基的碳氮源基础组分选自蛋白胨、酵母膏和牛肉粉中的一种或几种;
94.所述高密度发酵培养阶段所采用的培养基含有0.3~0.8%wt柑橘纤维、0.8~1.2%wt大豆低聚肽、0.18~0.22%wt大豆分离蛋白、1.8~2.2%wt甜乳清粉、0.5~1.2%wt葡萄糖、3~5%wt白砂糖、0.8~1.2%wt低聚半乳糖、0.3~0.7%wt西兰花汁、0.18~0.22%wt番茄汁、0.18~0.22%wt低聚果糖、0.18~0.22%wt低聚异麦芽糖、0.5~1.0%wt柠檬酸钠以及0.1~0.5%wt甘油;且其起始ph值为7.0-7.5。
95.在本技术的一个优选实施方案中,所述种子富集培养阶段包括一级富集培养和二级富集培养,所述一级富集培养的ph控制在4.5~5.0,所述二级富集培养的ph控制在3.5~4.0;所述高密度发酵培养阶段的ph控制在3.8~4.2。
96.优选的,具体在本实施例中,所述高密度发酵培养阶段所采用的培养基含有0.5%wt柑橘纤维、1%wt大豆低聚肽、0.2%wt大豆分离蛋白、2%wt甜乳清粉、0.8%wt葡萄糖、4%wt白砂糖、1%wt低聚半乳糖、0.5%wt西兰花汁、0.2%wt番茄汁、0.2%wt低聚果糖、0.2%wt低聚异麦芽糖、0.75%wt柠檬酸钠以及0.2%wt甘油。
97.具体在本实施例中,发酵生产的具体过程如下:
98.一级种子富集培养:鼠李糖乳杆菌的工作种子,以3-5%接种量接入装有100ml无菌的种子富集培养基的三角瓶中,36-39℃,ph值控制在4.5-5.0,厌氧培养10-15小时,直至od600值达到2.3-2.5,获得一级培养液。
99.二级种子富集培养:取一级培养液,按1-2%接种量接入5l无菌的种子富集培养基中,36-39℃,ph控制在3.5-4.0,厌氧培养10-15小时,直至od600值达到4.5-5.0,获得二级培养液;
100.一级高密度发酵培养:取二级培养液,按1-2%接种量接入200l无菌的高密度发酵培养基中,在36-39℃,50rpm搅拌下,通氮气保持罐压0.01-0.03mpa,ph控制在3.8-4.2,厌氧培养15-20小时,直至od600值达到2.3-2.5,获得三级培养液。
101.二级高密度发酵培养:将三级培养液转移至5000l大罐培养基中,在36-39℃,100rpm搅拌下,通氮气保持罐压0.01-0.03mpa,ph控制在3.8-4.2,厌氧培养15-20小时,直至od600值达到2.3-2.5,停止发酵,获得最终的发酵菌液,并降温至25℃以下。
102.实施例2仅在种子富集培养阶段采用常规的以蛋白胨、酵母膏和牛肉粉为基础碳氮源的培养基,而在高密度发酵培养阶段放弃了常规的碳氮源基础原料,采用上述特定组分复配的培养基,大大减少了发酵培养阶段的不良风味物质的产生,因此,步骤3)的洗脱次数可以减少一次。
103.实施例2的其他操作过程均与实施例1相同,具体不再赘述。
104.实施例3—嗜酸乳杆菌的冻干产品的制备方法
105.实施例3的嗜酸乳杆菌为嗜酸乳杆菌ms28(cgmccno.24084)。
106.实施例3的制备方法包括发酵生产、浓缩离心、菌泥洗脱、冻干保护和冷冻干燥五个步骤;其中步骤1)发酵生产的操作过程同实施例2的步骤1),步骤2)的浓缩离心同实施例1的步骤2),具体不再赘述。
107.实施例3的步骤3)菌泥洗脱——将步骤2)获得的35kg菌泥与525kg洗脱液(以约1:15的质量比)在搅拌罐中混合,以300-500rpm的搅拌速度,搅拌约10-15min,获得均匀的菌悬液;再静置该菌悬液,并监控菌悬液中的ph和电导率,直至达到ph达到平衡,并且,电导率上升速率不高于0.5ms/cm.min;再立刻开启搅拌,在300~500rpm搅拌下搅拌均匀,再将该菌悬液转移至高速离心机以12000-14000rpm的转速进行离心分离,并控制洗脱后菌泥的含水量约为73%wt。
108.具体在本实施例中,重复上述洗脱操作1次(即洗脱2次),具体来说,经过一次上述的洗脱操作之后,经第二次静置后的菌悬液(待ph达到平衡且电导率上升速率不高于0.5ms/cm.min),测得其ph值约为6.2(达到ph不低于6的标准),其电导率约为9.8ms/cm(电导率达到不高于10ms/cm的标准),再将其搅拌均匀,并进行离心分离,获得最终洗脱后的菌泥,其含水量约为74%,重量约为22kg。
109.实施例3的步骤4)冻干保护——冻干保护剂为含有5%wt麦芽糊精、5%wt海藻多糖、2%wt岩藻多糖、1%wt低聚木糖、1.3%wt柑橘纤维、5%wt胡萝卜浓缩汁和5%wt番茄浓缩汁的纯水溶液。洗脱后菌泥22kg与该冻干保护剂44kg(以约1:2的重量比)在搅拌罐中混合,搅拌速度300-500rpm,搅拌约10-15min,直至获得均匀(无结块)的乳化菌悬液。
110.实施例3的步骤5)真空冷冻干燥同实施例1的步骤5),具体不再赘述
111.实施例4—乳双歧杆菌的冻干产品的制备方法
112.实施例4的乳双歧杆菌为乳双歧杆菌ms106(cgmccno.24079)。
113.实施例4的制备方法包括发酵生产、浓缩离心、菌泥洗脱、冻干保护和冷冻干燥五个步骤;其中步骤1)发酵生产的操作过程同实施例2的步骤1),步骤2)的浓缩离心同实施例1的步骤2),具体不再赘述。
114.实施例4的步骤3)菌泥洗脱——将步骤2)获得的60kg菌泥与300kg洗脱液(以约1:5的质量比)在搅拌罐中混合,搅拌约10-15min,获得均匀的菌悬液;再静置该菌悬液,并监控菌悬液中的ph和电导率,直至达到ph达到平衡,并且,电导率上升速率不高于0.5ms/cm.min;再立刻开启搅拌,在300~500rpm搅拌下搅拌均匀,再将该菌悬液转移至高速离心机以12000-14000rpm的转速进行离心分离,并控制洗脱后菌泥的含水量约为75%wt。
115.具体在本实施例中,重复上述洗脱操作3次(即洗脱4次),具体来说,经过三次上述的洗脱操作之后,经第四次静置后的菌悬液(待ph达到平衡且电导率上升速率不高于0.5ms/cm.min),测得其ph值约为6(达到ph不低于6的标准),其电导率约为9.7ms/cm(电导
率达到不高于10ms/cm的标准),再将其搅拌均匀,并进行离心分离,获得最终洗脱后的菌泥,其含水量约为77%,重量约为36kg。
116.实施例4的步骤4)冻干保护——冻干保护剂为含有15%wt麦芽糊精、1.5%wt海藻多糖、3.0%wt岩藻多糖、2%wt水苏糖、1.5%wt柑橘纤维、2%wt浓缩橙汁、10%葡萄浓缩汁的纯水溶液;洗脱后菌泥36kg与该冻干保护剂144kg(以约1:4的重量比)在搅拌罐中混合,搅拌速度300-500rpm,搅拌约10-15min,直至获得均匀(无结块)的乳化菌悬液。
117.实施例4的步骤5)真空冷冻干燥的同实施例1的步骤5),具体不再赘述。
118.效果数据
119.为验证上述实施例1-4制备方法获得的益生菌冻干产品的效果,进行了下列对比实验。
120.对比例1的制备方法与实施例1的不同之处仅在于:省略了步骤3)的菌泥洗脱的操作;其他步骤均与实施例1相同。
121.同样的,对比例2-4与对应的实施例2-4的不同之处仅在于,省略了步骤3)的菌泥洗脱的操作。
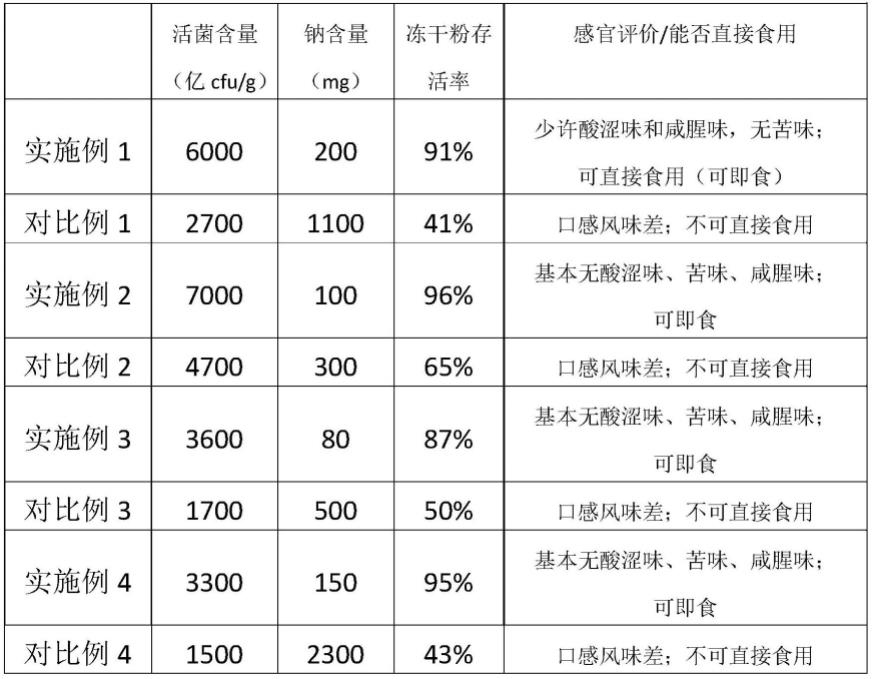
122.实施例1-4和对比例1-4,均各自做5个平行实验,按照益生菌生产工艺中所采用的常规检测方法对活菌含量、发酵菌数、钠含量和冻干粉存活率进行了检测;结果参见下表1。
123.此外,关于口感和风味的评价——挑选身体健康,无不良嗜好的20位食品专业研究人员组成感官评价小组。每个测试样品用三位数随机数编号,评价实施例1-4和对比例1-4(各自做5个平行实验)益生菌冻干粉的口感和风味(酸涩味、苦味、咸腥味),并作出整体的感官评价和能否直接食用的判断;结果参见下表1。
124.表1
[0125][0126]
1、活菌含量和冻干存活率
[0127]
从上表1可以看出,上述实施例1-4的益生菌冻干粉的平均活菌含量分别为:6000、7000、3600和3300亿cfu/g,远高于现有即食型益生菌粉的活菌含量水平(100~500亿cfu/g)。
[0128]
其次,对比例1-4获得的益生菌冻干粉的平均活菌含量,相比与实施例1-4的数据,分别降低了55%、32.9%、52.8%、54.5%。
[0129]
从冻干存活率上看,实施例1-4都在87%以上,而对比例1-4在41%~65%之间。
[0130]
因此,采用本实施例1-4的方法获得益生菌冻干粉,与省略了菌泥洗脱操作的对比例1-4的相比,显著提高了冻干存活率和活菌含量。
[0131]
2、钠离子含量
[0132]
从上表1可以看出,实施例1-4的益生菌冻干粉的纳离子含量显著低于对比例1-4。
[0133]
由于对比例1-4获得的益生菌冻干粉含有高钠钾离子,无法直接食用,需要通过稀释的方式降低盐离子浓度才能够获得最终可食用的产品,从而进一步降低了最终产品中的活菌含量。
[0134]
此外,钠钾离子服用过多,存在一定的健康风险;因此,即使将对比例1-4的产品稀释调配成可食用的终产品,其上市后也需要严格限制食用者的日均食用量,从而也限制了益生菌的摄入量。
[0135]
3、口感和风味
[0136]
从上表1可以看出,上述实施例1-4的益生菌冻干粉口感风味优良,可即食(冻干操作获得的冻干粉可以直接食用)。
[0137]
但对比例1-4的冻干粉口感风味差,无法直接食用,还需要在对比例1-4的冻干粉的基础上添加大量辅料进行稀释和调味改良才能获得最终可食用的产品,从而进一步降低了最终产品中的活菌含量。
[0138]
从上述对比可以看出,本技术实施例1-4获得的益生菌冻干粉具有更高的活菌含量和更低的钠含量,并且口感风味优良,无需稀释,也无需添加辅料调味改良,因此,实施例1-4的益生菌冻干粉可以直接食用,可以直接作为“即食”、高活菌含量的益生菌终产品;此外,本技术实施例1-4的工艺中所采用的冻干保护剂不需要再添加表面活性剂和酸性调节剂,因此获得的益生菌冻干粉更为健康,口感更优。
[0139]
4、关于实施例1与实施例2的对比
[0140]
实施例1与实施例2的区别在于,实施例1的步骤1)(发酵生产)采用的是常规的发酵生产工艺以及常规的高密度发酵培养基,实施例2的步骤1)的高密度发酵阶段放弃了常规的碳氮源基础原料,而采用特定组分复配的培养基。相比实施例1,实施例2的菌泥洗脱操作次数不仅可以减少一次,实施例2最终获得的益生菌冻干粉还进一步减少了发酵培养阶段的不良风味物质(酸涩味风味物质)和钠钾离子产生,进一步去除了酸涩味和咸腥味,获得的益生菌冻干粉的风味口感更优良,与此同时还获得了更高的产品活菌含量。
[0141]
应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施方式中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
[0142]
上文所列出的一系列的详细说明仅仅是针对本发明的可行性实施方式的具体说明,它们并非用以限制本发明的保护范围,凡未脱离本发明技艺精神所作的等效实施方式或变更均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1