用于肠道准备的特医食品及其制备方法与流程
1.本技术属于特医食品技术领域,具体涉及一种用于肠道准备的特医食品及其制备方法。
背景技术:
2.在很多诊断和手术过程开始之前,比如结肠镜检查、钡剂灌肠检查和结肠手术,肠道清洗都是很重要的。其中,结肠镜是筛查、诊断和治疗结肠病变的重要手段,其诊断的准确性和治疗的安全性与肠道准备的质量密切相关,充分的肠道准备可使患者获得较高的肠道清洁度,对实现高质量的肠镜诊疗具有重要意义。肠道准备不充分可降低结肠镜检查的有效性和安全性,且影响肠镜检查的腺瘤检出率。因此,对于肠道准备病人,高质量的肠道准备至关重要。
3.临床过程中在肠道准备的影响因素中,饮食规范可减少肠道中残留的食物残渣,从而提高肠道准备的清洁度。多项研究显示,与进食流质饮食相比,内镜检查前进食低渣/低纤维饮食(水不溶性纤维)的患者对肠道准备的耐受能力和再次进行类似肠道准备的意愿均较高,且肠道准备质量和不良反应率均无明显差异。
4.为了提高肠道准备的效果,传统方法一般包括饮食控制、缓泻剂、泻剂和灌肠剂。磷酸钠溶液和柠檬酸镁/皮可硫酸钠溶液也得到使用。但是在实际应用中发现,传统方法都有许多缺点:如饮食控制和缓泻剂耗灌肠使病人难受;泻剂、灌肠和磷酸盐的方法还可导致危险的脱盐脱水。而且该些方法还存在肠道中食物残渣清除效果不理想和使用量大等不足。
5.为了克服该传统肠道准备方法所存在的不足,目前也有公开报道关于用于肠道准备的特医食品,但是在实际应用中发现,现有报道的用于肠道准备的特医食品存在肠道准备效果不理想,有副作用等的不足。
技术实现要素:
6.本技术的目的是提供一种特医食品及其制备方法,以解决现有清肠剂或肠道准备特医食品存在肠道准备效果不理想、肠道准备时间长和易导致患者不适或脱盐脱水等副作用的技术问题。
7.为了实现上述申请目的,本技术的第一方面,提供了一种特医食品。本技术特医食品用于肠道镜检准备和/或胃部镜检准备的特医食品,包括如下重量份的组分:
8.[0009][0010]
本技术的第二方面,提供了本技术特医食品的制备方法。本技术特医食品的制备方法包括如下步骤:
[0011]
按照本技术特医食品的配方组分分别量取各原料组分;
[0012]
将量取的各组分进行混料处理,得到特医食品。
[0013]
与现有技术相比,本技术特医食品通过所含的组分复配,并在发挥各组分常规作用的基础上,起到了增效作用,赋予本技术特医食品具有以下有益效果:
[0014]
1.能够用于肠道镜检准备和/或胃部镜检准备中食用,并能够有效缩短肠道镜检准备和/或胃部镜检准备的时间,提高肠道镜检准备和/或胃部镜检准备效率;
[0015]
2.能够有效降低肠道和/或胃部中的食物内残留物,减少肠腔液发泡量,从而提高肠道镜检和胃部镜检的清晰度,降低气泡对镜检视野的干扰,以提高肠道镜检准备和/或胃部镜检准备的质量和有效性,而且还能够提高肠道镜检和胃部镜检的安全性;
[0016]
3.有利于规范患者的肠道镜检准备和/或胃部镜检准备病前24小时内的饮食,提供饱腹感,减少肠道和胃部食物残渣生成,提供各种营养素及电解质,明显减少肠道清洗剂的用量,提高镜检准备的安全性和患者对肠道准备的耐受能力。
[0017]
4.本技术特医食品分散体系稳定,其质量稳定,有益于营养成分含量均匀一致。
[0018]
本技术特医食品的制备方法将配方组分按照比例混合处理,使得配制的特医食品分散体系和质量稳定,而且能够使得给组分之间起到增效作用,赋予配制的特医食品能够提高镜检患者的饱腹感和耐受能力,减少肠道和胃部食物残渣生成,减少肠腔液气泡的产生量,并提供所需营养素及电解质,促进肠道清洁,提高肠道镜检准备和/或胃部镜检准备质量和安全性能以及镜检准备效果。另外,本技术特医食品的制备方法工艺条件易控,而且还能够保证配制的特医食品的性能、质量和功能稳定。
附图说明
[0019]
图1为本技术实施例特医食品的制备方法流程示意图;
[0020]
图2为图1中步骤s02中各组分进行混料处理的方法工艺流程示意图;
[0021]
图3为患者服用复方聚乙二醇电解质散后进行第一次胃镜的照片;
[0022]
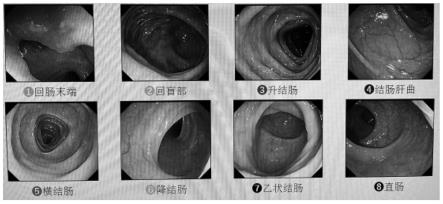
图4为患者服用复方聚乙二醇电解质散后进行第一次肠镜的照片;
[0023]
图5为患者服用实施例3提供的特医食品+复方聚乙二醇电解质散溶液进行第二次胃镜的照片;
[0024]
图6为患者服用实施例3提供的特医食品+复方聚乙二醇电解质散溶液进行第二次
肠镜的照片。
具体实施方式
[0025]
为使本技术实施例的目的、技术方案和技术效果更加清楚,对本技术实施例中的技术方案进行清楚、完整地描述,以下所描述的实施例是本技术一部分实施例,而不是全部的实施例。结合本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本技术保护的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行;所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0026]
在本技术的描述中,术语“和/或”,描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b的情况。其中a,b可以是单数或者复数。字符“/”一般表示前后关联对象是一种“或”的关系。
[0027]
在本技术的描述中,“至少一个”是指一个或者多个,“多个”是指两个或两个以上。“以下至少一项(个)”或其类似表达,是指的这些项中的任意组合,包括单项(个)或复数项(个)的任意组合。例如,“a,b,或c中的至少一项(个)”,或,“a,b,和c中的至少一项(个)”,均可以表示:a,b,c,a-b(即a和b),a-c,b-c,或a-b-c,其中a,b,c分别可以是单个,也可以是多个。
[0028]
需要理解的是,本技术实施例中所提到的相关成分的重量不仅仅可以指代各组分的具体含量,也可以表示各组分间重量的比例关系,因此,只要是按照本技术实施例相关组分的含量按比例放大或缩小均在本技术公开的范围之内。具体地,本技术实施例中所述的重量可以是μg、mg、g、kg等化工领域公知的质量单位。
[0029]
另外,除非上下文另外明确地使用,否则词的单数形式的表达应被理解为包含该词的复数形式。术语“包括”或“具有”旨在指定特征、数量、步骤、操作、元件、部分或者其组合的存在,但不用于排除存在或可能添加一个或多个其它特征、数量、步骤、操作、元件、部分或者其组合。
[0030]
第一方面,本技术实施例提供了一种特医食品。本技术实施例特医食品包括如下重量份的组分:
[0031]
[0032][0033]
其中,本技术实施例特医食品所含的水构成了溶剂体系,实施例中,水组分的重量份可以是1050~5800份,具体可以但不仅仅为1400重量份。具体可以在910~7200份,进一步在1050~5800份之间根据需要进行调整。另外,水组分应该符合医药或食品卫生等要求,如符合gb/t 50331-2002城市居民生活用水量标准或者《中国药典》2020年版纯化水标准的要求。
[0034]
本技术实施例特医食品所含的魔芋粉能够提供膳食纤维和胶体性质,在营养成分补充剂的基础上,能够在其他组分的增效作用下,提高胃和肠道的蠕动,从而提高胃部和肠道的镜检准备效果,并降低特医食品的副作用。实施例中,魔芋粉选用粘度为13000~28000mpa.s的魔芋粉。其中,魔芋粉的粘度可以按照ny/t 494-2010魔芋粉标准项下6.2.1粘度测试方法测得,采用dnj-1型粘度计,4号转子,12r/min,30℃。另外,该魔芋粉组分也应该符合医药或食品卫生等要求,如符合ny/t 494-2010魔芋粉标准。实施例中,魔芋粉组分的重量份可以是72~630份,具体可以但不仅仅为23重量份。具体可以在9~140份,进一步在72~630份之间根据需要进行调整。
[0035]
本技术实施例特医食品所含的果胶和结冷胶起到胶体的作用,能够有效调节特医食品的稳定性,提高其胃部和肠道的镜检准备效果。实施例中,结冷胶组分的重量份可以是0.3~5.1份,具体可以但不仅仅为0.6重量份。具体可以在0.2~7份,进一步在0.3~5.1份之间根据需要进行调整。另外,该结冷胶组分也应该符合医药或食品卫生等要求,如符合gb 25535-2010食品安全国家标准、食品添加剂、结冷胶标准。
[0036]
实施例中,果胶组分可以选用如下特性的果胶:果胶的酯化度(de
°
)为:35%<de
°
≤40%;和/或果胶的酰胺化度(da
°
)为:10%<da
°
≤15%。该de
°
和da
°
的果胶组分能够提高患者的胃肠蠕动能力,提高对肠胃中食物的消化能力,降低肠胃中食物残渣量,同时提高体系的稳定均匀性。具体实施例中,该果胶可以是以柑橘果皮为原料,经提取、精制而得柑橘高酯果胶,再经酰胺化、纯化等工序精制而得低酯果胶,且控制35%<酯化度(de
°
)≤40%,10%<酰胺化度(da
°
)≤15%,如海升果胶型号hsc220,酯化度和酰胺化度检测依据t/hnskjx 005-2021柑橘酰胺化标准中方法。该果胶组分也应该符合医药或食品卫生等要求,如符合gb 25533-2010食品安全国家标准、食品添加剂、果胶标准。实施例中,果胶组分的重量份可以是0.17~10.8份,具体可以但不仅仅为0.4重量份。具体可以在0.1~13份,进一步在0.17~10.8份之间根据需要进行调整。
[0037]
本技术实施例特医食品所含的麦芽糊精和食用葡萄糖等组分提供能量,协助其他组分,提高本技术实施例特医食品的胃部和肠道的镜检准备效果,并降低特医食品的副作用。实施例中,麦芽糊精组分的重量份可以是150~1862份,具体可以但不仅仅为250重量份。具体可以在120~2070份,进一步在150~1862份之间根据需要进行调整。另外,该麦芽
糊精组分也应该符合医药或食品卫生等要求,如符合gb/t 20884-2007麦芽糊精标准。
[0038]
实施例中,食用葡萄糖组分的重量份可以是73~420份,具体可以但不仅仅为220重量份。具体可以在90~530份,进一步在73~420份之间根据需要进行调整。该食用葡萄糖组分也应该符合医药或食品卫生等要求,如符合gb/t 20880-2018食用葡萄糖标准。
[0039]
本技术实施例特医食品所含的乳糖醇、异构化乳糖液、低聚果糖、抗坏血酸、维生素e、盐酸硫胺素、盐酸吡哆醇、烟酸、肌醇、牛磺酸、葡萄糖酸锌、硫酸镁、l-乳酸钙、食用盐、氯化钾等组分分别发挥各自的营养补充剂和矿物质以及电解质等相关作用,他们之间起到营养和电解质等增效作用,提高了患者肠道镜检准备和/或胃部镜检准备中的安全性能和耐受力。
[0040]
实施例中,乳糖醇组分的重量份可以是11~176份,具体可以但不仅仅为30重量份。具体可以在6~280份,进一步在11~176份之间根据需要进行调整。该乳糖醇组分也应该符合医药或食品卫生等要求,如符合gb 1886.98-2016食品安全国家标准、食品添加剂、乳糖醇(又名4-β-d吡喃半乳糖-d-山梨醇)标准。
[0041]
实施例中,异构化乳糖液组分的重量份可以是0.42~9.4份,具体可以但不仅仅为2重量份。具体可以在0.35~11份,进一步在0.42~9.4份之间根据需要进行调整。该异构化乳糖液组分也应该符合医药或食品卫生等要求,如符合gb 1886.176-2016食品安全国家标准、食品添加剂、异构化乳糖液标准。
[0042]
实施例中,低聚果糖组分的重量份可以是13~81份,具体可以但不仅仅为20重量份。具体可以在11~96份,进一步在13~81份之间根据需要进行调整。该低聚果糖组分也应该符合医药或食品卫生等要求,如符合gb/t 23528-2009低聚果糖标准。
[0043]
实施例中,抗坏血酸组分的重量份可以是0.3~2.6份,具体可以但不仅仅为0.51重量份。具体可以在0.2~3.3份,进一步在0.3~2.6份之间根据需要进行调整。该抗坏血酸组分也应该符合医药或食品卫生等要求,如符合gb 14754-2010食品安全国家标准、食品添加剂、维生素c(抗坏血酸)标准。
[0044]
实施例中,维生素e组分的重量份可以是0.06~0.47份,具体可以但不仅仅为0.08重量份。具体可以在0.05~0.6份,进一步在0.06~0.47份之间根据需要进行调整。该维生素e组分也应该符合医药或食品卫生等要求,如符合gb 1886.233-2016食品安全国家标准、食品添加剂、维生素e标准。
[0045]
实施例中,盐酸硫胺素组分的重量份可以是0.003~0.051份,具体可以但不仅仅为0.005重量份。具体可以在0.002~0.066份,进一步在0.003~0.051份之间根据需要进行调整。该盐酸硫胺素组分也应该符合医药或食品卫生等要求,如符合gb 14751-2010食品安全国家标准、食品添加剂、维生素b1(盐酸硫胺)标准。
[0046]
实施例中,盐酸吡哆醇组分的重量份可以是0.001~0.022份,具体可以但不仅仅为0.002重量份。具体可以在0.002~0.066份,进一步在0.001~0.022份之间根据需要进行调整。该盐酸吡哆醇组分也应该符合医药或食品卫生等要求,如符合gb 14753-2010食品安全国家标准、食品添加剂、维生素b6(盐酸吡哆醇)标准。
[0047]
实施例中,烟酸组分的重量份可以是0.01~0.069份,具体可以但不仅仅为0.002重量份。具体可以在0.007~0.093份,进一步在0.01~0.069份之间根据需要进行调整。该烟酸组分也应该符合医药或食品卫生等要求,如符合gb 14757-2010食品安全国家标准、食
品添加剂、烟酸标准。
[0048]
实施例中,肌醇组分的重量份可以是0.09~0.75份,具体可以但不仅仅为0.18份重量份。具体可以在0.07~0.98份,进一步在0.09~0.75份之间根据需要进行调整。该肌醇组分也应该符合医药或食品卫生等要求,如符合gb 1903.42-2020食品安全国家标准、食品营养强化剂、肌醇(环己六醇)标准。
[0049]
实施例中,牛磺酸组分的重量份可以是0.52~5.7份,具体可以但不仅仅为0.9份重量份。具体可以在0.35~8.2份,进一步在0.52~5.7份之间根据需要进行调整。该牛磺酸组分也应该符合医药或食品卫生等要求,如符合gb 14759-2010食品安全国家标准、食品添加剂、牛磺酸标准。
[0050]
实施例中,葡萄糖酸锌组分的重量份可以是0.072~0.69份,具体可以但不仅仅为0.14份重量份。具体可以在0.053~0.77份,进一步在0.072~0.69份之间根据需要进行调整。该葡萄糖酸锌组分也应该符合医药或食品卫生等要求,如符合gb 8820-2010食品安全国家标准、食品添加剂、葡萄糖酸锌标准。
[0051]
实施例中,硫酸镁组分的重量份可以是0.21~2.08份,具体可以但不仅仅为0.37份重量份。具体可以在0.13~2.91份,进一步在0.21~2.08份之间根据需要进行调整。该硫酸镁组分也应该符合医药或食品卫生等要求,如符合gb 29207-2012食品安全国家标准、食品添加剂、硫酸镁标准,无水。
[0052]
实施例中,l-乳酸钙组分的重量份可以是2.7~54.4份,具体可以但不仅仅为6.9份重量份。具体可以在1.5~63.6份,进一步在2.7~54.4份之间根据需要进行调整。该l-乳酸钙组分也应该符合医药或食品卫生等要求,如符合gb 25555-2010食品安全国家标准、食品添加剂、l-乳酸钙标准,五水。
[0053]
实施例中,食用盐组分的重量份可以是0.9~16份,具体可以但不仅仅为2份重量份。具体可以在0.7~21份,进一步在0.9~16份之间根据需要进行调整。该食用盐组分也应该符合医药或食品卫生等要求,如符合gb 2721-2015食品安全国家标准、食用盐标准。
[0054]
实施例中,氯化钾组分的重量份可以是1.1~25份,具体可以但不仅仅为2份重量份。具体可以在0.4~34份,进一步在1.1~25份之间根据需要进行调整。该氯化钾组分也应该符合医药或食品卫生等要求,如符合gb 25585-2010食品安全国家标准、食品添加剂、氯化钾标准。
[0055]
本技术实施例特医食品所含的酸度调节剂能够调节体系的ph,并保证体系ph的稳定,提高各组分之间的增效作用,提高特医食品在镜检准备的效果。实施例中,酸度调节剂组分的重量份可以是0.3~9份,具体可以但不仅仅为1份重量份。具体可以在0.1~11份,进一步在0.3~9份之间根据需要进行调整。另些实施例中,酸度调节剂包括柠檬酸、dl-苹果酸、乳酸、冰乙酸中的至少一种。其中,酸度调节剂如包括柠檬酸、dl-苹果酸、乳酸、冰乙酸中的至少一种也应该符合医药或食品卫生等要求,如柠檬酸符合gb 1886.235-2016食品安全国家标准、食品添加剂、柠檬酸标准,dl-苹果酸符合gb 25544-2010食品安全国家标准、食品添加剂、dl-苹果酸标准,乳酸符合gb 1886.173-2016食品安全国家标准、食品添加剂、乳酸标准,冰乙酸符合gb 1886.10-2015食品安全国家标准、食品添加剂、冰乙酸(又名冰醋酸)标准。
[0056]
在上述各实施例的基础上,本技术实施例特医食品还可以包括矫味剂,以调节本
申请实施例特医食品的口感,实施例中,矫味剂可以包括食品用香精和浓缩果蔬汁,其中,食品用香精可以为0.3~16份,浓缩果蔬汁可以为60~700份。
[0057]
浓缩果蔬汁不仅有能够改善特医食品的口感,还含有人体需要的营养成分,提高人体所需的营养成分,而且不增加在肠道或/和胃部产生食物残渣,保证肠道镜检准备和/或胃部镜检准备效率和效果,提高镜检的清晰度和有效性。实施例中,该浓缩果蔬汁可以包括白葡萄浓缩汁、水蜜桃浓缩汁、浓缩苹果青汁、荔枝浓缩汁、龙眼浓缩汁、椰子浓缩汁、雪梨浓缩汁、青瓜浓缩汁、冬瓜浓缩汁中的至少一种。该些种类浓缩果蔬汁可以丰富本技术实施例特医食品的口感和味道,并丰富营养成分,提高患者对肠道镜检准备和/或胃部镜检准备的耐受能力和安全性。另外,该浓缩果蔬汁组分应该符合医药或食品卫生等要求,如符合gb/t 31121-2014果蔬汁类及其饮料标准或者ny/t 434-2016绿色食品果蔬汁饮料标准,同时经活性炭脱色脱渣处理。实施例中,浓缩果蔬汁组分的重量份可以是72~630份,具体可以但不仅仅为110重量份。具体可以在60~700份,进一步在72~630份之间根据需要进行调整。
[0058]
食品用香精能够调节特医食品的口感和气味等,提高患者对镜检准备的耐受力。实施例中,食品用香精组分的重量份可以是0.6~14份,具体可以但不仅仅为1份重量份。具体可以在0.3~16份,进一步在0.6~14份之间根据需要进行调整。另外,食品用香精也应该符合医药或食品卫生等要求,如食品用香精符合gb 30616-2020食品安全国家标准、食品用香精标准。
[0059]
基于上文各实施例特医食品所含组分的含量等,在进一步实施例中,本技术实施例特医食品可以是包括如下重量份的组分:
[0060][0061][0062]
具体实施例中,本技术实施例特医食品可以但不仅仅是包括如下重量份的组分:
[0063][0064]
基于上文各实施例中特医食品,通过对本技术实施例特医食品所含组分和含量进行控制和优化,使得本技术实施例特医食品适用于肠道镜检准备和/或胃部镜检准备的特医食品。根据本技术实施例特医食品所含的组分和含量,其能够提供人体所需的营养素及电解质,提高了患者肠道镜检准备和/或胃部镜检准备中的安全性能。而且本技术实施例特医食品所含的组分复配起到了增效作用,有利于规范患者的肠道镜检准备和/或胃部镜检准备病前24小时内的饮食,提供饱腹感,减少肠道和胃部食物残渣生成,降低肠腔液的发泡性,明显减少肠道清洗剂的用量,提高镜检准备的安全性和患者对肠道准备的耐受能力,从而提高了患者再次进行类似肠道准备的意愿性。本技术实施例特医食品所含的组分之间的增效作用还能够有效缩短肠道镜检准备和/或胃部镜检准备的时间,提高肠道镜检准备和/或胃部镜检准备效率;降低了肠道和/或胃部中的食物内残留物,从而提高肠道镜检和胃部镜检的清晰度,降低气泡对镜检视野的干扰,以提高肠道镜检准备和/或胃部镜检准备的质量和有效性;另外,经检测,本技术实施例特医食品分散体系稳定,如能够在40℃下放置90天后,其所含矿物质分散均匀,其质量稳定,有益于营养成分含量均匀一致。
[0065]
第二方面,本技术实施例还提供了上文本技术实施例特医食品的制备方法。本技术实施例特医食品的制备方法工艺流程如图1所示,其包括如下步骤:
[0066]
s01:按照特医食品的配方组分分别量取各原料组分;
[0067]
s02:将量取的各组分进行混料处理,得到特医食品。
[0068]
其中,步骤s01中的特医食品为上文本技术实施例特医食品,因此,形成特医食品的配方组分为形成上文本技术实施例特医食品的组分。因此,量取的各原料组分种类和比例均如上文本技术实施例特医食品所含组分种类和含量比例,为了节约篇幅,在此不再对量取的各原料组分种类和比例进行赘述。
[0069]
步骤s02中的混料处理目的是为了使得各原料组分混合均匀,以提高各组分之间的增效作用,实施例中,该混料处理可以是如搅拌或其他能够实现各原料组分混合均匀的混合方式。
[0070]
实施例中,步骤s02中的将量取的各组分进行混料处理的方法工艺流程如图2所示,包括如下步骤:
[0071]
s021:将量取的魔芋粉、结冷胶、果胶、麦芽糊精、食用葡萄糖、乳糖醇、低聚果糖进
行第一混合处理,得到第一混合料;
[0072]
s022:将量取的异构化乳糖液、浓缩果蔬汁进行第二混合处理,得到第二混合料;
[0073]
s023:将量取的抗坏血酸、维生素、盐酸硫胺素、盐酸吡哆醇、烟酸、肌醇、牛磺酸进行第三混合处理,得到第三混合料;
[0074]
s024:将量取的葡萄糖酸锌、硫酸镁、l-乳酸钙、食用盐、氯化钾进行第四混合处理,得到第四混合料;
[0075]
s025:将第一混合料和第二混合料与将量取的水、酸度调节剂进行第五混合处理,得到第五混合料;
[0076]
s026:将第五混合料与第四混合料进行第六混合处理,得到第六混合料;
[0077]
s027:将第六混合料与第三混合料、食品用香精进行第七混合处理,得到第七混合料,该第七混合料即为上述特医食品。
[0078]
其中,步骤s021中的第一混合处理至步骤s027中的第七混合处理均是为了使得各原料组分混合均匀,以提高各组分之间的增效作用并形成稳定的分散体系,该些混合处理可以是如搅拌或其他能够实现各原料组分混合均匀的混合方式。具体混合条件可以根据各原料组分的特性等因素进行调节。如实施例中,第五混合处理、第六混合处理、第七混合处理中的至少一混合处理的温度为55~90℃,进一步可以是60~85℃。另些实施例中,当第五混合处理为搅拌处理时,其搅拌处理的搅拌转速可以是50~1000rpm,进一步可以是55~850rpm;搅拌时间可以是12~60min,进一步可以是15~40min。当第六混合处理为搅拌处理时,其搅拌处理的搅拌转速可以是50~1000rpm,进一步可以是55~800rpm;搅拌时间可以是5~45min,进一步可以是6~30min。当第七混合处理为搅拌处理时,其搅拌处理的搅拌转速为50~1000rpm,进一步可以是55~800rpm;搅拌时间为5~40min,进一步可以是6~30min。通过控制该些混合处理的温度和搅拌的条件,提高各组分的分散均匀性以形成稳定的分散体系,充分发挥各组分之间的增效作用。
[0079]
实施例中,步骤s025中的将第一混合料和第二混合料与将量取的水、酸度调节剂进行第五混合处理的方法包括如下步骤:
[0080]
先将水进行升温处理,再加入第一混合料和第二混合料以及第四混合料、酸度调节剂进行第五混合处理。
[0081]
通过先将水升温处理,提高第一混合料和第二混合料以及包括第三混合料、第四混合料等组分的分散效率和均匀性。实施例中,将水进行升温处理可以是升温至第五混合处理的温度区间,如为55~90℃,进一步可以是60~85℃。
[0082]
实施例中,待步骤s02中混料处理的步骤之后,还包括将经混料处理的混合物,具体可以是上述第七混合料进行包括灭菌处理的步骤。实施例中,该灭菌处理为高温灭菌,其温度可以为105~125℃,进一步可以是108~123℃;时间可以为5~60min,进一步可以是8~40min。通过高温灭菌,提高其卫生安全性和有效延长其保值期。灭菌前和/或灭菌后的本技术实施例特医食品可以装盛于医用或食品级瓶中或其他容器中,具体如医用或食品级透明玻璃瓶或耐蒸煮复合膜袋。规格可以是90g/瓶、100g/瓶、200g/瓶、500g/瓶,90g/袋、100g/袋、200g/袋、500g/袋,90ml/瓶、100ml/瓶、200ml/瓶、500ml/瓶,90ml/袋、100ml/袋、200ml/袋、500ml/袋等。
[0083]
因此,上述本技术实施例特医食品制备方法按照比例将相应的原料组分进行混料
处理,或进一步进行包括灭菌等后续处理,使得配制的特医食品分散体系和质量稳定,而且能够使得给组分之间起到增效作用,赋予配制的特医食品能够提高镜检患者的饱腹感和耐受能力,减少肠道和胃部食物残渣生成,并提供所需营养素及电解质,促进肠道清洁,降低肠腔液发泡性,提高肠道镜检准备和/或胃部镜检准备质量和安全性能以及效果。而且本技术实施例特医食品的制备方法工艺条件易控,而且还能够保证配制的特医食品的性能、质量和功能稳定。进一步还可以通过调节相应工艺条件如混料处理工艺条件,提高特医食品的制备效率和提高质量和功能的稳定等性能。
[0084]
为使本技术实施例特医食品及其制备方法和含有特医食品的化妆品能清楚地被本领域技术人员理解,以及本技术实施例特医食品及其制备方法进步性能显著的体现,以下通过多个实施例来举例说明上述技术方案。
[0085]
实施例1至实施例7
[0086]
本实施例1至实施例7分别提供一种特医食品及其制备方法。本实施例1至实施例7提供的特医食品分别包括如下文表1和表2中重量份和种类的组分。
[0087]
本实施例1至实施例7提供的特医食品的制备方法包括如下步骤:
[0088]
s1:按表1和表2中配方称取重量份的魔芋粉,结冷胶,果胶,麦芽糊精,食用葡萄糖,乳糖醇,低聚果糖,混匀,得物料a;
[0089]
s2:按表1和表2中配方称取重量份的异构化乳糖液、浓缩果蔬汁,混匀,得物料b;
[0090]
s3:按表1和表2中配方称取重量份的抗坏血酸,维生素,盐酸硫胺素,盐酸吡哆醇,烟酸,肌醇,牛磺酸,混匀,得物料c;
[0091]
s4:按表1和表2中配方称取重量份的葡萄糖酸锌,硫酸镁,l-乳酸钙,食用盐,氯化钾,混匀,得物料d;
[0092]
s5:按表1和表2中配方称取重量份的酸度调节剂,得物料e;
[0093]
s6:按表1和表2中配方称取重量份的食品用香精,得物料f;
[0094]
s7:按表1和表2中配方称取重量份的水,加热至温度t1℃,加入物料a、物料b及物料e,设定搅拌转速ra rpm下,搅拌ta min;加入物料d,设定搅拌转速rb rpm下,搅拌tb min;加入物料c、物料f,设定搅拌转速rc rpm下;搅拌tc min,得物料h;
[0095]
s8:将物料h于温度t2℃下灭菌td min,得到各特医食品。
[0096]
其中,步骤s7中的加热温度t1、转速ra至rc、搅拌ta至tc和步骤s8中的灭菌温度t2和时间td如下述表3中所示,步骤s8灭菌前将物料灌装于100ml容量透明玻璃瓶中。
[0097]
表1实施例1至7中特医食品所含组分及各组分重量份数
[0098]
物料名称实施例1实施例2实施例3实施例4实施例5实施例6实施例7水910105014001300300058007200浓缩果蔬汁6072110120340630700魔芋粉911232375125140结冷胶0.20.30.60.63.05.17果胶0.10.170.40.45.510.813麦芽糊精12015025027085018622070食用葡萄糖9073220215300420530乳糖醇6113030100176280
异构化乳糖液0.350.422269.411低聚果糖11132020508196抗坏血酸0.20.30.510.511.52.63.3维生素e0.050.060.080.080.220.470.6盐酸硫胺素0.0020.0030.0050.0050.0250.0510.066盐酸吡哆醇0.00080.0010.0020.0020.0110.0220.027烟酸0.0070.010.020.020.0350.0690.093肌醇0.070.090.180.180.510.750.98牛磺酸0.350.520.90.93.05.78.2葡萄糖酸锌0.0530.0720.180.180.300.690.77硫酸镁0.130.210.470.471.052.082.91l-乳酸钙1.52.76.96.925.154.463.6食用盐0.70.92291621氯化钾0.41.122142534酸度调节剂0.10.310.95.5911食品用香精0.30.61161416
[0099]
表2实施例1至7中特医食品原料的具体物质
[0100]
[0101][0102]
表3实施例1至7的特医食品的制备方法工艺参数
[0103][0104][0105]
表4实施例8至11中特医食品所含组分及各组分重量份数
[0106]
物料名称实施例8实施例9实施例10实施例11
水1400140014001400浓缩果蔬汁110110110110魔芋粉23232323结冷胶0.60.60.60.6果胶0.40.40.40.4麦芽糊精250250250250食用葡萄糖220220220220乳糖醇30303030异构化乳糖液2222低聚果糖20202020抗坏血酸0.510.510.510.51维生素e0.080.080.080.08盐酸硫胺素0.0050.0050.0050.005盐酸吡哆醇0.0020.0020.0020.002烟酸0.020.020.020.02肌醇0.180.180.180.18牛磺酸0.90.90.90.9葡萄糖酸锌0.180.180.180.18硫酸镁0.470.470.470.47l-乳酸钙6.96.96.96.9食用盐2222氯化钾2222酸度调节剂1111食品用香精1111
[0107]
表5实施例8至11中特医食品原料的具体物质
[0108]
[0109][0110]
表6实施例12至13和对比例1至5中特医食品所含组分及各组分重量份数
[0111]
物料名称实施例12实施例13对比例1对比例2对比例3对比例4对比例5水1400140014001400140014001400浓缩果蔬汁110110110110110110110魔芋粉232314281502323结冷胶0.60.680.10.60.68果胶0.40.4140.050.4140.4麦芽糊精250250250250250250250食用葡萄糖220220220220220220220乳糖醇30303030303030异构化乳糖液2222222低聚果糖20202020202020抗坏血酸0.510.510.510.510.510.510.51维生素e0.080.080.080.080.080.080.08盐酸硫胺素0.0050.0050.0050.0050.0050.0050.005盐酸吡哆醇0.0020.0020.0020.0020.0020.0020.002烟酸0.020.020.020.020.020.020.02肌醇0.180.180.180.180.180.180.18牛磺酸0.90.90.90.90.90.90.9葡萄糖酸锌0.180.180.180.180.180.180.18硫酸镁0.470.470.470.470.470.470.47l-乳酸钙6.96.96.96.96.96.96.9食用盐2222222氯化钾2222222酸度调节剂1111111食品用香精1111111
[0112]
表7实施例12至13和对比例1至5中特医食品原料的具体物质
[0113][0114][0115]
对比例6至对比例17
[0116]
对比例6至对比例17分别提供一种特医食品及其制备方法。对比例6至对比例12提供的特医食品分别包括如下文表8和表9中重量份和种类的组分。对比例13至对比例17提供的特医食品分别包括如下文表10和表11中重量份和种类的组分。
[0117]
表8对比例6至12中特医食品所含组分及各组分重量份数
[0118]
[0119][0120]
表9对比例6至12中特医食品原料的具体物质
[0121]
[0122][0123]
表10对比例13至17中特医食品所含组分及各组分重量份数
[0124]
物料名称对比例13对比例14对比例15对比例16对比例17水14001400140014001400浓缩果蔬汁110110110110110魔芋粉2323232323结冷胶0.60.60.60.60.6果胶0.40.40.40.40.4麦芽糊精250250250250250食用葡萄糖220220220220220乳糖醇030303030异构化乳糖液20222低聚果糖202002020抗坏血酸0.510.510.5100.51维生素e0.080.080.0800.08盐酸硫胺素0.0050.0050.0050.0050.005盐酸吡哆醇0.0020.0020.0020.0020.002烟酸0.020.020.020.020.02肌醇0.180.180.180.180牛磺酸0.90.90.90.90.9葡萄糖酸锌0.180.180.180.180.18硫酸镁0.470.470.470.470.47l-乳酸钙6.96.96.96.96.9食用盐22222氯化钾22222酸度调节剂11111食品用香精11111
[0125]
表11对比例13至17中特医食品原料的具体物质
[0126][0127][0128]
实施例1至实施例13和对比例1至对比例12中特医食品的相关性能测试
[0129]
1.特医食品稳定性测试
[0130]
1.1常温下特医食品稳定性测试:
[0131]
实验方法1:取实施例1至实施例13和对比例1至对比例12提供的特医食品所有灭菌后的样品,于常温下放置48小时,观察性状稳定性。
[0132]
实验结果1:对比例如对比例2、对比例6、对比例7、对比例8、对比例9、对比例10、对比例11、对比例12下样品肉眼可见分层,而本技术实施例中样品均未见肉眼可见分层。因此,本技术实施例特医食品在灭菌后常温下具有优异的稳定性,而且性能稳定。当特医食品所含的胶体含量过低时如对比例2、对比例6至对比例12,会导致医食品稳定性变差。
[0133]
1.2 40℃恒温下特医食品稳定性测试:
[0134]
试验方法2:取实施例1至实施例13项下灭菌后的样品及对比例1,对比例3至对比例5项下灭菌后的样品,分别于40℃恒温箱中放置1个月,观察性状稳定性。
[0135]
实验结果2:在高温灭菌和高温保存中,在本技术实施例提供的特医食品样品中,除了实施例12、实施例11、实施例10下样品肉眼可见分层,实施例13出现少量底部沉淀现象,其他实施例均没有出现分层现象。由实施例10至实施例13的现象可知,本技术实施例特医食品中,果胶的de
°
、da
°
、魔芋粉的粘度等性能也会对本技术实施例特医食品稳定性产生一定的影响,如果果胶的de
°
过高或da
°
过低,魔芋粉的粘度过高或过低有导致本技术实施例特医食品在高温灭菌和高温保存中出现分层或生成少量沉淀等现象,但是经实验测得,并不影响本技术实施例特医食品的胃部和肠道镜检准备效果。而在对比例提供的特医食品样品中,出现的明显的沉淀,特别是对比例1及对比例3底部结块,从而导致功能的明显降低或丧失。因此,本技术实施例特医食品在40℃下依然表现出良好的稳定性。
[0136]
试验方法3:取实施例1至实施例9项下灭菌后的样品及对比例4至对比例5项下灭菌后的样品。将各实施例项下样品置于40℃恒温箱中放置3个月。其中,于第0天及90天分别采用移液管从玻璃瓶的上、中、下3层依次分别移取1个样品,分别检测钙、镁含量。检测方法:钙,依据gb5009.92-2016第一法;镁,依据gb5009.241-2017第一法。
[0137]
试验结果3:实施例1至实施例9和对比例4至对比例5样品于40℃恒温箱中放置3个月后,上、中、下三层钙、镁含量测得结果如下表12所示。由表12可知,本技术实施例特医食品在高于常温下依然保持良好的稳定,波动较小,体系稳定。其中,实施例8和9的钙、镁含量分别在90天结果与0天结果比波动相对本技术其他实施例相对大,但是也明显小于对比例4和5的波动。由此可知,果胶的de
°
过高或da
°
过低对本技术其他实施例医食品所含营养素如钙、镁等在保存过程中的均匀性有影响,也即是对本技术其他实施例保存的稳定性有一定的影响。
[0138]
表12
[0139][0140][0141]
2.对小鼠肠粘膜通透性保护效果测试
[0142]
取清洁剂昆明小鼠90只,雌雄各半,平均体重30g,随机分为9组(a组、b组、c组、d组、e组、f组、g组、h组、k组),swc9101实验鼠饲料(供能比:蛋白质20.6%,脂肪12.0%,碳水化合物67.4%)。
[0143]
a组:swc9101实验鼠饲料,水。
[0144]
b组:swc9101实验鼠饲料,水中添加对比例样品(添加使用前摇匀),添加量30g/100g;对比例样品制备方法:魔芋精粉2.87份(魔芋精粉过200目,葡甘聚糖含量85%),海藻酸钠0.51份、柠檬酸0.2份、食用盐0.1份、氯化钾0.05份、葡萄糖40.95份、罗汉果甜苷0.03份、食品用香精0.72份、水204.57份。将水加热至60摄氏度,将柠檬酸、氯化钾、食用盐、罗汉果甜苷加入水中搅拌并溶解,再将魔芋精粉、葡萄糖、海藻酸钠混合后连同食品用香精加入,搅拌均匀后于121℃灭菌15分钟。
[0145]
c组:swc9101实验鼠饲料,水中添加对比例13样品(添加使用前摇匀),添加量30g/100g。
[0146]
d组:swc9101实验鼠饲料,水中添加对比例14样品(添加使用前摇匀),添加量30g/100g。
[0147]
e组:swc9101实验鼠饲料,水中添加对比例15样品(添加使用前摇匀),添加量30g/100g。
[0148]
f组:swc9101实验鼠饲料,水中添加对比例16样品(添加使用前摇匀),添加量30g/
100g。
[0149]
g组:swc9101实验鼠饲料,水中添加对比例17样品(添加使用前摇匀),添加量30g/100g。
[0150]
h组:swc9101实验鼠饲料,水中添加实施例3样品,添加量30g/100g。
[0151]
k组:swc9101实验鼠饲料,水。
[0152]
各组按照上述方案喂养,连续饲养3天后,于第4天下午14点开始禁食,不禁水(各组水同饲养期保持一致);a组至h组于第4天下午20点用水灌胃硫酸镁(灌服量0.5g/kg.bw),k组灌服等量生理盐水,禁食不禁水(各组水同饲养期保持一致);第5天上午8点用水灌服聚乙二醇(灌服量0.5g/kg.bw),禁食不禁水(各组均替换为添加10%宝矿力水特电解质固体饮料的水);各组均于第5天上午12点摘眼球取血1ml,离心,将血清置于-80℃冰箱中保存;采用分光光度法[黎君友,于燕.分光光度法测定血和小肠组织二胺氧化酶活性[j].氨基酸和生物资源,1996,18(4):28.]测定血清中dao(血清二胺氧化酶)含量[dao是具有高度活性的细胞内酶,当肠粘膜上皮细胞受损、坏死后dao便释放入血,以致血液中dao活性升高]。
[0153]
实验结果:各实验组的肠粘膜通透性保护测试效果如下表13所示。h组的dao明显低于a组至g组的含量。进一步实验得知,本技术其他实施例提供的特医食品样品实验组小鼠血液中dao含量均明显低于对比例的其他实施例提供的特医食品样品实验组小鼠血液中dao含量。由此可知,本技术实施例特医食品对清肠剂引起的肠粘膜通透性保护效果优异。
[0154]
表13肠粘膜通透性保护测试效果
[0155]
组别血清中dao(血清二胺氧化酶)含量(mg/ml)(n=10)a3.28
±
0.21b3.02
±
0.30c2.91
±
0.37d2.70
±
0.28e2.84
±
0.31f2.88
±
0.38g2.77
±
0.31h2.13
±
0.30k1.86
±
0.33
[0156]
3.对减少肠腔冲洗液发泡性的效果测试
[0157]
取雄性sd大鼠24只,每组3只,平体重300g;swc9101实验鼠饲料(供能比:蛋白质20.6%,脂肪12.0%,碳水化合物67.4%)。
[0158]
a组:swc9101实验鼠饲料,水。
[0159]
b组:swc9101实验鼠饲料,水中添加对比例样品(添加使用前摇匀),添加量50g/100g;对比例样品制备方法:魔芋精粉2.87份(魔芋精粉过200目,葡甘聚糖含量85%),海藻酸钠0.51份、柠檬酸0.2份、食用盐0.1份、氯化钾0.05份、葡萄糖40.95份、罗汉果甜苷0.03份、食品用香精0.72份、水204.57份。将水加热至60摄氏度,将柠檬酸、氯化钾、食用盐、罗汉果甜苷加入水中搅拌并溶解,再将魔芋精粉、葡萄糖、海藻酸钠混合后连同食品用香精加入,搅拌均匀后于121℃灭菌15分钟。
[0160]
c组:swc9101实验鼠饲料,水中添加对比例6样品(添加使用前摇匀),添加量50g/100g。
[0161]
d组:swc9101实验鼠饲料,水中添加对比例7样品(添加使用前摇匀),添加量50g/100g。
[0162]
e组:swc9101实验鼠饲料,水中添加对比例8样品(添加使用前摇匀),添加量50g/100g。
[0163]
f组:swc9101实验鼠饲料,水中添加对比例12样品(添加使用前摇匀),添加量50g/100g。
[0164]
g组:swc9101实验鼠饲料,水中添加实施例3样品,添加量50g/100g。
[0165]
h组:swc9101实验鼠饲料,水中添加实施例5样品,添加量50g/100g。
[0166]
各组按照上述方案喂养,连续饲养7天,于第7天下午16点开始禁食,不禁水(各组水同饲养期保持一致);a组至h组于第7天下午20点灌胃硫酸镁、聚乙二醇混合液(硫酸镁浓度0.8%,聚乙二醇浓度0.2%,每次3ml),每30min灌胃1次,连续灌服2次,禁食不禁水(各组水同饲养期保持一致);于第8天上午08点再次用水灌胃硫酸镁聚乙二醇混合液(硫酸镁浓度0.6%,聚乙二醇浓度0.3%,每次3ml),每15min灌胃1次,连续灌服6次,禁食不禁水(各组均替换为添加10%宝矿力水特电解质固体饮料的水);第8天上午12点麻醉后处死大鼠,剖取结肠,用5ml生理盐水冲洗,然后用胶管连接,使用50ml纯化水以4.0ml/min循环冲洗20min,收集循环冲洗后的肠腔冲洗液,分别量取30ml肠腔冲洗液置于100ml具塞量筒中,振摇10min(模拟肠道蠕动),分别于静置(tmin)0min、10min后观察并记录气泡的体积。
[0167]
实验结果:各实验组对减少肠腔冲洗液发泡性的效果如下表14所示。g、h组肠腔冲洗液发泡性体积明显低于a组至f组的含量。进一步实验得知,g、h组肠腔冲洗液振摇产生的气泡少,且静置一段时间易于消散,有利于降低肠腔内气泡的产生,降低肠镜检查时气泡对视野的观察影响,提高视野清晰度。
[0168]
表14减少肠腔液发泡性的效果
[0169][0170]
4.特医食品肠道准备效果测试
[0171]
4.1特医食品肠道准备效果的对照实验
[0172]
招募45名进行肠镜检查的志愿者。
[0173]
纳入标准:(1)有肠镜适应症检查需要,接受诊断性结肠镜的患者;(2)年龄35-60岁,性别不限;(3)无既往肾功能不全、恶性肿瘤等重大疾病史;(4)愿意配合开展研究调查。
[0174]
分组:将志愿者随机分为常规饮食组、对比例组和肠镜特医食品组;
[0175]
常规饮食组:镜检前1天进食常规饮食(如白米粥、牛奶、蒸水蛋、面条、馒头、豆腐),每日4餐,自备;
[0176]
肠镜特医食品组:镜检前1天进食本技术实施例3下样品,每日4次,每次200g。
[0177]
对比例组:镜检前1天进食对比例样品,每日4次,每次200g。
[0178]
对比例样品制备方法:魔芋精粉2.87份(魔芋精粉过200目,葡甘聚糖含量85%),海藻酸钠0.51份、柠檬酸0.2份、食用盐0.1份、氯化钾0.05份、葡萄糖40.95份、罗汉果甜苷0.03份、食品用香精0.72份、水204.57份。将水加热至60摄氏度,将柠檬酸、氯化钾、食用盐、罗汉果甜苷加入水中搅拌并溶解,再将魔芋精粉、葡萄糖、海藻酸钠混合后连同食品用香精加入,搅拌均匀后装成200g/袋,于121℃灭菌15分钟。
[0179]
各组均服用复方聚乙二醇电解质散,具体服用方法:检查前1天最后一次就餐(常规饮食、或者肠镜特医食品或者对比例样品)2小时后取复方聚乙二醇电解质散1盒,加750ml凉温开水冲服,30分钟内服用完毕;检查前4小时取复方聚乙二醇电解质散2盒,加1500ml凉温开水冲服,120分钟内服用完毕。服用期间来回走动,轻揉腹部,排便并观察至便样呈清水状(无色或者淡黄色透明水样)。
[0180]
统计并记录最后一次服用复方聚乙二醇电解质散溶液至便样呈清水状之间的时间。如2250ml复方聚乙二醇电解质散溶液未能有效达到便样呈清水状节点,继续补充复方聚乙二醇电解质散溶液并累计统计时间直至便样呈清水状节点。
[0181]
测试结果:
[0182]
常规饮食组3名便秘患者肠道准备失败,补充复方聚乙二醇电解质散溶液未能达到便样呈清水状要求,肠道准备失败,予以剔除。常规饮食组最后一次服用复方聚乙二醇电解质散溶液至便样呈清水状之间的时间为164.92
±
35.08min,对比例组最后一次服用复方聚乙二醇电解质散溶液至便样呈清水状之间的时间为123.72
±
30.63min,肠镜特医食品组最后一次服用复方聚乙二醇电解质散溶液至便样呈清水状之间的时间为82.87
±
22.54min,具体如下表15所示。
[0183]
表15改善肠道准备时间的效果
[0184]
组别时间(min)备注常规饮食组164.92
±
35.08n=12对比例组123.72
±
30.63n=15肠镜特医食品组82.87
±
22.54n=15
[0185]
4.2特医食品对患者胃部准备和肠道准备镜检清晰度效果的临床实验
[0186]
公司志愿者患者孙某男,40岁,因胃肠功能紊乱于医院消化内镜中心开展无痛胃镜和无痛肠镜检查。
[0187]
第一次镜检:时间2022年01月10日;镜检前1天进食白米粥,检查前1天最后一次就餐2小时后取复方聚乙二醇电解质散1盒,加750ml凉温开水冲服,30分钟内服用完毕;检查前4小时取复方聚乙二醇电解质散3盒,加2250ml凉温开水冲服,120分钟内服用完毕。最后一次服用复方聚乙二醇电解质散溶液120分钟候后便样仍有残渣,取复方聚乙二醇电解质散2盒,加1500ml凉温开水冲服,60分钟内服用完毕。190分钟后便样呈清水状,实施镜检。
[0188]
第二次镜检:时间2022年02月18日;镜检前1天进食本技术实施例肠镜特医食品4
袋(本技术实施例3下样品,每袋200g),检查前1天最后一次就餐2小时后取复方聚乙二醇电解质散1盒,加750ml凉温开水冲服,30分钟内服用完毕;检查前4小时取复方聚乙二醇电解质散2盒,加1500ml凉温开水冲服,120分钟内服用完毕。87分钟后便样呈清水状,实施镜检。
[0189]
结果:第一次镜检前食用常规饮食(白米粥),复方聚乙二醇电解质散溶液的服用量为4500ml,且胃镜检查时食管、贲门镜检视野较差,如图3所示。肠镜检查回肠末端、回盲部、升结肠、横结肠、降结肠、乙状结肠、直肠中均有明显黄色粪便残留液,如图4所示。
[0190]
第二次镜检前食用本技术实施例肠镜特医食品(本技术实施例3样品),复方聚乙二醇电解质散溶液的服用量为1500ml,且胃镜检查时食管、贲门镜检视野清晰,如图5所示;肠镜检查除横结肠、降结肠有少量粪便残留液外,其余部位均清洁准备良好,镜检视野清晰,如图6所示。
[0191]
以上所述实施例仅表达了本技术的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本技术专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本技术构思的前提下,还可以做出若干变形和改进,这些都属于本技术的保护范围。因此,本技术专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1