用于置换二尖瓣的假体瓣膜的制作方法与工艺
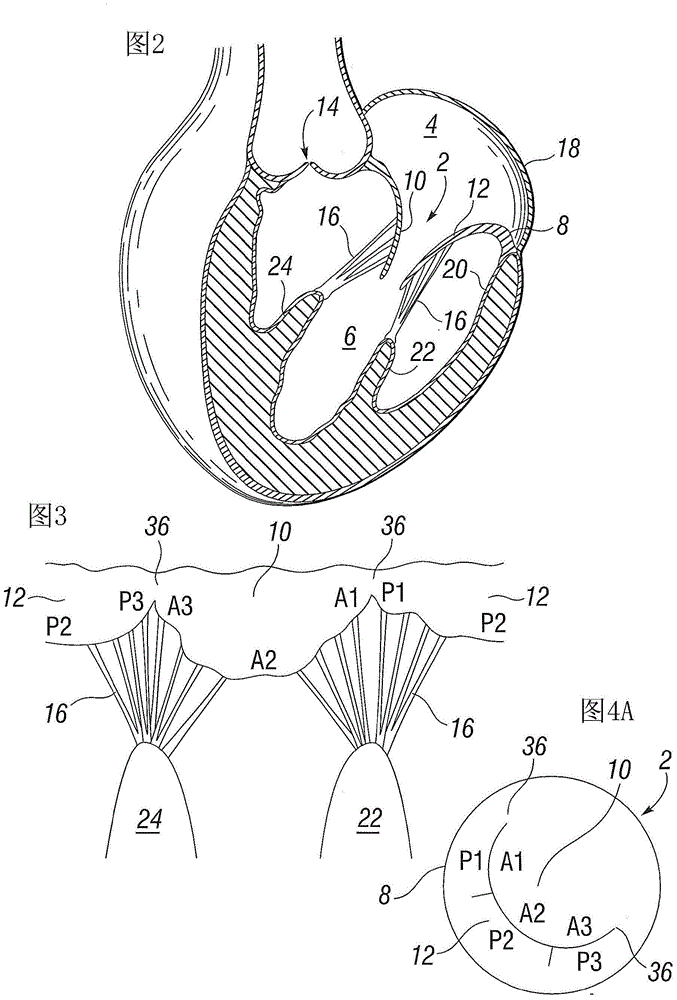
用于置换二尖瓣的假体瓣膜相关申请的交叉参考本申请要求享有2013年2月4日提交的美国专利申请号61/760,577和2013年12月11日提交的美国专利申请号61/914,648的优先权,该申请其全部内容被引入本文作为参考。发明领域本公开总体上涉及修复和/或置换天然心脏瓣膜的假体装置,具体涉及置换缺陷二尖瓣的假体瓣膜、以及将其递送和植入人心脏内的方法和装置。发明背景假体瓣膜多年来已被用于治疗心脏瓣膜障碍。天然心脏瓣膜(即,主动脉瓣、肺瓣、三尖瓣和二尖瓣)在确保充足血液供应通过心血管系统顺流方面具有至关重要的作用。先天畸形、炎性过程、感染状况或疾病可使这些心脏瓣膜效力降低。瓣膜的这种损坏可导致严重的心血管损害或死亡。多年来,这种障碍的确定性治疗是在心脏直视手术过程中进行的瓣膜外科修复或置换。然而,这种手术具有高侵入性,并且易有多种并发症。因此,有心脏瓣膜缺陷的老年和虚弱患者通常得不到治疗。近来,经血管技术已被研发以利用柔性导管引入和植入假体心脏瓣膜,其方式的侵入性远小于心脏直视手术。在这种技术中,假体瓣膜以压扁状态安装在柔性导管的端部分上,并被推进通过患者血管,直到瓣膜到达植入位点。然后使处于导管末端的瓣膜在缺陷性天然瓣膜位点处扩张至其功能尺寸,如通过膨胀其上安装了瓣膜的球囊。另一已知的植入假体主动脉瓣的技术是经顶点(transapical)法,其中在患者胸壁制造小切口,并推进导管通过顶点(即,底尖(bottomtip))。经顶点技术被公开于美国专利申请公开号2007/0112422,其被引入本文作为参考。如同经血管方式,经顶点方式可包括球囊导管,该球囊导管具有操纵机构,用于通过引导件将球囊扩张式假体心脏瓣膜递送至主动脉环。球囊导管可包括正处于远侧球囊近侧的偏转段,以利于假体心脏瓣膜以适当的定向在主动脉环内定位。上述技术和其它技术已为高手术风险的主动脉瓣疾病患者提供多种选择从而避免心脏直视手术和心肺分流术的后果。虽然用于主动脉瓣的装置和程序被很好地研发出来,但这种基于导管的程序却不一定适用于二尖瓣,因为主动脉和二尖瓣之间具有明显的差异。二尖瓣具有主动脉瓣中不存在的复杂瓣下机构,即腱索。外科二尖瓣修复技术(例如,二尖瓣环成形术)由于其高成功率和在修复后显示的临床改善已增加普及性。除现有的二尖瓣修复技术外,还有多种旨在使二尖瓣修复减少侵入性程序的新技术。这些技术的范围从反复Alfieri缝合程序,到基于冠状窦的二尖瓣解剖结构修饰,再到瓣下折术或心室重塑装置——其顺带矫正二尖瓣反流。然而,关于二尖瓣置换,极少侵入性减少选择是可用的。美国每年约有25,000次二尖瓣置换(MVR)。然而,估计超过300,000个符合治疗方针的患者由于其年龄和/或共存病而得不到治疗。因此,需要置换二尖瓣的最小侵入性技术。发明概述本文描述了假体二尖瓣、其部件和将期植入的方法和装置。假体装置被如下描述:其被配置以植入在心脏的天然二尖瓣区域,并且包括径向可压缩至径向压缩状态并且可从压缩状态自扩张至径向扩张状态的主体。假体装置还包括至少一个心室锚,其偶联至主体并布置在主体外侧,从而在主体压缩至压缩状态时,心室锚和主体外表面之间的瓣叶接收空间增加,以接收其之间的天然瓣膜瓣叶。在对主体或心室锚不存在任何显著外部向内力的情况下主体自扩张至扩张状态时,空间减少以捕获主体和心室锚之间的瓣叶。在一些实施方式中,用于植入在心脏天然二尖瓣区域的假体装置包括框架,该框架具有主体和偶联至主体并布置在主体外侧的至少一个心室锚。假体装置还包括多个瓣叶,该瓣叶被主体支撑,形成穿过主体的血流的单向瓣膜。主体径向可压缩至径向压缩状态以递送到身体中,并且可从压缩状态自扩张至径向扩张状态。心室锚包括固定地固定至主体的基体、与基体相对的自由端部分和在心室锚和主体之间限定瓣叶接收空间以接收天然瓣膜的瓣叶的中间部分。在对心室锚不存在任何径向内向力的情况下,主体从其压缩状态至其径向扩张状态的扩张导致瓣叶接收空间减少。在其它实施方式中,用于植入在天然二尖瓣区域的假体装置包括主体、至少一个心室锚和至少一个心房锚。主体被配置以布置在天然二尖瓣内,并且可压缩至压缩状态以递送到心脏中和可从压缩状态自扩张至扩张状态。至少一个心室锚偶联至主体并且布置在主体的外侧,从而在扩张状态下,心室锚和主体外表面之间存在瓣叶接收空间,以接收天然瓣膜瓣叶的自由边缘部分。心室锚包括啮合部分,其被配置以延伸到接收的天然瓣叶后方并接触天然二尖瓣环的心室面、接收的天然瓣叶的环连接部分或天然环的心室面和接收的天然瓣叶的环连接部分两者。至少一个心房密封构件偶联至主体并布置在主体外侧,并且被配置以在与心室锚的啮合部分相反的位置处接触天然二尖瓣环的心房部分、接收的天然瓣叶的环连接部分或天然环的心房面和接收的天然瓣叶的环连接部分两者,以止动(retention)假体装置和/或防止瓣周漏。还描述用于将假体装置送入心脏的示例性递送系统。一些实施方式包括内鞘,该内鞘具有远端部分,该远端部分具有至少一个纵向槽,该纵向槽从内鞘远端向近侧延伸。内鞘的远端部分被配置以包容处于径向压缩状态的假体装置。外鞘围绕内鞘同心地定位,并且内鞘和外鞘中至少一者可相对于另一者在第一位置(其中外鞘在至少部分纵向槽上方延伸)和第二位置(其中至少部分纵向槽不被外鞘覆盖)之间轴向地移动,从而允许内鞘内包容的假体装置的一部分通过槽径向向外扩张。还描述在心脏天然二尖瓣区域植入假体装置的示例性方法。一种这样的方法包括将径向压缩状态的假体装置递送到心脏中;使心室锚远离框架主体自扩张,同时保持主体处于压缩状态,从而增加心室锚和主体外表面之间的间隙;使主体定位在天然二尖瓣的环内,并使心室锚邻近天然二尖瓣瓣叶心室侧,从而将瓣叶布置在心室锚和主体外表面之间的间隙中;和使主体至自扩张至扩张状态,使得间隙减少,从而捕获主体外表面和心室锚之间的瓣叶。在一些情况下,可植入的假体瓣膜包括可径向折叠并且可径向扩张的环形框架和该框架内部支撑的瓣膜构件。在一些情况下,框架包括环形主体,限定贯穿其中的腔;至少一个心室锚,偶联至主体的心室端部分;和心房部分,偶联至主体并且远离主体径向延伸,其中心房部分包括多个径向延伸臂,并且其中至少一个臂包括盘旋或螺旋的区段。在一些情况下,其中至少一个臂包括盘旋的区段,该盘旋的区段包括多个基本上直线形的平行区段。在一些情况下,其中至少一个臂包括盘旋的区段,该盘旋的区段包括多个基本上曲线形的部分。在一些情况下,其中至少一个臂包括盘旋的区段,该盘旋的区段在接近主体的臂部分处包括多个基本上直线形的平行区段和在臂末端部分处包括多个基本上曲线形的部分。在一些情况下,其中臂至少一个包括盘旋的区段,该盘旋的区段的厚度从臂末端部分至接近主体的臂部分增加。在一些情况下,多个臂彼此独立地连接至主体,而没有将相邻臂相互连接的金属区段。在一些情况下,每个臂具有自由端部分,该自由端部分包括曲线形或圆形构件。在一些情况下,曲线形或圆形构件包括马蹄形构件,其包括两个径向向内指向主体的末端部分。在一些情况下,两个末端部分均包括圈环,该圈环具有贯穿其中形成的孔。在一些情况下,每个臂包括相对于主体和相邻臂具有柔性的单个金属丝或线圈。在一些情况下,其中至少一个臂包括螺旋的区段。在一些情况下,在心脏的天然二尖瓣区域植入假体装置的方法包括将递送装置远端部分内的假体装置递送至天然二尖瓣区域,收回递送装置的外鞘以暴露假体装置的心室锚,迫使心室锚远离递送装置径向扩张,推进假体装置穿过天然二尖瓣——因此心室锚移动到天然二尖瓣瓣叶后方,使心室锚朝向递送装置径向缩回,和收回递送装置的内鞘,从而使假体装置的主体在天然二尖瓣内径向扩张。在一些情况下,收回外鞘的行为使迫使锚扩张的锚扩展器暴露。在一些情况下,锚扩展器偶联至内鞘,并且收回外鞘的行为使得锚扩展器自内鞘弹性地径向延伸,从而迫使锚扩张。在一些情况下,收回内鞘的行为包括部分地收回内鞘,从而允许假体装置的心房部分在主体扩张前径向扩张。在一些情况下,收回内鞘的行为进一步包括完全收回内鞘,从而允许假体装置的主体部分径向扩张。在一些情况下,方法包括将定向装置引至患者心脏的天然二尖瓣区域,展开定向装置的回波发生臂(echogenicarm),利用回波心动描记术观察天然二尖瓣区域内的定向装置的回波发生臂,将定向装置的臂定向以对准天然二尖瓣的A2和P2区域,在臂对准A2和P2区域时沿穿过定向装置延伸的直线对准荧光镜的荧光镜轴线,从患者心脏移除定向装置,将假体装置引至天然二尖瓣区域,和将假体装置的锚在A2或P2区域其中一个处定位在其中一个天然二尖瓣瓣叶的后方,锚在荧光镜上可视。在一些情况下,回波发生臂包括两个回波发生臂,其远离定向装置的轴的远端部分径向延伸。在一些情况下,轴远端部分进一步包括荧光镜标记带,该荧光镜标记带具有布置在其中的第一和第二孔(aperture),并且对准荧光镜轴线的行为包括将荧光镜轴线对准从第一孔至第二孔延伸的直线。本发明的前述和其它目的、特征和优势将通过下文参考附图进行的详细描述显而易见。附图简述图1是人心脏的剖视图。图2是人心脏的另一剖视图,显示二尖瓣区域。图3是天然二尖瓣解剖结构的示意图,显示通过腱索附接至乳头肌的二尖瓣瓣叶。图4A是天然二尖瓣的图,显示Carpentier命名。图4B显示天然二尖瓣和瓣叶之间的间隙。图4C和4D显示定位在天然二尖瓣内的示例性假体瓣膜。图5是假体瓣膜的示例性实施方式的侧视图。图6显示相对于瓣膜纵轴旋转90度的图5的假体瓣膜。图7是图5所示假体瓣膜的心室(流出)视图。图8–10是相应于图5–7的视图,显示图5–7的假体瓣膜的框架的示例性实施方式。图11–16是图9的框架的一系列侧视图,无心房密封构件,显示心室锚和主体之间随主体径向压缩而增加的瓣叶接收空间。图17–22分别是相应于图11–16的一系列端视图。图23是心脏的剖视图,显示植入二尖瓣区域的图9的框架,其中天然二尖瓣瓣叶被捕获在主体和心室锚之间。图24显示图9的心房密封构件、主体和心室锚的示例性尺寸。图25显示框架的示例性实施方式,其中不包括心房密封构件,包括从主体的心室端向下延伸的“T”形推动构件。图26显示框架的示例性实施方式,其中不包括心房密封构件,包括从主体的心室端向下延伸的“V”形推动构件。图27–29显示假体瓣膜的示例性实施方式,其具有带有四个心室锚的框架。图30–32显示图27–29所示假体瓣膜的框架。图33是心脏剖视图,显示植入二尖瓣区域的图30–32的框架。图34是心脏剖视图,显示框架的一种实施方式,其包括延伸的心室锚和心房密封构件,其被植入二尖瓣区域,使得二尖瓣环和/或天然瓣叶被压缩在延伸的心室锚的端部和心房密封构件之间。图35和36是框架的示例性实施方式的侧视图,其包括“S”形心室锚。图37和38分别是框架的示例性实施方式的侧视图和顶视图,其中不包括心房密封构件,包括较宽形状的心室锚。图39是心脏剖视图,显示植入二尖瓣区域的框架的一种实施方式,其中心室锚在扩张后保持与框架体分离,并且心室锚接触二尖瓣瓣叶的下端,以利用来自腱索的张力固定框架。图40显示框架的示例性实施方式,其包括基本上平坦的心房密封构件。图41显示框架的示例性实施方式,其包括向上延伸的心房密封构件。图42显示框架的示例性实施方式,其包括向上延伸的心房密封构件和延伸的心室锚。图43显示框架的示例性实施方式,其中不包括心房密封构件,包括宽型设定(wide-set)的心室锚。图44描绘框架示例性实施方式的一系列侧视图,其中不包括心房密封构件,具有上掀至最终构型(configuration)的心室锚。图45描绘框架示例性实施方式的一系列侧视图,其中不包括心房密封构件,具有上卷至最终构型的心室锚。图46A–46C显示框架的示例性实施方式,其中不包括心房密封构件,其中主体与心室锚分开制造。图47A–47D显示框架的另一实施方式,其中不包括心房密封构件,其中主体与心室锚分开制造并且利用套筒附接。图48A–48C显示框架的另一实施方式,其中不包括心房密封构件,其中主体与心室锚分开制造并且利用带有机械锁的套筒附接。图49显示将假体瓣膜递送和植入在心脏的天然二尖瓣区域的递送系统的示例性实施方式。图50是图49的递送系统的远侧部分的详细视图。图51是图49的递送系统的手柄部分的剖视图,沿剖面线51–51截取。图52是图49的递送系统的手柄部分的剖视图,沿剖面线52–52截取。图53是图49的递送系统的可插入部分的剖视图,沿剖面线53–53截取。图54显示图49的递送系统,其中假体瓣膜位于带槽内鞘内,并且心室锚通过内鞘的槽向外延伸。图55是处于递送位置的图49的递送系统的剖视图,其在內鞘和外鞘内和鼻锥体和推轴(pushershaft)末端之间包含假体瓣膜。图56是图49的递送系统的远端部分的剖视图,显示递送系统外鞘被收回,使得心室锚通过内鞘的槽向外延伸。图57是心脏剖视图,显示左心室中利用图49的递送系统展开前的假体瓣膜心室锚。图58是左心室角度的心脏二尖瓣区域的视图,显示心室锚从递送系统中的槽延伸并且显示心室锚定位在各个二尖瓣瓣叶和心室壁之间。图59是心脏剖视图,显示假体瓣膜利用图49的递送系统被植入二尖瓣区域,其中天然瓣叶定位在心室锚和内鞘之间。图60是图49的递送系统的剖视图,显示带槽内鞘被收回至假体瓣膜心室锚接触包围带槽内鞘的缺口支持带(notchedretainingband)的点。图61是图49的递送系统的剖视图,显示带槽内鞘在带断开后被完全收回,并且假体瓣膜处于在从鞘中完全展开后的扩张状态。图62是左心室角度的心脏二尖瓣区域的视图,显示假体瓣膜的示例性实施方式被完全植入,并且二尖瓣瓣叶被捕获在主体和心室锚之间。图63显示根据另一实施方式用于递送至心脏的天然瓣膜区域的导管鞘内的假体瓣膜的示例性实施方式。图64显示图63的假体瓣膜,其中导管鞘被拉回,使得心室锚自由扩张,但主体保持压缩。图65显示图63的假体瓣膜,其中外鞘重新捕获主体,从而只有心室锚暴露。图66是心脏剖视图,显示图65的假体瓣膜采用经心房方式被植入天然二尖瓣区域。图67是心脏剖视图,显示图65的假体瓣膜采用经横膈膜(transeptal)方式被植入天然二尖瓣区域。图68是左心室角度的二尖瓣区域的视图,显示心房递送的假体瓣膜的实施方式,其具有在鞘之外延伸的心室锚并且定位在天然二尖瓣瓣叶和心室壁之间。图69是左心室角度的二尖瓣区域的视图,显示图68的假体瓣膜,其完全扩张并且锚定至天然二尖瓣瓣叶。图70是心脏剖视图,显示对接框架和单独展开的假体瓣膜的实施方式,该对接框架固定至二尖瓣区域的天然组织,该单独展开的假体瓣膜在对接框架的腔内固定至对接框架。图71是用于在天然二尖瓣区域植入以治疗二尖瓣反流的假体装置的实施方式的透视图。图72是图71的假体装置的侧视图。图73是图71的假体装置的另一侧视图。图74是图71的假体装置的端视图。图75–79是心脏剖视图,显示图71的假体装置经横膈膜递送。图80是图71的假体装置的可选实施方式的侧视图,包括假体瓣膜。图81是图71的假体装置的可选实施方式的部分侧视图,包括Z形切割(Z-cut)的框架体。图82是图71的假体装置的可选实施方式的部分侧视图,包括栅格状框架体和假体瓣膜。图83是图71的假体装置的可选实施方式的部分侧视图,包括螺旋状框架体。图84和85显示植入具有“L”形心室锚的示例性假体装置的示例性方法。图86和87显示植入另一具有“L”形心室锚的假体装置的另一示例性方法。图88是天然二尖瓣区域的心室视图。图89显示定向装置的示例性实施方式。图90显示图89的定向装置的臂部件的细节。图91–94显示图89的定向装置的示例性展开顺序。图95A和95B显示在心脏的天然二尖瓣区域中展开的图89的定向装置。图96显示荧光镜装置的示例性实施方式。图97和98是图89的定向装置的端视图,显示使定向装置定向的示例性方法的步骤。图99显示在荧光透视术下观察到的在心脏的天然二尖瓣区域中展开的图89的定向装置。图100A–100F显示假体装置的心房部分的多种示例性轴向构型。图101A–125B显示具有多种轴向和径向构型的假体装置的多种示例性心房部分,及其不同部件。图126–130显示另外的具有不对称径向构型的假体装置的心房部分。图131显示另外的具有总体上鞍形构型的假体装置的心房部分。图132A–132C显示假体装置的另一心房部分。图133A–133C显示假体装置的具有孔的另一心房部分。图134显示具有总体上截头锥形主体的假体装置。图135显示具有总体上截头锥形主体的假体装置的框架。图136显示另一假体装置,其具有跨越心房部分和主体心室端之间的两个织物。图137A–137B显示具有另一示例性心房部分的示例性框架。图138显示另一示例性假体装置。图139显示另一示例性假体装置。图140显示处于天然组织的假体装置。图141显示扩张辅助递送装置的示例性实施方式。图142显示图141的递送装置的近端部分的部分侧视图。图143–146显示图141的递送装置的远端部分的部分视图。图147–151显示图141的递送装置的示例性展开顺序。图152A–152E显示递送装置的示例性假体瓣膜固定装置。图153A–153G显示另一示例性假体瓣膜固定装置。图154–156显示递送装置的示例性展开顺序,包括图153A–G的操控装置(harnessdevice)。发明详述本文描述了主要旨在植入人心脏二尖瓣区域的假体瓣膜及其部件的实施方式,以及其植入装置和方法。假体瓣膜可用于协助恢复和/或代替缺陷性天然瓣膜的功能性。人心脏人心脏的相关部分显示在图1和2中。健康的心脏具有至下顶点38逐渐变细的总体上圆锥形状。心脏是四室的,包括左心房4、右心房26、左心室6和右心室28。心脏的左侧和右侧被壁隔离,该壁通常被称为中隔30。人心脏的天然二尖瓣2将左心房4连接至左心室6。二尖瓣2具有不同于其它天然心脏瓣膜如主动脉瓣14的解剖结构。二尖瓣2包括环部分8,其是二尖瓣口周围的天然瓣膜组织的环形部分;和一对瓣尖(cusp)或瓣叶10、12,从环8向下延伸到左心室6中。二尖瓣环8可形成“D”形、卵形或具有主轴和次轴的非圆形横截面形状。前叶10可大于后叶12,如图4A示意性显示,当其闭合在一起时瓣叶的邻接自由边缘之间形成总体上“C”形边界。图4B显示天然二尖瓣2,其中瓣叶10、12之间具有微小间隙3,如缺陷性天然二尖瓣不能完全闭合,其可导致二尖瓣反流和/或其它不期望的状况。在正常运转时,前叶10和后叶12合力充当单向瓣膜,仅允许血液从左心房4流至左心室6。左心房4接收来自肺静脉32的氧合血液。当左心房4的肌肉紧缩而左心室舒张时,聚集在左心房4中的氧合血液流入左心室6。当左心房4的肌肉放松而左心室6的肌肉紧缩时,左心室中的增加的血压将两个瓣叶推动到一起,从而闭合单向二尖瓣,因此血液无法流回左心房,取而代之的是通过主动脉瓣14被赶出左心室。为防止两个瓣叶10、12在压力下脱出和通过二尖瓣环8向左心房4回折,多个纤维索——被称为腱索16——将瓣叶10、12束缚至左心室6的乳头肌。参考图3和4,腱索16附接和延伸在后中乳头肌22和前叶10和后叶12的后中缘(分别是根据Carpentier命名确定的A1和P1区域)之间。类似地,腱索16附接和延伸在前外乳头肌24和前叶10和后叶12的前外缘(分别是根据Carpentier命名确定的A3和P3区域)之间。A2和P2区域相对不具有腱索附接点,并且提供可锚定假体二尖瓣的区域(参见图3)。另外,腱索的机构提供进入方式,以最小腱索缠结风险递送假体二尖瓣。假体瓣膜在天然二尖瓣不能正常工作时,假体瓣膜置换可有助于恢复适当的功能性。然而,与主动脉瓣14(其具有相对圆且坚固的环)(特别是在主动脉狭窄的情况下)相比,二尖瓣环8可相对较不坚固并且较不稳定。因此,可能不能仅依靠来自压抵天然二尖瓣环8的假体瓣膜的外表面的径向力的摩擦,就将被设计主要用于主动脉瓣的假体瓣膜固定在天然二尖瓣环8内。因此,本文描述的假体瓣膜可依靠心室锚,代替或补充径向摩擦力,来将假体瓣膜固定在天然二尖瓣环8内(例如,参见图23)。除为假体瓣膜提供锚定装置外,心室锚还可重塑左心室6,以有助于治疗二尖瓣反流的潜在病因——左心室扩大/舒张。心室锚可将天然二尖瓣瓣叶10、12更紧密地牵引在一起和牵引向左心房,并且从而通过腱索16将乳头肌22、24更紧密地牵引在一起,乳头肌22、24可积极地快速地重塑心室和防止左心室进一步扩大。因此,心室锚也可被称为张力构件或重塑构件。图5–7示例根据一个实施方式的示例性假体瓣膜100,其可被植入心脏的天然二尖瓣区域,以代替天然二尖瓣2的功能。假体瓣膜100包括框架102和被框架和/或在框架内支撑的瓣膜结构104。瓣膜结构104可包括多个假体瓣叶106(在示例的实施方式中是三个)和/或用于调控血液沿一个方向通过假体瓣膜100流动的其它部件。在图5和6中,例如,瓣膜结构104在框架102内被定向使得瓣膜结构的上端110是流入端,并且瓣膜结构的下端112是流出端。瓣膜结构104可包括各种适当材料中的任意种,如天然组织(例如,牛心包组织)或合成材料。瓣膜结构104可用适当的技术和机构被安装至框架102。在示例的实施方式中,例如,瓣叶106按照三尖瓣排列被缝合至框架102,如图7所示。描述关于假体瓣膜部件和组装件的另外的细节(包括将瓣叶安装至框架的技术)被描述于例如美国专利申请公开号2009/0276040A1和美国专利申请号12/393,010,其被引入本文作为参考。如图8–10所示,框架102可包括管状主体122、延伸自主体的心室端130的一个或多个心室锚126和任选地从主体的心房端132径向向外延伸的心房密封构件124。当框架102被植入心脏的天然二尖瓣区域时,如图23所示,主体122被定位在天然二尖瓣环8内,其中主体122的心室端130是下出口端,主体132的心房端132是上进口端,心室锚126位于左心室6中,并且心房密封构件124位于左心房4中。框架102可由丝网制成,并且可以是在径向扩张状态和径向压缩状态之间径向可折叠的和可扩张的(如图11–16和17–22的一系列连续阶段中示意性显示),以实现在心脏二尖瓣区域(或在另一天然心脏瓣膜镍)的递送和植入。图11–22显示的框架102的实施方式不包括心房密封构件124,尽管框架102的其它实施方式包括心房密封构件124。丝网可包括金属丝或支柱,其以栅格状图案排列,如例如图8–10显示的锯齿状或Z字型图案,但也可采用其它图案。框架102可包括形状记忆材料,如例如镍钛诺,以实现从径向压缩状态自扩张至扩张状态。在可选的实施方式中,框架102可以是通过扩张装置(如例如可膨胀的球囊)(未显示)可从径向压缩状态塑性扩张至扩张状态的。这种塑性扩张的框架可包括不锈钢、铬合金和/或其它适当的材料。在扩张状态下,如图8–10所示,框架102的主体122可形成开口管(open-endedtube)。瓣膜结构104可偶联至框架102的内表面——如经由框架内表面的材料层142,如下文讨论,并且可被固定在通过主体122形成的腔内,如图7所示。主体122的外表面的尺寸可类似于二尖瓣口,即,二尖瓣环8的内表面,但并非一定。在一些实施方式中,例如,主体122的外表面的直径尺寸可小于天然二尖瓣口的直径尺寸,使得扩张状态的主体122可适配在二尖瓣口内,而天然二尖瓣环8无显著拉伸,如图23中。在这种实施方式中,框架102无需依靠主体122的外表面和二尖瓣环8的内表面之间的压力配合或摩擦配合来进行假体瓣膜止动。取而代之,框架102可依靠心室锚126和/或心房密封构件124进行止动,如下文进一步描述。然而,在其它实施方式中,主体122可被配置以扩张至等于或大于天然二尖瓣口的尺寸,从而在被植入时产生压力配合。在其中主体122包括小于天然二尖瓣口直径尺寸的直径尺寸的实施方式中,主体可松散地坐落或“漂浮”在天然瓣叶10、12之间。如图4C所示,这种松散的配合可在瓣叶10、12和框架主体122之间产生间隙37。为防止血液在假体瓣膜100外侧和天然瓣膜组织之间流动(如通过间隙37),环形心房密封构件124可产生与二尖瓣环8心房侧上的天然组织的完全环形接触区域或密封。因此,如图4D所示,心房密封构件124可被设定尺寸以完全覆盖间隙37。框架102的末端可具有锯齿状或Z字型图案,如图8–10所示,例如包括在其上端连接在一起的一系列肩并肩“V”形部分。该图案可有利于压缩,并且可有助于最大化框架与天然组织连接的表面积。可选地,框架102的末端可具有直线边缘或一些其它图案。在一些实施方式中,主体122可包括至少一个从主体122的心室端130向下延伸的延伸构件或推动构件。图25所示的框架202例如包括叉204形式的延伸自主体222的“V”形部分中的一个的下顶点的延伸构件。叉204可具有倒置的“T”形状,包括下推动面(lowerpushingsurface)206。在另一实施方式中,图26所示的框架302包括“V”形推动构件304,其延伸自主体322的两个相邻下顶点,并且包括推动面306。推动面206和306分别可包括处于框架202和302上的最低点,并且可为在不接触心室锚226、326的情况下被赶出递送装置的框架提供推动面,如下文更详细描述。再次参考图8–10显示的实施方式,框架102的心房密封构件124可与主体122一体,并且可由与主体122相同的丝网栅格构成,使得心房密封构件124也可以是径向可折叠的和可扩张的。在扩张状态下,心房密封构件124可总体上是截头锥形的,并且从主体122的心房端132径向向外和轴向向下朝向主体122的心室端130延伸。心房密封构件124的外轮缘140可被设定尺寸和形状以在框架102被植入时接触二尖瓣环的心房侧和左心房8的组织,如图23所示。外轮缘140的端视图外形,如图10所示,可具有总体上圆形、卵形或总体上相应于心房壁18和二尖瓣环8的天然几何的其它形状。心房密封构件124和心房壁18组织和/或二尖瓣环8之间的接触可促进组织与框架一起向内生长,这可增强止动和减少瓣周漏。心房密封构件124期望地被设定尺寸,使得在假体瓣膜100被植入天然二尖瓣时,如图23所示,外轮缘140接触包围整个天然瓣膜的天然环8,因此完全覆盖天然瓣叶10、12之间的开口。心房密封构件124期望地包括血流不可透的密封层142。以这种方式,心房密封构件124能够阻止血液在假体瓣膜100外表面和天然瓣膜组织之间流回到左心房中。心房密封构件还确保全部或基本上全部血液在其从左心房流至左心室时通过单向瓣膜。如图5–7所示,至少一个生物相容性片或层142可连接至主体122的内表面和/或外表面和心房密封构件124,以形成至少一个层或封皮,覆盖丝网孔。层142可例如通过缝线连接至框架102。层142可形成流体阻塞和/或密封构件,其可至少部分地阻止血流穿过丝网以减少瓣周漏,并且可促进组织与框架102一起内向生长。层142可提供安装表面或支架,部分瓣膜结构104如瓣叶106可被固定于此。例如,图5和6中的虚线108表示可将瓣叶106的进口端缝补、缝合或以其它方式固定至层142的位置。瓣叶106进口端和层142之间的这个接合处可构成围绕层142的内周连续的密封,并且可阻止层142内表面和瓣叶106外表面之间的血流。这种密封可允许假体瓣膜100引导血液在多个瓣叶106之间流动。相同的层142和/或一个或多个单独的套头(cuff)144还可缠绕或覆盖框架102的端边缘,如主体122的心室端130和/或心房密封构件124的外轮缘140。这种套头144可覆盖和保护框架102的末端的尖锐边缘。例如,在图5所示的实施方式中,层142从外轮缘140,跨越心房密封构件124的上表面,沿主体122的内表面向下延伸,并且包括缠绕和覆盖主体122的心室末端部分的套头144。层142可被缝合至外轮缘140和主体122内表面。层142可包括阻止血流但可允许组织向内生长的半多孔织物。层142可包括合成材料,如聚酯材料或生物相容性聚合物。聚酯材料的一个实例是聚对苯二甲酸乙二醇酯(PET)。可使用替代材料。例如,层可包括生物学物质,如天然组织、心包组织(例如,牛、猪或马心包)或其它生物学组织。参考图8和9,一个或多个心室锚126可延伸自框架102的主体122,如主体的心室端130。心室锚126可用以将带有或不带有瓣膜结构104的框架102固定在心脏的天然瓣膜区域内。在图8和9所示的实施方式中,框架102包括两个沿直径相对的心室锚126,其可分别用以在框架102被植入二尖瓣区域时将框架102固定至前和后二尖瓣瓣叶10、12,如图23所示。在可选的实施方式中,框架102可具有三个或更多个心室锚126,其可围绕框架主体122成角度间隔。当框架102处于扩张状态时,如图9,框架的几何可导致心室锚126被推动抵靠主体122的外表面。可选地,心室锚126可被配置以在框架102处于扩张状态时与主体122外表面相隔(例如,参见图39)。在任何情况下,当框架102被径向压缩至压缩状态时,可增加心室锚126和主体122外表面之间的空间或间隙,如图11–16所示。在主体122和心房密封构件124处于压缩状态时,框架102可被插入二尖瓣口,使得相隔的心室锚126缠绕于瓣叶10、12并在瓣叶和心室壁20之间向上延伸(例如,参见图59)。参考图23,前心室锚146可位于前叶10后方,并且后心室锚148可位于后叶12后方。参考图3和4,两个心室锚期望地位于各自的瓣叶后方,接近大约在两个瓣叶汇合的接合处36之间的中途的瓣叶中间部分A2、P2。瓣叶10、12的这些中间部分A2、P2是期望的心室锚位置,因为与更接近接合处36的位置相比,这些位置的腱索16与瓣叶的附接较疏。当随后主体122被扩张或自扩张至扩张状态时,如图11–16所示,以相反顺序,心室锚被配置以在对心室锚没有外部压缩力的情况下相对于主体122径向向内枢转。这导致心室锚126和主体122外表面之间的间减少,从而实现在心室锚和主体之间捕获瓣叶10、12。相反,压缩主体122导致心室锚126远离主体枢转,以增加主体外表面和心室锚之间的间隙。在一些实施方式中,心室锚126的自由端或顶点162可在主体122在对心室锚无外部力的情况下被径向压缩或扩张时彼此保持基本上相同的距离。在一些实施方式中,如图23所示实施方式,框架被配置以在框架扩张至扩张状态时压缩主体和心室锚之间的天然二尖瓣瓣叶10、12。在其它实施方式中,如图39所示实施方式,心室锚不压缩或夹紧天然瓣叶抵靠主体,但仍通过在天然瓣叶10、12周围勾住心室锚防止假体瓣膜向左心房迁移。在这种实施方式中,假体瓣膜100可被固定就位,通过下文进一步描述的心房密封构件124防止向左心室迁移。参考图8–10所示的实施方式,每个心室锚126可包括由形状记忆材料(如例如镍钛诺)构成的柔性细长构件或丝150。在一些实施方式中,如图8所示,各丝150可包括偶联至主体122的第一附接位置156的第一端部分152和偶联至主体的第二附接位置158的第二端部分154。第一和第二端部分152、154构成心室锚的基础。主体的第一和第二附接位置152、154可处于或邻近主体122的心室端130。各丝150的两个端部分152、154可构成主体122的栅格网的丝或支柱的延伸。各丝150进一步包括沿主体纵向在端部分152、154之间延伸的中间部分160。中间部分160包括弯曲处162,其构成心室锚的自由端部分或顶点。丝150可具有垂直于丝长的圆形或非圆形横截面外形,如多角形横截面外形。参考图8A,丝150可包括矩形横截面形状,具有长度“L”和相对窄的宽度“W”,使得在附接至框架102的心室锚126的两个端部分152、154相向移动时,如在框架被压缩时,丝150主要沿宽度方向弯曲。这促进心室锚126沿远离主体122径向向外的方向弯曲,加宽心室锚126和主体122之间的间隙。此特征可有助于在植入过程中在心室锚126和主体122之间捕获瓣叶。心室锚可包括不同形状或构型。一些框架实施方式,如图8显示的框架102,包括总体上“U”或“V”形心室锚126,其在两个附接位置156、158处连接至主体122。心室锚126的上顶点162可如同楔形物用以有助于将心室锚移动到各个瓣叶后方,同时最小化腱索缠结的风险。各丝150的端部分152、154可分别从附接位置156、158向下延伸,在主体122的心室端130处。然后丝150可从各端部分152、154朝向顶点162向上回弯。丝150可被生物相容性材料覆盖,如在图5–7所示实施方式中。第一材料164可缠绕或涂覆至丝150的至少一些部分。第二材料166可跨越丝150的两个部分,形成网,其可改善组织向内生长。第一和第二材料164、166可包括相同材料或不同材料,如生物相容性半多孔织物,例如。覆盖材料164、166可增加组织内向生长,并且心室锚126增强止动。此外,覆盖材料可减少心室锚126的摩擦性以利于植入,和/或增加心室锚的摩擦性以增强止动。图24显示图9显示的框架102的实施方式的示例性尺寸。心房密封构件124的外轮缘140的直径“Dmax”可范围为约50mm至约70mm,并且在一个实例中为约50mm。主体122的外表面的直径“D主体”可范围为约23mm至约50mm,并且在一个实例中为约29mm。一个心室锚126的两个附接点156、158之间的距离“W1”可范围为约8mm至约50mm,并且在一个实例中为约25mm。框架102的总轴向高度“Hmax”可范围为约20mm至约40mm,并且在一个实例中为约30mm。外轮缘140至心室锚126的最低部分168的轴向高度“H1”可范围为约10mm至约40mm,并且在一个实例中为约23mm。心室锚126的顶点162至心室锚126的最低部分168的轴向距离“H2”可范围为约10mm至约40mm,并且在一个实例中为约18mm。主体122的下端130至心室锚126的最低部分168的轴向距离“H3”可范围为约0mm至约10mm,并且在一个实例中为约5mm。一些框架实施方式包括多于两个心室锚。例如,框架可具有两个或更多个心室锚,其配置以附接至沿天然瓣膜单个瓣叶的多个位置。在一些这样的实施方式(未显示)中,框架可包括附接至前二尖瓣瓣叶10的两个心室锚和/或附接至后二尖瓣瓣叶12的两个心室锚。心室锚还可附接至瓣叶其它区域以代替A2和P2区域;或除了A2和P2区域,心室锚还可附接至瓣叶其它区域。一些假体瓣膜实施方式包括围绕主体平均间隔的四个心室锚。图27–32显示一个这样的假体瓣膜实施方式400,其包括框架402,该框架402包括处于主体422直径相对侧的一对心室锚426和大约位于心室锚426之间中途的沿直径相对的一对接合处锚428。心室锚426从附接点456和458向下延伸,并且包括颈部450(参见图31)。这些心室锚426可与框架102的心室锚126的功能相似,用于捕获瓣叶和将框架402固定在二尖瓣口内,如图33所示。接合处锚428可从主体422上的相同附接位置456、458向上延伸(参见图30)。虽然心室锚426可夹住分别处于A2和P2区域的二尖瓣瓣叶10、12,接合处锚428可勾回(hookaround)并向上延伸到二尖瓣接合处36后方,不压缩瓣叶。接合处锚428的顶点464可向上延伸以邻接二尖瓣环8的心室侧并压缩心房密封构件424的外轮缘440和接合处锚428的顶点464之间的二尖瓣环8。二尖瓣环8的这种压缩可提供另外的止动,防止心房和心室移动。其它框架实施方式可包括多于四个心室锚。例如,框架可包括可啮合瓣叶10、12上多个位置和/或接合处36的六个或更多个心室锚。图34显示框架实施方式502,其包括延伸的心室锚526,该心室锚526被配置以围绕瓣叶10、12的末端延伸和在瓣叶后方向上延伸至接近向下延伸的截头锥形心房密封构件524的外轮缘540的位置。延伸的心室锚526的上顶点562接触二尖瓣环8的心室面和/或天然瓣叶10、12的邻近环的部分或瓣叶的环连接部分,同时心房密封构件524的外轮缘540接触二尖瓣环的心房面和/或瓣叶的环连接部分。延伸的心室锚526和心房密封构件524可被配置以彼此相对,并且期望地压缩二尖瓣环8和/或瓣叶10、12的环连接部分,以固定框架502,防止沿心房和心室方向移动。因此,在此实施方式中,心室锚526无需将天然瓣叶10、12压抵框架主体522的外表面。取而代之,如图34所示,瓣叶10、12可被松散地捕获在延伸的心室锚526和主体522的外表面之间。图35和36显示框架实施方式602,其包括颈状“S”形心室锚626。根据图35的侧视图,心室锚626的“S”形可见。始于主体622的心室端630上的一个附接点A,心室锚丝650向下延伸并从主体径向向外延伸至B点,然后向上和向外弯曲至C点,然后向上和向内弯曲至D点,然后向上和反向向外弯曲至最高点或顶点E。然后心室锚丝650遵循相似但镜像的路径继续反向延伸至第二附接点。根据图36的正视图,心室锚丝650形成关于延伸过体622中心的纵向中心轴线690对称的颈状,形成两个镜像半场。心室锚丝650的每个半场起始于主体622的心室端630上的附接点A,向下和向内弯曲(朝向另一半场)至B点,然后向上和向内弯曲至C点的颈状部分,然后向上和向外弯曲(远离另一半场)至D点,然后再次向上和向内弯曲至最高点或顶点E,在此这两个半场接合在一起。参考图35,主体622的纵向中心轴线690至C和E点的径向距离均大于轴线690至D点的径向距离。此外,两个C点之间的距离小于两个D点之间的距离。“S”形心室锚626可有助于更平均地沿丝650分布应力和减少某些位置如附接点A的应力浓度。图37和38显示框架实施方式702,其包括两个较宽形心室锚726。各较宽形心室锚726包括颈状中部780和宽上部782。上部782可总体上平行于框架702的流入口延伸,并且可围绕主体722的外表面弯曲。这种较宽形状可增加与天然瓣叶和/或其它心脏组织的表面接触,以减少压力并从而减少磨损。在一些实施方式中,较宽形心室锚726的宽上部782可具有曲度,该曲度相应于主体722外表面的曲度(参见图38),以进一步改善组织接触。较宽形心室锚可具有与心房密封构件较长的表面接触;从而增加止动性能和减少瓣周漏。图39显示框架实施方式802,其包括心室锚826,该心室锚826被配置以限定锚和主体822之间的间隔或间隙——甚至在框架802扩张后(虽然锚826可另外功能类似于心室锚126、使得锚826和框架主体822之间的间隙可在主体压缩和扩张时分别增加和减少,以利于将锚826布置在天然瓣叶后方)。间隙可被设定尺寸以利于在天然瓣叶极少压缩或无压缩的情况下捕获天然瓣叶10、12。由于极少或无瓣叶压缩发生,这种框架实施方式802可最小化对天然瓣叶的创伤。代替压缩瓣叶10、12以进行瓣膜止动的是,心室锚826可分别勾住瓣叶10、12的心室边缘40、42,同时框架的心房密封构件824下压二尖瓣环8的心房侧。通过向上牵引心室锚826抵靠瓣叶10、12的心室边缘,心房密封构件824和环8之间的接触导致主体822略微向上位移。心室锚的向上力结合腱索16对瓣叶的向下张力限制植入物朝向左心房4向上移动。图40显示框架实施方式902,其包括主体922、心室锚926和从主体922的上端932径向向外延伸的盘状心房密封构件924。在此实施方式中,心房密封构件924基本上垂直于上端932限定的框架开口延伸,而非朝向框架下端930向下延伸。盘状心房密封构件924可被平放在二尖瓣环8顶表面上,并提供增加的表面积接触,以进行组织向内生长。图41和42分别显示框架实施方式1002和1012,其包括心房密封构件1024,该心房密封构件1024具有总体上截头锥形部分1028,该总体上截头锥形部分1028从主体1022的上端1032径向向外和远离主体轴向向上延伸。心房密封构件1024还可包括总体上圆柱形上端或进口部分1029,该部分从截头锥形部分1028背向主体1022的上端1032进一步向上延伸。心房密封构件1024可总体上相应于心房壁18邻近二尖瓣环8的形状,并提供心房壁组织和心房密封构件1024之间增加的接触面积。框架1002包括心室锚1026,其从主体1022的心室端1030开始并且沿着主体的大部分长度延伸。图42显示的框架1012包括延伸的心室锚1050。延伸的锚1050可从主体1022的心室端1030沿着主体的外表面延伸,并且径向向外弯曲,形成沿着截头锥形部分1028的下表面延伸的上部1060。这种构型可允许延伸的心室锚1050至捕捉瓣叶10、12中的更多个和/或二尖瓣环8抵靠框架,从而减少瓣周漏和增强组织向内生长和止动。图43显示框架实施方式1102,其具有心室锚1126,该心室锚1126与图9显示的框架102的心室锚126相比具有较短力臂D2。较短力臂D2可导致心室锚附接点1156、1158处扭矩减少。距离D2可通过增加相邻心室锚1126的主体1122上的附接点1158和1156之间的距离D1来减少。框架1102的心室锚1126之间的距离D1大于框架102的附接点158和156之间的距离D1(参见图9),因此缩短相对于附接点1156的力F的力臂D2。附接点1156和1158处的扭矩减少可减少疲劳,因此提高框架1102的持久性。心室锚的一些实施方式可任选地还包括一个或多个倒钩(未显示),其可从心室锚朝向心室壁20或朝向瓣叶10、12径向突出。这种倒钩可有助于固定框架,具体地防止朝向左心室6移动。图44A–44D示例框架实施方式1202,其包括“上掀式”心室锚1226。各心室锚1226可以是指状的,并且可延伸自主体1222的下端1230上的仅一个附接点。可选地,各心室锚可包括丝或延伸自主体1222上的两个附接点的类似的构件。在示例的实施方式中,心室锚1226可预先成形,以功能性展开状态沿主体1222的外侧延伸,如图44D所示。在递送过程中,心室锚1226可部分或完全拉直,如图44A所示,并被递送装置如鞘固定在该状态。在框架1202被驱离鞘时,例如,心室锚1226弹回至其预先成形的形状,如图44B–44D所示,捕获心室锚1226和主体1222之间的瓣叶10、12。图45A–45E是框架实施方式1302,包括“上卷式”心室锚1326。如同图44的心室锚1226,各心室锚1326可以是指状的,并且可延伸自主体1322的下端1330上的两个或更多个点。心室锚1326可以曲线形状预先成形,如图45E所示,沿展开状态的主体1322那侧延伸。在递送过程中,心室锚1326可部分或完全拉直,如图45A所示,并且被递送装置如鞘固定在该状态。在框架1302被驱离鞘时,例如,心室锚1326被允许弹回至其预先成形的曲线形状,如图45B–45E所示,捕获心室锚1326和主体1322之间的瓣叶10、12。在一些框架实施方式中,一个或多个心室锚部件可单独由主体形成,并稍后组装在一起,形成框架。在一个这样的框架实施方式1402中,如图46A–46C所示,主体1422单独由至少一个心室锚部分1424形成。心室锚部分1424可包括一个或多个心室锚1426,该心室锚1426延伸自至少部分环形的基体1432,该基体1432可包括在其上端连接在一起的肩并肩“V”形支柱部分。在示例的实施方式中,心室锚1426的下端连接至基体1432的“V”形部分下顶点处。在主体和心室锚部分单独形成后,心室锚部分1424可附接至主体1422的下部1430。例如,可将基体1432布置在主体1422的外表面的对侧,然后缝合,焊接或以适当的方式附接至主体1422的下部1430,如通过利用锁定机构。基体1432可被附接至主体1422,使得基体的“V”形部分与主体1422的下端1430的相应“V”形部分重叠。在一些实施方式中,心室锚部分1424可包括全环,其中全部心室锚1426延伸自一个环形基体,使得心室锚预先彼此间隔。然后环形基体可被附接在主体1422的下端1430周围。在其它实施方式中,多个心室锚部分1424——每个具有一个或多个心室锚1426延伸自各自的包括部分环的基体1432——被固定至主体1422。图47A–47D和图48A–48C显示可选的框架实施方式,其中一个或多个心室锚部件由主体单独形成,并稍后组装在一起,形成框架。在这些框架实施方式中,主体可包括附接部分,锚部分可利用套筒被附接至该附接部分。例如,图47A–47D显示示例性框架1500,其包括主体1502,该主体1502具有至少两个心室锚附接部分1508;和至少一个心室锚1504,该心室锚1504具有两个附接部分1510,两个附接部分1510利用各自的套筒1506连接至各自的附接部分1508。类似地,图48A–48C显示示例性框架1600,其包括主体1602,该主体1602具有至少两个心室锚附接部分1608和至少一个心室锚1604,该心室锚1604具有两个附接部分1610,两个附接部分1610利用各自的套筒1606连接至各自的附接部分1608。套筒可包括,例如,具有超弹性和/或形状记忆特征的金属材料,如镍钛诺。在一些实施方式中,套筒可包括适于卷边工艺(crimpingprocess)的退火状态的金属。套筒可通过任何适当的附接手段(如通过焊接)被附接至锚部分和主体的附接部分。如图48A–48C所示,锚1604的附接部分1610和主体1602的附接部分1608可包括允许套筒1606将锚部分1604整合至主体1602(如通过形成机械锁)的几何特征,如窄区或裁切部分(cut-out)。框架的多部分构造,如图46–48所示,与一体式或一件式构造相比,可减少心室锚附接位置的应变和疲劳。相比之下,在包括一体式构造的一些实施方式中,心室锚最初被激光切割和扩张,使得其从主体下端向下延伸,然后邻近框架主体的外侧形成或弯曲至期望的构型。这种弯曲可拉紧和弱化弯曲部分。为避免心室锚塑性变形导致的应变,心室锚可在不塑性弯曲心室锚的情况下以期望的植入(展开)形状预先成形。然后可使心室锚弹性变形,如拉直和/或压缩,以配合递送装置,以通过身体递送至心脏的二尖瓣区域。变形的心室锚,一旦从递送装置的轴向约束释放,就可弹性地恢复其预先成形的形状,以利于捕获心室锚和框架主体之间的瓣叶10、12。上述框架多种实施方式中的任一种可与流体阻塞构件如瓣膜结构104组合,形成完全组装的假体瓣膜,该假体瓣膜可被植入天然二尖瓣内。在其它实施方式中,上述任何框架可在无流体阻塞构件的情况下提供,并且可用作支架或对接结构,用于在二阶段递送方法中接收单独的假体瓣膜。参考图70所示的示例性实施方式,对接框架103(其可具有类似于框架102的构造)可先被展开,例如通过上述任何锚定技术。然后,单独的假体瓣膜114可被递送和展开在通过之前展开的对接框架103形成的腔内。单独的假体瓣膜114期望地包括径向可压缩和可扩张的框架116,该框架116安装流体阻塞构件(图70中未显示),如具有多个瓣叶106的瓣膜结构104(参见图7)。当在对接框架103内扩张时,假体瓣膜114的框架116啮合对接框架103的内表面,从而将假体瓣膜114固定(如通过摩擦或机械锁定特征)在对接框架103内。可用于这种二阶段方法的假体瓣膜的实例被公开于美国专利号7,510,575,其被引入本文作为参考。在具体实施方式中,假体瓣膜可包括各种经导管心脏瓣膜中的任一种,如Sapien瓣膜,可购自EdwardsLifesciencesLLC(Irvine,CA)。如图23显所示在心室锚和框架主体之间捕获瓣叶10、12的技术可提供若干优点。第一,这可允许锚定到天然瓣叶10、12上以在二尖瓣区域内止动。第二,此技术可利用天然腱索16进行止动。第三,此技术可防止在左心室6紧缩和血液通过主动脉瓣冲出(收缩期前向运动)时前叶10被“拉”向主动脉瓣14。第四,此技术趋于迫使力天然瓣叶10、12围绕框架主体折叠,这可减少假体瓣膜100外侧和天然二尖瓣2之间的渗漏。第五,此技术允许从左心房4或左心室6植入,如下文详细描述。如上所述,各种框架实施方式可利用压缩瓣叶10、12之外的一种或多种锚定技术来将假体瓣膜100固定在二尖瓣口内的期望位置。这些锚定技术可包括,例如,利用天然腱索16的张力、延伸心室锚长使得心室锚顶点被挤压紧靠二尖瓣环8从而形成停止,和压缩心室锚顶点和框架心房密封构件外轮缘之间的二尖瓣环8和/或心房组织。递送方式下文描述的递送和植入在天然二尖瓣区域的多种方法和装置是关于假体瓣膜100描述的,但应理解相似的方法和装置可用于递送和/或植入假体瓣膜100的部件,如无瓣膜结构104的框架102或其它假体装置。假体瓣膜100可被从左心室6或左心房4递送至二尖瓣区域。基于天然二尖瓣2的解剖结构,可根据假体瓣膜100递送方向使用不同技术和/或器械。二尖瓣环8心室侧的递送可以多种方式完成。例如,可通过经顶点方式递送假体瓣膜100,其中经由心脏顶点38进入左心室6,如图57所示。二尖瓣环8心房侧的递送也可以多种方式完成。例如,可通过心房壁18采取经心房方式,如图66所示,例如通过穿过胸的切口。心房递送也可通过肺静脉32进行(参见图1)。另外,心房递送可通过经横膈膜方式进行,如图67所示,其中在中隔30的心房部分制造切口,以允许从右心房26进入——如经由下或上腔静脉34。心室方式一种将压缩假体装置如假体瓣膜100递送至二尖瓣区域的技术包括从左心室6进入天然二尖瓣区域,经顶点方式的一个实例。可选地,左心室6的进入可通过主动脉瓣14进行。以经顶点方式,左心室6的进入可通过胸切口和心脏顶点38切口进行,如图57所示。经顶点递送系统可用于经顶点方式。图49–53显示示例性经顶点递送系统或递送工具2000,其被配置以递送和植入假体瓣膜100。递送系统2000可包括关于中心轴线对准并且沿轴向方向可彼此相对滑动的一系列同心轴和鞘。递送系统2000可包括近侧手柄部分2002,用于在远端部分或插入部分2004被插入身体时医生在体外操纵。递送系统2000可包括延伸递送系统长度的内轴2006,并且包括引导丝(未显示)可穿过的腔2008。内轴2006可被定位在推轴2010的腔内,并且可具有在近侧延伸超过推轴近端并且在远侧延伸超过推轴远端的长度。递送系统2000可包括内轴2006外表面和推轴2010内表面之间的环形空间2012。此环形空间可用于盐水冲洗或远侧驱赶血液。递送系统2000进一步包括内鞘2014,其被同心地围绕至少远侧部分的推轴2010定位。内鞘2014可在递送位置(参见图55)和收回位置(参见图50)之间相对于推轴2010轴向滑动。在递送位置时,内鞘2014的远端部分2016被定位在推轴2010的远端或推动端2018的远侧。在递送位置时,内鞘2014的远端部分2016构成内腔,其可包含压缩的假体瓣膜100。在收回位置时(参见图50),内鞘2014的远端2017被定位在推动端2018的近侧或轴向对齐推动端2018。在内鞘2014从递送位置移向收回位置(通过相对于推轴2010近侧收回内鞘2014或相对于内鞘远侧推进推轴)时,推动端2018可将假体瓣膜100推到内鞘的远端部分2016外。如图50所示,内鞘2014包括一个或多个纵向布置的槽2028,其在近侧从内鞘远端2017延伸出去。这些槽2028可允许内鞘2014内包含的假体瓣膜100的心室锚126从假体瓣膜的压缩主体径向向外延伸,同时主体以压缩状态固定在内鞘镍。在图50所示的实施方式中,显示两个槽2028定向在内鞘2014的纵向中心轴线的直径相对侧上。此实施方式相应于假体瓣膜100,其包括两个对立的心室锚126。在其它实施方式中,内鞘2014可包括不同数量的槽2028,例如四个槽,该数量相应于所选假体瓣膜上心室锚位置的数量。在一些实施方式中,如图50显示,各槽2028的近端部分2020包括圆形开口,其角宽度大于槽的区域部分。断裂(break-away)或脆性固定带2022可被定位在内鞘2014的远端部分2016周围,如图50所示。带2022可有助于固定内鞘2014的远端部分2016,防止由于内鞘2014内包含的压缩假体瓣膜100的力而张开。带2022包括近侧边缘2024,该近侧边缘2024可包括位于内鞘2014的槽2028上的至少一个缺口2026。带2022可包括脆性材料,并且可被配置以在充足的轴向力施加于缺口2026时在缺口位置处撕裂或断裂。在使用中,带2022被配置以在瓣膜100从内鞘2014展开时,在瓣膜100的心室锚126的力下,在缺口2026处断裂,如下文进一步描述。外鞘2036被同心地围绕部分内鞘2014定位,并且可相对于内鞘轴向滑动。外鞘2036可被定位以覆盖内鞘2014的至少部分远端部分2016。在这样的覆盖位置时,如图55显示,心室锚可被包含在內鞘和外鞘之间。在负载后的递送系统2000被穿过身体且插入左心室6时,外鞘2036处于此覆盖位置。外鞘2036可被相对于鞘2014近侧收回以暴露槽2028和允许心室锚126在展开过程中通过内鞘2014的槽外弹。可选地,内鞘2014可被相对于外鞘2036向远侧推进,以暴露槽2028。参考图51,递送系统2000的手柄部分2002可包括促进内鞘2014和外鞘2036沿其各自的轴向移动范围来回滑动从而负载、递送和展开假体瓣膜100的部件。外鞘把手2052可被附接至外鞘2036的近端。医生可抓住外鞘把手2052并相对于递送系统2000的其余部分近侧或远侧推动或拉动外鞘2036。外鞘也可安装在导螺杆(未显示)上。递送系统2000的手柄部分2002可进一步包括外壳2054,其为医生提供把手或手柄以稳定握持递送系统2000,同时其用另一只手致动鞘。滑动导螺杆2056可被固定(例如,粘合、机械锁定等)至内鞘2014的近端部分2058,并且被定位在外壳2054内。导螺杆2056可在旋转方面相对于外壳2054固定,并且可被约束于外壳内的轴向滑动范围。可旋转的套筒2060可被同心地定位在外部外壳2054和内部导螺杆2056之间,并且可包括近侧调节器部分2062,其在外壳2054之外延伸,以提供给医生把手,以旋转可旋套筒2060。可旋套筒2060可相对于外壳2054自由旋转,但相对于外壳轴向固定。导螺杆2056可包括外部螺旋状开槽2064,该外部螺旋状开槽2064与可旋套筒2060上的向内突出的脊2066相互作用,因而在调节器2062相对于导螺杆2056和外壳2054旋转时,脊2066致使导螺杆2056轴向滑动,从而导致内鞘2014也轴向滑动。因此,医生可通过相对于外壳2054沿一个方向旋转调节器2062来向近侧移动内鞘2014,和通过沿相对于外壳相反方向旋转调节器来向远侧移动内鞘2014。外壳2054可相对于推轴2010固定,因而在调节器2062相对于外壳旋转时,导螺杆2056和内鞘2014一起相对于推轴2010和外壳2054轴向滑动。如图51所示,内轴2006穿过递送系统2000的手柄部分2002的全长,并且推轴2010可终止于手柄部分2002的近端帽2068或其附近。内轴2006外表面和推轴2010内表面之间的环形空间2012(参见图52和53)可流体连通地连接至手柄部分2002的末端帽2068中的至少一个冲洗端口2070。冲洗端口2070可提供入口以将流体注入环形空间2012和/或允许流体排出环形空间。如图49所示,鼻锥体2030可附接至内轴2006的远端。鼻锥体2030可从近侧基体2034至远侧顶点2032逐渐变细。基体2034的直径可约等于外鞘2036的直径。鼻锥体2030可被近侧收回——通过相对于递送系统2000的其余部分近侧滑动内轴2006,以倚靠外鞘2036和/或内鞘2014的远端进行配合,从而进一步包含压缩的假体瓣膜100,如图55所示。鼻锥体2030也可远离鞘向远侧移动,以为待负载和/或展开的假体瓣膜100提供空间。在穿过身体插入递送系统2000的过程中,逐渐变细的鼻锥体2030可充当楔形物以引导递送系统2000的插入部分2004进入身体,和提供防创伤末端以最小化在递送系统被推进穿过身体时对周围组织的创伤。为将假体瓣膜100负载到递送系统2000中,鼻锥体2030必须被远侧推进远离鞘,并且内鞘2014必须被远侧推进至递送位置,如图54所示(无固定带2022)。外鞘2036可被收回以暴露内鞘2014的槽2028。然后假体瓣膜100被定位在鼻锥体2030和内鞘2014之间和围绕内轴2006。然后假体瓣膜100被压缩至压缩状态和滑动到内鞘2014中,使得假体瓣膜的近端或下端邻近或接触推动端,如图56所示。可利用负载锥体或等同机构可将瓣膜100插入内鞘2014。在包括推动构件204的假体瓣膜100的实施方式中,如在图25中,推动构件204的底端206可接触推动端2018,如图56所示。可允许心室锚126通过各自的槽2028的圆形近端部分2020延伸出去,如图54所示。各槽的近端部分2020可具有允许心室锚126的两个端部分肩并肩位于槽内的充足角宽度,这可导致心室锚的中间部分具有期望的形状以植入瓣叶10、12后方。断裂固定带2022可被布置在内鞘2014的远端部分周围,使得带2022中的每个缺口2026位于各自的槽上,如图50所示。然后外鞘2036被远侧推进以覆盖槽2028,如图55所示,从而压缩心室锚126和将心室锚约束在外鞘2036内。可选地,假体瓣膜可在外鞘2036覆盖槽2028时被插入内鞘2014,使得心室锚126被定位在槽中,但无法延伸到槽外。心室锚126也可被约束在内鞘2014外表面和外鞘2036内表面之间。在任何情况下,一旦外鞘2036被收回,心室锚126就自由径向外弹。在假体瓣膜100处于内鞘2014内以后,可收回内轴2006,以牵引鼻锥体2030抵靠内鞘2014和/或外鞘2036的远端,如图55所示。在假体瓣膜100处于内轴2006内、鼻锥体2030被收回并且外鞘2036约束心室锚126的情况下,递送系统2000处于负载配置,并且准备好插入身体。在图55显示的负载配置中,负载后的递送系统2000——先是鼻锥体2030——可被通过心脏顶点38插入左心室6和定位在二尖瓣区域附近以展开。引导鞘(未显示)可在最初被插入穿过心脏切口,以提供将递送系统2000引入心脏的端口。另外,可经在递送系统2000之前被推进到心脏中的常规引导丝(未显示)来推进递送系统2000。然后可相对于递送系统其余部分近侧移动把手2052,以相对于内鞘2014收回外鞘2036并允许心室锚126远离内鞘2014外弹,如图56和57所示,使得心室延伸锚穿过槽2028的圆形近端部分2020。递送系统被期望地旋转定向,使得每个心室锚126定位在附接至天然二尖瓣瓣叶10、12其中一个的多组腱索16之间。接着,可向心房推进递送系统2000,使得鼻锥体2030进入天然二尖瓣口并且突出的心室锚126在各自的瓣叶10、12和心室壁20之间移动,如图58所示。然后,在保持递送系统2000的外壳2054稳定的同时,医生可相对于外壳旋转可旋套筒2060的调节器2062,以近侧收回内鞘2014。推动端2018在内鞘2014收回时保持固定,从而将压缩的假体瓣膜100留在与其从内鞘2014暴露和展开时相同的轴向位置。可选地,可使内鞘2014在推动端2060远侧移动时保持固定,从而将瓣膜100推到内鞘2014外。在相对于推动端2018收回内鞘2014时,推动端可对假体瓣膜100的近侧或最低表面产生远侧方向的轴向力。在具有推动构件204的假体瓣膜的实施方式中,推动构件204可将此轴向力直接指向主体122,防止推动端2018和心室锚126之间直接接触,以降低心室锚的损坏风险。在相对于假体瓣膜100收回内鞘2014时,首先暴露包括向下折叠的心房密封构件124的假体瓣膜的远侧部分或上部。参考图59和60,在内鞘2014已被收回越过假体瓣膜100的心房密封构件124的外轮缘时,心房密封构件可远离主体122径向外弹,围绕主体远端枢转。随着相对于假体瓣膜100收回内鞘2014,穿过槽2028的圆形近端部分2020的心室锚126端部穿过槽2028的较窄远侧部分被推向固定带2022,如图59和60所示。心室锚的端部最初肩并肩位于槽的较宽近端部分2020。当被推入槽2028的较窄部分时,每个心室锚126的两个端部可径向重叠或一个在另一个之上定向,而非肩并肩。在其它实施方式中,槽2028可较宽,使得心室锚126的两个端部可肩并肩相对于槽2028移动。在心室锚126移向槽2028的远端时,心室锚可接触固定带2022的缺口2026,如图60所示,并且可切割带2022或以其它方式使带在缺口位置撕裂或分开,如图61所示。当内鞘2014被收回越过假体瓣膜100的近端或下端时,假体瓣膜的压缩体可弹性地自扩张至扩张状态,如图61所示。在假体瓣膜扩张时,心室锚126和主体122外表面之间的间隙减少,在心室锚126和主体122之间捕获瓣叶10、12,如图23和62所示。假体瓣膜100的主体122的扩张可强制打开天然二尖瓣瓣叶10、12,保持天然二尖瓣2处于打开位置。然后假体瓣膜100可代替天然二尖瓣2的功能。在假体瓣膜100扩张后,可收回递送系统的内轴2006,将鼻锥体2030穿过假体瓣膜拉回,并且整个递送系统2000可被收回到体外。在一些实施方式中,递送系统2000可利用引导丝(未显示)被导入和/或导出身体。引导丝可被插入心脏并穿过天然二尖瓣口,然后可将引导丝近端穿过内轴2006的腔2008。然后可利用引导丝引导递送系统的路径,将递送系统2000穿过身体插入。心房方式可选地,假体瓣膜100可从左心房4递送至天然二尖瓣区域。参考图63–67,一种从二尖瓣区域心房侧递送假体瓣膜的方式利用递送导管2100。首先将假体瓣膜100从扩张状态压扁至径向压缩状态,并负载到递送导管2100的远端部分处第一鞘2102和任选地第二鞘中,如图63所示。利用递送导管2100引导假体瓣膜100穿过身体并进入左心房4。将假体瓣膜100在鞘2102内定向,使得假体瓣膜100的流出端112(支撑心室锚126的末端)最接近鞘远端,因此其先进入左心房4并且假体瓣膜的流入端110(心房密封构件124)最后进入。然后可以不同方式将鞘2102插入左心房4,一个实例是图66显示的经心房方式,另一实例是图67显示的经横膈膜方式。当利用递送导管2100经由患者血管系统进入心脏时,如图67所示,导管2100可包括柔性、可操纵导管。一旦处于左心房4中,可使第一鞘2102的远端2104移动越过二尖瓣环8,使得心室锚126被定位越过二尖瓣瓣叶10、12,然后从鞘展开心室锚。然后可利用定位在鞘2102内并且可相对于鞘轴向滑动的刚性推轴2106(参见图64),将假体瓣膜100部分地排出第一鞘2102的远端2104。当相对于推轴2106和假体瓣膜100近侧收回鞘2102时,推轴2106将假体瓣膜远侧推出鞘2102外,如图64所示。可选地,可使推轴2106向远侧移动,同时鞘2102保持原位,从而将假体瓣膜100远侧推出鞘外。当第一鞘2102被插入越过二尖瓣环8并越过瓣叶10、12下端时,可将假体瓣膜100部分地排出以释放心室锚126、如图64所示。释放的心室锚126在其从鞘2102释放时可外弹。任选地,然后可将鞘2102经主体122的暴露部分反向滑动,从而只显示心室锚,如图65所示。为完成此步骤,框架的心房端可包括诸如下列的特征(未显示):机械锁特征,用于将假体瓣膜100可释放地附接至推轴2106,使得推轴可将假体瓣膜拉回鞘2102中。然后将鞘2102和假体瓣膜100向心房、向近侧收回,使得向外突出的心室锚126在各自的瓣叶10、12和心室壁20之间移动,如图66–68所示。在其它实施方式中,如图44和45所示那些,在心室锚从鞘2102释放时,心室锚可弹性地向上偏转或围绕各自的瓣叶10、12弯曲。任选地,递送导管2100还可包括处于外鞘2102内的第二鞘(未显示),并且可包含推轴2106、心房密封构件124和框架主体122,但不包含锚126。在图63显示的位置时,第二鞘的远端可定位在锚126和主体122之间。在收回外部第一鞘2102时,如图64,第二鞘可保持在压缩框架主体122的位置,而锚126被释放以向外延伸。由于第二鞘保持覆盖和压缩主体122,无需用第一鞘2102再覆盖主体,如图65。取而代之,通过将第二鞘和推轴一齐近侧移动,来近侧移动假体瓣膜100。然后,为将假体瓣膜100从第二鞘排出,相对于推轴2106近侧收回第二鞘。在心室锚126定位在瓣叶10、12后方并且假体瓣膜100的其余部分从第一鞘2102排出后,假体瓣膜100可扩张至其功能尺寸,如图62和69所示,从而在心室锚126和主体122之间捕获瓣叶10、12。一旦假体瓣膜100被植入,就可将递送导管2100收回体外。在可选的假体瓣膜实施方式中,框架的主体和心房密封构件可以是可塑性扩张的,并且可在假体瓣膜定位在期望的位置时通过球囊导管(未显示)的球囊扩张。这种实施方式中的心室锚可呈现期望量的弹性,以协助在展开过程中在心室锚和主体之间定位瓣叶10、12。一旦假体瓣膜完全扩张,就可穿过扩张假体瓣膜收回球囊并收回体外。二尖瓣反流减少二尖瓣反流(MR)在天然二尖瓣无法适当闭合并且血液在心脏收缩的收缩期期间从左心室流入左心房时发生。MR是心脏瓣膜疾病的最常见形式。MR具有不同病因,如瓣叶脱出,乳头肌功能失调和/或左心室舒张导致的二尖瓣环拉伸。瓣叶中心部分的MR可被称为中心流MR(centraljetMR),并且较接近瓣叶一个接合处的MR可be被称为偏心流MR(eccentricjetMR)。不同于完全置换天然二尖瓣,另一治疗MR的方式是在瓣叶之间布置假体间隔物,该假体间隔物减少反流口区域,使二尖瓣在极少或无反流的情况下工作,同时最小化对天然瓣膜和左心室功能和周围组织的影响。关于MR治疗另外的信息可参考美国专利号7,704,277和美国公开号2006/0241745A1,其均被引入本文作为参考。图71显示示例性假体间隔物实施方式3000,其中间隔物或其它物体可利用本文描述的锚定思想悬浮或“漂浮”在瓣叶之间。假体间隔物3000可包括框架3002和间隔物体3004。间隔物体3004可包括聚氨酯、泡沫和/或其它适当的材料(一种或多种),并且可任选地被特氟隆和/或其它适当的材料(一种或多种)涂覆。间隔物体3004可包括共形于前叶10和后叶12之间的新月形接合处的新月形状(参见图4A和4B),或间隔物体可包括其它适当的形状,如椭圆、圆、沙漏等。根据间隔物体3004的形状和间隔物体相对于天然结构的定位,假体间隔物3000的实施方式可有助于治疗中心流MR、偏心流MR或两者。此外,间隔物体3004可包括最小横向横截面面积和坡形边缘。这种形状可减少来自从左心房经过二尖瓣流至左心室的血液的舒张力。这种形状还可在天然瓣膜围绕间隔物体闭合并且自然而然将较大部分收缩力施加于天然瓣叶和腱索时减少对间隔物体3004的收缩力。间隔物体3004的形状可因此减少在锚啮合位置处传递至天然瓣膜组织的力,这可降低啮合位置处穿孔和磨蚀和支撑瓣叶的天然腱索断裂的可能性。假体间隔物3000的总体最小尺寸可进一步提供减少递送系统所需横截面尺寸、允许经由较窄血管系统递送和/或身体和心脏较小侵入性切口的可能。框架3002可由坚固的柔性材料如镍钛诺制成。如图71所示,框架3002可包括框架体3006、前心室锚300、后心室锚3010、前心房锚3012和后心房锚3014。框架体3006可包括延伸穿过间隔物体3004的总体上纵向的列。框架体3006的不同实施方式在下文详细描述。框架3002可进一步包括从框架体3006穿过间隔物体3004横向延伸的一个或多个间隔物扩张器3024。扩张器3024可远离框架体弹性地扩张并且在展开过程中协助间隔物体3004扩张。在一些实施方式中,间隔物扩张器3024可以是圆柱形框架体3006的矩形裁切部分——如图71所示,远离框架体径向弯曲。前心室锚3008被配置以从框架体3006的心室端围绕前叶10的A2边缘延伸,并且在瓣叶后方向上延伸至二尖瓣环8的心室面上的一定位置处和/或前瓣叶的环连接部分,而前心房锚3012被配置以从框架体3006的心房端径向延伸至二尖瓣环8心房面上与前心室锚3008对立的位置处。类似地,后心室锚3010被配置以从框架体3006的心室端围绕后叶12的P2边缘延伸,并在瓣叶后方向上延伸至二尖瓣环8心室面上的一定位置处和/或后叶的环连接部分,而后心房锚3014被配置以从框架体3006的心房端径向延伸至二尖瓣环8的心房面上与后心室锚3010对立的位置处。心室锚3008、3010和心房锚3012、3014可分别包括宽啮合部分3016、3018、3020和3022,其可被配置以压缩二尖瓣环8和/或瓣叶10、12的环连接部分,以固定假体间隔物3000,防止沿心房和心室方向移动。宽啮合部分可提供锚和天然组织之间较大的接触面积,以分散负荷和降低损坏天然组织(如啮合位置的穿孔或磨蚀)的可能。示例构型的心室锚3008、3010围绕天然瓣叶10、12成圈,并且不将天然瓣叶压抵间隔物体3004的外表面,允许天然瓣叶围绕间隔物体3004自然打开和闭合。如图74所示,二尖瓣环8总体上是肾形,使得前后尺寸被称为环的副尺寸(minorsize)。由于假体间隔物3000可锚定在天然二尖瓣2的前和后区域,假体间隔物可根据环8的副尺寸被设定尺寸。二尖瓣环8的副尺寸的Echo和CT测量是设定假体间隔物3000尺寸的示例性方法。图75–79示例递送假体间隔物3000至心脏天然二尖瓣区域的示例性方法。可利用包括外鞘3030和内扭矩轴3032的递送系统将假体间隔物3000递送到心脏中。假体间隔物3000被压缩和负载到外鞘3030的远端,其中先负载心房锚3012、3014。如图75所示,心房锚弹性地近侧延伸,并且心室锚3008、3010弹性地远侧延伸,使得假体间隔物3000呈现充分窄的横截面面积,以配合在外鞘3030的腔内。在外鞘3030内,假体间隔物3000被定位使得框架体3006的心房邻接扭矩轴3032的远端,心房锚3012、3014处于扭矩轴和外轴内壁之间,压缩的间隔物3004邻接外鞘的内壁,并且心室锚3008、3010的远端邻近外鞘的远侧开口。扭矩轴3032可以以可释放地方式偶联至假体间隔物3000的心房端,如在框架体3006的近端。在进行负载后,递送系统可被引入左心房4——如经由心房中隔30,并且外鞘3030的远端可穿过天然二尖瓣2并进入左心室6,如图75所示。接着,可相对于扭矩轴3032收回外鞘3030,以从外鞘的远侧开口排出心室锚3008、3010。此时,可旋转扭矩轴3032,以按需旋转外鞘3030内的假体间隔物3000(或任选地,可同时旋转扭矩轴和外鞘),从而使心室锚对准天然瓣膜2的A2/P2方位。扭矩轴3032和假体间隔物3000之间的可释放附接可足以将扭矩从扭矩轴传递至假体,以按需旋转假体。心室锚3008、3010可预先成形,从而在其被逐渐排出外鞘3030时其开始彼此分开并围绕瓣叶的A2/P2区域压扁。这种卷曲动作可以是可取的,从而避免与心室壁缠结。在外鞘3030被收回至框架体3006的心室端时,如图76所示,心室锚3008、3010被完全排出外鞘并定位在瓣叶后方。然后整个递送系统和假体可被近侧移动,直到心室锚的啮合部分3016、3018邻接二尖瓣环8的心室侧和/或瓣叶10、12的环连接部分。接着,可相对于扭矩轴3032进一步收回外鞘3030,使得外鞘远端与框架体3006的心房端分开,如图77所示,这使得压缩的间隔物扩张器3024和压缩的间隔物体或其它体3004弹性地径向向外自扩张至完全扩张的功能状态。注意,间隔物体3004主要沿垂直于环副尺寸或朝向接合处36的方向扩张(参见图74)。在一些实施方式中,可使间隔物体3004从压缩状态去折叠或去卷曲至扩张状态,并且在一些实施方式中,可使间隔物体膨胀,如利用盐水或随时间硬化的环氧树脂。在间隔物体在瓣膜内扩张后,如图77所示,可进行间隔物的血液动力学评价,以评估假体间隔物3000在减少MR中的效率。根据评价结果,展开可继续进行,或假体间隔物3000可被再覆盖、收回和/或再定位以进行展开。从图77所示位置开始,外鞘3030可在间隔物体3004上被反向推进(通过相对于扭矩轴3032推进外鞘3030),致使间隔物体再压缩,如图76所示。在一些实施方式中,心室锚部是可再覆盖的,但在一些实施方式中心室锚可充分柔韧,从而被再拉直和再覆盖,在这种情况下,于是整个递送过程可逆转和重新开始。从图76所示位置开始,递送系统可被再定位,并且间隔物体3004可被再展开和再评估。在心室锚3008、3010和间隔物体3004被可接受地展开后,可进一步相对于假体间隔物3000和扭矩轴3032收回外鞘3030,以从外鞘排出心房锚3012、3014,如图78所示。在完全排出后,心房锚弹性地卷曲至图78显示的其最终展开位置,并且其啮合部分3020、3022压抵环8的心房侧和/或分别与心室锚的啮合部分3016、3018对立的、瓣叶10、12的环连接部分,从而在A2和P2区域压缩环和/或瓣叶的环连接部分,以将假体间隔物3000固定在天然二尖瓣区域2内。在心房锚3012、3014展开后,可从框架体3006的心房端释放扭矩轴3032。然后可收回递送系统至体外,留下植入的假体间隔物3000,如图79所示。在一些实施方式中,间隔物体3004可包括瓣膜结构3040,如图80和82所示的实施方式。瓣膜结构3040可结合天然二尖瓣2工作,调控左心房4和左心室6之间的血流。例如,瓣膜结构3040可定位在天然瓣叶之间,使得天然瓣叶包围在瓣膜结构外侧,使得一些血液穿过瓣膜结构流动,而其余血液在瓣膜结构外侧和天然瓣叶之间流动。瓣膜结构3040可包括三瓣叶构型,如本文参考瓣膜结构104所述和图5–7显示。在一些实施方式中,框架体3006可包括圆筒,其可任选地包括实体壁管(如在图71–74中)、网状丝栅格状3046(如在图82中)或其它圆柱形构型。参考图71–75,框架体3006和任选地锚中的一个或多个可由实体壁管如镍钛诺形成,其中心房锚由一部分管形成——如通过激光切割,并且心室锚由第二部分管形成,框架体由第一和第二部分之间的管部分形成。然后可使锚形成期望的植入构型,如通过热处理。在这种实施方式中,锚和框架体可以是一体式或整体式结构。在其它实施方式中,框架体3006可包括弹簧状螺旋螺旋的丝柱3050,如图83所示。这种螺旋柱3050可由具有圆形或矩形横截面的丝制成,并且可包括弹性柔性材料,如镍钛诺,提供横向柔度以共形于天然瓣膜结构,同时保持纵向柱刚度以递送。在其中一些这些实施方式中,框架体3006可包括四角形螺旋状线圈,其具有四个丝,该四个丝具有延伸形成心房锚3012、3014的四个心房端和延伸形成四个心室锚3008、3010的四个心室端。在其它实施方式中,框架体3006可包括多个纵向构件(未显示)。在一个这样的实例中,框架体3006可包括四个纵向构件:延伸形成前锚3012、3014的两个纵向构件和延伸形成后锚3008、3010的两个纵向构件。在其它实施方式中,框架体3006可包括沿框架体纵向方向的Z字型切割图案3050,如图81所示,该图案也可提供横向柔度,同时保持柱强度。在一些实施方式中,假体间隔物3000可具有另外的锚。在一些实施方式中(未显示),假体间隔物3000可具有三对锚:围绕后叶12的一对锚,如上述后锚3010和3014,和天然瓣叶10、12之间的每个接合处36的一对锚。这些接合处锚对可类似地包括心室锚和心房锚,并且可类似地压缩天然环8。在其它实施方式中,前锚3008和3012也可被包括,作为第四对锚。其它实施方式可包括这四对锚和/或另外的锚的其它组合。除填充反流口区域和阻止血液流向左心房外,假体间隔物3000还可张拉腱索,以防止左心室进一步扩大和防止二尖瓣环进一步舒张。锚定在二尖瓣接合处下方包括心室锚的假体装置一些实施方式(包括假体瓣膜和假体间隔物的)可被配置使得心室锚锚定在天然二尖瓣2的接合处36下方,而代替或补充锚定在天然二尖瓣瓣叶10、12的A2/P2区域后方。图84–87显示包括锚定在天然二尖瓣2的两个接合处36下方的心室锚的示例性假体装置实施方式和相关递送方法。这些接合处锚定思想主要用于假体瓣膜,但可以用于其它假体装置,包括假体间隔物。如图3、4和88所示,接合处36是天然二尖瓣2中前叶10和后叶12接合的区域。天然二尖瓣环8中邻近各接合处36的部分39,如图88所示,可相对于二尖瓣环8中邻近瓣叶A2/P2的中间部分部分更厚和/或更坚固,提供刚醒、稳定的位置来锚定假体装置。这些环区域39可包括可比天然瓣叶组织承载更大负荷的坚韧纤维组织,并且可形成天然凹面或腔。图84和85显示通过心室锚4002定位在其中一个腔39处而植入天然二尖瓣区域2的示例性假体装置4000。假体装置4000可以是具有瓣叶结构的假体瓣膜或具有用于减少MR的间隔物体3004的间隔物装置。腱索16附接至瓣叶10、12,邻近接合处36,该接合处36可能是心室锚在腔39中腱索后方定位的障碍。然而,可以绕过腱索16递送锚,如锚4002,以到达腔39。在这些天然腔39中腱索16后方定位心室锚的啮合部分,如啮合部分4004,对于将假体装置固定在天然二尖瓣区域2可以是可取的。然而,为避免缠结和/或损坏至天然腱索16,可期望先将锚啮合部分垂直地引导至瓣叶10、12后方A2/P2区域处后中乳头肌22的腱索16和前外乳头肌24的腱索16之间,如图84所示,然后移动或旋转锚啮合部分水平地围绕腱索16后方,朝向接合处腔39,如图85所示。在一些这种方法中,先将心室锚展开在瓣叶的A2/P2区域后方,然后旋转或扭转整个假体装置,以使锚啮合部分水平地移向腔39,如图84和85所示。例如,在前叶10后方展开的第一锚可移向其中一个腔39,而在后叶12后方展开的第二锚可移向另一个腔39。这种方法也可被称为“螺杆法”,因为整个假体被旋转以啮合锚与天然组织。如图84和85所示,包括弯曲的、曲线形的、钩状的或总体上“L”形的锚4002的假体装置4000可用于螺杆法。“L”形锚4002可包括从装置4000主体垂直向上延伸的腿部分4006、膝部分4008和从膝部分水平延伸并且终止于啮合部分4004的足部分4010。在这些实施方式中的一些中,“L”形锚4002可包括成圈的丝,其附接至装置4000主体两个位置处,使得丝形成一对腿部分4006、一对膝部分4008和一对足部分4010。在其它实施方式中,锚4002可具有其它类似的形状,如更具弧度的形状,而非图84显示的直角形状。在递送到心脏的过程中,足部分4010可围绕装置4000的主体外表面卷曲或缠绕。如图84所示,为将足部分4010在不缠结腱索的情况下垂直地移动至瓣叶10后方,腿部分4006可被定位略微偏离A2区域中心,较接近与期望递送腔39对立的腱索。如图84所示,腿部分4006被靠右定位,使得足部分4010可经过腱索16之间。在足部分4010清理腱索16并定位在瓣叶后方后,可旋转装置4000,以使啮合部分4004水平地移动到腔39中,如图85所示。注意,在图85中,腿部分4006可终止于定位A2/P2区域处、腱索16之间,以避免干扰腱索。虽然图84和85显示了单个锚4002,但可以对称方式在天然瓣膜2的对立侧递送前锚和后锚,每个腔39锚定一个。两个锚4002的足4010可指向相反的方向,从而图85显示的扭转动作可将其同时移动至两个腔39。在两个锚实施方式的递送过程中,两个足部分4010可缠绕装置4000的主体外表面,使得两个足部分4010彼此重叠。在类似的实施方式中,锚4002可包括桨形(例如参见图37),其具有沿相反方向延伸的两个足部分4010。虽然更难在腱索之间移动,但这些桨形锚可使装置4000以任一方向旋转,从而在腔39处啮合其中一个足部分4010。在一些实施方式中,桨形锚可足够宽,使得一个足部分4010可被定位在一个腔39处,而另一者足部分被定位在另一个腔处。由于锚4002各自附接至装置4000主体的两个位置处,锚可在主体被压缩时远离装置主体伸展,形成间隙,从而接收瓣叶,如上文参考图11–22详细描述。在一些实施方式中,锚可在主体被压缩时与主体分离,并且要么保持与主体分离,使得瓣叶不被挤压或压缩在锚和装置主体之间,要么在扩张过程中紧靠主体,以啮合瓣叶。在一些实施方式中,在主体然后扩张时,主体可移向锚,以减少间隙,同时对立锚的足部分4010之间的距离。图86和87显示通过心室锚5002定位在腔39而植入天然二尖瓣区域2的另一示例性假体装置5000和如此进行的相应方法。在此实施方式中,装置5000可包括每侧一对“L”形锚5002(图86和87中仅一对可见),其中每对包括用于定位在其中一个腔39中的一个锚和用于定位在另一个腔中的另一个锚。每个锚可包括从装置5000主体垂直延伸至膝部分5008的腿部分5006和从膝部分5008水平延伸至啮合部分5004的足部分5010。在其它实施方式中,锚5002可具有其它类似的形状,如更具弧度的形状,而非图86显示的成角形状。每对锚5002可包括弹性地柔性材料,如镍钛诺,使得其可预先挠曲和约束在扳起位置,以递送到瓣叶后方,如图86所示,和然后被释放,以弹性地弹开,以使啮合部分5004沿相反方向朝向两个腔39移动,如图87所示。可采用任何适当的约束和释放机构,如可释放的机械锁机构。在释放后,一个前锚和一个后锚可从相反方向被定位在一个腔39,并且第二前锚和第二后锚可从相反方向被定位在另一个腔。一些实施方式可包括装置5000每侧仅一个锚,该锚在被释放时沿相反方向朝向对立的腔39移动。由于每对锚5002最初被约束在一起,如图86所示,每对锚可如同具有两个与装置5000主体附接的附接点的单个锚工作。因此,在主体被压缩时,锚对可与主体分离或扩张远离主体,并且要么保持与主体分隔,使得瓣叶不被挤压或压缩在锚和装置主体之间,要么在扩张过程中紧靠主体,以啮合瓣叶。在一些实施方式中,在主体然后扩张时,主体可移向锚对,以减少间隙,同时保持对立锚对的足部分5010之间的距离。在图84–87所示的实施方式中,假体装置4000或5000可具有类似于图5所示实施方式的主框架体——心室锚4002、5002可从其延伸,并且可进一步包括一个或多个心房锚,如例如,类似于图5所示心房密封构件124的心房密封构件或类似于图71所示心房锚3012和3014的多个心房锚。心房锚可从假体装置心房端径向向外延伸,并接触与腔39对立的天然组织,从而压缩心房锚和心室锚4002、5002的啮合部分4004、5004之间的组织,以将假体装置固定在天然二尖瓣区域。心房锚和心室锚可包括宽接触区域,从而将负荷分布在较宽区域上和降低损坏天然组织的可能。假体二尖瓣的心房部分本文公开的假体装置的一些实施方式包括从主体心房端径向向外延伸的心房部分,而其它实施方式则不包括。如上所述,从假体二尖瓣主体心房端径向延伸的心房部分可提供若干优点。心房部分可与天然组织在二尖瓣环心房侧上生成全环形接触区域或密封,从而防止或减少假体瓣膜外侧和天然瓣膜组织之间的血流。这可有助于减少瓣周漏。心房部分还可作用以固定假体瓣膜,防止向左心室迁移。心房部分还可促进组织向内生长,这可进一步减少瓣周漏和增强假体瓣膜止动。在一些实施方式中,心房部分可与主体一体形成,并且可以是径向可折叠的和可扩张的,以利于递送。心房部分的形状可被选择以适应患者的解剖结构。心房部分(如同主体)可被至少一个生物相容性层覆盖,以阻止血液流动,进一步促进组织向内生长,和/或进一步适应患者的解剖结构。心房部分的构型可取决于若干因素,包括患者二尖瓣区域的结构和患者的医学状况(一种或多种)。下文描述几种可选的构型,其中每一种在一个或多个方面有不同。例如,从上观察的心房部分的构型(即,沿穿过主体中心延伸的纵向中心轴线),在本文中被称为“径向构型”,可在实施方式与实施方式之间不同。此外,从侧面观察的心房部分的构型(即,沿垂直于纵轴的轴线),在本文中被称为“轴向构型”,可实施方式与实施方式之间不同。心房部分的另外的特征也可在实施方式与实施方式之间不同,这取决于多种因素。这些另外的特征可非限制地包括,心房部分连接至主体的方式、连接心房部分的主体位置、用于覆盖心房部分的织物类型、径向构型对称(或不对称)、具有盘旋或螺旋构型臂的包括和制造心房部分的方法(一种或多种)。除了这种组合在结构上不可能的情况,本文公开的可选径向构型中的任一种均可与本文公开的可选轴向构型中的任一种组合应用,和进一步与本文描述的另外的变型中的任一种组合应用。心房部分的径向构型可影响心房部分的若干性质,如心房部分的径向刚度、轴向刚度、周向刚度和/或周向相关度。径向刚度是心房部分在径向方向的刚度。在一些情况下,径向刚度可被更具体地限定为心房部分外周上的一点响应施加于心房部分上该点的径向力所经过的径向距离。轴向刚度是心房部分在轴向方向的刚度。在一些情况下,轴向刚度可被更具体地限定为心房部分外周上一点响应施加于心房部分上该点的轴向力相对于主体所经过的轴向距离。周向刚度是心房部分在周向方向的刚度。在一些情况下,周向刚度可被更具体地限定为心房部分外周上一点响应施加于心房部分上该点的周向力(即,沿垂直于径向力和轴向力的方向施加的力)围绕主体中心纵轴所经过的角距离。心房部分的周向相关度是心房部分外周上一点的移位受心房部分外周上相邻点移位影响的程度。心房部分的其它性质还可根据心房部分的径向构型而改变。例如,径向构型可影响心房部分对天然组织造成创伤的倾向。而且,径向构型可影响心房部分、其部件、及其与主体的连接的疲劳故障抗性,特别是由于跳动的心脏的循环力导致的疲劳故障。进一步,径向构型可影响心房部分相对于主体弯曲或挠曲的能力,如在制造过程中从轴向地延伸构型到径向延伸构型或在展开过程中在压扁构型和展开构型之间。此外,心房部分的径向构型可影响整个假体瓣膜的性能,如关于防止瓣周漏、锚定假体瓣膜和促进组织向内生长。另外,心房部分的径向构型可影响多种其它性质,包括下文关于轴向构型描述的那些中的一些。下文关于心房部分的几个可选实施方式描述各种不同径向构型的性质。心房部分的轴向构型可类似地影响心房部分的若干性质,包括上文关于径向构型描述的那些中的一些。例如,假体瓣膜在天然二尖瓣处的引入可对天然组织造成创伤,具体地在锚定假体瓣膜的位置处。心房部分的轴向构型可影响这种创伤的程度和/或类型。进一步,轴向构型可影响天然组织和心房部分之间接触的总表面积,从而影响组织向内生长。另外,轴向构型还可影响心房部分对天然组织施加的力,从而影响密封的松紧度。此外,轴向构型还可影响假体瓣膜共形于天然二尖瓣解剖结构和相邻结构的程度。图100A–100F示意性示例不同的示例性轴向构型,其中每一个均显示半个主体7018和不同心房部分以及主体纵轴7016的剖视图。如图100A所示,心房部分7000可近似垂直于轴线7016、远离主体7018的心房端径向延伸。如图100B所示,心房部分7002可远离主体7018的心房端径向且心室向延伸,使得心房部分7002与主体7018的侧面形成锐角。在相关轴向构型中,心房部分可以任何期望的角度Θ或角度范围Θ(其中角度Θ在心房部分和主体侧面之间测量)远离主体延伸。例如,心房部分可以任何适当的锐角、任何适当的钝角或距主体侧面总体上0°至180°范围的任何角度远离主体延伸。如图100C所示,心房部分7004可总体上径向远离主体7018延伸至径向周边,从径向周边向心室卷曲,然后朝向主体延伸回来。如图100D所示,心房部分7006可从主体7018径向延伸,到达径向周边的一点,然后从径向周边朝向主体延伸回来。如图100E和100F所示,心房部分7008可包括框架,该框架不被直接紧固至主体7018。在具有这种构型的心房部分的实施方式中,心房部分可通过织物偶联至主体7018。如图100E所示,心房部分7008可相对于主体7018径向向外延伸。如图100F所示,心房部分7010可包括围绕主体7018的单个构件。其它轴向构型是可以的,尽管未示例在图100A–100F中。例如,在一些实施方式中,心房部分远离主体7018延伸,并且在径向周边附近向心房卷曲。具有不直接连接至主体7018的框架的轴向构型可呈现轴向刚度小于其它轴向构型,因为可对于心房部分相对于主体7018轴向移动可存在较少阻力。图100A、100C和100D示例的轴向构型可减少预期组织创伤,提供与天然组织接触的较大表面积,和/或更自然地适配二尖瓣解剖结构,但可相对于例如图100B示例的轴向构型提供与天然组织更松散和/或更不连续的接触。在一些实施方式中,还通过改变心房部分与主体7018的连接点位置来改动轴向构型。虽然图100A–100D示例了处于主体7018的心房端的连接点,但连接点无需处于末端,并且在一些实施方式中主体7018的心室端方向轴向地移位。这种构型示例在图100F中,其显示心房体轴向地移位至主体7018心房端下方的位置。图101A–140显示不同轴向和/或径向构型的心房部分的几个示例性实施方式。虽然心房部分的实施方式的其中几个与假体二尖瓣组合显示,但心房部分的不同实施方式均可与待植入天然二尖瓣区域的不同其它装置组合应用。虽然心房部分的实施方式的其中几个与具体数量的不同部件(例如,径向延伸臂)一起显示,但每个示例实施方式提供的不同部件的数量可在可选的实施方式中不同。图101A–101B显示示例性心房部分7020,其具有这样的径向构型:包括十二个臂7022,每个臂在起始端7024连接至主体7032,径向向外延伸,并且在末端7026连接至各自的圈环7028。织物覆盖物7030连接至臂7022、圈环7028和主体7032,并且跨越这些部件之间的间隙。心房部分7020具有类似于图100A示例的轴向构型:臂近似垂直于轴线7016远离主体7018径向延伸。每个臂7022独立于各相邻臂7022,即每个臂7022可相互独立地挠曲或弯曲。由此,具有独立臂的这种径向构型和其它径向构型呈现低周向相关度。连接至每个臂7022的末端7026的圈环7028有助于减少至患者组织由于心房部分7000和天然组织之间的接触而经受的创伤。图102A–102B显示示例性心房部分7040,其具有这样的径向构型:也包括十二个臂7042,每个臂在起始端7044连接至主体7052并径向向外延伸。心房部分7040具有这样的轴向构型:其中每个臂7042的末端7046远离主体7052沿轴向方向向心房弯曲。每个臂的末端7046可连接至马蹄形构件7048。每个臂7042的末端7046连接至马蹄形构件7048,使得马蹄形构件7048的末端径向向内指向主体7052。马蹄形构件7048的每个末端可以有小圈环7050,该小圈环7050具有贯穿其中形成的孔。图103A–103B显示示例性心房部分7060,其具有这样的径向构型:也包括十二个臂,每个臂在起始端7064连接至主体7074并径向向外延伸。其中四个臂7062A其末端7066连接至圈环7068,圈环7068的形状包括六个内向突起;其中四个臂7062B其末端7066连接至圈环7070,圈环7070的形状包括四个内向凸起;和其中四个臂7062C其末端7066连接至盘旋部分7072。心房部分7060具有这样的轴向构型:其中一些臂7062A、7062B、7062C同时径向和心室向延伸远离主体7074的心房端,因此其与主体7074的侧面形成锐角;并且其中其它臂7062A、7062B、7062C同时径向和心房向延伸远离主体7074的心房端,因此其与主体7074的侧面形成钝角。在可选的实施方式中,心房部分可类似于心房部分7060,但其十二个臂在其末端连接至形状包括六个内向突起的圈环。在另一可选的实施方式中,心房部分可类似于心房部分7060,但其十二个臂在其末端连接至形状包括四个内向突起的圈环。在再一可选的实施方式中,心房部分可类似于心房部分7060,但其十二个臂在其末端连接至盘旋部分。这些可选的实施方式可基于圈环或盘旋部分对心房部分性质的影响(包括其对天然组织造成创伤的倾向)被选择。图104显示示例性心房部分7080,其具有这样的径向构型:也包括十二个臂7082,每个臂在起始端7084连接至主体7090并径向向外延伸。每个臂7082在末端7086分叉,形成两个径向向外延伸的延伸部7088。心房部分7080具有这样的轴向构型:其中每个臂7082的起始端7084连接至主体7090——在从其心房端移位的点处(如图125B所示)。臂7082先向心房延伸远离其起始端7084,并径向卷起,因此其从主体7090径向向外延伸(如图102B所示)。延伸部7088向心房卷曲,因此心房部分7080的周边同时径向和心房向延伸远离主体7090的心房端(也如图102B所示)。心房部分7080的构件可以是曲线形的,以配合患者天然二尖瓣区域的解剖结构。图105显示示例性心房部分7100,其具有包括二十四个臂7102的径向构型。二十四个臂7102排列形成十二对臂,每对形成连续圈环——在每个臂对的起始端7104处附接至主体7108,延伸远离主体7108,并且再次连接在从主体7108径向移位的连接位置7106处。由于每个臂7102相互连接,这种径向构型提供的刚度大于其它径向构型。心房部分7100具有类似于图100A示例的轴向构型。图106显示示例性心房部分7120,其具有这样的径向构型:包括十二个臂7122,每个臂在起始端7124连接至主体7132,径向向外延伸,并在末端7126连接至圈环7128。这种径向构型与之前的径向构型的不同之处在于臂7122,其除径向延伸远离主体7132外,还成角地延伸远离其起始端7124,使得臂7122形成螺旋形图案。心房部分7120,如同其它具有独立臂的心房部分,呈现低周向相关度。然而,不同于其它构型中的多种,这种构型由于臂7122的螺旋构型而呈现低径向刚度。当其中一个臂7122承受径向力时,其可相对容易沿径向方向挠曲,因为其主要进行弯曲,而非压缩或拉伸。心房部分7120还包括在臂7122中点附近的七个连接点7130,其可用于促进织物覆盖物(未显示)与臂7122的附接。心房部分7020具有类似于图100A示例的轴向构型。图107显示示例性心房部分7140,其具有这样的径向构型:包括十二个臂7142,每个臂在起始端7144连接至主体7148并径向向外延伸。心房部分7140类似于心房部分7120,但臂7142不在其末端7146连接至圈环,并且臂7142不与主体7148一体形成,而是取而代之在起始端7144被机械地紧固至主体7148。因此,心房部分7140经历疲劳故障的可能小于其它类似的心房部分。心房部分7140具有类似于图100A示例的轴向构型。图108显示示例性心房部分7160,其具有这样的径向构型:包括十二个臂7162,每个臂在起始端7164连接至主体7172,径向向外延伸,并且在其末端7166连接至马蹄形构件7168,马蹄形构件7168的末端反向指向主体7172,类似于图102A–102B所示的实施方式。织物7170连接至臂7162、马蹄形构件7168和主体7172,并且跨越这些部件之间的间隙。这种径向构型与之前的构型的不同之处在于臂7162以盘旋形状形成,而非材料直线段。如图109A–109E示例,臂7162的盘旋形状可包括多个通过多个曲线形区段或弯曲部相互连接的基本上直线形平行区段(如图109A、109B和109E)、基本上曲线形部分(如图109C)和/或较靠近主体7172的较直线部分和较靠近臂7162末端7166的较曲线部分(如图109D)。如图109E示例,在一些实施方式中,盘旋形状可在较靠近主体7172时较厚和在较靠近臂7162的末端7166时较薄。臂7162包括盘旋形状可减少其刚度,并且可降低其由于疲劳而故障的可能。心房部分7160具有类似于图100A示例的轴向构型。盘旋臂的一个重要特征是其厚度:通过增加其厚度,减少其柔性,和同时减少其厚度,增加其柔性。图110A–110B显示示例性心房部分7180,其具有这样的径向构型:包括十二个臂7182,每个臂在起始端7184连接至主体7188并径向向外延伸。心房部分7180类似于心房部分7160,除了臂7182在无另外的构件附接至其末端7186的情况下形成。心房部分7180具有类似于图100B示例的轴向构型:臂7182向心室弯曲,远离主体7188径向移动,使得其相对于主体7188的侧面以锐角延伸。因此,心房部分7180提供较小与天然组织接触的表面积,但在植入时可比一些其它心房部分提供更紧密的密封。图111显示示例性心房部分7200,其具有类似于心房部分7160和7180的径向构型,除了臂7202在其末端7206连接至圈环7208。除心房部分7160、7180和7200外,本文描述的其它心房部分实施方式中的多个也可被改造包括具有盘旋形状的臂构件,并且在多种情况下这样做可减少改造构件(一种或多种)的刚度和/或疲劳故障可能。心房部分7200具有类似于图100A示例的轴向构型。图112显示示例性心房部分7220,其具有这样的径向构型:包括十一个臂7222,每个臂在起始端7224连接至主体7228并径向向外延伸。十一个臂7222被配置使得两个相邻臂7222之间存在的空间对于其它相邻臂7222之间的空间,其优点在下文关于图126–130描述。心房部分7220与之前的构型的不同之处在于臂7222以线圈状或螺旋状构型形成,而非材料直线段。如同心房部分7160、7180和7200中采用的盘旋形状,臂7222的构型中包括线圈形状可减少其刚度和/或疲劳故障可能。心房部分7220具有类似于图100B示例的轴向构型:臂7222向心室弯曲,径向向外延伸,使得其相对于主体7228的侧面以锐角延伸。因此,心房部分7220可提供较少与天然组织接触的表面积,但在植入时比一些其它心房部分提供更紧密的密封。织物7226连接至臂7222和主体7228,并跨越这些部件之间的间隙。图113显示示例性心房部分7240,其具有类似于心房部分7220的径向构型,除了其包括螺旋臂7242,该螺旋臂7242成角以及径向远离其处于主体7246的起始端7244延伸,使得臂7242形成螺旋形图案,如心房部分7120。如同心房部分7220和7240,本文描述的其它心房部分实施方式中的多个可被改造以包括具有螺旋构型的构件,并且在多种情况下这样做可减少改造构件(一种或多种)的刚度和/或疲劳故障可能。心房部分7240具有类似于图100A示例的轴向构型。图114显示示例性心房部分7260,其具有这样的径向构型:包括远离主体7266径向延伸的四个圈环7262。虽然心房部分7260显示具有四个圈环7262,但提供的圈环数量可在可选的实施方式中不同。四个圈环7262中的每一个均在其距主体7266最远点处包括更小的子圈环7264。各圈环7262和子圈环7264一起形成一个较大的中断的材料圈环。这种具体构型可在卷曲或弯曲心房部分7160时有所帮助,因为较大圈环的中断可使其更具柔性。心房部分7260具有类似于图100A示例的轴向构型。图115显示示例性心房部分7280,其具有这样的径向构型:包括远离主体7288径向延伸的四个圈环7282。四个圈环7282中每一个均在其距主体7288最远点处包括第二圈环7284,并且每个第二圈环7284在其距主体7288最远点处包括第三圈环7286。各圈环7282、第二圈环7284和第三圈环7286一起形成一个较大的中断的材料圈环。在示例的构型中,第二圈环7284具有第一径向尺寸,其小于其相应的第一角度尺寸。而且如示例,第三圈环具有第二径向尺寸,其小于其相应的第二角度尺寸,其中第一径向尺寸小于第二径向尺寸,并且第一角度尺寸大于第二角度尺寸。这种构型可在卷曲或弯曲心房部分7180时有所帮助,因为圈环的中断可使其更具柔性。心房部分7280具有类似于图100A示例的轴向构型。图116A–116B显示示例性心房部分7300,其具有这样的径向构型:包括十二个臂7302,每个臂在起始端7304连接至主体7314,从主体7314径向向外延伸,并在末端7306连接至具有Z字型构型的环形外周部分7308的内向顶点7310。Z字型部分7308围绕主体7314延伸,并且对于每个臂可包括两个或更多个Z。例如,示例的Z字型部分包括二十四个从主体7314径向向外指向的外向顶点7312点和二十四个径向向内指向主体7314的内向顶点7310。由于每个臂7302经由Z字型部分7308连接至其每个相邻臂,这种构型比具有独立臂构型呈现更高的周向相关度。心房部分7300具有这样的轴向构型:其中臂7302向心房延伸远离其处于主体7314的起始端7304,然后径向且心室向卷曲。Z字型部分7308径向且心房向卷曲,因此其同时径向和心房向延伸远离臂7302。图117A–117B显示示例性心房部分7320,其具有这样的径向构型:包括十二个臂7322,每个臂在起始端7324连接至主体7600,从主体7600径向向外延伸,并且在末端7326连接至第一外周Z字型部分7328的内向顶点7332。第一Z字型部分7328围绕主体7600延伸,并且包括从主体7600径向向外指向的24个外向顶点7334和径向向内指向主体7600的24个内向顶点7332。心房部分7320进一步包括第二Z字型部分7330,其围绕第一Z字型部分延伸,并且包括24个外向顶点7338和24个内向顶点7336。第二Z字型部分7330的各内向顶点7336连接至第一Z字型部分7328的其中一个外向顶点7334。由于第二Z字型部分7330,心房部分7320比心房部分7300具有更大轴向和径向刚度和更大周向相关度。心房部分7320具有类似于图100A示例的轴向构型。图118显示示例性心房部分7340,其具有类似于心房部分7320的径向构型。心房部分7340具有类似于图100E示例的轴向构型。心房部分7340不包括存在于心房部分7320中的臂,因此内部Z字型部分7342和外部Z字型部分7344仅经由织物7346连接至主体部分7348。由于Z字型部分仅通过织物7346连接至主体部分7348,心房部分7340具有低轴向刚度。图119A–119B显示示例性心房部分7360,其具有这样的径向构型:包括单个材料部分7362,围绕主体7366形成一系列圈环。如示例的,这些圈环可在一些位置彼此重叠,但不在其缠绕主体7366时的其它位置重叠。心房部分7360与主体7366的连接可位于从主体7366的心房端移位的位置处,并且该连接可通过缝线7364进行,如示例的。心房部分7360具有高周向相关度、低轴向刚度——由于其连接至主体7366和低径向刚度——由于施加于材料部分7362的径向力导致材料7362的圈环弯曲。心房部分7360具有类似于图100A示例的轴向构型,除了心房部分7360和主体7366之间的连接点位于从主体7366的心房端向心室移位的点。图120显示示例性心房部分7380,其具有这样的径向构型:包括围绕主体7386延伸的单个材料环7382,因此具有类似于图100F示例的轴向构型。单个材料环7382不连接至主体7386,除了经由织物7384。心房部分7380具有高周向相关度、低径向刚度——由于施加于环7382的径向力导致环7382径向位移和/或折叠和低轴向刚度——由于材料7382可独立于主体7386移动。图121显示示例性心房部分7400,其具有类似于心房部分7100的径向构型,除了其仅包括十二个臂7402,形成六个臂对,每对形成单个圈环7406。在其它实施方式中,可使用任何数量的臂对,未示例。心房部分7400具有相邻臂对之间的空间7404,其可用于容纳患者二尖瓣解剖结构的不同特征。作为一个实例,心房部分7400可被植入,使得主动脉瓣结构被定位在其中一个空间7404内。图122显示示例性心房部分7420,其具有类似于心房部分7400的径向构型,除了每个通过臂对7422形成圈环7424大于和宽于心房部分7400中的圈环。虽然图122中未显示,但圈环7424可被设定尺寸,使得相邻圈环7424彼此接触。图123A–123B显示示例性心房部分7440,其类似于心房部分7300,除了其具有类似于图100D示例的轴向构型:内向顶点7442指向主体7444,而且以微小角度指向主体7444的心室端130的方向。图124A–124B显示示例性心房部分7460,其类似于心房部分7300,除了其具有类似于图100C示例的轴向构型:心房部分向心室且径向向内卷曲,使得顶点7462反向指向主体7468。图125A–125B显示示例性心房部分7480,其类似于心房部分7460,除了其不连接至主体7482其心房端处。相反,心房部分7480连接至主体7482的从主体7482的心房端向心室端移位的点处。任何上述径向构型可被改造以适应患者二尖瓣区域的解剖结构。图112和126–130示例基于此目的改造的心房部分的实例。图126示例十二个臂7142中的一个被去除的心房部分7140。图127示例十二个臂7202中的一个被去除心房部分7200。图128示例从一侧去除两个臂7302并且从对侧去除两个臂7302和一段Z字型部分7308的心房部分7300。图129示例十二个臂7302中的六个被去除的心房部分7300。图130示例十二个臂7464中的八个和两段Z字型部分7466被去除的心房部分7460。作为此技术应用的一个实例,预期在植入假体瓣膜后沿主动脉瓣14的方向定向的臂或心房部分的其它部分可被去除,从而产生另外的空间和缓解对解剖结构特征的压力。类似地,可利用这些改造改变构型的刚度或周向相关度。类似地,上述任何心房部分的构型的三维可被进一步改变。心房体的轴向位置可取决于关于纵轴的角位置和/或径向位置。作为一个实例,心房部分可包括鞍形,以适应二尖瓣环的天然形状。这种构型显示在图131中,其示例心房部分7500,该心房部分7500类似于心房部分7300,除了其总体上是鞍形的。进一步,上述任何心房部分可被改变,使得其在平面图中的形状不是圆形或基本上圆形。作为一个实例,上述任何心房部分可总体上是肾形,以适应天然二尖瓣环的天然形状。图132A–132C显示示例性心房部分7520,其具有类似于心房部分7020的径向构型。示例的心房部分7520包括十个臂7522。心房部分7520具有这样的轴向构型:其中一些臂7522在主体7524的心房端附接至主体7524,而其它臂在从主体7524的心房端向心室移位的位置处附接至主体7524。另外,一些臂7522径向延伸远离主体7524,而其它臂径向且心室向延伸远离主体7524。图133A–133C分别显示示例性心房部分7540的顶视图、底视图和侧视图,其具有类似于心房部分7380的径向构型。心房部分7540包括单个材料部分7542,其围绕主体7544并通过织物7546偶联至主体7544。织物7546包括两个旁通孔7548,该旁通孔7548可允许血液以任一方向更快流过织物,因此减少施加于织物的压力。特别重要的是旁通孔降低施加于织物的收缩压力的能力——通过在假体瓣膜最初植入时允许一些血液通过该孔从左心室流至左心房。收缩压力若过高可导致心房部分与天然组织分离,从而阻止可持续的组织向内生长。因此,通过使一些血液流过心房部分7540并且从而降低对心房部分7540的收缩压力,旁通孔7548可促进组织向内生长——具体地,接合处36的区域中。在一些实施方式中,在可持续的组织内向生长已经发生后,患者可经历密封旁通孔的后续程序,从而进一步减少二尖瓣反流。图134显示示例性假体瓣膜7560,其具有主体7562,主体7562具有从主体7562心房端附近第一直径至相对主体7562心室端附近较小直径逐渐变细的总体上截头锥形形状。主体7562的逐渐变细的形状可有助于瓣膜7560共形于天然二尖瓣的形状,从而提供假体瓣膜和天然组织之间接触的较大表面积,因此可有助于增强密封、组织向内生长和装置植入时的稳定性。主体7562的逐渐变细的形状还可有助于增强假体瓣膜7560内提供的瓣叶的边缘的接合。提供具有较小心室端的瓣膜还可有助于减少瓣膜7560和腱索16或乳头肌22、24之间的干扰。瓣膜7560包括柔性织物7564,其从心房端延伸至主体7562的心室端。织物7564可有助于瓣膜7560共形于天然组织的形状,从而进一步增强密封和组织向内生长,和减少对天然组织的创伤。柔性织物7564可包括不同生物相容性材料,如例如,弹性材料,如弹性纤维(spandex),或非弹性体织物,如PET。在另一实施方式中,可选的瓣膜可具有类似于瓣膜7560的总体上截头锥形形状,并且可选瓣膜的心房端可配置有相对平坦的边缘,使得心房端的形状是非圆形。这种构型的一个优点是可选瓣膜的相对平坦边缘可有助于适应患者的二尖瓣解剖结构,因此可提高装置植入时的稳定性。图135显示示例性框架7570,其用于假体瓣膜并且具有主体7572和心房部分7574。主体7572具有总体上类似于主体7562的截头锥形形状的构型,并且心房部分7574具有类似于心房部分7040的构型。框架7570可被从心房部分7574周边延伸至主体7572的心室端的柔性织物(未显示)包覆,该柔性织物可有助于增强密封和组织向内生长,和减少对天然组织的创伤。在另一实施方式中,可选的框架可具有总体上类似于框架7570的截头锥形形状,并且可选框架的心房端可配置有相对平坦的边缘,使得心房端的形状是非圆形。这种构型的一个优点是可选框架的相对平坦边缘可有助于适应患者的二尖瓣解剖结构,因此可提高装置植入时的稳定性。图136显示假体瓣膜的示例性框架7580,其具有主体7582和心房部分7584,心房部分7584具有类似于心房部分7440的构型。类似于心房部分7440,心房部分7584包括具有多个向内顶点7590和向外顶点7588的Z字型支柱的外环。框架7580包括第一柔性截头锥形织物覆盖物7586A,其从心房部分7584上的从向外顶点7588延伸至主体7582的心室端。框架7580还包括第二柔性截头锥形织物覆盖物7586B,其从向内顶点7590延伸至主体7582的心室端。两层织物7586可有助于框架7580共形于天然组织的形状,从而增强密封和组织向内生长,和减少对天然组织的创伤。两层柔性织物7586可包括不同生物相容性材料,如例如,弹性材料,如弹性纤维。图137A–137B分别显示用于假体瓣膜的框架的另一示例性心房部分7720的顶视图和侧视图。更具体地,心房部分7720包括十个相对刚性(相对于臂7724)的径向延伸臂7722,每个臂具有与图102A–102B的臂7042(包括马蹄形构件7726)相同的构型。心房部分7720还包括两个相对柔性(相对于臂7722)的径向延伸臂7724,每个臂具有与图108的臂7162(包括马蹄形构件7726)相同的构型。在关于图137A–137B使用时,刚度可指代径向、轴向和/或周向刚度,如同上文限定的那些术语。在图137A–137B所示的实施方式中,两个臂7724可包括总体上Z形盘旋或类似的构型,或与臂7722的横截面外形相比可具有小横截面外形,以产生相对柔性。图137A–137B还显示,臂7722和7724(包括各自的马蹄形构件7726)的径向端部可使心房弯曲远离框架主体7728,并且框架主体7728可通过类似于套筒1506、1606的圆柱形偶联构件7730偶联至至少一个心室锚7732。在一些情况下,心房部分7720可具有约40mm和70mm之间的直径D3,其中55mm是一个示例性的适当的心房部分直径。在一些情况下,臂7722和/或7724可具有约5mm和25mm之间的长度L2,其中13mm是一个示例性的适当的臂长度。图138显示假体瓣膜7740的顶视图,其包括具有类似于图137A–137B的心房部分的框架。图138显示,框架可被覆盖在织物7742内(例如,如本申请其它位置描述)。图139显示假体瓣膜7760,其具有类似于假体瓣膜7740的构型。假体瓣膜7760可具有心房部分,包括心房曲线形部分7762,其心房卷曲远离假体瓣膜7760的主体7764。在一些情况下,心房曲线形部分7762可包括两个相对柔性的径向延伸臂(如臂7724或任何具有产生相对柔性的性质的臂,如本文其它位置描述(例如,具有盘旋形状的臂,如图109A–109E所示和本申请相应文本所述;或螺旋的构型,如图112–113所示和本申请相应文本描述)),其被覆盖在织物7766内。在一些情况下,心房曲线形部分7762可仅包括两个被覆盖在织物内的这种臂,虽然曲线形部分7762可包括更多或更少数量的相对柔性的径向延伸臂。图137A–139所示的任何实施方式可被以多种方式改造——例如,通过包括更多或更少的臂(例如,包括一个或三个或更多个相对柔性臂,或包括十一个或更多个或九个或更少个相对刚性臂)或通过合并本文描述的任何其它特征。进一步,图137A–139示例的心房部分可具有总体上圆形形状,如图138所示,或可具有长度可变的臂,因此可具有可选的形状,如卵形、椭圆形、D形或肾形。这种可选的形状可在一些情况下用于更好地共形于左心房的解剖结构。例如,臂长可变化,使得各臂末端在假体瓣膜被植入天然二尖瓣内时接触左心房壁。图137A–139示例的实施方式可提供某些优点。例如,在假体瓣膜被植入天然二尖瓣内时,假体瓣膜的心房部分(例如,图137A–139所示那些中的一个)可被定向,使得相对柔性臂或心房曲线形部分7762或两者被定位邻近左心房内的主动脉窦(即,在A2位置,通过Carpentier命名),从而减少对左心房的这个区域中的天然组织的创伤,减少施加于主动脉窦的压力,和降低主动脉窦被臂磨损和/或穿孔的可能。在一些情况下,图137A–139显示的心房部分可在A2和P2位置处具有相对柔性臂,或可具有相对刚性臂和相对柔性臂的各种其它排列。上述不同心房部分中的任一种可配备可跨越臂或所述构型的其它部件之间的开放空间的不同生物相容性织物中的任一种。适当的织物材料的若干实例在上文得到描述,包括合成材料如PET和生物学材料如牛心包。织物材料可基于期望的多孔性、血液渗透性或其它相关特征来选择。上述心房部分可通过多种方法制造,但在一个示例性方法中,其从单个金属材料管(例如,镍钛诺)激光切割而来。在其它实施方式中,不同部件(例如,几个臂)可被单独制造,然后连接至其它部件,形成单个假体装置。类似地,任何心房部分可通过多种方法附接至假体装置的主体,方法包括通过一体形成(即,从同件基体材料切割)或通过单独形成然后连接(例如,通过焊接或用缝线固定)。在假体瓣膜已被植入天然二尖瓣后,如图140示例,最初主要通过天然二尖瓣瓣叶对假体瓣膜外部施加的压力来防止瓣周漏,假体瓣膜外部充当假体间隔物,如同上述实施方式3000。然而,随时间过去,组织内向生长发生,并通过形成生物学组织和假体材料的实体障碍而增加假体瓣膜周围的血液堵塞,因此减少了对天然瓣叶和假体材料之间压力的依赖。心脏中的假体定向再参考图1–4,人心脏的天然二尖瓣2具有与其它天然心脏瓣膜非常不同的结构,包括环部分8、前叶10、后叶12和腱索16,腱索16将瓣叶10和12束缚至后中乳头肌和前外乳头肌22和24。如上文也说明,腱索16附接至A1、A3、P1和P3区域中的瓣叶10和12,余下A2和P2区域相对没有腱索附接点。这些解剖结构特征提供了可取的进入方式以递送假体至天然二尖瓣2附近。进一步,这些解剖结构特征使得将假体锚定在A2和P2区域中而非在A1、A3、P1或P3区域中以减少假体锚和腱索16之间的干扰是可取的。虽然心脏的总体结构是公知的,但每个人心脏的组分的具体尺寸足够可变到难以确定个体二尖瓣的确切定向和腱索以及各自的腱索附接点的确切位置。因此,确定引入假体至天然二尖瓣2的适宜定向和确定锚定假体的适宜位置可能是具有挑战性的。这个问题由于如下事实而加剧:二尖瓣假体通常在荧光透视术下递送,荧光透视术可使医生看到假体的金属部件,但不可看到患者心脏的软组织(包括腱索16)。图89示例荧光透视术定向装置6000,其可用于增强医生将假体定向在在期望的轴线上以递送和锚定的能力。该装置可在递送二尖瓣假体(例如,假体二尖瓣)前使用,以至增加医生在A2和P2区域中定向假体锚的能力。如图89示例,定向装置6000包括引导丝轴6002、内轴6004、外轴6006和手柄6008。轴6002、6004和6006均包括细长管形状,并且具有内腔,其中可布置其它部件。引导丝轴6002包括内腔,穿过其中可提供引导丝。内轴6004包括内腔,其中可布置引导丝轴6002,并且外轴6006包括内腔,其中可布置内轴6004。鼻锥体6010可被紧固至引导丝轴6002的远端。鼻锥体6010促进定向装置6000穿过人体。鼻锥体6010包括内腔,该内腔连通引导丝腔,使得通过引导丝轴6002提供的引导丝可继续通过鼻锥体6010并进入人体。内轴6004包括远侧部分6014和近侧部分6016。如示例的,内轴6004的远侧部分6014可包括非金属材料,而内轴6004的近侧部分6016可包括金属材料。外轴6006类似地包括远侧部分6020,其可包括非金属材料;和近侧部分6022,其可包括金属材料。这些材料组合的优点在下文讨论。图89还示例,内轴6004的近侧部分6016延伸超过外轴6006的近侧部分6022,并且和引导丝轴6002的近端延伸超过内轴6004的近侧部分6016。因此,通过相对调节各个轴的近侧部分,医生可控制各轴远侧部分的相对位置,从而控制装置的展开,如下文进一步说明。图89进一步示例,偶联至内轴6004的近侧部分6016的是密封构件6024,其防止流体通过内轴6004的腔流出人体。还示例,两个回波发生臂6012和荧光镜标记带6018偶联至内轴6004的远侧部分6014。展开构型的回波发生臂6012从内轴6004沿相反方向向外延伸,并且标记带6018包括两个布置在标记带6018对立侧上的孔6026。对立臂6012和对立孔6026的位置可相对移位任何角度,但在示例构型中,各臂6012从各孔6026角度移位90度。这些特征和角度尺寸的优点在下文描述。示例性回波发生臂6012显示在图90中。回波发生臂6012可包括连接部分6028和延伸部分6030。连接部分6028适于通过不同机构中的任一种可枢转地连接至内轴6004的远侧部分6014,如通过铰链,通过柔性材料,等。延伸部分6030包括回波发生材料,其允许通过回波心动描记术(心脏超声成像)观察臂6012。多种机构可用于引起臂6012从递送构型的轴向定向位置转变成展开构型的外向定向位置。例如,臂可被配置以在下列的力下自扩张:例如,弹簧、弹性材料或具有形状记忆的金属如镍钛诺。装置6000还可配置有致动线(例如,丝)(未显示),其贯穿装置主体并且允许医生控制臂6012的延伸和/或收回。虽然图89示例的实施方式允许臂相对于内轴6004一维旋转,但在可选的实施方式中,臂6012是二维或三维可旋转的,如通过万向接头(gimble)或万向接头连接(universaljointconnection)。图91–94示例荧光透视术定向装置6000从递送构型至展开构型的展开顺序。如图91示例,在递送构型下,外轴6006和鼻锥体6010形成连续的圆柱体,其允许装置6000穿过患者身体并进入心脏。如图92示例,装置的展开通过从鼻锥体6010收回外轴6006(或可选地,将鼻锥体6010从外轴6006驱出)开始。如图93示例,装置6000的展开通过下列继续:进一步分离鼻锥体6010和外轴6006并且推进内轴6004向远侧穿过外轴6006,直到回波发生臂6012开始从装置6000向外延伸。如图94示例,在展开构型下,鼻锥体6010与外轴6006分离,并且内轴6004已被远侧推进穿过外轴6006到达臂6012从装置6000完全向外延伸并且标记带6018完全暴露的点。如上所述,各轴6002、6004和6006的近侧部分是医生可及的。因此,医生可通过推进和收回内轴6004内的引导丝轴6002和外轴6006内的内轴6004来控制展开顺序。通过相对于外轴6006的近侧部分6022推进引导丝轴6002的近端,医生可将鼻锥体6010推离外轴6006的远侧部分6020。类似地,通过相对于外轴6006推进内轴6004的近侧部分6016,医生可相对于外轴6006的远侧部分6020推进内轴6004的远侧部分6014(臂6012和标记带6018偶联至其)。在医生已完成使用装置6000时,可通过逆转展开顺序将其从患者身体撤回。即,医生在装置6000处于其展开构型的情况下开始撤回。医生可相对于外轴6006收回内轴6004,直到标记带6018和臂6012被包围在外轴6006内。然后医生可相对于外轴6006收回引导丝轴6002,直到鼻锥体6010和外轴6006的远侧部分6020接触,形成连续的圆柱形身体。然后医生可从患者身体移出装置6000。在一个具体实施方式中,处于其递送构型的装置6000的宽度(W1)为33French,并且展开构型的装置6000的最大宽度(W2)(即,两个回波发生臂6012的对立端之间的距离)为33.5mm。图95A–99示例不同操作阶段中的装置6000。可利用不同方式将装置6000引入患者身体和推进至二尖瓣附近,包括通过经顶点或经横膈膜方式。图95A示例处于利用经顶点方式的处于天然二尖瓣2附近的展开构型的装置6000。可见,鼻锥体6010与内轴远侧部分6014分离,并且回波发生臂6012延伸远离内轴6004的远侧部分6014。还示例了腱索16、乳头肌22和24和二尖瓣的瓣叶10和12。图95B是回波心动描记术图像,其示例了端视图中处于天然二尖瓣2附近的其展开构型下的装置6000。由于二尖瓣的软组织和装置6000的回波发生臂6012在回波心动描记术中都可见,医生可利用回波心动描记术将装置6000的臂6012定向到相应于位置A2和P2的位置,在此有相对少的腱索16与瓣叶10、12附接点。即,医生可将臂6012定向到锚定假体期望的定向。在回波发生臂6012已被定向对准位置A2和P2后,可结束回波心动描记术,并可利用荧光镜在荧光透视术下观察患者心脏。图96示例示例性C臂荧光镜6032,其包括发送器6034、接收器6036和其上可安置患者的平面6038。发送器6034和接收器6036之间的路径限定了荧光镜轴线6040。如图97–99示例,可利用装置6000将荧光镜6032相对于患者定位在期望的定向。装置6000的标记带6018在荧光透视术下可见,并且如图89示例,具有自回波发生臂6012角度移位已知角度(如约90度)的两个孔6026。因此,臂6012在患者心脏内的定向可通过如下确定:旋转荧光镜6032,直到孔6026可见,因此对准了荧光镜轴线6040。如图97示例,得知孔6026自臂6012角度移位90度。图97还示例,荧光镜轴线6040已对准孔6026。因此,得知荧光镜轴线6040自臂6012角度移位90度。如图98示例,荧光镜轴线6040对准孔6026并垂直于臂6012。由于臂最初在回波心动描记术下对准位置A2和P2,现已知轴线6040垂直于这些位置之间轴线,并且递送至天然二尖瓣2附近并且沿荧光镜轴线6040的垂直轴线对齐的物件不太可能参与干扰腱索16或乳头肌22、24。因此,通过旋转荧光镜6032,直到标记带6018中的孔6026在荧光透视术下可见,因此对准轴线6040,可获得荧光镜6032相对于患者心脏的期望定向。图99示例在荧光透视术下看到的处于二尖瓣附近的展开构型的装置6000。外轴6006的远侧部分6020和内轴6004的远侧部分6014均在此视图中是不可见的,因为其包括非荧光透视材料。相比之下,鼻锥体6010、引导丝轴6002和标记带6018是可见的,因为其包括荧光透视材料。因此,内轴和外轴6004和6006远侧部分选择非荧光透视材料致使医生更好地观察将荧光镜6032定向在期望的轴线上的相关部件。如图99示例,回波发生臂6012可在荧光透视术下可见,例如,其中臂连接部分6028和臂延伸部分6030由不同材料制成,一是回波发生型和另一个是荧光透视型。在此示例实施方式中,臂6012可补充标记带6018,致使医生在荧光透视术下定向装置6000。定位标记带6018上的孔6026而非装置6000的另一部件(例如,臂6012)增加了其之间的距离,从而允许更准确的荧光镜定向。在荧光镜6032已被定向以孔6026对准轴线6040(因此与臂6012的角度已知和与A2和P2位置之间轴线的角度已知)后,可将装置6000从患者身体移出。通过保持患者在平面6038上的位置和保持荧光镜6032相对于患者心脏的定向,可在植入过程中利用轴线6040定向假体。二尖瓣假体(例如,假体二尖瓣)可被推进至患者天然二尖瓣2附近,并在荧光透视术下旋转,直到看见其锚横向延伸远离假体和递送装置的主体或总体上垂直于荧光镜轴线6040。由于假体的锚现定向在与装置6000位于患者心脏内时回波发生臂6012相同的轴线上,医生可更加确信锚现对准了天然瓣叶的A2和P2区域。为总结定向装置6000可提供的一些优点,首先注意,二尖瓣假体的递送和锚定位置是其成功植入是相关因素。进一步,确定递送和锚定的适宜定向由于相关材料的属性而非常困难:人软组织(例如,人心脏组织)在回波心动描记术下可见,但在荧光透视术下不可见。用于制造二尖瓣假体的材料通常在荧光透视术下可见,但在回波心动描记术下不可见。因此,定向装置6000利用回波心动描记术和荧光透视术的优点,允许医生确定递送和锚定假体的可取定向。扩张辅助递送系统关于具有不可相对于主体独立扩张的锚的假体装置实施方式(可以是这的情况:具有主体与心室锚不一体形成的框架的实施方式,如图47和48示例的那些),可采用具有强制扩张锚的机构的递送系统。图141–156示例了扩张辅助递送系统8000的一个实施方式,其被配置以递送和植入具有锚8052、主体8054和心房部分8056的示例性假体二尖瓣8050(参见图151),并且包括强制扩张假体瓣膜8050的部件的机构。递送系统8000在本文中关于示例性假体瓣膜8050和经顶点方式递送来描述,但应理解类似的系统可用于将可选的假体经由可选的递送方式递送至天然二尖瓣区域,和/或经过可选的展开顺序。例如,具有图101A–140描述的任何心房部分实施方式的假体可通过适当改动递送系统和相关递送方法而用于递送系统8000。因此图101A–140的心房部分实施方式在下文中通过示例性假体瓣膜8050来笼统表示,以简化描述。如图141示例,递送系统8000可包括关于中心轴线对准并且可沿轴向方向相对滑动的一系列同心鞘。递送系统8000可包括近侧手柄部分8008,该近侧手柄部分8008具有控制机构,用于医生在远侧部分8020插入患者身体时在患者体外进行操纵。递送系统8000可包括引导丝鞘8002,其贯穿递送系统长度并且包括腔——引导丝(未显示)可穿过其中。引导丝鞘8002可被定位在内鞘8004内,并且可具有近侧延伸超过内鞘8004近端和远侧延伸超过内鞘8004远端的长度。内鞘8004可被定位在外鞘8006内。递送系统8000的远侧部分8020还可包括附接至内鞘8004的一对锚扩展器8012和附接至引导丝鞘8002远端的鼻锥体。锚扩展器8012可由任何适当的材料(例如,镍钛诺)形成,使得锚扩展器8012在其不受外鞘8006约束时从内鞘8004弹性地径向延伸,如下文进一步说明。如图141、143、147–151和154–156示例,鼻锥体可包括不同构型。如图141示例,圆锥形鼻锥体8010总体上是圆锥形,并且由实心材料件形成。如图143示例,中空的鼻锥体8037包括中空的、总体上圆柱形的具有腔8038的近侧部分8040,和总体上圆锥形的远侧部分8042。如图147–151示例,菱形鼻锥体8046包括实心的、总体上菱形的构型。鼻锥体8010、8037和8046均提供给系统8000逐渐变细的远端,其可充当楔形物,以引导系统8000的远侧部分8020进入患者身体并在系统8000被推进穿过身体时减少周围组织遭受的创伤。这些构型的另外的优点在下文说明。如示例的,手柄部分8008包括至少三个控制机构:内鞘控制器8014、外鞘控制器8016和引导丝鞘控制器8018。利用这三个机构,引导丝鞘8002、内鞘8004、外鞘8006和手柄部分8008均可相对轴向滑动。由于这些部件的轴向可调性,各种构型都是可以的。如图146示例的构型(其中内鞘8004和外鞘8006已被相对于手柄8008沿近侧方向收回)可见,假体支撑体8022被定位在内鞘8004内。支撑体8022牢固地连接至手柄部分8008,因此可相对于引导丝鞘8002、内鞘8004和/或外鞘8006中的任一个轴向滑动,但不可相对于手柄8008轴向滑动。手柄8008可在结构上类似于上文描述和图49–55示例的递送系统2000的手柄部分2002。因此,手柄8008包括便于不同鞘彼此相对和相对于手柄8008本身的轴向调节的部件。具体地,手柄8008包括外壳8024,其为医生提供把手,从而在利用控制器致动鞘同时保持系统稳态。手柄8008还包括固定至内鞘8004末端的第一滑动导螺杆和固定至外鞘8006末端的第二滑动导螺杆。各滑动导螺杆在旋转方面固定,而相对于外壳8024可轴向滑动。第一可旋套筒可被同心地定位在外壳8024和第一滑动导螺杆之间,并且具有螺旋状开槽,该螺旋状开槽与从导螺杆突起的螺旋状脊相互作用。第二可旋套筒可被同心地定位在外壳8024和第二滑动导螺杆之间,并且具有螺旋状开槽,该螺旋状开槽与从第二滑动导螺杆突起的螺旋状脊相互作用。第一可旋套筒包括在外壳8024之外延伸的内鞘控制器8014,并且第二可旋套筒包括在外壳8024之外延伸的外鞘控制器8016。鉴于滑动导螺杆在旋转方面固定并且相对于外壳8024可轴向滑动,可旋套筒都是可旋的,但相对于外壳8024轴向固定。在这种构型下,通过相对于外壳8024旋转外鞘控制器8016,医生可使第二导螺杆相对于外壳8024轴向地滑动,从而使外鞘相对于手柄部分8024轴向地滑动。类似地,通过相对于外壳8024旋转内鞘控制器8014,医生可使第一导螺杆相对于外壳8024轴向地滑动,从而使内鞘相对于手柄部分8024轴向地滑动。在示例的构型下,第一滑动导螺杆每英寸可具有比第二滑动导螺杆更少的脊。因此,内鞘控制器一次旋转(其与第一滑动导螺杆相互作用)导致的内鞘轴向移位可大于外鞘控制器一次旋转导致的外鞘轴向移位。在可选的实施方式中,导螺杆可采用每英寸各种数量的脊,并且对于两个导螺杆而言,该数量可相同,或可不同(如示例的构型)。进一步,控制器8014、8016任一方向的旋转可导致鞘8004、8006沿任一轴向方向移位。例如,在一个实施方式中,内鞘控制器8014的顺时针旋转可导致内鞘8004远端远侧移动,而在另一实施方式中,内鞘控制器8014的顺时针旋转可导致内鞘8004的远端近侧移动。在一些实施方式中,控制器8014、8016沿相同方向的旋转可导致鞘8004、8006的远端沿相同方向移动,而在其它实施方式中,控制器8014、8016沿相同方向的旋转可导致鞘8004、8006的远端沿相反方向移动。在可选的实施方式中,可采用可选的鞘致动方法。例如,不同的鞘的推进和/或收回可由液压系统、电动机、滑轮系统或各种其它方法来控制。图142示例更详细的系统8000的近端部分和分解构型的引导丝鞘控制器8018。如图142示例,引导丝鞘控制器8018包括内螺纹杆8026和外螺母8028,该外螺母8028被配置以适配在螺纹杆8026上。通过将螺母8028紧固在杆8026上,安装在引导丝鞘8002上的弹性材料8030被轴向压缩,因此径向扩张并对引导丝鞘8002施加径向力,从而通过摩擦固定引导丝鞘8002相对于手柄8008的位置。图143更详细示例系统8000的远端部分8020。在图143示例的构型下,外鞘8006包含内鞘8004,并将附接的锚扩展器8012固定在基本上轴向的定向。图143还示例,内鞘8004包括两个对立的凹陷部分或开槽8034(图143中仅一个可见)和两个对立的开槽8036(图143中仅一个可见)。开槽8034通过缩小内鞘8004的外形而提供更多空间以使假体瓣膜8050的部分适配在外鞘8006内,同时通过不缩小内鞘8004其完整横截面的外形而保留一定额外强度。槽8036允许假体瓣膜被安装在内鞘8004内并且锚8052延伸到内鞘8004外,由此锚8052可先于假体瓣膜8050的主体8054展开。图143还示例更详细的鼻锥体8037。鼻锥体8037内的腔8038允许框架远侧部分(例如,心房部分)被固定在鼻锥体8037内。鼻锥体8037的近侧部分8040的直径略小于远侧部分8042的近端直径,并且被配置使得在鼻锥体8037到达外鞘8006附近时,外鞘8006可延伸超过鼻锥体8037的近侧部分8040,直到其接触鼻锥体8037的远侧部分8042的近端。图144–146示例系统8000的三种可能的构型——其中引导丝鞘8002已相对于内鞘8004和外鞘8006远侧延伸,和其中内鞘8004已延伸超过外鞘8006的远端。如图144所示,在内鞘8004延伸超过外鞘8006时,锚扩展器8012(其在此实施方式中是自扩张)开始从内鞘8004径向向外延伸。图145示例延伸完全超过外鞘8006的内鞘8004和完全径向延伸的锚扩展器8012。图146示例这样的构型:其中内鞘8004和外鞘8006已被相对于手柄8008收回,从而暴露假体支撑体8022,其目的在下文进一步说明。图147–151利用带有假体瓣膜8050的系统8000示例示例性的展开顺序。如关于图147–151所用,短语“近侧”和“远侧”用于表示构件相对于手柄8008的移动。近侧移动的构件朝向手柄8008移动,而远侧移动的构件远离手柄8008移动。图147示例递送构型的系统8000。如图147示例,具有锚8052、主体8054和心房部分8056的假体瓣膜8050已被负载于递送构型的递送系统8000中。为将假体瓣膜8050负载到系统8000中,使鼻锥体8046远侧延伸,并且使外鞘8006近侧收回,以暴露内鞘8004内的腔。然后将假体瓣膜8050定位,使得其包围径向扩张状态的引导丝鞘8002,并压缩至径向压缩状态。然后将径向压缩的主体8054和心房部分8056插入内鞘8004,并且将锚8052定位在槽8036内和内鞘外的开槽8034内。将主体8054近侧推进穿过内鞘,直到其停靠于支撑体8022。然后可使外鞘8006延伸到内鞘8004和锚8052上。因此,在图147示例的递送构型下,主体8054和心房部分8056被固定在内鞘8004内,而锚8052被固定在外鞘8006内。图148示例瓣叶捕获构型的系统8000。如图148示例,在递送系统8000的远端已被递送至天然二尖瓣区域(例如,左心室)后,医生可收回外鞘8006,使锚扩展器8012从内鞘8004径向向外延伸,准备瓣叶捕获。如图148示例,锚8052可被覆盖在织布8058内,织布8058被配置成相对厚、坚固而软。在具体实施方式中,织布8058可由编织的复式织布制成。织布8058覆盖锚8052,以提供较软表面来接触天然组织,因此减少创伤。织布8058还增加假体瓣膜8050和天然组织之间的接触表面积,从而利于组织向内生长和提供更稳固的安装。图148还示例,织布可被配置以产生腔或袋,锚扩展器8012可延伸到其中从锚扩展器8012传力至锚8052。在这种构型下,在外鞘8006被收回时,锚扩展器8012径向扩张,并牵拉织布8058,织布8058进而牵拉锚8052至图148显示的打开构型。在可选的实施方式中,锚8052可受力于其它机构而分开。例如,在一个可选的实施方式中,锚扩展器8012被直接紧固至锚8052。在另一可选的实施方式中,无锚扩展器,取而代之,提供缝线,该缝线被紧固至锚8012,贯穿系统8000的长度(例如,在内鞘8004和外鞘8006之间),并在手柄8008处离开系统8000。在这种可选的实施方式中,通过牵拉缝线,医生可迫使锚8012形成打开构型。另一可选的实施方式中,鼻锥体8037的中空部分8040可在锚8052和内鞘8004之间近侧延伸。在这种可选的实施方式中,可近侧收回锚8052和内鞘8004之间的鼻锥体8037,使得中空部分8040的近端部分迫使锚8052远离内鞘8004径向延伸。在锚8052已如图148示例被径向扩张后,利用上述方法定向对准患者解剖结构的荧光镜可被用于将锚8052在患者天然二尖瓣瓣叶的A2和P2区域内定向。在递送系统8000处于天然二尖瓣附近并且锚8052处于径向扩张构型的情况下,医生可利用荧光镜装置观察旋转中的系统8000。当医生在荧光透视术下观察到锚8052处于其最大宽度时(这表示锚8052对准了荧光透视轴线6040的垂直轴线),锚就对准了A2和P2区域,从而在通过锚8052捕获瓣叶时降低锚8052和腱索之间干扰的可能。在锚8052已利用荧光镜被径向扩张和角度定向时,可推进系统8000的远端穿过患者的天然二尖瓣,使得扩张的锚8052移动到天然瓣叶10、12后方,如上所述。图149示例闭合构型的系统8000。如图149示例,在锚8052被定位在天然瓣叶10、12后方后,可将外鞘8006远侧推进,以部分地再覆盖锚扩展器8012,从而迫使锚返回闭合构型,从而在锚8052和内鞘8004之间捕获天然瓣叶10、12。在锚8052已返回闭合构型并捕获瓣叶后,可近侧收回内鞘8004,使得心房部分8056可径向向外扩张,锚扩展器8012从织布8058内收回,并且内鞘8004滑离瓣叶和主体8054之间。图149显示内鞘略微收回。图150示例处于进一步收回构型的系统8000。如图150示例,内鞘8004被进一步收回,使得心房部分8056部分地径向向外扩张,并且锚扩展器从织布8058和锚8052完全收回。在图150中还可见,定位在心房部分8056内的鼻锥体8046的菱形和具体地鼻锥体8046的近侧部分可协助引导径向向外扩张时的心房部分8056。支撑体8022(图146)用于在收回内鞘8004时保持假体瓣膜8050的位置。在内鞘8004向图151显示的位置被进一步收回时,心房部分8056继续在左心房内径向向外扩张,并且主体8054开始在天然二尖瓣口内径向向外扩张。在内鞘8004的远端接近支撑体8022时,主体继续扩张,但连接至主体8054的锚8052的心室圈环8060继续被保留在内鞘8004内。为确保主体8054的径向扩张在主体8054完全处于内鞘8004外侧后以受控方式继续,从而防止圈环8060的损坏,提供给支撑体8022(图146)两个远侧突出臂8062,每个远侧突出臂沿径向压缩状态的主体8054的外部定位。在这种构型下,臂8062作用以部分地固定主体8054的心室端,直到圈环8060完全在内鞘8004外侧,此时假体瓣膜8050将完成到完全扩张构型的径向扩张,如图151示例。在可选的实施方式中,可利用可选的机构来确保主体8054的径向扩张以受控方式继续。在一个具体的可选实施方式中,一对钩或抓取构件可用于部分地固定主体8054的心室端,直到圈环8060完全处于内鞘8004外侧,从而确保主体8054的径向扩张受控。图151示例完全收回构型的系统8000和完全径向扩张构型的假体瓣膜8050。在植入天然二尖瓣区域后,假体瓣膜8050可总体上如图23、33、34、39和70中任一个所示定位。心房部分8056被定位在左心房内,并且被定位接触二尖瓣环的天然组织。主体8054被定位在天然二尖瓣口内,并且可包括瓣叶,如上所述。锚8052被定位使得天然二尖瓣瓣叶在锚8052和主体8054之间被捕获。在系统8000实现完全收回构型并且假体瓣膜8050实现完全扩张和展开构型后,可使外轴8006向鼻锥体8046远侧延伸,或可使引导丝轴8002近侧收回,使得鼻锥体8046移向外轴8006,从而使鼻锥体8046接触外轴8006。然后可将装置8000从患者身体收回,留下植入天然二尖瓣区域的假体瓣膜8050。可采用多种可选的展开顺序。在一个可选的展开顺序下,可在允许锚从递送系统径向向外延伸之前将心房部分展开。在这种可选的实施方式中,经顶点推进递送系统的远端穿过左心室并进入左心房,在此展开心房部分。然后足够多地收回递送系统,以使锚在左心室内展开和捕获瓣叶。在另一可选的展开顺序下,固定在鼻锥体内的心房部分可在锚和主体之后展开。在另一可选的展开顺序下,鼻锥体8037的中空部分8040可近侧延伸,固定假体的心房部分、主体和锚。在可选的实施方式中,可推进鼻锥体远离假体,从而使假体径向扩张。在不同实施方式中,可采用不同递送方式,并且递送系统的改造可采用经顶点、经中隔、经顶点、经股或主动脉方式(参见,例如,图63–67)。图152A–152C示例操控装置9000,其可用于递送系统,如系统8000、例如,代替支撑体8022。操控装置9000可包括主体部分9002、近侧连接部分9004——处于主体部分9002的近端和远侧连接部分9006——处于主体部分9002的远端。近侧连接部分9004可使操控装置9000偶联至递送系统8000(如从手柄开始并且穿过内鞘8004延伸的轴的远端),并且远侧连接部分9006可以可释放地偶联至假体瓣膜的近侧部分,如假体瓣膜8050的圈环8060(基于示例目的,瓣膜8050的裸框架的部分显示在图152B–152E中)。主体部分9002可具有总体上圆柱形形状。远侧连接部分9006可与主体部分9002一体形成,并且可包括主体部分9002的圆柱形延伸部,其中形成四个空间或凹陷9016A–9016D。圆柱形内通过空间9016A–9016D形成的远侧连接部分9006的结构可包括中央的逐渐变细的延伸部9008,其宽度主体9002的圆柱形直径朝向操控装置9000的远端逐渐减少。一对固定构件9010A、9010B可从延伸部9008径向向外延伸。每个固定构件9010A、9010B可包括偶联至延伸部9008的相对窄的颈部9012A、9012B和偶联至颈部9012A、9012B的相对宽的头部9014A、9014B。在一些情况下,脊对9020(仅显示一对)可使空间9016A–9016D彼此分隔。例如,示例的脊9020将空间9016A与空间9016C分隔。腔9018可延伸穿过操控装置9000,并且可被配置以容纳引导丝鞘8002,如上所述。图152B和152C示例搁置在操控装置9000的远侧连接部分9006内的假体瓣膜8050的圈环8060。在使用操控装置9000代替系统8000的支撑体8022的实施方式中,可收回內鞘和外鞘以暴露操控装置9000,并且可将假体瓣膜如瓣膜8050负载到操控装置9000中,如图152B–152C所示。然后可使內鞘和外鞘在操控装置9000上延伸,并且通过其固定瓣膜。内鞘可越过瓣膜8050的主体8054延伸,同时可允许锚8052延伸穿过内鞘8004的槽,如上所述。然后可使外鞘8006越过内鞘8004和锚8052延伸,也如上所述。在使用操控装置9000代替系统8000的支撑体8022的实施方式中,可采用类似于上述那些(包括使用锚扩展器8012的那些)的递送顺序以使锚8052远离主体8054扩张。操控装置9000的一个示例性优点是其可允许在假体瓣膜主体展开后迫使锚扩张。这可在第一次尝试时假体瓣膜主体的展开不造成最佳瓣膜布置的情况下具有优势。例如,在假体瓣膜从递送装置释放时,其可弹开,导致在天然瓣膜内移动。因此,迫使锚在主体展开后扩张的能力可允许医生调节假体瓣膜在天然瓣膜内的位置,从而达到更理想的布置。在一个实施方式中,图147–151示例的递送顺序可进行至图150显示的构型。此时,内鞘8004可被收回,直到假体瓣膜8050的主体8054完全不被鞘8004、8006覆盖,但圈环8060仍被操控装置9000固定在内鞘8004内,如图152D所示(以虚线显示展开的主体)。然后内鞘8004可被越过操控装置9000远侧推进,直到其接近主体8054的近端8055。在一些情况下,内鞘8004无法延伸至再次覆盖主体,因为主体8054的直径不能在患者体内再次充分缩小。因此,在内鞘8004伸向并接触主体8054的近端8055时,其将对主体8054的近侧部分施加远侧方向的力。由于圈环8060仍被操控装置9000固定在内鞘8004内,施加于假体瓣膜的远侧方向的力牵拉圈环8060抵靠固定构件9010A和9010B。这导致锚8052远离主体8054径向挠曲,如图152E所示(也以虚线显示展开的主体8054),允许医生按需进一步操纵假体瓣膜8050。在假体瓣膜8050被期望地定位在天然瓣膜内后,可收回内鞘以暴露操控装置9000。此时,圈环8060不再被限制在系统8000内,并且假体瓣膜从系统8000完全释放,如图151所示。图153A和153B示例操控装置9100的另一实施方式,其可被用来代替支撑体8022或操控装置9000。操控装置9100可包括内部锚控部分9102(在图153C中更具体显示)、外部锚控部分9104(在图153D中更具体显示)、间隔环9126(在图153E中更具体显示)和偶联至手柄部分8008的中空调节控制轴9106。如图153C所示,内部部分9102可包括主体9138、径向延伸远离内部部分9102的远端部分的一对远侧固定构件9108、径向延伸远离各自的固定构件9108的一对远侧对准突起9130和被布置在各自的近侧延伸部9142的近端并且径向延伸远离各自的近侧延伸部9142的一对锁定构件9128。如图153D示例,外部部分9104可包括中心腔9140、一对远侧固定构件9110、一对远侧对准突起9132径向延伸远离各自的固定构件9110、一对圈环接收通道9112、一对对准脊9134(仅示例一个)、螺纹部分9124和其近端的锁定构件9144。内部部分9102(例如,主体9138)和外部部分9104(例如,锁定部分9144)可包括各自的中心腔,以满足引导丝腔和贯穿其中的引导丝通过。内部部分9102、外部部分9104和环9126可由各种适当的材料形成,如各种适当的塑料或金属中的一种。图153F显示组装体中的内部部分9102、外部部分9104和环9126。图153G显示位于内轴8004内的操控装置9100。当操控装置9100用于系统如系统8000时(例如,代替支撑体8022或操控装置9000),外部部分9104可以是轴向可调节的,但在旋转方面相对于内部部分9102固定。例如,内部部分9102的主体9138可具有非圆形横截面,其被配置以插入外部部分9104的腔9140,该腔9140可具有匹配的非圆形横截面。如图153A–153B所示,内部和外部部分9102、9104可具有近端部分,其被配置以适配在轴9106的远端部分内。例如,外部部分9104的螺纹部分9124可被配置以啮合轴9106的内部表面形成的互补螺纹,并且内部部分9102的锁定构件9128可被配置以啮合轴9106的内部表面形成的环形开槽9136。操控装置9100的组装可通过将外部部分9104沿近侧方向完全旋入轴9106开始。然后可将内部部分9102通过外部部分9104的腔9140插入轴9106,直到锁定构件9128啮合开槽9136。内部部分9102的主体9138可具有错列的宽度,其从大于轴内部的第一宽度缩小至小于轴内部的第二宽度,使得内部部分9102无法插入轴9106,因此锁定部分9128在开槽9136近侧。然后可将外部部分9104沿远侧方向旋拧,以使其向远侧移动,直到锁定部分9144位于延伸部9142之间,防止锁定构件9128从开槽9136松动。然后可将环9126安装到外部部分9104上的螺纹9124远侧和脊9134近侧位置处。在这种构型下,间隔环9126可防止外部部分沿近侧方向被旋拧过远,使得锁定部分9144不再啮合延伸部9142。图153G显示组装后的操控装置9100,其位于内鞘8004内,并且突起9130、9132和脊9134可位于延伸内鞘8004的槽8036内。调节轴9106可被致动(例如,医生利用手柄部分8008的各个控制构件),以相对于內鞘和外鞘8004、8006以及内部和外部部分9102、9104旋转。突起9130、9132和脊9134位于槽8036内,限制内部和外部部分9102、9104相对于鞘8004旋转。因此,在调节轴旋转时,内部部分9102保持固定,被开槽9136内的锁定构件9128限制轴向运动和被槽8036内的突起9130限制旋转。在调节轴旋转时,外部部分9104被槽8036内的突起9132和脊9134限制旋转,并且螺纹9124与轴9106的内部表面形成的互补螺纹的啮合导致其轴向平移。因此,轴9106的致动可导致外部部分9104相对于内部部分9102轴向移动。在操控装置9100被组装后,可收回內鞘和外鞘8004、8006,以暴露操控装置9100,并且可将假体瓣膜如瓣膜8050负载到操控装置9100中,使得主体8054的近端停靠在固定构件9108的远侧表面,并且圈环8060延伸穿过圈环接收通道9112。然后可使內鞘和外鞘8004、8006延伸越过操控装置9100和其固定的瓣膜8050。内鞘8004可延伸越过瓣膜8050的主体8054,同时可使锚8052延伸穿过内鞘中的槽8036,如上所述。然后可使外鞘延伸越过内鞘和锚8052,也如上所述。在瓣膜8050被负载到鞘8004内的操控装置9100中后,圈环8060穿过通道9112,并且锚8052穿过圈环接收通道9112区域中的槽8036(如图153G最佳显示)。在这种构型下,圈环8060和锚8052可限制内部和外部部分9102、9104相对于内鞘8004旋转。因此,展开瓣膜8050的过程不需要突起9130、9132或脊9134,但其可通过提供额外限制而有所帮助。这些部件还可有助于限制内部和外部部分9102、9104相对于内鞘8004旋转——在瓣膜8050没有被负载到操控装置9100中时,例如,在无瓣膜8050的装置的论证期间或在将瓣膜8050负载到装置8000中的过程中。操控装置9100,通过允许医生在收回外鞘8006后和瓣膜8050从装置8000完全释放前的任何递送阶段控制锚8052的扩张和缩回,可以消除锚扩展器8012的需要。即,在一个实施方式中,图147–151示例的递送顺序可在不使用锚扩展器8012的情况下进行。为使锚8052径向伸展远离系统8000和瓣膜8050的主体8054,医生可致动调节轴9106,致使固定构件9108、9110至相背移动。内部部分9102的远端对主体8054的近端8055施加远侧方向的力,而沿近侧方向移动的外部部分9104的固定构件9110向锚8052的圈环8060施加近侧方向的力。这导致锚8052径向挠曲远离主体8054。为使锚8060至朝向系统8000和主体8054径向向内移动,医生可沿相反方向致动调节轴9106,致使固定构件9108、9110相向移动,因此使锚在其自身弹力下返回邻近主体8054的位置。图154–156示例瓣膜8050从类似于系统8000的系统展开的顺序,该系统包括操控装置9100和中空鼻锥体9122。如图154所示,瓣膜8050被负载在系统8000内,其中主体部分8054位于内鞘8004内,锚8052位于外鞘8006内,并且心房部分8056至少部分位于中空鼻锥体9122内。携带瓣膜8050的系统8000可通过多种递送方式(在有适当改造的情况下,可采用经中隔、经顶点、经股、主动脉或其它方式)被推进至患者天然瓣膜区域,如患者天然二尖瓣。然后可收回外鞘8006,以允许锚8052通过操控装置9100的致动而扩张。在图154显示的构型下,轴9106已被致动,致使外部部分9104相对于内部部分9102近侧移动(图153B),其进而导致锚8052径向扩张远离系统8000和主体8054(如图154所示)。在锚8052径向扩张远离系统8000后,可将系统8000和瓣膜8050推进穿过天然二尖瓣,使得锚8052定位在天然二尖瓣瓣叶与主体8054对立的位置(在A2和P2位置),并且使得心房部分8056定位在患者的左心房内。如图155所示,然后可使鼻锥体9122远侧延伸远离系统8000其余部分和瓣膜8050,从而释放心房部分8056并使其在患者左心房内扩张。如图156所示,然后可将轴9106致动,以使固定构件9108、9110相向而行,使锚返回其邻近内鞘8004的位置(紧靠天然瓣叶)。然后可将内鞘8004近侧收回,直到主体8054完全释放,而圈环8060仍被操控装置9100固定在内鞘8004的远端内,此时,医生可利用操控装置9100按需调整瓣膜8050的最终布置(以类似于上文关于操控装置9000(图152D–152E)描述的方式)。最后,可将内鞘8004完全近侧收回,直到瓣膜8050从系统8000完全释放。近侧收回内鞘8004经过圈环8060可使圈环8060从圈环接收通道9112径向向外扩张,允许假体瓣膜8050呈现其完全扩张的功能尺寸(如图151所示)。基于本文公开的原理可适用多种可能的实施方式,应理解,示例的实施方式仅仅是优选的实例,而不应被用来限制本公开的范围。相反,本发明的范围由所附权利要求限定。因此提出本发明全部在这些权利要求的范围和精神内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1