用于卵巢卵泡生长和成熟的方法与流程
政府支持
本技术在由nationalinstitutesofhealth授予的资助r37-ag012279和f32-ag034809下由美国政府支持完成。美国政府在本技术中具有某些权利。
背景
由小鼠胚胎干细胞(esc)体外形成的卵泡样结构由单一卵母细胞样细胞组成,其可以生长至直径70µm大小,由一层或多层紧密附着的体细胞所环绕。与在卵巢内正常卵泡形成过程中所观察到的类似,esc来源的卵泡样结构内的体细胞经胞间桥与其封闭的生殖细胞连接,其可以用于促进正常卵泡发育所需的细胞与细胞的相互作用。
概述
在一方面,本技术提供促进个体中哺乳动物卵母细胞的生长和成熟的方法。所述方法包括:将哺乳动物多能细胞工程改造以包含颗粒细胞特异性报告分子,其中所述颗粒细胞特异性报告分子的表达指示作为颗粒细胞或颗粒细胞前体细胞的细胞,将哺乳动物多能细胞在适合于所述多能细胞分化为颗粒细胞或颗粒细胞前体细胞的条件下体外培养,基于颗粒细胞特异性报告分子的表达分离颗粒细胞或颗粒细胞前体细胞经富集的群,并将颗粒细胞或颗粒细胞前体细胞经富集的群与哺乳动物卵巢组织接触,其中所述哺乳动物卵巢组织包含卵泡和/或不成熟卵母细胞,其中颗粒细胞或颗粒细胞前体细胞促进卵泡和/或不成熟卵母细胞的生长和成熟。
在一些实施方案中,颗粒细胞或颗粒细胞前体细胞的群和哺乳动物卵巢组织是自体的。
在一些实施方案中,哺乳动物卵巢组织是人的。
在一些实施方案中,颗粒细胞特异性报告分子包括在卵巢颗粒细胞特异性基因控制下的荧光报告分子。
在一些实施方案中,卵巢颗粒细胞特异性基因选自:叉头框l2(foxl2)、无翼型mmtv整合位点家族成员4(wnt4)、nr5a1、dax-1、atp-结合盒亚家族9(abca9)、乙酰辅酶a酰基转移酶2(线粒体3-氧代酰基-辅酶a硫解酶;acaa2)、肌动蛋白α2(平滑肌、主动脉)(acta2)、具有1型凝血酶基序的解整联蛋白样和金属肽酶(reprolysin样)17(adamts17)、adamts-样2(adamtsl2)、af4/fmr2家族成员1(aff1)、表达序列ai314831(ai314831)、醛酮还原酶家族1成员c14(akr1c14)、醛酮还原酶家族1、notch2以及成员c样(akr1cl)。
在一些实施方案中,荧光报告分子选自:dsred、绿色荧光蛋白(gfp)、黄色荧光蛋白(yfp)和橙色荧光蛋白(ofp)。
在一些实施方案中,将颗粒细胞或颗粒细胞前体细胞经富集的群与哺乳动物卵巢组织接触先体外后体内(exvivo)进行。在一些实施方案中,将颗粒细胞或颗粒细胞前体细胞经富集的群与哺乳动物卵巢组织接触体内(invivo)进行。
在一些实施方案中,哺乳动物多能细胞选自:胚胎干细胞(esc)、诱导多能干细胞(ipsc)、骨髓来源的细胞和外周血来源的细胞。
在另一方面,本技术提供在有需要的个体中提高一种或多种甾体激素水平的方法。所述方法包括:将多个哺乳动物多能细胞工程改造以包含颗粒细胞特异性报告分子,其中所述颗粒细胞特异性报告分子的表达指示作为颗粒细胞或颗粒细胞前体的细胞,将多个哺乳动物多能细胞在适合于所述哺乳动物多能细胞分化为颗粒细胞或颗粒细胞前体细胞的条件下体外培养,基于颗粒细胞特异性报告分子的表达分离颗粒细胞或颗粒细胞前体细胞经富集的群,并将有效量的颗粒细胞或颗粒细胞前体细胞经富集的群施用给个体,其中所述颗粒细胞或颗粒细胞前体细胞分泌一种或多种甾体激素,且其中施用颗粒细胞或颗粒细胞前体细胞经富集的群之后,所述个体相比于施用所述颗粒细胞或颗粒细胞前体细胞经富集的群之前的个体展示出一种或多种甾体激素的水平升高。
在一些实施方案中,所述方法还包括刺激颗粒细胞或颗粒细胞前体细胞以分泌甾体激素。
在一些实施方案中,甾体激素选自:雌二醇、雌三醇、雌酮、孕烯醇酮和黄体酮。
在一些实施方案中,通过卵泡刺激激素(fsh)、8-溴腺苷3′,5′-环单磷酸(8-br-camp)和黄体化激素(lh)刺激颗粒细胞或颗粒细胞前体细胞以分泌甾体激素。
在一些实施方案中,颗粒细胞或颗粒细胞前体细胞的群对于个体是自体的。
在一些实施方案中,个体是人。
在一些实施方案中,颗粒细胞特异性报告分子包括在卵巢颗粒细胞特异性基因控制下的荧光报告分子。
在一些实施方案中,卵巢颗粒细胞特异性基因选自:叉头框l2(foxl2)、无翼型mmtv整合位点家族成员4(wnt4)、nr5a1、dax-1、atp-结合盒亚家族9(abca9)、乙酰辅酶a酰基转移酶2(线粒体3-氧代酰基-辅酶a硫解酶;acaa2)、肌动蛋白α2(平滑肌、主动脉)(acta2)、具有1型凝血酶基序的解整联蛋白样和金属肽酶(reprolysin样)17(adamts17)、adamts-样2(adamtsl2)、af4/fmr2家族成员1(aff1)、表达序列ai314831(ai314831)、醛酮还原酶家族1成员c14(akr1c14)、醛酮还原酶家族1、notch2以及成员c样(akr1cl)。
在一些实施方案中,荧光报告分子选自:dsred、绿色荧光蛋白(gfp)、黄色荧光蛋白(yfp)和橙色荧光蛋白(ofp)。
在一些实施方案中,在施用前刺激颗粒细胞或颗粒细胞前体细胞。在一些实施方案中,在施用后刺激颗粒细胞或颗粒细胞前体细胞。
在一些实施方案中,哺乳动物多能细胞选自:胚胎干细胞(esc)、诱导多能干细胞(ipsc)或其他重编程体细胞、骨髓来源的细胞和外周血来源的细胞。
在一些实施方案中,个体具有降低的甾体激素分泌或缺乏甾体激素分泌。在一些实施方案中,降低的甾体激素分泌或缺乏甾体激素分泌是由于选自以下的病况:绝经、卵巢切除术、子宫切除术、卵巢早衰、原发性卵巢功能不全、化疗诱发的卵巢衰竭、特纳氏综合征。
附图简述
图1a是显示具有绿色荧光蛋白(gfp)的生殖细胞谱系表达的未分化的小鼠tgog2esc系的图像。
图1b是显示分化后3天具有gfp的生殖细胞谱系表达的tgog2esc系的图像。
图1c是显示分化后7天具有gfp的生殖细胞谱系表达的tgog2esc系的图像。
图1d是显示分化后10天具有gfp的生殖细胞谱系表达的tgog2esc系的图像。
图1e是显示分化后26天具有gfp的生殖细胞谱系表达的tgog2esc系的图像。
图2a是显示在分化esc中但不在未分化细胞中(第0天)的foxl2表达的图像。β-肌动蛋白,样品上样的阳性pcr对照基因;-rt,缺少逆转录酶的rna样品。
图2b是显示人(h)foxl2和小鼠(m)foxl2基因启动子的保守元件的图。
图2c是显示用foxl2-dsred构建体转染后,dsred在小鼠颗粒细胞中但不在293细胞中表达的图像。
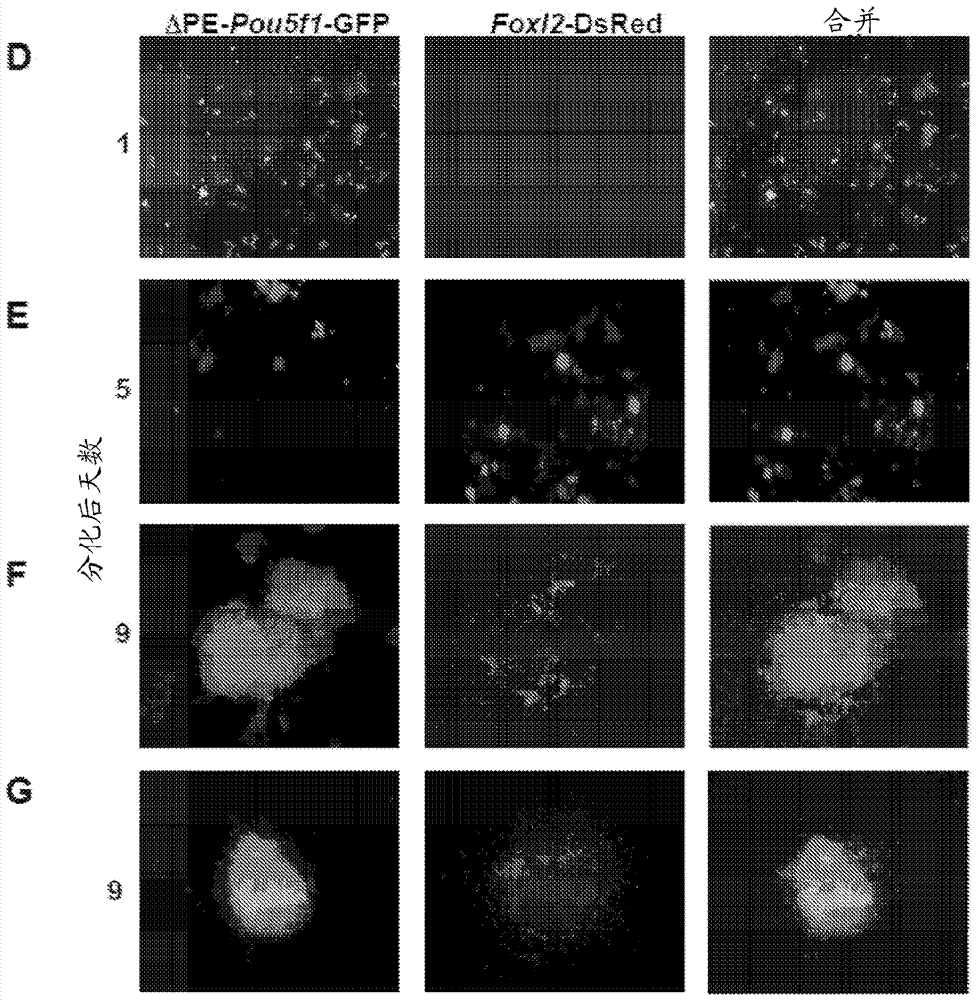
图2d为显示在共表达foxl2-dsred的tgog2escs的分化起始的第一天存在gfp表达且不存在dsred表达的图像。
图2e为显示共表达foxl2-dsred的tgog2escs的分化起始导致gfp表达的逐渐丧失(第1-5天),且在分化起始后5天检测到最低gfp,但在分化起始后5天观察到dsred的图像。
图2f-2g为显示分化起始后9天gfp信号重新出现且表达foxl2-dsred的细胞几乎排他地与表达gfp的细胞簇共定位的图像。
图3a为显示表达dsred的细胞在分化第5天是可检测的且可以通过facs分离(阴性,缺少foxl2-dsred的tgog2ecs的平行排序)的图像。
图3b为显示在分化的指示日时通过facs分离的表达foxl2-dsred的细胞中的早期颗粒细胞标志物的表达(-rt,缺少逆转录酶的rna样品;β-肌动蛋白,用于样品上样的阳性pcr对照基因)的图像。
图4a为显示在16天时共表达foxl2-dsred的tgog2escs的培养物中形成的卵泡样结构的图像。△pe-pou5f1-驱动的gfp表达在由多个表达foxl2-dsred的细胞所环绕的单一大细胞中可检测到。
图4b为显示在40天时共表达foxl2-dsred的tgog2escs的培养物中形成的卵泡样结构的图像。△pe-pou5f1-驱动的gfp表达在由多个表达foxl2-dsred的细胞所环绕的单一大细胞中可检测到。
图4c为显示分化16天后用foxl2-dsred转导的在由v6.5esc形成的卵泡样结构中可检测到表达dsred的细胞的图像。
图5a为显示分化起始后第10-16天之间从esc培养物中分离的foxl2-dsred阳性细胞表达分化颗粒细胞的标志物(–rt,缺少逆转录酶的rna样品;β-肌动蛋白,用于样品上样的阳性pcr对照基因)的图像。
图5b为显示由培养物中维持的facs-纯化的foxl2-dsred阳性细胞(2x103个细胞/孔)的雌二醇生产持续直至3天(fsh,100ng/ml;8-br-camp,1mm)的图。数据为3次独立培养物的平均值±sem(*,相对于媒介物对照p<0.05)。
图5b为显示由培养物中维持的facs-纯化的foxl2-dsred阳性细胞(2x103个细胞/孔)的黄体酮生产持续直至3天(fsh,100ng/ml;8-br-camp,1mm)的图。数据为3次独立培养物的平均值±sem(*,相对于媒介物对照p<0.05)。
图6a为显示分化后12天从esc培养物分离的表达foxl2-dsred的细胞注射前的野生型新生卵巢的图像。
图6b为显示分化后12天从esc培养物分离的表达foxl2-dsred的细胞注射后的野生型新生卵巢的图像。
图6c为显示移植后8天时卵巢间质内存在表达dsred的细胞(左);通过双免疫荧光,这些细胞经常伴随不成熟卵母细胞,其通过卵母细胞标志物dazl表达所鉴定(绿色;右图)的图像。
图6d为显示表达dsred的细胞仅在移植后14天时生长的卵泡的颗粒细胞层中发现的图像。
详细描述
上文引入的且在下文中更详尽地讨论的多个概念可以以众多方式中的任何方式来实施,因为所述概念不限于实施的任何具体方式。具体实施和应用的实例提供主要用于说明目的。
如本文所用,除非内容明确另有说明,单数形式“一个(a)”、“一个(an)”和“所述(the)”包括复数指示物。例如,提及“细胞”包括两个或多个细胞的组合,等等。
如本文所用,“约”将由本领域普通技术人员所理解且将取决于其所用的上下文而在一些程度内变化。如果存在该术语的使用对于本领域普通技术人员不清楚,根据其所使用的上下文,“约”将意指直至具体术语的加减10%。
如本文所用,向个体“施用”药剂、药物、化合物或细胞包括向个体引入或递送药剂、药物、化合物或细胞以行使其旨在的功能的任何途径。施用可以通过任何合适的途径来进行,例如,局部注射(例如,导管施用或直接卵巢内注射)、全身注射、静脉内注射、子宫内注射、口服、鼻内和肠胃外施用。施用包括自施用和由另一位施用。
如本文所用,“分化”指谱系定型(lineagecommitment)的发育过程。“谱系”指细胞发育的途径,其中前体或“祖先”细胞经历渐进的生理变化以成为具有特征性功能的特定细胞类型(例如,神经细胞、肌肉细胞或颗粒细胞)。分化在多个阶段发生,其中细胞逐渐变得更为特定直至它们变得完全成熟,这也称为“终末分化”。“终末分化的细胞”是已经变为特定谱系且已经达到分化的末期的细胞(即已经完全成熟的细胞)。卵母细胞是终末分化细胞类型的实例。
如本文所用,术语“富集的群”指颗粒细胞或颗粒细胞前体细胞的纯化的或半纯化的群。在一些实施方案中,颗粒细胞或颗粒细胞前体细胞的特定群通过从分化的多能细胞的群中分选颗粒细胞或颗粒细胞前体细胞来富集,例如,这通过荧光激活细胞分选术(facs)、磁力辅助的细胞分选(macs)、或本领域中已知的用于从细胞的一般群体中分离特定的细胞群的其他细胞纯化策略。例如但不限于,在一些实施方案中,颗粒细胞或颗粒细胞前体细胞经富集的群是已经通过facs从分化的多能细胞中分离的颗粒细胞或颗粒细胞前体细胞的纯化或半纯化的群。
如本文所用,术语“有效量”或“治疗有效量”指足以实现期望的作用的量,例如,将在有需要的个体中升高甾体激素水平的颗粒细胞的量。例如但不限于,在一些实施方案中,治疗有效量的颗粒细胞是相比于正常个体的甾体激素水平升高个体的甾体激素水平所需的颗粒细胞的量。在激素治疗应用的上下文中,在一些实施方案中,施用于个体的颗粒细胞或颗粒细胞前体细胞的量将取决于个体的病况或疾病状态,例如,更年期个体或已经进行子宫切除的个体,并取决于个体的特征,诸如一般健康、年龄、性别、体重和对药物的耐受。技术人员将能够根据这些和其他因素确定合适的剂量。
如本文所用,“卵泡”指由被体(不具有或具有膜-间质的粒层细胞)细胞所环绕的单一卵母细胞组成的卵巢结构。生殖腺的体细胞包围各个卵母细胞以形成卵泡。每一完全形成的卵泡包围在完整的基膜中。尽管这些新形成的卵泡中的一些几乎立即开始生长,但它们中的大多数保持静止状态直至它们退化或一些信号活化它们进入生长期。
如本文所用,术语“未成熟的卵母细胞”指停止在前期i的初级卵母细胞。
如本文所用,术语“成熟的卵泡”指具有环绕发育中的卵母细胞的活跃增殖的颗粒细胞的卵泡,所述发育中的卵母细胞响应于外源激素。例如但不限于,成熟或正在成熟的卵泡大小增加,这是由于颗粒细胞的增殖、减数分裂恢复后卵母细胞的膨大以及由于充满流体的腔的发育。
如本文所用,术语“成熟卵母细胞”指精子穿入或通过添加钙离子载体激活单性生殖后停滞在减数分裂的中期ii的能够受精的卵母细胞。
如本文所用,术语“刺激剂”指刺激颗粒细胞或颗粒细胞前体细胞以分泌甾体激素例如雌二醇或黄体酮的任何化合物、激素、钛、药物或其他试剂。例如但不限于,在一些实施方案中,刺激剂包括但不限于卵泡刺激激素(fsh)和8-溴腺苷3′,5′-环单磷酸(8-br-camp)。
一般背景
已经从起始衍生自小鼠esc或诱导的多能干细胞(ipsc)的卵母细胞生成了完全功能化的卵细胞。hayashi等人,science,338:971-975(2012)。来自分化中的小鼠esc或ipsc的原始生殖细胞(pgc)样细胞(pgclc)的特化体外遵循精确的时间框架。pgclc在3-6天之间形成并分化为esc或ipsc,其非常类似于胎龄12.5(e12.5)小鼠卵巢中存在的内源pgc。在一项研究中,将具有分散e12.5卵巢组织的esc分化起始后3、4和6天特化的体外来源的pgclc作为聚集体在成年雌性小鼠的卵巢囊(ovarianbursalsacs)下移植。hayashi等人,science,338:971-975(2012)。pgclc随后发育为胚泡阶段的卵母细胞。收获和体外成熟后,卵母细胞经历体外受精。胚胎发生后,将胚移植入受体雌性且它们发育为活的后代。其他研究已成功使用从成人卵巢纯化的女性生殖细胞或卵原细胞干细胞来产生有受精能力的卵细胞。zou等人,natcellbiol.,11:631-636(2009),zhang等人,jmolcellbiol.,3:132-141(2011),和white等人,natmed.,18:413-421(2012)。
这些研究证实小鼠esc和ipsc可以实际上分化(尽管以低频率)为能够受精和胚胎发生的卵母细胞。这些研究还证实pgclc(其在胎儿性腺中类似于内源pgc)需要与发育匹配的胚胎卵巢体细胞相互作用以实现其全部体内效力。为了提供卵发生、卵泡形成和最终从pgclc形成卵细胞所需的微环境因素(cues),需要发育匹配的卵巢体细胞来源。
由小鼠esc体外形成的卵泡样结构由单一卵母细胞样细胞组成,其可以生长至直径70µm大小,由一层或多层紧密附着的体细胞所环绕。与在卵巢内正常卵泡形成过程中所观察到的类似,esc来源的卵泡样结构内的体细胞经胞间桥与其封闭的生殖细胞连接,其可以用于促进正常卵泡发育所需的细胞与细胞的相互作用。此外,甾体产生途径基因的表达增加伴随雌激素分泌至培养基中,与从esc体外形成卵泡样结构一起发生。尽管这些观察结果共同地支持这一论断,即体外来源的卵泡样结构的体细胞具有与内源颗粒细胞在超结构和功能上相似的特征,但从分化中的esc分离并表征这些细胞尚很困难。
总体上,本技术涉及施用来源于多能细胞的经富集的分离的颗粒细胞促进卵腺体的形成和生长和/或促进卵母细胞成熟的方法。另外,本技术还涉及通过施用来源于多能细胞的经富集的分离的颗粒细胞用于增加个体中甾体激素水平的方法。
用于从多能细胞分离颗粒细胞或颗粒细胞前体细胞的方法
在一些实施方案中,本技术涉及从多能细胞鉴定和分离颗粒细胞或颗粒细胞前体细胞。
在一些实施方案中,多能细胞被工程改造以包含至少一种颗粒细胞特异性基因报告分子,其中所述颗粒细胞特异性基因报告分子的表达指示作为颗粒细胞或颗粒细胞前体细胞的细胞。
多能细胞包括但不限于胚胎干细胞(esc)、多能干细胞、诱导的多能干细胞(ipsc)或其他重编程的体细胞、骨髓来源的细胞、外周血来源的细胞。
多能细胞可以是任何哺乳动物多能细胞。多能细胞可以来源于的哺乳动物包括例如家畜,诸如绵羊、猪、牛和马;宠物动物,诸如犬和猫;实验室动物,诸如大鼠、小鼠、猴和兔。在一些实施方案中,哺乳动物是人。
在一些实施方案中,颗粒细胞特异性报告分子包括在卵巢颗粒细胞特异性基因的调节控制下的荧光报告分子。卵巢颗粒细胞特异性基因包括但不限于:叉头框l2(foxl2)、无翼型mmtv整合位点家族成员4(wnt4)、nr5a1、dax-1、atp-结合盒亚家族9(abca9)、乙酰辅酶a酰基转移酶2(线粒体3-氧代酰基-辅酶a硫解酶;acaa2)、肌动蛋白α2(平滑肌、主动脉)(acta2)、具有1型凝血酶基序的解整联蛋白样和金属肽酶(reprolysin样)17(adamts17)、adamts-样2(adamtsl2)、af4/fmr2家族成员1(aff1)、表达序列ai314831(ai314831)、醛酮还原酶家族1成员c14(akr1c14)、醛酮还原酶家族1、notch2、和成员c样(akr1cl)。荧光报告分子包括但不限于:海葵种(discosomasp.)红(dsred)、绿色荧光蛋白(gfp)、黄色荧光蛋白(yfp)和橙色荧光蛋白(ofp)。
在一些实施方案中,颗粒细胞特异性报告分子是在卵巢颗粒细胞特异性基因的调节控制下的非荧光报告分子。非荧光报告分子包括但不限于萤光素酶和β半乳糖苷酶。
颗粒细胞特异性报告分子可以通过本领域已知的任何方法来工程改造。例如但不限于,在一些实施方案中,颗粒细胞特异性报告分子通过如下工程改造:鉴定颗粒细胞特异性基因启动子,确定基因启动子的保守区,使用pcr从基因组dna分离保守区并将保守区克隆入含有荧光标志物的载体。
将多能细胞功能化以包含颗粒细胞特异性基因报告分子可以通过本领域已知的任何方法来完成。例如但不限于,在一些实施方案中,将颗粒细胞特异性基因报告分子通过施用电穿孔插入多能细胞中。其他插入颗粒细胞特异性基因报告分子的方法包括但不限于病毒转导、阳离子脂质体转染、基于多组分脂质的转染、磷酸钙、deae-葡聚糖和直接递送。
包含颗粒细胞特异性基因报告分子的多能细胞可以通过本领域已知的任何选择方法来选择。用于细胞选择的方法的实例包括但不限于荧光激活细胞分选术(facs)、差速贴壁、选择前体细胞或祖先细胞用于克隆扩增和选择抗生素抗性。
将包含颗粒细胞特异性基因报告分子的多能细胞群在适合于哺乳动物多能细胞分化为颗粒细胞或颗粒细胞前体细胞的条件下进行培养。可以通过本领域中常用的任何方法诱导多能细胞。例如但不限于,在有丝分裂无活性的小鼠胚胎成纤维细胞(mef)饲养层上培养的包含颗粒细胞特异性基因报告分子的未分化的esc如下来诱导分化:通过差速贴壁从mef中分离esc并将esc用15%fbs在不存在lif的情况下在明胶包被的板上以单层进行培养。分化的其他方法包括但不限于通过在悬滴中拟胚体形成的诱导。
在一些实施方案中,颗粒细胞特化的信号传导途径的生长因子或激活物被用于指导多能细胞分化为颗粒细胞或颗粒细胞前体细胞。颗粒细胞特化的信号传导途径的生长因子或激活物包括但不限于bfgf或notch信号传导途径的激活物例如jagged1或jagged2。
诱导多能细胞群的分化后,鉴定并分离颗粒细胞或颗粒细胞前体细胞。在一些实施方案中,通过在颗粒细胞特异性基因的控制下表达荧光来鉴定颗粒细胞或颗粒细胞前体细胞。在一些实施方案中,通过facs、基于抗体的免疫磁力分选(例如,磁力辅助的细胞分选(macs))、差速贴壁、克隆选择和扩增、或抗生素抗性将颗粒细胞或颗粒细胞前体细胞分离入颗粒细胞或颗粒细胞前体细胞的经富集的群中。
在一些实施方案中,使用对于颗粒细胞或颗粒细胞前体细胞选择性的或特异性的细胞表面标志物来分离颗粒细胞或颗粒细胞前体细胞。对于颗粒细胞或颗粒细胞前体细胞选择性的或特异性的细胞表面标志物包括但不限于抗mullarian激素受体和notch受体(notch2)。
卵巢组织中卵泡和不成熟卵母细胞的生长和成熟的方法
在一些实施方案中,使用颗粒细胞或颗粒细胞前体细胞经富集的群来促进卵巢组织中卵泡、卵泡样结构和/或未成熟卵母细胞的生长和成熟。
在一些实施方案中,将卵巢组织与颗粒细胞或颗粒细胞前体细胞经富集的群接触,其中颗粒细胞或颗粒细胞前体细胞促进卵巢组织中卵泡、卵泡样结构和/或未成熟卵母细胞的生长和成熟。在一些实施方案中,与卵巢组织接触后,颗粒细胞或颗粒细胞前体细胞迁移至卵巢组织中的卵泡、卵泡样结构和/或未成熟卵母细胞或卵母细胞前体细胞以产生或富集诱导卵泡和未成熟卵母细胞成熟的卵巢体细胞环境。
在一些实施方案中,将卵巢组织与颗粒细胞或颗粒细胞前体细胞经富集的群体内接触。在一些实施方案中,体内施用包括但不限于局部注射(例如导管施用或直接卵巢内注射)、全身注射、静脉内注射、子宫内注射和肠胃外施用。
在一些实施方案中,将卵巢组织与颗粒细胞或颗粒细胞前体细胞经富集的群先体外后体内接触。在一些实施方案中,先体外后体内接触包括但不限于卵巢组织的直接注射、与完整或离解的卵巢组织的聚集、和与卵巢组织共培养。在一些实施方案中,将先体外后体内接触的卵巢组织进行培养并且随后移植或植入个体的卵巢或周围组织中。用于移植或植入的方法包括但不限于移植到卵巢上、卵巢切开后注射或移植组织至卵巢内、和移植到输卵管内。
在一些实施方案中,将先体外后体内接触的卵巢组织进行培养随后在卵泡和/或卵母细胞生长和成熟后冷冻并储存。
卵巢组织可以是任何哺乳动物卵巢组织。卵巢组织可以来源于的哺乳动物包括例如家畜,诸如绵羊、猪、牛和马;宠物动物,诸如犬和猫;实验室动物,诸如大鼠、小鼠、猴和兔。在一些实施方案中,哺乳动物是人。
在一些实施方案中,颗粒细胞或颗粒细胞前体细胞经富集的群和卵巢组织是自体的。在一些实施方案中,颗粒细胞或颗粒细胞前体细胞经富集的群和卵巢组织是异源同种异体的。
在一些实施方案中,通过颗粒细胞或颗粒细胞前体细胞在卵巢组织中促进卵泡、卵泡样结构和/或未成熟卵母细胞或卵母细胞前体细胞的生长和成熟通过以下来测量:卵泡直径的增加、颗粒细胞数目的增加、甾体激素产生的增加、卵母细胞直径的增加或其组合。
成熟卵泡或卵母细胞的直径在物种之间有所不同且可以由本领域技术人员所鉴定,因为特定物种的成熟卵泡大小是本领域众所周知的。例如但不限于,在一些实施方案中,指示成熟或成熟中的卵泡的人卵泡的卵泡直径为大于约30μm的直径。可选地,或另外地,指示成熟或成熟中的卵泡的人卵泡的卵泡直径为这样的直径:约30μm-10,000μm、约50μm-5000μm、约100μm-2000μm、约200μm-1000μm、约300μm-900μm、约400μm-800μm或约500μm-700μm。
例如但不限于,在一些实施方案中,指示成熟或成熟中的卵母细胞的人卵母细胞的卵母细胞直径为大于约10μm的直径。可选地,或另外地,指示成熟或成熟中的卵母细胞的人卵泡的卵泡直径为这样的直径:约10μm-200μm、或约20μm-175μm、或约30μm-150μm、或约40μm-125μm、或约50μm-100μm、或约60μm-75μm。
在一些实施方案中,卵巢组织中颗粒细胞数目的增加通过将与颗粒细胞或颗粒细胞前体细胞接触之前卵巢组织中颗粒细胞的数目和与颗粒细胞或颗粒细胞前体细胞接触后卵巢组织中颗粒细胞的数目进行比较来测量。可选地或另外地,卵巢组织中颗粒细胞数目的增加通过将与颗粒细胞或颗粒细胞前体细胞接触之后卵巢组织中颗粒细胞的数目和未与颗粒细胞或颗粒细胞前体细胞接触的年龄匹配的卵巢组织进行比较来测量。
在一些实施方案中,将与颗粒细胞或颗粒细胞前体细胞接触的卵巢组织中颗粒细胞数目的增加测量为约1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%的百分比增加或者这些值的任意两个与例如与颗粒细胞或颗粒细胞前体细胞接触前的卵巢组织或未与颗粒细胞或颗粒细胞前体细胞接触的年龄匹配的卵巢组织比较时的百分比增加。
通过将颗粒细胞或颗粒细胞前体细胞与卵巢组织接触产生的甾体激素包括但不限于雌二醇、雌三醇、雌酮、孕烯醇酮和黄体酮。在一些实施方案中,将与颗粒细胞或颗粒细胞前体细胞接触的卵巢组织中产生的甾体激素的增加测量为约1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%的百分比增加或者这些值的任意两个与例如与颗粒细胞或颗粒细胞前体细胞接触前的卵巢组织或未与颗粒细胞或颗粒细胞前体细胞接触的年龄匹配的卵巢组织比较时的百分比增加。
用于增加个体中甾体激素的方法
在一些实施方案中,向个体施用有效量的颗粒细胞或颗粒细胞前体细胞经富集的群以增加甾体激素。
在一些实施方案中,颗粒细胞或颗粒细胞前体细胞分泌甾体激素。可选地或另外地,在一些实施方案中,通过刺激剂对颗粒细胞或颗粒细胞前体细胞进行刺激以分泌甾体激素。
由颗粒细胞或颗粒细胞前体细胞分泌的甾体激素包括但不限于雌二醇、雌三醇、雌酮、孕烯醇酮和黄体酮。
刺激剂包括但不限于:卵泡刺激激素(fsh)、8-溴腺苷3′,5′-环单磷酸(8-br-camp)和黄体化激素(lh)。
在一些实施方案中,颗粒细胞或颗粒细胞前体细胞在施用于个体前进行刺激,即颗粒细胞或颗粒细胞前体细胞先体外后体内刺激以分泌甾体激素。在一些实施方案中,颗粒细胞或颗粒细胞前体细胞在施用于个体后进行刺激,即颗粒细胞或颗粒细胞前体细胞体内刺激以分泌甾体激素。
在一些实施方案中,颗粒细胞或颗粒细胞前体细胞经富集的群对于个体是自体的。在一些实施方案中,颗粒细胞或颗粒细胞前体细胞经富集的群对于个体是异源的。
在一些实施方案中,个体具有降低的甾体激素分泌或缺乏甾体激素分泌。在一些实施方案中,降低的甾体激素分泌或缺乏甾体激素分泌是由于绝经、卵巢切除术、子宫切除术、卵巢早衰、原发性卵巢功能不全、化疗诱发的卵巢衰竭、特纳氏综合征。
在一些实施方案中,有需要的个体中甾体激素的增加是基于施用颗粒细胞或颗粒细胞前体细胞前个体中的甾体激素水平与施用颗粒细胞或颗粒细胞前体细胞后个体中的甾体激素水平之间的比较。
在一些实施方案汇总,个体中甾体激素的增加是基于施用颗粒细胞或颗粒细胞前体细胞后个体中的甾体激素水平相比于与被治疗的个体性别和年龄匹配且未施用颗粒细胞或颗粒细胞前体细胞的个体中的甾体激素水平。
在一些实施方案中,将施用颗粒细胞或颗粒细胞前体细胞的个体中产生的甾体激素的增加测量为约1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%的百分比增加或者这些值的任意两个与例如与颗粒细胞或颗粒细胞前体细胞接触前的个体或未施用颗粒细胞或颗粒细胞前体细胞的性别和年龄匹配的个体比较时的百分比增加。
有效量的颗粒细胞或颗粒细胞前体细胞可以在临床前试验和临床试验过程中通过医师和临床医师熟知的方法来测定。可用于本方法中的颗粒细胞或颗粒细胞前体细胞的有效量可以通过众多熟知的用于施用细胞的方法中的任何方法施用于有需要的个体。剂量和/或剂量方案将取决于被治疗的病况的特征,例如个体处于绝经或个体具有子宫切除、个体以及个体的历史。
本领域技术人员已知的用于施用细胞作为治疗的任何方法都可以采用。在一些实施方案中,将颗粒细胞或颗粒细胞前体细胞施用于个体,例如局部注射(例如导管施用或直接卵巢内注射)、全身注射、静脉内注射、子宫内注射和肠胃外施用。例如但不限于,在一些实施方案中,将颗粒细胞或颗粒细胞前体细胞直接注射入卵巢组织或卵巢中。
在一些实施方案中,个体是人。哺乳动物个体包括但不限于家畜,诸如绵羊、猪、牛和马;宠物动物,诸如犬和猫;实验室动物,诸如大鼠、小鼠、猴和兔。在一些实施方案中,哺乳动物是人。
试剂盒
在一些实施方案中,本技术涉及用于产生颗粒细胞或颗粒细胞前体细胞经富集的群的试剂盒。在一些实施方案中,试剂盒包括至少一种颗粒细胞特异性报告分子。
在一些实施方案中,颗粒细胞特异性报告分子包括在卵巢颗粒细胞特异性基因的调节控制下的荧光报告分子。荧光报告分子包括但不限于:海葵种(discosomasp.)红(dsred)、绿色荧光蛋白(gfp)、黄色荧光蛋白(yfp)和橙色荧光蛋白(ofp)。
在一些实施方案中,颗粒细胞特异性报告分子是在卵巢颗粒细胞特异性基因的调节控制下的非荧光报告分子。非荧光报告分子包括但不限于萤光素酶和β半乳糖苷酶。
卵巢颗粒细胞特异性基因包括但不限于:叉头框l2(foxl2)、无翼型mmtv整合位点家族成员4(wnt4)、nr5a1、dax-1、atp-结合盒亚家族9(abca9)、乙酰辅酶a酰基转移酶2(线粒体3-氧代酰基-辅酶a硫解酶;acaa2)、肌动蛋白α2(平滑肌、主动脉)(acta2)、具有1型凝血酶基序的解整联蛋白样和金属肽酶(reprolysin样)17(adamts17)、adamts-样2(adamtsl2)、af4/fmr2家族成员1(aff1)、表达序列ai314831(ai314831)、醛酮还原酶家族1成员c14(akr1c14)、醛酮还原酶家族1、notch2、和成员c样(akr1cl)。
在一些实施方案中,颗粒细胞特异性报告分子在递送载体中。递送载体包括但不限于质粒和病毒载体。
在一些实施方案中,试剂盒包括多个多能细胞。多能细胞包括但不限于胚胎干细胞(esc)、多能干细胞、诱导的多能干细胞(ipsc)或其他重编程的体细胞、骨髓来源的细胞、外周血来源的细胞。
多能细胞可以是任何哺乳动物多能细胞。多能细胞可以来源于的哺乳动物包括例如家畜,诸如绵羊、猪、牛和马;宠物动物,诸如犬和猫;实验室动物,诸如大鼠、小鼠、猴和兔。在一些实施方案中,哺乳动物是人。
在一些实施方案中,试剂盒还包括将颗粒细胞特异性报告分子插入多能细胞中的试剂。在一些实施方案中,试剂盒还包括用于培养多能细胞的试剂。
在一些实施方案中,试剂盒还包括如何使用试剂盒组分以产生颗粒细胞或颗粒细胞前体细胞经富集的群的说明书。例如但不限于,在一些实施方案中,说明书将公开如何将颗粒细胞特异性报告分子插入至多能细胞中,如何诱导多能细胞分化以及如何分离颗粒细胞或颗粒细胞前体细胞。
实施例
本实施例为使用本技术的非限制性实施。
实施例1.分化中esc培养物中的卵泡样结构形成
该实施例显示esc分化导致卵泡样结构的形成。
材料和方法
使用基本上描述于hübner等人,science,300:1251-56(2003)中的标准方法从tgog2(△pe-pou5f1-gfp)转基因雌性小鼠中生成具有绿色荧光蛋白(gfp)的生殖细胞谱系表达的未分化的小鼠xxesc系。
将未分化的tgog2esc维持于补充有15%热失活的esc-级胎牛血清(fbs;invitrogen,carlsbad,ca)、1%丙酮酸钠、1%非必需氨基酸、1%青霉素-链霉素(invitrogen)、103u/ml白血病抑制因子(lif;millipore,billerica,ma)和0.1mmβ-巯基乙醇(sigma-aldrich,st.louis,mo)的dmem中有丝分裂无活性的小鼠胚胎成纤维细胞(mef)饲养层上。对于分化,将esc通过差速贴壁从mef中分离,并用15%fbs在lif不存在的情况下在明胶包被的板上以单层进行培养,如描述于hübner等人,science,300:1251-56(2003)中。
使用nikoneclipsete2000-s倒置荧光显微镜和spot成像软件(diagnosticinstruments,sterlingheights,mi)进行活细胞成像。
结果
在未分化的tgog2esc集落中检测到gfp表达(图1a),而通过去除mef和lif起始分化导致在接下来3-7天上广泛分布的gfp表达的逐渐消失(图1b)。由gfp阳性细胞构成的不同集落的形成发生在起始分化后第7-26天(图1c-1d)。在分化的第16-40天检测到由体细胞环绕的单一大的gfp阳性卵母细胞样细胞组成的卵泡样结构(图1e)。
结果显示esc可以自发地分化为卵泡样结构。
实施例2.颗粒细胞特化和分离
本实施例显示用于追踪和鉴定从esc分化的颗粒细胞的方法。
材料和方法
为了鉴定并追踪分化中的esc培养物中的卵巢体细胞,在分化中的esc培养物中对早期颗粒细胞标志物foxl2的表达进行定位。定位揭示在第5天foxl2基因的激活(图2a)。使用genomevista鉴定出foxl2基因启动子的739bp区域。将该区域从小鼠基因组dna中分离并克隆入pdsred2-1载体(clontech,mountainview,ca,)或含有dsred完整可读框的plenti6慢病毒构建体(gatewaylentiviralsystem;invitrogen),因此产生在foxl2基因启动子控制下的dsred表达载体(图2b)。
使用小鼠颗粒细胞作为阳性对照和293细胞(invitrogen)作为阴性对照验证启动子活性和特异性(图2c)。为了验证foxl2基因启动子驱动的dsred表达,用foxl2-pdsred2-1构建体经电穿孔稳定转染未分化的tgog2esc,随后进行克隆选择和扩展。可选地,分化起始后使用由转染有foxl2-dsred慢病毒构建体(plenti6-foxl2-dsred)的293细胞产生的病毒上清液来病毒转导esc。通过荧光显微镜分析细胞的dsred表达并且通过荧光激活细胞分选术(facs)来分离。
对于facs,通过0.25%胰蛋白酶-edta(分化第10天前)或手工刮取将分化中的esc从板上移除。随后将细胞与800u/ml的iv型胶原酶(worthington,lakewood,nj)保持轻柔分散(gentledispersion)温育15分钟,随后与0.25%胰蛋白酶-edta温育10分钟以获得单细胞悬浮液(分化第10天后)。通过重悬浮在含有0.1%fbs的1x浓度的磷酸缓冲盐水(pbs)并过滤(35-µm孔径)制备用于facs的细胞。使用facsaria流式细胞仪(bdbiosciences,sanjose,ca)分析并分选细胞。
测量来自facs纯化的foxl2-dsred阳性细胞的培养基中的雌二醇和黄体酮浓度,所述foxl2-dsred阳性细胞已经重新铺板并且在存在pbs(媒介物)、100ng/ml卵泡刺激激素(fsh;niddk,nih,bethesda,md)或1mm8-溴腺苷3′,5′-环单磷酸(8-br-camp)(8-br-camp;sigma-aldrich)的情况下培养24、48或72小时。通过在所有培养物中提供热失活的15%fbs(其含有0.92pg/ml雄激素(测试的fbs的56个批次的平均值))而提供芳香化为雌激素所需的雄激素底物。雌二醇elisa来自alpco(salem,nh),且黄体酮elisa来自drginternational(mountainside,nj)。所有测定根据制造商指南进行。
结果
通过去除mef和lif将具有稳定转染的foxl2-dsred载体的未分化的tgog2esc诱导以分化。dsred表达阳性的细胞在第1天不存在(图2d),但最早至分化第5天被观察到(图2e)。到第9天,发现表达dsred的细胞紧密伴随表达gfp的集落(图2f-2g)。显著地,表达dsred的细胞几乎排他地与表达gfp的细胞簇在此时共定位(图2f-2g)。
在分化第5天时通过facs分离dsred阳性细胞的基因表达分析(图3a)揭示与存在早期卵巢颗粒细胞一致的不同的体细胞基因表达(图3b)。检测到的mrna为foxl2、无翼相关的mmtv整合位点4(wnt4)、卵泡抑素(fst)和kit配体(kitl;也称为干细胞因子或scf,或steel因子)。核受体亚家族5组a成员1(nr5a1;也称为甾体生成因子-1或sf-1)的表达在第7天变得可检测到(图3b)。
在分化的第16天,且持续直至第40天,多维卵泡样结构(其每一个由被表达dsred的细胞环绕的单一大(25–50µm)的gfp阳性细胞组成)通过直接荧光而观察到(图4a-4b)。为了确保这些观察结果并非特异于tgog2esc系,用foxl2-dsred转导的v6.5esc在诱导分化至少16天后也形成相同的卵泡样结构,所述卵泡样结构由被表达dsred的体细胞环绕的位于中心的卵母细胞样细胞构成(图4c)。
在分化第10天通过facs分离的表达dsred细胞的基因表达分析揭示存在与分化中的颗粒细胞通常相关联的多种标志物,包括卵泡刺激激素受体(fshr)、抗müllerian激素(amh;也称为müllerian抑制物或mis)、细胞色素p450家族19亚家族多肽1(cyp19a1;也称为芳香化酶)和甾体生成急性调节蛋白(star)(图5a)。分化第12天分离的dsred阳性细胞的亚培养后甾体生成的评估揭示培养基中存在雌二醇或黄体酮(图5b-5c)。另外,用fsh或8-br-camp处理导致雌二醇产量的显著增加,其证实这些细胞中存在功能性fsh受体和与甾体生成相关的camp介导的信号传导。然而,仅8-br-camp能够显著增强黄体酮产生(图5c)。
这些结果显示多能细胞能够分化为颗粒细胞或颗粒细胞前体细胞。另外,结果显示来源于多能细胞的颗粒细胞或颗粒细胞前体细胞能够通过颗粒细胞特异性基因报告分子进行追踪和鉴定,所述报告分子还可以用于分离颗粒细胞或颗粒细胞前体细胞,例如通过facs。因此,包含颗粒细胞特异性基因报告分子的多能细胞可用于追踪和分离颗粒细胞或颗粒细胞前体细胞的群。
实施例3.颗粒细胞的卵巢内移植
该实施例显示来源于多能细胞的颗粒细胞迁移至新生卵巢中的不成熟卵母细胞和发育中的卵泡。
材料和方法
在以下实验中使用了野生型c57bl/6雌性小鼠(charlesriverlaboratories,wilmington,ma,usa)。
表达foxl2-dsred的esc分化12天后,使用facs来分离dsred阳性细胞。对于每一实验,将200-500dsred阳性细胞使用pneumaticpicopump(worldprecisioninstruments,sarasota,fl)微注射入单个新生的(产后第2-4天)野生型小鼠卵巢中(图6a-6b)。随后将经注射的卵巢移植入6周龄的切除卵巢的野生型雌性小鼠的肾被膜下。在移植后8天和2周,移除经移植的卵巢并固定在4%低聚甲醛(pfa)中用于分析。
将固定的卵巢包埋在石蜡中,连续切片,封固在载玻片上并在二甲苯中脱蜡,随后在梯度乙醇系列中水化。抗原修复通过如下进行:将载玻片在柠檬酸钠(ph6.0)中煮沸5min,随后在tnk缓冲液(0.1mtris、0.55mnacl、0.1mmkcl、1%山羊血清、0.5%牛血清白蛋白和0.1%triton-x于pbs中)中封闭,与所需一级抗体(1:100稀释)在4°c温育过夜,并与缀合荧光团(fluor-conjugated)的二级抗体(1:250稀释,alexafluor-488或-568;invitrogen)在20°c下温育1小时。所用的一级抗体为来自serotec(mca2336;raleigh,nc)的小鼠抗dazl抗体和来自abcam(ab62341;cambridge,ma)的兔抗rfp抗体(用于检测dsred)。使用nikoneclipsete2000-s倒置荧光显微镜和spot成像软件(diagnosticinstruments)进行荧光图像分析。
结果
注射从分化后12天的esc培养物中分离的表达foxl2-dsred的细胞之前,野生型新生卵巢没有显示dsred(图6a)。注射从分化后12天的esc培养物中分离的表达foxl2-dsred的细胞之后,野生型新生卵巢显示dsred(图6b)。
在移植后8天,发现表达dsred的细胞分布在整个经注射的卵巢的基质。观察到这些细胞中的许多细胞紧密接近未成熟卵母细胞,如由对dsred和卵母细胞标志物dazl(精子缺乏样中删除的(deletedinazoospermia-like))的双免疫荧光染色所指示的(图6c)。在移植后14天,表达dsred的细胞不再在基质中观察到但排他地在生长中的卵泡的颗粒细胞层内检测到(图6d)。
这些结果显示颗粒细胞和颗粒细胞前体细胞天然迁移至发育中的卵泡或未成熟卵母细胞。因此,多个和一个颗粒细胞可用于促进卵泡、卵泡样结构和未成熟卵母细胞的生长和成熟。
实施例4.促进卵泡或卵泡样结构的生长和成熟的方法
该实施例将显示颗粒细胞促进卵泡和未成熟卵母细胞的生长和成熟。
材料和方法
将年龄和性别匹配的人个体分为两组。一组通过直接向卵巢中注射来施用颗粒细胞,其中所述颗粒细胞如上所述从来自每名个体的多能细胞工程改造,使得颗粒细胞对于每名个体是自体的。第二组(对照)不施用颗粒细胞。
使用本领域已知的方法,移除来自每名个体的卵巢组织样品并通过本领域已知的方法分析以测量卵泡直径和卵母细胞直径。
结果
预期来自用自体颗粒细胞处理的个体的卵巢将具有直径大于30μm的卵泡和/或直径大于10μm的卵母细胞。
这些结果将表明颗粒细胞和/或颗粒细胞前体细胞可用于促进卵泡和未成熟卵母细胞的生长和成熟。
实施例5.增加甾体激素的方法
该实施例将显示向有需要的个体施用颗粒细胞将提高个体中甾体激素的水平。
材料和方法
将年龄和性别匹配的患有化疗诱导的卵巢衰竭的人个体分为两组。一组通过直接向卵巢中注射来施用颗粒细胞,其中所述颗粒细胞如上所述从来自每名个体的多能细胞工程改造,使得颗粒细胞对于每名个体是自体的。第二组(对照)不施用颗粒细胞。
使用本领域已知的方法,将测量每名个体中的雌二醇和黄体酮的水平。
结果
预期施用有自体颗粒细胞的个体将相比于未处理的个体具有升高水平的雌二醇和黄体酮。
这些结果将表明颗粒细胞和/或颗粒细胞前体细胞可用于提高有需要的个体中的甾体激素水平。
等同方案
本技术将不限于本申请中所描述的具体实施方案,所述实施方案旨在作为本技术的各个方面的单个说明。可以进行本技术的许多改变和变化而不背离其精神和范围,如同对于本领域技术人员将是显而易见的。除了列举的那些外,本文本技术范围内的功能等同的方法和设备对于本领域技术人员从前述内容中也将是显而易见的。此类改变和变化旨在落入所附权利要求的范围之内。本技术将不仅仅限于所附的权利要求,连同此类权利要求所赋予的等同方案的全部范围。应理解本技术不限于具体的方法、试剂、化合物组合物或生物系统,这些当然是可以进行改变的。还应理解本文所用的术语仅用于描述具体实施方案的目的,并不旨在是限制性的。
- 还没有人留言评论。精彩留言会获得点赞!