用于治疗下肢脉管系统的设备和方法与流程
通过引用的并入
本申请要求于2015年5月21日提交的美国专利申请第14/718,427号、于2015年3月23日提交的美国临时专利申请第62/136,755号、于2014年9月8日提交的美国临时专利申请第62/047,558号、和于2014年6月19日提交的美国临时专利申请第62/014,554号的优选权权益,每个申请通过引用以其整体并入本文。于2014年2月28日提交的pct专利申请第pct/us2014/019607号、于2008年1月3日提交的美国专利申请第11/662,128号、于2009年2月25日提交并且于2013年5月14日被公布为美国专利申请第8,439,963号的美国专利申请第12/297,498号、和于2013年3月8日提交的美国专利申请第13/791,185号也均通过引用以其整体并入本文。
本申请涉及在经皮介入性手术中使用的方法和系统。具体而言,本申请涉及提供或维持通过身体通道诸如心腔和血管的流体流的方法和系统。
背景技术:
微创经皮手术或“锁孔(key-hole)”手术是其中将外科设备通过在皮肤中切割的小孔口插入患者的体腔的外科技术。这种形式的手术因为其允许患者忍耐较少的手术不适同时保持传统手术的益处已变得越来越流行。这种技术治疗的患者容易受到较低水平的不适、全身麻醉的需要、创伤、和感染的风险,并且其恢复时间相比于传统手术程序可以显著减少。
例如,锁孔手术能够用于腹腔镜手术和用于治疗心血管疾病。在治疗心血管疾病中,球囊血管成形术可以作为心脏直视手术的替代选择用于治疗部分闭塞的冠状动脉,在球囊血管成形术中球囊导管被插入通常靠近患者腹股沟的动脉并被引导至患者的心脏,在心脏中导管远端部分处的球囊被膨胀以使闭塞的脉管变宽或扩大从而帮助恢复血液流动至心脏组织。管状支撑设备(例如,支架)可以在堵塞的部位处部署以防止血管的将来闭塞(再狭窄)或塌缩。例如,支架可以是球囊导管的球囊上携带的可扩张的金属网管,或可以是自扩张的。当球囊膨胀时,球囊可扩张的支架扩张,以便支架推压血管壁。当支架例如通过塑性变形或借助机械锁定机构达到其扩张位置时,支架被布置以保持其扩张形状,从而在血管中形成有弹性的支架或支撑。该支撑结构(例如,支架)支撑血管壁并且使血管壁扩大,以维持血液流过脉管的路径。自扩张支架也是可用的,其通过适当地修改的导管保持在塌缩状态用于运输通过动脉,并且当在堵塞的部位处部署时其采取扩张状态。例如,导管可以包括保持支架在压缩或未扩张状态的保持套。一旦从支架移去或收回该套,支架就扩张以支撑血管壁和使血管壁扩大。
球囊血管成形术例如在急性病例和在冠状动脉完全闭塞的情况下不总是适合的措施。在这些情况下,通常的治疗是采用冠状动脉旁路。冠状动脉旁路手术是开胸程序或心脏直视程序,并且通常涉及将一块健康血管移植在冠状动脉上从而绕过堵塞并且恢复血液流动至冠状组织。健康血管通常是在旁路手术的过程期间自患者的腿或臂获得的静脉。为了进行该程序,患者的心脏必须通过打开胸腔、分离胸骨和切开围绕心脏的心包而被暴露,这导致显著的手术创伤。
传统冠状动脉旁路手术并不总是一个选项。某些患者不适合作为传统冠状动脉旁路手术的候选人,这是由于来自因手术造成的重大创伤的恢复低预期或高风险、感染的高风险、用作旁路移植的健康脉管的缺乏、显著的共发病和与开胸手术相关联的预期长的且复杂的恢复时间。例如,诸如糖尿病、年龄、肥胖和吸烟的因素可以排除真正需要这种治疗的一部分候选患者。
技术实现要素:
本申请提供了用于克服某些缺陷和/或改善经皮方法和系统的方法和系统。例如,根据数个实施例,本文描述的方法和系统可以改善治疗施用的靶向和定位,其可以有利地经由经皮技术对不适合更侵入性手术的患者提供治疗。本文描述的某些实施例可以通过使用微创性的经皮手术技术创建旁路在通道诸如冠状和/或外周血管中提供流体流。
在一些实施例中,一种低孔隙度假体可植入在第一脉管和第二脉管之间的瘘中,以通过将血流从第一脉管转向到第二脉管来治疗第一脉管中的闭塞。该假体包含以下元件或替代地实质上由元件以下组成:多个细丝,其被织造在一起成为织造结构;近端;远端;在近端和远端之间的侧壁;由侧壁限定的内腔;第一纵向区段,其被配置为锚定在第一脉管中;第二纵向区段,其被配置为锚定在第二脉管中;和在第一纵向区段和第二纵向区段之间的第三纵向区段。第一纵向区段是柱形,并且具有第一直径。第二纵向区段是截头锥形,并且逐渐过渡到大于第一直径的第二直径。第一纵向区段和第二纵向区段中的至少一个具有被配置为导向血流通过假体的内腔而不灌注通过假体的侧壁的孔隙度。
在一些实施例中,一种使瓣膜关闭不全的方法包含以下步骤或替代地实质上由以下步骤组成:在第一脉管和第二脉管之间形成瘘。第一脉管可以是动脉。第二脉管可以是静脉。形成瘘包含将第一导管插入第一脉管。第一导管包含超声发出换能器和被配置为从第一导管径向延伸的针。形成瘘进一步包含将第二导管插入第二脉管。第二导管包含超声接收换能器。形成瘘进一步包含从超声发出换能器发出超声信号,并且在超声信号被超声接收换能器接收之后,从第一导管延伸针。延伸针包含,离开第一脉管,横穿第一脉管和第二脉管之间的间质组织,并且进入第二脉管。该方法进一步包含将假体至少部分地部署在瘘中。在部署可植入假体之后,血液通过假体从第一脉管被转向到第二脉管。该方法进一步包含,使第二脉管中的瓣膜关闭不全。使第二脉管中的瓣膜关闭不全包含利用反向瓣膜刀切割瓣膜,并且利用支架填充第二脉管。
支架可以包含覆盖物或移植物。填充第二脉管可以包含覆盖第二脉管的侧副管(collateralvessel)。支架可以与假体分开。支架可以沿着第二脉管的长度与假体间隔开。支架可以与假体一体。
在一些实施例中,一种使瓣膜关闭不全的方法包含以下步骤或替代地实质上由以下步骤组成:在第一脉管和第二脉管之间形成瘘。形成瘘包含将导管插入脉管。第一导管包含被配置为从第一导管径向延伸的针。形成瘘进一步包含从第一导管延伸针。延伸针包含,离开第一脉管,横穿第一脉管和第二脉管之间的间质组织,并且进入第二脉管。该方法进一步包含将假体至少部分地部署在第一脉管和第二脉管之间的瘘中。在部署可植入假体之后,血液通过假体从第一脉管被转向到第二脉管。方法进一步包括使第二脉管中的瓣膜关闭不全。使第二脉管中的瓣膜关闭不全包含以下中的至少一个:利用反向瓣膜刀切割瓣膜,膨胀球囊,扩张临时支架和利用可植入支架填充第二脉管。
可植入支架可以包含覆盖物或移植物。填充第二脉管可以包含覆盖第二脉管的侧副管。可植入支架可以与假体分开。可植入支架可以与假体一体。第一导管可以包含超声发出换能器。形成瘘可以包含将第二导管插入第二脉管,第二导管包含超声接收换能器,从超声发出换能器发出超声信号,并且在超声信号被超声接收换能器接收之后,从第一导管延伸针。
在一些实施例中,一种使瓣膜关闭不全的方法包含以下步骤或替代地实质上由以下步骤组成:将假体至少部分地部署在第一脉管和第二脉管之间的瘘中。在部署可植入假体之后,血液通过假体从第一脉管被转向到第二脉管。该方法进一步包含使第二脉管中的瓣膜关闭不全。
使第二脉管中的瓣膜关闭不全可以包含,利用反向瓣膜刀切割瓣膜。使第二脉管中的瓣膜关闭不全可以包含用支架填充第二脉管。支架可以包含覆盖物或移植物。填充第二脉管可以包含覆盖第二脉管的侧副管。支架可以与假体分开。支架可以沿着第二脉管的长度与假体间隔开。支架的近侧节段可纵向地重叠假体的远侧节段。支架可以与假体一体。使第二脉管中的瓣膜关闭不全可以包含利用反向瓣膜刀切割瓣膜,并且用支架填充第二脉管。使第二脉管中的瓣膜关闭不全可以包含膨胀球囊和扩张临时支架中的至少一个。使第二脉管中的瓣膜关闭不全可以包含膨胀球囊。使第二脉管中的瓣膜关闭不全可以包含扩张临时支架。
在一些实施例中,一种用于治疗第一脉管中的闭塞的可植入假体包含:多个细丝,其被织造在一起成为织造结构;近端;远端;在近端和远端之间的侧壁;由侧壁限定的内腔;和足以导向流体流通过内腔而不灌注通过侧壁的孔隙度。
孔隙度可以在大约0%和大约50%之间。孔隙度可以在大约5%和大约50%之间。假体可以基本上没有移植物材料。假体可以包含具有所述孔隙度的第一纵向节段和具有与所述孔隙度不同的第二孔隙度的第二纵向节段。第二纵向节段可以具有与第一纵向节段不同的参数。该参数可以包含编织角度、细丝直径、细丝材料、织造结构直径、织造结构形状和补充支撑结构中的至少一个。假体可以进一步包含在第一纵向节段和第二纵向节段之间的第三纵向节段。第三纵向节段可以具有与第一纵向节段和第二纵向节段中的至少一个不同的参数。该参数可以包含编织角度、细丝直径、细丝材料、织造结构直径、织造结构形状和补充支撑结构中的至少一个。假体可以进一步包含补充支撑结构。补充支撑结构可以包含被织造在一起成为第二织造结构的第二多个细丝,第二多个细丝具有与所述多个细丝不同的参数。该参数可以包含编织角度、细丝直径、织造结构直径和细丝材料中的至少一个。补充支撑结构可以包含切割海波管。所述多个细丝可以包含包括形状记忆材料(例如,镍钛诺)的细丝和包括生物相容聚合物(例如,
在一些实施例中,一种用于治疗第一脉管中的闭塞的可植入假体包含:近端;远端;在近端和远端之间的侧壁;由侧壁限定的内腔;第一纵向区段,其被配置为锚定在第一体腔中;第二纵向区段,其被配置为锚定在第二体腔中;和在第一纵向区段和第二纵向区段之间的第三纵向区段。第一纵向区段和第三纵向区段中的至少一个包含足以导向流体流基本通过内腔而不灌注通过侧壁的孔隙度。
孔隙度可以在大约0%和大约50%之间。孔隙度可以在大约5%和大约50%之间。假体可以基本上没有移植物材料。第二纵向节段可以具有与第一纵向节段不同的参数。该参数可以包含编织角度、细丝直径、细丝材料、直径、形状和补充支撑结构中的至少一个。第三纵向节段可以包含与所述孔隙度不同的第二孔隙度。第一纵向节段可以是可扩张球囊。第二纵向节段可以是自扩张的。假体可以包含被织造在一起成为织造结构的多个细丝。所述多个细丝可以包含包括形状记忆材料(例如,镍钛诺)的细丝和包括生物相容聚合物(例如,
在一些实施例中,一种用于治疗第一脉管中的闭塞的可植入假体包含:多个细丝,其被织造在一起成为织造结构;近端;远端;在近端和远端之间的侧壁;由侧壁限定的内腔;和在大约5%和大约50%之间的孔隙度。
所述孔隙度可以被配置为导向流体流基本通过内腔。假体可以包含第一纵向节段和第二纵向节段,第一纵向节段具有所述孔隙度,第二纵向节段具有与所述孔隙度不同的第二孔隙度。
在一些实施例中,一种成套工具包含假体和瘘形成系统。该成套工具可以进一步包含使瓣膜失去能力的设备。在一些实施例中,一种成套工具包含假体和使瓣膜失去能力的设备。该成套工具可以包含包括假体的假体递送系统。在一些实施例中,一种方法包含将假体部署在第一脉管和第二脉管之间的瘘中。使瓣膜失去能力的设备可以包含反向瓣膜刀。使瓣膜失去能力的设备可以包含球囊。使瓣膜失去能力的设备可以包含静脉支架。静脉支架可以包含覆盖物或移植物。静脉支架可以与假体一体。
在一些实施例中,一种将流体流从第一脉管转向到第二脉管的方法包含将假体至少部分地部署在第一脉管和第二脉管之间的瘘中,其中第一脉管包含闭塞。假体包含被织造在一起成为织造结构的多个细丝,所述织造结构包含小于大约50%的孔隙度。在部署可植入假体之后,血液可以通过假体从第一脉管被转向到第二脉管。
第一脉管可以是动脉。脉管通道可以是静脉。该方法可以包含扩大瘘。第一脉管可以基本平行于第二脉管。部署假体可以包含允许假体自扩张。部署假体可以包含球囊扩张假体。部署假体可以包含部署织造结构并且部署补充支撑结构。部署补充支撑结构可以在部署织造结构之前。部署补充支撑结构可以在部署织造结构之后。补充支撑结构可以包含被织造成第二织造结构的第二多个细丝。补充支撑结构可以包含切割海波管。该方法可以进一步包含形成瘘。形成瘘可以包含将发射导管插入第一脉管,并且将目标导管插入第二脉管。发射导管可以包含超声发出换能器和被配置为从发射导管径向延伸的针。目标导管可以包含超声接收换能器。形成瘘可以包含从超声发出换能器发出超声信号,在发出超声信号期间和直到超声信号被超声接收换能器接收,进行以下至少一项:旋转发射导管,和纵向地移动发射导管;和在超声信号被超声接收换能器接收之后,从发射导管延伸针,其中延伸针包含:离开第二脉管,横穿第一脉管和第二脉管之间的间质组织,并且进入第二脉管。该方法可以进一步包含使第二脉管中的瓣膜关闭不全。使第二脉管中的瓣膜关闭不全可以包含利用反向瓣膜刀切割瓣膜。使第二脉管中的瓣膜关闭不全可以包含膨胀球囊。使第二脉管中的瓣膜关闭不全可以包含扩张支架。使第二脉管中的瓣膜关闭不全可以包含用支架填充第二脉管。支架可以包含覆盖物或移植物。填充第二脉管可以包含,覆盖第二脉管的侧副管。支架可以与假体分开。支架可以沿着第二脉管的长度与假体间隔开。支架的末端可以紧靠假体的末端。支架的一部分可以纵向地重叠假体的一部分。支架的该部分可以在假体的该部分的径向内部。该方法可以包含在部署假体之后扩张支架。假体的该部分可以在支架的该部分的径向内部。该方法可以包含在部署假体之前扩张支架。支架可以与假体一体。
在一些实施例中,一种用于维持下肢中的动脉和静脉之间的吻合的开放性的可植入假体包含:被配置为驻留在下肢动脉中的第一区段、被配置为驻留在下肢静脉中的第二区段、和纵向地在第一区段和第二区段之间的第三区段。第三区段被配置为维持动脉和静脉之间的吻合的开放性。
第一区段可以被配置为附着(appose)下肢动脉的壁。第一区段可以包含倒钩。第二区段可以被配置为附着下肢静脉的壁。第二区段可以包含倒钩。第一区段、第二区段和第三区段中的至少一个可以是自扩张的。第一区段、第二区段和第三区段中的至少一个可以是可扩张球囊。第二区段的长度可以大于第一区段的长度。第二区段可以被配置为使下肢静脉的瓣膜失去能力。第二区段可以被配置为覆盖下肢静脉的侧副管。
在一些实施例中,一种将流体流从下肢中的第一脉管转向到第二脉管的方法包含在第一脉管和第二脉管之间形成孔口,并且扩张孔口以形成吻合。
形成孔口可以包含将线材(wire)从第一血管推动到第二血管内。形成孔口可以包含将针从第一血管横穿入第二血管。扩张孔口可以包含利用至少一个球囊扩大孔口。扩大孔口可以包含利用具有逐渐更大直径的多个球囊。多个球囊中的第一个球囊可以具有约1.5mm的直径,并且其中多个球囊中的最后一个球囊可以具有约3mm的直径。多个球囊可以包含具有约1.5mm的直径的第一球囊、具有约2.0mm的直径的第二球囊、具有约2.5mm的直径的第三球囊、和具有约3.0mm的直径的第三球囊。利用多个球囊扩大孔口可以包含利用逐渐更大的球囊膨胀压力。该方法可以不包括(例如,没有或免于)放置假体(例如,而不使用支架、移植物、支撑架、或其他假体)。第一脉管和第二脉管的位置通过围绕第一脉管和第二脉管的解剖结构被维持。该方法可以进一步包含将假体放置在吻合中。将假体放置在吻合中可以包含将假体锚定在第一脉管和第二脉管中的至少一个中。第一脉管可以包含足底外侧动脉。第二脉管可以包含足底外侧静脉。
以上概括的和下面进一步详细陈述的方法描述了由从业者采取的某些行动;然而,应当理解,它们也可以包括由另一方指示那些行动。因此,行动诸如“使第一脉管中瓣膜关闭不全”包括“指示使第一脉管中瓣膜关闭不全”。
为了总结本发明和可以实现的优点的目的,本文描述了一些目标和优点。不一定需要依据任何具体的实施例实现所有的这些目标和优点。在一些实施例中,本发明可以以可以实现或优化一个优点或一组优点而不必要实现其他目标或优点的方式体现或者执行。
所有这些实施例意欲处于本文公开的发明的范围内。参考附图,这些和其他实施例从以下详细描述将是显而易见的,本发明不限于(一个或更多个)任何具体的公开的实施例。参考一些实施例描述的任选的和/或优选的特征可以与其他实施例结合并且并入其他实施例中。本文引用的所有参考文献,包括专利和专利申请,以其整体通过引用并入本文。
附图说明
本公开的这些和其他特征、方面和优点参照某些实施例的附图进行描述,所述附图意欲图示某些实施例并不意欲限制本发明,其中相同的参考数字用于相同的特征,并且其中:
图1示意性地图示了将信号从第一体腔导向到第二体腔中的目标设备的发射设备的示例实施例。
图2是沿着图1的虚线b–b的横截面表示。
图3示意性地图示了发射设备的示例实施例。
图4示意性地图示了目标设备的示例实施例。
图5示意性地图示了发射设备的另一示例实施例。
图6示意性地图示了用于发射的定中心设备和/或目标设备的示例实施例。
图7示意性地图示了在诸如动脉-静脉动脉化的程序之后在恰当位置的假体。
图8是提供流体流的设备的示例实施例的侧透视图。
图9示出了用作两个血管之间的分路的图8的设备。
图10是提供流体流的设备的另一示例实施例的侧透视图。
图11是提供流体流的设备的又一示例实施例的侧透视图。
图12是提供流体流的设备的又一示例实施例的侧透视图。
图13是提供流体流的设备的又一示例实施例的侧透视图。
图14a是超声发射导管的示例实施例的示意性侧横截面视图。
图14b是在圆14b内的图14a的超声发射导管的远端部分的放大示意性侧横截面视图。
图15a是超声目标导管的示例实施例的示意性侧视图。
图15b是在圆15b内的图15a的超声目标导管的放大示意性侧横截面视图。
图15c是在圆15c内的图15a的超声目标导管的放大示意性侧横截面视图。
图16是检测导管对准的图的示例实施例。
图17是假体递送系统的示例实施例的示意性侧视图。
图18是假体的示例实施例的示意性侧视图。
图19是假体的另一示例实施例的示意性侧视图。
图20a-图20h示意性地图示了实现逆行灌注的方法的示例实施例。
图21是超声接收换能器的示例实施例的示意性透视图。
图22是超声接收换能器的另一示例实施例的示意性横截面视图。
图23a是瓣膜刀(valvulotome)的示例实施例的示意性透视图。
图23b是反向瓣膜刀的示例实施例的示意性透视图。
图24是lemaitre设备的示例实施例的示意性透视图。
图25a是假体的又一示例实施例的示意性侧视图。
图25b是假体的又一示例实施例的示意性侧视图。
图25c是假体的又一示例实施例的示意性侧视图。
图26a和图26b示意性地图示了用于实现逆行灌注的方法的另一示例实施例。
图27示意性地图示了用于实现逆行灌注的假体和方法的另一示例实施例。
图28a和图28b分别示意性地图示了脚的动脉和静脉。
图29示意性地图示了吻合设备的示例实施例。
图30示意性地图示了被吻合设备耦接的两个血管的示例实施例。
图31a示意性地图示了与静脉支架的示例实施例分开的动静脉瘘支架(fistulastent)的示例实施例。
图31b示意性地图示了包含集成的静脉支架的动静脉瘘支架的示例实施例。
图31c示意性地图示了包含集成的静脉支架的瘘支架的示例实施例。
具体实施方式
虽然某些实施例和示例在下面描述,但是本发明延伸超过具体公开的实施例和/或应用以及其显而易见的改变和等同物。本文公开的发明的范围不应当被下面描述的任何(一个或更多个)具体的实施例限制。
微创手术可以提供用于治疗更广泛的患者的手段,包括当前从标准手术技术排除的那些患者。一个这样的程序是经皮原位冠状静脉动脉化(picva),其是基于导管的冠状动脉旁路程序,在该程序中通过在冠状动脉和相邻的冠状静脉之间建立通路而“绕过”患病动脉中的闭塞。以这种方式,动脉血被转向到静脉系统内并且可以以逆行方式(逆行灌注)灌注心脏组织并且恢复血液供给至缺血组织。执行如picva的程序的一些示例设备和方法在pct公开第wo99/049793号和美国专利公开第2004/0133225号中描述,其在此通过引用以其整体并入。
成功执行使血流从冠状动脉转向相邻静脉的微创程序迄今为止具有低成功率,很多时候是由于不能从动脉适当地靶向静脉。由于没有适当的系统和方法,这类程序(例如,尝试通过x射线荧光检查和位于导管远端端头上的成像超声探针的组合来靶向静脉,例如如美国专利公开第2004/0133225号中所描述的)甚至在开始之前常常就注定要失败。实际上,这样的布置可能难以导航(navigate),并且相邻静脉的定位就临床医生而言可需要相当多的技巧。一般而言,用于进行靶向的系统和方法(诸如使用本文描述的导管的那些系统和方法)的改进通常可以能够实现诸如picva的程序和经血管的手术。如果没有这种改进,这类经皮技术对于传统心脏直视外科手术和其他类型旁路手术来说仍然是次要的。
根据数个实施例,本申请描述了在微创手术程序中可使用的方法和系统,其可降低传统手术的性能来治疗诸如冠心病和严重肢体缺血的状况。例如,可以治疗可能否则不能接受诸如冠状动脉旁路手术或外周动脉旁路手术的手术的患者,并且手术创伤的量、感染风险和/或恢复时间与传统手术相比可以被降低或显著降低。
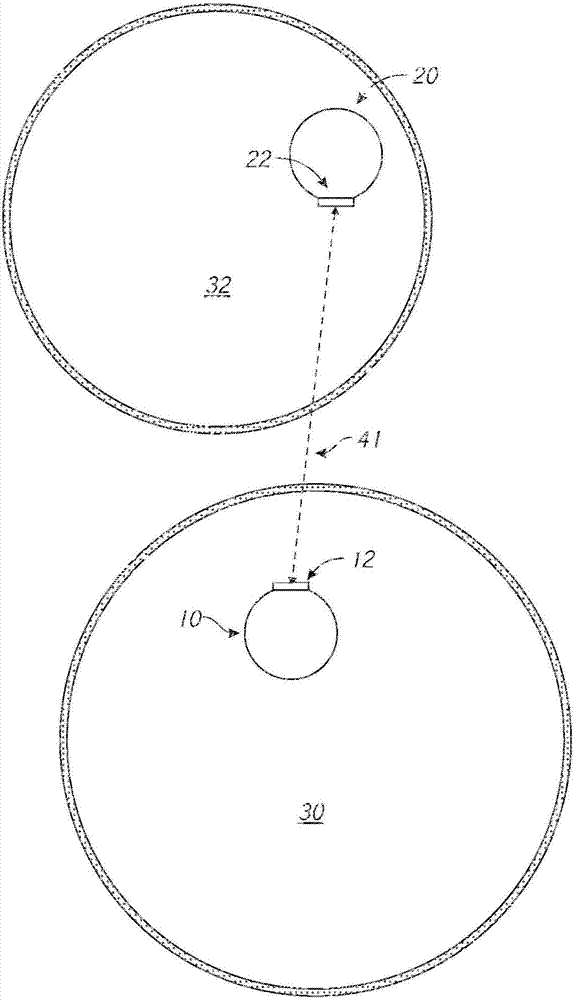
图1示意性地图示了将信号从第一体腔30导向到第二体腔35中的目标设备20的发射设备10的示例实施例。发射设备10包括信号发送器12。发射设备10可以包括,例如,包含细长柔性杆状部分和端头部分的导管,并且可以提供在患者身体内施用治疗的管道(conduit)。发射设备10可以适合于定位和移动通过患者身体内的第一内腔或脉管30(例如,心室、冠状动脉、冠状静脉、外周动脉、外周静脉)。发射设备10的细长部分包括包围空间的外鞘11,其限定了内腔13。内腔13内的空间根据需要可以被适当地划分或细分从而限定用于施用治疗、控制发射设备10的定位等的通路。例如,这样的细分可以纵向地或同中心地以轴向方式实现。
发射设备10包括信号换能器12。信号换能器12配置为提供或发出从发射设备10向外导向的信号40。在图1中示出的实施例中,信号40以垂直于发射设备10的纵向轴线的方向从发射设备10径向地向外导向。如下面更详细提及的,在一些实施例中,信号40的方向不需要垂直于发射设备10的纵向轴线并且可以与发射设备10的纵向轴线成一定角度导向。信号换能器12可以因此形成信号生成装置的至少一部分。
信号换能器12与信号发送器50连接。信号发送器50可以适当地选自超声源或适合的电磁源,诸如激光、微波辐射、无线电波等。在一些实施例中,如下面进一步详细描述的,信号发送器50被配置为生成超声信号,超声信号被转发至信号换能器12,信号换能器12转而将信号40导向出第一体腔30进入周围组织。
目标设备20位于患者体内的相邻的第二体腔或脉管32(例如,心室、冠状动脉、冠状静脉、外周动脉、外周静脉)内。第一体腔30和第二体腔32被居间组织34分开,居间组织34有时被称为间质组织或隔膜。第一体腔30和第二体腔32对于它们各自长度的至少一部分以平行的方式彼此靠近定位。例如,已知身体的许多静脉和动脉对于它们的总长度的至少一部分彼此平行延伸。
目标设备20可以采取与发射设备10的布置相似的布置。例如,目标设备20可以包括包含细长柔性杆状部分和端头部分的导管。对于另一示例,可以实现目标设备20在体腔32内的精细移动和定位。对于又另一示例,目标设备20可以包括包围空间并限定内腔23的外鞘21。内腔23可以被适当地划分,例如与发射设备10一样。
目标设备20包括配置为从发射设备10的换能器12接收信号40的接收换能器22。接收换能器22组成信号检测装置的至少一部分。在使用中,当接收换能器22接收从信号换能器12发送的信号40时,接收换能器22将接收的信号发送至信号检测器60。信号检测器60配置为例如经由输出显示器61向系统的使用者提供输出读数。输出显示器61可以是可视显示器、音频显示器(例如,接收到信号后嘟嘟响或发出一些其他声音)等。
以这种方式,导向的信号40的发送和检测可以允许发射设备10相对于目标设备20的导航和定位。在使用中,发射设备10和目标设备20可以通过系统的使用者操纵,直到输出显示器61指示信号40正被目标设备40接收。
在一些实施例中,信号40包括超声信号或者是超声信号。信号40是指向性的并通过信号换能器12以窄圆锥体或圆弧的形状发出(例如,随着距信号换能器12的距离增加,信号带的宽度增加)。因此,发射设备10和目标设备20之间的对准精度不仅取决于信号检测,而且取决于两个装置之间的距离——因为信号束宽度在更远的距离处更大。这种水平的误差被称为“位置不确定性”。对于位置不确定性,可能存在某一水平的公差;然而,如果将要精确地指导治疗,则不确定性的量应当被降低或最小化。例如,如果信号换能器12的直径d为1mm并且超声信号的频率为30mhz,则位置不确定性x(例如,中心线任一侧上的误差裕度)在发射设备10和目标设备20之间的5mm垂直间距下为1mm。对于临床应用,(对于接收点处10mm的总信号束宽度)位置不确定性通常不应当超过大约±5mm。在一些实施例中,位置不确定性在大约±0.01mm和大约±4.50mm之间或在大约±0.1mm和大约±2mm之间。在一些实施例中,位置不确定性不超过大约±1mm。
信号40的强度可以是检测中的因素,并且随着发射设备10和目标设备20之间的距离增加,信号强度通常减小。该距离部分地由设备10、20之间的居间组织34的量确定。举例来说,如果信号40是超声信号,则当发射设备10和目标设备20被超过大约20mm的固体组织(例如,居间组织34)分开时,信号的显著衰退可以被预期。相对于距离,居间组织34的密度也可以对信号40的衰退具有影响(例如,与较不密集组织相比,较密集的组织使信号衰退更多)。
超声信号的频率也可以影响信号换能器的厚度,对于标准超声陶瓷换能器(例如,压电式换能器(pzt)),在30mhz下,信号换能器的厚度为0.075mm。
图2是沿着图1的虚线b–b的横截面表示。发射设备相对于目标设备的正确定向(orientation)可以是检测中的因素,因为定向线41可以确定将在哪里应用治疗。如果指向信号40与用于递送治疗的装置相联系(例如,平行和纵向地偏移),对患者中精确放置治疗的临床需要可以更好的发挥作用。例如,以这种方式,系统的使用者可以通过确保发射设备10和目标设备20经由信号40的发送和接收被正确地定位而将治疗施用至正确的位置。图2中的定向线41不仅表示信号行进的方向而且表示可将治疗沿其施用至患者的路径。
图3示意性地图示发射设备10的示例实施例。发射设备10包括相对于发射设备10的纵向轴线以斜角定向的信号换能器120。当发射设备进入体腔30时(图1和2),信号40以沿发射设备10的行进(例如,向前行进、横向行进)的方向的角度发送。在一些实施例中,波束角大约垂直于发射设备10的纵向轴线。在一些实施例中,当0°对应于在行进方向中的发射设备10的纵向轴线时,波束角在与垂线成大约20°和大约60°之间,与垂线成大约30°和大约50°之间,或与垂线成大约45°。
发射设备10包括中空针或套管17,其是施用治疗的示例装置。在发射设备10的行进期间,中空针17以未部署的(undeploy)或缩回的状态位于发射设备10的内腔13内。中空针17可以在使用者认为适当的时间经由外鞘11中的孔口16从发射设备10部署(deploy)/延伸(例如,在信号40被目标设备20检测到之后)。孔口16可以允许内腔13和体腔30之间的流体连通(图1)。如图3的示例实施例所图示的,中空针17可以沿着平行于信号40的方向的路径行进。中空针17可以用于刺穿居间组织34(图1)。在一些实施例中,中空针17进行穿过居间组织34的整体的通行,并且这样做允许发射设备10进入第二体腔32(图2)。如果需要,由中空针17制造的通过居间组织34的路径可以随后被加宽以允许第一体腔30和第二体腔32之间的流体连通。
适合在数个实施例中使用的治疗装置可以包括,例如,选自以下组中的设备和/或仪器:套管、激光器、辐射发出设备、探针、钻头、刀片、线材、针、其适合的组合等。
在一些实施例中,中空针17包括传感器19,传感器19可以帮助进一步确定中空针17的端头相对于发射设备10的位置信息。在一些实施例中,传感器19被配置为检测流体静压的改变。适合在本文描述的系统和方法中使用的其他传感器可以包括温度传感器、氧合传感器和/或颜色传感器。
任选地,中空针17可以包括附加的信号换能器122。在图3中示出的实施例中,信号换能器122位于导丝14的末端上的中空针17的端头附近。如果需要,信号换能器122也可以或可替代地位于中空针17上。在使用中,利用产生指向信号和非指向信号脉冲的短发送脉冲驱动信号换能器122。信号脉冲可以由安装在目标设备20上的接收换能器22检测。从导丝14或中空针17到接收换能器22的距离和因此到目标设备20的距离可以至少部分地由基于信号脉冲自信号换能器122的发送和接收换能器22上信号脉冲的接收之间的延迟的时间确定。
图4示意性地图示目标设备20的示例实施例。在图4中示出的实施例中,目标设备20位于体腔32内。如上面所提及的,目标设备20包括用于接收信号40的接收换能器22。接收换能器22可以是单向的(例如,仅仅能够接收来自一个方向的信号)或全向的(例如,能够接收来自任何方向的信号)。箭头a示出已经实现动脉-静脉动脉化(也称为picva)之后血流的反向方向。目标设备20包括全向超声信号接收换能器60。任选的反射锥形体601可以将信号40导向至圆盘形接收换能器60上。透声窗602可以将反射锥形体601与接收换能器60分开。在一些实施例中,全向超声信号接收换能器可以通过在目标设备20的外鞘周围定位柔性压电材料诸如聚二氟乙烯(pvdf)的圆筒而被获得。这样,圆筒可以以与接收换能器60相似或等同的方式起作用。
在图4中图示的实施例中,目标设备20包括任选的通路25,用于将药剂诸如治疗剂施用至患者。在一些实施例中,通路25起管道的作用以允许施加封堵材料251,封堵材料251用于至少部分地阻塞或闭塞体腔32。封堵材料251可以适当地选自基于凝胶的物质。封堵材料251也可以或者可替代地包括栓塞形成构件(例如,球囊,自扩张支架等)。封堵材料251的放置可以通过移动目标设备20而被导向。目标设备20的内腔23内存在引导构件24可以允许使用者按照需要精确地操纵目标设备20的位置。
再次参照图2,发射设备10包括可以任选地被定向的信号换能器12以便信号40以非垂直于信号换能器12的角度发送。图5示意性地图示了发射设备10的另一示例实施例。在一些实施例中,例如在图5中所示出的发射设备10,信号换能器是信号换能器阵列123的形式。信号换能器阵列123包括多个信号换能器元件124,其可以共同被定向以至少部分地限定信号束宽度和相对于发射设备10的角度。元件124的较小尺寸可以允许信号换能器123不占据发射设备10的内腔13的显著比例。
图5中示出的实施例可用于超声束形成信号。图5示出经由延迟元件51分别连接至发送器50的信号换能器元件124的阵列,所述延迟元件51允许至每个元件124的信号相对于彼此被延迟。延迟元件可以提供或确保来自每个元件124的超声波阵面被对准从而以期望的角度产生超声40的波束。例如,在其中信号40包括可见光的一些实施例中,也可以或可替代地使用led的阵列。
图6示意性地图示用于发射的定中心设备10和/或目标设备20的示例实施例。为了帮助第一体腔30中的发射设备10和第二体腔32中的目标设备20之间的对准过程,设备10、20的一个或两个可以包括用于在它们的体腔内使各自设备居于中心的装置。
在一些实施例中,定中心装置包括可膨胀的囊状物或球囊111,可膨胀的囊状物或球囊111在未部署状态时位于内腔13、23中,并且当设备10、20到达患者内期望位置时可以膨胀。球囊111可以设置在外鞘11、21的外表面上。球囊111是环形形状,从而使得它至少部分地以类似环状的(toroidal)或圆圈状(doughnut)的方式环绕设备10、20。球囊111可以被布置使得它在设备10、20的仅一侧或仅两个相对侧膨胀。如图6中所图示,球囊111在发射设备10的一侧上部署。
在一些实施例中,定中心装置包括位于内腔13、23中或外鞘11、21中制造的凹处内的在未部署或缩回状态的一个或更多个环结构112。当设备10、20到达患者内的期望位置时,一个或更多个环结构112可以从设备10、20径向向外地扩张,从而在体腔30、32内使设备10、20居于中心。环结构112的向外扩张可以由压缩一定长度的线材而被适当地实现,例如使得它从外鞘11、21向外弯成弓形。采用该构造的定中心设备可以包括围绕外鞘11、21的周边以径向空间间隔平行布置的多个可压缩长度的线材或者其他适当的柔性材料。可以经由近侧和/或远侧靠近多个线材的末端定位的滑动构件(未示出)引起多个线材的压缩。滑动构件能够沿着设备10、20的纵向轴线平移移动。如图6中所图示的,目标设备20包括完全部署的定中心装置112,其允许目标设备20在体腔32内居于中心。
在体腔30、32内使设备10、20居于中心的其他可能的装置包括,但不限于,可扩张的中国灯笼形设备、可逆地可扩张的支架、线圈、螺旋线、可缩回的探针或支腿(leg)、其组合和类似物。
在一些实施例中,定中心装置或其他装置(例如,球囊、具有不同长度的金属支座(stand-off)等)可以用于将设备10、20定向在体腔30、32内而不是在体腔中心或基本上在体腔的中心。例如,设备10可以靠近体腔30的壁定向,针17将在体腔30的壁处离开体腔30,例如,由于针17穿过内腔内空间,这可以提供更短的超声信号路径和/或降低误差。对于另一示例,设备10可以靠近与体腔30壁相对的体腔30壁定向,在那里针17将离开体腔30,这可以例如提供针17推压的坚固表面。对于又一示例,设备20可以靠近体腔32的壁定向,在那里针17将进入体腔32,这可以例如提供更短的超声信号路径。不居于中心也不靠近脉管壁的其他设备定向也是可能的(例如,远离内腔的壁和/或中心的一些直径的分数,例如1/2、1/3、1/4等)。
示例
本文描述的方法和系统根据数个实施例表明了在心血管手术中的具体应用。某些方面通过下面的非限制性示例进一步图示,其中系统被临床医生使用以执行动脉静脉连接(picva)的程序,从而能够在冠状动脉的闭塞之后逆行灌注心脏组织。
通过标准的锁孔手术技术(例如,在导丝上进行跟踪、通过引导导管进行跟踪)将发射导管10插入到闭塞的冠状动脉中。通过标准的锁孔手术技术(例如,在导丝上进行跟踪、通过引导导管进行跟踪)将目标导管20插入到与冠状动脉平行延伸的冠状静脉中。冠状静脉没有闭塞并且,因此,提供血液流动至心肌的可替代通路,从而有效地使冠状动脉中的闭塞被绕过。
发射导管10包括pzt超声换能器12(例如,可从美国新墨西哥州albuquerque的ctspiezoelectricproducts购得),pzt超声换能器12被定向以便在该示例中指向性的超声束以45°角(相对于发射设备的纵向轴线),优选地以动脉30中血液流动的方向发送,但是包括大约90°在内的其他角也是可能的。超声换能器12被激活,并且在该示例中30mhz的指向性超声信号40从发射导管10发送,但是其他频率也是可能的。目标导管20包括全向的超声接收换能器60。为了帮助定位发射导管10和目标导管20二者,导管10、20二者都包括定中心或定向装置,在该示例中其是环形可膨胀的球囊111的形式,但是其他定中心或定向装置也是可能的或缺少定中心或定向装置也是可能的。当发射导管10被认为在靠近冠状动脉30内的闭塞部位的适合位置时,发射导管10上的定中心装置111由临床医生部署。这可以经由标准的荧光检查成像技术和/或根据物理阻力确定。目标导管20然后在相邻的冠状静脉32内移动,直到导向的超声信号40被信号接收换能器60检测到。为了使得在发射导管10和目标导管20之间实现更精密的对准,目标导管20上的定中心装置111可以在检测到信号40之前或之后部署。
在接收发送的信号40之后,临床医生可以确定发射导管10和目标导管20都旋转地和纵向地正确定位在它们各自的血管30、32内,以允许开始动脉-静脉连接程序。经由通过目标导管20中的通路25施用凝胶封堵材料251,目标导管20可以被用于封堵冠状静脉32内的血液流动。可以相对于接收信号换能器60的位置在静脉血液流动的下游的冠状静脉32中的位置处施用封堵材料251。
临床医生然后可以通过基本上沿着一路径从发射导管10部署中空针17来开始静脉-动脉连接,其中该路径平行于并且接近于超声信号40通过冠状动脉30和冠状静脉32之间的居间组织34所采用的路径,或者中空针17可以穿过在冠状静脉32内的某点处与超声信号路径相交的路径。中空针17任选地包括接近其端头的传感器19,其被配置为检测流体静压或多普勒流动的改变,从而使得当中空针17通过两个脉管30、32之间时,使用者可以监测从动脉压力到静脉压力的过渡。任选地,中空针17包括在部署期间在中空针17的孔或内腔中的导丝14。一旦中空针17和导丝14穿过居间组织34,中空针17可以缩回到发射导管10的内腔13中,留下导丝14在适当的位置。在一些实施例中,一旦中空针17穿过居间组织34,使用者可以分开地使导丝14通过中空针17的孔或内腔并且然后将针17缩回到发射导管10内。
临床医生从患者收回发射导管10,留下导丝14在适当的位置。进一步的导管装置然后沿着导丝14滑动。图7示意性地图示在诸如动脉-静脉动脉化的程序之后在适当位置的假体26(诸如可扩张的支架26)。关于包含支架和支架移植物的可能的假体的进一步细节在下面提供。支架26可以被部署以使冠状动脉30和冠状静脉32之间的居间组织34中的穿孔变宽,其中间断的箭头a表示通过第一和第二体腔30、32之间的支架26的血流方向(例如,动脉血因此转向静脉系统并且能够逆行灌注心肌组织)。支架26可以封堵体腔32中向上的流动,迫使体腔32中的血流与体腔30中的血流在相同的方向。支架26的移植材料可以在体腔30和体腔32之间形成液密的腔。目标导管20从患者收回,留下封堵材料251在适当的位置。任选地,进一步的封堵或缝合可以插入冠状静脉以抑制或防止动脉血流的逆转,如本文进一步详细描述的。
尽管上面描述的具体示例是关于心血管外科,但是本文描述的方法和系统可以在其他形式的手术中具有深远的应用。例如,可以考虑涉及需要将治疗从一个体腔(例如,对于治疗外周动脉疾病)朝向另一相邻体腔导向的任何手术。因此,在神经外科、泌尿外科和一般血管外科领域中的应用也是可能的。该类型的治疗不限于在体腔之间形成通路。例如,本文描述的方法和系统也可以在导向技术诸如导管消融术、心室的非接触式标测、递送药物至身体的精确区域和诸如此类中使用。
以上描述了通过经皮手术有效地绕过动脉中闭塞的某些技术。这些技术包括在第一通道和靠近第一通道的第二通道之间建立通路或通道以通过第三通道使第一通道和第二通道互连,所述第一通道诸如闭塞上游的动脉、静脉或心室,所述第二通道诸如动脉、静脉或心室。流体诸如血液可以经由互连第三通道而从第一通道转向到第二通道内。在第一通道包括动脉并且第二通道包括静脉的实施例中,动脉血液可以以逆行方式(逆行灌注)灌注到组织内。
如上面所描述的,第一身体通道和第二身体通道之间的互连通道可以通过例如从位于第一通道内的第一导管向外部署针以便针穿过第一通道和第二通道之间的间质组织或隔膜而建立。第二导管可以位于第二通道中,从而提供接收从第一导管发送的信号(例如超声信号)的目标设备。通过监测接收的信号,可以确定第一导管相对于第二导管的位置,从而确保针以正确的位置和定向部署以在第一通道和第二通道之间建立用于流体流动的通道。
为了提供或维持血液流动通过互连通道或通路,可以将包含内腔的结构插入在通道中,以支撑间质组织和/或以抑制或防止通道关闭。例如,如本文中所描述的,管可以包括使用球囊导管在通路中扩张或自扩张的支架。递送该结构的导管(例如球囊导管或允许自扩张的导管)可以通过在通道中由第一导管部署的导丝引导至通路。
诸如动脉、静脉和心室的通道可以随着心脏跳动而搏动,例如这是由于心脏壁、外周肢体的移动和/或通道自身内压力的波动。这种搏动可以引起通道相对于彼此的移动,其可以对于其间的互连通道内的结构强加应力。这种应力与单一通道内的结构经历的应力相比可能是大的。例如由于支架支柱的疲劳失效,应力可以导致结构的过早失效。该结构的失效可能导致对间质组织的损伤和/或互连通道的闭塞,这可能导致显著并发症或治疗的完全失败。
图8图示用于提供或维持通过至少一个通道的流体流的设备或植入物或假体100。设备100包括第一或近端部分102、第二或远端部分104、以及近端部分102和远端部分104之间的中间部分106。设备包括用于流体通过设备100的孔或内腔110。设备100,例如至少设备100的中间部分106,包括柔性聚合物管108。柔性聚合物管108可以至少部分地限定内腔110。
设备100包括包含网状物112和网状物114的支撑结构(例如,至少一个支架)。在一些实施例中,网状物112的至少一部分被嵌入靠近设备100的近端部分102的管108的外壁。在一些实施例中,网状物114的至少一部分(例如线材或支柱)被嵌入靠近设备110的远端部分104的管108的外壁。网状物112、114可以包括生物相容的金属(诸如不锈钢)和/或形状记忆材料(诸如镍钛诺或铬钴)。
线材网112、114可以分别使端部102、104变硬。在中间部分106不包括网状物的一些实施例中,中间部分106与端部102、104相比可以是相对柔性的,和/或端部102、104可以具有相对高的径向刚性。
在一些实施例中,设备100的端部102、104是沿直径可扩张的。例如,线材网112、114在形成或制造之后与设备100将被部署在其内的通道(诸如血管)相比可以具有更小的直径。当设备100处于在通道中的适合位置时,端部102、104可以向外地扩张或变形,以便端部102、104的各自直径增加,例如以邻接通道的内部侧壁。例如通过网状物112、114的材料(例如,线材、支柱)的塑性变形和/或通过提供布置为将网状物112、114机械地锁紧在扩张位置的锁紧机构,端部102、104被配置为无限期地(indefinitely)维持扩张的直径。设备100的中间部分106可以是沿直径可扩张的,例如经由管108的塑性变形。
图9示出图8的设备100,其被部署以在第一通道116和第二通道118之间提供流体流动路径。通道116、118可以包括冠状血管,例如冠状动脉116和冠状静脉118,或者反之亦然。通道116、118可以包括外周血管(例如,四肢中的血管),例如股动脉或其他外周动脉116和股静脉或其他外周静脉118,或者反之亦然。设备100的端部102、104和中间部分106已经被扩张成与通道116、118的内壁接触并推压通道116、118的内壁。设备100的远端部分104位于第二通道118内,并且设备100的近端部分102位于第一通道116内。中间部分106延伸通过在通道116、118之间外科形成的开口或互连通道130。
设备100的扩张的端部102、104是有弹性的,并且对通道116、118的内壁赋予向外的径向力。由于设备100的端部102、104的径向刚性,端部102、104被保持或锚定在各自的通道116、118内的适当位置。设备100在通道116、118内的滑动因此被防止或减小。以这种方式,设备100的端部102、104可以将设备100锚定或固定在适当的位置,在使用中,同时提供或维持通过管108的内腔110的流体流(图8)。以这种方式,设备100可以充当第一通道116和第二通道118之间的分路。
设备100的中间部分106可以是柔性的,例如允许中间部分106形成由第一通道116、第二通道118和互连通道130的组合形成的‘s’形(图9)。响应于通道116、118的相对移动,柔性中间部分106可以允许设备100的端部102、104相对于彼此移动。
在中间部分106不包括线材网而是包括柔性聚合物材料的管108的实施例中,中间部分106可能不易于由于例如在通过通道116、118的相对移动所赋予的循环或其他应力造成的网疲劳而被损坏。
设备100的中间部分106具有足够的弹性以维持互连通道130的扩大,以便互连通道130保持打开以经由管108的内腔110提供或维持从动脉116到静脉118的血液流动路径(图8)。经由互连通道130从动脉116到静脉118的血流可以因此被提供或维持通过管108的内腔110。设备100至少部分地支撑动脉116、静脉118和互连通道130,从而为通过设备100的流体连通提供路径。
设备100的近端部分102和远端部分104被布置以便,当设备100以远端部分104在静脉118中和近端部分102在动脉116中部署时,例如如图9中所示出,扩张的远端部分104的直径足以保持远端部分104在静脉118内,并且扩张的近端部分102的直径足以保持近端部分102在动脉116内。近端部分102的直径可以因此与远端部分104的直径不同。通过为端部102、104和中间部分106选择适合的直径,可以为某些解剖结构和/或个体患者的解剖结构定制设备100。
现在将描述用于定位图8的设备100以在闭塞的动脉116和静脉118(例如,冠状动脉116和冠状静脉118,或外周动脉116和外周静脉118)之间提供分路从而实现动脉血的逆行灌注的示例程序,例如如图9中所示出的。
可以经由通常在患者的腹股沟区域中切割的小孔口将导管插入患者的动脉系统。导管被供应至动脉116并被引导至闭塞部位上游的位置,例如在靠近且平行于或基本平行于静脉118的部位处。将中空针从导管部署,通过动脉116的壁,通过使动脉116和静脉118分开的间质组织132,并通过静脉118的壁。针的路径建立互连通道或开口130,其允许血液在动脉116和静脉118之间流动。针的部署可以通过耦连至动脉116中导管的发送器(例如,指向超声发送器)和耦连至静脉118中导管的接收器(例如,全向超声接收器)引导,或者反之亦然,例如如本文和美国专利申请第11/662,128号中描述的。形成开口130的其他方法也是可能的(例如,从静脉到动脉,利用或不利用指向超声引导,利用诸如本文所描述的其他类型的引导,等)。
在针从通道130收回之前,将导丝(例如,如关于图3的导丝14所描述的)插入通过中空针并进入静脉118。然后缩回针,留下导丝在动脉116、通道130和静脉118中的适当位置。携带针的导管然后可以从患者的身体收回。导丝可以用于引导进一步的导管至动脉116和静脉118之间的互连通道130。
携带非扩张状态的设备100的导管朝向互连通道130推进,由导丝引导例如由快速交换的内腔引导或引导通过内腔110。例如,导管可以包括配置为扩张设备100的至少一部分的球囊导管和/或配置为允许设备100的至少一部分的自扩张的导管。设备100的远端部分104穿过互连通道130并进入静脉118,留下近端部分102在动脉116中。设备100的中间部分106至少部分地在通道130中,并至少部分地在动脉116和静脉118内。中间部分106弯曲以采用弯曲的或“s”形构型,这取决于部位的解剖结构。采取这样的曲率可以使延伸通过互连通道130并任选地进入通道116、118的至少一个的中间部分106的形状与至少互连通道130的形状一致。
例如,设备100的远端部分104在球囊膨胀之后或通过自扩张而扩张,从而增加远端部分104的直径并抵靠静脉118的内壁锚定远端部分104。导管可以适合于例如通过球囊的膨胀来扩张设备100的中间部分106,以便互连通道130可以被加宽或扩大以获得从动脉116到静脉118的血流(例如,足够的血流)。例如,设备100的近端部分102在球囊膨胀之后或通过自扩张而扩张,从而增加近端部分102的直径并抵靠动脉116的内壁锚定近端部分102。
在设备100的端部102、104例如由于自扩张和/或球囊扩张而扩张之后,并且在部署之后改善或不改善扩张的情况下,导管和导丝从患者的身体收回。以这种方式,将设备100被锚定或固定在静脉118、动脉116和互连通道130内的适当位置,如图9中所示出的。在设备100包括支架移植物的实施例中,可以在动脉116和静脉118之间形成液密通道的移植物能够抑制或防止血液在静脉118中顺行流动,因为这样的通道被封堵,其可以是除了静脉118中的封堵剂之外的附加项或取代静脉118中的封堵剂。
导管可以适合于选择性地单独或组合扩张设备100的近端部分102、远端部分104和/或中间部分106,例如通过提供两个或更多个单独膨胀的球囊或球囊部分、配置为同时扩张设备100的所有部分的单个球囊或配置为扩张设备100的一个或更多个选择的部分的单个球囊。例如,端部102、104可以是自扩张的,并且中间部分106可以通过球囊扩张以扩大通道130。在包括球囊扩张的一些实施例中,设备100的所有部分或选择部分可以例如通过穿过设备100整个长度的球囊或通过纵向隔开以选择性地使设备100的选择部分膨胀的多个球囊而被同时扩张,和/或通过球囊或多个球囊而被相继扩张。在包括至少部分自扩张的一些实施例中,设备100的所有部分或选择部分可以例如通过设备100上或周围的鞘的近侧缩回而扩张,这可以导致随着鞘向近侧缩回设备100从远侧到近侧部署。设备100从近侧到远侧的部署和设备100首先中间然后两端的部署也是可能的。在一些实施例中,例如在设备100至少部分地是圆锥形的或锥形的实施例中,圆锥形的或锥形的球囊可以用于至少部分地扩张设备100。在某些这样的实施例中,靠近静脉118的球囊的部分可以比靠近动脉116的球囊的部分具有更大的直径,例如使得设备100可以适应于由于静脉118中的压力或血流的任何增加而导致的改变的静脉直径。
其他步骤可以被包括在该程序中。例如,在设备100部署之前,球囊导管可以被引导至互连通道130并被定位,以便导管的可膨胀的球囊部分位于互连通道130中。在球囊膨胀之后,球囊推压互连通道130的壁以使互连通道130加宽或扩大以易于随后插入设备100。
图10图示了提供通过至少一个通道的流体流的另一设备134。设备134包括网状物136和聚合物管108。网状物136示出为在聚合物管108外侧,但是如本文所描述,其也可以或可替代地在聚合物管的内侧上和/或在聚合物管108之内。如关于设备100所描述的,设备134包括近端部分102、远端部分104和中间部分106。在图10所图示的实施例中,网状物136沿着设备134的整个长度包括沿着中间部分106延伸。
在一些实施例中,网状物136的细丝或支柱的间距沿着设备134的长度改变。例如,织造或分层的细丝网状物的缠绕密度可以被改变和/或切割网状物的窗口大小型式可以被改变。
在一些实施例中,间距在近端部分102和远端部分104中可以是相对小的,并且间距在中间部分106中可以是相对大的。换句话说,网状物136的密度或窗口大小在中间部分106中可以是相对低的,并且网状物136的密度或窗口大小在端部102、104中可以是相对高的。在某些这样的实施例中,中间部分106与端部102、104相比可以是柔性的。相对刚性端部102、104可以接合和锚定在通道中。虽然中间部分106中的网状物136可以经受应力诸如循环应力,但在使用中,由于低的密度或窗口大小造成的中间部分106的相对高的柔性使得应力的影响较低,这是因为中间部分能够响应于应力而弯曲。设备134和具体地网状物136的细丝或支柱138的疲劳失效风险与沿着其整个长度具有均匀柔性的设备相比可以因此降低。
在一些实施例中,间距在近端部分102和远端部分104中可以是相对大的,并且间距在中间部分106中可以是相对小的。换句话说,网状物136的密度在中间部分106中可以是相对高的(或者网状物136的窗口大小可以是相对小的),并且网状物136的密度在端部102、104中可以是相对低的(或者网状物136的窗口大小可以是相对大的)。在某些这样的实施例中,中间部分106可以具有足以抑制或防止通道130塌缩的径向强度,然而仍足够柔性以响应于应力(诸如循环应力)而弯曲。端部102、104可以接合和锚定在通道中。
图11图示了提供通过至少一个通道的流体流的另一设备或植入物或假体140。如关于设备100所描述的,设备140包括近端部分102、远端部分104和中间部分106。设备140包括聚合物管108和包含第一网状物142和第二网状物144的支撑结构。第一网状物142从近端部分102朝向(例如,进入)中间部分106延伸,并且任选地进入远端部分104。第二网状物144从远端部分104朝向(例如,进入)中间部分106延伸,并且任选地进入近端部分102。网状物142、144因此至少在中间部分106处彼此重叠。网状物142、144二者都可以在管108外侧上,在管108内侧上,或者嵌入管108内,或者一个网状物可以在管108外侧上,在管108内侧上,或者嵌入管108内,同时其他网状物不同地在管108外侧上,在管108内侧上,或嵌入管108内(例如,一个网状物在管108内侧并且一个网状物在管108外侧)。网状物142、144可以如下形成,例如,通过在聚合物管108的周围或内侧的网格构造的缠绕线材,通过在聚合物管108周围或内侧放置切割管,通过被嵌入聚合物管108中,其组合或诸如此类。
在一些实施例中,网状物142、144的密度在它们各自的端部102、104中是相对高的(或者网状物142、144的窗口大小是相对小的)并且朝向中间部分106降低密度(或者增加窗口大小)。总缠绕密度(诸如,网状物142、144二者合起来的缠绕密度)在中间部分106中可以比在端部102、104中更低,或者总窗口大小(例如,网状物142、144二者合起来的窗口大小)在中间部分106中可以比在端部102、104中更大。在某些这样的实施例中,中间部分106与端部102、104相比是相对柔性的。在一些实施例中,网状物142、144不延伸进入中间部分,并且不存在网状物可以使得中间部分106与端部102、104相比相对柔性。在一些实施例中,当窗口大小(例如,沿着设备140的锥形部分纵向地)增加时,因为支柱和/或细丝的宽度保持基本恒定或恒定或者不与窗口大小以相同的比例增加,所以密度减小,网状物覆盖范围减小,和/或孔隙度增加,这可以提供沿着纵向长度的柔性改变。
第一网状物142和第二网状物144可以包含不同的材料,对于设备140的具体应用,不同的材料可以允许设备140的各自远端部分102和近端部分104的每个的性能最优化。例如,设备140的远端部分104处的第二网状物144可以包括相对柔性的金属合金,以易于插入通过两个血管之间的互连通道,同时设备140的近端部分102处的第一网状物142可以包括相对无弹性的金属合金以在近端部分104处提供高弹性度从而将设备140牢固地锚定在适当的位置。第一网状物142和第二网状物144可以包括相同的材料组成(例如,二者都包含镍钛诺)但包括不同的线材直径(规格(gauge))或支柱厚度。
图12图示了提供通过至少一个通道的流体流的另一设备或植入物或假体150。设备150包括支撑结构(例如,支架)152和移植物154。如关于设备100所描述的,设备150包括近端部分102、远端部分104和中间部分106。近端部分102包括柱形的或大体柱形的部分,并且远端部分104包括柱形的/圆柱形或大体柱形/圆柱形的部分。近端部分102的直径小于远端部分104的直径。在一些实施例中,近端部分102的直径大于远端部分104的直径。中间部分106在近端部分102和远端部分104之间具有锥形的或截头锥形/截头圆锥形的形状。支架152可以包括细丝(例如,织造的、分层的)、切割管或板、和/或其组合。
支架152的参数遍及(across)一个部分和/或遍及多个部分可以是均匀的或基本均匀的,或者在一个部分内和/或遍及多个部分可以改变。例如,近端部分102处的支架152可以包括切割管或板,远端部分102处的支架152可以包括切割管或板,和中间部分106处的支架152可以包括细丝(例如,织造的或分层的)。某些这样的实施例可以通过近端部分102和远端部分104以及中间部分106的良好的柔性(例如,对第三通道大小和动态应力的适应性)提供良好的锚定。
支架152在不同的部分中可以包含不同的材料。例如,近端部分102处的支架152可以包含铬钴和/或钽,远端部分104处的支架152可以包含镍钛诺,并且中间部分106处的支架152可以包含镍钛诺。某些这样的实施例可以通过每个部署区域(例如,近端部分102接合动脉的侧壁,远端部分104接合静脉的侧壁,和中间部分106接合动脉和静脉之间的通道的侧壁)中的设备150提供良好的锚定和/或壁附着(apposition)。在远端部分104是自扩张的一些实施例中,由于改变的脉管直径(例如,如果静脉直径由于血压或血流的增加而增加),远端部分104可以例如通过进一步自扩张来进行适应。
支撑结构材料和类型的组合也是可能的。例如,近端部分处的支架152可以包括包含铬钴和/或钽的切割管或板,远端部分104处的支架152可以包括包含镍钛诺的切割管或板,并且中间部分106处的支架152可以包括包含镍钛诺的细丝。
在支架152包括包含切割管或板的至少一部分的实施例中,切割型式可以相同。例如,切割型式在近端部分102和远端部分104中可以相同,但是与直径的改变成比例。在一些实施例中,窗口大小或支柱密度在部分102、104、106内,在部分102、104、106的两个或更多个内,和/或从支架152的一个末端到支架152的另一个末端是均匀的或基本均匀的。在支架152包括包含细丝的至少一部分的实施例中,缠绕可以是相同的。例如,缠绕在近端部分102和远端部分104中可以是相同的,但是由于直径的改变而改变。在一些实施例中,缠绕密度或孔隙度在部分102、104、106内,在部分102、104、106的两个或更多个内,和/或从支架152的一个末端到支架152的另一个末端是均匀的或基本均匀的。在支架152包括包含切割管或板的至少一部分和包含细丝的至少一部分的实施例中,切割型式和缠绕可以被配置为导致均匀的或基本均匀的密度。不均匀性也是可能的,例如如本文所描述的。
如关于管108所描述的,移植物154可以包括材料并附接至支架152。移植物154通常为设备150的至少一部分形成液密的通道。虽然图示仅围绕中间部分106,但是移植物154可以延伸设备150的整个长度,或者可以部分地重叠入柱形端部102、104的至少一个。
图13图示了提供通过至少一个通道的流体流的另一设备160。设备160包括支撑结构(例如,支架)和移植物164。如关于设备100所描述的,设备160包括近端部分102、远端部分104和中间部分106。近端部分102包括锥形的或截头锥形的部分,并且远端部分104包括锥形的或截头锥形的部分。近端部分102的近端的直径小于远端部分104的远端的直径。在一些实施例中,近端部分102的近端的直径大于远端部分104的远端的直径。中间部分106在近端部分102和远端部分104之间具有锥形的或截头锥形的形状。在一些实施例中,部分102、104、106的倾斜的角度是相同的或基本相同的(例如,如图13中所图示的)。在一些实施例中,至少一部分的倾斜的角度比至少一个其他部分更尖锐(sharp)或更窄。截头锥形的近端部分102和远端部分104可以允许在身体通道中的更好锚定,例如因为动脉从心脏随着距离趋于呈锥形,并且静脉朝向心脏随着距离趋于呈锥形,并且端部102、104可以被配置为至少部分地对应于这样的解剖学呈锥形。
图12图示了设备150,其包括第一柱形的或直的部分、圆锥形的或锥形的部分和第二柱形的或直的部分。图13图示了设备160,其包括一个或更多个圆锥形的或锥形的部分(例如,整个设备160是圆锥形的或锥形的或包括多个圆锥形的或锥形的部分)。在一些实施例中,设备150、160的组合是可能的。例如,对于设备的剩余部分,设备可以包括柱形的或直的部分和圆锥形的或锥形的部分。在某些这样的实施例中,设备的长度可以在大约1cm和大约10cm之间(例如,大约5cm),其包括柱形的或直的部分和圆锥形的或锥形的部分,所述柱形的或直的部分的直径在大约1mm和大约5mm之间(例如,大约3mm)且长度在大约0.5cm和大约4cm之间(例如,大约2cm),所述圆锥形的或锥形的部分的直径从柱形的或直的部分的直径增加到在大约3mm和大约10mm之间(例如,大约5mm)的直径且长度在大约1cm和大约6cm之间(例如,大约3cm)。这样的设备在其后可以缺少另一柱形的或圆锥形的部分。
如上面关于支撑结构152所描述的,支撑结构162可以包括细丝(例如,织造的、分层的)、切割管或板、相同的材料、不同的材料和其组合。
如关于管108所描述的,移植物164可以包括材料并附接至支架162。移植物164通常为设备160的至少一部分形成液密的通道。虽然图示为仅围绕中间部分106,但是移植物164可以延伸设备160的整个长度,或者可以部分地重叠入截头锥形的端部102、104的至少一个。
在一些实施例中,设备150和设备160的组合是可能的。例如,近端部分102可以是柱形的或大体柱形的(例如,如在设备150中),远端部分104可以是锥形的或截头锥形的(例如,如在设备160中),近端部分102具有比远端部分104的远端更大的直径。对于另一示例,近端部分102可以是锥形的或截头锥形的(例如,如在设备160中),远端部分104可以是柱形的或基本柱形的(例如,如在设备150中),而且近端部分102的近端具有比远端部分104更大的直径。在每个示例中,中间部分106在近端部分102和远端部分104之间可以具有锥形的或截头锥形的形状。
本文描述的可移植设备的示例部署装置在2009年8月24日提交的美国专利申请第12/545,982号和2012年6月1日提交的美国专利申请第13/486,249号中描述,其每一篇的全部内容在此通过参考并入。装置通常包括在近端处的具有使用者可致动的触发器的把手和在远端处的配置为在触发器致动之后推和/或拉以释放设备的管状构件的组合。其他递送设备也是可能的。递送设备可以包括在导丝(例如,已经在动脉和静脉之间经横穿组织的针导航的导丝)上可滑动的部分和/或可以是通过导管的内腔可跟踪的。
虽然本文详细示出或描述了某些实施例和示例,但是那些实施例的具体特征和方面的不同组合、子组合、改进、变化、替换和省略是可能的,其一些现在将仅以示例的方式描述。
设备,例如设备的支架、设备的网状物、设备的支撑结构等可以是自扩张的。例如,网状物可以包括形状记忆材料,诸如镍钛诺,其在经历变形之后能够回复至预设定形状。在一些实施例中,支架可以被制造为在扩张配置中期望的形状,并且是可压缩的以装配在套筒内,用于在导管上运输至血管部位。为了部署和扩张支架,套筒从支架撤回以允许形状记忆材料回复至预设定形状,这可以将支架锚定在通道中,并且如果支架具有足够的径向强度,这可以使通道扩大。球囊导管的使用不需要使完全自扩张的支架扩张,但是可以用于例如改善或优化部署。
设备可以包括一个或更多个自扩张部分,和例如使用球囊导管通过变形可扩张的一个或更多个部分。例如,在图11中所示出的实施例中,第一网状物142可以包括通过球囊导管可扩张的不锈钢,和第二网状物144可以包括部署后自扩张的镍钛诺。
关于本文中描述的任何实施例,包含移植物154、164的聚合物管108可以包括任何适合的顺应性或柔性聚合物,诸如ptfe、硅酮、聚对苯二甲酸乙二醇酯(pet)、聚氨酯诸如聚碳酸酯芳族生物耐久热塑性聚氨酯弹性体(例如,chronoflex
网状物可以包括任何适合的材料,例如镍、钛、铬、钴、钽、铂、钨、铁、锰、钼、其组合(例如,镍钛诺、铬钴、不锈钢)和诸如此类。网状物可以包括生物可降解的、生物可吸收的或生物相容的聚合物(例如,聚乳酸(pla)、聚乙醇酸(pga)、聚乙醇酸-乳酸(plga)、聚己酸内酯(pcl)、聚原酸酯、聚酸酐、其组合等)和/或玻璃,并且可以缺少金属。例如,如前面关于图11所描述的,不同的材料可以用于网状物的部分或在相同的网状物内。例如,设备100的远端部分104处的网状物114和近端部分102处的网状物112可以包括不同的材料。对于另一示例,网状物112和/或网状物114可以包括金属合金(例如,包括钴、铬、镍、钛、其组合和类似物)与不同类型的金属合金组合(例如,形状记忆合金与非形状记忆合金组合,第一形状记忆合金与不同于第一形状记忆合金的第二形状记忆合金组合,包层(clad)材料(例如,包括包含不透射线材料的芯,所述不透射线材料诸如钛、钽、铼、铋、银、金、铂、铱、钨等))和/或非金属材料,诸如聚合物(诸如聚酯纤维)、碳和/或生物可吸收玻璃纤维。在一些实施例中,至少一个网状物112、114包括镍钛诺和不锈钢。镍钛诺可以允许一些自扩张(例如,部分的和/或全部的自扩张),并且网状物可以然后例如使用球囊进一步扩张。
虽然在图8、10和11中一般图示为织造细丝网状物,但是可以使用可提供期望弹性度的任何其他结构。例如,以相反方向缠绕的细丝层可以在细丝末端处融合以提供可扩张的结构。对于另一示例,金属板可以被切割(例如,激光切割、化学蚀刻、等离子体切割等)以形成穿孔,然后以管状形状热定型,或者金属管(例如,海波管)可以被切割(例如,激光切割、化学蚀刻、等离子切割等)以形成穿孔。切割管(包括卷成管的切割板)可以热定型以赋予扩张构造。
可以被织造或编织,或分层或以其他方式布置的细丝或线材或条带通常是细长的并且具有圆形、椭圆形、正方形、矩形等横截面。示例非织造细丝可以包括以第一方向缠绕的第一细丝层和以第二方向缠绕的第二细丝层,至少一些的细丝末端耦接在一起(例如,通过耦接至可扩张的环)。示例编织型式包括一个在一个之上在一个之下/一-上-一-下-一(one-over-one-under-one)、一个在两个之上在两个之下/一-上-二-下-二(one-over-two-under-two)、两个在两个之上在两个之下/二-上-二-下-二(two-over-two-under-two)、和/或其组合,但是其他编织型式也是可能的。在细丝交叉处,细丝可以螺线形地包裹、以滑动的关系交叉、和/或其组合。细丝可以是松散的(例如,通过织造保持在一起)和/或包括焊接点、耦接元件诸如套筒、和/或其组合。细丝的末端可以向后弯曲、蜷曲(例如,具有也可以充当不透射线标记物的不透射线材料的末端蜷曲,所述不透射线的材料诸如钛、钽、铼、铋、银、金、铂、铱、钨等)、扭曲、球焊接、耦接至环、其组合和诸如此类。织造末端可以包括细丝末端和/或向后弯曲的细丝,并且可以包括开孔(opencell)、固定的或未固定的细丝、焊接点、粘合剂、或融合的其他手段、不透射线标记物、其组合和诸如此类。细丝的参数遍及一个部分和/或遍及多个部分可以是均匀的或基本均匀的,或在一个部分内和/或遍及多个部分可以变化。例如,近端部分102可以包括第一参数并且远端部分104可以包括不同于第一编织型式的第二参数。对于另一示例,近端部分102和远端部分104可以每个包括第一参数并且中间部分106可以包括不同于该参数的第二参数。对于又另一示例,近端部分102、远端部分104和中间部分106的至少一个可以包括第一参数和不同于第一参数的第二参数二者。细丝参数可以包括,例如,细丝类型、细丝厚度、细丝材料、细丝数量、织造型式、分层、缠绕方向、孔距(pitch)、角度、交叉类型、细丝耦接或其缺乏、细丝末端处理、织造末端处理、分层末端处理、层的数量、存在或不存在焊接点、不透射线性、编织型式、密度、孔隙度、细丝角度、编织直径、缠绕直径和形状设置。
管或板可以被切割以形成支柱或开孔型式,支柱是切割之后剩下的管或板的部分,并且开孔或穿孔或窗口是切掉的部分。管(例如,海波管)可以被直接切割,或者板可以被切割然后卷成管。管或板可以在切割之前或之后设定形状。管或板可以被焊接或以其他方式耦接至其自身、至另一管或板、至细丝、至移植材料等。切割可以通过激光、化学蚀刻剂、等离子体、其组合和诸如此类。示例切割型式包括螺线形螺旋(helicalspiral)、织造类、线圈、单个环、连续环、开孔、闭孔、其组合等。在包含连续环的实施例中,可以使用挠曲的(flex)连接器、非挠曲的连接器和/或其组合耦接环。在包含连续环的实施例中,环连接器(例如,挠曲的、非挠曲的和/或其组合)可以横贯环峰、环谷、支柱的中间部分和/或其组合(例如,峰-峰、谷-谷、中间-中间、峰-谷、峰-中间、谷-中间、谷-峰、中间-峰、中间-谷)。管或板或其部分在切割之前或之后可以被磨光或抛光。例如,可以形成内部脊以帮助流体流动。切割管或板的参数遍及一个部分和/或遍及多个部分可以是均匀的或基本均匀的,或在一个部分内和/或遍及多个部分可以变化。例如,近端部分102可以包括第一参数,并且远端部分104可以包括不同于第一参数的第二参数。对于另一示例,近端部分102和远端部分104可以每个包括第一参数,并且中间部分106可以包括不同于该参数的第二参数。对于另一示例,近端部分102、远端部分104和中间部分106的至少一个可以包括第一参数和不同于第一参数的第二参数二者。切割管或板参数可以包括,例如,径向支柱厚度、周向支柱宽度、支柱形状、开孔形状、切割型式、切割类型、材料、密度、孔隙度、管直径和形状设定。
在一些实施例中,穿孔可以提供具有相对柔性中间部分和相对刚性端部的网状物。支撑结构可以代替地是布置在管内的开孔泡沫。
支架、支架移植物或其一部分的细丝,和/或切割支架、支架移植物或其一部分的支柱可以被表面修饰,例如以携带药物诸如血栓修饰因子(thrombosismodifier)、流体流动修饰因子、抗生素等。支架、支架移植物或其一部分的细丝,和/或切割支架、支架移植物或其一部分的支柱可以至少部分地覆盖有例如嵌入聚合物层或一系列聚合物层内的包括药物的涂层,所述药物诸如血栓修饰因子、流体流动修饰因子、抗生素等,所述聚合物层与聚合物管108相比可以是相同的或不同的。
支架、支架移植物、或其一部分的细丝和/或切割支架、支架移植物或其一部分的支柱的厚度(例如,直径)可以在大约0.0005英寸和大约0.02英寸之间、在大约0.0005英寸和大约0.015英寸之间、在大约0.0005英寸和大约0.01英寸之间、在大约0.0005英寸和大约0.008英寸之间、在大约0.0005英寸和大约0.007英寸之间、在大约0.0005英寸和大约0.006英寸之间、在大约0.0005英寸和大约0.005英寸之间、在大约0.0005英寸和大约0.004英寸之间、在大约0.0005英寸和大约0.003英寸之间、在大约0.0005英寸和大约0.002英寸之间、在大约0.0005英寸和大约0.001英寸之间、在大约0.001英寸和大约0.02英寸之间、在大约0.001英寸和大约0.015英寸之间、在大约0.001英寸和大约0.01英寸之间、在大约0.001英寸和大约0.008英寸之间、在大约0.001英寸和大约0.007英寸之间、在大约0.001英寸和大约0.006英寸之间、在大约0.001英寸和大约0.005英寸之间、在大约0.001英寸和大约0.004英寸之间、在大约0.001英寸和大约0.003英寸之间、在大约0.001英寸和大约0.002英寸之间、在大约0.002英寸和大约0.02英寸之间、在大约0.002英寸和大约0.015英寸之间、在大约0.002英寸和大约0.01英寸之间、在大约0.002英寸和大约0.008英寸之间、在大约0.002英寸和大约0.007英寸之间、在大约0.002英寸和大约0.006英寸之间、在大约0.002英寸和大约0.005英寸之间、在大约0.002英寸和大约0.004英寸之间、在大约0.002英寸和大约0.003英寸之间、在大约0.003英寸和大约0.02英寸之间、在大约0.003英寸和大约0.015英寸之间、在大约0.003英寸和大约0.01英寸之间、在大约0.003英寸和大约0.008英寸之间、在大约0.003英寸和大约0.007英寸之间、在大约0.003英寸和大约0.006英寸之间、在大约0.003英寸和大约0.005英寸之间、在大约0.003英寸和大约0.004英寸之间、在大约0.004英寸和大约0.02英寸之间、在大约0.004英寸和大约0.015英寸之间、在大约0.004英寸和大约0.01英寸之间、在大约0.004英寸和大约0.008英寸之间、在大约0.004英寸和大约0.007英寸之间、在大约0.004英寸和大约0.006英寸之间、在大约0.004英寸和大约0.005英寸之间、在大约0.005英寸和大约0.02英寸之间、在大约0.005英寸和大约0.015英寸之间、在大约0.005英寸和大约0.01英寸之间、在大约0.005英寸和大约0.008英寸之间、在大约0.005英寸和大约0.007英寸之间、在大约0.005英寸和大约0.006英寸之间、在大约0.006英寸和大约0.02英寸之间、在大约0.006英寸和大约0.015英寸之间、在大约0.006英寸和大约0.01英寸之间、在大约0.006英寸和大约0.008英寸之间、在大约0.006英寸和大约0.007英寸之间、在大约0.007英寸和大约0.02英寸之间、在大约0.007英寸和大约0.015英寸之间、在大约0.007英寸和大约0.01英寸之间、在大约0.007英寸和大约0.008英寸之间、在大约0.008英寸和大约0.02英寸之间、在大约0.008英寸和大约0.015英寸之间、在大约0.008英寸和大约0.01英寸之间、在大约0.01英寸和大约0.02英寸之间、在大约0.01英寸和大约0.015英寸之间、或在大约0.015英寸和大约0.02英寸之间。其他厚度也是可能的,包括大于或小于所确认的厚度的厚度。包含某些材料(例如,生物可降解材料、具有较低回复力的材料等)的细丝和/或支柱可以比所确认的厚度更厚。
例如,细丝和/或支柱的厚度可以基于以下的至少一种:设备或设备部分大小(例如,直径和/或长度)、孔隙度、径向强度、材料、细丝和/或支柱的数量、切割型式、织造型式、分层型式和诸如此类。例如,较大的细丝和/或支柱厚度(例如,大于大约0.006英寸)可以用于用来治疗大脉管诸如冠状脉管的大的设备或者设备部分,中型的细丝和/或支柱厚度(例如,在大约0.003英寸和大约0.006英寸之间)可以用于用来治疗中型脉管诸如外周脉管的中型设备或设备部分,并且小的细丝和/或支柱厚度(例如,小于大约0.003英寸)可以用于用来治疗小脉管诸如静脉和神经血管的小设备或设备部分。
支架、支架移植物、或第一端部、第二端部、中间部分或其子部分的内直径或外直径,例如考虑细丝或支柱厚度,可以在大约1mm和大约12mm之间、在大约1mm和大约10mm之间、在大约1mm和大约8mm之间、在大约1mm和大约6mm之间、在大约1mm和大约4mm之间、在大约1mm和大约2mm之间、在大约2mm和大约12mm之间、在大约2mm和大约10mm之间、在大约2mm和大约8mm之间、在大约2mm和大约6mm之间、在大约2mm和大约4mm之间、在大约4mm和大约12mm之间、在大约4mm和大约10mm之间、在大约4mm和大约8mm之间、在大约4mm和大约6mm之间、在大约6mm和大约12mm之间、在大约6mm和大约10mm之间、在大约6mm和大约8mm之间、在大约8mm和大约12mm之间、在大约8mm和大约10mm之间、或在大约10mm和大约12mm之间。某些这样的直径可以适合于治疗,例如,冠状血管。例如考虑细丝或支柱厚度,支架、支架移植物或其一部分的内直径或外直径可以在大约1mm和大约10mm之间、在大约1mm和大约8mm之间、在大约1mm和大约6mm之间、在大约1mm和大约4mm之间、在大约1mm和大约2mm之间、在大约2mm和大约10mm之间、在大约2mm和大约8mm之间、在大约2mm和大约6mm之间、在大约2mm和大约4mm之间、在大约4mm和大约10mm之间、在大约4mm和大约8mm之间、在大约4mm和大约6mm之间、在大约6mm和大约10mm之间、在大约6mm和大约8mm之间、或在大约8mm和大约10mm之间。某些这样的直径可以适合于治疗,例如,静脉。例如考虑细丝或支柱厚度,支架、支架移植物或其一部分的内直径或外直径可以在大约6mm和大约25mm之间、在大约6mm和大约20mm之间、在大约6mm和大约15mm之间、在大约6mm和大约12mm之间、在大约6mm和大约9mm之间、在大约9mm和大约25mm之间、在大约9mm和大约20mm之间、在大约9mm和大约15mm之间、在大约9mm和大约12mm之间、在大约12mm和大约25mm之间、在大约12mm和大约20mm之间、在大约12mm和大约15mm之间、在大约15mm和大约25mm之间、在大约15mm和大约20mm之间、或在大约20mm和大约25mm之间。某些这样的直径可以适合于治疗,例如,外周脉管。例如考虑细丝或支柱厚度,支架、支架移植物、或其一部分的内直径或外直径可以在大约20mm和大约50mm之间、在大约20mm和大约40mm之间、在大约20mm和大约35mm之间、在大约20mm和大约30mm之间、在大约30mm和大约50mm之间、在大约30mm和大约40mm之间、在大约30mm和大约35mm之间、在大约35mm和大约50mm之间、在大约35mm和大约40mm之间、在大约40mm和大约50mm之间。某些这样的直径可以适合于治疗,例如,主动脉。其他直径也是可能的,包括大于或小于所确认的直径的直径。设备的直径可指的是第一端部、第二端部、或中间部分的直径,其每一个可以为扩张的或未扩张的形式。当设备的所有部分为扩张的或未扩张的形式时,设备的直径可指的是设备的平均直径。
支架、支架移植物、或第一端部、第二端部、中间部分、或其子部分的长度可以在大约5mm和大约150mm之间、在大约5mm和大约110mm之间、在大约5mm和大约70mm之间、在大约5mm和大约50mm之间、在大约5mm和大约25mm之间、在大约5mm和大约20mm之间、在大约5mm和大约10mm之间、在大约10mm和大约150mm之间、在大约10mm和大约110mm之间、在大约10mm和大约70mm之间、在大约10mm和大约50mm之间、在大约10mm和大约25mm之间、在大约10mm和大约20mm之间、在大约20mm和大约150mm之间、在大约20mm和大约110mm之间、在大约20mm和大约70mm之间、在大约20mm和大约50mm之间、在大约20mm和大约25mm之间、在大约25mm和大约150mm之间、在大约25mm和大约110mm之间、在大约25mm和大约70mm之间、在大约25mm和大约50mm之间、在大约50mm和大约150mm之间、在大约50mm和大约110mm之间、在大约50mm和大约70mm之间、在大约70mm和大约150mm之间、在大约70mm和大约110mm之间、或在大约110mm和大约150mm之间。其他长度也是可能的,包括大于或小于所确认的长度的长度。
支架、支架移植物、或第一端部、第二端部、中间部分、或其子部分的孔隙度可以在大约5%和大约95%之间、在大约5%和大约50%之间、在大约5%和大约25%之间、在大约5%和大约10%之间、在大约10%和大约50%之间、在大约10%和大约25%之间、在大约25%和大约50%之间、在大约50%和大约95%之间、在大约50%和大约75%之间、在大约50%和大约60%之间、在大约60%和大约95%之间、在大约75%和大约90%之间、在大约60%和大约75%之间、和其组合。支架的密度可以是该支架的孔隙度的倒数。被移植物覆盖的支架部分的孔隙度可以为大约0%。对于支架的某些部分,孔隙度可以随目的而变化。例如,中间部分可以具有低孔隙度以增加通过设备的流体流,同时端部可以具有较低的孔隙度以增加柔性和壁附着。
图25a是假体500的又一示例实施例的示意性侧视图。假体或支架或设备500包括被织造一起成为织造结构的多个细丝502和/或实质上由所述多个细丝502组成。支架500可以没有移植物材料,如在下面进一步详述的。
也可以被描述为线材、条带、股线等的细丝502可以被织造、编织、分层、或以交叉方式被以其他方式布置。细丝502通常是细长的并且具有圆形、椭圆形、正方形、矩形等横截面。示例非织造细丝可以包括以第一方向缠绕的第一细丝层和以第二方向缠绕的第二细丝层,至少一些细丝末端被耦接在一起(例如,通过耦接至可扩张的环)。示例织造型式包括一个在一个之上在一个之下/一-上-一-下-一(如在图25a中示出)、一个在两个之上在两个之下/一-上-二-下-二(one-over-two-under-two)、两个在两个之上在两个之下/二-上-二-下-二(two-over-two-under-two)、和/或其组合,但是其他织造型式也是可能的。在细丝502的交叉处,细丝502可以螺线形地包裹、以滑动的关系交叉、和/或其组合。细丝502可以是松散的(例如,通过织造保持在一起)和/或包括焊接点、耦接元件诸如套筒、和/或其组合。细丝502的末端可以向后弯曲、蜷曲(例如,具有也可以充当不透射线标记物的不透射线材料的末端蜷曲,所述不透射线的材料诸如钛、钽、铼、铋、银、金、铂、铱、钨等)、扭曲、球焊接(ballweld)、耦接至环、其组合和诸如此类。织造末端可以包括细丝502末端和/或向后弯曲的细丝502,并且可以包括开孔(opencell)、固定的或非固定的细丝502、焊接点、粘合剂、或融合的其他手段、不透射线标记物、其组合和诸如此类。
支架500包括微孔504或细丝502之间的开放的未覆盖的区域。支架500的孔隙度可以被计算为微孔504的外表面积除以支架500的总外表面积。孔隙度可以受诸如例如细丝502的数量、编织角度506、细丝502的尺寸(例如,直径)、和其组合的参数影响。
支架500的孔隙度可以小于50%(例如,比开放稍微更多被覆盖)、在大约0%(例如,几乎没有开放区域)和大约50%之间、在大约0%和大约45%之间、在大约0%和大约40%之间、在大约0%和大约35%之间、在大约0%和大约30%之间、在大约0%和大约25%之间、在大约0%和大约20%之间、在大约0%和大约15%之间、在大约0%和大约10%之间、在大约0%和大约5%之间、在大约5%和大约50%之间、在大约5%和大约45%之间、在大约5%和大约40%之间、在大约5%和大约35%之间、在大约5%和大约30%之间、在大约5%和大约25%之间、在大约5%和大约20%之间、在大约5%和大约15%之间、在大约5%和大约10%之间、在大约10%和大约50%之间、在大约10%和大约45%之间、在大约10%和大约40%之间、在大约10%和大约35%之间、在大约10%和大约30%之间、在大约10%和大约25%之间、在大约10%和大约20%之间、在大约10%和大约15%之间、在大约15%和大约50%之间、在大约15%和大约45%之间、在大约15%和大约40%之间、在大约15%和大约35%之间、在大约15%和大约35%之间、在大约15%和大约25%之间、在大约15%和大约20%之间、在大约20%和大约50%之间、在大约20%和大约45%之间、在大约20%和大约40%之间、在大约20%和大约35%之间、在大约20%和大约35%之间、在大约20%和大约25%之间、在大约25%和大约50%之间、在大约25%和大约45%之间、在大约25%和大约40%之间、在大约25%和大约35%之间、在大约25%和大约35%之间、在大约30%和大约50%之间、在大约30%和大约45%之间、在大约30%和大约40%之间、在大约30%和大约35%之间、在大约35%和大约50%之间、在大约35%和大约45%之间、在大约35%和大约40%之间、在大约40%和大约50%之间、在大约40%和大约45%之间、在大约45%和大约50%之间、和其组合。
在孔隙度小于大约50%的一些实施例中,血液在正常的脉管压力(例如,跨过脉管的压降,从传入脉管到传出脉管的压降)下不能灌注通过支架500的侧壁。在某些这样的实施例中,在不具有(例如,基本上不具有、没有、基本上没有)移植物材料的情况下而且在依然不具有通过支架500的侧壁的血液损失或基本血液损失的情况下,流入支架500的近端的血液能够被导向通过支架500的内腔,到达支架500的远端。相比之下,在某些所谓的“流动转向支架”中,孔隙度被具体设计为大于大约50%以便确保到传出脉管的灌注。
支架500的密度可以是孔隙度的倒数(例如,细丝502的外表面积除以支架500的总外表面积)。支架500的密度可以是100%减去上面提供的孔隙度值。
细丝502相对于垂直于支架500的纵向轴线的轴线(例如,如在图25a中通过示例虚线图示的)成一编织角度506。编织角度506能够从刚好多于90°到刚好在180°之下的范围内。编织角度506能够是锐角或钝角。在一些实施例中,编织角度506在大约90°和大约180°之间、在大约120°和大约180°之间、在大约150°和大约180°之间、在大约160°和大约180°之间、在大约170°和大约180°之间、在大约160°和大约170°之间、在大约165°和大约175°之间、其组合和诸如此类。在一些实施例中,编织角度506越靠近180°,支架500的径向强度越大。具有更大径向强度的设备500可以帮助保持瘘(例如,如在本文中描述的那样形成的)打开或开放。其他因素也能够影响径向强度,诸如细丝502直径,细丝502材料、细丝502的数量等。
细丝502都可以相同,或一些细丝502可以具有不同的参数(例如,材料、尺寸、其组合和诸如此类)。在一些实施例中,一些细丝502包含形状记忆材料(例如,包含镍钛诺),而其他细丝502包含另一材料(例如,包含芳族聚酰胺纤维(例如,
图25b是假体520的又一示例实施例的示意性侧视图。假体或支架或设备520包括被织造在一起成为第一织造结构的第一多个细丝522和被织造在一起成为第二织造结构的第二多个细丝524,和/或基本上由所述第一多个细丝522和第二多个细丝524组成。支架520可以没有移植物材料,如在本文中进一步详细地描述的。第一多个细丝522可以类似于关于图25a描述的支架500的细丝502。在一些实施例中,细丝522可以缺乏足够的保持瘘打开和/或附着动脉和/或静脉的侧壁的径向力。在某些这样的实施例中,细丝524可以充当提供径向力的补充支撑结构。细丝524可以是径向向外的细丝522(例如,如在图25b中图示的)、径向向内的细丝522、和/或与细丝522被集成在一起(例如,使得第一和第二织造结构不容易分开)。细丝524可以是与细丝522相同或不同的材料、与细丝522相同或不同的厚度等,和/或细丝524可以利用与细丝522相同或不同的参数(例如,编织角度)被编织,导致细丝524具有更大的径向力。细丝524可以被耦接到细丝522(例如,在单个可部署支架520中)或被单独地部署。例如,如果细丝524被部署并且然后细丝522被部署,细丝524能够撑开瘘并允许细丝522在由细丝524建立的内腔内扩张而无实质的反力。对于另一示例,如果细丝522被部署并且然后细丝524被部署,细丝524能够在需要扩张力时充当细丝522的部分上的扩张力。
尽管在图25b中被图示为包含第二织造结构,但是补充支撑结构可以额外地或替代地包含螺线形线圈、切割海波管、其组合和诸如此类。假体520的孔隙度的确定可以主要基于第一织造结构的孔隙度,使得补充支撑结构可以被主要设计用于提供径向力(例如,足以保持瘘打开或开放)。
尽管被图示为跨越支架500的长度一致或基本上一致,但是支架500和细丝502的参数可以跨越支架500变化,例如如关于图25c描述的。一致性可以降低制造成本,减少对精确放置的要求,和/或具有其他优点。不一致性可以允许沿着不同长度对于特定性质和/或功能的专门化或定制,和/或具有其他优点。
图25c是假体540的又一示例实施例的示意性侧视图。假体或支架或设备540包括被织造在一起成为织造结构的多个细丝542和/或基本上由所述多个细丝542组成。支架540可以没有移植物材料,如在本文中进一步详细地描述的。支架540包含第一纵向区段或节段或部分544和第二纵向区段或节段或部分546。诸如孔隙度(例如,如在图25b中图示的)、编织角度、编织类型、细丝542参数(例如,直径、材料等)、补充支撑结构的存在(例如,补充支撑结构544)、支架直径、支架形状(例如,柱形、截头锥形)、其组合等的参数可以在第一纵向区段524和第二纵向区段546之间不同。孔隙度可以随着针对支架540的某些部分的目的而改变。例如,可以被配置用于放置在动脉和瘘中的第一纵向区段544可以具有低孔隙度(例如,小于大约50%,如关于图25a的支架500描述的)以增加通过支架500的流体流,而可以被配置用于放置在静脉中的第二纵向区段可以具有更高的孔隙度以增加柔性和壁附着。
在一些实施例中,支架包含第一纵向区段、第二纵向区段和第三纵向区段,第一纵向区段包含被配置为将流从动脉转向到瘘内的低孔隙度织造件和/或基本上由所述低孔隙度织造件组成并且没有补充支撑结构,第二纵向区段包含被配置为将血流转向通过瘘的所述低孔隙度织造件和/或基本由所述低孔隙度织造件组成并且包含被配置为撑开瘘的补充支撑结构,第三纵向区段包含被配置为将流从瘘转向到静脉内的低孔隙度织造件和/或基本上由所述低孔隙度织造件组成。在某些这样的实施例中,第一纵向区段可以被配置为图25a的支架500,而第三纵向区段可以被配置为图25a的支架500或图25c的支架540。
第一纵向区段544和第二纵向区段546之间的差异可以在制造期间(例如,由于编织参数、形状设定等)和/或在现场(例如,在部署期间和/或之后(例如,通过支架包装))被赋予。
例如如在本文中描述的第一纵向区段544和第二纵向区段546之间的其他变化(例如,包括激光切割部分、额外的纵向区段等)也是可能的。在一些实施例中,支架包含第一纵向区段、第二纵向区段和第三纵向区段,第一纵向区段包含被配置为将流从动脉转向到瘘内的低孔隙度织造件和/或基本上由所述低孔隙度织造件组成,第二纵向区段包含被配置为被放置在瘘中以将血液转向通过瘘和/或撑开瘘的低孔隙度激光切割部分和/或基本上由所述低孔隙度激光切割部分组成,第三纵向区段包含被配置为将流从瘘转向到静脉内的低孔隙度织造件和/或基本上由所述低孔隙度织造件组成。在某些这样的实施例中,第一纵向区段可以被配置为图25a的支架500,而第三纵向区段可以被配置为图25a的支架500或图25c的支架540。
图27示意性地图示了假体720的示例实施例,在下面关于图27中的解剖结构进一步详细地描述假体720。假体720包含第一纵向区段722、第二纵向区段724、以及在第一纵向区段722和第二纵向区段724之间的第三纵向区段726。例如由于低孔隙度织造结构,即使当实质缺少移植物材料时,假体720的孔隙度也可以允许流体基本流过假体720的内腔而基本不灌注通过侧壁。
在假体720被用于外周血管系统中的实施例中,第一纵向区段722可以被描述为动脉区段,第二纵向区段724可以被描述为静脉区段,并且第三纵向区段726可以被描述为过渡区段。第一纵向区段722被配置为附着动脉700或另一体腔的侧壁。例如,对于一些外周动脉,第一纵向区段722可以具有在大约2mm和大约4mm之间(例如,大约3mm)的扩张直径。第二纵向区段724被配置为附着静脉702或另一体腔的侧壁。例如,对于一些外周静脉,第二纵向区段724可以具有在大约5mm和大约7mm之间(例如,大约6mm)的扩张直径。在一些实施例中,不是如在图27中图示的大体柱形,第二纵向区段724和第三纵向区段726可以具有包含从第一纵向区段722的更小直径到更大直径成锥度的截头锥形的形状。
假体720的长度可以被配置或被定尺寸为将假体720锚定在动脉700和/或静脉702中(例如,足以阻止或防止假体720的纵向移动或迁移)并跨越动脉700和静脉702之间的间质组织t。例如,对于一些外周动脉,第一纵向区段722在扩张或部署状态下的长度可以在大约20mm和大约40mm之间(例如,大约30mm)。又例如,对于一些外周静脉,第二纵向区段724在扩张或部署状态下的长度可以在大约10mm和大约30mm之间(例如,大约20mm)。对于又一个示例,对于一些外周血管系统,第三纵向区段726在扩张或部署状态下的长度可以在大约5mm和大约15mm之间(例如,大约10mm)。假体720在扩张或部署状态下的总长度可以在大约30mm和大约100mm之间、在大约45mm和大约75mm之间(例如,大约60mm)。尽管间质组织t被图示为大约2mm厚,但是其他尺寸是可能的,取决于部署部位的特定解剖结构。例如如在本文中描述的假体720、第一纵向区段722和/或第二纵向区段724的其他尺寸也是可能的。
第三纵向区段726包含从第一纵向区段722的更小直径到第二纵向区段724扩张的截头锥形或锥形形状。纵向区段722、724、726之间的过渡点可以是明显的或不明显的。例如,过渡区段可以被认为包括第一纵向区段722和第三纵向区段726的一部分,或第三纵向区段726可以被认为包括具有与第一纵向区段722相同的直径的柱形部分。纵向区段722、724、726可以在上述的形状和尺寸上、和/或在其他方式(例如,材料、型式等)上不同。例如,一个或更多个部分可以是柱形、截头锥形等,如在图12、图13和图27中图示并在本文中描述的。
第一纵向区段722和/或第三纵向区段726可以包含相对高的径向力,例如被配置为保持瘘开放,而第二纵向区段724可以包含相对低的径向力。在一些实施例中,第一纵向区段722和/或第三纵向区段726包含可球囊扩张支架、具有高编织角度的织造支架和/或诸如此类。在一些实施例中,第二纵向区段724包含自扩张支架、具有低编织角度的织造支架和/或诸如此类。激光切割支架、织造支架、不同的切割型式、不同的织造型式和诸如此类的组合在本文中进一步详细地描述。在一些实施例中,纵向区段722、724、726可以是一体的或分开的。第二纵向区段724可以相对柔软,例如包含相对低的径向力,这可以帮助第二纵向区段724在血流的脉动期间随着解剖结构挠曲。
在一些实施例中,第二纵向区段724和/或第三纵向区段726可以包含一些移植物材料(例如,包含硅酮)。移植物材料可以阻止或防止血流通过假体720的侧壁,和/或可以被用来携带药物。例如,取决于移植物材料的目的,移植物材料可以或不可以堵塞或基本上堵塞假体720的多个部分的微孔。
假体720的近端和/或远端可以是非创伤性的,例如包含末端治疗、低编织角度、小细丝直径、其组合和诸如此类。
支架、支架移植物、或第一端部、第二端部、中间部分、或其子部分的径向强度或耐压力可以在大约0.1n/mm和大约0.5n/mm之间、在大约0.2n/mm和大约0.5n/mm之间、在大约0.3n/mm和大约0.5n/mm之间、在大约0.1n/mm和大约0.3n/mm之间、在大约0.1n/mm和大约0.2n/mm之间、在大约0.2n/mm和大约0.5n/mm之间、在大约0.2n/mm和大约0.3n/mm之间、或在大约0.3n/mm和大约0.5n/mm之间。
支架、支架移植物、或第一端部、第二端部、中间部分、或其子部分的某些参数值可以关联(例如,成比例的)。例如,支柱或细丝的厚度与包含所述支柱或细丝的设备部分的直径的比可以在大约1:10和大约1:250之间、在大约1:25和大约1:175之间、或在大约1:50和大约1:100之间。对于另一示例,设备或其部分的长度与设备或其部分的直径的比可以在大约1:1和大约50:1之间、在大约5:1和大约25:1之间、或在大约10:1和大约20:1之间。
设备的部分可以包括不透射线材料。例如,支架、支架移植物、或第一端部、第二端部、中间部分、或其子部分的细丝和/或支柱可以包括钛、钽、铼、铋、银、金、铂、铱、钨、其组合和诸如此类(例如,至少部分地由其制成)。对于另一示例,支架、支架移植物或其部分的细丝和/或支柱可以包括具有大于大约9克/立方厘米密度的材料(例如,至少部分地由其制成)。单独的不透射线标记物可以附接至设备的某些部件。例如,不透射线标记物可以加入到设备或其部件的近端(例如,中间部分的近端部件、远端部分的近端部件)、设备或其部件的远端(例如,中间部分的远端部件、近端部分的远端部件)和/或其他部件。例如,设备末端之间的不透射线标记物可以用于划分材料、部分等之间的过渡。不透射线性可以跨越设备的长度而变化。例如,近端部分可以具有第一不透射线性(例如,由于远端部分材料和/或单独的标记物),并且远端部分可以具有不同于第一不透射线性的第二不透射线性(例如,由于远端部分材料和/或单独的标记物)。
在一些实施例中,设备包括聚合物管,并且不提供支撑结构。这样的设备的中间部分通过例如降低中间部分内的聚合物管的壁厚度可以比端部相对地更柔性。
当网状物或其他支撑结构与聚合物管结合提供时,支撑结构可以位于管外侧周围、管的内孔中、或嵌入管壁内。可以提供多于一个支撑结构,在这种情况下每个支撑结构可以相对于管具有不同的位置。
设备的端部中的一个或两个可以包括配置为抓住或紧握血管的内侧壁的锚定元件诸如挂钩、隆凸或倒钩。在没有锚定元件的情况下,扩张后的端部的径向力可以足以抓住或紧握血管的内侧壁。
在中间部分和端部之间不需要明确限定的过渡。例如,网状物类型、材料、壁厚度、柔性等可以从端部朝向中间部分或从中间部分朝向端部逐步地改变。
例如如关于设备134、140所描述的,当从端部朝向中间部分移动时,设备的柔性可以逐步地增加。柔性的改变可以由于网状物密度(例如,缠绕密度、窗口大小)、管厚度或其他因素的改变。设备的柔性沿着支撑结构(例如,支架)的整个长度,或沿着支撑结构的某些部分(例如,沿着整个端部、沿着整个中间部分、沿着一个端部和中间部分而不沿着另一个端部,等)可以是均匀的或基本均匀的。
虽然本文描述的设备可以特别适合用作经皮手术中经血管的分路,但是该设备可以在许多其他医学应用中使用。例如,设备可以在血管成形术中使用,用于治疗具有曲折或扭结路径的闭塞血管,或其中脉管在支架的位置处或附近可能经受偏转或变形。例如,支架也可以在经皮程序期间在主动脉移植程序中或穿孔之后用于修复受损的血管。在某些这样的情况下,响应于脉管的移动,设备的中间部分可以允许设备符合血管的形状并且变形,而具有降低的疲劳失效风险,同时保持端部固定或锚定在适当的位置。对于另一示例,设备可以用于在健康的动脉和健康的静脉之间形成分路,用于透析进入和/或药物施用的进入(例如,癌症治疗的间歇性注入,其可能损伤脉管)。
再次参照图4和图7,封堵材料251可以用于帮助抑制或防止动脉血流的反向。如现在将进一步详细描述的,另外的或其他的方法和系统可以用于抑制或防止动脉血流的反向,或者,换句话说,用于抑制或防止现在流入静脉的动脉血流在静脉中以血流的正常的程序前(pre-procedure)方向流动,从而使得含氧血绕过下游组织诸如脚。
在缺乏治疗时,外周血管病(pvd)可能向严重肢体缺血(cli)进展,后者的特征是深度慢性疼痛以及限制血管再生选项并频繁地导致截肢的大量组织损失。估计cli具有大约每年50-100/100,000的发病率,并且cli与发病后在6个月时具有高达20%的死亡率相关。
介入放射科医师已经积极地尝试通过试图打开慢性完全闭塞(cto)或通过在内膜下空间中使用如medtronic-pioneer导管的这样的产品绕过cto来治疗cli,所述导管将线材穿入(tunnel)靠近cto的内膜下空间然后试图再进入闭塞远侧的脉管。一旦线材在适当的位置,使用者可以任选地建立更宽的通路然后放置支架以提供越过闭塞的旁路导管。如果线材能够穿过闭塞,治疗pad的常规途径诸如经皮经管腔血管成形术(pta)、支架术(stenting)和药物洗脱球囊(deb)也可以或可替代地在cli治疗中使用。
来自amputee-coalition.org网站,下面是关于cli问题的一些统计资料:
·在美国,存在近二百万人忍受肢体缺损。
·在忍受肢体缺损的那些人中,主要要因是:
·血管疾病(54%)(包括糖尿病和外周动脉疾病(pad)),
·创伤(45%),和
·癌症(少于2%)。
·在美国,每年发生大约185,000例截肢。
·在2007年,与截肢相关的医院花费总计超过65亿美元。
·截肢后的存活率基于许多因素而变化。由于血管疾病(包括pad和糖尿病)而截肢的那些人面临报道为在9%和15%之间的30天死亡率和1年60%,三年42%,和5年35%-45%的长期存活率。
·几乎一半的因血管异常疾病而失去肢体的人将在5年内死亡。这比患有结肠直肠癌、乳腺癌和前列腺癌的人经历的5年死亡率高。
·高达55%的下肢截肢的患有糖尿病的人将在2到3年内需要将第二条腿截肢。
自二十世纪早期,cli已经通过开腿静脉动脉化进行外科治疗。多年以来,使用这样的开腿手术途径的许多小系列的临床试验已经公布,如lu等人通过在europeanjournalofvascularandendovascularsurgery,31卷,493-499页中题目为“meta-analysisoftheclinicaleffectivenessofvenousarterializationforsalvageofcriticallyischemiclimbs”的2006荟萃分析文章所概括的。该文章具有以下结果和结论:
·结果:
总计56个研究被选择用于综合评述。没有确定随机对照试验(rct)。包括228个患者的七个患者系列匹配选择标准。整1年脚保留为71%(95%ci:64%-77%)和1年二期通畅率为46%(95%ci:39%-53%)。避免大截肢的大多数患者经历成功的创伤愈合、休息痛消失和不存在严重并发症。
·结论:
基于有限的证据,静脉动脉化在大截肢在患有“不能动手术的”慢性严重下肢缺血的患者中进行之前被视为可行的替代方案。
在本文描述的其他疾病中,本文描述的方法和系统可以用于在膝下(below-the-knee)(btk)血管系统中使用血管内的微创手术方法建立动-静脉(av)瘘。这样的方法可以适合于以下患者:(i)具有如rutherford5或6所定义的有症状的严重肢体缺血的临床诊断(严重的缺血性溃疡或症状明显的坏疽);(ii)已经由血管外科医生和干预者(interventionist)评估并且确定手术或血管内治疗是不可能的;和/或(iii)明确表明大截肢。
在一些实施例中,系统或成套工具任选地包括一个或更多个以下部件:第一超声导管(例如,动脉导管、包含针的发射导管等);第二超声导管(例如,静脉导管、目标导管等);和假体(例如,递送系统中包覆的镍钛诺支架移植物(例如,7fr(大约2.3mm)递送系统))。系统或成套工具任选地进一步包括超声系统、控制系统(例如,计算机)。一些使用者可以已经具有可连接至(一个或更多个)超声导管的适合的超声系统。上面描述的导管和假体可以在该系统或成套工具中使用,并且其他的、另外的和/或修改的可能部件的细节在下面描述。
图14a是超声发射导管170的示例实施例的示意性的侧横截面视图,所述超声发射导管170包括针172(例如,第一超声导管、动脉导管(例如,如果针从动脉延伸进入静脉)、静脉导管(例如,如果针从静脉延伸进入动脉))。将导管170放置入动脉,针172以缩回的状态在导管170的内腔内部。导管170可以在导丝(例如,0.014英寸(大约0.36mm)导丝)上前进和/或被放置通过动脉(例如,股动脉)中的鞘,并推进直到动脉的完全闭塞点(在胫动脉中)。导管170包括包含推进器环176的把手174。推进器环176的纵向或远侧推进可以推进针172离开导管170的内腔、离开动脉并进入静脉,如本文所描述。针172的其他推进机构也是可能的(例如,转动的、机动化的等)。推进针172后之前、之后和/或期间,导丝(例如,0.014英寸(大约0.36mm)导丝)可以被放置通过针172(例如,如关于图3的导丝14所描述的),并且该导丝可以被称为横穿导丝(crossingwire)。
图14b是圆14b内图14a的超声发射导管170的远侧部分的放大示意性侧横截面视图。在推进或发射之后,针172从导管170的内腔173径向地向外延伸。在一些实施例中,内腔173在超声发送设备178近侧结束。针172可以沿着与由超声发送设备178发射的指向的超声信号的路径对准(例如,平行于该路径)的路径延伸。图14b也示出内腔175,其可以用于容纳跟踪导管170至期望位置的导丝。
图15a是超声目标导管180(例如,第二超声导管、动脉导管(例如,如果针从静脉延伸进入动脉))、静脉导管(例如,如果针从动脉延伸进入静脉)的示例实施例的示意性侧视图。图15b是圆15b内图15a的超声目标导管180的放大示意性侧横截面视图。图15c是圆15c内图15a的超声目标导管180的放大示意性侧横截面视图。导管180可以在导丝(例如,0.014英寸(大约0.36mm)导丝)上前进和/或被放置通过静脉(例如,股静脉)中的鞘,并推进直到靠近和/或平行于导管170的远端和/或动脉中的闭塞的点(例如,在胫静脉中)。导管180包括超声接收换能器182(例如,全向超声接收换能器),其可以充当静脉中的目标,用于对准导管170的针172。导管180可以停留在原处或保持静止或基本静止同时纵向地旋转或移动导管170以获得表示针172与导管180对准并在导管180的方向中的好的或最佳的超声信号。
导管170、180可以连接至超声收发器,其与运行收发器软件的计算机连接并且由其控制。如本文进一步详细描述的,导管170包括平坦的或指定的超声发送器178,其配置为在从导管170的内腔173推进之后以针172路径的方向发送具有低角展度(angularspread)或紧密波束(例如,小的波束宽度)的超声信号。导管180包括全向(360度)超声接收器182,其配置为充当由导管170的指向发送器178发出的超声信号的目标。导管170被旋转直到峰值超声信号被显示,这表明针172与导管180对准,使得在针172延伸(例如,通过纵向地推进把手174的环176)之后,针172可以离开导管170在其中驻留的动脉,通过间质组织,并进入导管180在其中驻留的静脉。
图16是用于检测导管对准的图的示例实施例,如可以在超声系统的显示设备(例如,笔记本电脑、平板电脑、智能手机、其组合和类似物的屏幕)上显示的。图16中的图示出源自动脉中的发送导管的信号已经被静脉中的接收导管接收。来自右边的第二频率包络(envelope)是接收的信号。从所图示的屏幕的左侧到第二频率包络的前缘的距离可以表示导管之间的距离。操作者可以使动脉中的导管旋转地和纵向地移动,例如直到第二包络是最大的,这表示导管被正确地定向。
图17是假体(例如,支架、支架移植物)递送系统190的示例实施例的示意性侧视图。在一些实施例中,递送系统190是7fr(大约2.3mm)递送系统。图18是假体(例如,支架、支架移植物)200的示例实施例的示意性侧视图。在图17中,假体(例如,假体200、本文描述的其他假体等)是以压缩的或蜷曲的状态靠近递送系统190的远端192。在一些实施例中,假体200包括覆盖有移植材料的形状记忆支架,例如如上面所描述的。一旦横穿线材从动脉延伸至静脉,例如如本文所描述的由于被推进通过针172,递送系统190可以在横穿线材上被推进。假体200可以从递送系统190部署,例如通过挤压递送系统190的触发器把手194,使外盖鞘向近侧缩回和/或向远侧推进假体200。假体200可以在动脉和静脉之间并通过间质组织建立流动路径。其他类型的递送系统和假体也是可能的。
再次参照图17,提供了递送系统190的一些非限制性示例尺寸。触发器把手194的行进距离196可以,例如,在大约0.4英寸(大约1cm)和大约12英寸(大约30cm)之间、在大约1英寸(大约2.5cm)和大约8英寸(大约20cm)之间、或在大约2英寸(大约5cm)和大约6英寸(大约15cm)之间(例如,大约2英寸(大约5cm))。在一些实施例中,触发器把手194的行进距离196至少与待部署(例如,在径向扩张状态)的假体200的长度一样长。在一些实施例中,传动机构或其他机构可以被采用以将触发器把手194的行进距离196降低为小于待部署(例如,在径向扩张状态)的假体200的长度。例如,基于以下的至少一项,可以调整距离196:待部署的假体200的长度、待部署的假体200的缩短(foreshortening)程度、部署机构(例如,外鞘是否被向近侧缩回,假体200是否被向远侧地向前推,或以上两种情况,递送系统190是否包括传动机构等)、其组合和诸如此类。外鞘或导管部分的长度197可以,例如,在大约40英寸(大约1020mm)和大约50英寸(大约1270mm)之间、在大约46英寸(大约1170mm)和大约47英寸(大约1190mm)之间、或在大约46.48英寸(大约1180mm)和大约46.7英寸(大约1186mm)之间。递送系统190从近端端头到远端端头的总长度198可以,例如,在大约40英寸(大约1000mm)和大约60英寸(大约1500mm)之间。例如基于以下至少一项,可以调整长度197、198:待部署的假体200的长度、待部署的假体200的缩短程度、患者的高度、正在被治疗的闭塞的位置、其组合和诸如此类。在一些实施例中,将触发器把手194与血管进入点隔开例如在大约10cm和大约30cm之间(例如,至少大约20cm)可以有利地提供使用者更简单的处理或管理。在某些这样的实施例中,长度197可以在大约120cm和大约130cm之间(例如,对于顺行入路)或在大约150cm和大约180cm之间(例如,对于对侧入路)。
再次参照图18,提供了假体200的一些非限制性示例尺寸,这取决于至少在压缩状态中的环境。结构支柱的厚度201可以,例如,在大约0.05mm和大约0.5mm之间或在大约0.1mm和大约0.2mm之间(例如,大约0.143mm)。结构支柱的支柱之间的间隔202可以,例如,在大约0.005mm和大约0.05mm之间或在大约0.01mm和大约0.03mm之间(例如,大约0.025mm)。连接支柱的厚度203可以,例如,在大约0.05mm和大约0.5mm之间或在大约0.1mm和大约0.2mm之间(例如,大约0.133mm)。结构部件的纵向长度204可以,例如,在大约1mm和大约5mm之间或在大约2.5mm和大约3mm之间(例如,大约2.8mm)。结构部件之间的纵向长度205可以,例如,在大约0.25mm和大约1mm之间或在大约0.5mm和大约0.6mm之间(例如,大约0.565mm)。结构部件内的支柱的长度206(包括来回地缠绕的所有部分)可以,例如,在大约25mm和大约100mm之间或在大约65mm和大约70mm之间(例如,大约67.62mm)。假体200的总纵向长度可以,例如,在大约25mm和大约150mm之间或在大约50mm和大约70mm之间(例如,大约62mm)。如本文所描述,包括各种尺寸的许多激光切割支架、织造支架和其组合是可能的。本文描述的支柱可以包括线材或细丝或未从海波管或板切割的部分。
假体200的近端和/或远端可以任选地包括环210。例如,环210可以帮助将假体200锚定在动脉和/或静脉中。环210的圆周宽度211可以,例如,在大约0.25mm和大约1mm之间或在大约0.5mm和大约0.75mm之间(例如,大约0.63mm)。例如,环210的纵向长度212可以在大约0.25mm和大约2mm之间或在大约0.5mm和大约1mm之间(例如,大约0.785mm)。在一些实施例中,假体200的总长度与环210的纵向长度212的比可以在大约50:1和大约100:1之间(例如,大约79:1)。例如基于以下至少一项,可以调整环210的尺寸211、212:支柱厚度、假体的直径(例如,相对于脉管)、假体的总长度、材料、形状设定性质、其组合和诸如此类。
图19是假体220的另一示例实施例的示意性侧视图。假体200可以具有假体220的形状,例如在径向扩张的状态(例如,在从递送系统190部署之后)中的形状。图19图示包括第一部分221和第二部分225的假体220的示例形状。第一部分221具有大体柱形的或柱形的形状,所述形状具有在大约15mm和大约25mm之间的长度222(例如,大约21mm)和在大约2.5mm和大约5mm之间的直径223(例如,大约3.5mm)。第二部分225具有大体截头锥形的或截头锥形的形状,所述形状具有在大约30mm和大约50mm之间的长度226(例如,大约41mm)和在大约4mm和大约10mm之间、在大约4mm和大约7mm之间(例如,大约5.5mm)等的最大直径227。第二部分225远离第一部分221的锥形的角度可以在大约0.02度和大约0.03度之间(例如,大约0.024度)。
关于可以根据本文描述的方法和系统使用的假体的进一步细节在2013年3月8日提交的美国专利申请第13/791,185号中描述,其在此通过引用以其整体并入。
图20a-图20h示意性地图示了实现逆行灌注的方法的示例实施例。该程序将关于外周血管系统诸如小腿描述,也可以改为适合于其他体腔(例如心脏的、其他外周的等)。为了清楚,某些步骤诸如麻醉、切口细节、缝合等可以被省略。在一些实施例中,该程序可以从静脉到动脉执行(例如,利用来自下面的静脉导管)。
获得进入股动脉和股静脉的入口。例如使用塞尔丁格(seldinger)技术,将引导器鞘(例如,7fr(大约2.3mm))插入股动脉并将引导器鞘(例如,6fr(大约2mm))插入股静脉。将导丝(例如,0.014英寸(大约0.36mm)、0.035英寸(大约0.89mm)、0.038英寸(大约0.97mm))插入通过股动脉中的引导器鞘并引导进入胫后或胫前的患病动脉300的远侧部分。将第二导丝(例如,0.014英寸(大约0.36mm)、0.035英寸(大约0.89mm)、0.038英寸(大约0.97mm))或勒除器被插入通过股静脉中的引导器鞘。在使用勒除器的实施例中,本文描述的第三导丝、第四导丝等是准确的——即使编号可能不是连续的。
将静脉进入针经皮插入目标静脉,例如胫静脉(例如,近端胫静脉(ptv))。在一些实施例中,静脉进入针可以在超声下被引导。在一些实施例中,对比剂被可以注入朝向脚的隐静脉(逆行),然后对比剂将流入ptv。该流动路径可以使用荧光检查捕获,从而使得不通过超声或除超声之外,还可以通过荧光检查引导静脉进入针。
可以在发射导管310可能将要驻留的地方下面的近侧和远侧(例如,几英寸或几厘米)进入目标静脉。在一些实施例中,目标静脉可以是在踝中。一旦静脉进入针在静脉中,将第三导丝(或“第二”导丝,在这种情况下使用勒除器/捕捉器(snare)代替第二导丝)插入静脉进入针并在目标静脉中顺行推进直到股静脉。该进入方法可以有利地减少由于逆行推进线材穿过静脉瓣而导致的问题,其在下面进一步详细描述。例如使用荧光检查引导来捕捉(snare)第三导丝,并将其拉动通过股静脉鞘。将目标导管320在已经被捕捉的第三导丝上插入股静脉鞘。目标导管320在第三导丝上推进进入静脉系统,直到目标导管靠近胫后或胫前的患病动脉的远侧部分中的导丝和/或与所述导丝平行和/或靠近闭塞304,如图20a中所示出。
在一些实施例中,第三导丝可以包括超声接收换能器(例如,全向的),其被安装从而为由发射导管310发出的信号提供目标,或者目标导管320可以在第三导丝上前进,上述任一种情况可以允许省略某些技术(例如,股静脉进入、引入静脉引导器鞘、插入第二导丝、顺行推进第三导丝直到股静脉、捕捉第三导丝、在第三导丝上推进目标导管320)。
在一些实施例中,可以例如使用超声直接进入ptv,其可以允许将目标导管320直接放置入ptv,例如使用小的鞘,这可以允许省略某些技术(例如,股静脉进入、引入静脉引导器鞘、插入第二导丝、顺行推进第三导丝直到股静脉)。
在一些实施例中,导管320不是线上(over-the-wire)的导管,而是包括导丝和超声接收换能器(例如,全向的)。导管320可以如上面所讨论的作为第三导丝,作为第二导丝,或当直接进入ptv时作为通过小的鞘的导丝而被插入。
超声换能器通常包括两个电极,所述电极包括被可振动的陶瓷隔开的表面。进入的或接收的超声信号波可以耦合到长度延伸型式中,如图21中所示出的。图21是超声接收换能器350的示例实施例的示意性透视图。如果换能器350的近端或顶端352和换能器的远端或底端354是传导性的并且电连接至线材,换能器可以接收超声信号。在一些实施例中,换能器350的长度356在大约0.1mm和大约0.4mm之间(例如,大约0.25mm)。在一些实施例中,换能器350的重叠长度358在大约0.1mm和大约0.3mm之间(大约0.2mm)。在一些实施例中,换能器350的直径与其所安装到的导丝相似、基本相似或相同。在一些实施例中,一排或一系列层压材料可以增强换能器350的信号接收能力。
在一些实施例中,包括超声接收换能器的导丝可以包括压电膜(例如,包括塑料),其可增强换能器的信号接收能力。图22是超声接收换能器360的另一示例实施例的示意性横截面视图。图22中示出的超声接收换能器360包括任选的内腔368。超声接收换能器360包括一系列的层362、364和366。层362可以包括聚合物(例如,聚偏二氟乙烯(pvdf))层。层364可以包括无机化合物(例如,碳化钨)层。层366可以包括聚合物(例如,聚酰亚胺)层。层366的厚度可以在大约25微米(μm或微米)和大约250μm之间(例如,至少大约50μm)。
发射导管310在靠近闭塞304和闭塞304近侧的股动脉和胫动脉中的导丝上前进,如图20b中所示出。导管310可以更接近闭塞304,这取决于逆行灌注过程的解剖体那部分处的适合性。在一些实施例中,导管310可以设置在胫后动脉或胫前动脉的远侧部分,例如靠近导管320。在一些实施例中,导管310可以设置在踝的几英寸或几厘米内。
发射导管310发出指向超声信号。如图20c中箭头311、312所示出的,纵向旋转和移动发射导管310,直到信号被目标导管320接收。一旦信号被接收,这表明对准,使得针从发射导管310的延伸将导致成功进入静脉,横穿针314被推出导管310、离开胫动脉300并进入胫静脉302,如图20d中所示出的。放置横穿针314以在动脉300和静脉302之间形成瘘的准确度可以例如使用对比剂和荧光检查确认。
在一些实施例中,超声信号可以用于确定动脉300和静脉302之间的距离。再次参照图16,从所图示的屏幕的左侧到第二频率包络的前缘的距离可以被用作导管之间距离的指示。
再次参照图16,显示设备可以图形地示出信号对准峰值,以允许使用者确定对准位置。在一些实施例中,信号对准可以改变阈值以上或以下的颜色,例如从红色到绿色。在一些实施例中,例如当对准信号跨越阈值时,可以发出音频信号,这可以允许使用者保持专注于患者而不是基本连续不断地监视屏幕。
在一些实施例中,屏幕上的水平线在程序期间可以上移以表明达到该点的最大信号值或峰值。这条线可以称为“峰值保持”。如果达到更大的信号值,则水平线移动以匹配该更高的值。如果没有操纵能够将峰值提升到超过水平线,则那可以表明最大对准。如果信号峰值下降到水平线以下的某个量,则导管可能已经移动并且不再被适当地对准。因为由水平线表示的对准水平先前在程序期间已经达到,所以使用者知道这样的对准水平可以通过进一步旋转操纵和/或纵向操纵来达到。
第四导丝316(例如,0.014英寸(大约0.36mm))(或“第三”导丝,在这种情况下使用勒除器代替第二导丝)被放置通过导管310的横穿针314的内腔并且以(静脉302的)逆行方向朝向脚进入胫静脉302,如图20e中所示出。外部套压力可以在针横穿点以上施加,以降低动脉300中的流动,从而抑制或防止血肿的形成,和/或使静脉充血以促进瓣膜穿过。导管310、320可以被移除,留下导丝316在适合的位置,从股动脉中的引导器鞘延伸,通过动脉树,并进入胫静脉302。
代替本文描述的指向超声技术或除指向超声技术之外,还可以使用从动脉300到静脉302穿过导丝316的某些技术。
在一些实施例中,止血带可以应用至腿,其可以增加静脉直径。在一些实施例中,封堵剂(例如,如关于图4和图7所讨论的,封堵球囊等)可以用于增加静脉直径。例如,静脉流可以倒退,使静脉扩大。较大的静脉直径可以为横穿针314产生更大的目标,使利用横穿针314更容易进入静脉300。
在一些实施例中,pta球囊可以在目标静脉中使用,并且针导管(例如,outback,可购自cordis)可以在荧光检查下靶向pta球囊。横穿针314可以刺穿pta球囊,并且pta球囊压力的降低可以确认横穿针314的适当对准。pta球囊可以增加静脉直径,为横穿针314产生更大的目标,使利用横穿针314更容易进入静脉300。导丝316可以被推进通过横穿针314并进入pta球囊。
在一些实施例中,pta球囊包括例如嵌入球囊的聚合物中的网状物(例如,织造网)。当刺穿不具有这种网状物的球囊时,球囊材料可能破裂并引起栓子(例如,下游漂浮的球囊块)。网状物可以帮助限制球囊材料的撕裂,这可以抑制或防止球囊材料引起栓子。
在一些实施例中,沿着导管的轴线纵向地隔开的两个pta球囊可以在目标静脉中使用,并且针导管可以靶向pta球囊中的一个。在通过横穿针314刺穿pta球囊中的一个之后,pta球囊之间的井(well)中的对比剂可以被释放,这是因为刺穿的球囊不再充当对比剂的坝(dam)。对比剂的释放可以通过使用荧光检查被监控。pta球囊可以在相同的导管上或在不同的导管上。
在一些实施例中,沿着导管的轴线纵向地隔开的两个pta球囊可以在目标静脉中使用,并且针导管可以靶向pta球囊之间的空间或井。在通过横穿针314刺穿井之后,井中的对比剂可以被干扰。对比剂的干扰可以通过使用荧光检查被监控。pta球囊可以在相同的导管上或在不同的导管上。
在pta球囊可以在目标静脉中与超声目标组合使用的一些实施例中,pta球囊导管包括pta球囊和超声接收换能器(例如,全向的)。在某些这样的实施例中,发射导管310可以在荧光检查下靶向pta球囊和/或可以靶向超声接收换能器,如本文所描述的。横穿针314可以刺穿pta球囊,并且pta球囊的压力降低可以确认横穿针314的适当对准。pta球囊可以增加静脉直径,为横穿针314产生更大的目标,使利用横穿针314更容易进入静脉300。导丝316可以被推进通过横穿针314并进入pta球囊。
在一些实施例中,lemaitre设备(例如,unballoontmnon-occlusivemodelingcatheter(非闭塞型导管),可购自马萨诸塞州的burlington的lemaitrevascular)可以在目标静脉中使用。在一些实施例中,lemaitre设备可以增加静脉直径。较大的静脉直径可以为横穿针314产生更大的目标,使利用横穿针314更容易进入静脉300。在一些实施例中,针314可以刺入lemaitre设备。在某些这样的实施例中,lemaitre设备可以充当横穿针314的网状物目标(例如,包括在荧光检查下可见的不透射线材料)。lemaitre设备的网状物可以通过向远推进网状物的近侧部分和/或向近侧缩回网状物的远侧部分(例如,像伞一样一起推动末端)和/或通过使网状物自扩张(例如,在网状物的至少一些部分包括形状记忆材料的实施例中)而被径向地扩张。在一些实施例中,lemaitre设备可以紧握横穿线材以当lemaitre设备接近时将横穿线材保持在目标静脉中。
在一些实施例中,发射导管310可以包括具有第一极性的第一磁体,并且目标导管320可以包括具有第二极性的第二磁体。当磁体足够接近以使磁力移动导管310、320的一个或两个时,横穿针314可以被推进以在动脉300和静脉302之间建立瘘。在一些实施例中,第一磁体可以与横穿针314周向对准,和/或发射导管310可以被磁屏蔽以提供旋转对准。在一些实施例中,第二磁体可以是纵向相对薄的以提供纵向对准。在一些实施例中,横穿针314和/或导丝316可以从动脉300被磁性地拉到静脉302,或者反之亦然。一些系统可以包括超声引导和磁引导二者。例如,超声引导可以用于初始对准,而磁引导可以用于精确对准。
再次参照图20a-20h,携带假体340的假体递送系统330在导丝316上前进通过动脉300和静脉300之间的间隙区(interstitialspace),然后进入静脉300,如图20f中所示出的。在一些实施例中,单独的pta球囊导管(例如,大约2mm)可以在导丝316上前进以在引入假体递送系统330之前预扩大动脉300和静脉302之间的瘘。pta球囊导管的使用可以取决于,例如,假体340的径向强度。
假体340例如通过操作触发器把手194(图17)从假体递送系统330部署。在一些实施例中,例如,如果假体340不能扩张和/或推进,则可以移除假体递送系统330,并且在导丝316上推进pta导管(例如,大约2mm)以试图扩大或进一步扩大动脉300和静脉302之间的瘘。然后可以重新尝试部署假体340(例如,通过自扩张、球囊扩张等)。在一些实施例中,假体340的部署可以重塑脉管,例如使脉管的直径扩张至少大约10%、至少大约20%、至少大约30%或更多、在大约0%和大约10%之间、在大约0%和大约20%之间、在大约0%和大约30%之间或更多。在假体340是自扩张的实施例中,重塑程度可以随时间改变,例如当脉管扩张时假体340扩张或当脉管收缩时假体340收缩。
一旦假体340部署,如图20g中所示出的,可以利用pta导管扩大瘘。pta导管的直径(例如,大约3mm至大约6mm)可以至少部分地基于以下选择:动脉300的直径、静脉302的直径、间质组织的组成、假体340的特性、其组合和诸如此类。在一些实施例中,假体递送系统330可以包括(例如,在假体340的近侧或远侧的)pta球囊导管,其可用于本文描述的任选的pta球囊导管技术的一个、几个或全部。在假体包括圆锥形部分的实施例中,pta球囊可以包括圆锥形部分。一旦假体340在适当的位置,可以移除假体递送系统330,如图20h中所示出的。av瘘因此被形成在动脉300和静脉302之间。各种导管310、320、330和假体340的放置的确认可以在荧光检查下使用对比剂注入贯穿部分或整个程序确认。
在一些实施例中,标记物(例如,夹子、柳叶刀、剪刀、铅笔等)可以被施加至皮肤(例如,粘附到皮肤、放置在其顶部上等),从而在假体340的部署之前近似地标记由横穿针314在动脉300和静脉302之间形成的瘘的位置。在使用者使用在瘘上膨胀的血压计以避免出血的实施例中,血流的缺乏可以致使瘘部位的可视化或甚至估计困难,标记物可以提供这种识别。在发送导管和接收导管在瘘形成之后被移除的实施例中,跨越点可能对于使用者难以感觉或确定,而标记物可以提供这样的识别。如果瘘将被扩大,则扩大球囊的中点可以优选地与瘘的中点对准(例如,以增加通过间隙区的孔或使其最大化)。在一些实施例中,标记物可以在荧光检查下可视化(例如,包括不透射线的材料)以允许使用者在假体340的部署之前在荧光检查下看到或记住瘘的位置。
一旦假体340在适当的位置,血液流过静脉302并进入脚的障碍是静脉中的瓣膜。操纵导丝穿过静脉瓣可能是挑战性的,例如因为来自动脉的压力可能不足以扩充静脉并使瓣膜关闭不全(incompetent)。申请人已经发现可以使用许多技术的一种或更多种诸如pta导管、支架(例如,被覆盖的支架、支架移植物等)和瓣膜刀使av瘘远侧的静脉瓣失去能力或使其关闭不全,如下面进一步详细描述的。使静脉瓣失去能力可以允许血液经逆行灌注从股动脉流动,在静脉302中逆行,并在静脉中逆行至小静脉(venuole)和至脚的静脉循环远部的毛细血管以提供含氧血液至cli患者的脚。
在一些实施例中,高压pta球囊导管可以用于使静脉瓣关闭不全(例如,当膨胀至大于大约10atm(大约1013千帕斯卡(kpa))时)。
在一些实施例中,可以将一个或更多个支架跨过一个或更多个静脉瓣放置,以致使那些瓣膜关闭不全。例如,这样的支架应当具有使瓣膜保持打开的足够径向力。支架可能强有力地使瓣膜破裂。在一些实施例中,支架包含覆盖物或移植物。某些这样的实施例能够覆盖静脉侧副管。在一些实施例中,支架是裸露的或没有覆盖物或移植物。某些这样的实施例能够降低成本。静脉支架可以沿着静脉的长度(例如整个长度)延伸。例如,在一些实施例中,ptv的整个长度与被覆盖的支架成一直线,覆盖静脉侧副管,干扰静脉瓣。
在一些实施例中,静脉支架与瘘假体分开。单独的静脉支架可以允许在一些性质(诸如尺寸(例如,长度、直径)、材料(例如,有或没有覆盖物或移植物))和其他性质上更灵活。图31a示意性地图示了与静脉支架342的示例实施例分开的动静脉瘘支架340的示例实施例。静脉支架342可以与瘘支架340间隔开(例如,如在图31a中图示的),紧靠瘘支架340,或与瘘支架340重叠、套叠或同轴(例如,瘘支架340的远侧节段至少部分地在静脉支架342的近侧节段内部,或静脉支架342的近侧节段至少部分地在瘘支架340的远侧节段内部)。在瘘支架340和静脉支架342重叠的实施例中,静脉支架342的放置首先能够允许静脉支架342的面向逆行血流方向的近端被瘘支架340覆盖,以减少或消除可能由于静脉支架342的远端而发生的血流干扰。在瘘支架340和静脉支架342重叠的实施例中,静脉支架342的放置其次能够通过瘘支架340,使得两个支架340、342能够共享至少一个部署参数(例如,使支架部署设备在相同导丝上前进)。静脉支架342可以在瘘支架340之前或之后被部署。静脉支架342可以具有在大约2cm和大约30cm之间的长度(例如,大约2cm、大约3cm、大约4cm、大约5cm、大约6cm、大约7cm、大约8cm、大约9cm、大约10cm、大约11cm、大约12cm、大约13cm、大约14cm、大约15cm、大约16cm、大约17cm、大约18cm、大约19cm、大约20cm、大约21cm、大约22cm、大约23cm、大约24cm、大约25cm、大约26cm、大约27cm、大约28cm、大约29cm、大约30cm、在这样的值之间的范围等)。
在一些实施例中,静脉支架与瘘假体一体。一体的静脉支架可以允许在一些性质(诸如尺寸(例如,长度、直径)、材料(例如,有或没有覆盖物或移植物))和其他性质上更灵活。图31b示意性地图示了包含集成的静脉支架的示例实施例动静脉瘘支架344。图31c示意性地图示了包含集成的静脉支架的瘘支架344的示例实施例。支架344包含被配置为锚定在动脉中的第一部分346、被配置为锚定在静脉中并填充一定长度的静脉的第二部分350、以及纵向地在第一部分346和第二部分350之间的第三部分348。在第一部分346和第二部分350具有不同直径的实施例中(例如,如在图31c中图示的),第三部分348可以是呈锥形的。在一些实施例中,被配置为填充静脉的第二部分350的一部分具有与第二部分350的其他部分不同的性质(例如,直径、材料、径向强度、其组合和诸如此类)。第二区段350的长度可以大于第一区段346的长度。例如,第二区段350可以具有被配置为填充脉管(诸如ptv)的长度。第二区段350可以具有在大约2cm和大约30cm之间的长度(例如,大约2cm、大约3cm、大约4cm、大约5cm、大约6cm、大约7cm、大约8cm、大约9cm、大约10cm、大约11cm、大约12cm、大约13cm、大约14cm、大约15cm、大约16cm、大约17cm、大约18cm、大约19cm、大约20cm、大约21cm、大约22cm、大约23cm、大约24cm、大约25cm、大约26cm、大约27cm、大约28cm、大约29cm、大约30cm、在这样的值之间的范围等)。
在一些原位旁路程序中,隐静脉被附连至大腿中的动脉和小腿中的另一动脉,绕过动脉中的所有堵塞。在某些这样的程序中,静脉不从患者剥出,纵长倒转(flip),并用作假体,而是停留在原处以便血流是逆行的(针对静脉的瓣膜)。可将标准瓣膜刀从下面放入隐静脉和并且将其以塌缩状态推进至顶部、打开然后以打开状态向后拉,沿着路径切割静脉瓣。这种瓣膜刀的切割表面面向后,从而在这些程序期间在缩回期间切割。图23a是瓣膜刀400的示例实施例的示意性透视图,所述瓣膜刀400可以与这样的程序一起使用,包括面向近侧的刀片402。
在本文描述的方法的一些实施例中,静脉瓣远侧的入口是不可用的,使得向后拉瓣膜刀是不可能的,但是如本文描述的向前推动反向瓣膜刀是可能的。图23b是可以与这种程序一起使用的瓣膜刀410的示例实施例的示意性透视图。反向瓣膜刀410包括面向前或远侧的一个或多个刀片412(例如,2-5个刀片(例如,3个刀片)),以便当反向瓣膜刀410向远侧推进时可以切割瓣膜。至少因为逆行进入至待失去能力的静脉先前不被认为是问题,所以不存在先验动机来反转瓣膜刀的刀片的方向从而形成如本文所描述的反向瓣膜刀410。反向瓣膜刀410可以在导丝414上前进,导丝414可以被操纵进入静脉,用于使静脉瓣关闭不全。如本文所描述的在动脉和静脉之间形成瘘之后,静脉中的流体流是以与静脉中流体流的天然的或正常的或程序前的方向相反的方向,以便以与天然流体流相反的方向但是以瘘后流体流的方向推动反向瓣膜刀410。
其他系统和方法也能够用于使静脉中的瓣膜关闭不全(例如,切割球囊、旋切术(atherectomy)、激光切除、超声切除、加热、射频(rf)切除、具有正被推进和/或缩回的创伤的或非无创伤的端头的导管(例如,引导器鞘)、其组合和诸如此类)。
在使这种瓣膜关闭不全之前以逆行方式穿过静脉瓣也可以是有挑战性的。图24是lemaitre设备420的示例实施例的示意性透视图,lemaitre设备420可以用于径向地扩张静脉并因此扩张它们的瓣膜。lemaitre设备420包括可扩张的椭圆形的或长形的叶形422,例如自扩张的镍钛诺网。在一些实施例中,pta球囊导管可以用于径向地扩张静脉并因此径向地扩张它们的瓣膜。在一些实施例中,将止血带应用至腿可以径向地扩张静脉并因此径向地扩张它们的瓣膜。在径向扩张之后,可以将导丝推进通过(一个或更多个)伸展的瓣膜(例如,通过扩张设备诸如lemaitre设备)和导管(例如,pta、支架递送、旋切术等)或其他线上(over-the-wire)设备可以在导丝上推进。
图26a和26b示意性地图示了用于实现逆行灌注的方法的另一示例实施例。再次参照图20e,瘘可以利用在本文中描述的技术和/或其他技术中的一种或更多种借助于延伸其中的导丝606被建立在包括闭塞604的动脉600和静脉602之间。携带假体620的假体递送系统在导丝606上前进通过动脉600和静脉602之间的间隙区并进入静脉602,如在图26a中示出的。在一些实施例中,单独的pta球囊导管(例如,大约2mm)能够在导丝606上前进以在假体递送系统的引入之前预先扩大动脉600和静脉602之间的瘘。pta球囊导管的使用可以取决于例如假体620的径向强度。假体620可以是图25a-25c的支架500、520、540或其变化(例如,如关于图25c描述的),支架包括被配置为转向血流的未被覆盖的且低孔隙度的织造细丝。
未被覆盖的织造细丝的流动转向性质可以取决于血管腔的某些血流动力学特性。例如,如果闭塞604不完全使得一些压降可以发生在假体620的内腔与闭塞604和假体620之间的动脉600部分之间,血液可以能够流过假体620的侧壁而非进入瘘。再次参照图4和封堵材料251的描述,封堵材料608可以被可选地提供在动脉600中以进一步闭塞动脉600,这能够阻止可能引起和/或允许血液流过假体620的侧壁的流体动力学效果。对于另一示例,动脉600和静脉602之间的压降可以引起和/或允许血液沿静脉血流的正常方向流过假体的侧壁而非流过假体的内腔以实现逆行灌注。再次参照图4和封堵材料251的描述,封堵材料610可以被可选地提供在静脉602中,从而在正常静脉流下闭塞瘘下游的静脉602部分,这能够阻止可能引起和/或允许血液流过假体620的侧壁的流体动力学效果。
例如通过操作触发器把手194(图17),从假体递送系统部署假体620。在一些实施例中,例如如果假体620不能扩张和/或推进,假体递送系统可以被移除,并且pta导管(例如,大约2mm)在导丝620上推进以尝试扩大或进一步扩大动脉600和静脉602之间的瘘。假体620的部署然后可以被重新尝试(例如,通过自扩张、球囊扩张等)。在一些实施例中,假体620的部署可以重塑脉管,例如如在本文中描述的那样扩张脉管的直径。在假体620为自扩张的实施例中,重塑的程度可以随着时间而改变,例如当脉管扩张时假体620扩张或当脉管收缩时假体620收缩。假体620可以顺从假体620被部署在其中的解剖结构。例如,在手术台或台面上在扩张状态下,假体620可以为大体柱形,但是假体620可以顺从脉管和瘘的直径,其中假体620被部署在血管和瘘中使得假体可以具有在不同纵向节段中的不同直径、锥度、非柱形形状、其组合和诸如此类。
在假体620包含补充支撑结构(例如,如关于图25b描述的)的一些实施例中,假体的部署可以包含部署第一织造结构,并且在部署第一织造结构之前、期间和/或之后,部署补充支撑结构。
瘘可以可选地在部署假体620之前、期间和/或之后利用pta导管被扩大。pta导管的直径(例如,大约3mm至大约6mm)可以至少部分地基于以下进行选择:动脉600的直径、静脉602的直径、间质组织的成分、假体620的特性、其组合和诸如此类。
一旦假体620在适当位置中,假体递送系统就可以被移除,如在图26b中示出的。av瘘由此被形成在动脉600和静脉602之间。即使假体缺少或没有移植物材料,由于低孔隙度(例如,小于大约50%孔隙度或在本文中描述的其他值)的血流动力学效果,血液也流过假体620的内腔。图26b示出了封堵材料608、610未被使用的实施方式。一旦假体620在适当位置中,就可以例如如在本文中描述的那样使静脉中的瓣膜关闭不全。
在假体620包含可以被单独部署的两组多个细丝(例如,如关于图25b的某些实施例描述的)的实施例中,多个细丝可以被至少部分地同时部署,在没有介入步骤的情况下被顺序地部署,或在具有介入步骤(诸如在本文描述的pta步骤)的情况下被顺序地部署。
图27示意性地图示了用于实现逆行灌注的假体720和方法的另一示例实施例。尽管一些尺寸并且甚至“10mm”的示例尺度被提供,但是在其中图示的特征的形状、尺寸、位置关系等可以改变。假体720被定位在包括闭塞704的动脉700中、在静脉702中,并且跨越动脉700和静脉702之间的间质组织t。假体720可以例如如在本文中描述的那样和/或利用其他方法被定位。在一些实施例中,假体720通过具有与5fr(1.67mm)内直径的递送系统在具有2fr(0.67mm)外直径的导丝上被递送。
在一些实施例中,其第一纵向区段722、第二纵向区段724、和/或第三纵向区段726、或其一个或更多个部分的孔隙度可以在大约0%和大约50%之间并在其之间的范围内变动,例如如在本文中描述的。来自动脉700的血流可以通过假体720被转向到静脉702内,例如由于血流动力学力,诸如动脉700和静脉702之间的压力差。假体720的低孔隙度可以允许流体基本流过假体720的内腔而基本不灌注通过假体720的侧壁。在一些实施例中,朝向假体720的末端的近侧部分和/或远侧部分可以被配置为附着脉管侧壁,例如具有更低的孔隙度,因为血液不可能流过那些部分。
在本文中描述的技术可以对形成心脏附近、外周中、或甚至下肢(足底弓)中的两个体腔之间的瘘有用。图28a和图28b分别示意性地图示脚的动脉和静脉。瘘或吻合可以被形成在脚的两个血管之间。在一个示例中,从动脉到静脉的通道在中间外侧足底中从足底外侧动脉到足底外侧静脉被形成。
向脚供应血液的动脉被闭塞,并且内膜下空间钙化。线材被向远侧推动,并横穿到相邻静脉。动脉和静脉之间的孔利用1.5mm球囊被扩大,例如因为小动静脉瘘都不应造成在该位置处或在该位置中对患者的任何太大的伤害。在扩大之后,血液开始从动脉流至静脉而无泄漏。在这样的流动被确认之后,空间的进一步扩大利用更大的球囊(2.0mm、2.5mm、3.0mm)以更大的压力(例如,20-30atm)被执行。即使没有放置支架、移植物、支撑架(scaffolding)、或其他类型的设备,泄漏也惊人地极小或不存在。不包括假体的程序可以降低成本、程序时间、复杂性、其组合和/或诸如此类。足底外侧静脉直接进入前脚的静脉弓,使其成为向脚的该部分供应血液的杰出候选物。患者在程序之前在脚中有许多疼痛,并且在程序之后在脚中没有疼痛,表明血液能够如在本文中描述的那样被逆行供应通过静脉。瘘或吻合维持设备可以对于某些情况被可选地省略,诸如对于远侧或下肢动脉和静脉可以被描述为“胶着(glued)”在周围组织(例如,中间的足底外侧动脉和静脉)中的血液透析的情况。
在一些情况下,瘘或吻合维持设备可以被可选地使用。若干瘘维持设备在文本中进行描述。图29示意性地图示了吻合设备800的示例实施例。吻合设备包括第一区段802、第二区段804、以及可选地纵向地在第一区段802和第二区段804之间的第三区段806。第一区段802可以被配置为锚定在第一体腔(例如血管,诸如动脉或静脉)中。第一区段802可以包括可扩张构件、倒钩等。第二区段804可以被配置为锚定在第二体腔(例如血管,诸如动脉或静脉,其可以是第一体腔的相反类型)中。第三区段806可以被配置为跨越在第一体腔和第二体腔的内腔之间。在一些实施例中,在第一体腔和第二体腔的内腔之间的空间通常包含脉管壁,使得第三区段806的尺寸可以很小或甚至被省略。
一些吻合设备可用和/或已经被研发用于治疗更大脉管中的孔(例如,来自medtronic的spyder、来自johnsonandjohnson的corlink、来自st.judemedical的symmetry、来自cardica的pas-port和来自roxmedical的roxcoupler)。例如如果被重新定尺寸和/或被重新构造,这样的设备可以适于应用于外周或下肢中。其他设备也是可能的。
图30示意性地图示了利用跨越血管902和904的壁的吻合设备800被耦接在一起的两个血管902和904的示例实施例。血管902是动脉,如通过具有厚壁示意性地示出的,并且血管904是静脉。血管和其他体腔的其他组合也是可能的。在通道906例如如在本文中描述的那样(例如,利用线材、可部署针、一个或更多个球囊等)被形成在第一血管902和第二血管904之间之后,吻合设备800被部署。例如,吻合设备800部署系统的远端可以驻留在第一血管902中,并且部分地延伸通过通道906。吻合设备800的第一区段802可以被部署通过通道906和在第二血管904中。在部署后,第一区段802可以自扩张,例如以附着第二血管904的壁。吻合设备800的第三区段806可以被部署通过通道906。在部署后,第三区段806可以自扩张,例如从而附着通道906周围的组织并维持通过通道906的开放性。吻合设备800的第二区段804可以被部署在第一血管902中。在部署后,第二区段804可以自扩张,例如从而附着第一血管902的壁。第一区段802、第二区段804和第三区段806中的一个或更多个可以利用球囊被扩张。不同的球囊或一系列球囊能够被用于吻合设备800的不同区段802、804、806。
虽然一些示例实施例已经在本文中详细公开,但是这已经通过示例并且仅出于说明的目的进行。上述的实施例不意欲关于所附权利要求的范围作为限制。发明人预想到可以对本发明进行各种替换、改变和修改而不背离权利要求书中所限定的本发明的精神和范围。
虽然本文描述的设备可以在流过设备的流体是液体诸如血液的应用中使用,但是设备也可以或可替换地在应用诸如流体是气体诸如空气的气管或支气管手术中使用。在一些实施例中,流体可以包含固体物质,例如栓子或,包含在流体包括食物颗粒的胃外科手术中的固体物质。
虽然本发明易于各种修改和可替换形式,但是其具体的示例已经在附图中示出并且在本文中详细描述。但是,应当理解,本发明不限于所公开的具体的形式或方法,而是,相反,本发明覆盖落入所描述的各种实施例和所附权利要求的精神和范围内的所有的修改、等同物和可替换方案。本文公开的任何方法不必以所叙述的顺序执行。本文公开的方法包括由从业者采取的某些行动;但是,它们也可以包括这些行动的任何第三方指示,无论其明确地或隐含地。例如,行动诸如“使第一脉管中的瓣膜关闭不全”包括“指示使第一脉管中的瓣膜关闭不全”。本文公开的范围也包含任何和所有的重叠、子范围和其组合。语言诸如“高达”、“至少”、“大于”、“小于”、“之间”等包括所叙述的数字。冠以术语诸如“大约”或“近似地”的数字包括所述的数字。例如,“大约10mm”包括“10mm”。冠以术语诸如“基本上/大体”的术语或短语包括所述的术语或短语。例如,“基本平行/大体平行”包括“平行”。
- 还没有人留言评论。精彩留言会获得点赞!