一种具有强耐盐能力的智能型胰岛素递送体系及制备工艺的制作方法
本发明属于生物材料领域,具体涉及一种含苯硼酸酯片段和谷氨酸片段的复合纳米药物递送体系及其制备工艺。
技术背景
糖尿病是一种全球范围内的公共流行疾病,预计到2035年人数将增至5.92亿。目前,糖尿病患者需要终生治疗来维持血糖浓度在正常水平和防止急性并发症的发生。对于胰岛素依赖性糖尿病患者,每天一次或多次皮下注射胰岛素是最为有效的治疗方法,而这同时给患者带来极大的痛苦。因此,亟需寻找一种能够根据人体血糖浓度波动而智能的调节胰岛素释放的给药体系。近年来,基于苯硼酸的糖响应材料引起研究者极大的兴趣。这种材料在构建自律性胰岛素递送体系中有很大潜在应用价值。在此基础上设计出来的苯硼酸酯基糖响应材料可有效降低苯硼酸的pka,提高材料糖灵敏性。由于糖分子与有机硼的结合能力高于频哪醇,当加入葡萄糖时,疏水片段上的苯硼酸与糖分子结合,以苯硼酸酯-糖复合物的形式离去,此时疏水片段的疏水性减弱,亲水性增加,纳米粒子的内核疏松,胰岛素释放。
到目前为止,糖响应型纳米胰岛素递送体系在生理条件(ph7.4,0.15mpbs)下的稳定性是一个重要因素。聚肽作为生物相容性和生物可降解性材料之一,通过自组装可形成独特的二级结构,这赋予纳米粒子在结构和性质上诸多特性提供潜在的可能。将聚肽片段引入糖响应体系,旨在提高胰岛素递送体系在生理条件下的稳定性。聚谷氨酸苄酯(pblg)在生理条件下会形成稳定的二级结构,如α-螺旋,β-折叠。这种二级结构在改善递送体系稳定性方面有一定的效果。以共自组装方式,pblg和ppbdema作为疏水片段提供疏水驱动力,形成纳米胶束的疏水内核,片段刚性的适当提高,必然会对纳米粒子的稳定性做出贡献。另外,聚肽具有很好的生物相容性和生物可降解性,这在实际应用中具有很大的价值。
技术实现要素:
本发明采用共自组装方法,制备一种生物相容性好、可降解的复合纳米药物递送体系,在生理条件下(如0.15mpbs,ph7.4及37℃),纳米粒子能稳定存在而不会因为高盐离子强度而自身瓦解,同时,能高度识别不同糖浓度,即正常血糖浓度不发生响应,高血糖浓度所包裹药物分子稳定释放,从而实现药物分子智能可控释放,达到治疗疾病的目的。
本发明提出,在生理条件下(如0.15mpbs,ph7.4及37℃),一种具有强耐盐能力的智能型胰岛素递送体系,其特征在于,两亲性聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg)与聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema)通过共自组装的方式得到复合纳米药物载体;复合纳米药物载体包裹胰岛素形成包裹胰岛素的复合纳米粒子药物递送体系;
聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg)的结构式如下:
22≤m≤440,10≤n≤100,其中m,n均为整数;
聚合物聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema)结构式如下:p-2或p-3
22≤p≤440,10≤q≤100,其中p、q均为整数;
或
22≤p≤440,10≤q≤100,其中p、q均为整数。
聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg)与聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema)共自组装,聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg)与聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema)可以按任意比例,优选聚乙二醇-嵌-聚谷氨酸苄酯的质量百分含量为10-75%。
一种具有强耐盐能力的智能型胰岛素递送体系的制备方法,其具体步骤如下:
①合成聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg)与聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema);
1)通过自由基聚合反应得到聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema);
p-2的制备,包括以下步骤:
(1)以聚乙二醇单甲醚(mpeg-oh)为原料,通过与2-溴丙酰溴进行一步酰化反应得到引发剂甲氧基聚乙二醇-溴(mpeg-br);
(2)将大分子引发剂甲氧基聚乙二醇-溴(mpeg-br)、苯硼酸酯单体(pbdema)、cubr2、五甲基二乙烯三胺(pmdeta)和苯甲醚加入到schlenk瓶中,对体系进行除水除氧,氮气保护下加入cubr,将schlenk瓶置于70~100℃下反应。反应后,采用中性al2o3柱子除铜盐,在冰的正己烷和无水乙醚的混合液沉淀三次,v正/v乙=4/1,得到聚合物p-2;
上述优选甲氧基聚乙二醇-溴(mpeg-br)、cubr2、五甲基二乙烯三胺(pmdeta)、cubr的摩尔比为mpeg-br:cubr2:pmdeta:cubr=1:0.05:1.25:1,其中苯硼酸酯单体(pbdema)可根据重复单元进行调节。
p-3的制备,包括以下步骤:
(1)以聚乙二醇单甲醚(mpeg-oh)和tscl(对甲苯磺酰氯)为原料,在溶剂dcm(二氯甲烷)和tea(三乙胺)作用下,得到单端ts保护的甲氧基聚乙二醇(mpeg-ts),接着在dmf(n,n-二甲基甲酰胺)中与nan3(叠氮化钠)反应得到单端叠氮化的甲氧基聚乙二醇(mpeg-n3),mpeg-n3与炔基端小分子链转移试剂(alkyne-cpad)通过click反应得到大分子链转移试剂(mpeg-cpad);
(2)将大分子链转移试剂(mpeg-cpad)、2-苯硼酸酯-5-乙基-5’-羟甲基-1,3-二氧己环)丙烯酸酯单体(pbdema)、aibn和无水甲苯加入到schlenk瓶中,对体系进行除水除氧,氮气保护下,将schlenk瓶加热反应,反应后,采用中性al2o3柱子除铜盐,在冰的无水乙醚中沉淀,得到聚合物p-3;
上述优选aibn:mpeg-cpad的摩尔比=1:5,其中2-苯硼酸酯-5-乙基-5’-羟甲基-1,3-二氧己环)丙烯酸酯单体(pbdema)可根据聚合物中重复单元个数进行调节。
其中:
(2-苯硼酸酯-5-乙基-1,3-二氧己环)丙烯酸酯(pbdema)的制备步骤如下:
惰性气体环境中,以1,1,1-三羟甲基丙胺与苯硼酸为反应原料,甲苯为反应溶剂,置于90~140℃下反应,反应体系浓缩,抽真空得到白色固体为2-苯硼酸酯-5-乙基-5,-羟甲基-1,3-二氧六环(1);在无水无氧条件下,以(1)和丙烯酰氯作为反应物,在溶剂二氯甲烷(ch2cl2)和三乙胺(et3n)作用下,通过酰化反应得到2-苯硼酸酯-5-乙基-1,3-二氧己环)丙烯酸酯(pbdema)(2)。
2)通过开环聚合反应得到聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg);
以γ-苄基-l-谷氨酸(h-glu(obzl)-oh)为起始原料,通过三光气法制备得到l-谷氨酸-γ-苄酯n-羧基内酸酐(blg-nca);以甲氧基聚乙二醇氨基盐酸盐(mpeg-nh2·hcl)作为引发剂引发blg-nca单体开环聚合得到聚合物聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg);
在无水无氧环境下,称取mpeg-nh2·hcl于充满氮气的反应瓶中,将其放到油浴中抽真空进一步除水,加入干燥dmf溶解;将blg-nca溶解在干燥dmf中,然后加入到mpeg-nh2·hcl溶液中,加热反应,反应结束后,反应体系在无水乙醚中沉淀,用chcl3溶解,重复沉淀溶解结晶,真空干燥,得到mpeg-b-pblg;
其中l-谷氨酸-γ-苄酯n-羧基内酸酐(blg-nca)的合成步骤如下:
无水无氧条件下,以γ-苄基-l-谷氨酸(h-glu(obzl)-oh)和三光气(btc)为起始反应物,以thf作为反应溶剂,置于40~60℃下反应,至溶液变澄清透明(黄色)。除去溶剂thf,于正己烷/四氢呋喃体积比为3/1中进行重结晶三次,得到白的针状晶体,为blg-nca。
②制备复合纳米药物递送体系:
避光条件下,将聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg)、聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema)溶于有机溶剂中,得到聚合物有机溶液,将聚合物有机溶液加入到含有胰岛素的水溶液中,在通风的条件下搅拌均匀并使部分有机溶剂挥发,得到混合液,然后将混合液转移至渗析袋中,在超纯水中渗析得到对应的包裹胰岛素的复合纳米粒子药物递送体系;
在上述混合液中整个聚合物材料的浓度优选为0.5~1.0mg/ml。
制备包裹胰岛素的复合纳米粒子药物递送体系时,胰岛素占聚合物的质量分数为10%~100%;
所用的甲氧基聚乙二醇氨基盐酸盐(mpeg-nh2·hcl)和聚乙二醇单甲醚(mpeg-oh)的分子量优选为1000~20000。
原子转移自由基聚合法(atrp)所用的大分子引发剂为mpeg-br,可逆加成-断裂链转移聚合(raft)所用的大分子链转移试剂为mpeg-cpad,其分子量优选为1000~20000。
所用的有机溶剂优选为n,n-二甲基甲酰胺(dmf)或四氢呋喃(thf)。
基于聚乙二醇-嵌-聚谷氨酸苄酯(mpeg-b-pblg)和聚乙二醇-嵌-聚苯硼酸酯(mpeg-b-ppbdema)的成功制备,通过共自组装的方式利用聚肽片段特有的二级结构提高纳米粒子的耐盐稳定性,加强生理条件下糖响应片段识别糖浓度的能力。
附图说明:
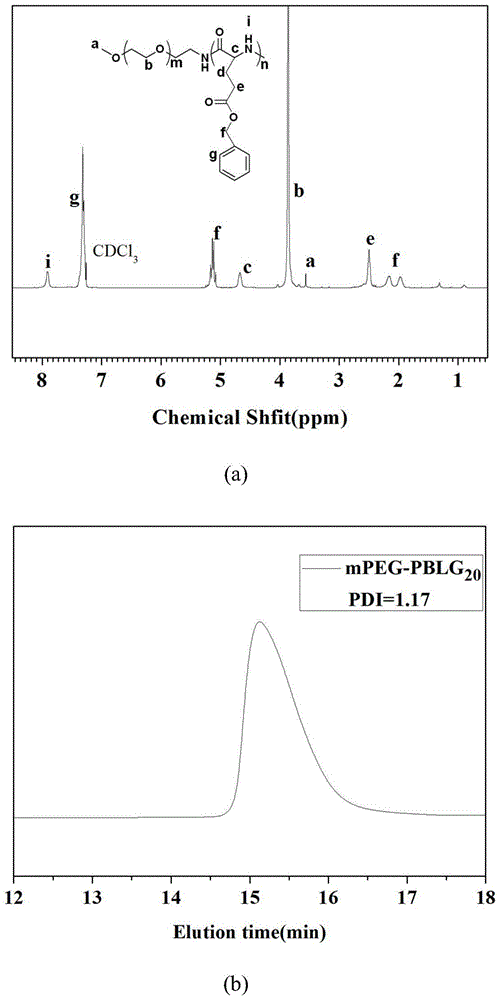
图1为实施例1中聚合物p-1相关表征图:
(a)聚合物p-1的1hnmr表征
(b)聚合物p-1的gpc表征
图2为实施例1中聚合物p-2相关表征图:
(a)聚合物p-2的1hnmr表征
(b)聚合物p-2的gpc表征
图3为实施例1以p-1质量分数为75%复合纳米载体的药物递送体系tem图;
图4实施例1聚合物p-1的质量百分含量为75%的复合纳米粒子在0.15mpbs不同糖浓度下胰岛素释放情况;
图5实施例1聚合物p-1的质量百分含量为75%的复合纳米粒子在0.15mpbs中脉冲式糖响应释放情况。
具体实施方式:
下面结合实施例对本发明进一步说明,但本发明并不仅限于以下实施例。
实施例1
①合成聚合物mpeg-b-pblg(p-1)
1)称量6.0g(22.0mmol)γ-苄基-l-谷氨酸(h-glu(obzl)-oh)和2.6g(8.8mmol)三光气(btc),加入到充满氮气干燥的schlenk瓶中,于氮气保护下加入150mlthf(溶剂用量约为1.0gh-glu(obzl)-oh/25mlthf),于50℃油浴中搅拌反应,至溶液变澄清透明(黄色),继续反应半小时。将反应液快速转移至单口烧瓶,旋蒸除去溶剂thf。封上反应瓶,转移到手套箱中用n-hexane/thf(v/v=3/1)进行重结晶两次。将得到的晶体真空干燥,密封后于-20℃保存。得到针状晶体5.86g为blg-nca。
2)在无水无氧环境下,称取0.50g(0.1mmol)mpeg110-nh2·hcl于充满氮气的25ml圆底schlenk瓶中,将其放到一定温度油浴中抽真空进一步除水。加入2ml超干dmf溶解,取0.79g(3.0mmol)blg-nca溶解在2ml超干dmf中,将之快速加入mpeg110-nh2·hcl溶液中,于40℃下反应3d。反应结束后,反应体系在无水乙醚中沉淀,用chcl3溶解,重复沉淀溶解过程三次,真空干燥,得到mpeg110-b-pblg20;
②合成聚合物mpeg-b-ppbdema(p-2)
1)向装有分水器的250ml的三口圆底烧瓶中加入1,1,1-三羟甲基丙烷(17.8g,133.0mmol)、苯硼酸(16.0g,131.0mmol)、甲苯150ml。加热至120℃左右回流反应6h,待分水器中有大约2.5ml的水反应结束。对反应体系浓缩,真空干燥。得白色固体26.6g为2-苯硼酸酯-5-乙基-5,-羟甲基-1,3-二氧六环。
在充满惰性气体连接有恒压滴液漏斗的250ml圆底烧瓶中,依次加入2-苯硼酸酯-5-乙基-5,-羟甲基-1,3-二氧六环(15.0g,63.0mmol),三乙胺(8.0g,78.0mmol)、除水的二氯甲烷(100ml),低温下,缓慢滴加丙烯酰氯(7.2g,78.0mmol)的ch2cl2(10ml)溶液反应。反应结束后,将体系用硅藻土除盐,旋蒸浓缩。柱层析分离,石油醚和乙酸乙酯(v/v=10/1)为展开剂分离收集第一个纯点,旋蒸浓缩真空干燥得到白色固体13.6g为2-苯硼酸酯-5-乙基-1,3-二氧己环)丙烯酸酯(pbdema)。
2)对接有恒压滴液漏斗的100ml三口烧瓶除水除氧,在氮气保护下依次加入mpeg5000-oh(10.0g,2.0mmol))、三乙胺(0.56ml,4.0mmol)、溶剂二氯甲烷50ml,置于冰浴条件下,缓慢滴加2-溴丙酰(0.66ml,4.0mmol)的二氯甲烷(5ml)稀释溶液,滴加完毕后室温下反应48小时。反应液经过滤(除盐),有机相分别经0.1m盐酸,0.1m碳酸氢钠,去离子水洗涤并对所有水相用二氯甲烷萃取,有机相于无水硫酸钠中干燥,接着浓缩,在乙醚中沉淀,真空干燥得到白色粉末状固体7.6g为大分子引发剂为mpeg-br。
3)分别将大分子引发剂mpeg110-br(196.7mg,0.038mmol)、pbdema(2.1g,7.66mmol)、cubr2(0.43mg,0.002mmol)、pmdeta(0.045mmol)和2.0ml苯甲醚加入到schlenk瓶中,对体系进行除水除氧,氮气保护下加入cubr(5.45mg,0.038mmol),将schlenk瓶放入90℃油浴中反应40h。反应体系中性al2o3柱子除铜盐,在冰的正己烷和无水乙醚的混合液(v正/v乙=4/1)沉淀三次,得到聚合物mpeg110-b-ppbdema75;
③制备复合纳米药物递送体系:
1)聚合物p-1的质量百分含量为10%:称取9.0mg聚合物p-2和1.0mg聚合物p-1,充分溶解在1ml四氢呋喃(thf)中,缓慢滴加至10ml超纯水中,滴加完后,在通风橱敞口搅拌,使部分thf挥发。将溶液转移至mwco3500渗析袋中,在超纯水中渗析,直至thf渗析完全,得到聚合物浓度为1mg/ml的复合纳米粒子溶液。
2)聚合p-1的质量百分含量为30%:称取7.0mg聚合物p-2和3.0mg聚合物p-1,其他步骤同1);
3)聚合p-1的质量百分含量为50%:称取5.0mg聚合物p-2和5.0mg聚合物p-1,其他步骤同1);
4)聚合p-1的质量百分含量为75%:称取2.5mg聚合物p-2和7.5mg聚合物p-1,其他步骤同1);
④制备包裹胰岛素的复合纳米药物递送体系:
1)聚合物p-1的质量百分含量为10%:称取9.0mg聚合物p-2和1.0mg聚合物p-1,充分溶解在1ml四氢呋喃(thf)中;称取一定量的fitc-ins充分溶解在ph2.0左右的相应体积的稀hcl溶液中,冰浴条件下搅拌5~6h,用1.0mnaoh溶液调节ph6.0左右,得到一定浓度的fitc-ins溶液,在低温(15℃)快速搅拌下将聚合物的thf溶液缓慢滴加到10mlfitc-ins溶液中。滴加完后,在通风橱敞口搅拌,使thf部分挥发。将溶液转移至mwco14000渗析袋中,在超纯水中渗析去除未包裹的fitc-ins,得到包裹胰岛素的复合纳米粒子;
2)聚合p-1的质量百分含量为30%:称取7.0mg聚合物p-2和3.0mg聚合物p-1,其它步骤同1);
3)聚合p-1的质量百分含量为50%:称取5.0mg聚合物p-2和5.0mg聚合物p-1,其它步骤同1);
4)聚合p-1的质量百分含量为75%:称取2.5mg聚合物p-2和7.5mg聚合物p-1,其它步骤同1);
实施例2:
①合成聚合物mpeg-b-pblg(p-1)
1)l-谷氨酸-γ-苄酯n-羧基内酸酐(blg-nca)的合成见实施例1。
2)在无水无氧环境下,称取mpeg44-nh2·hcl(0.20g,0.1mmol)于充满氮气的25ml圆底schlenk瓶中,将其放到一定温度油浴中抽真空进一步除水。加入1.6ml超干dmf溶解,取blg-nca(2.10g,8.0mmol)溶解在6ml超干dmf中,将之快速加入mpeg44-nh2·hcl溶液中,于40℃下反应3d。反应结束后,反应体系在无水乙醚中沉淀,用chcl3溶解,重复沉淀溶解过程三次,真空干燥,得到mpeg44-b-pblg60;
②合成聚合物mpeg-b-ppbdema(p-2)
1)2-苯硼酸酯-5-乙基-1,3-二氧己环)丙烯酸酯(pbdema)和大分子引发剂甲氧基聚乙二醇-溴(mpeg-br)见实施例1。
2)分别将大分子引发剂mpeg44-br(81.1mg,0.038mmol)、单体(pbdema)(1.56g,5.7mmol)、cubr2(0.43mg,0.002mmol)、pmdeta(8.23mg,0.048mmol)和1.5ml苯甲醚加入到schlenk瓶中,对体系进行除水除氧,氮气保护下加入cubr(5.45mg,0.038mmol),将schlenk瓶放入90℃油浴中反应40h。反应体系中性al2o3柱子除铜盐,在冰的正己烷和无水乙醚的混合液(v/v=4/1)沉淀三次,得到聚合物mpeg44-b-ppbdema75;
③制备复合纳米药物递送体系:
1)聚合物p-1的质量百分含量为10%:称取4.5mg聚合物p-2和0.5mg聚合物p-1,充分溶解在1mln,n-二甲基甲酰胺(dmf)中,低温快速搅拌下缓慢滴加至10ml超纯水中。将溶液转移至mwco3500渗析袋中,在超纯水中渗析,直至dmf渗析完全,得到聚合物浓度为0.5mg/ml的复合纳米粒子溶液。
2)聚合p-1的质量百分含量为30%:称取7.0mg聚合物p-2和3.0mg聚合物p-1,其它步骤同1);
3)聚合p-1的质量百分含量为50%:称取5.0mg聚合物p-2和5.0mg聚合物p-1,其它步骤同1);
4)聚合p-1的质量百分含量为75%:称取2.5mg聚合物p-2和7.5mg聚合物p-1,其它步骤同1);
实施例3:
①合成聚合物mpeg-b-pblg(p-1)
1)l-谷氨酸-γ-苄酯n-羧基内酸酐(blg-nca)的合成见实施例1。
2)在无水无氧环境下,称取0.10g(0.1mmol)mpeg22-nh2·hcl于充满氮气的25ml圆底schlenk瓶中,将其放到一定温度油浴中抽真空进一步除水。加入1.0ml超干dmf溶解,取3.15g(8.0mmol)blg-nca溶解在9ml超干dmf中,将之快速加入mpeg44-nh2·hcl溶液中,于40℃下反应3d。反应结束后,反应体系在无水乙醚中沉淀,用chcl3溶解,重复沉淀溶解过程三次,真空干燥,得到mpeg22-b-pblg100;
②合成两亲性聚合物mpeg-b-ppbdema(p-3)
1)2-苯硼酸酯-5-乙基-1,3-二氧己环)丙烯酸酯(pbdema)合成步骤见实施例1。
2)在连接有恒压滴液漏斗的充满惰性气体的三口圆底烧瓶中,依次加入mpeg5000-oh(10.0g,2.0mmol),二氯甲烷(40ml),三乙胺(0.4g,4.0mmol),恒压滴液漏斗中加入对甲苯磺酰氯tscl(3.8g,20.0mmol),thf(4ml)和chcl2(20ml)低温下缓慢滴加后于常温下反应。反应液用饱和食盐水洗,有机相用无水mgso4干燥,过滤旋蒸浓缩于冰无水乙醚中沉淀三次,抽干得到单端ts保护的甲氧基聚乙二醇(mpeg-ts);在洁净干燥的单口瓶中,依次加入mpeg-ts与叠氮化钠nan3(mpeg-ts与nan3摩尔比为1:3)在80℃下加热回流反应36h。反应结束,减压浓缩反应液,用二氯甲烷溶解后,用饱和食盐水洗,收集有机相,置于无水mgso4中干燥,过滤浓缩得到浅黄色固体为mpeg-n3;向25ml的schlenk瓶中依次加入炔基端小分子链转移试剂(alkyne-cpad)(76.0mg,0.24mmol),甲氧基聚乙二醇叠氮化物(mpeg-n3)(1.0g,0.21mmol),pmdeta(10ul)以及dmf(5.0ml),对体系进行除水除氧,在氮气保护下加入cubr(3.0mg,0.02mmol)于室温下反应24h。反应体系中性al2o3柱子除铜盐,在并无水乙醚中沉淀3次,真空干燥得到粉红色固体粉末为大分子链转移试剂(mpeg5000-cpad)。
3)分别将大分子链转移试剂mpeg5000-cpad(530mg,0.1mmol)、单体(2.74g,10mmol)、aibn(3.0mg,0.02mmol)和2.0ml无水甲苯加入到schlenk瓶中,对体系进行除水除氧,将schlenk瓶放入80℃油浴中反应16h。反应体系中性al2o3柱子除铜盐,在冰的无水乙醚中沉淀三次,得到聚合物mpeg44-b-ppbdema60;
③制备复合纳米药物递送体系:
1)聚合物p-1的质量百分含量为10%:称取4.5mg聚合物p-2和0.5mg聚合物p-1,充分溶解在1ml四氢呋喃(thf)中,低温快速搅拌下缓慢滴加至10ml超纯水中。将溶液转移至mwco3500渗析袋中,在超纯水中渗析,直至thf渗析完全,得到聚合物浓度为0.5mg/ml的复合纳米粒子溶液。
2)聚合p-1的质量百分含量为30%:称取7.0mg聚合物p-2和3.0mg聚合物p-1,其它步骤同1);
3)聚合p-1的质量百分含量为50%:称取5.0mg聚合物p-2和5.0mg聚合物p-1,其它步骤同1);
4)聚合p-1的质量百分含量为75%:称取2.5mg聚合物p-2和7.5mg聚合物p-1,其它步骤同1);
实施例1中聚合物p-1的1hnmr表征和gpc表征分别见图1(a)和(b);
实施例1中聚合物p-2的1hnmr表征和gpc表征分别见图2(a)和(b);
实施例1以p-1质量分数为75%复合纳米载体的药物递送体系tem图见图3;
实施例1聚合物p-1的质量百分含量为75%的复合纳米粒子在0.15mpbs不同糖浓度下胰岛素释放情况见图4;从图4可以看出,在1.0mg/ml(人体正常血糖浓度)的糖浓度下,胰岛素释放量很低,90h后释放量不到20%;在3.0mg/ml(非正常血糖浓度,即病理血糖浓度)的糖浓度下,能呈现出好的释放胰岛素行为,整体能够很好地区分正常血糖浓度与非正常血糖浓度,本发明其他比例在3.0mg/ml的糖浓度下也具有类似效果,但在1.0mg/ml的糖浓度下,同样释放出大量胰岛素,在胰岛素释放的可控性与稳定性方面不如75%的复合纳米粒子。
实施例1聚合物p-1的质量百分含量为75%的复合纳米粒子在0.15mpbs中脉冲式糖响应释放情况见图5。从图5可以看出,当包裹胰岛素的复合纳米粒子交替反复置于1.0mg/ml与3.0mg/ml的糖浓度下,可以看出,1.0mg/ml的糖浓度下,复合纳米粒子几乎没有胰岛素释放;转移至3.0mg/ml糖浓度时,释放略有上升,再次置于1.0mg/ml低糖浓度时,释放停止,这种趋势持续至60h,之后胰岛素累计释放量开始明显上升。对于75%的复合纳米粒子,只有在高糖浓度刺激下,胰岛素才会持续释放,而一旦这种高糖刺激停止,胰岛素释放随之停止,在本发明其他比例的也具有类似效果,但其他比例在低糖浓度1.0mg/ml下也出现不同程度的释放,其在胰岛素智能自律性释放行为上不如75%的复合纳米粒子效果好。
- 还没有人留言评论。精彩留言会获得点赞!