一种具有鞘含双芯结构特征的载药纳米纤维及其制备方法与流程
技术领域
本发明属于材料学领域,涉及一种新型纳米层次物质的构效关系建立技术,具体来说是一种具有鞘含双芯结构特征的载药纳米纤维及其制备方法。
背景技术:
高压静电纺丝技术(电纺)是一种自上而下(top-down)的纳米制造技术,通过外加电场力克服喷头尖端液滴的液体表面张力和粘弹力而形成射流,在静电斥力、库仑力和表面张力共同作用下,被雾化后的液体射流被高频弯曲、拉延、分裂,在几十毫秒内被牵伸千万倍,经溶剂挥发或熔体冷却在接收端得到纳米级纤维。该技术工艺过程简单、操控方便、选择材料范围广泛、可控性强、被认为是最有可能实现连续纳米纤维工业化生产的一种方法,应用该技术制备功能纳米纤维具有良好的前景。
电纺聚合物功能纳米纤维一般以成纤聚合物为基材,通过加入活性成分而赋予纳米纤维功能,并充分利用电纺纳米纤维膜的独特性能而充分发挥活性成分的效用。这些独特的性能包括纤维直径小、纤维表面积巨大、纤维呈三维网状多孔结构、孔隙率高、纤维具有纳米尺度范围的直径却同时具有宏观范围的长度等。在生物医药领域,一般将药物加入聚合物溶液,形成共溶溶液作为纺丝液,通过普通电纺过程的快速干燥和成型,获得药物均匀分布在整个纳米纤维的载药纳米纤维。绝大部分载药纳米纤维都是该类药物均匀分布的、结构单一的纳米纤维,通过聚合物基材的理化性能和纳米纤维膜的特点而获得所需要的药物缓控释性能。虽有少量通过同轴电纺和并列电纺调控药物在纳米纤维中的分布,以获得所需药物控释性能的电纺芯鞘纳米纤维和乔纳斯纳米纤维,但是关于其他各种结构特征的纳米结构的制备,以及这些结构在提供药物的控释性能方面的应用还很少被报道。
技术实现要素:
针对现有技术中的上述技术问题,本发明提供了一种具有鞘含双芯结构特征的载药纳米纤维及其制备方法,所述的这种具有鞘含双芯结构特征的载药纳米纤维及其制备方法要解决现有技术中的纳米纤维缓释效果不能有效控制的技术问题。
本发明提供了一种具有鞘含双芯结构特征的载药纳米纤维,包括两个内芯部,两个所述的内芯部的外周设置有外鞘部,所述的外鞘部和所述的内芯部沿长度方向延伸,所述的外鞘部由水溶性聚合物构成,一个内芯部由胃溶型聚合物构成,另外一个内芯部由肠溶型聚合物构成,在所述的外鞘部和两个内芯部中均含有药物。
进一步的,药物在外鞘部水溶性聚合物的溶解下发生第一级快速释放;一个内芯部的药物在胃溶型聚合物的溶解下发生第二级释放;另外一个内芯部的药物在肠溶型聚合物的溶解下发生第三级的缓慢释放。
进一步的,一个内芯部由Eudragit E100 胃溶型聚合物构成,另外一个内芯部有Eudragit L100 肠溶型聚合物构成,所述的外鞘部由聚乙烯吡咯烷酮构成。
本发明还提供了上述的一种具有鞘含双芯结构特征的载药纳米纤维的制备方法,包括如下步骤:
1)采用可纺的水溶性聚合物和药物的共溶溶液配成鞘部工作流体,装入第一注射器中,所述的第一注射器安装在一个第一注射泵中,所述的第一注射泵和一个纺丝头的总毛细管连接;
2)采用可纺的胃溶型聚合物和药物的共溶溶液配成芯部一边的工作流体,装入第二注射器中,所述的第二注射器安装在一个第二注射泵中,所述的第二注射泵和一个纺丝头的第一弯曲毛细管连接;
3)采用可纺的肠溶型聚合物和药物的共溶溶液配成芯部另一边的工作流体,装入第三注射器中,所述的第三注射器安装在一个第三注射泵中,所述的第三注射泵和一个纺丝头的第二弯曲毛细管连接;
4)所述的第一弯曲毛细管的直线段设置在所述的总毛细管中,所述的第二弯曲毛细管的直线段设置在所述的第一弯曲毛细管中,所述的第一弯曲毛细管和第二弯曲毛细管的弯曲部从总毛细管的侧壁伸出;
5)开启高压发生器,所述的高压发生器和所述的纺丝头连接,通过三台注射泵分别控制三股流体的泵入流速,在高压静电的作用下,以组合纺丝头出口为模板,通过纤维接收板收集纳米纤维,制备出具有鞘含双芯结构特征的载药纳米纤维。
本发明还提供了实现上述方法的电纺装置,包括一个第一注射器,第一注射器中装有采用可纺的水溶性聚合物和药物的共溶溶液配成的鞘部工作流体;一个第二注射器,所述的第二注射器中装有可纺的胃溶型聚合物和药物的共溶溶液配成的一个芯部的工作流体;第三注射器,所述的第三注射器中装有可纺的肠溶型聚合物和药物的共溶溶液配成的另外一个芯部的工作流体;所述的第一注射器安装在一个第一注射泵中,所述的第二注射器安装在一个第二注射泵中,所述的第三注射器安装在一个第三注射泵中;还包括一个纺丝头,所述的纺丝头包括一个总毛细管、一个第一弯曲毛细管和一个第二弯曲毛细管,所述的第一弯曲毛细管的直线段设置在所述的总毛细管中,所述的第二弯曲毛细管的直线段设置在所述的第一弯曲毛细管中,所述的第一弯曲毛细管和第二弯曲毛细管的弯曲部从总毛细管的侧壁伸出;所述的第一注射器和一个纺丝头的总毛细管连接;所述的第二注射器和第一弯曲毛细管连接;所述的第三注射器和第二弯曲毛细管连接;还包括一个高压发生器,所述的高压发生器和所述的纺丝头连接,在纺丝头出口的下端设置有纤维接收板。
本发明公开了三级控释电纺载药纳米纤维。该纳米纤维具有鞘含并列双芯的结构特征;纳米纤维通过鞘部和并列芯部采用不同的聚合物基材,在复合结构的支撑下,能够调控所载的药物通过三级方式逐步从纤维内部释放。本发明方法制备工艺简单,单步有效、制备的纳米纤维鞘内所含并列结构清晰;而且纳米纤维直径小、线性好、直径分布均匀、纤维表面光滑。通过将纳米纤维膜剪切成薄片,可以直接开发出多种药物的经口给药系统,提供符合人体生理特征的药物控释方式。
本发明和已有技术相比,其技术进步是显著的。本发明通过一种鞘含双芯的纳米结构特征控制所载药物活性成分能够以三级控释方式逐步从纳米纤维中释放出来。将纳米纤维膜剪切成薄片,可以直接开发出多种药物的经口给药系统,提供符合人体生理特征的药物控释方式。
附图说明
图1为本发明制备三级控释电纺载药纳米纤维的过程观察图。
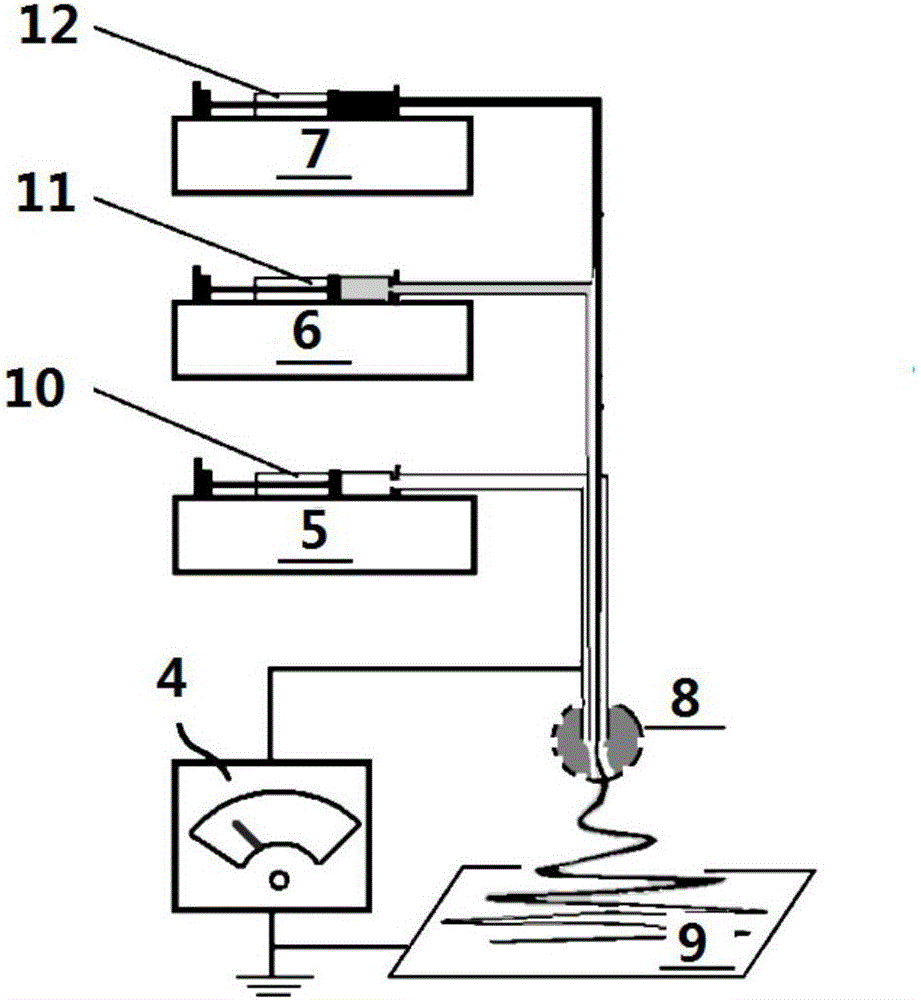
图2是本发明所使用的电纺装置的结构示意图,4-高压发生器、5-第一注射泵、6-第二注射泵、7-第三注射泵、8-纺丝头、9-纤维接收板、10-第一注射器、11-第二注射器、12-第三注射器。
图3本发明所采用的纺丝头整体外形示意图,1-总毛细管、2-第一弯曲毛细管、3-第二弯曲毛细管。
图4为本发明制备三级控释电纺载药纳米纤维的扫描电子显微镜图。
图5为本发明制备三级控释电纺载药纳米纤维的透射电子显微镜图。
图6 为本发明制备三级控释电纺载药纳米纤维的结构示意图。
图7为本发明制备三级控释电纺载药纳米纤维的药物三级控释特征图。
具体实施方式
以下结合附图和实施例对本发明进行详细说明。这些实施例仅用于解释本发明而不是用于限制本发明。凡采用与本发明相同或相似的方法,或做出的等价修改,均应落入本发明保护范围。
实施例1:多射流电纺工艺的实施
将8克聚乙烯吡咯烷酮和1克酮洛芬共溶于100克乙醇中,配成鞘部的工作流体。
将13克尤特奇E-100和1克酮洛芬共溶于100克乙醇中,配成并列芯一边的工作流体。
将13克尤特奇L-100和3克酮洛芬共溶于100克乙醇中,配成并列芯另一边的工作流体。
将上述溶液分别装入相应的注射器中,并安装到相应注射泵上,连接各工作流体到三级组合纺丝头各个入口中,接通高压纺丝头和高压静电发生器。
按照如下参数实施高压静电纺丝工艺:调节鞘液流量为1.4 mL/h;调节含尤特奇E-100和尤特奇L-100芯液流体流量分别为0.5 和1.0 mL/h。接收板离喷丝口距离为20 cm ,电压15 kV。环境温度为 (21±3) ℃,环境湿度为61±4%。在上述工作条件下,对电纺过程进行原位放大拍摄,结果如图1所示,从纺丝头出来一个由三股流体形成的复合泰勒锥,锥体的顶端发出一个直线射流,直线射流下面是高频拉伸的不稳定区。所制备的纳米纤维通过一个接地的铝箔包裹纸板进行收集。
实现上述方法的电纺装置(如图2所示),包括一个第一注射器5,第一注射器10中装有采用可纺的水溶性聚合物和药物的共溶溶液配成的鞘部工作流体;一个第二注射器6,所述的第二注射器11中装有可纺的胃溶型聚合物和药物的共溶溶液配成的一个芯部的工作流体;第三注射器7,所述的第三注射器12中装有可纺的肠溶型聚合物和药物的共溶溶液配成的另外一个芯部工作流体;所述的第一注射器10安装在一个第一注射泵5中,所述的第二注射器11安装在一个第二注射泵6中,所述的第三注射器12安装在一个第三注射泵7中;还包括一个纺丝头8(如图3所示),所述的纺丝头包括一个总毛细管1、一个第一弯曲毛细管2和一个第二弯曲毛细管3,所述的第一弯曲毛细管2的直线段设置在所述的总毛细管1中,所述的第二弯曲毛细管3的直线段设置在所述的第一弯曲毛细管2中,所述的第一弯曲毛细管2和第二弯曲毛细管3的弯曲部从总毛细管1的侧壁伸出;所述的第一注射器10和一个纺丝头8的总毛细管1连接;所述的第二注射器11和第一弯曲毛细管2连接;所述的第三注射器12和第二弯曲毛细管3连接;还包括一个高压发生器4,所述的高压发生器4和所述的纺丝头8连接,在纺丝头出口的下端设置有纤维接收板9。
进一步的,所述的第一弯曲毛细管2的直线段穿出所述的总毛细管1的出口端,所述的第二弯曲毛细管3的直线段穿出所述的第一弯曲毛细管2的出口端。
实施例2:三级控释电纺载药纳米纤维的形貌与结构的表征分析
采用场发射扫描电镜(FESEM)对实施例1所制备纤维进行表面喷金后观察,结果如图4所示。所制备的纤维呈现良好的线性状态、没有串珠结构产生、纤维表面光滑、纤维堆积均匀。直径为 680 ± 120 nm,分布比较均匀,直径分布比较集中。
采用高分辨透射电子显微镜(TEM)对所制备纤维内部结构进行观察,结果如图5所示,纳米纤维的鞘含并列双芯结构清晰,包括两个并列的内芯部,两个所述的内芯部的外周设置有外鞘部,所述的外鞘部和所述的内芯部沿长度方向延伸,所述的外鞘部和所述的内芯部中均含有药物。纤维的结构如图6所示,所述的外鞘部11的药物44分散于水溶性聚合物中,一个内芯部22的药物44分散于胃溶型聚合物中,另外一个内芯部33的药物44分散于肠溶型聚合物中。
具体的,在纳米纤维的径向截面中,所述的第一内芯部22和所述的第二内芯部33在一个圆周中,所述的第一内芯部22的面积小于所述的第二内芯部33的面积。
实施例3:三级控释电纺载药纳米纤维所提供的酮洛芬缓控释性能
按中国药典2015版附录ⅩD释放度测定第二法浆法,采用RCZ-8A智能溶出实验仪进行对上述所得的载药纳米纤维进行体外溶出试验。控制转速50rpm,温度为37±0.1℃。在前2h内采用不加酶的人工胃液900mL为溶出介质,后面采用不加酶的人工肠液(pH6.8的磷酸盐缓冲溶液)900mL为溶出介质,考察具有药物径向隔离分布特征纳米纤维的药物体外控释性能。按预定时间取样5mL,0.22µm微孔滤膜过滤,得到溶出液样品,并立刻补充同体积等温新鲜介质。对样品适当稀释后,在λmax =264nm处,采用紫外可见分光光度计进行紫外测定,计算药物酮洛芬的溶出量和累积溶出百分比,重复6次。结果如图7所示,从图中可以看出,通过聚合物基材在鞘含双芯结构调控下的逐步溶解,药物能够以一种三级控制释放模式进行释放。初期鞘部药物的快速释放可以获得良好的初期治疗效果;随后通过尤特奇E-100在酸性条件下的溶解和尤特奇L-100在中性条件下的溶解,药物能够逐步地缓慢释放。通过药物的这种多级控释,有望既克服病人初期血药浓度过高而导致的毒副作用而加强用药安全性,同时由于药物能够保持较长时间的缓慢释放,避免因血药浓度过低而失去治疗效果,又能避免病人的频繁给药,增加病人的耐受性和方便性。
实施例4:中药活性成分阿魏酸的三级控释电纺载药纳米纤维
按照实施例1的纺丝液调配方法和实施工艺条件,制备阿魏酸的三级控释电纺载药纳米纤维,按照实施例4进行药物体外溶出实验,检测纤维对药物的控释性能,结果表明,药物阿魏酸的体外释放具有明显的三级控释特点。
实施例5:造影剂钆喷酸葡甲胺盐的三级控释电纺载药纳米纤维
按照实施例1的纺丝液调配方法和实施工艺条件,制备用于消化道疾病检测的胃肠道核磁共振造影剂钆喷酸葡甲胺盐的三级控释电纺载药纳米纤维。
本发明的纳米纤维中,一个芯部聚合物基材为Eudragit E100 胃溶型,在胃的酸性条件下能溶解,释放出所载药物;另外一个芯部聚合物基材为为Eudragit L100 肠溶型,在胃的酸性条件下不溶解,要经过胃到结肠位置后,才溶解释放出所载药物;而鞘部的聚乙烯吡咯烷酮是水溶性聚合物,无论酸碱都溶解。所以载药纤维在口服后,可以依次从口腔到胃到肠,通过聚合物的分步溶解,控制药物多级释放。
按照实施例4进行药物体外溶出实验,检测纤维对药物的控释性能,结果表明,造影剂钆喷酸葡甲胺盐的体外释放具有明显的三级控释特点。
- 还没有人留言评论。精彩留言会获得点赞!