一种负载顺铂的水凝胶载药体系及其制备方法与流程
本发明属于高分子药物载体领域,具体涉及一种负载顺铂的水凝胶载药体系及其制备方法。
背景技术:
由于铂类药物抗癌谱广,在抗癌领域得到迅速发展,且顺铂已成为癌症化疗中主要的药物之一。顺铂临床多以注射剂使用,但是由于顺铂在体内易与蛋白质类物质结合而导致药物失效,且顺铂较长的半衰期导致它具有长期生物毒性,因此临床应用受到了限制。为了解决直接注射给药的强毒副作用,近年来研究人员将常规化疗药物与高分子药物载体结合形成具有局部缓释作用的高分子药物储库,通过瘤周/瘤内局部给药后对药物进行控制释放,保证在体内的安全性和有效性。在目前已知的高分子材料中,水凝胶因其优益的仿生性能、良好的生物相容性、生物体可降解性、载药量大等受到人们的重视。其中,可注射自愈合水凝胶由于其可直接注射到病灶部位而不需要外科手术,方便快捷等优点越来越受到科研工作者的关注。
普鲁兰多糖是一种线型微生物多糖,具有良好的生物相容性,抗氧化性,能够被体内酶降解等优点,是一种良好的药物载体材料。普鲁兰多糖富含羟基,易被氧化形成富含醛基的氧化多糖。聚氨基酸类共聚物是一类新型的生物可降解高分子材料。由于ε-聚赖氨酸在降解过程中能释放出天然的小分子氨基酸,因此具有良好的生物相容性,容易被机体吸收和代谢,故该材料在药物载体及药物控制释放等方面受到广泛关注。枝化聚乙烯亚胺是一种阳离子性水溶性聚胺,其分子链中含有大量的氨基n原子,易交联。且小分子量的枝化聚乙烯亚胺毒性小,富含氨基,易被生物体代谢出去,已被应用于药物释放、ph及生物传感器构建等多个领域。因此将富含醛基的氧化多糖与富含氨基的聚合物结合,极易发生席夫碱反应,使聚合物链之间交联形成具有网络结构的水凝胶。
技术实现要素:
本发明旨在提供一种负载广谱抗癌药物-顺铂的水凝胶载药体系的制备方法。本发明原料简单易得,制备工艺纯熟,制备周期短,易于操作,不需要昂贵的仪器,且制备的水凝胶体系可以通过物理吸附和共价交联两种载药方式载药,使载药体系更加稳定。
为实现上述目的,本发明采用如下技术方案:
氧化普鲁兰多糖的合成:将普鲁兰多糖(mn=250000)溶于双蒸水中配成25mg/ml的溶液,加入高碘酸钾,避光室温搅拌反应1.5h后,加入丙三醇继续室温搅拌15min,以终止氧化反应。然后,将反应液转移至透析袋(mw=6000)中,4℃条件下进行透析纯化3d,冷冻干燥,即得氧化普鲁兰多糖。普鲁兰多糖的重复单元、高碘酸钾和丙三醇的摩尔比为1:1:1。
负载顺铂的水凝胶载药体系的制备:37℃下将氧化普鲁兰多糖溶于双蒸水中,使氧化普鲁兰多糖的浓度为0.05g/ml,然后在溶液中加入顺铂,使之完全溶解,使顺铂的浓度为1.5mg/ml。在上述混合溶液中同时加入0.5g/ml的ε-聚赖氨酸(mn=4000)溶液和0.26g/ml的枝化聚乙烯亚胺(mn=600)溶液,迅速混合均匀。室温下反应40-80s,即得载药水凝胶体系。将制得的载药水凝胶放入双蒸水中冲洗3次,冷冻干燥3d,即得干燥的水凝胶载药体系。氧化普鲁兰多糖、ε-聚赖氨酸、枝化聚乙烯亚胺、顺铂的质量分数比为:1:0.025~0.225:0.0026~0.013:0.03。
本发明的显著优点在于:所述水凝胶载药体系所用原料简单易得,制备工艺纯熟,制备周期短,制备的载药水凝胶生物相容性好,顺铂可以通过共价反应和吸附作用两种方式载入水凝胶,使载药体系更加稳定。此外,载药水凝胶的自愈合性与可注射性使其可直接注射到病人的病灶部位,不需要外科手术,减轻了病人的痛苦;温度和ph敏感性使得水凝胶载药体系能够在肿瘤环境更快的释放药物;同时,由于水凝胶体系能够对顺铂进行控制释放,进一步减少了药物的毒副作用。
附图说明
图1是实施例5制得的载药水凝胶体系扫描电镜图(氧化普鲁兰多糖、ε-聚赖氨酸、聚乙烯亚胺和顺铂的质量比为100:22.5:1:0.03)。
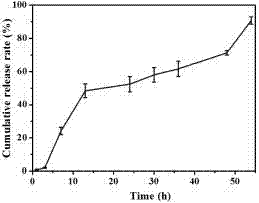
图2是顺铂在ph7.4的磷酸盐缓冲溶液条件下从实施例5制得的水凝胶体系中的体外累积释放曲线图(氧化普鲁兰多糖、ε-聚赖氨酸、聚乙烯亚胺和顺铂的质量比为100:22.5:1:0.03)。
具体实施方式
为进一步公开而不是限制本发明,以下结合实例对本发明作进一步的详细说明。
实施例1
1)称取10.000g普鲁兰多糖溶于400ml双蒸水中,磁力搅拌充分溶解。
2)将10ml232mg/ml的高碘酸钾溶液加入1)溶液中,反应1.5h。
3)在2)溶液中加入0.72ml丙三醇反应15min,以终止氧化反应。
4)将溶液3)置于透析袋中于4℃下透析3天,期间每隔6~8h换一次水。
5)将透析后的溶液4)真空冷冻干燥3天得到纯的氧化普鲁兰多糖。
6)称取1.000g氧化普鲁兰多糖固体,加入20ml双蒸水于37℃溶解。
7)在溶液6)中加入30mg顺铂,于37℃充分溶解。
8)在溶液7)中加入250μl0.5g/ml的ε-聚赖氨酸溶液,充分混匀。
9)在上述溶液8)中加入30μl0.26g/ml的枝化聚乙烯亚胺溶液,迅速混合均匀。室温下反应80s。
10)将制得的载药水凝胶放入双蒸水中冲洗3次。-20℃条件下预冻12h,后真空冷冻干燥3天。
实施例2
1)称取10.000g普鲁兰多糖溶解于400ml双蒸水中,磁力搅拌充分溶解。
2)2)将10ml232mg/ml的高碘酸钾溶液加入1)溶液中,反应1.5h。
3)在2)中加入0.72ml丙三醇反应15min,以终止氧化反应。
4)将溶液3)置于的透析袋中于4℃下透析3天,期间每隔6~8h换一次水。
5)将透析后的溶液4)真空冷冻干燥3天得到纯净的氧化普鲁兰多糖固体。
6)称取1.000g氧化普鲁兰多糖固体,加入20ml双蒸水于37℃溶解。
7)在溶液6)中加入30mg顺铂,于37℃充分溶解。
8)在溶液7)中加入350μl0.5g/ml的ε-聚赖氨酸溶液,充分混匀。
9)在上述溶液8)中加入30μl0.26g/ml的枝化聚乙烯亚胺溶液,迅速混合均匀。室温下反应75s。
10)将制得的载药水凝胶放入双蒸水中冲洗3次。-20℃条件下预冻12h,后真空冷冻干燥3天。
实施例3
1)称取10.000g普鲁兰多糖溶解于400ml双蒸水中,磁力搅拌充分溶解。
2)将10ml232mg/ml的高碘酸钾溶液加入1)溶液中,反应1.5h。
3)在2)中加入0.72ml丙三醇反应15min,以终止氧化反应。
4)将溶液3)置于透析袋中于4℃下透析3天,期间每隔6~8h换一次水。
5)将透析后的溶液4)真空冷冻干燥3天得到纯净的氧化普鲁兰多糖固体。
6)称取1.000g氧化普鲁兰多糖固体,加入20ml双蒸水于37℃溶解。
7)在溶液6)中加入30mg顺铂,于37℃充分溶解。
8)在溶液7)中加入450μl0.5g/ml的ε-聚赖氨酸溶液,充分混匀。
9)在上述溶液8)中加入20μl0.26g/ml的枝化聚乙烯亚胺溶液,迅速混合均匀。室温下反应80s。
10)将制得的载药水凝胶放入双蒸水中冲洗3次。-20℃条件下预冻12h,后真空冷冻干燥3天。
实施例4
1)称取10.000g普鲁兰多糖溶解于400ml双蒸水中,磁力搅拌充分溶解。
2)将10ml232mg/ml的高碘酸钾溶液加入1)溶液中,反应1.5h。
3)在2)中加入0.72ml丙三醇反应15min,以终止氧化反应。
4)将溶液3)置于透析袋中于4℃下透析3天,期间每隔6~8h换一次水。
5)将透析后的溶液4)真空冷冻干燥3天得到纯净的氧化普鲁兰多糖固体。
6)称取1.000g氧化普鲁兰多糖固体,加入20ml双蒸水于37℃溶解。
7)在溶液6)中加入30mg顺铂,于37℃充分溶解。
8)在溶液7)中加入450μl0.5g/ml的ε-聚赖氨酸溶液,充分混匀。
9)在上述溶液8)中加入30μl0.26g/ml的聚乙烯亚胺溶液,迅速混合均匀。室温下反应60s。
10)将制得的载药水凝胶放入双蒸水中冲洗3次。-20℃条件下预冻12h,后真空冷冻干燥3天。
实施例5
1)称取10.000g普鲁兰多糖溶解于400ml双蒸水中,磁力搅拌充分溶解。
2)将10ml232mg/ml的高碘酸钾溶液加入1)溶液中,反应1.5h。
3)在2)中加入0.72ml丙三醇反应15min,以终止氧化反应。
4)将溶液3)置于透析袋中于4℃下透析3天,期间每隔6~8h换一次水。
5)将透析后的溶液4)真空冷冻干燥3天得到纯净的氧化普鲁兰多糖固体。
6)称取1.000g氧化普鲁兰多糖固体,加入20ml双蒸水于37℃溶解。
7)在溶液6)中加入30mg顺铂,于37℃充分溶解。
8)在溶液7)中加入450μl0.5g/ml的ε-聚赖氨酸溶液,充分混匀。
9)在上述溶液8)中加入40μl0.26g/ml的聚乙烯亚胺溶液,迅速混合均匀。室温下反应45s。
10)将制得的载药水凝胶放入双蒸水中冲洗3次。-20℃条件下预冻12h,后真空冷冻干燥3天。
实施例6
1)称取10.000g普鲁兰多糖溶解于400ml双蒸水中,磁力搅拌充分溶解。
2)将10ml232mg/ml的高碘酸钾溶液加入1)溶液中,反应1.5h。
3)在2)中加入0.72ml丙三醇反应15min,以终止氧化反应。
4)将溶液3)置于透析袋中于4℃下透析3天,期间每隔6~8h换一次水。
5)将透析后的溶液4)真空冷冻干燥3天得到纯净的氧化普鲁兰多糖固体。
6)称取1.000g氧化普鲁兰多糖固体,加入20ml双蒸水于37℃溶解。
7)在溶液6)中加入30mg顺铂,于37℃充分溶解。
8)在溶液7)中加入450μl0.5g/ml的ε-聚赖氨酸溶液,充分混匀。
9)在上述溶液8)中加入50μl0.26g/ml的聚乙烯亚胺溶液,迅速混合均匀。室温下反应40s。
10)将制得的载药水凝胶放入双蒸水中冲洗3次。-20℃条件下预冻12h,后真空冷冻干燥3天。
以上所述仅为本发明的制备方法,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
- 还没有人留言评论。精彩留言会获得点赞!