医药组合物用于制备治疗脑神经萎缩相关疾病的用途的制作方法
本发明系关于一种治疗脑神经萎缩相关疾病的医药组合物。
先前技术
近年来,随着老化人口急速增加,阿兹海默症(alzheimer’sdisease),也就是老年失智症,俨然已成为全球性的流行疾病。根据国际失智协会的统计,2015年全球失智患者为4680万人,平均每3秒就有一人罹患失智症,且预计2030年全球失智患者将会是现在的两倍,因此如何预防和治疗失智症,将是重要的课题。
失智症(dementia,又称痴呆症)是一种慢性、渐进性的退化性疾病,可分为退化性失智症及血管性失智症这两大类。大部份患者属于退化性失智症,其中又以阿兹海默症(alzheimer’sdisease)、额颞叶型失智症(frontotemporallobedegeneration)、路易氏体失智症(dementiawithlewybodies)最为常见。血管性失智症则是因为罹患过脑中风或脑血管病变,因脑部血液循环不良,导致脑细胞死亡而造成智力减退。失智症早期常见的症状是难以记住最近发生的事情,随着疾病的发展,症状可能会包含:易怒、具攻击性、无法正常言语、容易迷路、情绪不稳定、丧失生存动力、丧失长期记忆、难以自理和行为异常等,因此当患者的状况变差时,往往会开始脱离家庭和社会关系,并逐渐丧失身体机能,最终导致死亡。
现今预防失智症的研究中,多数以阿兹海默症为主。虽然阿兹海默氏症的真正成因至今仍然不明,但β-淀粉样蛋白(β‐amyloid)的异常堆积、神经纤维丛聚集(neurofibrillarytangles),以及广泛的脑神经发炎反应(neuro‐inflammation)皆是主要的病理特征,并且严重的影响神经修复与再生功能。
目前失智症的治疗,主要使用乙酰胆碱酶抑制剂(acetyl‐cholinesteraseinhibitor)或nmda受体拮抗剂(nmdaanatagonist)来推迟疾病的发展或改善患者的精神、行为症状,并不能有效的阻止或恢复已经受损的大脑神经细胞,此外,上述药物对患者本身有抽搐、呼吸困难等副作用产生,因此在医疗上仍需要更好的治疗方式来改善并减缓失智症疾病。
技术实现要素:
有鉴于此,本发明提供一种治疗脑神经萎缩相关疾病的医药组合物,该医药组合物包含脂肪干细胞,可用于提升失智症患者脑内的兴奋性突触的功效,并改善失智症患者大脑记忆储存区的功能。
本发明提供一种医药组合物用于制备治疗脑神经萎缩相关疾病的用途,所述医药组合物包含脂肪干细胞。
在本发明的实施例中,其中治疗脑神经萎缩相关疾病为改善失智症者大脑记忆存储区的功能。
在本发明的实施例中,其中改善失智症者大脑记忆存储区的功能为改善50%到60%。
在本发明的实施例中,其中治疗脑神经萎缩相关疾病为提升失智症者的兴奋性突触的功效。
在本发明的实施例中,其中所述提升失智者的兴奋性突触的功效为提升50%~60%。
在本发明的实施例中,其中治疗脑神经萎缩相关疾病为增加失智症者的大脑内侧前额叶皮质锥体神经突触数量度。
在本发明的实施例中,其中所述增加失智症者的大脑内侧前额叶皮质椎体神经突触数量度为增加90%~108%
在本发明的实施例中,其中治疗脑神经萎缩相关疾病为增加失智症者的大脑海马回锥体的神经突触数量度。
在本发明的实施例中,其中所述增加失智症者大脑海马回椎体的神经突触数量度为70%~80%。
在本发明的实施例中,其中脂肪干细胞浓度为6×104/ul~7×104/ul。
在本发明的实施例中,其中脂肪干细胞的植入位置为靠近右脑的穹窿区fornixarea(ap:-0.2、ml:-0.5、dv:-6)。
图式简单说明
图1a为对照组与失智症组的大脑组织切片图,与对照组相比,失智症组的组织颜色较深。
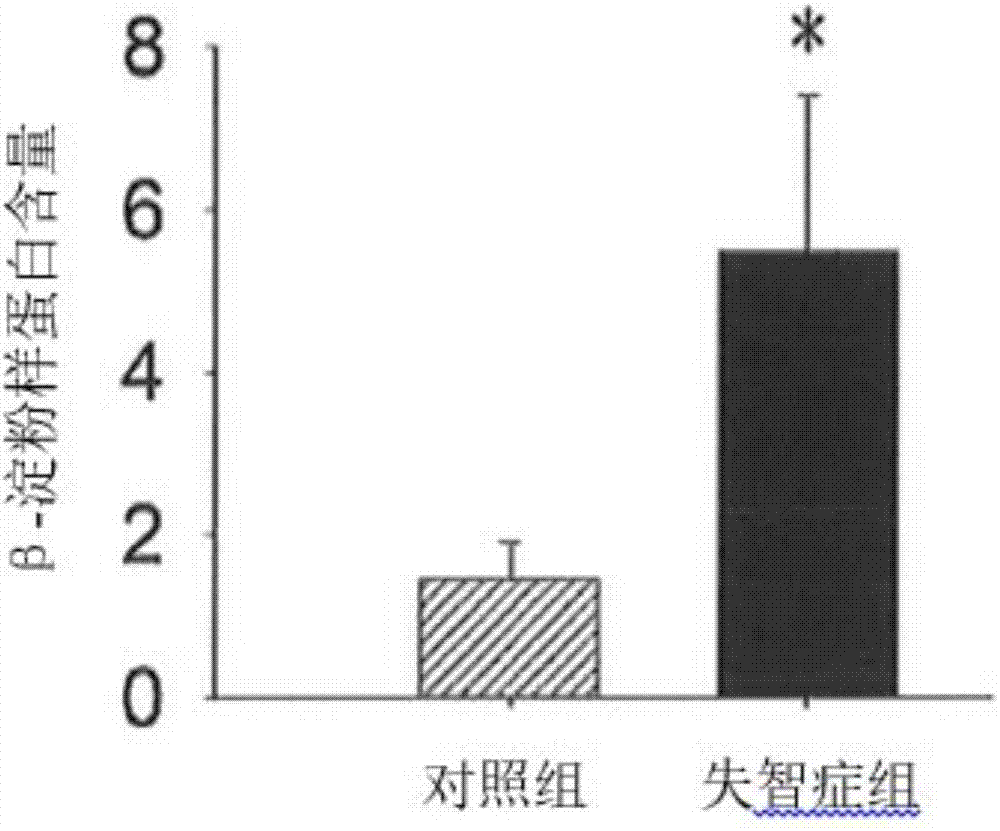
图1b为对照组与失智症组的β-淀粉样蛋白含量,与对照组相比,失智组的β-淀粉样蛋白含量确实较高。
图2a为实验组第3天的大脑染色结果图,其中蓝色荧光为dapi,黄色荧光为抗核抗体anti-humannucleiantibody(mab1281)。
图2b为实验组第14天的大脑染色结果图,其中蓝色荧光为dapi,黄色荧光为抗核抗体anti-humannucleiantibody(mab1281)。
图3为各组老鼠的空间记忆测试结果图,其中各点代表各组大鼠逃脱水迷宫所需时间,时间越长代表记忆功能越差,第五天的结果显示,实验组的记忆功能改善至与对照组相似,并与失智症组有显著差异(失智症组记忆功能较差)。
图4为各组老鼠的兴奋性突触功效测试结果图,其中与对照组相比,失智症组大鼠的麸胺酸(谷氨酸)后突触(glutamatergicpostsynaptic)含量明显下降,然而实验组的大鼠,其脑内麸胺酸后突触(glutamatergicpostsynaptic)的含量较失智症组的高。
图5a为各组大鼠大脑内侧前额叶皮质锥体神经元部位,在单一神经细胞的四个位置,包括:基底突触的近端、基底突触的远端、顶突触的近端及顶突触的远端,计算神经突触的数量,其中近端系指靠近神经元细胞本体的位置。
图5b为各组老鼠大脑内侧前额叶皮质锥体神经元的神经树突密度统计结果,失智症组的老鼠其神经突触相较于对照组有显著的降低,而实验组显示退化的神经突触数量密度又有显著的增加,且回到与对照组的神经突触数量相当。
图6a为各组大鼠大脑ca1海马回锥体神经元部位,在单一神经细胞基底突触靠近细胞本体近端的第2分枝及顶突触靠近细胞本体近端的第3分枝拍照10μm的距离得之。
图6b为各组大鼠大脑ca1海马回锥体神经元神经树突密度统计结果,失智症组的老鼠其神经突触相较于对照组有显著的降低,而在实验组显示退化的神经突触数量密度又有显著的增加,且回到与对照组的神经突触数量相当。
实施方式
本发明所述脂肪干细胞(adipose-derivedstemcells,adscs)是一种存在于脂肪组织中的间质干细胞(mesenchymalstemcells,msc),可以通过脂肪抽吸术或脂肪切除术获得,因此容易获取,且对病人的创伤较少。此外,脂肪干细胞可以由自体萃取后植入,患者易于接受,且减少了抗排斥药物与长时间体外培养等缺点。再者,脂肪干细胞群易于分离,在体外培养时,可快速、稳定地扩增,不易衰老,因此适用于本发明的医药组合物。
本发明实施方式中使用的adscs经中国医药大学试验伦理委员会同意,国玺干细胞应用技术股份有限公司(新竹,台湾)提供。
实施动物
1.将wistar大鼠分成对照组、失智症组以及实验组三个组别,其中失智症组与实验组的大鼠,在第0-28天,每天将300pmole淀粉样蛋白(β-amyloid)分别植入于脑内,植入位置为ap:0.4、ml:1.5、dv:3.3,以产生失智症现象,并且于第14天时,将本发明的医药组合物(含有1×106/15ul的脂肪干细胞,亦即为含有6×104/ul~7×104/ul的脂肪干细胞)植入于实验组的大鼠脑内,植入位置为靠近右脑的穹窿区fornixarea(ap:-0.2、ml:-0.5、dv:-6),而对照组则于第14天以针穿刺大鼠大脑。
实施例一、β-淀粉样蛋白染色
将对照组与失智症组的大鼠大脑,以抗体anti-aβ1-42进行染色,如图1a-1b,由图中可知,与对照组相比,失智症组的组织颜色较深,由此可知,失智症组的β-淀粉样蛋白含量确实较高。
实施例二、免疫荧光染色
将实验组大鼠植入本发明的医药组合物后,分别于第3天(如图2a)及第2周(图2b)牺牲,并以抗体anti-humannucleiantibody(mab1281)进行大脑染色,结果如图2a、2b,图中蓝色荧光为dapi,黄色荧光为anti-humannucleiantigen(mab1281)。
由图2b可知,本发明医药组合物于植入大鼠脑后的第14天,仍可看见脂肪干细胞的存活,且其细胞态样与植入脑后的第3天(图2a)时一样。
实施例三、空间记忆(spatialmemory)测试
将对照组、失智症组及实验组的大鼠,置放于水迷宫(morriswatermaze)中,连续5天,每天观察各组大鼠的移动模式,用以进行空间记忆的测试。如图3,图中各点代表各组大鼠逃脱水迷宫所需时间,时间越长代表记忆功能越差。图中第五天的结果显示,实验组的记忆功能改善至与对照组相似(实验组相较于失智症组改善50%~60%),并与失智症组有显著差异(失智症组记忆功能较差),由此可知,本发明的医药组合物能改善失智症者大脑记忆储存区的功能。
实施例四、兴奋性突触(excitatorysynapses)功效测试
将对照组、失智症组及实验组的大鼠大脑,以抗体突触后密度蛋白95(postsynapticdensityprotein95,psd‐95)进行西方式点墨法分析,用以表示各组大鼠大脑的麸胺酸(即谷氨酸)后突触(glutamatergicpostsynaptic)的含量,结果如图4。
由图4可看出,与对照组相比,失智症组大鼠的麸胺酸后突触(glutamatergicpostsynaptic)含量明显下降(失智组较对照组下降80%~90%),然而实验组的大鼠,其脑内麸胺酸后突触(glutamatergicpostsynaptic)的含量较失智症组的高(实验组较失智组高出50%~60%),由此可知,本发明医药组合物能有效提升失智症者的兴奋性突触的功效。
实施例五、树突棘密度(dendriticspinedensity)分析
将对照组、失智症组及实验组的大鼠大脑,以荧光染剂(luciferyellow)标记神经,用以分析各组大鼠大脑的神经树突密度。
图5a显示,图中各组大鼠大脑内侧前额叶皮质锥体神经元(medialprefrontalcorticalpyramidalneurons)部位,在单一神经细胞的四个位置,包括:基底突触(basaldendrite)的近端(proximalend)、基底突触(basaldendrite)的远端(distalend)、顶突触(apicaldendrite)的近端(proximalend)及顶突触(apicaldendrite)的远端(distalend),计算神经突触的数量,其中近端是指靠近神经元细胞本体的位置。计算方式为在各组的代表区域拍照4段10μm的距离,计数上面的神经突触数量后,再算其平均值。统计结果如图5b所示,失智症组的老鼠其神经突触相较于对照组有显著的降低(失智组较对照组降低40%~45%),而实验组显示退化的神经突触数量密度又有显著的增加(实验组较失智组增加90%~108%),且回到与对照组的神经突触数量相当。
如图6a,图中显示各组大鼠大脑ca1海马回锥体神经元(ca1hippocampalpyramidalneurons)部位,在单一神经细胞基底突触靠近细胞本体近端的第2分枝及顶突触靠近细胞本体近端的第3分枝拍照10μm的距离得之。统计方式为在各组代表区域拍照4段10μm的距离,计数上面的神经突触数量后,再算其平均值。统计结果如图6b所示,失智症组的老鼠其神经突触相较于对照组有显著的降低(失智组较对照组降低30%~40%),而在实验组显示退化的神经突触数量密度又有显著的增加(实验组较失智组增加70%~80%),且回到与对照组的神经突触数量相当。
由以上结果可知,本发明医药组合物能有效提升失智症者的神经树突密度。
- 还没有人留言评论。精彩留言会获得点赞!