眼部炎性病症和疾病的组合治疗的制作方法
本申请案主张2016年5月9日提交的第62/333,549号美国临时申请案的35u.s.c.§119(e)下的权益,所述申请案的内容通过其上整体引用并入本文中。
背景技术:
取决于发炎位置,眼部发炎可以以许多不同严重程度的眼部病症形式显现。归因于眼部发炎的病症包含葡萄膜炎、过敏性结膜炎、巩膜炎、视神经炎、角膜炎等。眼部发炎有在自身免疫病症、环境刺激物和损伤如手术范围内的许多原因。一些形式的眼部发炎继发于细菌或病毒感染,而一些眼部发炎的病因不明。症状可包括眼痛、眼睛发红、畏光、飞蚊症、视力丧失或此类症状的组合。
葡萄膜炎是这些眼部炎性病症的典型,且通过葡萄膜(其涵盖虹膜、睫状体和脉络膜)的发炎表征。视网膜发炎也被归类为葡萄膜炎。解剖学上葡萄膜炎可分类为前部(例如虹膜炎和虹膜睫状体炎)、中间(例如睫状体炎和周边葡萄膜炎)、后部(例如脉络膜炎和视网膜炎)及弥漫性(例如虹膜炎加中间葡萄膜炎、脉络膜视网膜炎)(也称作全葡萄膜炎)。参见《墨克诊疗手册(merckmanualofdiagnosisandtherapy)》,第19版,爱思唯尔出版社(elsevierpress)(2011)。
前葡萄膜炎的反复发作可对眼睛的内部结构造成永久性和严重的损伤。复发性前葡萄膜炎可导致相当多的周边前粘连和继发性青光眼的形成。慢性前葡萄膜炎还可引起角膜内皮细胞功能障碍且甚至是白内障形成。后部发炎可导致持续的病理性玻璃体改变和视网膜功能障碍,其中的任一种都可导致顽固性视力丧失。
在急性和慢性发炎期间,由发炎的组织和白细胞释放多种发炎介体。这些介体和白细胞的浓度指示发炎水平或程度。典型的眼部发炎治疗以炎性反应为目标。抗炎甾族制剂(例如,皮质甾类泼尼松龙和地塞米松)是治疗葡萄膜炎和其它眼部炎性病况的药物选择。眼部发炎的其它治疗涉及免疫调节剂,如环孢素、他克莫司和西罗莫司(即雷帕霉素)。然而,由严重和许多副作用导致使用甾类和其它免疫调节剂变得复杂。因此,非常期望开发有效的替代治疗,其不会呈现非期望的免疫调节副作用,但还可以与此类标准免疫调节和其它抗炎剂组合使用。
技术实现要素:
本揭示提供通过向有需要的受试者施予能够与醛反应的化合物和抗炎剂的组合来治疗眼部炎性病症和疾病的方法。在一些实施例中,所述化合物具有化学式(i)的结构。
或其药学上可接受的盐,
其中,
x、y和x各自独立地为附有nh2的n、ch或c,其中x、y和z中之一是n;
r1选自由以下组成的群组:
其中,
ra各自独立地为c1-6烷基,且
rb是经取代或未经取代的c1-6烷基;
r2各自独立地为卤素、羟基、氨甲酰基、氨基,或未经取代或经取代的芳基;且
p为0、1、2或3。
在一些实施例中,抗炎剂选自抗炎甾类化合物、非甾类抗炎化合物、抗代谢物、免疫抑制性抗生素、烷基化剂和抗炎细胞因子抗体。
在各种实施例中,可用组合疗法治疗的眼部炎性病症包含过敏性结膜炎、干眼综合症、睑板腺功能障碍、白内障、圆锥形角膜、大疱和其它角膜病变、法曲氏(fuch's)内皮营养不良、眼部瘢痕类天疱疮、与光反应性角膜切除术(prk)愈合和其它角膜愈合相关的病况、与泪脂质降解或泪腺功能障碍相关的病况、葡萄膜炎(例如前葡萄膜炎、中间葡萄膜炎、后葡萄膜炎、全葡萄膜炎、非感染性葡萄膜炎和感染性葡萄膜炎)、角膜炎、巩膜炎、虹膜炎、睫状体炎、眼部移植物抗宿主疾病(gvhd)、视神经炎、史蒂文琼森眼综合症(ocularstevensjohnsonsyndrome)、睑炎、眼部红斑痤疮(有或没有睑板腺功能障碍)、白内障术后、持续角膜侵蚀以及与角膜外伤、角膜移植和屈光手术相关的炎症。特定来说,组合疗法用于治疗葡萄膜炎,如前葡萄膜炎、中间葡萄膜炎、后葡萄膜炎和全葡萄膜炎。
在一些实施例中,式(i)的稠合双环胺化合物可以通过相同或不同的投与途径,与抗炎剂依次或同时投与。在一些实施例中,投与双环胺化合物后接着投与抗炎剂。在一些实施例中,投与抗炎剂后接着投与稠合双环胺化合物。在一些实施例中,例如为了避免任何不利的相互作用和/或使治疗有效性最大化,允许投与稠合双环胺化合物与投与抗炎剂之间存在治疗上有效的时间间隔。
在一些实施例中,配制双环胺化合物和/或抗炎剂用于向感染眼部炎性病症或疾病的眼睛局部投与。在一些实施例中,将双环胺化合物和/或抗炎剂与眼科学上可接受的赋形剂一起配制。示例性的眼科学上可接受的赋形剂包含张力剂、防腐剂、缓冲剂、润湿剂、粘度增强剂、润滑剂、螯合剂和抗氧化剂等中的一或多种。
在一些实施例中,将双环胺化合物与环糊精一起配制,在一些实施例中,所述环糊精可选自α-环糊精、β-环糊精、γ-环糊精、其衍生物及其组合。特定来说,用于本方法中的环糊精选自β-环糊精、γ-环糊精、其衍生物及其组合。
在一些实施例中,稠合双环胺化合物可以以下浓度存在:约0.05%重量/体积至约10%重量/体积、约0.1%重量/体积至约5%重量/体积、约0.2%重量/体积至约4%重量/体积、约0.3%至约3%重量/体积、约0.4%重量/体积至约2%重量/体积或约0.5%重量/体积至约1.5%重量/体积。在一些实施例中,稠合双环胺化合物可以以下浓度存在:约0.05%重量/体积、约0.1%重量/体积、约0.2%重量/体积、约0.3%重量/体积、约0.4%重量/体积、约0.5%重量/体积、约0.6%重量/体积、约0.7%重量/体积、约0.8%重量/体积、约0.9%重量/体积、约1%重量/体积、约1.5%重量/体积、约2%重量/体积、约3%重量/体积、约4%重量/体积、约5%重量/体积、约6%重量/体积、约7%重量/体积、约8%重量/体积、约9%重量/体积或约10%重量/体积。
在另一方面,进一步提供包括稠合双环胺化合物和抗炎剂的试剂盒。在一些实施例中,所述试剂盒可包括单或多个剂量的双环胺化合物和抗炎剂。所述剂量在适当的情况下可呈固体形式如片剂和囊片,或呈粉末形式如设置于胶囊中。在一些实施例中,所述剂量可呈液体形式如用于注射或局部投与的溶液,或设置成凝胶或乳膏形式用于局部投与。
在一些实施例中,为了局部投与,所述试剂盒包括在单次使用的小瓶特别是单次使用的塑性挤注小瓶中的,呈单药物组合物或单独组合物形式的双环胺化合物和抗炎剂溶液。用于局部投与的试剂盒可包括单个剂量或多个剂量。
附图说明
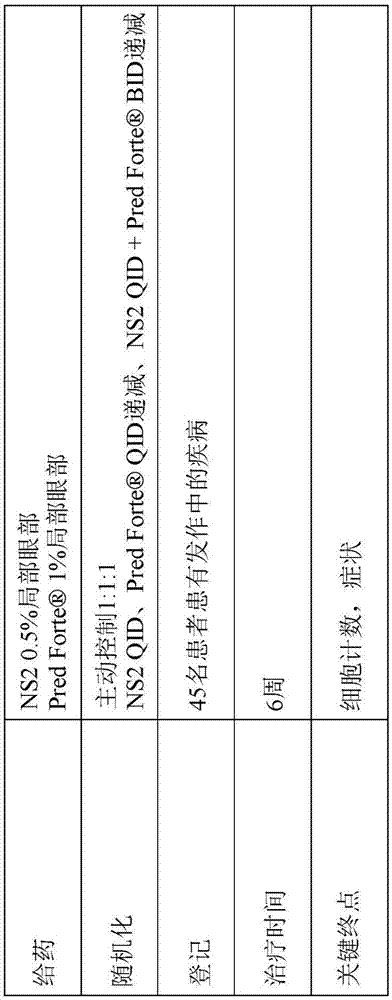
图1示出检验葡萄膜炎治疗的临床研究的基础参数。
图2示出按前房细胞计数(其为葡萄膜炎的标志物),用单独的ns2化合物和与乙酸泼尼松龙(pred
图3是治疗组(即ns0.5%;ns20.5%+pred
具体实施方式
本揭示提供用于治疗眼部炎性病症和疾病的稠合双环胺化合物和抗炎剂的组合。进一步提供用于治疗眼部炎性病症和疾病的医药组合物。
除非上下文另外明确指示,否则如本说明书和所附权利要求书中所用,单数形式“一(a/an)”和“所述”包含多个指示物。因此,例如,参看“一种化合物”包含多于一种化合物,且参看“一种赋形剂”包含多于一种赋形剂。
除非另外说明,否则进一步理解使用“或”意指“和/或”。类似地,“包括(comprise/comprises/comprising)”、“包含(include/includes和including)”是可互换的且并不意欲限制。并且,在使用术语“包括”描述各种实施例的情况下,所属领域的技术人员会理解在一些特定例子中,可使用语言“主要由……组成”或“由……组成”替代性地描述实施例。
以上包含附图的一般性描述和以下详细描述仅是示例性和解释性的,且不限定本揭示。
本文所用的章节标题仅处于组织目的,且不应理解为限制所描述的标的物。
5.1.定义
参看本揭示,除非以其它方式具体界定,否则用于本文描述中的技术和科学术语具有所属领域的一般技术人员通常所理解的含义。因此,以下术语既定具有以下含义:
“组合疗法”或“治疗上有效的组合”是指同步或按任何次序分开地投与第一医药活性剂和至少第二医药活性剂以提供治疗上有效的疾病或病症治疗。
如本文所用,“烷基”意指直链或支链非环状烃,优选地具有1至10个碳原子(c1-10),更优选地具有1至6个碳原子(c1-6)。
单独或作为较大部分(如“芳烷基”、“芳烷氧基”或“芳氧基烷基”中)的一部分使用的“芳基”是指具有总共五至十四个环成员的单环或双环系统,其中系统中的至少一个环是芳香族且其中系统中的每个环含有3至7个环成员。术语“芳基”可与术语“芳基环”互换使用。芳基的非限制性实例包含苯基、萘基和联二苯。
“卤素”是指氟、氯、溴和碘。
“羟基”是指基团-oh。
“氨甲酰基”是指基团-c(o)nh2。
“氨基”是指基团-nh2。经取代的氨基是指基团-nhr'、nr'r'和nr'r'r',其中每个r'独立地选自经取代或未经取代的烷基、环烷基、环杂烷基、烷氧基、芳基、杂芳基、杂芳基烷基、酰基、烷氧羰基、硫基、亚磺酰基、磺酰基等。如下文进一步描述,作为实例而非限制,示例性氨基包含二甲氨基、二乙氨基、三甲铵、三乙铵、甲基磺酰氨基、呋喃基-氧基-磺氨基等。
“经取代的”(不管前面是否有术语“任选地”),意指指定部分中的一或多个氢被合适的取代基替换。除非另外指示,否则“任选地经取代的”基团在基团的每个可取代位置处均可具有合适的取代基,且当任何既定结构中的多于一个位置可被选自指定基团的多于一个取代基取代时,所述取代基在每一位置处可相同或不同。本文的实施例中所设想的取代基的组合优选地是导致形成稳定或化学上可行的化合物的那些。如本文所用,术语“稳定”是指在经受病况时大体上不改变的化合物,以允许其生产、检测以及在某些实施例中其回收、纯化,并用于本文所揭示的目的中的一或多种。
“任选地经取代的”基团的可取代碳原子的合适的单价取代基独立地为卤素;-(ch2)0-4ro;-(ch2)0-4oro;-o-(ch2)0-4ro,-o-(ch2)0-4c(o)oro;-(ch2)0-4ch(oro)2;-(ch2)0-4sro;-(ch2)0-4ph,其可被ro取代;-(ch2)0-4o(ch2)0-1ph,其可被ro取代;-ch=chph,其可被ro取代;-(ch2)0-4o(ch2)0-1-吡啶基,其可被ro取代;-no2;-cn;-n3;-(ch2)0-4n(ro)2;-(ch2)0-4n(ro)c(o)ro;-n(ro)c(s)ro;-(ch2)0-4n(ro)c(o)nro2;-n(ro)c(s)nro2;-(ch2)0-4n(ro)c(o)oro;-n(ro)n(ro)c(o)ro;-n(ro)n(ro)c(o)nro2;-n(ro)n(ro)c(o)oro;-(ch2)0-4c(o)ro;-c(s)ro;-(ch2)0-4c(o)oro;-(ch2)0-4c(o)sro;-(ch2)0-4c(o)osiro3;-(ch2)0-4oc(o)ro;-oc(o)(ch2)0-4sr-,sc(s)sro;-(ch2)0-4sc(o)ro;-(ch2)0-4c(o)nro2;-c(s)nro2;-c(s)sro;-sc(s)sro,-(ch2)0-4oc(o)nro2;-c(o)n(oro)ro;-c(o)c(o)ro;-c(o)ch2c(o)ro;-c(noro)ro;-(ch2)0-4ssro;-(ch2)0-4s(o)2ro;-(ch2)0-4s(o)2oro;-(ch2)0-4os(o)2ro;-s(o)2nro2;-(ch2)0-4s(o)ro;-n(ro)s(o)2nro2;-n(ro)s(o)2ro;-n(oro)ro;-c(nh)nro2;-p(o)2ro;-p(o)ro2;-op(o)ro2;-op(o)(oro)2;siro3;-(c1-4直链或支链亚烷基)o-n(ro)2;或-(c1-4直链或支链亚烷基)c(o)o-n(ro)2,其中每个ro可如下文所定义的那样被取代且独立地为氢、c1-6脂肪族、-ch2ph、-o(ch2)0-1ph、-ch2-(5-6元杂芳环)或具有0-4个独立地选自氮、氧或硫的杂原子的5-6元饱和、部分不饱和或芳基环,或不管以上定义,两个单独出现的ro(与其中间原子结合在一起)形成具有0-4个独立地选自氮、氧或硫的杂原子的3-12元饱和、部分不饱和或芳基单环或双环,其可如下文所定义的那样被取代。
ro(或通过将两个单独出现的ro与其中间原子结合在一起形成的环)的合适的单价取代基独立地为卤素、-(ch2)0-2r·、-(卤基r·)、-(ch2)0-2oh、-(ch2)0-2or·、-(ch2)0-2ch(or·)2;-o(卤基r·)、-cn、-n3、-(ch2)0-2c(o)r·、-(ch2)0-2c(o)oh、-(ch2)0-2c(o)or·、-(ch2)0-2sr·、-(ch2)0-2sh、-(ch2)0-2nh2、-(ch2)0-2nhr·、-(ch2)0-2nr·2、-no2、-sir·3、-osir·3、-c(o)sr·、-(c1-4直链或支链亚烷基)c(o)or·或-ssr·,其中每个r·为未经取代的或前面是“卤基”的r·仅被一或多个卤素取代,且独立地选自c1-4脂肪族、-ch2ph、-o(ch2)0-1ph或具有0-4个独立地选自氮、氧或硫的杂原子的5-6元饱和、部分不饱和或芳基环。ro的饱和碳原子的合适的二价取代基包含=o和=s。
“任选地经取代的”基团的饱和碳原子的合适的二价取代基包含以下:=o、=s、=nnr*2、=nnhc(o)r*、=nnhc(o)or*、=nnhs(o)2r*、=nr*、=nor*、-o(c(r*2))2-3o-或-s(c(r*2))2-3s-,其中每个单独出现的r*选自氢、可如下文所定义的那样被取代的c1-6脂肪族或具有0-4个独立地选自氮、氧或硫的杂原子的未经取代的5-6元饱和、部分不饱和或芳基环。结合到“任选地经取代的”基团的邻位可取代碳的合适的二价取代基包含:-o(cr*2)2-3o-,其中每个单独出现的r*选自氢、可如下文所定义的那样被取代的c1-6脂肪族或具有0-4个独立地选自氮、氧或硫的杂原子的未经取代的5-6元饱和、部分不饱和或芳基环。
r*的脂肪族基团的合适的取代基包含卤素、-r·、-(卤基r·)、-oh、-or·、-o(卤基r·)、-cn、-c(o)oh、-c(o)or·、-nh2、-nhr·、-nr·2或-no2,其中每个r·是未经取代的或前面是“卤基”的r·仅被一或多个卤素取代,且独立地为c1-4脂肪族、-ch2ph、-o(ch2)0-1ph或具有0-4个独立地选自氮、氧或硫的杂原子的5-6元饱和、部分不饱和或芳基环。
“任选地经取代的”基团的可取代氮的合适的取代基包含
“药学上可接受的盐”是指在合理医学判断范围内适合用于与人类和低级动物的组织接触而没有不当毒性、刺激、过敏反应等,且与合理的效益/风险比相称的那些盐。药学上可接受的盐在所属领域中是众所周知的。例如,berge,s.m.等,1977,《药物科学杂志(jpharmasci.)》66:1-19,通过引用并入本文中。本文所述的化合物的药学上可接受的盐包含衍生自合适的无机酸和有机酸和碱的那些。药学上可接受的无毒性酸加成盐的实例是氨基与无机酸(如氢氯酸、氢溴酸、磷酸、硫酸和过氯酸)或有机酸(如乙酸、草酸、顺丁烯二酸、酒石酸、柠檬酸、丁二酸或丙二酸)形成的盐,或通过使用所属领域中使用的其它方法(如离子交换)形成的盐。其它药学上可接受的盐包含己二酸酯、海藻酸盐、抗坏血酸盐、天冬氨酸盐、苯磺酸盐、苯甲酸盐、硫酸氢盐、硼酸盐、丁酸盐、樟脑酸盐、樟脑磺酸盐、柠檬酸盐、环戊烷丙酸盐、二葡糖酸盐、十二烷基硫酸盐、乙磺酸盐、甲酸盐、反丁烯二酸盐、葡庚糖酸盐、甘油磷酸盐、葡糖酸盐、半硫酸盐、庚酸盐、己酸盐、氢碘化物、2-羟基-乙磺酸盐、乳糖酸盐、乳酸盐、月桂酸盐、月桂基硫酸盐、苹果酸盐、顺丁烯二酸盐、丙二酸盐、甲磺酸盐、2-萘磺酸盐、烟酸盐、硝酸盐、油酸盐、草酸盐、棕榈酸盐、双羟萘酸盐、果胶酸盐、过硫酸盐、3-苯丙酸盐、磷酸盐、特戊酸盐、丙酸盐、硬脂酸盐、丁二酸盐、硫酸盐、酒石酸盐、硫氰酸盐、对甲苯磺酸盐、十一烷酸盐、戊酸盐等。
衍生自适当的碱的盐包含碱金属盐、碱土金属盐、铵盐和n+(c1-4烷基)4盐。代表性碱金属盐或碱土金属盐包含钠盐、锂盐、钾盐、钙盐、镁盐等。适当时,其它药学上可接受的盐包含使用抗衡离子(如卤离子、氢氧根、羧酸根、硫酸根、磷酸根、硝酸根、低级烷基磺酸根和芳基磺酸根)形成的无毒铵、季铵和胺阳离子。
“赋形剂”或“载剂”是指例如充当用于活性成份或组合物的填充剂或稳定剂的药物组合物或配制物的任何组分。
“治疗有效量”是指相比于对应的尚未接收此类量的受试者,引起疾病或病症的改进治疗、愈合、预防或改善,或疾病或病症的进展速率减缓,且还包含可有效增强普通生理功能的量。
如本文所用,疾病、病症或综合症的“治疗(treating或treatment)”包含(i)预防在受试者体内出现疾病、病症或综合症,即使疾病、病症或综合症的临床症状不在受试者(其可接触或易患所述疾病、病症或综合症,但尚未经历或显现出所述疾病、病症或综合症的症状)体内产生;(ii)抑制疾病、病症或综合症,即遏制其发展;以及(iii)缓解疾病、病症或综合症,即使疾病、病症或综合症消退。
“防治性治疗”是指向未显现出疾病、病变或医学病症的体征或症状或仅显现出疾病、病变或病症的早期体征或症状的受试者施用的治疗,使得治疗是出于消除、预防或减小疾病、病变或医学病症发展的风险的目的而施用的。防治性治疗充当针对疾病或病症的预防性治疗。
5.2.眼部炎性病症和疾病的组合疗法
本揭示提供用于眼部炎性病症和疾病的治疗的稠合双环胺化合物和抗炎剂的组合。不受任何操作理论的限制,稠合双环化合物呈现出与毒性醛的共轭形成。所述化合物在治疗眼部炎性病症、葡萄膜炎(以单一疗法或与抗炎甾类组合的形式)中显示是有效的。
因此,本揭示提供治疗眼部炎性病症或疾病的方法,包括向患有眼部炎性病症或疾病的受试者投与治疗有效量的式(i)的化合物。
或其药学上可接受的盐,
其中,
x、y和x各自独立地为附有nh2的n、ch或c,其中x、y和z中之一是n;
r1选自由以下组成的群组:
其中,
ra各自独立地为c1-6烷基,且
rb是经取代或未经取代的c1-6烷基;且
r2各自独立地为卤素、羟基、氨甲酰基、氨基,或未经取代或经取代的芳基;且
p为0、1、2或3;以及
抗炎剂。
在一些实施例中,式(i)的化合物是式(1a)的化合物:
或其药学上可接受的盐,其中r1、r2和p如上文所定义。
在一些实施例中,对于式(1a)的化合物,r1是
其中,
ra各自独立地为c1-6烷基;
r2各自独立地为卤素、羟基、氨甲酰基、氨基,或未经取代或经取代的芳基;且
p为0、1、2或3。
在一些实施例中,每个ra独立地为直链c1-6烷基。在一些实施例中,每个ra独立地选自由以下组成的群组:甲基、乙基和丙基。在一些实施例中,每个ra是甲基。
在一些实施例中,r2是卤素,特别是cl或f,且p为1或2。
在一些实施例中,式(i)的化合物为化合物(2):
或其药学上可接受的盐。化合物(2)在本文中也称作ns2。
在治疗眼部炎性病症和疾病的方法中,上文的稠合双环胺化合物与抗炎剂组合投与。可用于与稠合双环胺化合物组合来治疗眼部发炎的抗炎剂包含甾类、非甾类抗炎化合物、抗代谢物、免疫抑制性抗生素、烷基化剂和抗炎细胞因子抗体等。
在一些实施例中,抗炎剂是甾类,特别是具有免疫调节、抗炎性质的甾类。在一些实施例中,抗炎剂是糖皮质甾类,其被广泛用作控制炎性和自身免疫性疾病的有效治疗。在一些实施例中,糖皮质甾类是皮质甾类或其前药。在一些实施例中,皮质甾类选自皮质醇、可的松、泼尼松、泼尼松龙、甲基泼尼松、曲安西龙、倍他米松、地塞米松和其前药。在一些实施例中,皮质甾类前药是乙酸泼尼松龙。
在一些实施例中,稠合双环胺化合物与非甾类抗炎化合物组合使用。这些化合物通常充当酶环加氧酶(cox)的抑制剂,抑制环加氧酶-1(cox-1)和/或环加氧酶-2(cox-2)同工酶。不同类别的非甾类抗炎化合物包含水杨酸酯、丙酸衍生物、乙酸衍生物、烯醇酸、邻氨基苯甲酸衍生物和选择性的cox抑制剂。可组合使用的示例性非甾类抗炎化合物包含乙酰水杨酸、二氟尼柳、双水杨酯、布洛芬、右布洛芬、那普洛仙、非诺洛芬、酮基布洛芬、右酮洛芬、氟比洛芬、奥沙普嗪、洛索洛芬、吲哚美辛、托麦汀、舒林酸、依托度酸、酮咯酸、双氯芬酸、乙酰氯芬酸、萘丁美酮、吡罗昔康、美洛昔康、替诺昔康、屈噁昔康、氯诺昔康、苯基丁氮酮、甲芬那酸、甲氯芬那酸、氟芬那酸、托芬那酸和塞内昔布等。在一些实施例中,针对眼睛的局部应用,非甾类抗炎化合物可选自双氯芬酸、氟比洛芬、酮基布洛芬、溴芬酸和奈帕芬胺。
在一些实施例中,用于与稠合双环胺化合物组合使用的抗炎剂是抗代谢物。在一些实施例中,抗代谢物是细胞毒性嘌呤类似物,例如硫唑嘌呤和巯嘌呤。在一些实施例中,抗代谢物是抗叶酸化合物。示例性的抗叶酸化合物是甲氨蝶呤。在一些实施例中,抗代谢物是肌苷单磷酸脱氢酶抑制剂(impdh),如霉酚酸和其前药霉酚酸吗啉乙酯。在一些实施例中,用于组合疗法的抗代谢物是二氢乳清酸脱氢酶抑制剂,如来氟米特(leflunomide)。
在一些实施例中,用于与稠合双环胺化合物组合使用的抗炎剂是烷基化剂。示例性的烷化剂包含环磷酰胺和苯丁酸氮芥等。
在一些实施例中,用于与稠合双环胺化合物组合使用的抗炎剂是免疫调节抗生素。可用于本文中的治疗的免疫抑制性抗生素包含结合亲环素和/或钙调神经磷酸酶并抑制t淋巴细胞活动的那些。在一些实施例中,免疫调节抗生素选自环孢灵、他克莫司、雷帕霉素和其衍生物。
在一些实施例中,用于组合疗法的抗炎剂是抗炎抗体,如靶向炎性细胞因子的抗体(如tnfα、il-1、il-4、il-5或il-17)或靶向炎性反应中的免疫系统细胞活性的抗体(如b细胞表达cd20)。在一些实施例中,抗炎生物剂选自依那西普、英利昔单抗、阿达木单抗、达利珠单抗、利妥昔单抗、托珠单抗(toclizumab)、聚乙二醇化赛妥珠单抗和戈利木单抗。
可用稠合双环胺化合物和抗炎剂的组合治疗的眼部炎性病症包含过敏性结膜炎,包含春季角膜结膜炎和特应性角膜结膜炎;干眼综合症和睑板腺功能障碍;白内障;圆锥形角膜;大疱和其它角膜病变;法曲氏内皮营养不良;眼部瘢痕类天疱疮;与光反应性角膜切除术(prk)愈合和其它角膜愈合相关的病况、与泪脂质降解或泪腺功能障碍相关的病况;葡萄膜炎,包含前葡萄膜炎、中间葡萄膜炎、后葡萄膜炎、全葡萄膜炎、非感染性葡萄膜炎和感染性葡萄膜炎;角膜炎;巩膜炎;虹膜炎;睫状体炎;眼部移植物抗宿主疾病(gvhd);视神经炎;史蒂文琼森眼综合症;睑炎;眼部红斑痤疮,有或没有睑板腺功能障碍;白内障术后;持续角膜侵蚀;以及与角膜外伤、角膜移植和屈光手术相关的炎症。
在一些实施例中,组合疗法用于治疗葡萄膜炎。在一些实施例中,用组合治疗的葡萄膜炎是前葡萄膜炎,其包含虹膜睫状体炎和虹膜炎病症且涉及前房和虹膜,其中后一指示也影响睫状体。绝大部分的葡萄膜炎是前葡萄膜炎。在一些实施例中,可用组合治疗的葡萄膜炎是中间葡萄膜炎,也称作平坦部炎(parsplanitis),其涉及玻璃体腔中细胞的发炎或炎性物质在平坦部上沉积。在一些实施例中,可用组合治疗的葡萄膜炎是后葡萄膜炎,其涉及视网膜和脉络膜中的葡萄膜的发炎。在一些实施例中,可用组合治疗的葡萄膜炎是全葡萄膜炎(即弥漫性葡萄膜炎),其是前段(例如虹膜和睫状体)和后段(例如视网膜和脉络膜)两者的葡萄膜的发炎。
应理解,尽管以上描述是针对利用稠合双环胺化合物和抗炎剂的组合治疗的,但葡萄膜炎治疗的数据指示稠合双环胺化合物在单独使用(即以单一疗法)时具有疗效。因此,对于本揭示中所述的用组合疗法治疗的每一眼部炎性病症和疾病及眼部炎性病症和疾病中的每一种,还提供利用稠合双环胺化合物的治疗,如无抗炎剂辅助投与的化合物(2),例如以单一疗法。
在一些实施例中,稠合双环胺化合物和抗炎剂的组合用于治疗黄斑变性。因此,在一些实施例中,治疗黄斑变性的方法包括向有需要的受试者施予本文所述的治疗有效量的稠合双环胺化合物(特别是化合物(2))和如本文所述的抗炎剂。因此,所描述的用于治疗眼部炎性病症和疾病的稠合双环化合物和抗炎剂的每一个组合还可应用于治疗黄斑变性。在一些实施例中,可处理的黄斑变性形式选自年龄相关性黄斑变性、斯塔加特氏病(stargardtdisease)、遗传形式的青少年黄斑变性、湿黄斑变性、干黄斑变性和干年龄相关性黄斑变性的继发性地图状萎缩(geographicatrophy,ga)
5.3.医药组合物
在另一方面,本揭示提供用于治疗眼部炎性病症和疾病的医药组合物。在一些实施例中,当分开投与稠合双环胺化合物和抗炎剂时,可将化合物和抗炎剂制备成单独医药组合物。例如,如果通过不同途径投与,则化合物和抗炎剂的单独医药组合物也用于同时投与中。
在一些实施例中,将化合物和致炎剂制备成混杂物用于通过相同途径同时投与。在此类医药组合物中,将化合物和相容性抗炎剂配制成单药物组合物。可在通过混合化合物和抗炎剂的单独组合物来投与前不久制备医药组合物。在一些实施例中,提供化合物和抗炎剂作为稳定组合物且不需要在使用前混合化合物和抗炎剂。因此,在一些实施例中,提供如上所述的稠合双环胺化合物和抗炎剂的医药组合物。在一些实施例中,提供式(i)的化合物(特别是式(1a)的化合物)和抗炎剂的医药组合物。在一些实施例中,医药组合物包括化合物(2)和抗炎剂。
在一些实施例中,医药组合物包括如上所述的稠合双环胺化合物和甾类。在一些实施例中,与稠合双环胺化合物一起制备成医药组合物的甾类选自皮质醇、可的松、泼尼松、泼尼松龙、甲基泼尼松、曲安西龙(triacmcinolone)、倍他米松、地塞米松和其前药。在一些实施例中,甾类前药是乙酸泼尼松龙。在一些实施例中,配制稠合双环胺化合物和甾类(如乙酸泼尼松龙)的医药组合物用于局部眼用投与。
在一些实施例中,医药组合物包括如上所述的稠合双环胺化合物和非甾类抗炎剂。在一些实施例中,与稠合双环胺化合物一起制备成医药组合物的非甾类抗炎剂选自乙酰水杨酸、二氟尼柳、双水杨酯、布洛芬、右布洛芬、那普洛仙、非诺洛芬、酮基布洛芬、右酮洛芬、氟比洛芬、奥沙普嗪、洛索洛芬、吲哚美辛、托麦汀、舒林酸、依托度酸、酮咯酸、双氯芬酸、乙酰氯芬酸、萘丁美酮、吡罗昔康、美洛昔康、替诺昔康、屈噁昔康、氯诺昔康、苯基丁氮酮、甲芬那酸、甲氯芬那酸、氟芬那酸、托芬那酸、和塞内昔布。在优选实施例中,将双环稠合胺化合物与选自双氯芬酸、氟比洛芬、酮基布洛芬、溴芬酸和奈帕芬胺的非甾类抗炎剂一起配制成医药组合物,特别用于局部眼用投与。
在一些实施例中,医药组合物包括稠合双环胺化合物和抗代谢物。在一些实施例中,与稠合双环胺化合物一起制备成医药组合物的抗代谢物选自硫唑嘌呤、巯嘌呤、甲氨蝶呤、霉酚酸、霉酚酸吗啉乙酯和来氟米特。在一些实施例中,配制稠合双环胺化合物和抗代谢物的医药组合物用于局部眼用投与。
在一些实施例中,医药组合物包括稠合双环胺化合物和烷基化剂。在一些实施例中,与稠合双环胺化合物一起制备成医药组合物的烷基化剂选自环磷酰胺和苯丁酸氮芥。在一些实施例中,配制稠合双环胺化合物和烷基化剂的医药组合物用于局部眼用投与。
在一些实施例中,医药组合物包括稠合双环胺化合物和免疫调节抗生素。在一些实施例中,与稠合双环胺化合物一起制备成医药组合物的免疫调节抗生素选自环孢灵、他克莫司、雷帕霉素和其衍生物。在一些实施例中,配制稠合双环胺化合物和免疫调节抗生素的医药组合物用于局部眼用投与。
可以使用一或多种生理上或药物学上可接受的载剂或赋形剂的常规方式配制如本文所述的稠合双环胺化合物和抗炎剂,无论是分开地或呈混杂物形式。例如,可配制稠合双环胺化合物和其药学上可接受的盐和溶剂合物用于通过例如注射、吸入或吹入(通过口或鼻)投与或经口、经颊、舌下、经皮、经鼻、经眼、不经肠或经直肠投与。在一些实施例中,向眼睛投与双环稠合胺化合物以治疗眼部炎性疾病或病症。
可以配制稠合双环胺化合物和抗炎剂用于多种模式的投与,包含内吸、局部和定域投与。技术和配制物通常可在《雷明顿:医药科学和实践(remington:thescienceandpracticeofpharmacy)》,第21版,lww(2005)中发现。对于不经肠投与,医药组合物可肌内、静脉内、腹膜内或皮下投与。对于注射,可在液体溶液中,优选地在生理上相容的缓冲液(如汉克氏溶液(hank'ssolution)或林格氏溶液(ringer'ssolution))中配制化合物。此外,化合物可被配制成固体形式并在使用前立即再溶解或悬浮。也包含冻干形成。
在一些实施例中,将稠合双环胺化合物和抗炎剂(分开地或呈混杂物形式)与一或多种医药学上可接受的赋形剂或载剂一起配制到医药组合物中。
对于经口投与,医药组合物可呈例如通过常规手段利用药学上可接受的赋形剂如结合剂(例如预胶凝玉米淀粉、聚乙烯吡咯烷酮或羟丙基甲基纤维素);填料(例如乳糖、微晶纤维素或钙磷酸氢盐);润滑剂(例如硬脂酸镁、滑石或二氧化硅);崩解剂(例如马铃薯淀粉或羟基乙酸淀粉钠);或润湿剂(例如月桂基硫酸钠)制备的片剂、锭剂或胶囊的形式。可通过所属领域中众所周知的方法涂布片剂。
用于经口投与的液体制剂可呈例如溶液、糖浆或悬浮液的形式,或其可以干燥产品形式呈现,以便在使用前用水或其它合适的媒剂复水。可通过常规手段利用药学上可接受的添加剂如悬浮剂(例如山梨糖醇糖浆、纤维素衍生物或氢化食用脂肪);乳化剂(例如卵磷脂或阿拉伯胶);非水性媒剂(例如杏仁油、油性酯、乙基醇或分馏的植物油);以及防腐剂(例如甲基或丙基对羟基苯甲酸盐或山梨酸)制备此类液体制剂。所述制剂按需要还可含有缓冲盐、调味剂、着色剂和/或甜味剂。可适宜地配制用于经口投与的制剂以控制活性化合物的释放。
对于通过吸入(例如肺传送)的投与,可以从加压包或喷洒器中喷射出的气雾剂喷雾形式方便地传送稠合双环胺化合物和/或抗炎剂,其中使用合适的喷射剂,例如二氯二氟甲烷、三氯氟甲烷、二氯四氟乙烷、二氧化碳或其它合适的气体。在加压气雾剂的情况下,可通过提供用以传送计量数量的阀门来确定剂量单位。可将用于吸入器或吹入器中的例如明胶的胶囊和药筒配制成含有化合物和合适的粉末基质如乳糖或淀粉的粉末混合物。
在一些实施例中,可将稠合双环胺化合物和/或抗炎剂配制成用于通过注射(例如通过快速注射或持续输注)的不经肠投与。用于注射的配制物可呈例如在安瓿或多剂量容器中的单位剂型,其含或不含添加的防腐剂。组合物可呈如在油性或水性媒剂中的悬浮液、溶液或乳液的此类形式,且可含有赋形剂如悬浮剂、稳定剂和/或分散剂。替代地,活性成分可呈粉末形式,以便在使用前用合适的媒剂(例如灭菌的无热原质水)复水。
在一些实施例中,还可将稠合双环胺化合物和/或致炎剂配制成贮存制剂。可通过植入(例如皮下或肌内)或通过肌内注射投与此类长效配制物。因此,例如,药学上的活性化合物可与合适的聚合或疏水性材料(例如呈可接受油中的乳液形式)或离子交换树脂,或呈微溶性衍生物形式(例如呈微溶性盐形式)一起配制。控释配制品还包含透皮贴剂。
脂质体是另一种可制备的药物传送系统,特别是制备成可注入形式。因此,在一些实施例中,可以脂质体传送系统的形式投与药物活性剂。脂质体在所属领域中是众所周知的。脂质体可由多种磷脂如磷脂酰胆碱、胆固醇和十八胺形成。适用于组合疗法的各种形式的脂质体涵盖所有类型的脂质体,包含但不限于小单层囊泡、大单层囊泡和多层囊泡。
在一些实施例中,可将稠合双环胺化合物和/或抗炎剂制备成快速分裂或溶解的剂型,其可用于药物活性剂的快速吸收,特别是经颊和舌下吸收。快速溶化剂型有益于对吞咽典型的固体剂型(如囊片和片剂)有困难的病人,如老年和儿科病人。此外,快速溶化剂型避开与例如可咀嚼剂型相关的缺点,在所述可咀嚼剂型情况下,活性剂在患者口中保留的时间长度在确定掩味剂的量和患者可抵触喉部活性剂沙砾感的程度中起重要作用。
在一些实施例中,本文所述的稠合双环胺化合物和/或抗炎剂并入到含有通常适合于局部药物投与的局部载剂且包括任何所属领域中已知的此类物质的局部配制物中。可以选择局部载剂从而得到呈期望形成(例如呈软膏、洗剂、乳膏、凝胶、油、溶液等形式)的组合物,且可由天然存在或合成来源的物质构成。优选的是选定的载剂不会对活性剂或局部配制物的其它组分造成不利影响。用于本文的合适的局部载剂的实例包含水、醇和其它无毒有机溶剂、甘油、矿物油、硅酮、石油膏、羊毛脂、脂肪酸、植物油、对羟苯甲酸酯、蜡等。
在一些实施例中,稠合双环胺化合物和/或抗炎剂可并入到软膏中,所述软膏通常是半固体制剂,其通常基于矿脂或其它石油衍生物。如所属领域的技术人员将了解的,待使用的特定软膏基质是将实现最优药物传送且优选地将实现其它期望特性如软化等的软膏基质。如同其它载剂或媒剂,软膏基质应是惰性、稳定、无刺激性和非致敏的。在一些实施例中,配制软膏用于眼用应用,所述软膏可包含水包油或油包水的粘稠液体或半固体乳液。软膏可含有油相、乳化剂和水相。在一些实施例中,软膏可包括矿脂和/或脂肪醇如十六烷醇或十八烷醇。乳化剂通常可为非离子型、阴离子型、阳离子型或两性表面活性剂。
在一些实施例中,稠合双环胺化合物和/或抗炎剂可并入到凝胶配制物中,所述凝胶配制物通常是由悬浮液(由小无机粒子构成)(两相系统)或大致上均匀地分布在载剂液体中的大有机分子(单相凝胶)组成的半固体系统。尽管凝胶通常采用水性载剂液体,但醇和油也可以用作载体液体。
在一些实施例中,医药组合物包括一或多种防腐剂以保护医药组合物免于抗菌(例如酵母菌、霉菌、细菌)活性或使组合物中的组分稳定。防腐剂包含但不限于苯甲酸钠、苯甲酸、乙二胺四乙酸、山梨酸、苄索氯铵、苯扎氯铵、溴硝丙二醇、对羟基苯甲酸丁酯、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯、thiomerosol、丙酸钠、氯己定、氯丁醇、氯甲酚、甲酚、咪唑烷脲、酚、苯汞盐、山梨酸钾、丙二醇及其混合物。一般来说,医药组合物如固体配制物、溶液、软膏等中的防腐剂的总量可呈现为0.001g/l至0.10g/l,如每100ml溶液悬浮液或100g配制物中的0.01g。如在本文中所提及,在一些实施例中,没有使用防腐剂。
在一些实施例中,将稠合双环胺化合物和/或抗炎剂(特别是被制备成溶液时,如用于不经肠或局部眼用投与)与环糊精一起制备成包含络合物形式。特定来说,对于局部眼用投与,将稠合双环胺化合物与环糊精一起配制,如美国专利公开案第20120302601号中所述,通过引用并入本文中。
在一些实施例中,用于医药组合物中的环糊精可选自α-环糊精、β-环糊精、γ-环糊精、其衍生物及其组合。特定来说,用于本方法中的环糊精选自β-环糊精、γ-环糊精、其衍生物及其组合。
在一些实施例中,环糊精或其衍生物选自羧基烷基环糊精、羟基烷基环糊精、磺基烷基醚(sulfoalkylether)环糊精和烷基环糊精。在各种实施例中,环糊精中的烷基是甲基、乙基、丙基、丁基或戊基。
在一些实施例中,环糊精是α-环糊精或其衍生物。在一些实施例中,α-环糊精或其衍生物选自羧基烷基-α-环糊精、羟基烷基-α-环糊精、磺基烷基醚-α-环糊精、烷基-α-环糊精及其组合。在一些实施例中,α-环糊精衍生物中的烷基是甲基、乙基、丙基、丁基或戊基。
在一些实施例中,环糊精是β-环糊精或其衍生物。在一些实施例中,β-环糊精或其衍生物选自羧基烷基-β-环糊精、羟基烷基-β-环糊精、磺基烷基醚-β-环糊精、烷基-β-环糊精及其组合。在一些实施例中,β-环糊精衍生物中的烷基是甲基、乙基、丙基、丁基或戊基。
在一些实施例中,β-环糊精或其衍生物是羟基烷基-β-环糊精或磺基烷基醚-β-环糊精。在一些实施例中,羟基烷基-β-环糊精是羟丙基-β-环糊精。在一些实施例中,磺基烷基醚-β-环糊精是磺基丁醚-β-环糊精。在一些实施例中,β-环糊精或其衍生物是烷基-β-环糊精,特定来说甲基-β-环糊精。在一些使用甲基-β-环糊精的实施例中,β-环糊精是任意的甲基化β-环糊精。
在一些实施例中,环糊精是γ-环糊精或其衍生物。在一些实施例中,γ-环糊精或其衍生物选自羧基烷基-γ-环糊精、羟基烷基-γ-环糊精、磺基烷基醚-γ-环糊精和烷基-γ-环糊精。在一些实施例中,γ-环糊精衍生物中的烷基是甲基、乙基、丙基、丁基或戊基。在一些实施例中,γ-环糊精或其衍生物是羟基烷基-γ-环糊精或磺基烷基醚-γ-环糊精。在一些实施例中,羟基烷基-γ-环糊精是羟丙基-γ-环糊精。
当用于配制物中时,环糊精可以以下量存在:约0.1重量/体积至约30%重量/体积,约0.1重量/体积至约20%重量/体积,约0.5%重量/体积至约10%重量/体积,或约1%重量/体积至约5%重量/体积。在一些实施例中,环糊精以以下量存在:约0.1%重量/体积,约0.2%重量/体积,约0.5%重量/体积,约1%重量/体积,约2%重量/体积,约3%重量/体积,约4%重量/体积,约5%重量/体积,约6%重量/体积,约7%重量/体积,约8%重量/体积,约9%重量/体积,约10%重量/体积,约12%重量/体积,约14%重量/体积,约16%重量/体积,约18%重量/体积,约20%重量/体积,约25%重量/体积或约30%重量/体积或更多。
在一些实施例中,配制稠合双环胺化合物和抗炎剂(分开地或呈混杂物形式)用于眼用投与。对于眼用局部投与,剂型包含溶液、软膏、凝胶(例如粘稠或半粘稠)、乳液、悬浮液和固体滴眼剂等。特定来说,基于通过患者或医学专业人士的配制和投与的简易性,水溶液通常是优选的。在一些实施例中,组合物提供为冻干配制物形式,其可用适当的药学上可接受的溶液重配。
在一些实施例中,将眼用组合物与一或多种眼用药学上可接受的添加剂或赋形剂一起配制。因此,在一些实施例中,眼用组合物进一步包括眼用药学上可接受的添加剂或赋形剂中的一或多种。
在一些实施例中,一或多种眼用药学上可接受的添加剂或赋形剂选自张力剂、防腐剂、缓冲剂、润湿剂、粘度增强剂、润滑剂、螯合剂和抗氧化剂。
在一些实施例中,眼用组合物可具有一或多种张力剂,其可用于调节组合物的张力,例如,达到天然泪液的张力。作为实例而非限制,合适的张力剂包含聚葡萄糖(例如聚葡萄糖40或70)、右旋糖、甘油、氯化钾、丙二醇和氯化钠。还可使用一或多种盐的等效量,所述盐由阳离子(例如,钾、铵)和阴离子(如氯离子、柠檬酸根、抗坏血酸根、硼酸根、磷酸根、碳酸氢根、硫酸根、硫代硫酸根、硫酸氢根、硫酸氢钠盐和硫酸铵盐)构成。张力剂的量将依据待添加的特定试剂而变化。然而,一般来说,组合物可具有呈足以使得最终组合物具有眼科学上可接受的摩尔渗透压浓度(osmolarity)的量的张力剂。在一些实施例中,眼用组合物的摩尔渗透压浓度(osmolality)为约200至约1000mosm/l或约200至约500mosm/l,或所述范围内的任何特定值(例如200mosm/l、210mosm/l、220mosm/l、230mosm/l、240mosm/l、250mosm/l、260mosm/l、270mosm/l、280mosm/l、290mosm/l、300mosm/l、310mosm/l、320mosm/l、330mosm/l、340mosm/l、350mosm/l、360mosm/l、370mosm/l、380mosm/l、390mosm/l或400mosm/l)在特定实施例中,利用张力剂将眼用配制物调节至在约250至约450mosm/l或约250至约350mosm/l范围内的摩尔渗透压浓度。
在一些实施例中,眼用组合物可具有一或多种防腐剂,例如,以在储存期间以及当在治疗上投与到眼睛上时,延长存放期或限值溶液中的细菌生长。可使用的防腐剂包含苯扎氯铵、苄索氯铵、苯扎溴铵、氯化十六烷基吡啶、氯丁醇、乙二胺四乙酸(edta)、硝酸苯汞、乙酸苯汞、对羟基苯甲酸甲酯/对羟基苯甲酸丙酯(methyl/propylparaben)、苯乙醇、苯甲酸钠、丙酸钠、山梨酸和过硼酸钠等。溶液中的防腐剂的量可为提高存放期、限制细菌生长或以其它方式保存眼部溶液、对眼组织具有极少毒性的水平(参见例如《美国药典(theunitedstatespharmacopeia)》,第22修订版,和《国家处方集(nationalformulary)》,第17版,马里兰州罗克维尔(rockvillemd))。可通过所属领域的技术人员确定适合用于眼部配制物中的防腐剂的水平。在一些实施例中,可以约0.001至约1.0%重量/体积的量使用防腐剂。例如,防腐剂以约0.005至约0.05%重量/体积、0.005至约0.04%重量/体积、0.01至约0.03%重量/体积、0.01至约0.02%重量/体积或约0.01至约0.015%重量/体积的量存在。在一些实施例中,防腐剂的量可为约0.005、0.01、0.012、0.014、0.016、0.018、0.02、0.03、0.04或0.05%重量/体积。在一些实施例中,眼用组合物中不使用防腐剂。
在一些实施例中,眼用组合物可具有一或多种缓冲剂以便调节和/或维持眼部溶液的ph在指定ph范围内。一般来说,缓冲容量应足够大以维持产品ph为了合理的长保存期,但也应足够低以允许将产品快速再调节至投与上的生理ph。一般来说,约0.01至0.1的缓冲容量可用于眼用溶液,特别是在提供足够的缓冲能力并最小化对眼睛的不利影响(例如刺激)的浓度下。作为实例而非限制,示例性的缓冲剂包含适当情况下,以下试剂的多种盐(例如钠、钾等)、酸或碱,包含:乙酸盐、硼酸盐、磷酸盐、碳酸氢盐、碳酸盐、柠檬酸盐、四硼酸盐、二磷酸盐、缓血酸胺、羟乙基吗啉和tham(三羟甲基-甲烷)等。在一些实施例中,缓冲剂可以以下量存在:约0.5mm至约100mm、约1mm至约50mm、约1mm至约40mm、约1mm至约30mm、约1mm至约20mm或约1mm至约10mm。在一些实施例中,缓冲剂可以以下量存在:约0.5mm、约1mm、约5mm、约10mm、约20mm、约30mm、约40mm、约50mm或约100mm。
在一些实施例中,示例性缓冲剂是磷酸盐,特别是磷酸钠,其可通过标准程序(例如通过混合适当量的一或多种单碱磷酸盐、二碱磷酸盐等)来制备。特定来说,适用的磷酸盐缓冲液由碱金属和/或碱土金属的磷酸盐(如磷酸钠或磷酸钾,包含单碱磷酸钠、二碱磷酸钠、单碱磷酸钾和二碱磷酸钾)制备。在一些实施例中,磷酸盐缓冲剂可以以下量存在:约0.5mm至约100mm、约1mm至约50mm、约1mm至约40mm、约1mm至约30mm、约1mm至约20mm或约1mm至约10mm。在一些实施例中,磷酸盐缓冲剂可以以下量存在:约0.5mm、约1mm、约5mm、约10mm、约20mm、约30mm、约40mm、约50mm或约100mm。
在一些实施例中,眼用组合物可具有一或多种润湿剂。一般来说,润湿剂可使眼睛含水并限制眼睛的干燥。润湿剂通常是亲水性聚合物,作为实例而非限制包含聚山梨醇酯20和80、泊洛沙姆282和泰洛沙泊。在一些实施例中,润湿剂也包含纤维素基聚合物如羟丙基甲基纤维素(hpmc)和羧甲基纤维素(cmc)、聚乙烯吡咯烷酮以及聚乙烯醇等。在一些实施例中,润湿剂如hpmc的浓度在约0.1%至约2%重量/体积、约0.5%至约1%重量/体积范围内或所述范围内的任何特定值。在一些实施例中,润湿剂如hpmc的浓度在约0.1%至约1.0%重量/体积范围内,或所述范围内的任何特定值(例如0.1-0.2%、0.2-0.3%、0.3-0.4%、0.4-0.5%、0.5-0.6%、0.6-0.7%、0.7-0.8%、0.8-0.9%、0.9-1.0%;约0.2%、约0.21%、约0.22%、约0.23%、约0.24%、约0.25%、约0.26%、约0.27%、约0.28%、约0.29%、约0.30%、约0.70%、约0.71%、约0.72%、约0.73%、约0.74%、约0.75%、约0.76%、约0.77%、约0.78%、约0.79%、约0.80%、约0.81%、约0.82%、约0.83%、约0.84%、约0.85%、约0.86%、约0.87%、约0.88%、约0.89%或约0.90%)。
在一些实施例中,眼用组合物可具有一或多种粘度增强剂。粘度增强剂通常提高眼部溶液的粘度以增加溶液在眼睛上的滞留时间,且在一些例子中,以在眼睛表面上提供保护层。粘度增强剂包含呈多种分子量形式并呈多种相容性组合形式的卡波普凝胶(carbopolgel)、聚葡萄糖40(分子量为40,000道尔顿(dalton))、聚葡萄糖70(分子量为70,000道尔顿)、明胶、甘油、cmc、羟乙基纤维素、hpmc、甲基纤维素、乙基纤维素、聚乙二醇、泊洛沙姆407、聚山梨醇酯80、丙二醇、聚乙烯醇和聚乙烯吡咯烷酮(聚维酮)等。在一些实施例中,含有药物学活性剂的眼用组合物的粘度在约10至约150厘泊(centipoise)(cpi)、约15至约120cpi、约20至约90cpi范围内(或所述范围内的任何特定值)。在一些实施例中,眼用组合物的粘度在约15cpi至约30cpi范围内,或所述范围内的任何特定值(即约15cpi、约16cpi、约17cpi、约18cpi、约19cpi、约20cpi、约20cpi、约22cpi、约23cpi、约24cpi、约25cpi、约26cpi、约27cpi、约28cpi、约29cpi、约30cpi)。在一些实施例中,含有环糊精的眼用组合物的粘度在约70cpi至约90cpi范围内,或所述范围内的任何特定值(即约70cpi、约71cpi、约72cpi、约73cpi、约74cpi、约75cpi、约76cpi、约77cpi、约78cpi、约79cpi、约80cpi、约81cpi、约82cpi、约83cpi、约84cpi、约85cpi、约86cpi、约87cpi、约88cpi、约89cpi或约90cpi)。特定来说,约25至约50cp的粘度适用于眼用溶液。
在一些实施例中,眼用组合物可具有一或多种润滑剂。眼部润滑剂可接近内生泪液的稠度并辅助天然泪液积累。润滑剂可包含非磷脂基试剂和磷脂基试剂。非磷脂基的眼部润滑剂包含但不限于丙二醇;乙二醇;聚乙二醇;羟丙基甲基纤维素;羧甲基纤维素;羟丙基纤维素;聚葡萄糖,如聚葡萄糖70;水溶性蛋白质,如明胶;乙烯基聚合物,如聚乙烯醇、聚乙烯吡咯烷酮、聚维酮;矿脂;矿物油;以及卡波姆,如卡波姆934p、卡波姆941、卡波姆940和卡波姆974p。非磷脂润滑剂还可包含上述试剂中的任一种的相容性混合物。
在一些实施例中,眼用组合物可包含一或多种抗氧化剂。作为实例而非限制,合适的抗氧化剂包含edta(例如二钠edta)、亚硫酸氢钠、焦亚硫酸钠、硫代硫酸钠、硫脲和α-生育酚。
在各种实施例中,眼用组合物的ph可在距生理ph(特别是在眼睛的外部环境中的生理ph)1.0至1.5ph单位内。人体泪液的ph近似为ph7.4。因此,眼用溶液的ph可为高于或低于ph7.4约1.0至1.5ph单位。在一些实施例中,眼用溶液的ph为约ph6.0至约ph8.5。在一些实施例中,眼用溶液的ph为约ph6.0至约ph8.0。在一些实施例中,眼用溶液的ph为约6.5至约8.0。在一些实施例中,眼用溶液的ph为约7.0至约8.0。在一些实施例中,眼用溶液的ph为约7.0至约7.5。在一些实施例中,眼用溶液的ph为约6.5、约7、约7.5、约8或约8.5。所属领域的技术人员可选择使眼用组合物的稳定性和眼睛对固有病况的不同ph的耐受性平衡的ph。如在所属领域中众所周知的,可通过使用适当的缓冲剂和/或利用适当的基质(例如氢氧化钠)或酸(例如氢氯酸)调节溶液的ph。
5.4.投与和有效剂量
可通过多种途径,分开或同时向患有眼部炎性病症或疾病的受试者投与稠合双环胺化合物和抗炎剂。在一些实施例中,可通过以下方式投与医药组合物:注射、吸入或吹入(通过口或鼻)或经口、经颊、舌下、经皮、经鼻、眼用、不经肠或经直肠投与。对于亲本投与,医药组合物可肌内、静脉内、腹膜内和皮下投与。
在治疗眼部炎性疾病或病症的方法中,以治疗有效量投与稠合双环胺化合物和抗炎剂以治疗患有眼部炎性疾病或病症的受试者。一般来说,用组合疗法治疗的受试者是哺乳动物,例如犬、猫、马或兔。在一些实施例中,受试者是非人类灵长类动物,例如猴、黑猩猩或大猩猩。在一些实施例中,受试者是人类,在本文中有时被称作患者。在一些实施例中,人类患者是成年患者。在一些实施例中,人类患者是儿科患者。
在治疗眼部炎性病症或疾病的方法中,可依次或同时投与稠合双环胺化合物和抗炎剂或其医药组合物。在一些实施例中,通过相同途径同时投与稠合双环胺化合物和抗炎剂。在一些实施例中,通过不同途径同时投与稠合双环化合物和抗炎剂。在一些实施例中,通过相同途径依次投与稠合双环胺化合物和抗炎剂。在一些实施例中,通过不同途径依次投与稠合双环胺化合物和抗炎剂。在一些实施例中,投与稠合双环胺化合物后接着投与抗炎剂。在一些实施例中,投与抗炎剂,接着投与稠合双环胺化合物。在于不同时间投与稠合双环胺化合物和抗炎剂的情况下,在一些实施例中,允许投与之间有足够量的时间或治疗上有效的时间间隔,以避免稠合双环胺化合物与抗炎剂之间的任何不利相互作用和/或与用于相应医药组合物中的赋形剂和/或载剂的不利相互作用,并且还使治疗有效性最大化。
在治疗眼部炎性病症或疾病的方法中,以治疗有效量投与稠合双环胺化合物和抗炎剂以治疗眼部炎性疾病或病症。在一些实施例中,剂量在以下方面是治疗上有效的:预防在此前经受过所述疾病或病症的受试者中出现眼部炎性病症或疾病;抑制眼部炎性疾病或病症,或综合症,即遏制眼部炎性病症的产生或发展;或缓解眼部炎性疾病或病症,如使眼部炎性疾病或疾病消退,或减轻或消除眼部炎性疾病或病症的相关症状。
在一些实施例中,以有效量投与稠合双环胺化合物和抗炎剂以对未显现出眼部炎性疾病或病症的体征或症状或仅显现出眼部疾病或病症的早期体征或症状的受试者进行防治性治疗,使得治疗是出于消除、预防或减小疾病、病变或医学病症发展的风险的目的而施用的。
确定治疗有效剂量可考虑:治疗是否用于发作中的疾病或病症或用于防治性治疗,眼部炎性病症的本质,病况的严重程度,疾病或病症的阶段,投与途径(例如内吸传送相对于定域传送),受试者(依物种、年龄、体重、一般健康状况、性别、饮食而定)投与时间和药物相互作用等。
在一些实施例中,对于全身性投与,可以约0.01mg/kg至约50mg/kg且优选地约1mg/kg至约25mg/kg(受试者每天的体重)的剂量水平一天一次或多次、每周一次、两周一次或每月一次经口或非经肠地投与稠合双环胺化合物,以获得期望的治疗效果。
对于局部眼用投与,稠合双环胺化合物可以以下浓度存在:约0.05%重量/体积至约10%重量/体积、约0.1%重量/体积至约5%重量/体积、约0.2%重量/体积至约4%重量/体积、约0.3%至约3%重量/体积、约0.4%重量/体积至约2%重量/体积或约0.5%重量/体积至约1.5%重量/体积。在一些实施例中,稠合双环胺化合物可以以下浓度存在:至少约0.05%重量/体积、约0.1%重量/体积、约0.2%重量/体积、约0.3%重量/体积、约0.4%重量/体积、约0.5%重量/体积、约0.6%重量/体积、约0.7%重量/体积、约0.8%重量/体积、约0.9%重量/体积、约1%重量/体积、约1.5%重量/体积、约2%重量/体积、约3%重量/体积、约4%重量/体积、约5%重量/体积、约6%重量/体积、约7%重量/体积、约8%重量/体积、约9%重量/体积或约10%重量/体积。局部投与的量可为每剂量约20至约100ul、每剂量约30至80ul或每剂量约40至60ul。可通过液滴数量(其中取决于所用装置的类型,一个液滴是~40-60微升/液滴(例如~50微升/液滴))来估计体积。一般来说,向眼睛投与单液滴。在一些实施例中,每天一次、每周一次、两周一次或每月一次地投与化合物。在一些实施例中,可根据需要每天一次、每天两次、每天三次、每天四次、每天五次、每天六次、每天七次、每天八次或更多次地投与化合物,以达到治疗效果。在一些实施例中,每2天一次或每3天一次地局部投与化合物。在一些实施例中,每周一次、每两周一次或每月一次地局部投与化合物。
抗炎剂的剂量将考虑除了用于确定稠合双环胺化合物的治疗有效剂量中的因素之外的以下因素:抗炎剂的类型、稠合双环胺化合物与抗炎剂的相互作用(如协同作用的存在)和组合的任何不利影响(例如毒性)等。在一些实施例中,可使用标准剂量的抗炎化合物。在《医师案头参考(physician'sdeskreference)》,第70版,《pdr网(pdrnetwork)》(2016)(通过引用并入本文中)和可用于审批通过的药物的处方信息中,指南是可用的。
可以5至80毫克/天(例如0.05mg/kg至1.5mg/kg),依据给药结果每天一次、每天两次、每天三次至多每天四次地全身性(例如经口)投与甾类。初始治疗可以是每天一次持续2天或更多天、3天或更多天、4天或更多天,接着是每天一次、每天两次、每天三次或每天4次的约0.5至1mg/kg的维持剂量。
对于局部眼用投与,甾类可以以下浓度存在:约0.1重量/体积至约2%重量/体积、约0.2重量/体积至约1.75%重量/体积、0.5%重量/体积至约1.5%重量/体积、0.75%重量/体积至约1.25%重量/体积。在一些实施例中,甾类以以下浓度存在:约0.1重量/体积、0.2%重量/体积、0.5%重量/体积、0.75%重量/体积、1%重量/体积、1.25%重量/体积、1.5%重量/体积、约1.75%重量/体积或约2%重量/体积。可根据需要每天一次、每天两次、每天三次、每天四次、每天五次、每天六次、每天七次、每天八次或更多次地应用眼用甾类溶液。对于初始治疗,可前两天每两小时一次且然后每天2次、每天3次或至多每天4次地应用甾类。用作稠合双环胺化合物的佐剂的示例性甾类是pred
可以取决于非甾类抗炎化合物的特定类型的0.1mg/kg(例如10mg)至约1.5mg/kg(例如约100mg)每天一次、每天两次、每天三次、至多每天四次地全身性(例如经口)投与非甾类抗炎化合物。对于眼用配制物,依据药物的特定类型,非甾类抗炎化合物可以0.01%至约0.5%重量/体积的量存在。可每天一次、每天两次、每天三次、至多每天四次地投与眼用配制物。特定的处方信息可用于溴芬酸、双氯芬酸、氟比洛芬、酮基布洛芬和奈帕芬胺的经口和眼用配制物。参见《医师案头参考》,第70版,《pdr网》(2016),通过引用并入本文中。
以取决于试剂的特定类型的剂量投与抗代谢物。例如,以每周一次约0.1mg/kg(例如7.5mg)至约0.4mg/kg(例如25mg)的剂量开具甲氨蝶呤处方药用于经口或静脉内投与。将硫唑嘌呤以约2至3毫克/千克/天的剂量经口投与,且然后基于临床响应调节。当全身性(例如经口)投与时,可以约500毫克/天至1克/天的剂量开具霉酚酸和其前药(霉酚酸吗啉乙酯)处方药。参见例如baltatzis等,2003,《眼科学(ophthalmology)》110(5):1061-1065。可每天一次、每天两次、每天三次或至多每天四次地投与含有约1%重量/体积至约5%重量/体积的霉酚酸或霉酚酸吗啉乙酯的眼用配制物。参见例如wo2006116591,通过引用并入本文中。
可全身性(例如经口)投与免疫调节抗生素环孢灵。可以每天2.5mg/kg至约5mg/kg投与环孢灵。初始剂量可使用较低剂量且所述剂量逐渐增加至最大剂量。可以每天0.10mg/kg至0.15mg/kg的剂量全身性(例如经口)投与他克莫司。可以约2至6毫克/天的剂量全身性(例如经口)投与雷帕霉素。初始剂量可处于较高剂量下,接着是初始治疗后的较低剂量。可以约0.002%重量/体积至约0.2%重量/体积、更优选地0.02%重量/体积至约0.1%重量/体积的浓度制备免疫调节抗生素的眼用配制物。参见例如第7083803号美国专利。0.05%环孢灵(0.5mg/ml)的眼用配制物可以名称
烷基化剂的细胞毒性作用会限制其使用。通常以约1g/cm2的剂量静脉内投与环磷酰胺。可每两周一次用环磷酰胺进行治疗。可以约每天约0.1mg/kg至0.2mg/kg的剂量经口投与苯丁酸氮芥。
在抗炎剂是生物剂的情况下,可根据处方信息投与。可25mg一周两次地皮下投与依那西普。可以约3mg/kg至约5mg/kg的剂量通过在第0周、第2周和第6周输注来静脉内投与英利昔单抗。可在初始治疗后每8周执行一次维持治疗。以每两周40mg的剂量皮下投与阿达木单抗
可通过所属领域的技术人员(如医师或其它医务人员)确定治疗的持续时间。在一些实施例中,有效给药方案下的治疗可持续至多2周、4周、6周或8周或更长。在一些实施例中,治疗可为至多3个月、4个月、6个月或至多8个月。在一些实施例中,根据需要治疗可持续至多一年或更长、或2年或更长、或无限期以治疗眼部炎性病症或疾病。所属领域的技术人员可鉴于本申请案中提供的指南确定有效剂量、治疗方案和治疗的持续时间,以用组合治疗来治疗眼部炎性病症。
在另一方面,可将双环胺化合物和抗炎剂设置成试剂盒形式。在一些实施例中,所述试剂盒包括如本文所述的双环胺化合物和抗炎剂。在一些实施例中,所述试剂盒含有单个剂量或多个剂量的双环胺化合物和抗炎剂。在适当情况下,可将试剂盒中的双环胺化合物和/或抗炎剂设置成固体或粉末形式,如片剂或囊片或胶囊。在一些实施例中,例如为了足够用于所限定的治疗周期(例如天、周、月等)的剂量,可将固体形式设置在小瓶或泡罩包装中。在一些实施例中,如对于局部投与,试剂盒中的双环胺化合物和/或抗炎剂呈凝胶或乳膏形式。
在一些实施例中,可将试剂盒的双环胺化合物和/或抗炎剂设置成溶液形式,或粉末形式,以便用合适的药学上可接受的溶液如无菌水或盐水重配。可将溶液设置在小瓶、导管、安瓿、针筒等中。在一些实施例中,为了局部眼用投与,将双环胺化合物和/或抗炎剂设置在一次性小瓶优选地单次使用小瓶(如带折断盖或撕裂盖的塑料瓶)中。试剂盒还可包含测量装置,如滴管、分级杯或小瓶,以测量和/或分配溶液。
6.实例
实例1:随机、研究者掩蔽的比较物对照试验,用于研究在前葡萄膜炎患者中的ns2化合物滴眼剂
葡萄膜炎是涉及葡萄膜结构(例如虹膜、睫状体和脉络膜)的眼睛发炎。具体地说,前葡萄膜炎是指眼前段中的葡萄膜炎。其还可涉及眼后段或整个眼睛(全葡萄膜炎)。前葡萄膜炎的临床体征和症状可包含疼痛、视物模糊、结膜皮肤充血、前房细胞、前房闪辉(flare)、纤维蛋白沉积和角膜内皮炎性沉淀物。葡萄膜炎并非单一的疾病实体,而是呈与多组感染性和非感染性病况相关的眼部发炎形式。
ns2是被配制成用于本研究的作为局部滴眼剂的新型醛捕捉剂。毒性醛代谢物如丙二醛(mda)的积聚与前葡萄膜炎和其它眼部和全身性疾病相关。有迹象表明预防毒性醛形成和积聚可防止与眼部疾病相关的发炎、纤维化和氧化性损伤(sandikci等,2003,《皮肤性病学报(actadermvenereol)》,83(5):342-6;cejkova等,2007《组织学与组织病理学(histolhistopathol)》22(9):997-1003;balci等,2011,《分子视觉(molvis)》17:443-7;turk等,2014,《眼部免疫与发炎(oculimmunolinflamm)》22(2):127-32;serbecic等,2005,《细胞和组织研究(celltissueres.)》320(3):465-75;demir等,2005,《眼科(ophthalmologica)》219(1):49-53;demir等,2010,《英国眼科学杂志(brjophthalmol.)》94(8):1083-7)。此外,考虑到与长期皮质甾类使用相关的青光眼、白内障和角膜溃疡的发病率,需要皮质甾类的安全和有效的替代方案作为葡萄膜炎和其它形式的眼部发炎的第一线和辅助治疗。将本研究设计成评定ns2滴眼剂相比于活性比较物pred
所提议的概念验证研究将使用0.5%剂量水平的ns2。所述剂量是基于ind104,497下的1期临床研究结果和以0.5%、0.25%和0.1%(重量/体积)qid(ou)给药的9个月的犬研究而选择的。在临床研究中,0.5%ns2组中的7天qid给药耐受性良好且ns2的血浆水平保持在每个受试者的检测极限(5ng/ml)以下。ns2在犬研究中的耐受性也良好,且在宏观或微观评估期间未注意到异常发现。基于其中0.5%ns2被qid局部投与的9个月的犬研究的安全性和7天1期临床研究,提议最长治疗持续时间为6周。
为了允许持续暴露,在组1和组2中将以每天4次的剂量投与ns20.5%。浓度为10μm的醛在细胞培养中具有细胞毒性(maeda等,2012,《自然-化学生物学(natchembiol.)》8(2):170-8)。因此,在炎性疾病中,醛组织浓度很可能显著降低。在灵长类动物中,单个剂量的0.5%ns2产生在17.6μm(正好在给药后)至1.2μm(给药后三小时)范围内的前眼组织浓度。这些数据表明,在本研究中的投与时程下,葡萄膜炎受试者中的ns2组织水平应超过醛组织水平,可能消除大多数(如果并非全部)的游离醛。
总之,本研究是比较物对照临床试验,其中多达45名患有非感染性前葡萄膜炎的受试者将被随机分组(1:1:1)到接收组中:
组1-ns2眼用滴剂(0.5%);
组2-ns2眼用滴剂(0.5%)和pred
组3-pred
给药时程概括于表1中。
表i:滴眼剂方案的给药时程
组2患者将交替给药ns2和pred
基于预定义的急救准则,所有未表现出临床反应的患者均可获得急救治疗。急救治疗将由在治疗医师的临床判断下给药的治疗组成。获救的患者将在急救后一周接受后续评定,且然后其将停止参与本研究。
每个受试者的研究参与将由筛检/随机问诊(问诊1)、第4天(问诊2)、第1周(第8天+/-1天;问诊3)、第2周(第15天+/-1天;问诊4)、第4周(第29天+/-3天;问诊5)和第8周(第57天+/-3天;问诊6/eot)组成。本研究的总时间约8周。
对于每个受试者,将执行最多6次安排问诊和eot/et问诊一周后的后续/eos电话:用于本研究的整个评定时程提供于表2中。
表2.问诊和评定时程
*将绘制所有受试者的一般实验室(有差异的cbc和cmp)作为基线测量。将获得经历首次前葡萄膜炎并发性症状的患者(只要其病史对葡萄膜炎的风险因素来说是显著的)或经历重复并发性症状的患者的葡萄膜炎-特定实验室(hla-b27、rpr、fta-abs、ace、ana)和胸部x射线。
**可以在研究者的判断下,在第4天至第4周问诊时采集额外的眼部照片,以记录任何临床上显著的发现。
***研究结束后第9周问诊将由随访电话组成,以收集最终安全性数据。
研究药物将由患者(或护理人员)而自行投与。将指导受试者按照他们被分配的治疗分支投与研究药物。随机分组到ns2或pred
评估研究方案和结果。非感染性前葡萄膜炎发作的患者的局部眼部ns2的ii期临床试验显示在统计学上不可区分ns2与护理皮质甾类投与标准品的眼前房中的减少炎性细胞计数。在假定的促炎角色中,醛在发炎早期表现出上调,且通过涉及结合某些氨基酸残基的新型发信机制改变蛋白质功能。足够的醛结合改变蛋白质特别是激酶和蜂窝式受体的功能,且然后产生促炎转录因子的刺激,这又导致由细胞因子介导的炎性反应。细胞因子是发炎的典型靶标,而迄今为止醛已被忽略,且因此代表治疗炎性疾病的新靶标。
炎性路径受th1和th2细胞因子平衡的影响,认为所述细胞因子各自引起两种共同类型的炎症、自体免疫疾病和过敏。鉴于过敏性结膜炎(常见的影响眼睛的过敏性疾病)的局部眼部ns2的ii期临床试验的阳性数据,以及非感染性前葡萄膜炎的阳性结果,ns2现已证明在自身免疫类炎症中有效,且因此ns2,至少在眼睛中,代表广泛的抗炎药物候选,可用于治疗许多炎性疾病。
2015《美国哮喘、过敏和免疫学会(americanacademyofasthma,allergy,andimmunology)》所呈现的数据指示在细胞因子风暴的小鼠模型中,全身性投与ns2显著降低th1(或自身免疫相关)和th2(或过敏相关)炎性细胞因子两者的水平,而上调了辨识最多的抗炎细胞因子il-10。2015《视觉与眼科学研究协会(associationforresearchinvisionandophthalmology)》(或arvo)所呈现的数据指示在眼部发炎的大鼠模型中,局部眼部ns2的活性与局部眼部皮质甾类投与的活性相比是有利的。
基于所提议的醛在调节炎症中的角色,除了ns2在减少il-5和其它th2细胞因子方面的临床前活性之外,还在过敏性结膜炎患者中启动单个剂量的局部眼部ns2的ii期临床试验,且在2016年2月从所述试验中获得正面结果。此前已报告试验设计和来自所述试验的数据。在单滴滴眼剂之后,局部眼部ns2显著减少过敏性结膜炎中的眼部发痒和流泪。给药14天后,ns2的积极临床作用持续。
基于葡萄膜炎的临床前模型中ns2在消除th1细胞因子以及眼部发炎中的临床前活性,在非感染性前葡萄膜炎(可导致失明的罕见但严重的自身免疫类眼部疾病)发作的患者中启动局部眼部ns2的ii期试验。前葡萄膜炎ii期试验的设计是随机、平行组、研究者掩蔽的比较物对照试验,以评估ns2眼用溶液对前葡萄膜炎患者的安全性和功效。所述试验评定前葡萄膜炎的体征和症状,包含前房细胞计数,其被用作前葡萄膜炎立项研究的主要终点。本研究在美国的15个临床点进行。
将患有非感染性前葡萄膜炎的四十五(45)名受试者随机分组到三个治疗组:两个单药疗法组和一个组合治疗组中的每一个中。所述组是:ns2眼用滴剂0.5%,每天给药四(4)次持续6周;predforte,即乙酸泼尼松龙眼用悬浮液1%,每天给药四(4)次,且然后历经6周递减;以及组合治疗组,其中每天四(4)次给药ns2眼用滴剂0.5%持续6周,这与单药疗法组的方案相同。每天两(2)次给药pred
对患者进行长达8周的随访且为了安全性和功效在六次安排的问诊时进行监测。通过标准眼科检查程序(包含裂隙灯检查)评定功效,且根据所建立的葡萄膜炎标尺对治疗反应进行分级。问诊时程包含筛检随机化问诊、第4天电话后续问诊和第1周、第2周、第4周和第8周的诊所问诊。
基于标准的预定义急救准则,使所有未表现出临床反应的患者均可获得急救治疗,所述急救治疗由在治疗医师的临床判断下选定和给药的药剂组成。对获救的患者进行研究问诊结束后8周的随访。
如上文初始所论述,研究结果显示在所述前葡萄膜炎人群中,ns2对前房细胞计数(简称为acc)产生临床上有意义的作用。这一点可见于以下两者:达到acc的0级治疗反应的患者的比例以及通过对acc的至少1级的改进的比例。在大多数问诊中,所述三个治疗组的这些acc治疗作用相当。在第2周研究问诊时,0级acc治疗反应见于33%的ns2患者、31%的pred
对于末次观测值结转(lastobservationcarriedforward,locf)和非locfmitt人群两者,acc的减少模式在三个治疗组当中是相当的。值得注意的是对前房闪辉的反应与针对前房细胞计数所述的作用类似。
尽管试验规模小且未正式发动,但在这些目标眼科检查终点中的任一个上,所述三个治疗组之间未证明有统计学上显著的不同。
通常,ns2在前葡萄膜炎人群中耐受性良好,且在本研究(包含眼部检查得分、内眼压力、角膜厚度和视力)期间没有安全性问题。在经ns2治疗的组中,眼部刺痛和灼热的频率增加。这些类型的不良事件在目前的局部眼部治疗中并不少见。ns2组中的一名受试者和组合组中的一名受试者由于刺痛不良事件而退出。没有严重的不良事件。
结果已描述为非常令人鼓舞的临床试验,其中ns2证明在前葡萄膜炎中的清晰活性,无显著的不利影响迹象。这表明ns2可为针对前葡萄膜炎患者的重要的未来治疗选择。不具眼压上升性质或白内障产生的与局部皮质甾类相当的疗效会使得这种抗炎治疗成为治疗葡萄膜炎的有吸引力的治疗选择。
此外,基于两项眼部研究中两项临床上有意义的活动的成功证明,并在临床眼科学专家的鼓励下,目前正在对罕见和常见疾病的额外眼部发炎ii期试验设计进行评估。
然而显然常用局部皮质甾类治疗非感染性前葡萄膜炎和其它眼部疾病,皮质甾类常常导致白内障、青光眼和其它导致显著和昂贵的发病率的眼部并发症。因此,在眼部发炎以及影响身体其它方面的炎症中,对新型非甾类治疗存在大量需求。鉴于ns2已在两种主要形式的眼部发炎中表现出活性,ns2的其它潜在指示是ns2成功完成临床开发并获得监管机构的上市许可。有许多其中ns2可具有临床效用的疾病,并且总体来说,所述疾病代表许多患者。例如,据估计有约1百万过敏性结膜炎患者对抗组织胺(所述疾病的治疗支柱)具有抗性,且需要局部皮质甾类以有效对症控制。品牌皮质甾类治疗平均每个疗程可花费多达400美元。基于2015ims数据,局部眼部皮质甾类呈现约15亿美元的收益,其中约80%来自品牌产品。因此,目前用于治疗眼部发炎的新型非甾类抗炎药剂的市场是相当大的。
本申请案中所引用的所有出版物、专利、专利申请案和其它文献都通过整体引用并入于此以用于所有目的,其程度就如同单独指示各个出版物、专利、专利申请案或其它文献通过引用并入以用于所有目的。
虽然已示出并描述了多个特定实施例,但应了解可在不脱离本发明的精神和范围的情况下进行多种变更。
- 还没有人留言评论。精彩留言会获得点赞!