可穿戴传感器的生物淤积预防以及与其相关的使用和校准方法与流程
本申请要求于2016年7月18日提交的美国临时申请号62/363,577、以及于2016年7月18日提交的美国临时申请号62/363,572的优先权。两个美国临时申请的公开内容通过引用以其整体并入本文。
关于联邦资助研究或开发的声明
不适用。
本文公开和/或请求保护的发明概念涉及可穿戴传感器的使用和校准的装置和方法,所述可穿戴传感器包括但不限于糖尿病前期可穿戴传感器。更具体而言,本文公开和/或请求保护的发明概念涉及可穿戴传感器,其被配置为减少和/或消除此类可穿戴传感器的生物淤积(biofouling)。
背景
存在用于连续检测分析物的众多装置和方法,所述分析物可能存在于患者的流体样品包括例如患者的间质液样品中。当此类装置留置在患者体内,例如在患者的角质层或表皮组织中时,已被证明在检测和连续监测指示特定疾病或病症(例如,仅作为示例,糖尿病)的分析物的浓度方面是有效的。另外,当装置留置在患者体内时,此类装置可以有效地递送例如药物和/或其它治疗化合物。然而,此类留置的可穿戴的传感器存在显著的问题—生物传感器的微针的生物淤积,这减少了生物传感器本身的准确性,寿命以及在一些情况下,一致的功能。生物淤积指与伤口愈合过程相关的自然现象,其中留置传感器和/或其微针被患者的身体感知为外来物。因此,触发了生物应答(例如包括不同的止血、炎症、增殖和成熟阶段的伤口愈合级联),其促使细胞和蛋白质(和/或其它生物物质)与微针结合,从而损害、危害和/或破坏生物传感器功能。相应地,目前需要改善的留置的可穿戴的生物传感器,其减轻和/或消除生物淤积过程的有害效应,且从而改善生物传感器的连续功能、主动传感和可佩戴的持续时间。在一个实施方案中,此类改善的传感器(以及与其相关的使用方法)可以包括微针阵列,其包括至少一根微针,所述至少一根微针包含抑制伤口愈合过程的至少一种化合物。另外(或可选地),改善的留置的可穿戴的生物传感器还可以包括至少一个压电元件,其可以接收来自检测器的电信号,导致至少一个压电元件振动,从而移除和/或去除沉积在生物传感器的微针上或其中的任何细胞、蛋白质和/或其它生物物质。本文公开和请求保护的发明概念涉及此类改善的装置和方法。
附图的几个视图的描述
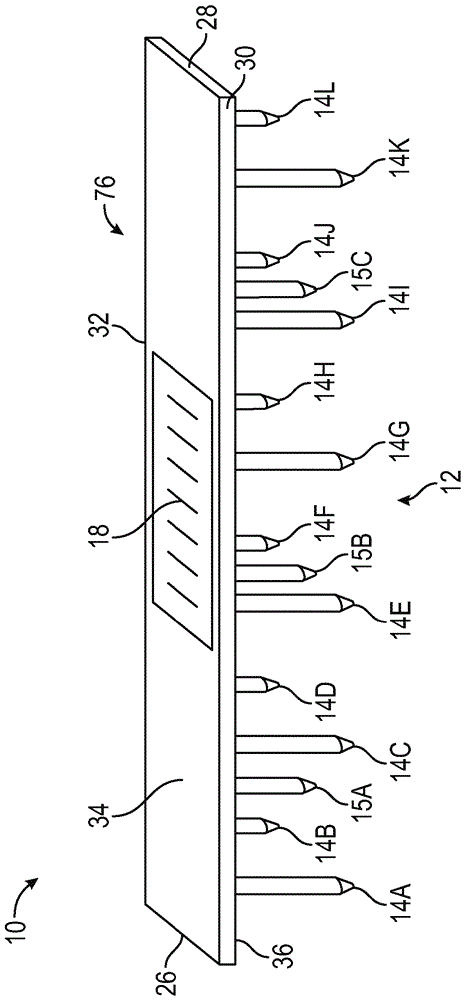
图1是本文公开和/或请求保护的改善的留置的可穿戴的生物传感器的一个实施方案的透视侧视图。
图1a是图1的留置的可穿戴的生物传感器的另外实施方案的透视侧视图,所述生物传感器进一步包括多根校准微针。
图2a是本文公开和/或请求保护的改善的留置可穿戴生物传感器的改善微针的一个实施方案的正面侧视图。
图2b是图2a中描绘的本文公开和/或请求保护的改善的留置的可穿戴的生物传感器的改善微针的尖端部分的一个实施方案的详细正面侧视图,其中进一步示出了荧光团传感器。
图3是本文公开和/或请求保护的发明概念的改善微针的尖端部分的一个实施方案的详细示意图,其中至少一种抗伤口愈合化合物与形成微针的聚合物材料结合,使得抗伤口愈合化合物包被到微针的至少一个表面上,以预防、减轻和/或消除生物传感器的生物淤积。
图4是本文公开和/或请求保护的发明概念的改善的留置的可穿戴的生物传感器的一个实施方案的侧视图,其中所述生物传感器留置在患者的表皮组织内,并且与患者的流体样品流体连通。
图5是描绘本文公开和/或请求保护的发明概念的可选实施方案的示意图,其包括用于预防、减轻和/或消除生物传感器的生物淤积的压电元件。
详细描述
在通过示例性附图、实验、结果和实验室程序详细解释本发明概念的至少一个实施方案之前,应理解,本发明概念并不限于其对下述描述中阐述或者附图、实验和/或结果中示出的构造细节和元件布置的应用。本发明概念能够具有其它实施方案,或者能够以各种方式实践或进行。照此,本文使用的语言预期给予最广泛的范围和含义;并且实施方案意欲是示例性的—而非穷举性的。另外,应理解,本文采用的措辞和术语是用于描述的目的,并且不应视为限制性的。
除非本文另有定义,否则结合本文公开和请求保护的发明概念使用的科学和技术术语应该具有本领域普通技术人员通常理解的含义。此外,除非上下文另有要求,否则单数术语应该包括复数,并且复数术语应该包括单数。前述技术和程序一般根据本领域众所周知的和在本说明书自始至终可以引用且讨论的各种一般和更具体的参考文献中所述的常规方法执行。与本文所述的分析化学、合成有机化学、以及医学和药物化学结合利用的命名法以及实验室程序和技术是本领域众所周知和常用的那些。
说明书中提及的所有专利、公开的专利申请和非专利出版物指示了本文公开和请求保护的发明概念所属领域的技术人员的技术水平。在本申请的任何部分中引用的所有专利、公开的专利申请和非专利出版物明确地通过引用以其整体并入本文,其程度如同每个个别专利或出版物具体地和个别地指出通过引用并入。
根据本公开内容,无需过度实验即可制造和执行本文公开且请求保护的所有装置、试剂盒和/或方法。虽然已根据优选实施方案描述了本文公开和请求保护的发明概念的组合物和方法,但对于本领域技术人员显而易见的是,可以对本文描述的组合物和/或方法以及方法的步骤或步骤顺序应用变化,而不脱离本文公开和请求保护的发明概念的概念、精神和范围。对于本领域技术人员显而易见的所有此类类似的取代和修改被认为在如由所附权利要求限定的本发明概念的精神、范围和概念内。
如根据本公开内容利用的,除非另有说明,否则下述术语应理解为具有下述含义:
当在权利要求和/或说明书中与术语“包含/包括”结合使用时,词语“一个”或“一种”可以意指“一个/种”,但它也与“一个或多个/一种或多种”、“至少一个/种”以及“一个/种或多于一个/种”的含义一致。除非上下文另有明确说明,否则单数形式“一个”、“一种”和“该/所述”包括复数指示物。因此,例如,提及“化合物”可以指1种或多种、2种或更多种、3种或更多种、4种或更多种或更多数目标化合物。术语“多个”指“两个或更多个”。权利要求中术语“或”的使用用于意指“和/或”,除非明确指出仅指可选方案或可选方案是互相排斥的,尽管公开内容支持仅指可选方案和“和/或”的定义。本申请自始至终,术语“约”用于指示值包括装置的固有误差变化、用于确定值的方法、或研究物体中存在的变化。例如但不作为限制,当利用术语“约”时,指定值可以从指定值变化±20%或±10%、或±5%、或±1%、或±0.1%,如此类变化适于执行所公开的方法并且如本领域普通技术人员所理解的那样。术语“至少一个”的使用应理解为包括一个以及多于一个的任何数目,包括但不限于2、3、4、5、10、15、20、30、40、50、100等。术语“至少一个”可以延伸直到100或1000或更多,这取决于与之连接的术语;另外,100/1000的数量并不视为限制性的,因为更高的限制也可产生令人满意的结果。另外,术语“x、y和z中的至少一个”的使用应理解为包括单独的x、单独的y和单独的z,以及x、y和z的任何组合。例如,序数数字术语(即“第一”、“第二”、“第三”、“第四”等)的使用仅用于区分两个或更多个项目的目的,并不意欲例如暗示一个项目相对于另一个的任何顺序或次序或重要性或者任何添加次序。
如本说明书和权利要求中所使用的,术语“包含(comprising)”(以及任何形式的包含,例如“包含(comprise)”和“包含(comprises)”)、“具有(having)”(以及任何形式的具有,例如“具有(have)”和“具有(has)”)、“包括(including)”(以及任何形式的包括,例如“包括(includes)”和“包括(include)”)、或“含有(contain)”(以及任何形式的含有,例如“含有(contains)”和“含有(contain)”)是包含性的或开放式的,并且不排除另外未列举的要素或方法步骤。
如本文使用的,术语“或其组合”指该术语之前列出的项目的所有排列和组合。例如,“a、b、c或其组合”预期包括以下中的至少一种:a、b、c、ab、ac、bc或abc,并且如果次序在特定背景下是重要的,则也是ba、ca、cb、cba、bca、acb、bac或cab。继续该实例,明确包括的是含有一个或多个项目或术语的重复的组合,例如bb、aaa、aab、bbc、aaabcccc、cbbaaa、cababb等等。本领域技术人员应理解,除非根据上下文另外显而易见,否则通常对任何组合中的项目或术语的数目没有限制。
如本文使用的,术语“基本上”意指随后描述的事件或情况完全发生、或者随后描述的事件或情况在很大程度上或范围内发生。例如,术语“基本上”意指随后描述的事件或情况在至少90%的时间、或至少95%的时间、或至少98%的时间发生。
如本文使用的,短语“与……结合”包括两个部分彼此的直接结合以及两个部分彼此的间接结合。结合的非限制性实例包括一个部分通过直接键或通过间隔基团与另一个部分的共价结合,一个部分直接或借助于与部分结合的特异性结合对成员与另一个部分的非共价结合,例如通过将一个部分溶解于另一个部分中或通过合成、并且将一个部分包被到另一个部分上,将一个部分掺入另一个部分内。
术语“抗伤口愈合化合物”包括减轻、抑制和/或消除伤口愈合过程和/或级联的任何化合物、物质或其组合。抗伤口愈合化合物的实例包括但不限于免疫抑制化合物、皮质类固醇、壳聚糖、非甾体抗炎药、包括但不限于阿司匹林、萘普生和/或布洛芬、以及抗凝化合物及其组合。抗伤口愈合化合物可以掺入微针阵列的每根、一些或所有微针上或其中,包括但不限于经由将抗伤口愈合化合物包被到微针阵列的每根、一些或所有微针的一个或多个表面上。可选地或除此之外,抗伤口愈合化合物可以在微针阵列的制造过程中浸渍在形成微针的聚合物材料内。
如本文使用的,术语“生物淤积”指细胞、蛋白质和/或其它生物物质在留置、可穿戴生物传感器的微针阵列的微针的至少一个表面上和/或微针中的累积和/或附聚,使得生物传感器的功能受损、危害和/或消除。此类细胞、蛋白质、其它生物物质包括但不限于纤维蛋白、纤连蛋白、糖蛋白、生长因子、激肽、细胞因子、趋化因子、成纤维细胞、血小板、促炎因子(包括但不限于血清素、缓激肽、前列腺素、前列环素、血栓素和组胺)、蛋白酶、巨噬细胞、单核细胞、吞噬细胞、血管活性胺、类二十烷酸、白细胞和嗜中性粒细胞(包括多形核嗜中性粒细胞)。
如本文使用的,术语“电路”可以是模拟和/或数字元件、或者一个或多个适当编程的处理器(例如,微处理器)以及相关的硬件和软件、控制器或硬连线逻辑。另外,“元件”可以执行一种或多种功能。术语“元件”可以包括硬件,诸如处理器(例如,微处理器)和专用集成电路(asic)、现场可编程门阵列(fpga)、硬件和软件的组合、和/或类似物。如本文使用的,术语“处理器”意指单个处理器或多个处理器,其独立工作或一起工作以共同执行任务。
如本文使用的,术语“流体样品”应理解为包括可以根据本文公开和请求保护的发明概念利用的任何类型的生物流体样品。可以利用的生物样品的实例包括但不限于全血或其任何部分(即血浆或血清)、唾液、痰、脑脊髓液(csf)、肠液、腹腔液、囊液、汗液、间质液、泪液、粘液、尿、膀胱冲洗液、精液、组合等等。在一个非限制性实施方案中,根据本文公开和/或请求保护的发明概念利用的流体样品是间质液。
术语“患者”包括人和兽医学主体。在某些实施方案中,患者是哺乳动物。在某些其它实施方案中,患者是人,包括但不限于婴儿、幼儿、儿童、年轻人、成年人和老年人群体。用于治疗目的的“哺乳动物”指被分类为哺乳动物的任何动物,包括人、驯养动物和农场动物、非人灵长类动物以及动物园、运动或宠物动物,例如犬、马、猫、牛等。
术语“压电”、“压电现象”和/或“压电效应”意指某些材料响应机械应力和/或压力变化而生成电荷的能力。另外,这些术语包括反向(即,反向压电效应),这意指当暴露于电场、电信号或电输入时,此类材料伸展、压缩和/或振动。压电材料/元件的实例包括但不限于石英、块磷铝矿、黄玉、电气石、蔗糖、罗谢尔盐、钛酸钡和锆钛酸铅。
术语“无线通信”意指无线执行且递送的数据通信,并且包括通过无线通信技术和装置使用无线信号,在两个或更多个装置之间的连接和通信的所有程序和形式。术语无线通信包括但不限于卫星、移动、无线网络、红外和蓝牙通信。
现在转到特定实施方案,本文公开和请求保护的发明概念涉及用于减轻和/或消除微针阵列的生物淤积,从而改善生物传感器的性能和寿命的装置和方法。虽然本文主要在患者的间质液样品的背景下讨论患者的流体测试样品,但本领域普通技术人员应该容易理解,本文公开和/或请求保护的发明概念具有对所有类型的患者的流体样品的应用。另外,尽管本文描述的大多数实施方案涉及葡萄糖的检测和连续监测,但本领域普通技术人员应该容易理解,本文公开和/或请求保护的发明概念不仅限于葡萄糖检测,还可以用于可能存在于患者的流体样品中的任何数目或类型的分析物的检测和监测。更具体而言,本文公开和请求保护的发明概念涉及改善的留置、可穿戴生物的传感器以及与其相关的使用方法的实施方案,其减轻或消除生物淤积的效应。
考虑实际上在生物学、化学或生物化学分析和测定领域中使用的任何试剂都可以用于本文请求保护和公开的发明概念的装置和方法中,作为用于检测存在于患者的流体样品中的目标分析物的传感器。考虑这些试剂在与目标分析物结合时可以经历物理和/或化学变化,由此通过试剂-分析物复合物生成的信号的强度、颜色、性质、频率、荧光、波长或类型与患者的流体样品内存在的分析物浓度成正比或成反比。这些试剂可以含有或包含指示剂染料、金属、酶、荧光团、聚合物、抗体和电化学反应性成分和/或化学品,当与目标分析物反应时,其可以显示出颜色、荧光或波长中的变化。在一个实施方案中,试剂(其充当分析物传感器)包含荧光团和/或荧光染料,所述荧光团和/或荧光染料与每根微针的至少一个外表面上、每根微针内(包括但不限于,在每根微针的尖端部分内)、或者微针阵列的每根微针的外侧上和其内的聚合物材料结合。分析物传感器包含的荧光团和/或荧光染料可以与微针阵列的每根微针的外表面上或每根微针的尖端内的聚合物材料结合。此类荧光团和荧光染料包括但不限于荧光素、罗丹明、曙红、俄勒冈绿、德克萨斯红、香豆素衍生物、花青、靛羰花青、氧杂羰花青、硫杂羰花青、部花青、方酸衍生物、吡啶并噁唑、硝基苯并噁二唑、苯并噁二唑、蒽醌、芘衍生物、尼罗红、尼罗蓝、甲酚紫、噁嗪、原黄素、吖啶橙、吖啶黄、金胺、结晶紫、孔雀石绿、卟吩、酞菁、胆红素、硼酸酯及其组合。在一个非限制性实施方案中,试剂是硼酸酯荧光团。
本文公开和/或请求保护的发明概念可以检测与患者的流体样品相关的某些条件,包括但不限于样品的比重、浓度和/或ph。如本文所公开的,本文公开和/或请求保护的装置、试剂盒和方法可以用于分析患者的任何流体样品,包括但不限于全血、血浆、血清、尿或间质液。在一个非限制性实施方案中,患者的流体样品是间质液。
在一个实施方案中,分析物传感器至少包含荧光团,所述荧光团与形成微针阵列的微针的聚合物材料共价结合。当包含至少一种荧光团时,分析物传感器主要根据光诱导电子转移的原理起作用。在患者的流体样品中不存在目标分析物(例如,葡萄糖)的情况下,荧光团传感器的胺基的氮充当富电子中心,并且荧光团被猝灭。然而,在存在目标分析物(例如,葡萄糖)的情况下,分析物分子与荧光团传感器结合,从而抑制猝灭效应并导致荧光的发射,所述荧光的强度为与目标分析物的浓度成正比。如本文进一步讨论的,微针阵列可以另外包括至少一根校准针。与微针阵列包含的其它微针不同,包含至少一根校准微针的分析物传感器不被患者的流体样品中存在的至少一种分析物激活;相反,至少一根校准针的分析物传感器总是“开启”,连续且不断地发射信号(例如,当分析物传感器包括至少一种荧光团时,分析物传感器发射连续且恒定的荧光信号),其强度指示目标分析物的已知和/或预先计算的浓度。
现在参考附图,且更具体地参考图1,其中显示了本文公开和/或请求保护的改善的留置的可穿戴的生物传感器10的实施方案。生物传感器10包括微针阵列12、基底16和检测器18。
微针阵列12包括多根微针14a-14l。虽然在图1显示为包括十二(12)根微针,但本领域普通技术人员应该容易理解,微针阵列12可以包括实现本文公开和/或请求保护的发明概念的任何数目的微针。仅作为示例且非限制地,微针阵列12可以包括1、2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、150、200、250、300、350、400、450、500、550、600、650、700、750、800、850、900、950、1000或大于1000根微针。微针14a-14l可以由能够实现本文公开和/或请求保护的发明概念的任何材料构成。此类材料一般是热稳定、生物学和化学相容、安全、柔性、不吸湿、惰性和光学透明的。此类材料包括但不限于聚合物材料,例如,仅作为示例,聚丙烯酰胺、聚(甲基乙烯基醚-alt-马来酸酐)(pmve/ma)、麦芽糖、羧甲基纤维素、支链淀粉、透明质酸钠、硫酸软骨素/糊精、海藻酸钠、羟丙基纤维素、pmve/ma-聚(乙二醇)、聚乙烯醇(pva)、pva-糊精、聚(乳酸共乙醇酸)(plga)、聚乳酸、聚乙醇酸、聚碳酸酯、聚苯乙烯、聚二甲基硅氧烷(pdms)和/或其组合。在一个非限制性实施方案中,微针14a-14l由聚丙烯酰胺构成。
微针14a-14l的尺寸可以是相同的、不同的或其组合,条件是微针14a-14l能够刺穿并驻留在患者的表皮组织中,使得它们保持与患者的流体样品连续接触。通常,微针14a-14l具有以下尺寸为:(1)等于或小于150微米、或约300至约1,500微米、或约400至约1,400微米、或约500至约1,300微米、或约600至约1,200微米、或约700至约1,100微米、或约800至约1,000微米、或约900微米的长度;(2)约100至约500微米、或约200至约450微米、或约250至约400微米、或约300至约350微米的宽度;以及(3)约15至约100微米、或约25至约90微米、或约35至约80微米、或约45微米至约70微米、或约55至约60微米的厚度。另外并且如关于图2a和2b进一步讨论的,微针14a-14l的至少一部分(包括但不限于尖端部分)浸渍和/或包被(经由与形成每根微针14a-14l的聚合物材料结合)有至少一种抗伤口愈合化合物(如图3中所示),当微针14a-14l留置在患者的角质层或表皮组织内,并且与患者的流体样品接触时,所述抗伤口愈合化合物减轻和/或消除生物淤积。如关于图2a和2b进一步讨论的,微针阵列12的每根微针14a-14l含有和/或包被有至少一种荧光团传感器,所述传感器与形成微针阵列12的每根微针14a-14l的聚合物材料结合。相应地,在存在目标分析物(例如,葡萄糖)的情况下,荧光团传感器发射荧光信号,其指示患者的流体样品中的目标分析物的浓度和/或与其成正比。此类荧光信号由检测器18(在本文中更详细地讨论)接收,所述检测器18解释特定荧光信号,并且将其与患者的流体样品内存在的目标分析物的浓度相关联。
留置的可穿戴的生物传感器10还包括基底16,在一个非限制性实施方案中,所述基底16包括第一端26、第二端28、第一侧30、第二侧32、顶部部分34和底部部分36。虽然在图1中显示为在形状中基本上是矩形,但本领域普通技术人员应该容易理解,基底16可以是有助于实现本文公开和/或请求保护的发明概念的任何形状。此类形状包括但不限于圆形、三角形、正方形、菱形、五边形、六边形、七边形、八边形、九边形、十边形、斜方形、梯形、斜方形和平行四边形。
基底16优选地由耐用、柔性、超薄、轻质、可拉伸的“皮肤状”膜构成,其经由柔软接触顺应地粘附和/或层压到患者皮肤的表面上—类似于众所周知的胶粘绷带和/或透皮贴剂的那种。在一个实施方案中,基底16的底部部分36包括用于将生物传感器10固定到患者的皮肤的粘合材料(未示出)。可选地,生物传感器10可以仅经由基底16和患者皮肤之间的范德华相互作用粘附并固定到患者的皮肤;然而,本领域普通技术人员应该容易理解,基底16可以经由本领域通常已知的任何方式固定到患者的皮肤。此类耐用的柔性材料可以包括但不限于织造织物,塑料例如聚氯乙烯(pvc)、聚乙烯和/或聚氨酯,聚(二甲基硅氧烷)(pdms)或胶乳,和/或其组合。此类粘合材料可以包括但不限于丙烯酸酯物质,包括但不限于甲基丙烯酸酯和环氧二丙烯酸酯/乙烯基树脂和/或其组合。优选地,基底16是胶带或薄膜,其中粘合剂(未示出)将微针阵列12的微针14a-14l牢固地固定在沿着基底16的底部部分36的位置中。相应地,当此类微针14a-14l留置在患者的角质层或表皮组织内时,微针阵列12的每根微针14a-14l保持牢固地和/或永久地固定到或穿过基底16的底部部分36。用于固定微针阵列12的微针14a-14l的这种此类和方式是本领域通常已知的。虽然在图1中显示为沿着基底16的底部部分36均匀间隔开,但本领域普通技术人员应该容易理解,微针14a-14l可以以能够实现本文公开和/或请求保护的发明概念的任何配置定位。例如,微针14a-14l(或如本文所考虑的更多或更少的微针)可以在基底16的底部部分36上或穿过基底16的底部部分36随机地或以任何预定的配置定位。
留置的可穿戴的生物传感器10进一步包括检测器18,其接收由荧光团传感器(如图2a和2b中更详细地示出)发射的荧光信号,所述荧光团传感器包含在微针阵列12的每根微针14a-14l内和/或包被到其上。相应地,在一个实施方案中,检测器18包括荧光计,包括但不限于微荧光计、滤波荧光计或分光荧光计。如图1中所示,在一个非限制性实施方案中,检测器18位于(并且在一个实施方案中,可以永久地附接到)基底16的顶部部分34;然而,本领域普通技术人员应该理解,检测器18可以位于基底16的任何部分上,统计上检测器18能够接收由荧光团传感器(在图2a和2b中更详细地示出)发射的荧光信号,所述荧光团传感器包含在微针阵列12的每根微针14a-14l内和/或包被到其上。
如下文更具体地讨论的(并且如图5中所示),检测器18包括电路(包括但不限于控制器、微处理器、存储器和/或接口),其允许检测器18:(a)基于由分析物传感器接收的信号来关联并计算至少一种目标分析物的浓度;并且(b)与至少一个外部装置无线通信,使得由检测器18收集的数据(包括但不限于荧光和计算的浓度)可以与此类至少一个外部装置无线通信。此后,基于此类数据在此类至少一个外部装置上的展示,用户(包括但不限于医生、护士或负责对患者施用护理的人员(包括患者他/她自己)可以解释、监测且开发用于治疗患者的有效治疗计划。
生物传感器10被配置成使得微针阵列12和检测器18经由与基底16的连接或通过基底16连接而彼此邻近地定位。由于这种紧密接近,通过检测器18接收的来自荧光团传感器(在图2a和2b中更详细地示出)的荧光信号损失被减轻、最小化和/或消除,所述荧光团传感器包含在微针阵列12的每根微针14a-14l内和/或包被到其上—从而导致患者的流体样品内包含的目标分析物的浓度的更准确检测。
现在参考图1a,其中示出了图1的留置的可穿戴的生物传感器10的非限制性的另外实施方案,其中生物传感器10的微针阵列12进一步包括多根校准微针15a-15c。虽然在图1a中显示为包括三根校准微针15a-15c,但本领域普通技术人员应该容易理解,微针阵列12可以包括任何数目的校准微针(包括但不限于单根校准微针),并且此类校准微针可以以实现本文公开和/或请求保护的发明概念的任何配置进行定向。出于简化的目的,本文不重复生物传感器10的描述,因为与关于图1和图1a描述的实施方案的唯一差异是多根校准微针15a-15c的包含和功能。
与微针14a-14l类似地构成且构造多根校准微针15a-15c,其中每根校准微针15a-15c包括荧光团传感器(未示出,但其与形成校准微针15a-15c的聚合物材料结合),其发射指示至少目标分析物(例如,仅作为示例,葡萄糖)的浓度的荧光信号,所述目标分析物可以存在于患者的流体样品中。然而,校准针15a-15c的荧光团传感器总是活跃的(即,它们不是通过目标分析物与荧光团传感器的结合而分开激活的),并且因而,不断地发射可以由检测器18接收的荧光信号。由校准微针15a-15c的荧光团传感器发射的恒定荧光信号可以被预校准和/或预选择,以发射以指示目标分析物的已知浓度的强度的荧光信号。对于校准微针15a-15c的每个荧光团传感器,此类强度(以及相应地,已知浓度)可以是相同的、不同的、或相同和不同的组合。相应地,通过将此类荧光信号与由校准微针15a-15c的荧光团传感器发射的恒定荧光信号进行比较,通过检测器18可以精确地计算由微针14a-14l主动传感的目标分析物(例如,葡萄糖)的浓度。另外,校准微针15a-15c可以进一步用于检测微针14a-14l的生物淤积是否正在发生,因为检测器18能够检测与由校准针15a-15c的荧光团传感器发射的恒定荧光信号相比,由微针14a-14l的荧光团传感器发射的荧光信号中的变化。如果检测到生物淤积,则可以根据本文公开和/或请求保护的发明概念并如本文所述实现适当的补救。
现在参考图2a和2b,其中显示了本文公开和/或请求保护的发明概念的改善微针14a的实施方案。虽然如上文讨论的,图2a和2b显示了单根微针14a,但本领域普通技术人员应该容易理解,微针阵列12可以包括实现本文公开和/或请求保护的发明概念的任何数目的微针。然而,出于说明和简化的目的,图2a和2b中仅示出了一根微针14a。关于微针14a的下述描述同样适用于微针阵列12包括的任何和所有微针,包括例如微针14a-14l。
现在参考图2a,微针14a包括基部部分22、尖端部分24、从基部部分22到尖端部分24延伸微针14a的长度的孔23、以及在尖端部分24的孔23的远端处的开口25。虽然微针14a在图2a(以及图2b、3和4)中描述为包括开口25,但本领域普通技术人员应该容易理解,本文公开和/或请求保护的发明概念并不限于该实施方案。例如,在一个非限制性实施方案中,微针14a可以由多孔水凝胶(包括但不限于聚丙烯酰胺)形成。在该实施方案中,开口25不是必需的,因为患者的流体样品能够通过多孔水凝胶形成微针14a并在其中扩散,由此在患者的流体样品内包含的至少一种目标分析物与和微针14a结合和/或聚合和/或浸渍在微针14a中的至少一种分析物传感器结合。
如图2a中所示并且如本文所讨论的,微针14a的基部部分22牢固地固定到基底16的底部部分36。在一个实施方案中,微针14a的基部部分22固定到基底16的底部部分36可以经由本领域通常已知的任何机制实现,包括但不限于经由粘合剂或在生物传感器10的制造过程期间的无缝集成。在可选的非限制性实施方案中,微针14a经由直接集成在检测器18中或附接到检测器18(即,通过基底16)牢固地固定,使得荧光团传感器响应患者的流体样品中目标分析物的检测而生成且发射荧光信号通过孔23直接传输到检测器18(从而减轻信号损失)。在另一个可选的非限制性实施方案中,基底16包括在基底16各处的预先形成的开口(未示出)。微针14a(以及微针阵列12包括的任何和所有微针)可以通过基底16浇铸,使得形成微针14a的材料的一部分存在于基底的顶部部分34上,从而形成用于将微针14a固定在基底16中并穿过基底16的固定边缘。在该实施方案中,微针14a围绕铸件(未示出)形成,其中所述铸件可以是有助于形成微针14a(以及微针阵列12的任何和所有微针)的任何结构和形状。在一个非限制性实施方案中,铸件可以是至少一根线或惰性杆,其可以在微针14a形成之后从微针14a中去除,包括但不限于在微针14a形成后,经由从微针14a和基底16中拉动铸件。
现在参考图2b,其中显示了图2a中描绘的微针14a的尖端部分24的详细视图。微针14a的尖端部分24包括多个分析物传感器20a-20e,其与构成微针14a的聚合物材料结合。由于分析物传感器20a-20e与此类聚合物材料结合,分析物传感器20a-20e可以在微针14a的尖端部分24内结合(例如,如图2b中所示,在微针14a的尖端部分24的至少一个内表面24a上),或者可选地(或另外),在微针14a的尖端部分24的至少外表面24b上。在可选的非限制性实施方案中,分析物传感器20a-20e可以分开包括在用于构建微针14a的聚合物材料中,使得在微针14a聚合时,分析物传感器20a-20e配置在形成微针14a的聚合物材料内。相应地,在该实施方案中,分析物传感器20a-20e配置在微针14a的整个结构内,并且不仅限于微针14a的尖端部分24。虽然图2b中描绘了五个分析物传感器20a-20e,但本领域普通技术人员应容易理解,任何数目标分析物传感器可以用于实现本文公开和/或请求保护的发明概念。如先前在上文所讨论的,当此类分析物传感器包含至少一种荧光团时,此类至少一种荧光团传感器和/或荧光染料包括但不限于荧光素、罗丹明、曙红、俄勒冈绿、德克萨斯红、香豆素衍生物、花青、靛羰花青、氧杂羰花青、硫杂羰花青、部花青、方酸衍生物、吡啶并噁唑、硝基苯并噁二唑、苯并噁二唑、蒽醌、芘衍生物、尼罗红、尼罗蓝、甲酚紫、噁嗪、原黄素、吖啶橙、吖啶黄、金胺、结晶紫、孔雀石绿、卟吩、酞菁、胆红素和硼酸酯。在一个非限制性实施方案中,至少一个分析物传感器包含硼酸酯荧光团。
虽然荧光团传感器20a-20e可以适于检测可能存在于患者的流体样品中的任何目标分析物,但出于说明的目的,分析物传感器20a-20e在下文关于患者的流体样品中葡萄糖的检测进行描述。在一个非限制性实施方案中,分析物传感器20a-20e包含由报告荧光团和单体缀合位点的葡萄糖受体组成的分子。在该实施方案中,整个分析物传感器20a-20e与形成微针14a,并且更具体而言,如图2b中所示,微针14a的尖端部分24的至少一个内部部分24a的聚合物材料结合。当包含至少一种荧光团时,分析物传感器20a-20e基于诱导电子转移的原理进行操作。例如,在不存在葡萄糖的情况下,包含分析物传感器20a-20e的受体的胺基的氮充当富电子中心,从而经由来自受体的电子转移使荧光团猝灭。然而,在葡萄糖的存在下,葡萄糖分子与葡萄糖受体结合,并且葡萄糖受体的氧化还原状态改变。因此,抑制了荧光团经由电子转移的猝灭,导致来自荧光团的荧光的发射,所述荧光的强度与葡萄糖(或待监测的特定分析物)的浓度成正比。在该实施方案中,由分析物传感器20a-20e的荧光团发射的荧光通过形成微针14a的光学透明聚合物材料(例如,通过聚合物材料本身或通过孔23向上)传播,在其中它由检测器18接收。在可选的非限制性实施方案中,微针14a的至少一部分可以包括至少一种反射包覆材料,至少一种反射包覆材料促进由分析物传感器20a-20e发射的信号(例如,当分析物传感器包含至少一种荧光团时,荧光信号)通过微针14a的孔23传播到检测器18。在一个非限制性实施方案中,至少一种反射包覆材料包含金属银,所述金属银经由将微针14a浸入含有所述金属的溶液中、或经由将金属银喷射到微针14a的至少一部分上,而施加到微针14a的至少一部分。基于由分析物传感器20a-20e接收的荧光信号的强度,检测器18随后关联并计算患者的流体样品中存在的葡萄糖的浓度。随后,并且如关于图5进一步讨论的,检测器将相关联的荧光/浓度信息无线通信到至少一个外部装置,用于展示和进一步分析。此后,基于此类数据在此类外部装置上的展示,用户(包括但不限于医生、护士或负责对患者施用护理的人员(包括患者他/她自己)可以解释、监测且开发用于治疗患者的有效治疗计划。检测器18可以被编程为以预定间隔(例如,仅作为示例,每1、2或5分钟)接收来自分析物传感器20a-20e的荧光信号,或可选地,检测器可以连续接收此类荧光信号。相应地,检测器18可以以预定间隔或连续地关联并计算荧光/浓度数据和/或无线通信此类数据。
分析物传感器20a-20e对于葡萄糖的亲和力足够低以允许动态传感,并且当葡萄糖是待监测的分析物时,它/它们对于d-葡萄糖具有的结合亲和力超过其它碳水化合物。此类结合亲和力足够强,以检测患者的流体样品中存在的低水平葡萄糖,尤其是当此类患者的流体样品是间质液时。
现在参考图3,其中显示了本文公开和/或请求保护的发明概念的一个非限制性实施方案,其中微针14a的尖端部分24包被有抗伤口愈合化合物,以预防、减轻和/或消除生物淤积过程。仅出于简化的目的,抗伤口愈合化合物的非限制性实例在图3中描述为不同的参考数字35a、35b、35c和35d。然而,本领域普通技术人员应该容易理解,任何数目或组合的抗伤口愈合化合物都可以用于实现本文公开和/或请求保护的发明概念的目的。此外,本文公开和/或请求保护的发明概念的抗伤口愈合化合物,包括抗伤口愈合化合物35a-35d,可以包含相同、不同、或相同和不同化合物、药物和/或组合物的组合。另外,虽然图3中仅描绘了微针14a的尖端部分24,但本领域普通技术人员应该容易理解,关于抗伤口愈合化合物的下述描述同样适用于留置的可穿戴的生物传感器的微针阵列12包含的每根微针。另外,尽管图3将抗伤口愈合化合物35a-35d描绘为基本上位于微针14a的尖端部分24上和其中,但本领域普通技术人员应该容易理解,抗伤口愈合化合物35a-35d(以及本文公开和/或请求保护的发明概念的任何抗伤口愈合化合物)可以位于微针14a的任何部分中和/或其上,包括但不限于,微针14a的整个长度中和/或其上。
当微针14a留置在患者的表皮组织内时,由于患者的身体将微针14a(以及微针阵列12的任何和所有微针)感知为外来物,触发伤口愈合过程。因此,触发生物应答(例如伤口愈合级联),其导致细胞、蛋白质和/或其它生物物质结合和/或阻塞微针14a(尤其是尖端部分24a),从而损害、危害和/或破坏留置的可穿戴的生物传感器10的功能—一种称为生物淤积的过程。
在一个实施方案中,如图3中所示,通过将至少一种抗伤口愈合化合物35a-35d结合到微针14a的尖端部分24的至少一个内表面24a和至少一个外表面24b上,可以预防、减轻和/或消除生物淤积的效应。虽然在图3中显示为仅与尖端部分24的内表面24a和外表面24b结合,但本领域普通技术人员应该容易理解,抗伤口愈合化合物35a-35d可与微针14a的任何表面结合,并且不仅限于尖端部分24。至少一种抗伤口愈合化合物35a-35d可以经由本领域通常已知的任何方法与微针14a的表面结合,所述方法包括但不限于经由浸没、浸入和/或喷涂,将至少一种抗伤口愈合化合物35a-35d施加到微针14a的尖端部分24(和/或微针14a的任何部分或整体)。在另外的实施方案中,至少一种抗伤口愈合化合物35a-35d可以分别混合到用于形成微针14a的聚合物材料(或微针阵列12包含的任何和/或所有微针)内,使得抗伤口愈合化合物浸渍在形成微针14a的聚合物材料内。在一个实施方案中,至少一种抗伤口愈合化合物35a-35d可以包含时间释放制剂,由此当与患者的流体样品接触时,所述抗伤口愈合化合物以预定间隔释放。
在插入患者的表皮组织内之后,微针14a与患者的流体样品例如患者的间质液(未示出)接触。患者的流体样品(未示出)与微针14a的外表面24b和微针14a的内表面24a两者接触(经由通过开口25流入微针14a的孔23内的流体样品,或者,如上文所讨论的,当微针14a由多孔聚合物水凝胶形成时,经由通过孔扩散到微针14a的孔23内)。一旦微针14a(以及微针阵列12包括的其它微针)插入患者的表皮组织内,微针14a就被患者的流体样品(例如患者的间质液)水合。与患者的流体样品的这种水合允许经由分析物与分析物传感器20a-20e的结合实时检测患者的流体样品中存在的目标分析物(例如,葡萄糖)、以及抗伤口愈合化合物35a-35d的释放两者,所述抗伤口愈合化合物预防、减轻和/或消除如本文所讨论的生物淤积过程。
现在参考图4,其中显示了本文公开和/或请求保护的发明概念的改善的留置的可穿戴的生物传感器10的一个非限制性实施方案,其中生物传感器10留置在患者的表皮组织38内,并且与患者的流体样品和流体连通。在该非限制性实施方案中,留置的可穿戴的生物传感器10包括:微针阵列12,其包括多根微针14a、14c、14e、14g、14i、14k(为了简单起见,统称为微针14);基底16,其包括第一端26、第二端28、第一侧30、第二侧32(未示出)、顶部部分34和底部部分36;以及检测器18。每根微针14包括多个分析物传感器20a、20c、20e、20g、20i和20k(为了简单起见,统称为分析物传感器20),以及与形成微针14的聚合物材料结合的至少一种抗伤口愈合化合物35a、35c、35e、35g、35i和35k(为了简单起见,统称为至少一种抗伤口愈合化合物35)。
生物传感器10经由压力,包括但不限于经由施加到基底16的顶表面34的压力,施加到患者的表皮组织38,并且在一个非限制性实施方案中,经由基底16的底表面上存在的粘合剂保持在适当的位置。一旦施加,微针阵列12就刺穿患者的表皮组织38,从而使多根微针14与患者的流体样品40流体连通,在一个非限制性的实施方案中,所述患者的流体样品40是患者的间质液。患者的流体样品40水合包括外表面和内表面两者的多根微针14(经由患者的流体样品40扩散通过开口并进入多根微针14包括的每根微针的孔内))。作为这种水合的结果,释放多种抗伤口愈合化合物35,其从而预防、减轻和/或消除生物淤积过程(例如,仅作为示例,通过抑制或减轻伤口愈合过程的炎症阶段和/或预防细胞42、蛋白质和/或其它生物物质在多根微针14的每根微针周围和/或其内的累积和附聚)。另外,水合导致患者的流体样品40扩散到多根微针14的每根微针内。如果患者的流体样品40含有目标分析物(例如,葡萄糖)(未示出),则目标分析物与多个分析物传感器20结合,由此,当多个分析物传感器20包含至少一种荧光团时,多个分析物传感器20发射荧光信号,其随后由检测器18检测(例如,通过向上移动或穿过多根微针14的每根光学透明微针的长度)。然后,基于从多个分析物传感器20接收的荧光信号的强度,检测器18关联并计算浓度。一旦关联并计算,检测器18(经由内部电路(未示出))将关联并计算的数据无线传输到至少一个外部装置,包括但不限于计算机监视器和移动装置,例如笔记本电脑、平板电脑和/或便携式电话(未示出)。然后,外部装置显示关联并计算的数据,使得基于此类数据在此类外部装置上的展示,用户可以解释、监测且开发用于患者的有效治疗计划。
现在参考图5,其中显示了本文公开和/或请求保护的发明概念的另外实施方案,其中压电元件44a-44l掺入微针阵列12的每根微针14a-14l内。
另外,图5示出了从检测器18的控制器46到至少一个外部装置48的关联并计算的数据的无线通信和传输,所述外部装置48包括但不限于笔记本电脑、便携式电话、平板电脑和计算机/计算机监视器。该数据的传输适用于本文公开和/或请求保护的发明概念的任何和所有实施方案。例如,在检测器基于从先前讨论的分析物传感器接收的信号(例如,荧光信号)关联并计算患者的流体样品中存在的目标分析物的浓度之后,然后将该数据无线传输到至少一个外部装置48。
在一个非限制性实施方案中,微针阵列12的每根微针14a-14l包括至少一个压电元件44a-44l。至少一个压电元件44a-44l检测微针阵列12的每根微针14a-14l内的压力变化和/或差异(例如,由于起因于本文讨论的生物淤积过程的细胞、蛋白质和/或其它生物物质(未显示)的累积或附聚,起因于微针阵列12各自的阻塞或部分阻塞的压力变化和/或差异)。在检测到压力变化和/或差异(由图5中的δp表示)时,电信号被发送到检测器18,在其中它由控制器46接收。在接收到指示与微针14a-14l中的任何或全部相关的压力变化和/或差异的电信号之后,控制器46随后将电信号(由图5中的e表示)递送到微针阵列12的每根微针14a-14l,所述电信号由至少一个压电元件44a-44l接收。响应电信号的接收,至少一个压电元件44a-44l振动,所述振动由此移除并去除(由于生物淤积已累积或附聚在微针阵列12的每根微针14a-14l上或其内的)任何细胞、蛋白质和/或其它生物物质。
虽然图5描绘了微针阵列12的每根微针的单个压电元件,但本领域普通技术人员应该容易理解,每根微针可以包括多于一个压电元件,或者可选地,仅某些微针14a-14l可以包括压电元件。压电元件44a-44l可以是相同组成、不同组成、或相同和不同组成的组合。另外,不是响应指示压力变化和/或差异的接收信号发送电信号,而是可以将检测器18的控制器46编程或预编程,以将一种或多种电信号递送至以规则的预定间隔的一个、一些或所有压电元件44a-44l,从而连续地预防细胞、蛋白质和/或其它生物物质在微针阵列12的一根、一些或所有微针14a-14l上或其内的累积和/或附聚。
在可选的非限制性实施方案中,生物传感器10可以包括至少一个压电元件,其配置在基底16的顶部部分34上。在该实施方案中,检测器18(经由控制器46)能够将电信号递送到至少一个压电元件,从而导致至少一个压电元件的振动。由至少一个压电元件生成的振动信号随后由一根、一些或所有微针14a-14l(仅作为示例,经由存在于基底16的顶部部分34上的微针14a-14l的边缘部分,其将微针14a-14l固定到基底16)接收,从而预防、减轻和/或消除细胞、蛋白质和/或生物物质在微针阵列12的一根、一些或所有微针14a-14l上或其内的累积和/或附聚。
发明概念的非限制性实施例
用于连续检测和监测患者的流体样品中的至少一种分析物的留置的可穿戴的生物传感器装置,所述装置包括:微针阵列,所述微针阵列包括由至少一种聚合物材料构成的多根微针,其中所述多根微针嵌入患者的表皮组织中,使得所述多根微针与患者的流体样品连续接触,并且进一步地,其中所述多根微针中的每根微针的至少一个表面包含至少一种抗伤口愈合化合物,当微针阵列嵌入患者的表皮组织中时,所述抗伤口愈合化合物抑制伤口愈合过程;与多根微针中的每根微针的聚合物材料可操作地结合的多个分析物传感器,所述多个分析物传感器生成指示患者的流体样品中存在的至少一种分析物的浓度的信号;具有顶部部分和底部部分的基底,其中微针阵列永久地附接到基底的底部部分;以及检测器,其中所述检测器包括用于接收由多个分析物传感器生成的信号的电路,计算患者的流体样品中存在的至少一种分析物的浓度,并且将浓度传输到外部装置用于诊断和评估所提出的治疗。
生物传感器装置,其中所述聚合物材料是聚丙烯酰胺。
生物传感器装置,其中所述流体样品选自间质液和血液。
生物传感器装置,其中所述基底的底部部分包括用于将基底固定到患者的表皮组织的粘合剂。
生物传感器装置,其中所述检测器选自微荧光计、滤波荧光计或分光荧光计。
生物传感器装置,其中所述多个分析物传感器包含至少一种荧光团,其中所述至少一种荧光团选自荧光素、罗丹明、曙红、俄勒冈绿、德克萨斯红、香豆素衍生物、花青、靛羰花青、氧杂羰花青、硫杂羰花青、部花青、方酸衍生物、吡啶并噁唑、硝基苯并噁二唑、苯并噁二唑、蒽醌、芘衍生物、尼罗红、尼罗蓝、甲酚紫、噁嗪、原黄素、吖啶橙、吖啶黄、金胺、结晶紫、孔雀石绿、卟啉、酞菁、胆红素、硼酸酯及其组合。
生物传感器装置,其中存在于患者的流体样品中的至少一种分析物是葡萄糖。
生物传感器装置,其中所述至少抗伤口愈合化合物选自免疫抑制化合物、皮质类固醇、壳聚糖、非甾体抗炎药、阿司匹林、萘普生、布洛芬、抗凝化合物及其组合。
用于连续检测和监测患者的流体样品中的至少一种分析物的留置的可穿戴的生物传感器装置,所述装置包括:微针阵列,所述微针阵列包括由至少一种聚合物材料构成的多根微针,其中所述多根微针嵌入患者的表皮组织中,使得所述多根微针与患者的流体样品连续接触,并且进一步地,其中所述多根微针中的至少一根微针包括至少一个压电元件;具有顶部部分和底部部分的基底,其中微针阵列永久地附接到基底的底部部分;以及检测器,其中所述检测器包括用于接收由至少一个压电元件生成的信号的电路,计算患者的流体样品中存在的至少一种分析物的浓度,并且将浓度传输到外部装置用于诊断和评估所提出的治疗,进一步地,其中所述检测器接收由至少一个压电元件生成的第一电信号,并且将第二电信号递送到至少一个压电元件,导致至少一个压电元件的振动。
生物传感器装置,其中所述聚合物材料是聚丙烯酰胺。
生物传感器装置,其中所述流体样品选自间质液和血液。
生物传感器装置,其中所述至少一个压电元件选自石英、块磷铝矿、黄玉、电气石、蔗糖、罗谢尔盐、钛酸钡和锆钛酸铅。
生物传感器装置,其中所述基底的底部部分包括用于将基底固定到患者的表皮组织的粘合剂。
生物传感器装置,其中存在于患者的流体样品中的至少一种分析物是葡萄糖。
用于连续检测和监测患者的流体样品中的至少一种分析物的留置的可穿戴的生物传感器装置,所述装置包括:微针阵列,所述微针阵列包括由聚合物材料构成的多根微针,所述多根微针包括至少一根校准微针,其中所述多根微针嵌入患者的表皮组织中,使得所述多根微针与患者的流体样品连续接触;与多根微针中的每根微针的聚合物材料可操作地结合的多个分析物传感器,所述多个分析物传感器在至少一种分析物的存在下生成信号,所述信号指示患者的流体样品中存在的至少一种分析物的浓度,并且进一步地,其中与至少一根校准针的聚合物材料可操作地结合的多个分析物传感器在暴露于患者的流体样品时发射恒定信号;具有顶部部分和底部部分的基底,其中微针阵列永久地附接到基底的底部部分;以及检测器,其中所述检测器包括用于接收由多个分析物传感器生成的信号的电路,计算患者的流体样品中存在的至少一种分析物的浓度,并且将浓度传输到外部装置用于诊断和评估所提出的治疗。
生物传感器装置,其中所述聚合物材料是聚丙烯酰胺。
生物传感器装置,其中所述流体样品选自间质液和血液。
生物传感器装置,其中所述基底的底部部分包括用于将基底固定到患者的表皮组织的粘合剂。
生物传感器装置,其中所述检测器选自微荧光计、滤波荧光计或分光荧光计。
生物传感器装置,其中所述多个分析物传感器包含至少一种荧光团,其中所述至少一种荧光团选自荧光素、罗丹明、曙红、俄勒冈绿、德克萨斯红、香豆素衍生物、花青、靛羰花青、氧杂羰花青、硫杂羰花青、部花青、方酸衍生物、吡啶并噁唑、硝基苯并噁二唑、苯并噁二唑、蒽醌、芘衍生物、尼罗红、尼罗蓝、甲酚紫、噁嗪、原黄素、吖啶橙、吖啶黄、金胺、结晶紫、孔雀石绿、卟啉、酞菁、胆红素、硼酸酯及其组合。
生物传感器装置,其中存在于患者的流体样品中的至少一种分析物是葡萄糖。
因此,根据本文公开和请求保护的发明概念,已提供了改善的留置的可穿戴的生物传感器的装置和方法,其预防、减轻和/或消除生物传感器(以及用于校准生物传感器的装置和与其相关的方法)的生物淤积效应。如本文所述,本文公开和请求保护的发明概念涉及改善的、留置的可穿戴的生物传感器,与其相关的使用方法,用于预防、减轻和/或消除生物淤积对生物传感器的效应的装置和方法,以及与生物传感器的校准有关的装置和方法的实施方案。此类本文公开和/或请求保护的发明概念完全满足上文阐述的目的和优点。尽管已结合上文阐述的具体附图、实验、结果和语言描述了本文公开和请求保护的发明概念,但很明显,许多可选物、修改和变化对于本领域技术人员是显而易见的。相应地,预期涵盖落入本文公开和请求保护的发明概念的精神和广泛范围内的所有此类可选方案、修改和变化。
- 还没有人留言评论。精彩留言会获得点赞!