用于治疗骨髓纤维化的方法和组合物与流程
本申请请求保护2016年7月27日提交的美国临时申请序列号62/367,289的优先权权益。前述申请的公开内容通过引用以其整体由此并入。
发明背景
骨髓纤维化是主要影响老年人的罕见的疾病。骨髓纤维化是bcr-abl1阴性骨髓增生性肿瘤,其从头呈现(原发性)或可能之前是真性红细胞增多症(真性红细胞增多症后)或特发性血小板增多症(特发性血小板增多症后)。临床特征包括进行性贫血、明显的脾肿大、纤维化(例如,骨髓纤维化)、全身症状(例如,疲劳、盗汗、骨痛、瘙痒和咳嗽)和体重减轻[tefferia(2000)nengljmed342:1255-1265]。根据目前鉴定的预后因素,存活中位数从小于2年到超过15年变化。已经在具有骨髓纤维化的患者中描述了牵涉jak2、mpl、tet2、asxl1、idh1/idh2、cbl、ikzf1、lnk和ezh2的突变[jamesc等(2005)nature434:1144-1148,2005;scottlm等(2007)nengljmed356:459-468,2007;pikmany等(2006)plosmed3:e270;delhommeauf等(2009)nengljmed360:2289-2301;carbuccian等(2009)leukemia23:2183-2186;greena等(2010)nengljmed362:369-370;tefferia等(2010)leukemia24:1302-1309;grandfh等(2009)blood113:6182-6192;jagerr等(2010)leukemia24:1290-1298;ohst等(2010)blood116:988-992;和ernstt等,natgenet.42:722-726]。一些突变在骨髓纤维化中以高频率发生(例如,约50%患者中的jak2突变),并且直接(例如jak2或mpl突变)或间接(例如lnk或cbl突变)诱导jak-stat超活化。
骨髓纤维化的唯一疗法是骨髓移植。然而,治疗相关的死亡率高,并且只有少数患者有资格进行移植。许多其它目前可用的治疗在逆转骨髓纤维化的过程中不是有效的,无论是原发性疾病还是继发性疾病。骨髓纤维化治疗包括例如细胞还原疗法(例如,用羟基脲治疗);用雄激素和/或促红细胞生成素治疗贫血;和脾切除术。这些疗法尚未证明存活中的改善,并且在很大程度上被视为姑息性的[cervantesf.,myelofibrosis:biologyandtreatmentoptions,europeanjournalofhaematology,2007,79(suppl.68)13-17]。更近来,jak抑制剂已用于治疗骨髓纤维化。jak抑制剂似乎可用于减少骨髓纤维化患者中的脾肿大,但它们对疾病的影响在很大程度上是另外地姑息性的[gupta等(2012)blood120:1367-1379]。特别地,jak抑制剂对疾病的许多表现(并发症)有很少至没有影响,所述表现包括例如血细胞减少症、输血依赖性、加速或急变期(blastphase)疾病和纤维化。此外,jak抑制剂已显示在一些患者中引起或恶化血小板减少症、贫血和中性粒细胞减少症。
因此,对于治疗骨髓纤维化的有效疗法存在高度未满足的需求。因此,本公开内容的一个目的是提供用于治疗或预防骨髓纤维化、特别是治疗或预防骨髓纤维化的一种或多种并发症的方法。
发明概述
部分地,本公开内容涉及以下发现:actriib拮抗剂(抑制剂)可以用于治疗骨髓纤维化,特别是改善疾病的各种并发症,所述并发症包括例如脾肿大、髓外造血和纤维化。特别地,本文呈现的数据显示,gdf捕获物多肽减少骨髓纤维化的jak2v617f模型中的脾肿大、髓外造血和纤维化。因此,在某些方面,本公开内容涉及用于治疗骨髓纤维化、特别是治疗或预防骨髓纤维化的一种或多种并发症(例如,脾肿大、髓外造血、贫血和纤维化)的组合物和方法,其通过向有需要的患者施用有效量的一种或多种actriib拮抗剂、任选地与用于治疗骨髓纤维化的一种或多种其它支持疗法或活性剂组合实施。虽然gdf捕获物多肽可通过actriib拮抗作用之外的机理影响骨髓纤维化[例如,gdf11、gdf8、激活蛋白b、bmp6、gdf3和bmp10中的一种或多种的抑制可能是药剂抑制一系列其它因子、包括可能tgf-β超家族的其它成员的活性的趋势的指示剂,以及这种集体抑制可能导致对例如骨髓纤维化的期望效应],但本公开内容证明可基于actriib拮抗作用选择希望的治疗剂。因此,虽然不希望受限于特定的作用机制,但预期其它actriib拮抗剂[例如,actriib受体的拮抗剂,一种或多种actriib配体(例如,gdf11、gdf8、激活蛋白b、bmp6、gdf3和bmp10)的拮抗剂,一种或多种i型受体(例如,alk4、alk5和/或alk7)的拮抗剂,一种或多种共同受体的拮抗剂,和/或一种或多种actriib下游信号传导组分(例如,smads)的拮抗剂]或这些拮抗剂的组合]将用于治疗骨髓纤维化,特别是用于治疗或预防一种或多种骨髓纤维化并发症(例如,脾肿大、髓外造血、贫血和纤维化)。这些药剂在本文中统称为“actriib拮抗剂”或“actriib抑制剂”。
因此,在某些方面,本公开内容涉及用于治疗骨髓纤维化的方法,其包括向有需要的患者施用有效量的actriib拮抗剂。在一些实施方案中,本公开内容涉及用于治疗骨髓纤维化的一种或多种并发症的方法,其包括向有需要的患者施用有效量的actriib拮抗剂。在某些方面,本公开内容涉及预防骨髓纤维化的方法,其包括向有需要的患者施用有效量的actriib拮抗剂。在一些实施方案中,本公开内容涉及预防骨髓纤维化的一种或多种并发症的方法,其包括向有需要的患者施用有效量的actriib拮抗剂。在某些方面,本公开内容涉及降低骨髓纤维化的进展速率,其包括向有需要的患者施用有效量的actriib拮抗剂。在一些实施方案中,本公开内容涉及降低骨髓纤维化的一种或多种并发症的进展速率,其包括向有需要的患者施用有效量的actriib拮抗剂。在某些方面,本公开内容涉及降低骨髓纤维化的严重性的方法,其包括向有需要的患者施用有效量的actriib拮抗剂。在一些实施方案中,本公开内容涉及降低骨髓纤维化的一种或多种并发症的严重性方法,其包括向有需要的患者施用有效量的actriib拮抗剂。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中所述患者具有原发性骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中所述患者具有真性红细胞增多症后骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中所述患者具有特发性血小板增多症后骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据国际预后评分系统(internationalprognosticscoringsystem,ipss),所述患者具有低风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据ipss,所述患者具有中等-1风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据ipss,所述患者具有中等-2风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据ipss,所述患者具有高-风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据动态ipss(dipss),所述患者具有低风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据dipss,所述患者具有中等-1风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据dipss,所述患者具有中等-2风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据dipss,所述患者具有高-风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据dipss-plus,所述患者具有低风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据dipss-plus,所述患者具有中等-1风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据dipss-plus,所述患者具有中等-2风险骨髓纤维化。在某些方面,本公开内容涉及治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中根据dipss-plus,所述患者具有高-风险骨髓纤维化。在某些方面,根据用于骨髓纤维化的任何公认的风险分层模型(例如,ipss、dipps和dipss-plus),actriib拮抗剂可用于预防或延迟骨髓纤维化的风险进展。例如,在一些实施方案中,根据ipss、dipps或dipss-plus,actriib拮抗剂可用于预防或延迟从低风险至中等-1风险的骨髓纤维化风险进展。在其它实施方案中,根据ipss、dipps或dipss-plus,actriib拮抗剂可用于预防或延迟从中等-1风险至中等-2风险的骨髓纤维化风险进展。在更其它实施方案中,根据ipss、dipps或dipss-plus,actriib拮抗剂可用于预防或延迟从中度-2风险至高风险的骨髓纤维化风险进展。在某些方面,根据用于骨髓纤维化的任何公认的风险分层模型(例如,ipss、dipps和dipss-plus),actriib拮抗剂可用于促进或增加骨髓纤维化风险消退。例如,在一些实施方案中,根据ipss、dipps或dipss-plus,actriib拮抗剂可用于促进或增加从高风险至中等-2风险的骨髓纤维化风险消退。在其它实施方案中,根据ipss、dipps或dipss-plus,actriib拮抗剂可用于促进或增加从中等-2风险至中等-1风险的骨髓纤维化风险消退。在更其它实施方案中,根据ipss、dipps或dipss-plus,actriib拮抗剂可用于促进或增加从中等-1风险至低风险的骨髓纤维化风险消退。在某些方面,本公开内容涉及应用actriib拮抗剂来自治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中患者包含与骨髓纤维化相关的一种或多种基因突变。例如,在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中骨髓纤维化与选自下列的一种或多种基因突变相关:jak246/1单倍型的缺合子性、jak2v617f、idh1、idh2、ezh2、srsf2、asxl1、jak1、jak2、jak3、tyk2、mpl、calr、calr+asxl1-、calr-askl1+、calr+askl1+、calr-askl1-、tet2、thpo和lnk。在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中骨髓纤维化与janus激酶(jak)(例如,jak1、jak2和/或jak3)中的一种或多种基因突变相关。在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中骨髓纤维化与jak2中的一种或多种基因突变相关。在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中骨髓纤维化与jak2v617f突变相关。在某些方面,本公开内容涉及应用actriib拮抗剂来治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中骨髓纤维化与一种或多种升高的血清标志物相关,所述升高的血清标志物选自:升高的血清il-8水平、升高的血清il-2r水平和升高的游离血清轻链水平。在某些方面,本公开内容涉及应用actriib拮抗剂来治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中患者已经用janus激酶抑制剂(例如,鲁索利替尼(ruxolitinib)、fedratinib(sar302503)、monoelotinib(cyt387)、帕克替尼、来他替尼(lestaurtinib)、azd-1480、bms-911543、ns-018、ly2784544、sep-701、xl019和at-9283)治疗。在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中患者不耐受janus激酶抑制剂。在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中患者对janus激酶抑制剂具有不足的反应。在某些方面,本公开内容涉及应用actriib拮抗剂来治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,其中患者已经用羟基脲治疗。在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中患者不耐受羟基脲。在一些实施方案中,actriib拮抗剂可用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,其中患者对羟基脲具有不足的反应。
如本文所述,骨髓纤维化是造血的克隆性肿瘤病症,其与在患者中的疾病进展期间可能表现出的各种临床并发症相关。本公开内容的实施例证明actriib拮抗剂可用于减轻许多这些临床并发症,表明actriib拮抗剂可用于更广泛地治疗各种并发症骨髓纤维化,这与目前骨髓纤维化疗法中的许多相反,其仅治疗疾病的一个或有限数量的并发症。因此,在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的无效造血或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的髓外造血或降低其进展速率和/或严重性。例如,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中脾中的髓外造血(脾髓外造血)或降低其进展速率和/或严重性。在其它实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中肝中的髓外造血(肝髓外造血)或降低其进展速率和/或严重性。在甚至其它实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中肺中的髓外造血(肺髓外造血)或降低其进展速率和/或严重性。在更其它实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中淋巴结中的髓外造血(淋巴髓外造血)或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防骨髓纤维化患者中器官或组织的炎症和/或增大(大小)或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者的脾中的炎症和/或增大(大小)或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者的肝中的炎症和/或增大(大小)或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者的肺(一个或多个)中的炎症和/或增大(大小)或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者的淋巴结(一个或多个)中的炎症和/或增大(大小)或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的脾肿大或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的肝肿大或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的纤维化或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的骨髓纤维化或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的脾纤维化或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的肝纤维化或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的肺纤维化或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的淋巴结纤维化或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的骨硬化或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防骨髓纤维化(osteomyelofibrosis)或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防骨髓纤维化的一种或多种血液相关的并发症或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的贫血或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的血小板减少症或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的全血细胞减少症或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的异型红细胞症或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的出血或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防骨髓纤维化的一种或多种全身症状(例如,疲劳、瘙痒、体重减轻、盗汗、发热、腹痛或不适、感觉异常和早饱)或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中组织和/或器官中的疼痛或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的骨痛或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的关节痛或降低其进展速率和/或严重性。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的肌痛或降低其进展速率和/或严重性。在某些方面,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的恶病质或降低其进展速率和/或严重性。在某些方面,本公开内容涉及通过施用有效量的actriib拮抗剂增加骨髓纤维化患者中的红细胞水平。在某些方面,本公开内容涉及通过施用有效量的actriib拮抗剂增加骨髓纤维化患者中的血红蛋白水平。在某些方面,要根据本文描述的方法治疗的骨髓纤维化患者具有贫血。在一些实施方案中,actriib拮抗剂可用于治疗、预防具有骨髓纤维化的患者中的贫血或降低其进展速率和/或严重性。在某些方面,本公开内容涉及应用actriib拮抗剂治疗、预防患者中的骨髓纤维化或骨髓纤维化的并发症或降低其进展速率和/或严重性的方法,所述患者已经施用一种或多种血细胞输入(全血细胞或红细胞输入)。在一些实施方案中,本公开内容涉及方法应用actriib拮抗剂治疗、预防患者中的骨髓纤维化或骨髓纤维化的并发症或降低其进展速率和/或严重性的方法,所述患者是血细胞输入-依赖性的。在某些方面,actriib拮抗剂可用于减少具有骨髓纤维化的患者中的血细胞输入负荷。例如,相对于actriib拮抗剂治疗开始前的相等时间,actriib拮抗剂可用于将血细胞输入减少大于约30%、40%、50%、60%、70%、80%、90%或100%,持续4至8周。在一些实施方案中,在具有骨髓纤维化的患者中,相对于actriib拮抗剂治疗开始前的相等时间,actriib拮抗剂可用于将血细胞输入减少大于约50%,持续4至8周。在某些方面,actriib拮抗剂可用于减少具有骨髓纤维化的患者中的铁超载。例如,actriib拮抗剂可用于减少具有骨髓纤维化的患者中的器官或组织中的铁超载。在一些实施方案中,actriib拮抗剂可用于减少具有骨髓纤维化的患者的脾中的铁超载。在一些实施方案中,actriib拮抗剂可用于减少具有骨髓纤维化的患者的肝中的铁超载。在一些实施方案中,actriib拮抗剂可用于减少具有骨髓纤维化的患者的心脏中的铁超载。
在本文所述的任何方法中,可对骨髓纤维化患者进一步施用一种或多种另外的活性剂和/或支持疗法(除了施用一种或多种actriib拮抗剂),其用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性。例如,在一些实施方案中,可对患者进一步施用一种或多种支持疗法或活性剂,其选自:输血(全血或红细胞输入),铁螯合剂(例如,去铁胺、去铁酮和地拉罗西),皮质类固醇,泼尼松,esas(例如,促红细胞生成素、依泊汀α、依泊汀β、达贝泊汀α和甲氧基聚乙二醇-依泊汀β),雄激素,达那唑,沙利度胺,来那度胺,细胞减灭剂,羟基脲,白消安,melphalm,克拉屈滨,脾切除术,放射疗法,阿司匹林,pomalidonmide,janus激酶抑制剂,mtor抑制剂(例如,雷帕霉素、西罗莫司、deforolimus、依维莫司、temsirolimus、nvp-bez235、bgt226、sf1126、pk1-587、ink128、azd8055和azd2014)和组蛋白脱乙酰酶抑制剂(例如,givinostat、panobinostat和pracinostat)。在某些方面,本公开内容涉及用于治疗、预防骨髓纤维化或骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法,所述方法包括向有需要的患者施用:a)janus激酶抑制剂;和b)actriib拮抗剂,其中janus激酶抑制剂和actriib拮抗剂以有效量施用。在一些实施方案中,在用janus激酶抑制剂治疗之前施用actriib拮抗剂。在其它实施方案中,在用janus激酶抑制剂治疗后施用actriib拮抗剂。在甚至其它实施方案中,actriib拮抗剂与janus激酶抑制剂同时施用。待根据本文所述的方法使用的janus激酶抑制剂可为抑制选自jak1、jak2和jak3的一种或多种janus激酶的药剂。例如,janus激酶抑制剂可为在基于细胞的测定中抑制jak1、jak2和jak3中的一种或多种的信号传导的药剂。在一些实施方案中,待根据本文所述方法使用的janus激酶抑制剂选自:鲁索利替尼、fedratinib(sar302503)、monoelotinib(cyt387)、帕克替尼、来他替尼、azd-1480、bms-911543、ns-018、ly2784544、sep-701、xl019和at-9283。在一些优选的实施方案中,待根据本文所述方法使用的janus激酶抑制剂是鲁索利替尼。
janus激酶抑制剂(例如,鲁索利替尼)已被批准用于治疗多种病症,包括例如骨髓纤维化。此外,还有许多其它临床研究正在进行,以确定janus激酶抑制剂治疗各种其它疾病的效力。janus激酶抑制剂疗法的常见不良副作用是贫血。虽然血细胞输入和epo受体激活剂疗法可用于在使用janus激酶抑制剂治疗的患者中治疗贫血,但这些贫血疗法也与患者中的不良作用有关(例如,促进或增加铁超载、对epo的反应不充分和epo不耐受)。因此,本领域需要在使用janus激酶抑制剂治疗的患者中增加红细胞/血红蛋白水平和治疗贫血的可选方法。部分地,本公开内容涉及发现actriib拮抗剂(抑制剂)可以用于在使用janus激酶抑制剂治疗的患者中增加红细胞和血红蛋白水平。因此,在某些方面,本公开内容涉及在使用janus激酶抑制剂治疗的患者中增加红细胞/血红蛋白水平和治疗或预防贫血的组合物和方法,其通过向有需要的患者施用有效量的一种或多种actriib拮抗剂、任选地与用于治疗贫血的一种或多种其它支持疗法或活性剂组合实施。虽然gdf捕获物多肽可通过actriib拮抗作用以外的机制影响红细胞和/或血红蛋白水平[例如,gdf11、gdf8、激活蛋白b、bmp6、gdf3和bmp10中的一种或多种的抑制可为药剂抑制一系列其它因子的活性的趋势的指示物,所述其它因子可能包括tgf-β超家族的其它成员,并且这种集体抑制在使用janus激酶抑制剂治疗的患者中可导致对例如红细胞水平和/或血红蛋白水平的期望效应],但本公开内容证明可基于actriib拮抗作用选择希望的治疗剂。因此,虽然不希望受特定作用机制的束缚,但预期其它actriib拮抗剂[例如,actriib受体的拮抗剂,一种或多种actriib配体(例如,gdf11、gdf8、激活蛋白b、bmp6、gdf3和bmp10)的拮抗剂,一种或多种i型受体(例如,alk4、alk5和/或alk7)的拮抗剂,一种或多种共同受体的拮抗剂,和/或一种或多种actriib下游信号传导组分(例如,smads)的拮抗剂]或这些拮抗剂的组合]将用于治疗用janus激酶治疗的患者,特别是用于治疗或预防与janus激酶疗法相关的一种或多种并发症(例如,贫血、血小板减少和/或中性粒细胞减少症)。此类药剂在本文中统称为“actriib拮抗剂”或“actriib抑制剂”。
在某些方面,本公开内容涉及通过向有需要的患者施用有效量的actriib拮抗剂来增加用janus激酶抑制剂治疗的患者中的红细胞水平和/或血红蛋白水平的方法。在一些实施方案中,actriib拮抗剂可用于治疗或预防用janus激酶抑制剂治疗的患者中的贫血。在一些实施方案中,在开始actriib拮抗剂治疗之前,可以对用janus激酶抑制剂治疗的患者施用一次或多次血细胞输入。在一些实施方案中,用janus激酶抑制剂治疗的患者是血细胞输入-依赖性的。在某些方面,本公开内容涉及应用actriib拮抗剂减少用janus激酶抑制剂治疗的患者中的血细胞输入负荷的方法。例如,在用janus激酶抑制剂治疗的患者中,相对于actriib拮抗剂治疗开始前的相等时间,actriib拮抗剂可用于将血细胞输入减少大于约30%、40%、50%、60%、70%、80%、90%或100%,持续4至8周。在一些实施方案中,在用janus激酶抑制剂治疗的患者中,相对于actriib拮抗剂治疗开始前的相等时间,actriib拮抗剂可用于将血细胞输入减少大于约50%,持续4至8周。在某些方面,本公开内容涉及应用actriib拮抗剂减少用janus激酶抑制剂治疗的患者中的铁超载的方法。在一些实施方案中,actriib拮抗剂可用于减少用janus激酶抑制剂治疗的患者的肝中的铁含量。在一些实施方案中,actriib拮抗剂可用于减少用janus激酶抑制剂治疗的患者的脾中的铁含量。在一些实施方案中,actriib拮抗剂可用于减少用janus激酶抑制剂治疗的患者的心脏中的铁含量。在一些实施方案中,在用janus激酶抑制剂治疗之前施用actriib拮抗剂。在其它实施方案中,在用janus激酶抑制剂治疗之后施用actriib拮抗剂。在更其它实施方案中,actriib拮抗剂与janus激酶抑制剂同时施用。在某些方面,用janus激酶抑制剂治疗的患者已经用抑制选自jak1、jak2和jak3的janus激酶的一种或多种的药剂治疗。在一些实施方案中,janus激酶抑制剂在基于细胞的测定中抑制jak1、jak2和jak3中的一种或多种的信号传导。例如,可用选自下列的一种或多种janus激酶抑制剂治疗患者:鲁索利替尼、fedratinib(sar302503)、monoelotinib(cyt387)、帕克替尼、来他替尼、azd-1480、bms-911543、ns-018、ly2784544、sep-701、xl019和at-9283。在一些实施方案中,患者可用鲁索利替尼治疗。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少gdf11的药剂(例如,gdf11拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对gdf11抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少gdf11。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少gdf11。如本文所述的,各种抑制gdf11的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制gdf11的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少gdf8的药剂(例如,gdf8拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对gdf8抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少gdf8。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少gdf8。如本文所述的,各种抑制gdf8的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制gdf8的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf11、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少gdf3的药剂(例如,gdf3拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对gdf3抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少gdf3。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少gdf3。如本文所述的,各种抑制gdf3的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制gdf3的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf11、bmp6、bmp10、actriib、alk4、alk5和alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少bmp6的药剂(例如,bmp6拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对bmp6抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少bmp6。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少bmp6。如本文所述的,各种抑制bmp6的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制bmp6的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf3、gdf11、bmp10、actriib、alk4、alk5和alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少bmp10的药剂(例如,bmp10拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对bmp10抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少bmp10。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少bmp10。如本文所述的,各种抑制bmp10的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制bmp10的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf3、gdf11、bmp6、actriib、alk4、alk5、alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)的药剂(例如,激活蛋白拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对激活蛋白抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少激活蛋白。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少激活蛋白。如本文所述的,各种抑制激活蛋白的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制激活蛋白的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:gdf8、gdf3、gdf11、bmp6、bmp10、actriib、alk4、alk5和alk7。在某些优选实施方案中,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少激活蛋白b的药剂。在一些实施方案中,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合基本上不结合激活蛋白a(例如,以高于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)和/或抑制激活蛋白a活性。在某些优选实施方案中,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少激活蛋白b、但基本上不结合激活蛋白a(例如,以高于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)和/或抑制激活蛋白a活性的药剂。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少actriib的药剂(例如,actriib拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对actriib抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少actriib。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少actriib。如本文所述的,各种抑制actriib的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制actriib的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf3、gdf11、bmp6、bmp10、alk4、alk5和alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少alk4的药剂(例如,alk4拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对alk4抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少alk4。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少alk4。如本文所述的,各种抑制alk4的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制alk4的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf3、gdf11、bmp6、bmp10、actriib、alk5和alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少alk5的药剂(例如,alk5拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对alk5抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少alk5。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少alk5。如本文所述的,各种抑制alk5的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制alk5的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf3、gdf11、bmp6、bmp10、actriib、alk4和alk7。
在某些方面,待根据本文所述的方法和用途使用的actriib拮抗剂或拮抗剂的组合是抑制至少alk7的药剂(例如,alk7拮抗剂)。可以例如使用基于细胞的测定、包括本文所述的那些(例如,smad信号传导报道分子测定)测定对alk7抑制的影响。因此,在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合可以结合至少alk7。配体结合活性可以例如使用结合亲和力测定(包括本文所述的那些)来测定。在一些实施方案中,本公开内容的actriib拮抗剂或拮抗剂的组合以至少1x10-7m(例如,至少1x10-8m、至少1x10-9m、至少1x10-10m、至少1x10-11m或至少1x10-12m)的kd结合至少alk7。如本文所述的,各种抑制alk7的actriib拮抗剂可以根据本文所述的方法和用途使用,包括例如配体捕获物(例如,actriib多肽、gdf捕获物、促滤泡素抑制素多肽和flrg多肽)、抗体、小分子、核苷酸序列及其组合。在某些实施方案中,抑制alk7的actriib拮抗剂或拮抗剂的组合可以进一步抑制以下中的一种或多种:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和/或激活蛋白be)、gdf8、gdf3、gdf11、bmp6、bmp10、actriib、alk5和alk4。
部分地,本公开内容涉及为actriib多肽的actriib拮抗剂。术语“actriib多肽”总起来说是指天然存在的actriib多肽以及其截短物(truncations)和变体,诸如本文所述的那些(例如,gdf捕获物多肽)。优选地,actriib多肽包含actriib多肽的配体结合结构域或其修饰(变体)形式、基本上由其组成或由其组成。例如,在一些实施方案中,actriib多肽包含actriib多肽的actriib配体结合结构域(例如,actriib细胞外结构域的一部分)、基本上由其组成或由其组成。优选地,待根据本文描述的方法使用的actriib多肽是可溶性多肽。
在某些方面,本公开内容涉及包含actriib多肽的组合物及其用途。例如,在一些实施方案中,本公开内容的actriib多肽包含与seqidno:1的氨基酸29-109的序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:1的氨基酸29-109的序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸[天然存在的(e或d)或人工酸性氨基酸]。在其它实施方案中,actriib多肽可以包含与seqidno:1的氨基酸25-131的序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:1的氨基酸25-131的序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在其它实施方案中,actriib多肽可以包含与seqidno:1的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:1的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在甚至其它实施方案中,actriib多肽可以包含与seqidno:2的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在其它实施方案中,actriib多肽可以包含与seqidno:2的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有其它实施方案中,actriib多肽可以包含与seqidno:3的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在其它实施方案中,actriib多肽可以包含与seqidno:3的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在其它实施方案中,actriib多肽可以包含与seqidno:4的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:4的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:4的位置79处包含酸性氨基酸。在其它实施方案中,actriib多肽可以包含与seqidno:5的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:5的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:4的位置79处包含酸性氨基酸。在其它实施方案中,actriib多肽可以包含与seqidno:6的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:6的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:4的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:24的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:25的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:28的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:29的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:29的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:30的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:30的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:31的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:31的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:45的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:45的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:50的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:50的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:53的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:53的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:54的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,actriib多肽可以包含与seqidno:54的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,其中所述actriib多肽在关于seqidno:1的位置79处包含酸性氨基酸。在还有甚至其它实施方案中,actriib多肽可以包含与seqidno:58的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在某些实施方案中,待根据本文所述的方法和用途使用的actriib多肽在对应于seqidno:1的l79的位置处不包含酸性氨基酸。
如本文所述的,actriib多肽及其变体(gdf捕获物)可以是同多聚体,例如同二聚体、同三聚体、同四聚体、同五聚体和更高级的同多聚体复合体。在某些优选实施方案中,actriib多肽及其变体是同二聚体。在某些实施方案中,本文所述的actrii多肽二聚体包含与第二actriib多肽共价或非共价缔合的第一actriib多肽,其中第一多肽包含actriib结构域和相互作用对的第一成员(或第二成员)的氨基酸序列(例如,免疫球蛋白的恒定结构域),且第二多肽包含actriib多肽和相互作用对的第二成员(或第一成员)的氨基酸序列。
在某些方面,actriib多肽、包括其变体(例如,gdf捕获物)可以是融合蛋白。例如,在一些实施方案中,actriib多肽可以是融合蛋白,其包含actriib多肽结构域和一种或多种异源(非actriib)多肽结构域。在一些实施方案中,actriib多肽可以是融合蛋白,其具有作为一个结构域的衍生自actriib多肽的氨基酸序列(例如,actriib受体的配体结合结构域或其变体)和一个或多个提供所期望的性质(诸如改善的药物代谢动力学、更容易的纯化、靶向特定组织等)的异源结构域。例如,融合蛋白的结构域可以增强体内稳定性、体内半衰期、摄取/施用、组织定位或分布、蛋白复合体的形成、融合蛋白的多聚化和/或纯化中的一种或多种。任选地,融合蛋白的actriib多肽结构域直接连接(融合)至一个或多个异源多肽结构域,或间插序列(诸如接头)可以位于actriib多肽的氨基酸序列和一个或多个异源结构域的氨基酸序列之间。在某些实施方案中,actriib融合蛋白包含位于异源结构域和actriib结构域之间的相对非结构性接头。该非结构性接头可以对应于actriib的细胞外结构域的c-末端(“尾”)处的大致15个氨基酸的非结构性区域,或者其可以是3至15、20、30、50或更多相对不含二级结构的氨基酸的人工序列。接头可以富含甘氨酸和脯氨酸残基,并且可以例如含有苏氨酸/丝氨酸和甘氨酸的重复序列。接头的实例包括但不限于,序列tggg(seqidno:18)、sggg(seqidno:19)、tgggg(seqidno:16)、sgggg(seqidno:17)、ggggs(seqidno:20)、gggg(seqidno:15)和ggg(seqidno:14)。在一些实施方案中,actriib融合蛋白可以包含免疫球蛋白的恒定结构域,包括例如免疫球蛋白的fc部分。例如,衍生自igg(igg1、igg2、igg3或igg4)、iga(iga1或iga2)、ige或igm免疫球蛋白的fc结构域的氨基酸序列。例如,免疫球蛋白结构域的fc部分可以包含与seqidno:9-13中任一个具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,基本上由其组成,或由其组成。这种免疫球蛋白结构域可以包含一种或多种氨基酸修饰(例如,缺失、添加和/或取代),其赋予改变的fc活性,例如,一种或多种fc效应子功能的降低。在一些实施方案中,actriib融合蛋白包含如式a-b-c中所示的氨基酸序列。例如,b部分是n-和c-末端截短的actriib多肽,如本文所述的。a和c部分可以独立地为零个、一个或多于一个氨基酸,且a和c部分两者对b都是异源的。a和/或c部分可以经由接头序列附着至b部分。在某些实施方案中,actriib融合蛋白包含前导序列。所述前导序列可以是天然actriib前导序列或异源前导序列。在某些实施方案中,所述前导序列是组织纤溶酶原激活物(tpa)前导序列。
actriib多肽、包括其变体(例如,gdf捕获物)可以包含纯化子序列,诸如表位标签、flag标签、多组氨酸序列和gst融合物(fusion)。任选地,actriib多肽包含一个或多个修饰的氨基酸残基,其选自:糖基化氨基酸、加入聚乙二醇的氨基酸、法呢基化氨基酸、乙酰化氨基酸、生物素化氨基酸和/或与脂质部分缀合的氨基酸。actriib多肽可以包含至少一种n-连接的糖,且可以包括两种、三种或更多种n-连接的糖。这种多肽还可以包含o-连接的糖。通常,优选actriib多肽在哺乳动物细胞系中表达,所述哺乳动物细胞系合适地介导多肽的天然糖基化以减少患者中不利的免疫应答的可能性。actriib多肽可以在以适合于患者使用的方式将蛋白糖基化的多种细胞系(包括人工改造的昆虫或酵母细胞,和哺乳动物细胞如cos细胞、cho细胞、hek细胞和nso细胞)中产生。在一些实施方案中,actriib多肽被糖基化且具有可获得自中国仓鼠卵巢细胞系的糖基化模式。在一些实施方案中,本公开内容的actriib多肽在哺乳动物(例如,小鼠或人)中表现出至少4、6、12、24、36、48或72小时的血清半衰期。任选地,actriib多肽在哺乳动物(例如,小鼠或人)中可以表现出至少6、8、10、12、14、20、25或30天的血清半衰期。
在某些方面,本公开内容提供了包含一种或多种本公开内容的actriib拮抗剂和药学上可接受的载体的药物制剂。药物制剂还可以包含一种或多种额外活性剂,诸如用于治疗骨髓纤维化、特别是治疗或预防骨髓纤维化的一种或多种并发症(例如,脾肿大、髓外造血、贫血和纤维化)和/或用janus激酶抑制剂治疗的患者的化合物。通常,药物制剂优选地将是无致热原的(意味着无致热原至管理用于治疗用途的产品质量的规章需要的程度)。
在某些情况下,当将本公开内容的actriib拮抗剂或拮抗剂的组合施用于本文所述的病症或状况时,可期望监控在施用actriib拮抗剂期间对红细胞的作用,或确定或调整actriib拮抗剂的给药,以减少对红细胞的不期望的作用。例如,红细胞水平、血红蛋白水平或血细胞比容水平的增加可以引起血压的不期望的增加。
在某些方面,actriib拮抗剂是抗体或抗体组合。在一些实施方案中,抗体结合至少actriib。在某些实施方案中,结合actriib的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合actriib的抗体抑制一种或多种tgf-β超家族配体、tgf-β超家族i型受体或tgf-β超家族共同受体与actriib的结合。在某些实施方案中,结合actriib的抗体抑制一种或多种tgf-β超家族配体与选自下列的actriib的结合:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)、gdf8、gdf11、gdf3、bmp6、bmp10、bmp9和bmp5。在一些实施方案中,抗体结合至少gdf11。在某些实施方案中,结合gdf11的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合gdf11的抗体抑制gdf11-actriib结合。在一些实施方案中,抗体结合至少gdf8。在某些实施方案中,结合gdf8的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合gdf8的抗体抑制gdf8-actriib结合。在一些实施方案中,抗体结合至少bmp6。在某些实施方案中,结合bmp6的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合bmp6的抗体抑制bmp6-actriib结合。在一些实施方案中,抗体结合bmp10。在某些实施方案中,结合至少bmp10的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合bmp10的抗体抑制bmp10-actriib结合。在一些实施方案中,抗体结合至少gdf3。在某些实施方案中,结合gdf3的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合gdf3的抗体抑制gdf3-actriib结合。在一些实施方案中,抗体结合至少激活蛋白(例如激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)。在某些实施方案中,结合激活蛋白(例如激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合激活蛋白(例如激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)的抗体抑制激活蛋白-actriib结合。在一些实施方案中,抗体结合激活蛋白b。在某些实施方案中,结合激活蛋白b的抗体抑制actriib信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合激活蛋白b的抗体抑制激活蛋白b-actriib结合。在一些实施方案中,抗体是结合actriib、gdf11、gdf8、激活蛋白a、激活蛋白b、bmp6和bmp10中的一种或多种的多特异性抗体或多特异性抗体的组合。在一些实施方案中,抗体结合至少alk4。在某些实施方案中,结合alk4的抗体抑制alk4信号传导,任选地如在基于细胞的测定、例如本文所述的那些中测量。在某些实施方案中,结合alk4的抗体抑制一种或多种actriib配体,ii型受体或共同受体与alk4的结合。在某些实施方案中,结合alk4的抗体抑制一种或多种选自以下的actriib配体与alk4的结合:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)、gdf8、gdf11、bmp6、bmp10和gdf3。在一些实施方案中,所述抗体结合至少alk5。在某些实施方案中,结合alk5的抗体抑制alk5信号传导,任选地如在基于细胞的测定、诸如本文所述的那些中测量。在某些实施方案中,结合alk5的抗体抑制一种或多种actriib配体、ii型受体或共受体与alk5的结合。在某些实施方案中,结合alk5的抗体抑制一种或多种选自以下的actriib配体与alk5的结合:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)、gdf8、gdf11、bmp6、bmp10和gdf3。在一些实施方案中,所述抗体结合至少alk7。在某些实施方案中,结合alk7的抗体抑制alk7信号传导,任选地如在基于细胞的测定、诸如本文所述的那些中所测量。在某些实施方案中,结合alk7的抗体抑制一种或多种actriib配体、ii型受体或共同受体与alk7的结合。在某些实施方案中,结合alk7的抗体抑制一种或多种选自以下的actriib配体与alk7的结合:激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)、gdf8、gdf11、bmp6、bmp10和gdf3。在一些实施方案中,所述抗体结合至少gdf11。在某些方面,多特异性抗体或多特异性抗体的组合在基于细胞的测定中抑制以下中的一种或多种的信号传导:actriib、gdf11、gdf8、激活蛋白a、激活蛋白b、gdf3、bmp6和bmp10。在一些实施方案中,抗体是嵌合抗体、人源化抗体或人抗体。在一些实施方案中,所述抗体是单链抗体、f(ab’)2片段、单链双抗体、串联单链fv片段、串联单链双抗体或包含单链双抗体和免疫球蛋白重链恒定区的至少一部分的融合蛋白。
在某些方面,所述actriib拮抗剂是小分子抑制剂或小分子抑制剂的组合。在一些实施方案中,所述小分子抑制剂是至少actriib的抑制剂。在一些实施方案中,所述小分子抑制剂是至少alk4的抑制剂。在一些实施方案中,所述小分子抑制剂是至少alk5的抑制剂。在一些实施方案中,所述小分子抑制剂是至少alk7的抑制剂。在一些实施方案中,所述小分子抑制剂是至少gdf11的抑制剂。在一些实施方案中,所述小分子抑制剂是至少gdf8的抑制剂。在一些实施方案中,所述小分子抑制剂是至少bmp6的抑制剂。在一些实施方案中,所述小分子抑制剂是至少bmp10的抑制剂。在一些实施方案中,所述小分子抑制剂是至少gdf3的抑制剂。在一些实施方案中,所述小分子抑制剂是至少激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)的抑制剂。在一些实施方案中,所述小分子抑制剂是至少激活蛋白b的抑制剂。
在某些方面,所述actriib拮抗剂是核酸抑制剂或核酸抑制剂的组合。在一些实施方案中,所述核酸抑制剂是至少actriib的抑制剂。在一些实施方案中,所述核酸抑制剂是至少alk4的抑制剂。在一些实施方案中,所述核酸抑制剂是至少alk5的抑制剂。在一些实施方案中,所述核酸抑制剂是至少alk7的抑制剂。在一些实施方案中,所述核酸抑制剂是至少gdf11的抑制剂。在一些实施方案中,所述核酸抑制剂是至少gdf8的抑制剂。在一些实施方案中,所述核酸抑制剂是至少bmp6的抑制剂。在一些实施方案中,所述核酸抑制剂是至少bmp10的抑制剂。在一些实施方案中,所述核酸抑制剂是至少gdf3的抑制剂。在一些实施方案中,所述核酸抑制剂是至少激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白e、激活蛋白ae和激活蛋白be)的抑制剂。在一些实施方案中,所述核酸抑制剂是至少激活蛋白b的抑制剂。
在某些方面,所述actriib拮抗剂是促滤泡素抑制素(follistatin)多肽。在一些实施方案中,所述促滤泡素抑制素多肽包含与seqidno:63的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,所述促滤泡素抑制素多肽包含与seqidno:64的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,所述促滤泡素抑制素多肽包含与seqidno:65的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,所述促滤泡素抑制素多肽包含与seqidno:66的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。在一些实施方案中,所述促滤泡素抑制素多肽包含与seqidno:67的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。
在某些方面,所述actriib拮抗剂是flrg多肽。在一些实施方案中,所述flrg多肽包含与seqidno:68的氨基酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。
附图简述
图1显示人actriia(seqidno:36)和人actriib(seqidno:2)的细胞外结构域的比对,且基于多个actriib和actriia晶体结构的复合分析,本文推论直接接触配体的残基用方框表示。
图2显示各种脊椎动物actriib蛋白和人actriia(seqidno:37-43)的多重序列比对以及衍生自比对的共有actrii序列(seqidno:44)。
图3显示gdf捕获物actriib(l79d20-134)-hfc的完整氨基酸序列(seqidno:45),包括tpa前导序列(双下划线)、actriib细胞外结构域(seqidno:1中的残基20-134;单下划线)和hfc结构域。天然序列中位置79处取代的天冬氨酸加双下划线且突出显示,通过测序揭示为成熟融合蛋白中的n-末端残基的甘氨酸也这样。
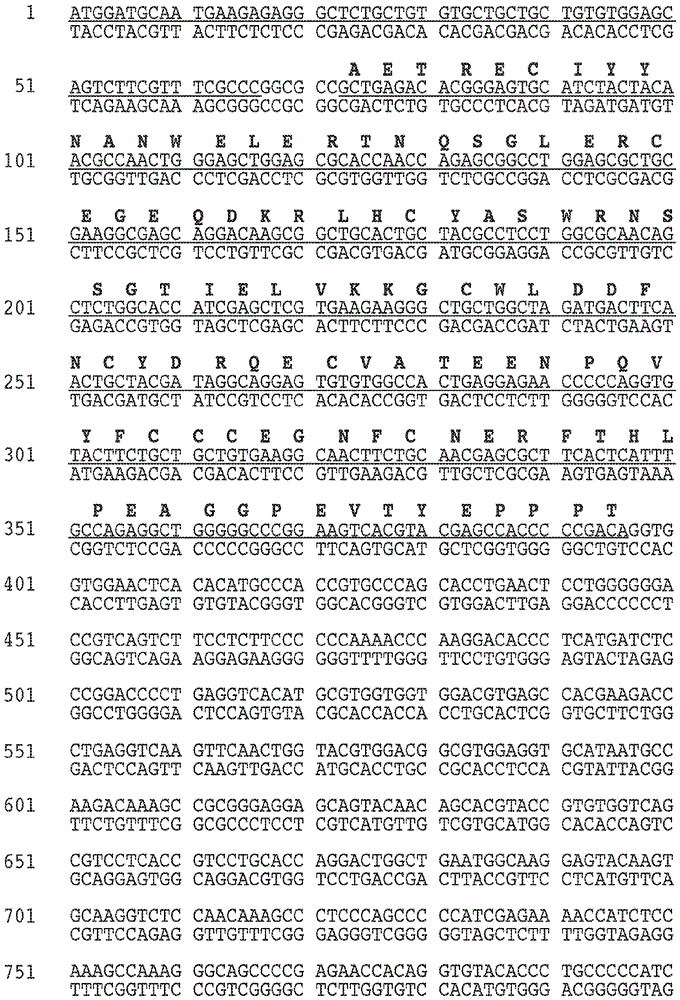
图4a和4b显示编码actriib(l79d20-134)-hfc的核苷酸序列。seqidno:48对应于有义链,且seqidno:49对应于反义链。tpa前导序列(核苷酸1-66)加双下划线,且actriib细胞外结构域(核苷酸76-420)加单下划线。
图5显示截短的gdf捕获物actriib(l79d25-131)-hfc的完整氨基酸序列(seqidno:50),包括tpa前导序列(双下划线)、截短的actriib细胞外结构域(seqidno:1中的残基25-131;单下划线)和hfc结构域。天然序列中位置79处取代的天冬氨酸加双下划线且突出显示,通过测序揭示为成熟融合蛋白中的n-末端残基的谷氨酸也这样。
图6a和6b显示编码actriib(l79d25-131)-hfc的核苷酸序列。seqidno:51对应于有义链,且seqidno:52对应于反义链。tpa前导序列(核苷酸1-66)加双下划线,且截短的actriib细胞外结构域(核苷酸76-396)加单下划线。也显示了actriib细胞外结构域(seqidno:1中的残基25-131)的氨基酸序列。
图7显示没有前导序列的截短的gdf捕获物actriib(l79d25-131)-hfc的氨基酸序列(seqidno:53)。截短的actriib细胞外结构域(seqidno:1中的残基25-131)加下划线。天然序列中位置79处取代的天冬氨酸加双下划线且突出显示,通过测序揭示为成熟融合蛋白中的n-末端残基的谷氨酸也这样。
图8显示没有前导序列、hfc结构域和接头的截短的gdf捕获物actriib(l79d25-131)的氨基酸序列(seqidno:54)。天然序列中位置79处取代的天冬氨酸加下划线且突出显示,通过测序揭示为成熟融合蛋白中的n-末端残基的谷氨酸也这样。
图9a和9b显示编码actriib(l79d25-131)-hfc的可选核苷酸序列。seqidno:55对应于有义链,且seqidno:56对应于反义链。tpa前导序列(核苷酸1-66)加双下划线,截短的actriib细胞外结构域(核苷酸76-396)加下划线,且细胞外结构域的野生型核苷酸序列中的取代加双下划线且突出显示(与seqidno:51相比,图6a和6b)。还显示actriib细胞外结构域的氨基酸序列(seqidno:1中的残基25-131)。
图10显示图9a和9b中所示的可选核苷酸序列(seqidno:55)的核苷酸76-396(seqidno:57)。图9a和9b中所示的相同核苷酸取代在此处也加下划线且突出显示。seqidno:57仅编码具有l79d取代的截短的actriib细胞外结构域(对应于seqidno:1中的残基25-131),例如actriib(l79d25-131)。
图11显示应用clustal2.1来自人igg同种型的fc结构域的多重序列比对。铰链区通过虚下划线显示。
图12显示actriib(25-131)-hfc(seqidno:58)的完整、未加工的氨基酸序列。tpa前导序列(残基1-22)和双截短的actriib细胞外结构域(残基24-131,使用基于seqidno:1中的天然序列的编号)各自标有下划线。突出显示的是谷氨酸,其通过测序揭示为成熟融合蛋白的n-末端氨基酸,其相对于seqidno:1位于25位。
图13a和13b显示编码actriib(25-131)-hfc的核苷酸序列(编码链显示在顶部,seqidno:59,并且互补序列显示在底部3'-5',seqidno:60)。编码tpa前导序列(核苷酸1-66)和actriib细胞外结构域(核苷酸73-396)的序列标有下划线。还显示了actriib(25-131)的相应氨基酸序列。
图14a和14b显示编码actriib(25-131)-hfc的可选核苷酸序列(编码链显示于顶部,seqidno:61,并且互补序列显示于底部3'-5',seqidno:62)。该序列在初始转化体中赋予更高水平的蛋白质表达,使细胞系发育成为更快速的过程。编码tpa前导序列(核苷酸1-66)和actriib细胞外结构域(核苷酸73-396)的序列加下划线,并且突出显示ecd的野生型核苷酸序列中的取代(参见图13a和13b)。还显示了actriib(25-131)的相应氨基酸序列。
发明详述
1.概述
转化生长因子-β(tgf-β)超家族含有多种生长因子,其共享共同的序列元件和结构基序。已知这些蛋白质对脊椎动物和无脊椎动物中的大量细胞类型发挥生物学作用。超家族成员在胚胎发育期间在模式形成和组织指定中发挥重要作用,并且可以影响多种分化过程,包括脂肪形成、肌细胞生成、软骨形成、心脏发生、造血、神经发生和上皮细胞分化。通过操纵tgfβ家族成员的活性,通常可能在生物体中引起显著的生理变化。例如,piedmontese和belgianblue牛品种在gdf8(也称为肌肉生长抑制素(myostatin))基因中携带功能丧失突变,其导致肌肉量明显增加[参见,例如,grobet等(1997)natgenet.17(1):71-4]。而且,在人中,gdf8的无活性等位基因与增加的肌肉量相关,并据报道与非凡的强度相关[参见,例如,schuelke等(2004)nengljmed,350:2682-8]。
tgf-β信号传导由i型和ii型丝氨酸/苏氨酸激酶受体的异聚复合体介导,在配体刺激时其磷酸化和活化下游smad蛋白(例如,smad蛋白1、2、3、5和8)[参见例如,massagué(2000)nat.rev.mol.cellbiol.1:169-178]。这些i型和ii型受体是跨膜蛋白,由具有富含半胱氨酸的区域的配体-结合细胞外结构域、跨膜结构域和具有预期的丝氨酸/苏氨酸特异性的胞质结构域构成。i型受体是信号传导所必需的。ii型受体是结合配体和i型受体活化所必需的。在配体结合后i型和ii型激活蛋白受体形成稳定的复合体,导致i型受体被ii型受体磷酸化。
两种相关的ii型受体(actrii)actriia和actriib已被鉴定为激活蛋白的ii型受体[参见,例如,mathewsandvale(1991)cell65:973-982;和attisano等(1992)cell68:97-108]。除激活蛋白外,actriia和actriib可与几种其它tgf-β家族蛋白生物化学相互作用,所述其它tgf-β家族蛋白包括例如bmp6、bmp7、nodal、gdf8和gdf11[参见,例如,yamashita等(1995)j.cellbiol.130:217-226;leeandmcpherron(2001)proc.natl.acad.sci.usa98:9306-9311;yeoandwhitman(2001)mol.cell7:949-957;和oh等(2002)genesdev.16:2749-54]。alk4是对于激活蛋白、特别是激活蛋白a的主要i型受体,并且alk-7也可作为对于其它激活蛋白、特别是对于激活蛋白b的受体。
激活蛋白是属于tgf-β超家族的二聚体多肽生长因子。有三种主要的激活蛋白形式(a、b和ab),其是两个紧密相关的β亚基的同/异二聚体(分别为βaβa、βbβb和βaβb)。人基因组还编码激活蛋白c和激活蛋白e,其主要在肝中表达,且含有βc或βe的异二聚体形式也是已知的。
在tgf-β超家族中,激活蛋白是独特和多功能的因子,其可在卵巢和胎盘细胞中刺激激素产生,支持神经元细胞存活,取决于细胞类型正面或负面影响细胞周期进展,且至少在两栖动物胚胎中诱导中胚层分化[depaolo等(1991)procsocepbiolmed.198:500-512;dyson等(1997)currbiol.7:81-84;和woodruff(1998)biochempharmacol.55:953-963]。而且,发现从经刺激的人单核细胞白血病细胞分离的红细胞分化因子(edf)与激活蛋白a相同[murata等(1988)pnas,85:2434]。已建议激活蛋白a促进骨髓中的红细胞生成。在几种组织中,激活蛋白信号传导被其相关的异二聚体抑制素拮抗。例如,在促卵泡激素(fsh)从垂体释放期间,激活蛋白促进fsh分泌和合成,而抑制素阻止fsh分泌和合成。可调节激活蛋白生物活性和/或结合激活蛋白的其它蛋白包括促滤泡素抑制素(fs)、促滤泡素抑制素-相关蛋白(fsrp,也称为flrg或fstl3)和α2-巨球蛋白。
如本文所述的,结合“激活蛋白a”的药剂是特异性结合βa亚基的药剂,无论是在分离的βa亚基的情况下还是作为二聚的复合体(例如,βaβa同二聚体或βaβb异二聚体)。在异二聚体复合体(例如,βaβb异二聚体)的情况下,结合“激活蛋白a”的药剂对βa亚基内存在的表位是特异性的,但不结合复合体的非-βa亚基(例如,复合体的βb亚基)内存在的表位。类似地,本文公开的拮抗(抑制)“激活蛋白a”的药剂是抑制由βa亚基介导的一种或多种活性的药剂,无论是在分离的βa亚基的情况下还是作为二聚的复合体(例如,βaβa同二聚体或βaβb异二聚体)。在βaβb异二聚体的情况下,抑制“激活蛋白a”的药剂是特异性抑制βa亚基的一种或多种活性,但不抑制复合体的非-βa亚基(例如,复合体的βb亚基)的活性的药剂。这个原理也适用于结合和/或抑制“激活蛋白b”、“激活蛋白c”和“激活蛋白e”的药剂。本文公开的拮抗“激活蛋白ab”的药剂是抑制由βa亚基介导的一种或多种活性和由βb亚基介导的一种或多种活性的药剂。
生长和分化因子-8(gdf8)也称为肌肉生长抑制素。gdf8是骨骼肌质量的负调节物。gdf8在发育中的骨骼肌和成体骨骼肌中高度表达。在转基因小鼠中gdf8无效突变特征在于骨骼肌的显著肥大和增生[mcpherron等,nature(1997)387:83-90]。在家畜中[参见例如,ashmore等(1974)growth,38:501-507;swatland和kieffer,(1994)j.anim.sci.38:752-757;mcpherron和lee,(1997)proc.natl.acad.sci.usa94:12457-12461;和kambadur等,(1997)genomeres.7:910-915]以及引人注目地在人中[参见例如,schuelke等(2004)nengljmed,350:2682-8],在天然存在的gdf8突变中骨骼肌质量的类似增加是明显的。研究也已经显示,在人中与hiv-感染相关的肌肉消瘦伴随有gdf8蛋白表达的增加[参见例如,gonzalez-cadavid等,(1998)pnas95:14938-43]。此外,gdf8可以调节肌肉-特异性的酶(例如,肌酸激酶)的产生和调节成肌细胞细胞增殖[参见例如,国际专利申请公开号wo00/43781]。gdf8前肽可非共价结合成熟的gdf8结构域二聚体,灭活其生物学活性[参见例如,miyazono等(1988)j.biol.chem.,263:6407-6415;wakefield等(1988)j.biol.chem.,263;7646-7654;和brown等(1990)growthfactors,3:35-43]。结合gdf8或结构相关蛋白且抑制它们的生物学活性的其它蛋白包括促滤泡素抑制素,和可能地,促滤泡素抑制素-相关蛋白[参见例如,gamer等(1999)dev.biol.,208:222-232]。
生长和分化因子(gdf11),也称为bmp11,是一种分泌蛋白[mcpherron等(1999)nat.genet.,22:260-264]。gdf11在小鼠发育期间在尾芽、肢芽、上颌和下颌弓和背根神经节中表达[参见例如,nakashima等(1999)mech.dev.,80:185-189]。gdf11在中胚层和神经组织两者的模式化(patterning)中起独特的作用[参见例如,gamer等(1999)devbiol.,208:222-32]。gdf11已显示是在发育中的鸡肢体中的软骨发生和肌发生的负调节物[参见例如,gamer等(2001)devbiol.,229:407-20]。gdf11在肌肉中的表达也提示其以类似于gdf8的方式在调节肌肉生长中的作用。此外,gdf11在脑中的表达提示gdf11还可具有与神经系统的功能相关的活性。有趣的是,发现gdf11在嗅上皮中抑制神经发生[参见例如,wu等(2003)neuron.,37:197-207]。
部分地,本公开内容涉及发现actriib拮抗剂(抑制剂)可以用于治疗骨髓纤维化患者,特别是改善疾病的各种并发症,包括例如脾肿大、髓外造血和纤维化。特别地,本文呈现的数据显示,gdf捕获物多肽在骨髓纤维化的jak2v617f模型中减少脾肿大、髓外造血和纤维化。因此,在某些方面,本公开内容涉及治疗骨髓纤维化、特别是治疗或预防骨髓纤维化的一种或多种并发症(脾肿大、髓外造血、贫血和纤维化)的组合物和方法,其通过向有需要的患者施用有效量的一种或多种actriib拮抗剂、任选地与用于治疗骨髓纤维化的一种或多种其它支持疗法或活性剂组合实施。
在本发明的上下文中和在使用每个术语的特定上下文中,本说明书中使用的术语通常具有其在本领域中的普通含义。下文或说明书别处讨论了某些术语,以在描述本发明的组合物和方法和如何制备和使用它们方面,向实施者提供另外的指导。术语的任何使用的范围或含义将根据使用该术语的具体上下文而显而易见。
就其所有的语法形式和拼写变化形式而论的“同源的”是指两种蛋白之间的关系,所述蛋白具有“共同的进化来源”,包括来自相同的生物物种的超家族的蛋白,以及来自不同生物物种的同源蛋白。这种蛋白(和它们的编码核酸)具有序列同源性,如通过它们的序列相似性所反映的,无论是在百分比同一性方面,还是通过特定残基或基序和保守位置的存在。然而,在通常使用中和在本申请中,术语“同源的”当被副词诸如“高度地”修饰时,可以指序列相似性,且可能或可能不涉及共同的进化来源。
就其所有的语法形式而论的术语“序列相似性”是指核酸或氨基酸序列之间同一性或一致性的程度,所述序列可能或可能不共有共同的进化来源。
相对于参考多肽(或核苷酸)序列的“百分比(%)序列同一性”被定义为在比对序列和如果需要,引入缺口以实现最大百分比序列同一性,且不把任何保守取代看做序列同一性的一部分后,在候选序列中与在参考多肽(核苷酸)序列中氨基酸残基(或核酸)相同的氨基酸残基(或核酸)的百分数。为了确定百分比氨基酸序列同一性起见的比对可以在本领域的技能范围内的各种方式实现,例如,使用可公开获得的计算机软件,如blast、blast-2、align或megalign(dnastar)软件。本领域技术人员可确定合适的用于比对序列的参数,包括在所比较的序列的整个长度上实现最大比对所需的任何算法。然而,对本文来说,%氨基酸(核酸)序列同一性值使用序列比较计算机程序align-2产生。align-2序列比较计算机程序由genentech,inc.设计,且源代码已同用户文件一道提交至u.s.copyrightoffice,washingtond.c.,20559,在那里它注册为u.s.copyrightregistrationno.txu510087。align-2程序可公开获得自genentech,inc.,southsanfrancisco,calif.,或可从源代码编译。align-2程序应经编译以在unix操作系统上使用,包括digitalunixv4.0d。所有的序列比较参数由align-2程序设置,并且不改变。
就其所有语法形式而论的“激动”是指活化蛋白和/或基因(例如,通过活化或放大蛋白的基因表达或通过诱导失活的蛋白进入活性状态)、或增加蛋白和/或基因的活性的过程。
就其所有语法形式而论的“拮抗”是指抑制蛋白和/或基因(例如,通过抑制或降低蛋白的基因表达或通过诱导活性蛋白进入失活状态)、或降低蛋白和/或基因的活性的过程。
在整个说明书和权利要求书全文中结合数值使用的术语“约”和“近似”表示本领域技术人员熟悉和可接受的准确度的区间。通常,这种准确度区间是±10%。可选地和特别是在生物学系统中,术语“约”和“近似”可意指在给定值的一个数量级内的值,优选地≤5倍,和更优选地≤2倍。
本文公开的数值范围包括定义该范围的数字。
术语“一个/种(a)”和“一个/种(an)”包括复数指代物,除非使用该术语的上下文明确地另外指明。术语“一个/种(a)”(或“一个/种(an)”)以及术语“一个/种或多个/种”和“至少一个/种”在本文中可互换使用。此外,本文使用的“和/或”应被认为具体公开了两个/种或更多个/种指定的特征或组分的每一个/种,含或不含另一个特征或组分。因此,在本文的短语如“a和/或b”中使用的术语“和/或”意图包括“a和b”、“a或b”、“a”(单独)和“b”(单独)。同样地,在短语如“a、b和/或c”中使用的术语“和/或”意图包括以下方面的每一个:a、b和c;a、b或c;a或c;a或b;b或c;a和c;a和b;b和c;a(单独);b(单独);和c(单独)。
在整个说明书中,词语“包含(comprise)”或变化形式如“包含(comprises)”或“包含(comprising)”将被理解为意思是包括所述的整体(integer)或整体组,但不排除任何其它整体或整体组。
2.actriib拮抗剂
部分地,本公开内容涉及发现actriib拮抗剂(抑制剂)可以用于治疗骨髓纤维化患者,特别是改善疾病的各种并发症,包括例如脾肿大、髓外造血和纤维化。特别地,本文呈现的数据显示,gdf捕获物多肽在骨髓纤维化的jak2v617f模型中减少脾肿大、髓外造血和纤维化。虽然可溶性gdf捕获物多肽可通过actriib拮抗作用以外的机制影响骨髓纤维化[例如,gdf11、gdf8、激活蛋白b、bmp6、gdf3和bmp10中的一种或多种的抑制可为药剂抑制一系列其它因子的活性的趋势的指示物,所述其它因子可能包括tgf-β超家族的其它成员,并且这种集体抑制可导致对例如骨髓纤维化的期望效应],但本公开内容证明可基于actriib拮抗作用选择希望的治疗剂。因此,虽然不希望受特定作用机制的束缚,但预期其它actriib拮抗剂[例如,actriib受体的拮抗剂,一种或多种actriib结合配体(例如,gdf11、gdf8、激活蛋白、bmp6、gdf3和bmp10)的拮抗剂,一种或多种i型受体(例如,alk4、alk5和/或alk7)的拮抗剂,一种或多种共同受体的拮抗剂,一种或多种actriib下游信号传导组分(例如,smads)的拮抗剂,或这些拮抗剂的组合]将用于治疗骨髓纤维化,特别是用于治疗或预防各种骨髓纤维化相关的并发症(例如,脾肿大、髓外造血和纤维化)。此类药剂在本文中统称为“actriib拮抗剂”或“actriib抑制剂”。
a.actriib多肽及其变体
在某些方面,本公开内容涉及actriib多肽及其变体(例如,gdf捕获物)。特别地,本公开内容提供了单独或与一种或多种另外的支持疗法组合应用actriib多肽治疗骨髓纤维化、特别是治疗或预防骨髓纤维化的一种或多种并发症(例如,脾肿大、髓外造血、贫血和纤维化)和/或用janus激酶抑制剂治疗的患者的方法。如本文所用的,术语“actriib”是指来自任何物种的激活蛋白受体iib型(actriib)蛋白家族,和通过诱变或其它修饰衍生自这种actriib蛋白的变体。本文提及actriib应理解为提及任何一种目前鉴定的形式。actriib家族的成员通常是跨膜蛋白,其由包含富含半胱氨酸的区域的配体-结合细胞外结构域、跨膜结构域和具有预测的丝氨酸/苏氨酸激酶活性的胞质结构域构成。
术语“actriib多肽”包括包含actriib家族成员的任何天然存在的多肽以及其保留有用活性的任何变体(包括突变体、片段、融合物和肽模拟物(peptidomimetic)形式)的多肽。这种变体actriib多肽的实例在整个本公开内容中以及国际专利申请公开号wo2006/012627和wo2008/097541(其整体引入本文作为参考)中提供。本文所述的所有actriib-相关多肽的氨基酸编号基于下文提供的人actriib前体蛋白序列(seqidno:1)的编号,除非另外特别指出。
人actriib前体蛋白序列如下:
信号肽用单下划线表示;细胞外结构域以粗体表示;且潜在的内源n-连接的糖基化位点用双下划线表示。
加工的(成熟)细胞外actriib多肽序列如下:
在一些实施方案中,可以产生具有在n-端的“sgr…”序列的蛋白。细胞外结构域的c-端“尾”通过单下划线表示。“尾”缺失的序列(δ15序列)如下:
在seqidno:1的位置64处具有丙氨酸(a64)的actriib的形式也报道于文献中[hilden等(1994)blood,83(8):2163-2170]。申请人已经确定,包含具有a64取代的actriib的细胞外结构域的actriib-fc融合蛋白具有对激活蛋白和gdf11相对低的亲和力。对比起来,在位置64处具有精氨酸(r64)的相同的actriib-fc融合蛋白具有对激活蛋白和gdf11的低纳摩尔至高皮摩尔范围的亲和力。因此,在本公开内容中,具有r64的序列用作人actriib的“野生型”参考序列。
在位置64处具有丙氨酸的actriib的形式如下:
信号肽通过单下划线表示,且细胞外结构域通过粗体表示。
可选的a64形式的加工的(成熟)细胞外actriib多肽序列如下:
在一些实施方案中,可以产生具有在n-端的“sgr…”序列的蛋白。细胞外结构域的c-端“尾”通过单下划线表示。“尾”缺失的序列(δ15序列)如下:
编码人actriib前体蛋白的核酸序列在下文显示(seqidno:7),由genbank参考序列nm_001106.3的核苷酸25-1560组成,其编码actriib前体的氨基酸1-513。所示的序列提供位置64处的精氨酸,且可经修饰以代之以提供丙氨酸。信号序列加下划线。
编码加工的细胞外人actriib多肽的核酸序列如下(seqidno:8)。
所示的序列提供位置64处的精氨酸,且可被修饰以代之以提供丙氨酸。
人actriib细胞外结构域和人actriia细胞外结构域的氨基酸序列比对在图1中图解说明。该比对显示了两种受体内被认为直接接触actrii配体的氨基酸残基。例如,复合actrii结构表明actriib-配体结合袋部分地由残基y31、n33、n35、l38至t41、e47、e50、q53至k55、l57、h58、y60、s62、k74、w78至n83、y85、r87、a92和e94至f101定义。在这些位置,预期保守突变将是耐受的。
此外,actriib通常在脊椎动物中是充分保守的,且一大段细胞外结构域完全保守。例如,图2描绘人actriib细胞外结构域与各种actriib直向同源物相比的多重序列比对。许多结合actriib的配体也是高度保守的。因此,根据这些比对,可能预测配体-结合结构域内对于正常的actriib-配体结合活性重要的关键氨基酸位置,以及预测可能在不显著改变正常的actriib-配体结合活性的情况下耐受取代的氨基酸位置。因此,根据本文公开的方法有用的活性的人actriib变体多肽可以包括来自另一种脊椎动物actriib的序列的相应位置的一个或多个氨基酸,或可以包括类似于人或其它脊椎动物序列中的残基的残基。
不意图进行限制,以下实例举例说明这种定义活性actriib变体的方法。人细胞外结构域(seqidno:2)中的l46在爪蟾属(xenopus)actriib(seqidno:42)中是缬氨酸,和因此该位置可被改变和任选地可被改变为另一疏水残基,如v、i或f或非极性残基如a。在人细胞外结构域中的e52在爪蟾属中是k,表明该位点可耐受多种变化,包括极性残基如e、d、k、r、h、s、t、p、g、y和可能地a。在人细胞外结构域中的t93在爪蟾属中是k,表明在该位置处广泛的结构变异是耐受的,且极性残基是有利的,如s、k、r、e、d、h、g、p、g和y。在人细胞外结构域中的f108在爪蟾属中是y,且因此y或其它疏水基团如i、v或l应是耐受的。在人细胞外结构域中的e111在爪蟾属中是k,表明带电荷残基在该位置处将是耐受的,包括d、r、k和h,以及q和n。在人细胞外结构域中的r112在爪蟾属中是k,表明碱性残基在该位置处是耐受的,包括r和h。人细胞外结构域的位置119处的a相对地保守性差,且在啮齿类动物中作为p(seqidnos:37和39)和在爪蟾属中作为v出现,因此基本上任何氨基酸在该位置处都应该是耐受的。
此外,actrii蛋白质在结构/功能特征方面、特别是在配体结合方面已在本领域中得到表征[attisano等(1992)cell68(1):97-108;greenwald等(1999)naturestructuralbiology6(1):18-22;allendorph等(2006)pnas103(20:7643-7648;thompson等(2003)theembojournal22(7):1555-1566;以及美国专利号:7,709,605、7,612,041和7,842,663]。除了本文的教导之外,这些参考文献提供了关于如何产生保留一种或多种所需活性(例如配体结合活性)的actrii变体的充分指导。
例如,称为三指毒素折叠的定义结构基序对于i型和ii型受体的配体结合是重要的,并且由位于每个单体受体的细胞外结构域内的不同位置的保守半胱氨酸残基形成[greenwald等(1999)natstructbiol6:18-22;和hinck(2012)febslett586:1860-1870]。因此,由这些保守半胱氨酸的最外侧界定的人actriib的核心配体结合结构域对应于seqidno:1的位置29-109(actriib前体)。因此,在这些半胱氨酸分界的核心序列侧翼的结构上较不有序的氨基酸可以在n末端被截短约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27或28个残基,和/或在c末端被截短约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个残基,而不必改变配体结合。用于n-末端和/或c-末端截短的示例性actriib细胞外结构域包括seqidno:2、3、5和6。
attisano等显示actriib细胞外结构域c末端的脯氨酸结的缺失降低受体对激活蛋白的亲和力。含有目前seqidno:1的氨基酸20-119的actriib-fc融合蛋白“actriib(20-119)-fc”相对于actriib(20-134)-fc具有降低的与gdf11和激活蛋白的结合,actriib(20-134)-fc包括脯氨酸结区域和完整的近膜结构域(参见,例如,美国专利号7,842,663)。然而,相对于野生型,actriib(20-129)-fc蛋白保留相似但略微降低的活性,即使脯氨酸结区域被破坏。因此,在氨基酸134、133、132、131、130和129(相对于seqidno:1)处停止的actriib细胞外结构域都预期是活性的,但在134或133处停止的构建体可能是最活跃的。类似地,不预期残基129-134(相对于seqidno:1)的任一处的突变通过大的边缘(margins)改变配体结合亲和力。为了支持这一点,本领域已知p129和p130的突变(相对于seqidno:1)基本上不减少配体结合。因此,本公开内容的actriib多肽可早在氨基酸109(最终半胱氨酸)结束,然而,在109和119或在109和119之间(例如,109、110、111、112、113、114、115、116、117、118或119)形成结束预期具有降低的配体结合。氨基酸119(相对于本发明的seqidno:1)保守性差,且因此容易被改变或截短。在128(相对于seqidno:1)处或更后终止的actriib多肽应保留配体-结合活性。相对于seqidno:1在119和127处或其之间(例如,119、120、121、122、123、124、125、126或127)终止的actriib多肽将具有中等结合能力。取决于临床或实验背景,任何这些形式对于使用都可能是期望的。
在actriib的n-末端,预期在氨基酸29处或之前(相对于seqidno:1)开始的蛋白将保留配体-结合活性。氨基酸29表示最初的半胱氨酸。位置24处(相对于seqidno:1)的丙氨酸至天冬酰胺突变在基本上不影响配体结合的情况下引入n-连接的糖基化序列[美国专利号7,842,663]。这证实了信号切割肽和半胱氨酸交联区之间的区域(对应于氨基酸20-29)中的突变是良好耐受的。具体而言,在位置20、21、22、23和24处(相对于seqidno:1)开始的actriib多肽应保留一般的配体-结合活性,且在位置25、26、27、28和29处(相对于seqidno:1)开始的actriib多肽也被预期保留配体-结合活性。已经证实,例如,美国专利号7,842,663,令人惊讶地,在22、23、24或25处开始的actriib构建体将具有最大活性。
合起来,actriib的活性部分(例如,配体-结合部分)的通式包含seqidno:1的氨基酸29-109。因此,actriib多肽可以例如包含与actriib的部分具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,基本上由其组成,或由其组成,所述actriib的部分开始于对应于seqidno:1的氨基酸20-29中任一个的残基(例如,开始于氨基酸20、21、22、23、24、25、26、27、28或29中任一个)且结束于对应于seqidno:1的任一个氨基酸109-134的位置(例如,结束于氨基酸109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133或134中任一个)。其它实例包括这样的多肽,其开始于seqidno:1的20-29(例如,位置20、21、22、23、24、25、26、27、28或29中任一个)或21-29(例如,位置21、22、23、24、25、26、27、28或29中任一个)的位置且结束于seqidno:1的119-134(例如,位置119、120、121、122、123、124、125、126、127、128、129、130、131、132、133或134中任一个)、119-133(例如,位置119、120、121、122、123、124、125、126、127、128、129、130、131、132或133中任一个)、129-134(例如,位置129、130、131、132、133或134中任一个)或129-133(例如,位置129、130、131、132或133中任一个)的位置。其它实例包括这样的构建体,其开始于seqidno:1的20-24(例如,位置20、21、22、23或24中任一个)、21-24(例如,位置21、22、23或24中任一个)或22-25(例如,位置22、22、23或25中任一个)的位置且结束于seqidno:1的109-134(例如,位置109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133或134中任一个)、119-134(例如,位置119、120、121、122、123、124、125、126、127、128、129、130、131、132、133或134中任一个)或129-134(例如,位置129、130、131、132、133或134中任一个)的位置。还预期在这些范围内的变体,特别是与seqidno:1的相应部分具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的那些。
本文所述的变异可以各种方式组合。在一些实施方案中,actriib变体包含在配体-结合袋中仅仅1、2、5、6、7、8、9、10或15个保守氨基酸变化,和在配体-结合袋的位置40、53、55、74、79和/或82处的0、1或多个非保守改变。结合袋外的位点(在所述位点处变异性可特别良好耐受)包括细胞外结构域的氨基和羧基末端(如上文所指出的),和位置42-46和65-73(相对于seqidno:1)。在位置65处的天冬酰胺至丙氨酸的改变(n65a)实质上改善r64背景中的配体结合,并且因此预期对r64背景中的配体结合没有有害作用[美国专利号7,842,663]。这种改变可能消除a64背景中n65的糖基化,因此证明该区域中显著改变可能是耐受的。尽管r64a变化耐受性差,但r64k是良好耐受的,且因此另一碱性残基诸如h可在位置64处耐受[美国专利号7,842,663]。另外,本领域描述的诱变程序的结果表明,存在经常对于保守是有利的actriib中的氨基酸位置。相对于seqidno:1,这些包括位置80(酸性或疏水氨基酸)、位置78(疏水的,且特别是色氨酸)、位置37(酸性的,且特别是天冬氨酸或谷氨酸)、位置56(碱性氨基酸)、位置60(疏水氨基酸,特别是苯丙氨酸或酪氨酸)。因此,本公开内容提供了在actriib多肽中可能是保守的氨基酸构架。可能期望保守的其它位置如下:位置52(酸性氨基酸)、位置55(碱性氨基酸)、位置81(酸性)、98(极性或带电荷的,特别是e、d、r或k),全部相对于seqidno:1。
先前已经证明,将进一步的n-连接的糖基化位点(n-x-s/t)添加至actriib细胞外结构域被良好耐受(参见,例如,美国专利号7,842,663)。因此,n-x-s/t序列通常可以在本公开内容的actriib多肽中的图1中限定的配体结合袋外部的位置引入。用于引入非内源性n-x-s/t序列的特别合适的位点包括氨基酸20-29、20-24、22-25、109-134、120-134或129-134(相对于seqidno:1)。还可以将n-x-s/t序列引入actriib序列和fc结构域或其它融合组分之间的接头中。通过在就预先存在的s或t而言的正确位置引入n,或者通过在对应于预先存在的n的位置处引入s或t,可以最小的努力引入这种位点。因此,将产生n-连接的糖基化位点的期望的改变是:a24n、r64n、s67n(可能与n65a改变组合)、e105n、r112n、g120n、e123n、p129n、a132n、r112s和r112t(相对于seqidno:1)。由于糖基化提供的保护,任何预测被糖基化的s都可以在不产生免疫原性位点的情况下改变为t。同样地,预测被糖基化的任何t都可以改变为s。因此,预期改变s67t和s44t(相对于seqidno:1)。同样地,在a24n变体中,可以使用s26t改变。因此,本公开内容的actriib多肽可以是具有一个或多个如上所述的额外的非内源性n-连接的糖基化共有序列的变体。
在某些实施方案中,本公开内容涉及包含至少一种actriib多肽(其包括其片段、功能变体和修饰形式)的actriib拮抗剂。优选地,用于根据本公开内容应用的actriib多肽是可溶性的(例如,actriib的细胞外结构域)。在一些实施方案中,用于根据本公开内容应用的actriib多肽抑制(拮抗)一种或多种tdf-β超家族配体[例如,gdf11、gdf8、激活蛋白(激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白e)、bmp6、gdf3和/或bmp10的活性(例如,smad信号传导)。在一些实施方案中,用于根据本公开内容应用的actriib多肽结合一种或多种tdf-β超家族配体[例如,gdf11、gdf8、激活蛋白(激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、激活蛋白e)、bmp6、gdf3、bmp10和/或bmp9]。在一些实施方案中,本公开内容的actriib多肽包含与actriib的部分具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,基本上由其组成,或由其组成,所述actriib的部分开始于对应于seqidno:1的氨基酸20-29的残基(例如,开始于氨基酸20、21、22、23、24、25、26、27、28或29中任一个)和结束于对应于seqidno:1的氨基酸109-134的位置(例如,结束于氨基酸109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133或134中任一个)。在一些实施方案中,本公开内容的actriib多肽包含与seqidno:1的氨基酸29-109具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,由其组成,或基本上由其组成。在一些实施方案中,本公开内容的actriib多肽包含与seqidno:1的氨基酸29-109具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,由其组成或基本上由其组成,其中对应于seqidno:1的l79的位置是酸性氨基酸(天然存在的酸性氨基酸d和e或人工酸性氨基酸)。在某些优选实施方案中,本公开内容的actriib多肽包含与seqidno:1的氨基酸25-131具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,由其组成或基本上由其组成。在某些优选实施方案中,本公开内容的actriib多肽包含与seqidno:1的氨基酸25-131具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列,由其组成或基本上由其组成,其中对应于seqidno:1的l79的位置是酸性氨基酸。在一些实施方案中,本公开内容的actriib多肽包含与seqidno:1、2、3、4、5、6、24、25、28、29、30、31、33、34、35、45、50、53、54和58中的任一个的氨基酸序列具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、97%、98%、99%或100%同一性的氨基酸序列,由其组成或基本上由其组成。在一些实施方案中,本公开内容的actriib多肽包含与seqidno:1、2、3、4、5、6、24、25、28、29、30、31、33、34、35、45、50、53、54和58中的任一个的氨基酸序列具有至少70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、97%、98%、99%或100%同一性的氨基酸序列,由其组成或基本上由其组成,其中对应于seqidno:1的l79的位置是酸性氨基酸。在一些实施方案中,本公开内容的actriib多肽包含至少一种actriib多肽,其中对应于seqidno:1的l79的位置不是酸性氨基酸(即,不是天然存在的酸性氨基酸d或e或人工酸性氨基酸残基)。
在某些方面,本公开内容涉及gdf捕获物多肽(也称为“gdf捕获物”)。在一些实施方案中,本公开内容的gdf捕获物是在actriib多肽(例如,“野生型”或未修饰的actrii多肽)的细胞外结构域(也称为配体结合结构域)中包含一个或多个突变(例如,氨基酸添加、缺失、取代和其组合)的变体actriib多肽,从而使得变体actriib多肽与相应的野生型actriib多肽相比具有一种或多种改变的配体结合活性。在优选实施方案中,本公开内容的gdf捕获物多肽保留至少一种与相应的野生型actriib多肽类似的活性。例如,优选的gdf捕获物结合并抑制(例如拮抗)gdf11和/或gdf8的功能。在一些实施方案中,本公开内容的gdf捕获物进一步结合并抑制tdf-β超家族的配体中的一种或多种。因此,本公开内容提供了对一种或多种actriib配体具有改变的结合特异性的gdf捕获物多肽。
为了举例说明,可以选择一种或多种突变,相对于一种或多种actriib结合配体如激活蛋白(激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、和/或激活蛋白e)、特别是激活蛋白a,其增加改变的配体结合结构域对gdf11和/或gdf8的选择性。任选地,相对于野生型配体结合结构域的比率,改变的配体结合结构域对激活蛋白结合的kd与对gdf11和/或gdf8结合的kd的比率为至少2-、5-、10-、20、50-、100-或甚至1000-倍。任选地,相对于野生型配体结合结构域,改变的配体结合结构域对抑制激活蛋白的ic50与对抑制gdf11和/或gdf8的ic50的比率为至少2-、5-、10-、20-、50-、100-或甚至1000-倍。任选地,改变的配体结合结构域抑制gdf11和/或gdf8的ic50为抑制激活蛋白(例如,激活蛋白a)的ic50的至多1/2、1/5、1/10、1/20、1/50、1/100或甚至1/1000。
在某些优选的实施方案中,本公开内容的gdf捕获物被设计为优先结合gdf11和/或gdf8(也称为肌肉生长抑制素)。任选地,gdf11和/或gdf8结合捕获物可进一步结合激活蛋白b。任选地,gdf11和/或gdf8结合捕获物可进一步结合bmp6。任选地,gdf11和/或gdf8结合捕获物可进一步结合bmp10。任选地,gdf11和/或gdf8结合捕获物可进一步结合激活蛋白b和bmp6。在某些实施方案中,例如,与野生型actriib多肽相比,本公开内容的gdf捕获物对激活蛋白(例如,激活蛋白a、激活蛋白a/b、激活蛋白b、激活蛋白c、激活蛋白e)具有减少的结合亲和力。在某些优选的实施方案中,本公开内容的gdf捕获物多肽对激活蛋白a具有减少的结合亲和力。
actriib蛋白的氨基酸残基(例如,e39、k55、y60、k74、w78、l79、d80和f101)在actriib配体结合袋中且有助于介导与其配体(包括例如激活蛋白a、gdf11和gdf8)结合。因此,本公开内容提供了gdf捕获物多肽,其包含actriib受体的改变的配体结合结构域(例如,gdf8/gdf11结合结构域),其在那些氨基酸残基处包含一个或多个突变。
作为具体实例,actriib的配体结合结构域的带正电荷的氨基酸残基asp(d80)可以突变为不同的氨基酸残基,以产生优先结合gdf8而不是激活蛋白的gdf捕获物多肽。优选地,将相对于seqidno:1的d80残基改变为选自以下的氨基酸残基:不带电荷的氨基酸残基、负电荷氨基酸残基和疏水性氨基酸残基。作为进一步的具体实例,可以改变seqidno:1的疏水残基l79以赋予改变的激活蛋白-gdf11/gdf8结合性质。例如,l79p取代比激活蛋白结合在更大程度上降低gdf11结合。相反,用酸性氨基酸[天冬氨酸或谷氨酸;l79d或l79e取代]置换l79大大降低激活蛋白a结合亲和力,同时保留gdf11结合亲和力。在示例性实施方案中,本文所述的方法利用gdf捕获物多肽,其为在对应于seqidno:1的位置79的位置处包含酸性氨基酸(例如,d或e)的变体actriib多肽,其任选地与一个或多个额外氨基酸取代、添加或缺失组合。
在一些实施方案中,本公开内容预期为了诸如增强治疗功效或稳定性(例如,贮存期限和对体内蛋白水解降解的抗性)的目的,通过修饰actriib多肽的结构来制备功能变体。变体可通过氨基酸取代、缺失、添加或其组合产生。例如,合理的是预期用异亮氨酸或缬氨酸独立置换亮氨酸、用谷氨酸独立置换天冬氨酸、用丝氨酸独立置换苏氨酸或用结构相关的氨基酸类似置换氨基酸(例如,保守突变)对所得分子的生物学活性将不具有较大影响。保守置换是在其侧链上相关的氨基酸家族内发生的那些。本公开内容的多肽的氨基酸序列中的变化是否导致功能同源物可通过评估变体多肽在细胞中以类似于野生型多肽的方式产生反应、或结合一种或多种tgf-β配体(包括例如bmp2、bmp2/7、bmp3、bmp4、bmp4/7、bmp5、bmp6、bmp7、bmp8a、bmp8b、bmp9、bmp10、gdf3、gdf5、gdf6/bmp13、gdf7、gdf8、gdf9b/bmp15、gdf11/bmp11、gdf15/mic1、tgf-β1、tgf-β2、tgf-β3、激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、nodal、神经胶质细胞衍生的神经营养因子(gdnf)、neurturin、artemin、persephin、mis和lefty)的能力容易地确定。
在某些实施方案中,本公开内容预期actriib多肽的特定突变以便改变多肽的糖基化。这种突变可经选择,以便引入或消除一个或多个糖基化位点,如o-连接或n-连接的糖基化位点。天冬酰胺-连接的糖基化识别位点通常包含三肽序列,天冬酰胺-x-苏氨酸或天冬酰胺-x-丝氨酸(其中“x”是任何氨基酸),其被合适的细胞糖基化酶特异性识别。还可通过添加一个或多个丝氨酸或苏氨酸残基至多肽的序列或通过对多肽的序列取代一个或多个丝氨酸或苏氨酸残基进行改变(对于o-连接的糖基化位点)。糖基化识别位点的第一或第三氨基酸位置的一个或两个处的多种氨基酸取代或缺失(和/或第二位置处的氨基酸缺失)导致在修饰的三肽序列处非-糖基化。增加多肽上的碳水化合物部分的数目的另一种方式是通过糖苷化学或酶促偶联至多肽。取决于使用的偶联模式,糖(一个或多个)可附着至:(a)精氨酸和组氨酸;(b)游离的羧基;(c)游离的巯基,如半胱氨酸的那些;(d)游离的羟基,如丝氨酸、苏氨酸或羟脯氨酸的那些;(e)芳族残基,如苯丙氨酸、酪氨酸或色氨酸的那些;或(f)谷氨酰胺的酰胺基。除去多肽上存在的一个或多个碳水化合物部分可经化学和/或酶促实现。化学去糖基化可牵涉例如,将多肽暴露于化合物三氟甲磺酸或等效的化合物。这种处理导致除了连接糖(n-乙酰葡糖胺或n-乙酰半乳糖胺)之外的大部分或所有的糖切割,同时使氨基酸序列保持完整。多肽上碳水化合物部分的酶促切割可通过使用多种内切和外切糖苷酶实现,如thotakura等[meth.enzymol.(1987)138:350]所述的。在合适的情况下,多肽的序列可依赖于使用的表达系统的类型进行调整,这是因为哺乳动物、酵母、昆虫和植物细胞都可引入可受所述肽的氨基酸序列影响的不同糖基化模式。通常,用于在人中使用的本公开内容的多肽可在提供正确糖基化的哺乳动物细胞系中表达,如hek293或cho细胞系,尽管其它哺乳动物表达细胞系预期也是有用的。
本公开内容进一步预期了产生actriib多肽的突变体、特别是组合突变体组,以及截短突变体的方法。组合突变体的库对于鉴定功能活性的(例如,tgf-β超家族配体结合)actriib序列尤其有用。筛选这种组合文库的目的可以是产生例如,具有改变的性质的多肽变体,如改变的药物代谢动力学或改变的配体结合。多种筛选测定在下文提供且这种测定可用于评价变体。例如,可筛选actriib变体结合一种或多种tgf-β超家族配体(例如,bmp2、bmp2/7、bmp3、bmp4、bmp4/7、bmp5、bmp6、bmp7、bmp8a、bmp8b、bmp9、bmp10、gdf3、gdf5、gdf6/bmp13、gdf7、gdf8、gdf9b/bmp15、gdf11/bmp11、gdf15/mic1、tgfβ1、tgfβ2、tgfβ3、激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白ac、nodal、神经胶质细胞衍生的神经营养因子(gdnf)、neurturin、artemin、persephin、mis和lefty)以阻止tgf-β超家族配体与tgf-β超家族受体的结合和/或干扰由tgf-β超家族配体引起的信号传导的能力。
actriib多肽的活性也可在基于细胞的测定或体内测定中测试。例如,可以评估actriib多肽对骨髓纤维化敏锐度中牵涉的基因的表达的影响。在需要的情况下,这可在一种或多种重组actrii配体蛋白(例如,bmp2、bmp2/7、bmp3、bmp4、bmp4/7、bmp5、bmp6、bmp7、bmp8a、bmp8b、bmp9、bmp10、gdf3、gdf5、gdf6/bmp13、gdf7、gdf8、gdf9b/bmp15、gdf11/bmp11、gdf15/mic1、tgf-β1、tgf-β2、tgfβ3、激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、nodal、神经胶质细胞衍生的神经营养因子(gdnf)、neurturin、artemin、persephin、mis和lefty)存在的情况下进行,且细胞可经转染,以便产生actriib多肽和任选地actriib配体。同样地,actriib多肽可施用于小鼠或其它动物,并且可使用本领域公认的方法评估对骨髓纤维化的影响。类似地,actriib多肽或其变体的活性可在血细胞前体细胞中测试对这些细胞的生长的任何影响,例如,通过如本文所述的测定和本领域众所周知的那些。smad-响应报道基因可在这种细胞系中用于监控对下游信号传导的影响。
可产生组合衍生的变体,相对于参考actriib多肽,其具有增加的选择性或通常增加的效力。这种变体,当从重组dna构建体表达时,可用于基因治疗规程中。同样地,诱变可产生变体,其具有显著不同于相应的未修饰的actriib多肽的细胞内半衰期。例如,可以使改变的蛋白变得对蛋白水解降解或导致未修饰多肽的破坏或以其它方式失活的其它细胞过程更稳定或较不稳定。这种变体和编码它们的基因可通过调节多肽的半衰期用于改变多肽复合体水平。例如,短的半衰期可产生更短暂的生物学作用,并且当诱导型表达系统的一部分时,可允许更紧密控制细胞内的重组多肽复合体水平。在fc融合蛋白中,可在接头(如果有的话)和/或fc部分中进行突变以改变actriib多肽的半衰期。
组合文库可通过编码多肽文库的简并基因文库产生,所述多肽各自至少包括潜在的actriib序列的一部分。例如,合成的寡核苷酸的混合物可经酶促连接至基因序列,从而使得潜在的actriib编码核苷酸序列的简并组可作为个别多肽表达,或者可选地,作为较大的融合蛋白组表达(例如,对于噬菌体展示)。
存在许多可自简并寡核苷酸序列产生潜在的同源物的文库的方式。简并基因序列的化学合成可在自动dna合成仪中进行,且合成的基因然后可连接至合适的载体用于表达。简并寡核苷酸的合成是本领域众所周知的[narang,sa(1983)tetrahedron39:3;itakura等(1981)recombinantdna,proc.3rdclevelandsympos.macromolecules,ed.agwalton,amsterdam:elsevierpp273-289;itakura等(1984)annu.rev.biochem.53:323;itakura等(1984)science198:1056;和ike等(1983)nucleicacidres.11:477]。这种技术已经用于其它蛋白的定向进化[scott等,(1990)science249:386-390;roberts等(1992)pnasusa89:2429-2433;devlin等(1990)science249:404-406;cwirla等,(1990)pnasusa87:6378-6382;以及美国专利号:5,223,409、5,198,346和5,096,815]。
另一方面,其它形式的诱变可用于产生组合文库。例如,本公开内容的actriib多肽可通过使用例如丙氨酸分区诱变进行筛选[ruf等(1994)biochemistry33:1565-1572;wang等(1994)j.biol.chem.269:3095-3099;balint等(1993)gene137:109-118;grodberg等(1993)eur.j.biochem.218:597-601;nagashima等(1993)j.biol.chem.268:2888-2892;lowman等(1991)biochemistry30:10832-10838;和cunningham等(1989)science244:1081-1085],通过接头分区诱变[gustin等(1993)virology193:653-660;和brown等(1992)mol.cellbiol.12:2644-2652;mcknight等(1982)science232:316],通过饱和诱变[meyers等,(1986)science232:613];通过pcr诱变[leung等(1989)methodcellmolbiol1:11-19];或通过随机诱变,包括化学诱变[miller等(1992)ashortcourseinbacterialgenetics,cshlpress,coldspringharbor,ny;和greener等(1994)strategiesinmolbiol7:32-34],从文库产生和分离。接头分区诱变,特别是在组合的背景下,是一种用于鉴定截短(生物活性)形式的actriib多肽的有吸引力的方法。
本领域已知用于筛选通过点突变和截短制备的组合文库的基因产物,且在这方面,用于筛选cdna文库的具有特定性质的基因产物的广泛范围的技术。这种技术将通常可适用于通过actriib多肽的组合诱变产生的基因文库的快速筛选。用于筛选大基因文库的最广泛使用的技术一般包括克隆基因文库至可复制的表达载体,用所得载体文库转化合适的细胞,且在其中期望活性的检测促进相对容易地分离编码其产物被检测的基因的载体的条件下表达组合基因。优选的测定包括tgf-β配体(例如,bmp2、bmp2/7、bmp3、bmp4、bmp4/7、bmp5、bmp6、bmp7、bmp8a、bmp8b、bmp9、bmp10、gdf3、gdf5、gdf6/bmp13、gdf7、gdf8、gdf9b/bmp15、gdf11/bmp11、gdf15/mic1、tgf-β1、tgf-β2、tgf-β3、激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、nodal、神经胶质细胞衍生的神经营养因子(gdnf)、neurturin、artemin、persephin、mis和lefty)结合测定和/或tgf-β配体-介导的细胞信号传导测定。
如本领域技术人员将认识到的,本文所述的大多数所述突变、变体或修饰可以在核酸水平上进行,或者在一些情况下,通过翻译后修饰或化学合成进行。这种技术是本领域中众所周知的,并且其中一些在本文中描述。部分地,本公开内容鉴定了actriib多肽的功能活性部分(片段)和变体,其可用作在本文所述发明的范围内生成和使用其它变体actriib多肽的指导。
在某些实施方案中,本公开内容的actriib多肽的功能活性片段可以通过筛选从编码actriib多肽的核酸(例如,seqidnos:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62)的相应片段重组产生的多肽来获得。此外,可以使用本领域已知的技术如常规的merrifield固相f-moc或t-boc化学而化学合成片段。可以产生(重组或通过化学合成)片段并进行测试以鉴定可以起actrii受体和/或一种或多种配体(例如,bmp2、bmp2/7、bmp3、bmp4、bmp4/7、bmp5、bmp6、bmp7、bmp8a、bmp8b、bmp9、bmp10、gdf3、gdf5、gdf6/bmp13、gdf7、gdf8、gdf9b/bmp15、gdf11/bmp11、gdf15/mic1、tgf-β1、tgf-β2、tgf-β3、激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、nodal、神经胶质细胞衍生的神经营养因子(gdnf)、neurturin、artemin、persephin、mis和lefty)的拮抗剂(抑制剂)作用的那些肽基片段。
在某些实施方案中,除了在actriib多肽中天然存在的任何修饰之外,本公开内容的actriib多肽可进一步包含翻译后修饰。这种修饰包括但不限于,乙酰化、羧基化、糖基化、磷酸化、脂质化(lipidation)和酰化。作为结果,actriib多肽可含有非-氨基酸元件,诸如聚乙二醇、脂质、多糖或单糖和磷酸酯。这种非-氨基酸元件对配体捕获物多肽的功能性的影响可如本文对于其它actriib变体所述进行测试。当本公开内容的多肽在细胞中通过切割新生形式的多肽产生时,翻译后加工也可能对于蛋白的正确折叠和/或功能是重要的。不同的细胞(例如,cho、hela、mdck、293、wi38、nih-3t3或hek293)具有用于这种翻译后活性的特定细胞机器和特征性机制,且可经选择以确保actrii多肽的正确修饰和加工。
在某些方面,本公开内容的actriib多肽包括具有actriib多肽的至少一部分(结构域)和一个或多个异源部分(结构域)的融合蛋白。这种融合结构域的众所周知的实例包括但不限于多组氨酸、glu-glu、谷胱甘肽s-转移酶(gst)、硫氧还蛋白、a蛋白、g蛋白、免疫球蛋白重链恒定区(fc)、麦芽糖结合蛋白(mbp)或人血清白蛋白。可以选择融合结构域以便赋予期望的性质。例如,一些融合结构域对于通过亲和层析分离融合蛋白特别有用。为了亲和纯化起见,使用亲和层析的相关基质,如谷胱甘肽-、淀粉酶-和镍-或钴-缀合的树脂。许多这种基质可以“试剂盒”形式获得,如pharmaciagst纯化系统和与(his6)融合配偶体一起有用的qiaexpresstm系统(qiagen)。作为另一实例,融合结构域可经选择,以便促进actriib多肽的检测。这种检测结构域的实例包括各种荧光蛋白(例如,gfp)以及“表位标签”,其通常是针对其可利用特异性抗体的短的肽序列。针对其可容易利用特异性单克隆抗体的众所周知的表位标签包括flag、流感病毒血细胞凝集素(ha)和c-myc标签。在一些情况下,融合结构域具有蛋白酶切割位点,如对于因子xa或凝血酶,其允许相关的蛋白酶部分地消化融合蛋白,且由此从其中释放重组蛋白。释放的蛋白然后可通过随后的层析分离与融合结构域分离。可以选择的其它类型的融合结构域包括多聚化(例如,二聚化、四聚化)结构域和功能结构域(其赋予额外的生物学功能),包括例如来自免疫球蛋白的恒定结构域(例如,fc结构域)。
在某些方面,本公开内容的actriib多肽含有一种或多种能够“稳定化”多肽的修饰。“稳定化”意指增加体外半衰期、血清半衰期的任何物质,无论这是由于药剂的破坏减少、肾脏清除率降低还是其它药物代谢动力学作用。例如,这种修饰增加多肽的贮存期限、增加多肽的循环半衰期和/或减少多肽的蛋白水解降解。这种稳定修饰包括但不限于,融合蛋白(包括例如,包含actriib多肽结构域和稳定剂结构域的融合蛋白)、糖基化位点的修饰(包括例如,添加糖基化位点至本公开内容的多肽)和碳水化合物部分的修饰(包括例如,从本公开内容的多肽除去碳水化合物部分)。如本文所用的,术语“稳定剂结构域”不仅是指在融合蛋白的情况下的融合结构域(例如,免疫球蛋白fc结构域),而且还包括非蛋白修饰,如碳水化合物部分或非蛋白部分,如聚乙二醇。在某些优选实施方案中,actriib多肽与稳定化多肽的异源结构域(“稳定剂”结构域)、优选增加多肽体内稳定性的异源结构域融合。已知具有免疫球蛋白的恒定结构域(例如,fc结构域)的融合物赋予广泛范围的蛋白期望的药物代谢动力学性质。同样地,与人血清白蛋白的融合可以赋予期望的性质。
可用于人igg1的fc部分(g1fc)的天然氨基酸序列的实例在下文显示(seqidno:9)。虚下划线表示铰链区,且实下划线表示具有天然存在的变体的位置。部分地,本公开内容提供了包含与seqidno:9具有70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列、基本上由其组成或由其组成的多肽。根据seqidno:9(参见uniprotp01857)中使用的编号系统,g1fc中天然存在的变体将包括e134d和m136l。
任选地,igg1fc结构域在残基如asp-265、赖氨酸322和asn-434处具有一个或多个突变。在某些情况下,相对于野生型fc结构域,具有这些突变中的一个或多个(例如,asp-265突变)的突变体igg1fc结构域具有减少的结合fcγ受体的能力。在其它情况下,相对于野生型igg1fc结构域,具有这些突变中的一个或多个(例如,asn-434突变)的突变体fc结构域具有增加的结合mhci类相关fc-受体(fcrn)的能力。
可用于人igg2的fc部分(g2fc)的天然氨基酸序列的实例在下文显示(seqidno:10)。虚下划线表示铰链区,且双下划线表示其中在序列(根据uniprotp01859)中存在数据库冲突的位置。部分地,本公开内容提供了包含与seqidno:10具有70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列、基本上由其组成或由其组成的多肽。
可用于人igg3的fc部分(g3fc)的氨基酸序列的两个实例在下文显示。g3fc中的铰链区可最多达其它fc链中的4倍长,且含有三个相同的15-残基区段,前面是类似的17-残基区段。在下文显示的第一g3fc序列(seqidno:11)含有由单一15-残基区段组成的短的铰链区,而第二g3fc序列(seqidno:12)含有全长铰链区。在每种情况下,虚下划线表示铰链区,且实下划线表示根据uniprotp01859具有天然存在的变体的位置。部分地,本公开内容提供了包含与seqidno:11和12具有70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列、基本上由其组成或由其组成的多肽。
当转变为seqidno:11中使用的编号系统时,g3fc(例如,参见uniprotp01860)中的天然存在的变体包括e68q、p76l、e79q、y81f、d97n、n100d、t124a、s169n、s169del、f221y,且本公开内容提供了包含g3fc结构域的融合蛋白,所述结构域含有这些变异中的一种或多种。此外,人免疫球蛋白igg3基因(ighg3)显示特征在于不同的铰链长度的结构多态性[参见uniprotp01859]。具体地,变体wis缺乏大部分v区和所有的ch1区。除了铰链区中正常存在的位置11之外,其在位置7处具有额外的链间二硫键。变体zuc缺乏大部分v区、所有的ch1区和部分的铰链。变体omm可以代表等位基因形式或另一种γ链亚类。本公开内容提供了包含g3fc结构域的额外融合蛋白,所述结构域含有这些变体中的一种或多种。
可用于人igg4的fc部分(g4fc)的天然氨基酸序列的实例在下文显示(seqidno:13)。虚下划线表示铰链区。部分地,本公开内容提供了包含与seqidno:13具有70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列、基本上由其组成或由其组成的多肽。
相对于g1fc序列(seqidno:9),本文呈现了fc结构域中的多种人工改造的突变,且g2fc、g3fc和g4fc中的类似突变可衍生自在图11中它们与g1fc的比对。由于不等的铰链长度,基于同种型比对(图11)的类似的fc位置在seqidno:9、10、11、12和13中具有不同的氨基酸编号。还可理解,在由铰链、ch2和ch3区组成的免疫球蛋白序列(例如,seqidno:9、10、11、12和13)中给定的氨基酸位置将通过与当编号包含如uniprot数据库中那样整个igg1重链恒定结构域(由ch1、铰链、ch2和ch3区组成)时的相同位置不同的编号来鉴定。例如,在人g1fc序列(seqidno:9)、人igg1重链恒定结构域(uniprotp01857)和人igg1重链中选择的ch3位置之间的对应如下。
应理解,融合蛋白(例如,免疫球蛋白fc融合蛋白)的不同元件可以与期望功能性一致的任何方式排列。例如,actriib多肽结构域可位于异源结构域的c-末端,或者可选地,异源结构域可位于actriib多肽结构域的c-末端。actriib多肽结构域和异源结构域在融合蛋白中不需要相邻,且另外的结构域或氨基酸序列可包括在任一结构域的c-或n-末端或在结构域之间。
例如,actriib受体融合蛋白可包含如式a-b-c中所示的氨基酸序列。b部分对应于actriib多肽结构域。a和c部分可独立地是零、一个或超过一个氨基酸,且a和c部分两者当存在时对b都是异源的。a和/或c部分可通过接头序列附着至b部分。接头可以富含甘氨酸(例如,2-10、2-5、2-4、2-3个甘氨酸残基)或甘氨酸和脯氨酸残基,且可例如含有苏氨酸/丝氨酸和甘氨酸的单一序列,或苏氨酸/丝氨酸和/或甘氨酸的重复序列,例如,ggg(seqidno:14)、gggg(seqidno:15)、tgggg(seqidno:16)、sgggg(seqidno:17)、tggg(seqidno:18)、sggg(seqidno:19)或ggggs(seqidno:20)单现基因或重复序列。在某些实施方案中,actriib融合蛋白包含如式a-b-c中所示的氨基酸序列,其中a是前导(信号)序列,b由actriib多肽结构域组成,且c是增强体内稳定性、体内半衰期、摄取/施用、组织定位或分布、蛋白复合体形成和/或纯化的一种或多种的多肽部分。在某些实施方案中,actriib融合蛋白包含如式a-b-c中所示的氨基酸序列,其中a是tpa前导序列,b由actriib受体多肽结构域组成,且c是免疫球蛋白fc结构域。优选的融合蛋白包含seqidno:24、25、28、29、31、33、34、45、50、53和58中任一个所示的氨基酸序列。
在优选的实施方案中,待根据本文所述的方法使用的actriib多肽是分离的多肽。如本文所用的,分离的蛋白或多肽是已经与其天然环境的组分分开的蛋白或多肽。在一些实施方案中,本公开内容的多肽被纯化至大于95%、96%、97%、98%或99%纯度,如通过例如,电泳(例如,sds-page、等电点聚焦(ief)、毛细管电泳)或层析(例如,离子交换或反相hplc)所测定的。用于评估抗体纯度的方法是本领域众所周知的[参见,例如,flatman等,(2007)j.chromatogr.b848:79-87]。在一些实施方案中,待根据本文描述的方法使用的actriib多肽是重组多肽。
本公开内容的actriib多肽可通过多种本领域已知的技术产生。例如,本公开内容的多肽可使用标准蛋白化学技术合成,如描述于bodansky,m.principlesofpeptidesynthesis,springerverlag,berlin(1993)和grantg.a.(ed.),syntheticpeptides:auser'sguide,w.h.freemanandcompany,newyork(1992)的那些。此外,自动肽合成仪可市售获得(例如,advancedchemtechmodel396;milligen/biosearch9600)。可选地,本公开内容的多肽,包括其片段或变体,可使用各种表达系统[例如,大肠杆菌(e.coli)、中国仓鼠卵巢(cho)细胞、cos细胞、杆状病毒]重组产生,如本领域众所周知的。在进一步的实施方案中,本公开内容的修饰或未修饰的多肽可通过使用例如,蛋白酶,例如,胰蛋白酶、嗜热菌蛋白酶、胰凝乳蛋白酶、胃蛋白酶或成对碱性氨基酸转换酶(pace),消化重组产生的全长actriib多肽产生。计算机分析(使用市售可得的软件,例如,macvector,omega,pcgene,molecularsimulation,inc.)可用于鉴定蛋白酶剪切位点。可选地,可以使用化学切割(例如,溴化氰、羟胺等)从重组生成的全长actriib多肽产生这种多肽。
b.编码actriib多肽的核酸
在某些实施方案中,本公开内容提供了编码actriib多肽(包括其片段、功能变体(例如gdf捕获物)和融合蛋白)的分离和/或重组的核酸。例如,seqidno:7编码天然存在的人actriib前体多肽(上文所述的r64变体),而seqidno:8编码actriib(上文所述的r64变体)的加工的细胞外结构域。主题核酸可以是单链的或双链的。这种核酸可以是dna或rna分子。这些核酸可用于例如,制备如本文描述的基于actrii的配体捕获物多肽的方法中。
如本文所用的,分离的核酸(一种或多种)是指已经与其天然环境的组分分开的核酸分子。分离的核酸包括在正常包含核酸分子的细胞中包含的核酸分子,但所述核酸分子存在于染色体外或不同于其天然的染色体位置的染色体位置。
在某些实施方案中,编码本公开内容的actriib多肽的核酸被理解为包括作为seqidno:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62的任一个的变体的核酸。变体核苷酸序列包括差异一个或多个核苷酸取代、添加或缺失的序列,包括等位基因变体,且因此,将包括与seqidno:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62中任一个指定的核苷酸序列不同的编码序列。
在某些实施方案中,本公开内容的actriib多肽由分离和/或重组核酸序列编码,所述核酸序列与seqidno:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62中任一个具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性。本领域普通技术人员将理解,和与seqidno:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62互补的序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的核酸序列及其变体也在本公开内容的范围内。在进一步实施方案中,本公开内容的核酸序列可以是分离的、重组的,和/或与异源的核苷酸序列融合或在dna文库中。
在其它实施方案中,本公开内容的核酸还包括在高度严格条件下与seqidno:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62中指定的核苷酸序列,seqidno:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62的互补序列或其片段杂交的核苷酸序列。如上文所讨论的,本领域普通技术人员将容易理解,可以改变促进dna杂交的适当严格条件。本领域普通技术人员将容易理解,可以改变促进dna杂交的适当严格条件。例如,可在6.0x氯化钠/柠檬酸钠(ssc)中在约45℃进行杂交,随后为在50℃的2.0xssc洗涤。例如,在洗涤步骤中的盐浓度可选自在50℃约2.0xssc的低严格性至在50℃约0.2xssc的高严格性。此外,在洗涤步骤中的温度可从在室温约22℃的低严格条件增加至在约65℃的高严格条件。温度和盐两者可以改变,或温度或盐浓度可以保持恒定,而改变另一个变量。在一个实施方案中,本公开内容提供了核酸,其在室温6xssc的低严格条件下杂交,随后为在室温的2xssc洗涤。
由于遗传密码的简并性而不同于如seqidno:7、8、26、32、48、49、51、52、55、56、57、59、60、61和62中所示的核酸的分离的核酸也在本公开内容的范围内。例如,许多氨基酸由超过一个三联体指定。规定相同的氨基酸的密码子,或同义密码子(例如,cau和cac是组氨酸的同义密码子)可导致“沉默”突变,其不影响蛋白的氨基酸序列。然而,预期的确导致主题蛋白的氨基酸序列变化的dna序列多态性将存在于哺乳动物细胞中。本领域技术人员将理解,由于天然等位基因变异,编码特定蛋白的核酸的一个或多个核苷酸(至多约3-5%的核苷酸)的这些变异可存在于给定物种的个体中。任何和所有这种核苷酸变异和所产生的氨基酸多态性在本公开内容的范围内。
在某些实施方案中,本公开内容的重组核酸可以与在表达构建体中的一种或多种调节性核苷酸序列可操作地连接。调节性核苷酸序列通常将适合于用于表达的宿主细胞。许多类型的合适表达载体和合适的调节性序列是本领域已知的并且可用于多种宿主细胞中。一般,一种或多种调节性核苷酸序列可包括但不限于,启动子序列、前导或信号序列、核糖体结合位点、转录起始和终止序列、翻译起始和终止序列、和增强子或激活物序列。本公开内容预期如本领域已知的组成型或诱导型启动子。启动子可以是天然存在的启动子,或组合超过一个启动子的元件的杂合启动子。表达构建体可存在于细胞中的附加体(如质粒)上,或表达构建体可插入染色体中。在一些实施方案中,表达载体含有选择标记基因以允许选择转化的宿主细胞。选择标记基因是本领域众所周知的并且可以随使用的宿主细胞而改变。
在某些方面,在表达载体中提供本文公开的主题核酸,所述表达载体包含编码actriib多肽且可操作连接至至少一种调节性序列的核苷酸序列。调节性序列是本领域公认的且经选择以指导actriib多肽的表达。因此,术语调节性序列包括启动子、增强子和其它表达控制元件。示例性调节性序列描述于goeddel;geneexpressiontechnology:methodsinenzymology,academicpress,sandiego,ca(1990)。例如,当与其可操作连接时控制dna序列表达的各种各样表达控制序列的任一种可用于这些载体中,以表达编码actriib多肽的dna序列。这种有用的表达控制序列包括例如,sv40的早期和晚期启动子、tet启动子、腺病毒或巨细胞病毒立即早期启动子、rsv启动子、lac系统、trp系统、tac或trc系统、其表达受t7rna聚合酶指导的t7启动子、噬菌体λ的主要操纵基因和启动子区、fd外壳蛋白的控制区、3-磷酸甘油酸激酶或其它糖酵解酶的启动子、酸性磷酸酶(例如,pho5)的启动子、酵母α-交配因子的启动子、杆状病毒系统的多面体启动子和已知控制原核或真核细胞或它们的病毒的基因表达的其它序列,和其各种组合。应理解,表达载体的设计可取决于诸如待转化的宿主细胞的选择和/或期望表达的蛋白类型的因素。此外,还应考虑载体的拷贝数、控制该拷贝数的能力和由载体编码的任何其它蛋白(诸如抗生素标记物)的表达。
本公开内容的重组核酸可通过将克隆的基因或其部分连接到适合于在原核细胞、真核细胞(酵母、禽类、昆虫或哺乳动物)或两者中表达的载体中来产生。用于产生重组actriib多肽的表达载体包括质粒和其它载体。例如,合适的载体包括以下类型的质粒:pbr322-衍生的质粒、pembl-衍生的质粒、pex-衍生的质粒、pbtac-衍生的质粒和puc-衍生的质粒,其用于在原核细胞如大肠杆菌中表达。
一些哺乳动物表达载体含有促进载体在细菌中繁殖的原核序列和在真核细胞中表达的一个或多个真核转录单位两者。pcdnai/amp、pcdnai/neo、prc/cmv、psv2gpt、psv2neo、psv2-dhfr、ptk2、prsvneo、pmsg、psvt7、pko-neo和phyg衍生的载体是适合于转染真核细胞的哺乳动物表达载体的实例。这些载体的一些用来自细菌质粒如pbr322的序列修饰,以促进在原核和真核细胞两者中的复制和抗药性选择。可选地,病毒如牛乳头瘤病毒(bpv-1)或eb病毒(phebo、prep-衍生的和p205)的衍生物可用于蛋白在真核细胞中的瞬时表达。其它病毒(包括逆转录病毒)表达系统的实例可见于下文的基因疗法递送系统的描述中。用于制备质粒和转化宿主生物的各种方法是本领域众所周知的。对于原核和真核细胞两者的其它合适的表达系统,以及通用的重组程序,例如molecularcloningalaboratorymanual,第3版,sambrook、fritsch和maniatis编辑,(coldspringharborlaboratorypress,2001)。在一些实例中,可能期望通过使用杆状病毒表达系统来表达重组多肽。这种杆状病毒表达系统的实例包括pvl-衍生的载体(如pvl1392、pvl1393和pvl941)、pacuw-衍生的载体(如pacuw1)和pbluebac-衍生的载体(如含有β-gal的pbluebaciii)。
在优选实施方案中,载体将经设计以用于在cho细胞中产生主题actriib多肽,如pcmv-script载体(stratagene,lajolla,calif.)、pcdna4载体(invitrogen,carlsbad,calif.)和pci-neo载体(promega,madison,wisc.)。如将显而易见的,主题基因构建体可用于导致主题actrii多肽在培养物中繁殖的细胞中表达,例如,以产生蛋白,包括融合蛋白或变体蛋白,用于纯化。
本公开内容还涉及用重组基因转染的宿主细胞,所述重组基因包括一种或多种主题actriib多肽的编码序列。宿主细胞可以是任何原核或真核细胞。例如,本公开内容的actriib多肽可在细菌细胞如大肠杆菌、昆虫细胞(例如,使用杆状病毒表达系统)、酵母或哺乳动物细胞[例如,中国仓鼠卵巢(cho)细胞系]中表达。其它合适的宿主细胞是本领域技术人员已知的。
因此,本公开内容进一步涉及产生主题actriib多肽的方法。例如,用编码actriib多肽的表达载体转染的宿主细胞可在合适的条件下培养,以允许发生actriib多肽的表达。多肽可经分泌并从细胞和包含多肽的培养基的混合物分离。可选地,actriib多肽可保留在细胞质中或膜级分中,并且收获细胞,裂解并分离蛋白。细胞培养物包括宿主细胞、培养基和其它副产物。用于细胞培养的合适培养基是本领域众所周知的。主题多肽可使用本领域已知用于纯化蛋白的技术从细胞培养基、宿主细胞或两者分离,所述技术包括离子交换层析、凝胶过滤层析、超滤、电泳、用对actriib多肽的特定表位特异性的抗体的免疫亲和纯化、和用结合融合至actriib多肽的结构域的药剂的亲和纯化(例如,a蛋白柱可用于纯化actriib-fc融合蛋白)。在一些实施方案中,actriib多肽是含有促进其纯化的结构域的融合蛋白。
在一些实施方案中,纯化通过一系列柱层析步骤实现,包括例如,以任何顺序的以下的三种或更多种:a蛋白层析、q琼脂糖凝胶层析、苯基琼脂糖凝胶层析、尺寸排阻层析和阳离子交换层析。纯化可以用病毒过滤和缓冲液更换完成。actriib蛋白可纯化至>90%、>95%、>96%、>98%或>99%的纯度,如通过尺寸排阻层析所测定的,和>90%、>95%、>96%、>98%或>99%的纯度,如通过sdspage所测定的。纯度的靶水平应该是足以在哺乳动物系统、特别是非-人灵长类动物、啮齿类动物(小鼠)和人中实现期望的结果的纯度。
在另一个实施方案中,编码在重组actriib多肽的期望部分的n-末端的纯化前导序列如聚-(his)/肠激酶切割位点序列的融合基因可允许通过亲和层析使用ni2+金属树脂纯化表达的融合蛋白。然后纯化前导序列可随后通过用肠激酶处理来除去,以提供纯化的actriib多肽。参见,例如,hochuli等(1987)j.chromatography411:177;和janknecht等(1991)pnasusa88:8972。
用于制备融合基因的技术是众所周知的。基本上,编码不同多肽序列的各种dna片段的连接根据常规技术进行,采用平端或交错端末端用于连接,限制性酶消化以提供合适的末端,在合适的情况下补平粘端,碱性磷酸酶处理以避免不期望的连接,和酶促连接。在另一个实施方案中,融合基因可通过常规技术(包括自动dna合成仪)合成。另一方面,基因片段的pcr扩增可使用锚定引物进行,其在两个相邻的基因片段之间产生互补的突出端,其可随后被退火以产生嵌合基因序列。参见,例如,currentprotocolsinmolecularbiology,ausubel等编辑,johnwiley&sons:1992。
c.抗体拮抗剂
在某些方面,待根据本文公开的方法和用途使用的actriib拮抗剂是抗体(actriib拮抗剂抗体)或抗体的组合。actriib拮抗剂抗体或抗体的组合可以结合例如一种或多种actriib结合配体(例如,激活蛋白、gdf11、gdf8、gdf3、bmp10和bmp6)、actriib受体、i型受体(例如,alk4、alk5和/或alk7)和/或actriib共同受体。如本文所述的,可以单独或与一种或多种支持疗法或活性剂组合使用actriib拮抗剂抗体,以治疗骨髓纤维化,特别是治疗或预防骨髓纤维化的一种或多种并发症(例如,脾肿大、髓外造血、贫血和纤维化)和/或用janus激酶抑制剂治疗的患者。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少激活蛋白。如本文所用的,激活蛋白抗体(或抗-激活蛋白抗体)通常是指以足够的亲和力结合激活蛋白、从而使得所述抗体可用作靶向激活蛋白的诊断剂和/或治疗剂的抗体。在某些实施方案中,激活蛋白抗体与不相关的非-激活蛋白蛋白的结合程度小于所述抗体与激活蛋白的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,激活蛋白抗体结合在来自不同物种的激活蛋白中保守的激活蛋白的表位。在某些优选实施方案中,抗-激活蛋白抗体结合人激活蛋白。在一些实施方案中,激活蛋白抗体可以抑制激活蛋白结合i型和/或ii型受体(例如,actriib、alk4、alk5和/或alk7),且因此抑制激活蛋白-介导的信号传导(例如,smad信号传导)。在一些实施方案中,激活蛋白抗体可以抑制激活蛋白结合actriib共同受体,且因此抑制激活蛋白介导的信号传导(例如,smad信号传导)。应当注意,激活蛋白a与激活蛋白b具有相似序列同源性,且因此结合激活蛋白a的抗体在一些情况下也可以结合和/或抑制激活蛋白b,其也适用于抗-激活蛋白b抗体。在一些实施方案中,本公开内容涉及多特异性抗体(例如,双特异性抗体)及其用途,所述抗体结合激活蛋白且进一步结合例如一种或多种额外actriib配体[例如,gdf11、gdf8、gdf3、bmp10和bmp6]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体。在一些实施方案中,结合激活蛋白的多特异性抗体不结合或基本上不结合bmp9(例如,以大于1x10-7m的kd结合bmp9或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,结合激活蛋白的多特异性抗体不结合或基本上不结合激活蛋白a(例如,以大于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含激活蛋白抗体和一种或多种额外的结合例如一种或多种额外actriib超家族配体[例如,gdf8、gdf11、gdf3和bmp6]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体的抗体。在一些实施方案中,包含激活蛋白抗体的抗体的组合不包含bmp9抗体。在一些实施方案中,包含激活蛋白抗体的抗体的组合不包含激活蛋白a抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少激活蛋白b的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少激活蛋白b。如本文所用的,激活蛋白b抗体(或抗-激活蛋白b抗体)通常是指以足够的亲和力结合激活蛋白b、从而使得所述抗体可用作靶向激活蛋白b的诊断剂和/或治疗剂的抗体。在某些实施方案中,激活蛋白b抗体与不相关的非-激活蛋白b蛋白的结合程度小于所述抗体与激活蛋白的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,激活蛋白b抗体结合在来自不同物种的激活蛋白b中保守的激活蛋白b的表位。在某些优选实施方案中,抗-激活蛋白b抗体结合人激活蛋白b。在一些实施方案中,激活蛋白b抗体可以抑制激活蛋白b结合i型和/或ii型受体(例如,actriib、alk4、alk5和/或alk7),且因此抑制激活蛋白b-介导的信号传导(例如,smad信号传导)。在一些实施方案中,激活蛋白b抗体可以抑制激活蛋白b结合共同受体,且因此抑制激活蛋白b介导的信号传导(例如,smad信号传导)。应当注意,激活蛋白b与激活蛋白a具有相似序列同源性,且因此结合激活蛋白b的抗体在一些情况下也可以结合和/或抑制激活蛋白a。在一些实施方案中,本公开内容涉及多特异性抗体(例如,双特异性抗体)及其用途,所述抗体结合激活蛋白b且进一步结合例如一种或多种额外actriib配体[例如,gdf11、gdf8、gdf3、bmp10和bmp6]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体。在一些实施方案中,结合激活蛋白b的多特异性抗体不结合或基本上不结合bmp9(例如,以大于1x10-7m的kd结合bmp9或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,结合激活蛋白b的多特异性抗体不结合或基本上不结合激活蛋白a(例如,以大于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含激活蛋白b抗体和一种或多种额外的结合例如一种或多种额外actriib配体[例如,gdf8、gdf11、gdf3、bmp6和bmp10]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体的抗体。在一些实施方案中,包含激活蛋白b抗体的抗体的组合不包含bmp9抗体。在一些实施方案中,包含激活蛋白b抗体的抗体的组合不包含激活蛋白a抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少gdf8的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少gdf8。如本文所用的,gdf8抗体(或抗-gdf8抗体)通常是指以足够的亲和力结合gdf8、从而使得所述抗体可用作靶向gdf8的诊断剂和/或治疗剂的抗体。在某些实施方案中,gdf8抗体与不相关的非-gdf8蛋白的结合程度小于所述抗体与gdf8的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,gdf8抗体结合在来自不同物种的gdf8中保守的gdf8的表位。在某些优选实施方案中,抗-gdf8抗体结合人gdf8。在一些实施方案中,gdf8抗体可以抑制gdf8结合i型和/或ii型受体(例如,actriib、alk4、alk5和/或alk7),且因此抑制gdf8-介导的信号传导(例如,smad信号传导)。在一些实施方案中,gdf8抗体可以抑制gdf8结合共同受体,且因此抑制gdf8介导的信号传导(例如,smad信号传导)。应当注意,gdf8与gdf11具有高度序列同源性,且因此结合gdf8的抗体在一些情况下也可以结合和/或抑制gdf11。在一些实施方案中,本公开内容涉及多特异性抗体(例如,双特异性抗体)及其用途,所述抗体结合gdf8且进一步结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf11、gdf3、bmp10和bmp6]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体。在一些实施方案中,结合gdf8的多特异性抗体不结合或基本上不结合bmp9(例如,以大于1x10-7m的kd结合bmp9或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,结合gdf8的多特异性抗体不结合或基本上不结合激活蛋白a(例如,以大于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含gdf8抗体和一种或多种额外的结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf11、gdf3、bmp6、bmp10和bmp15]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体的抗体。在一些实施方案中,包含gdf8抗体的抗体的组合不包含bmp9抗体。在一些实施方案中,包含gdf8抗体的抗体的组合不包含激活蛋白a抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少gdf11的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少gdf11。如本文所用的,gdf11抗体(或抗-gdf11抗体)通常是指以足够的亲和力结合gdf11、从而使得所述抗体可用作靶向gdf11的诊断剂和/或治疗剂的抗体。在某些实施方案中,gdf11抗体与不相关的非-gdf11蛋白的结合程度小于所述抗体与gdf11的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,gdf11抗体结合在来自不同物种的gdf11中保守的gdf11的表位。在某些优选实施方案中,抗-gdf11抗体结合人gdf11。在一些实施方案中,gdf11抗体可以抑制gdf11结合i型和/或ii型受体(例如,actriib、alk4、alk5和/或alk7),且因此抑制gdf11-介导的信号传导(例如,smad信号传导)。在一些实施方案中,gdf11抗体可以抑制gdf11结合共同受体,且因此抑制gdf11介导的信号传导(例如,smad信号传导)。应当注意,gdf11与gdf8具有高度序列同源性,且因此结合gdf11的抗体在一些情况下还可以结合和/或抑制gdf8。在一些实施方案中,本公开内容涉及多特异性抗体(例如,双特异性抗体)及其用途,所述抗体结合gdf11且进一步结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf8、gdf3、bmp10和bmp6]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体。在一些实施方案中,结合gdf11的多特异性抗体不结合或基本上不结合bmp9(例如,以大于1x10-7m的kd结合bmp9或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,结合gdf11的多特异性抗体不结合或基本上不结合激活蛋白a(例如,以大于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含gdf11抗体和一种或多种额外的结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf8、gdf3、bmp6和bmp10]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体的抗体。在一些实施方案中,包含gdf11抗体的抗体的组合不包含bmp9抗体。在一些实施方案中,包含gdf11抗体的抗体的组合不包含激活蛋白a抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少bmp6的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少bmp6。如本文所用的,bmp6抗体(或抗-bmp6抗体)通常是指可以足够的亲和力结合bmp6、从而使得所述抗体可用作靶向bmp6的诊断剂和/或治疗剂的抗体。在某些实施方案中,bmp6抗体与不相关的非-bmp6蛋白的结合程度小于所述抗体与bmp6的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,bmp6抗体结合在来自不同物种的bmp6中保守的bmp6的表位。在某些优选实施方案中,抗-bmp6抗体结合人bmp6。在一些实施方案中,bmp6抗体可以抑制bmp6结合i型和/或ii型受体(例如,actriib、alk4、alk5和/或alk7),且因此抑制bmp6-介导的信号传导(例如,smad信号传导)。在一些实施方案中,bmp6抗体可以抑制bmp6结合共同受体,且因此抑制bmp6介导的信号传导(例如,smad信号传导)。在一些实施方案中,本公开内容涉及多特异性抗体(例如,双特异性抗体)及其用途,所述抗体结合bmp6且进一步结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf8、gdf3、bmp10和gdf11]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体。在一些实施方案中,结合bmp6的多特异性抗体不结合或基本上不结合bmp9(例如,以大于1x10-7m的kd结合bmp9或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,结合bmp6的多特异性抗体不结合或基本上不结合激活蛋白a(例如,以大于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含bmp6抗体和一种或多种额外的结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf8、gdf11、gdf3和bmp10]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体的抗体。在一些实施方案中,包含bmp6抗体的抗体的组合不包含bmp9抗体。在一些实施方案中,包含bmp6抗体的抗体的组合不包含激活蛋白a抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少gdf3的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少gdf3。如本文所用的,gdf3抗体(或抗-gdf3抗体)通常是指可以足够的亲和力结合gdf3、从而使得所述抗体可用作靶向gdf3的诊断剂和/或治疗剂的抗体。在某些实施方案中,gdf3抗体与不相关的非-gdf3蛋白的结合程度小于所述抗体与gdf3的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,gdf3抗体结合在来自不同物种的gdf3中保守的gdf3的表位。在某些优选实施方案中,抗-gdf3抗体结合人gdf3。在一些实施方案中,gdf3抗体可以抑制gdf3结合i型和/或ii型受体(例如,actriib、alk4、alk5和/或alk7),且因此抑制gdf3-介导的信号传导(例如,smad信号传导)。在一些实施方案中,gdf3抗体可以抑制gdf3结合共同受体,且因此抑制gdf3介导的信号传导(例如,smad信号传导)。在一些实施方案中,本公开内容涉及多特异性抗体(例如,双特异性抗体)及其用途,所述抗体结合gdf3且进一步结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf8、bmp6、bmp10和gdf11]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体。在一些实施方案中,结合gdf3的多特异性抗体不结合或基本上不结合bmp9(例如,以大于1x10-7m的kd结合bmp9或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,结合gdf3的多特异性抗体不结合或基本上不结合激活蛋白a(例如,以大于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含gdf3抗体和一种或多种额外的结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae、激活蛋白be)、gdf8、gdf11、bmp6和bmp10]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体的抗体。在一些实施方案中,包含gdf3抗体的抗体的组合不包含bmp9抗体。在一些实施方案中,包含gdf3抗体的抗体的组合不包含激活蛋白a抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少bmp10的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少bmp10。如本文所用的,bmp10抗体(或抗-bmp10抗体)通常是指可以足够的亲和力结合bmp10、从而使得所述抗体可用作靶向bmp10的诊断剂和/或治疗剂的抗体。在某些实施方案中,bmp10抗体与不相关的非-bmp10蛋白的结合程度小于所述抗体与bmp10的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,bmp10抗体结合在来自不同物种的bmp10中保守的bmp10的表位。在某些优选实施方案中,抗-bmp10抗体结合人bmp10。在一些实施方案中,bmp10抗体可以抑制bmp10结合i型和/或ii型受体(例如,actriib、alk4、alk5和/或alk7),且因此抑制bmp10-介导的信号传导(例如,smad信号传导)。在一些实施方案中,bmp10抗体可以抑制bmp10结合共同受体,且因此抑制bmp10介导的信号传导(例如,smad信号传导)。在一些实施方案中,本公开内容涉及多特异性抗体(例如,双特异性抗体)及其用途,所述抗体结合bmp10且进一步结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、gdf8、gdf11、gdf3和bmp6]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体。在一些实施方案中,结合bmp10的多特异性抗体不结合或基本上不结合bmp9(例如,以大于1x10-7m的kd结合bmp9或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,结合bmp10的多特异性抗体不结合或基本上不结合激活蛋白a(例如,以大于1x10-7m的kd结合激活蛋白a或具有相对适度的结合,例如,约1x10-8m或约1x10-9m)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含bmp10抗体和一种或多种额外的结合例如一种或多种额外actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、gdf8、gdf3、bmp6、bmp10和gdf11]、一种或多种i型受体和/或ii型受体(例如,actriib、alk4、alk5和/或alk7)和/或一种或多种共同受体的抗体。在一些实施方案中,包含bmp10抗体的抗体的组合不包含bmp9抗体。在一些实施方案中,包含bmp10抗体的抗体的组合不包含激活蛋白a抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少actriib的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少actriib。如本文所用的,actriib抗体(抗-actriib抗体)通常是指以足够的亲和力结合actriib、从而使得所述抗体可用作靶向actriib的诊断剂和/或治疗剂的抗体。在某些实施方案中,actriib抗体与不相关的非-actriib蛋白的结合程度小于所述抗体与actriib的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白-蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,抗-actriib抗体结合在来自不同物种的actriib中保守的actriib的表位。在某些优选实施方案中,抗-actriib抗体结合人actriib。在一些实施方案中,抗-actriib抗体可以抑制一种或多种actriib配体[例如,gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、gdf11、bmp6、gdf3和bmp10]结合actriib。在一些实施方案中,抗-actriib抗体是多特异性抗体(例如,双特异性抗体),其结合actriib和一种或多种actriib配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac)、gdf3、bmp6和bmp10]、i型受体(例如,alk4、alk5和/或alk7)、共同受体和/或额外的ii型受体(例如,actriia)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含抗-actriib抗体和一种或多种额外的结合例如一种或多种actriib配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)bmp6、gdf3和bmp10]、共同受体、i型受体(例如,alk4、alk5和/或alk7)和/或额外ii型受体(例如,actriia)的抗体。应当注意,actriib与actriia具有序列相似性,且因此结合actriib的抗体在一些情况下也可以结合和/或抑制actriia。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少alk4的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少alk4。如本文所用的,alk4抗体(抗-alk4抗体)通常是指以足够的亲和力结合alk4、从而使得所述抗体可用作靶向alk4的诊断剂和/或治疗剂的抗体。在某些实施方案中,抗-alk4抗体与不相关的非-alk4蛋白的结合程度小于所述抗体与alk4的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白-蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,抗-alk4抗体结合在来自不同物种的alk4中保守的alk4的表位。在某些优选实施方案中,抗-alk4抗体结合人alk4。在一些实施方案中,抗-alk4抗体可以抑制一种或多种actriib配体[例如,gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、gdf11、bmp6、gdf3和bmp10]结合alk4。在一些实施方案中,抗-actriia抗体是多特异性抗体(例如,双特异性抗体),其结合alk4和一种或多种gdf/bmp配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac)、gdf3、bmp6和bmp10]、ii型受体(例如,actriib)、共同受体和/或额外i型受体(例如,alk5和/或alk7)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含抗-alk4抗体和一种或多种额外的结合例如一种或多种actriib配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、bmp6和bmp10]、共同受体、ii型受体(例如,actriib)和/或额外i型受体(例如,alk5和/或alk7)的抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少alk5的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少alk5。如本文所用的,alk5抗体(抗-alk5抗体)通常是指以足够的亲和力结合alk5、从而使得所述抗体可用作靶向alk5的诊断剂和/或治疗剂的抗体。在某些实施方案中,抗-alk5抗体与不相关的非-alk5蛋白的结合程度小于所述抗体与alk5的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白-蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,抗-alk5抗体结合在来自不同物种的alk5中保守的alk5的表位。在某些优选实施方案中,抗-alk5抗体结合人alk5。在一些实施方案中,抗-alk5抗体可以抑制一种或多种actriib配体[例如,gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、gdf11、bmp6、gdf3和bmp10]结合alk5。在一些实施方案中,抗-alk5抗体是多特异性抗体(例如,双特异性抗体),其结合alk5和一种或多种actriib配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac)、gdf3、bmp6和bmp10]、ii型受体(例如,actriib)、共同受体和/或额外i型受体(例如,alk4和/或alk7)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含抗-alk5抗体和一种或多种额外的结合例如一种或多种actriib配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、bmp6和bmp10]、共同受体、ii型受体(例如,actriib)和/或额外i型受体(例如,alk4和/或alk7)的抗体。
在某些方面,actriib拮抗剂抗体或抗体的组合是抑制至少alk7的抗体。因此,在一些实施方案中,actriib拮抗剂抗体或抗体的组合结合至少alk7。如本文所用的,alk7抗体(抗-alk7抗体)通常是指以足够的亲和力结合alk7、从而使得所述抗体可用作靶向alk7的诊断剂和/或治疗剂的抗体。在某些实施方案中,抗-alk7抗体与不相关的非-alk7蛋白的结合程度小于所述抗体与alk7的结合的约10%、9%、8%、7%、6%、5%、4%、3%、2%或小于约1%,如例如通过放射免疫测定(ria)、biacore或其它蛋白-蛋白相互作用或结合亲和力测定所测量的。在某些实施方案中,抗-alk7抗体结合在来自不同物种的alk7中保守的alk7的表位。在某些优选实施方案中,抗-alk7抗体结合人alk7。在一些实施方案中,抗-alk7抗体可以抑制一种或多种actriib配体[例如,gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、gdf11、bmp6、gdf3和bmp10]结合alk7。在一些实施方案中,抗-alk7抗体是多特异性抗体(例如,双特异性抗体),其结合alk7和一种或多种actriib配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac)、gdf3、bmp6和bmp10]、ii型受体(例如,actriib)、共同受体和/或额外i型受体(例如,alk4和/或alk5)。在一些实施方案中,本公开内容涉及抗体的组合及其用途,其中抗体的组合包含抗-alk7抗体和一种或多种额外的结合例如一种或多种actriib配体[例如,gdf11、gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和激活蛋白be)、bmp6和bmp10]、共同受体、ii型受体(例如,actriib)和/或额外i型受体(例如,alk4和/或alk5)的抗体。
术语抗体在本文以最广含义使用,且包含各种抗体结构,包括但不限于单克隆抗体、多克隆抗体、多特异性抗体(例如,双特异性抗体)和抗体片段,只要它们显示期望的抗原-结合活性。抗体片段是指除了完整抗体以外的分子,其包含结合完整抗体所结合的抗原的完整抗体的一部分。抗体片段的实例包括但不限于fv、fab、fab'、fab'-sh、f(ab')2;双抗体;线性抗体;单链抗体分子(例如,scfv);和由抗体片段形成的多特异性抗体[参见,例如,hudson等(2003)nat.med.9:129-134;plückthun,thepharmacologyofmonoclonalantibodies,vol.113,rosenburg和moore编辑,(springer-verlag,newyork),pp.269-315(1994);wo93/16185;和美国专利号5,571,894;5,587,458;和5,869,046]。双抗体是具有两个抗原结合部位的抗体片段,其可以是二价的或双特异性的[参见,例如,ep404,097;wo1993/01161;hudson等(2003)nat.med.9:129-134(2003);和hollinger等(1993)proc.natl.acad.sci.usa90:6444-6448]。三链抗体和四链抗体(tetrabodies)也描述于hudson等(2003)nat.med.9:129-134中。单-结构域抗体是包含抗体的所有或一部分重链可变结构域或所有或一部分轻链可变结构域的抗体片段。在某些实施方案中,单-结构域抗体是人单-结构域抗体[参见,例如,美国专利号6,248,516]。本文公开的抗体可以是多克隆抗体或单克隆抗体。在某些实施方案中,本公开内容的抗体包含与其附着且能够被检测的标记(例如,所述标记可以是放射性同位素、荧光化合物、酶或酶辅因子)。在某些优选实施方案中,本公开内容的抗体是分离的抗体。在某些优选实施方案中,本公开内容的抗体是重组抗体。
本文的抗体可以是任何类别的。抗体的类别是指由其重链所具有的恒定结构域或恒定区的类型。存在5种主要类别的抗体:iga、igd、ige、igg和igm,且这些类别中的几种可进一步分为亚类(同种型),例如,igg1、igg2、igg3、igg4、iga1和iga2。对应于不同类别的免疫球蛋白的重链恒定结构域被称为α、δ、ε、γ和μ。
通常,用于本文公开的方法中的抗体特异性结合其靶抗原,优选地具有高结合亲和力。亲和力可表示为kd值,且反映固有结合亲和力(例如,具有最小化的亲合力(avidity)作用)。一般,结合亲和力在体外测量,无论是在无细胞的设置还是细胞缔合的设置下。本领域已知的许多测定的任一种,包括本文公开的那些,可用于获得结合亲和力测量结果,包括例如,biacore、放射性标记的抗原-结合测定(ria)和elisa。在一些实施方案中,本公开内容的抗体以至少1x10-7或更强、1x10-8或更强、1x10-9或更强、1x10-10或更强、1x10-11或更强、1x10-12或更强、1x10-13或更强或1x10-14或更强的kd结合它们的靶抗原(例如,alk4、alk5、alk7、actriib、gdf3、激活蛋白、gdf11、gdf8、bmp10和/或bmp6)。
在某些实施方案中,kd通过以目标抗体的fab形式和其靶抗原进行的ria测量,如由以下测定所述的。fab对抗原的溶液结合亲和力通过在滴定系列的未标记抗原存在的情况下用最小浓度的放射性标记的抗原(例如,125i-标记的)平衡fab,然后用抗-fab抗体-包被的板捕获结合的抗原来测量[参见,例如,chen等(1999)j.mol.biol.293:865-881]。为了确立该测定的条件,多孔板(例如,来自thermoscientific的microtiter®)用捕获性抗-fab抗体(例如,来自cappellabs)包被(例如,过夜)且随后用牛血清白蛋白封闭,优选地在室温(约23℃)。在非-吸附板中,放射性标记的抗原与系列稀释的目标fab混合[例如,与抗-vegf抗体fab-12的评估一致,presta等,(1997)cancerres.57:4593-4599]。然后将目标fab温育,优选地过夜,但温育可持续更长时间段(例如,约65小时)以确保达到平衡。其后,将混合物转移至捕获板用于温育,优选地在室温温育约1小时。然后除去溶液,并将板洗涤几次,优选地用聚山梨醇酯20和pbs混合物。当板已经干燥时,加入闪烁体(例如,来自packard的microscint®),并将板在γ计数器(例如,来自packard的topcount®)上计数。
根据另一个实施方案,kd使用表面等离振子共振测定,使用例如biacore®2000或biacore®3000(biacore,inc.,piscataway,n.j.)用约10响应单位(responsiveunit)(ru)的固定化抗原cm5芯片测量。简言之,羧甲基化葡聚糖生物传感器芯片(cm5,biacore,inc.)用n-乙基-n'-(3-二甲基氨丙基)-碳二亚胺盐酸盐(edc)和n-羟基琥珀酰亚胺(nhs)根据供应商的说明书活化。例如,抗原可用10mm乙酸钠ph4.8稀释至5µg/ml(约0.2µm),然后以5µl/分钟的流速注射以实现近似10响应单位(ru)的偶联蛋白。在注射抗原后,注射1m乙醇胺以封闭未反应的基团。对于动力学测量,以近似25µl/min的流速注射在含0.05%聚山梨醇酯20(tween-20®)表面活性剂的pbs(pbst)中的2倍系列稀释的fab(0.78nm至500nm)。缔合速率(kon)和解离速率(koff)使用例如,简单的一比一langmuir结合模型(biacore®evaluation软件版本3.2),通过同时拟合缔合和解离传感图计算。平衡解离常数(kd)计算为比率koff/kon[参见,例如,chen等,(1999)j.mol.biol.293:865-881]。如果通过上述表面等离振子共振测定,结合速率超过例如,106m-1s-1,则结合速率可通过使用测量在渐增浓度的抗原存在的情况下pbs中20nm抗-抗原抗体(fab形式)的荧光发射强度的增加或减少(例如,激发=295nm;发射=340nm,16nm带通)的荧光猝灭技术测定,如在分光计,诸如停流装备的分光光度计(avivinstruments)或带有搅拌杯的8000-系列slm-aminco®分光光度计(thermospectronic)中所测量的。
抗体片段可以通过各种技术制备,所述技术包括但不限于完整抗体的蛋白水解消化以及由重组宿主细胞(例如,大肠杆菌或噬菌体)产生,如本文所述的。人alk4、alk5、alk7、actriib、激活蛋白(激活蛋白a、激活蛋白b、激活蛋白c和激活蛋白e)、gdf11、gdf8、bmp10、gdf3和bmp6的核酸和氨基酸序列是本领域已知的。此外,许多用于生成抗体的方法是本领域众所周知的,其中一些在本文中描述。因此,根据本公开内容使用的抗体拮抗剂可由技术人员基于本领域的知识和本文提供的教导常规制备。
在某些实施方案中,本文提供的抗体是嵌合抗体。嵌合抗体是指其中重链和/或轻链的一部分源自特定的来源或物种,而重链和/或轻链的剩余部分源自不同的来源或物种的抗体。某些嵌合抗体描述于例如,美国专利号4,816,567;和morrison等,(1984)proc.natl.acad.sci.usa,81:6851-6855。在一些实施方案中,嵌合抗体包含非-人可变区(例如,源自小鼠、大鼠、仓鼠、兔或非-人灵长类动物如猴的可变区)和人恒定区。在一些实施方案中,嵌合抗体是“类别转换的”抗体,其中类别或亚类已从亲本抗体改变。通常,嵌合抗体包括其抗原-结合片段。
在某些实施方案中,本文提供的嵌合抗体是人源化抗体。人源化抗体是指包含来自非-人高变区(hvr)的氨基酸残基和来自人构架区(fr)的氨基酸残基的嵌合抗体。在某些实施方案中,人源化抗体将包含基本上所有的至少一个且一般两个可变结构域,其中所有或基本上所有的hvr(例如,cdr)对应于非-人抗体的那些,且所有或基本上所有的fr对应于人抗体的那些。人源化抗体任选地可至少包含源自人抗体的抗体恒定区的一部分。抗体的“人源化形式”,例如,非-人抗体,是指已经历人源化的抗体。人源化抗体和制备它们的方法综述于例如,almagro和fransson(2008)front.biosci.13:1619-1633且进一步描述于例如,riechmann等,(1988)nature332:323-329;queen等(1989)proc.nat'lacad.sci.usa86:10029-10033;美国专利号5,821,337;7,527,791;6,982,321;和7,087,409;kashmiri等,(2005)methods36:25-34[描述sdr(a-cdr)嫁接];padlan,mol.immunol.(1991)28:489-498(描述了“表面重建(resurfacing)”);dall'acqua等(2005)methods36:43-60(描述“fr改组”);osbourn等(2005)methods36:61-68;和klimka等br.j.cancer(2000)83:252-260(描述fr改组的“指导的选择”方法)。可用于人源化的人构架区包括但不限于:使用“最佳拟合(best-fit)”方法选择的构架区[参见,例如,sims等(1993)j.immunol.151:2296];源自轻链或重链可变区的特定亚组的人抗体的共有序列的构架区[参见,例如,carter等(1992)proc.natl.acad.sci.usa,89:4285;和presta等(1993)j.immunol.,151:2623];人成熟(体细胞成熟)构架区或人种系构架区[参见,例如,almagro和fransson(2008)front.biosci.13:1619-1633];和源自筛选fr文库的构架区[参见,例如,baca等,(1997)j.biol.chem.272:10678-10684;和rosok等,(1996)j.biol.chem.271:22611-22618]。
在某些实施方案中,本文提供的抗体是人抗体。人抗体可使用本领域已知的各种技术产生。人抗体总体描述于vandijk和vandewinkel(2008)curr.opin.pharmacol.5:368-74(2001)以及lonberg,curr.opin.immunol.20:450-459。例如,人抗体可通过施用免疫原(例如,gdf11多肽、激活蛋白b多肽、actriia多肽或actriib多肽)至转基因动物来制备,所述转基因动物已经修饰以响应于抗原攻击产生完整人抗体或具有人可变区的完整抗体。这种动物一般含有所有或一部分的人免疫球蛋白基因座,其置换内源免疫球蛋白基因座或其在染色体外存在或随机整合至动物的染色体中。在这种转基因动物中,内源免疫球蛋白基因座通常已被灭活。对于从转基因动物获得人抗体的方法的综述,参见,例如,lonberg(2005)nat.biotech.23:1117-1125;美国专利号6,075,181和6,150,584(描述xenomouse™技术);美国专利号5,770,429(描述humab®技术);美国专利号7,041,870(描述k-mmouse®技术);和美国专利申请公开号2007/0061900(描述velocimouse®技术)。来自由这种动物产生的完整抗体的人可变区可被进一步修饰,例如,通过与不同的人恒定区组合。
本文提供的人抗体还可通过基于杂交瘤的方法制备。已描述了用于产生人单克隆抗体的人骨髓瘤和小鼠-人种间骨髓瘤(heteromyeloma)细胞系[参见,例如,kozborj.immunol.,(1984)133:3001;brodeur等(1987)monoclonalantibodyproductiontechniquesandapplications,pp.51-63,marceldekker,inc.,newyork;和boerner等(1991)j.immunol.,147:86]。通过人b-细胞杂交瘤技术产生的人抗体还描述于li等,(2006)proc.natl.acad.sci.usa,103:3557-3562。额外的方法包括描述于例如,美国专利号7,189,826(描述从杂交瘤细胞系产生单克隆人igm抗体)和倪,现代免疫学(2006)26(4):265-268(2006)(描述人-人杂交瘤)中的那些。人杂交瘤技术(trioma技术)还描述于vollmers和brandlein(2005)histol.histopathol.,20(3):927-937(2005)和vollmers和brandlein(2005)methodsfindexp.clin.pharmacol.,27(3):185-91。本文提供的人抗体还可通过分离选自人-衍生的噬菌体展示文库的fv克隆可变-结构域序列产生。这种可变-结构域序列然后可与期望的人恒定结构域组合。用于从抗体文库选择人抗体的技术是本领域已知的且在本文描述。
例如,本公开内容的抗体可通过筛选组合文库的具有期望的一种或多种活性的抗体来分离。产生噬菌体展示文库和筛选这种文库的具有期望的结合特征的抗体的多种方法是本领域已知的。这种方法综述于例如,hoogenboom等(2001)的methodsinmolecularbiology178:1-37,o'brien等编辑,humanpress,totowa,n.j.,且进一步描述于例如,mccafferty等(1991)nature348:552-554;clackson等,(1991)nature352:624-628;marks等(1992)j.mol.biol.222:581-597;marks和bradbury(2003)的methodsinmolecularbiology248:161-175,lo编辑,humanpress,totowa,n.j.;sidhu等(2004)j.mol.biol.338(2):299-310;lee等(2004)j.mol.biol.340(5):1073-1093;fellouse(2004)proc.natl.acad.sci.usa101(34):12467-12472;和lee等(2004)j.immunol.methods284(1-2):119-132。
在某些噬菌体展示方法中,vh和vl基因的所有组成成分(repertoires)分别通过聚合酶链反应(pcr)克隆并在噬菌体文库中随机重组,其然后可针对抗原-结合噬菌体进行筛选,如描述于winter等(1994)ann.rev.immunol.,12:433-455中的。噬菌体一般作为单链fv(scfv)片段或作为fab片段展示抗体片段。来自免疫的来源的文库在不需要构建杂交瘤的情况下提供针对免疫原(例如,alk4、alk5、alk7、actriib、激活蛋白、gdf11、gdf8、gdf3、bmp10或bmp6)的高-亲和力抗体。另一方面,首次用于实验的(naive)所有组成成分可被克隆(例如,从人)以在没有任何免疫的情况下提供针对广泛范围的非-自身且以及自身抗原的单一来源的抗体,如描述于griffiths等(1993)emboj,12:725-734中的。最后,首次用于实验的文库还可通过如下合成制备:从干细胞克隆未重排v-基因区段并使用包含随机序列的pcr引物,以编码高度可变的cdr3区和实现体外重排,如描述于hoogenboom和winter(1992)j.mol.biol.,227:381-388中的。描述人抗体噬菌体文库的专利出版物包括例如:美国专利号5,750,373和美国专利公开号2005/0079574、2005/0119455、2005/0266000、2007/0117126、2007/0160598、2007/0237764、2007/0292936和2009/0002360。
在某些实施方案中,本文提供的抗体是多特异性抗体,例如,双特异性抗体。多特异性抗体(一般单克隆抗体)具有对一种或多种(例如,两种、三种、四种、五种、六种或更多种)抗原上的至少两个不同的表位(例如,两个、三个、四个、五个或六个或更多个)的结合特异性。
用于制备多特异性抗体的技术包括但不限于重组共表达具有不同特异性的两个免疫球蛋白重链/轻链对[参见,例如,milstein和cuello(1983)nature305:537;国际专利公开号wo93/08829;和traunecker等(1991)emboj.10:3655,和美国专利号5,731,168(“杵-臼(knob-in-hole)”人工改造)]。多特异性抗体也可以通过如下制备:人工改造静电指导作用用于制备抗体fc-异二聚的分子(参见,例如,wo2009/089004a1);交联两种或多种抗体或片段[参见,例如,美国专利号4,676,980;和brennan等(1985)science,229:81];使用亮氨酸拉链以产生双特异性抗体[参见,例如,kostelny等(1992)j.immunol.,148(5):1547-1553];使用“双抗体”技术用于制备双特异性抗体片段[参见,例如,hollinger等(1993)proc.natl.acad.sci.usa,90:6444-6448];使用单链fv(sfv)二聚体[参见,例如,gruber等(1994)j.immunol.,152:5368];和制备三特异性抗体(参见,例如,tutt等(1991)j.immunol.147:60。可以将多特异性抗体制备为全长抗体或抗体片段。本文还包括具有三个或更多个功能性抗原结合部位的人工改造的抗体,包括“章鱼抗体(octopusantibody)”[参见,例如,us2006/0025576a1]。
在某些实施方案中,本文公开的抗体是单克隆抗体。单克隆抗体是指获得自一群基本上均质的抗体的抗体,即,构成该群体的个别抗体是相同的和/或结合相同的表位,除了可能的变体抗体,例如,含有天然存在的突变或在产生单克隆抗体制剂期间产生,这种变体通常以较少量存在。与一般包括针对不同表位的不同抗体的多克隆抗体制剂相反,单克隆抗体制剂的每个单克隆抗体针对抗原上的单一表位。因此,修饰语“单克隆”表示抗体获得自抗体的基本均质群体的性质且不应解释为需要通过任何特定方法产生抗体。例如,待根据本发明的方法使用的单克隆抗体可通过多种技术制备,所述技术包括但不限于杂交瘤方法、重组dna方法、噬菌体展示方法和利用含有所有或部分的人免疫球蛋白基因座的转基因动物的方法,这种方法和制备单克隆抗体的其它示例性方法在本文中描述。
例如,通过使用源自激活蛋白的免疫原,抗-蛋白/抗-肽抗血清或单克隆抗体可通过标准规程制备[参见,例如,antibodies:alaboratorymanual,harlow和lane编辑(1988)coldspringharborpress:1988]。哺乳动物如小鼠、仓鼠或兔可用激活蛋白多肽的免疫原性形式、能够引发抗体应答的抗原片段或融合蛋白免疫。赋予蛋白或肽免疫原性的技术包括与载体缀合或本领域众所周知的其它技术。激活蛋白多肽的免疫原性部分可在佐剂存在的情况下施用。免疫进展可通过检测血浆或血清中的抗体效价来监控。标准elisa或其它免疫测定可与作为抗原的免疫原一起用于评估抗体产生的水平和/或结合亲和力的水平。
用激活蛋白的抗原制剂免疫动物后,可获得抗血清,并且如果期望,可从血清分离多克隆抗体。为了产生单克隆抗体,产生抗体的细胞(淋巴细胞)可从免疫的动物收获,且通过标准体细胞融合程序与无限增殖化细胞如骨髓瘤细胞融合,以得到杂交瘤细胞。这种技术是本领域众所周知的且包括例如,杂交瘤技术[参见,例如,kohler和milstein(1975)nature,256:495-497]、人b细胞杂交瘤技术[参见,例如,kozbar等(1983)immunologytoday,4:72]和产生人单克隆抗体的ebv-杂交瘤技术[cole等(1985)monoclonalantibodiesandcancertherapy,alanr.liss,inc.pp.77-96]。杂交瘤细胞可针对与激活蛋白多肽特异性反应的抗体的产生进行免疫化学筛选,且从包含这种杂交瘤细胞的培养物分离单克隆抗体。
在某些实施方案中,一个或多个氨基酸修饰可引入本文提供的抗体的fc区,由此产生fc区变体。fc区变体可包含在一个或多个氨基酸位置处包含氨基酸修饰(例如,取代、缺失和/或添加)的人fc区序列(例如,人igg1、igg2、igg3或igg4fc区)。
例如,本公开内容预期具有一些但并非所有效应子功能的抗体变体,对于其中抗体的体内半衰期是重要的、但某些效应子功能[例如,依赖补体的细胞毒性(cdc)和抗体依赖性细胞毒作用(adcc)]是不必要的或有害的应用,这使得它成为期望的候选物。可进行体外和/或体内细胞毒性测定以证实cdc和/或adcc活性的减少/耗尽。例如,可进行fc受体(fcr)结合测定以确保抗体缺乏fcγr结合(因此可能缺乏adcc活性),但保留fcrn结合能力。介导adcc的原代细胞nk细胞仅表达fcγriii,而单核细胞表达fcγri、fcγrii和fcγriii。造血细胞上的fcr表达概述于例如,ravetch和kinet(1991)annu.rev.immunol.9:457-492。评估目标分子的adcc活性的体外测定的非限制性实例描述于美国专利号5,500,362;hellstrom,i.等(1986)proc.natl.acad.sci.usa83:7059-7063];hellstrom,i等(1985)proc.natl.acad.sci.usa82:1499-1502;美国专利号5,821,337;bruggemann,m.等(1987)j.exp.med.166:1351-1361。可选地,可采用非-放射性测定方法(例如,acti™,用于流式细胞术的非-放射性细胞毒性测定;celltechnology,inc.mountainview,calif.;和cytotox96®非-放射性细胞毒性测定,promega,madison,wis.)。用于这种测定的有用效应细胞包括外周血单核细胞(pbmc)和天然杀伤(nk)细胞。可选地,或另外,目标分子的adcc活性可体内评估,例如,在动物模型中,如公开于clynes等(1998)proc.natl.acad.sci.usa95:652-656中的。也可进行c1q结合测定以证实抗体不能结合c1q且因此缺乏cdc活性[参见,例如,wo2006/029879和wo2005/100402中的c1q和c3c结合elisa]。为了评估补体活化,可进行cdc测定[参见,例如,gazzano-santoro等(1996)j.immunol.methods202:163;cragg,m.s.等(2003)blood101:1045-1052;和cragg,m.s和m.j.glennie(2004)blood103:2738-2743]。fcrn结合和体内清除率/半衰期测定也可使用本领域已知的方法进行[参见,例如,petkova,s.b.等(2006)intl.immunol.18(12):1759-1769]。具有减少的效应子功能的本公开内容的抗体包括具有fc区残基238、265、269、270、297、327和329的一个或多个的取代的那些(美国专利号6,737,056)。这种fc突变体包括在氨基酸位置265、269、270、297和327的两个或更多个处具有取代的fc突变体,包括残基265和297取代为丙氨酸的所谓的“dana”fc突变体(美国专利号7,332,581)。
在某些实施方案中,可能期望产生半胱氨酸人工改造的抗体,例如,“thiomab”,其中抗体的一个或多个残基被半胱氨酸残基取代。在具体实施方案中,取代的残基出现在抗体的可及位点。通过用半胱氨酸取代那些残基,反应性硫醇基团由此位于抗体的可及位点,且可用于使抗体与其它部分如药物部分或接头-药物部分缀合,以产生免疫缀合物,如本文进一步描述的。在某些实施方案中,以下残基中的任何一种或多种可被半胱氨酸取代:轻链的v205(kabat编号);重链的a118(eu编号);和重链fc区的s400(eu编号)。半胱氨酸人工改造的抗体可如例如美国专利号7,521,541中所述产生。
此外,用于筛选抗体以鉴定期望的抗体的技术可影响获得的抗体的性质。例如,如果抗体用于在溶液中结合抗原,可能期望测试溶液结合。用于测试抗体和抗原之间的相互作用以鉴定特别期望的抗体的多种不同的技术是可用的。这种技术包括elisa、表面等离振子共振结合测定(例如,biacore结合测定,biacoreab,uppsala,sweden)、夹心测定(例如,igeninternational,inc.,gaithersburg,maryland的顺磁珠系统)、蛋白质印迹、免疫沉淀测定和免疫组织化学。
在某些实施方案中,预期本文提供的抗体和/或结合多肽的氨基酸序列变体。例如,可能期望改进抗体和/或结合多肽的结合亲和力和/或其它生物学性质。抗体和/或结合多肽的氨基酸序列变体可通过将合适的修饰引入编码抗体和/或结合多肽的核苷酸序列或通过肽合成来制备。这种修饰包括例如,抗体和/或结合多肽的氨基酸序列内的残基的缺失和/或插入和/或取代。可进行缺失、插入和取代的任何组合以获得最终的构建体,只要最终的构建体具有期望的特征,例如,靶结合(例如,和激活蛋白诸如激活蛋白e和/或激活蛋白c结合)。
可在hvr中进行改变(例如,取代),例如以改进抗体亲和力。这种改变可在hvr“热点”,即由在体细胞成熟过程中经历高频率的突变的密码子编码的残基[参见,例如,chowdhury(2008)methodsmol.biol.207:179-196(2008)]和/或sdrs(a-cdrs)中进行,且测试所得变体vh或vl的结合亲和力。本领域已描述通过构建二级文库和从其中重新选择的亲和力成熟[参见,例如,hoogenboom等,methodsinmolecularbiology178:1-37,o'brien等编辑,humanpress,totowa,n.j.,(2001)]。在亲和力成熟的一些实施方案中,通过多种方法的任一种将多样性引入经选择用于成熟的可变基因中(例如,易错pcr、链改组或寡核苷酸指导的诱变)。然后产生二级文库。然后筛选该文库以鉴定具有期望亲和力的任何抗体变体。引入多样性的另一种方法牵涉hvr指导的方法,其中几个hvr残基(例如,一次4-6残基)被随机化。牵涉抗原结合的hvr残基可被特别鉴定,例如,使用丙氨酸分区诱变或建模。具体而言,经常靶向cdr-h3和cdr-l3。
在某些实施方案中,取代、插入或缺失可在一个或多个hvr内发生,只要这种改变基本上不减少抗体结合抗原的能力。例如,基本上不减少结合亲和力的保守改变(例如,如本文提供的保守取代)可在hvr中进行。这种改变可在hvr“热点”或sdr之外。在上述提供的变体vh和vl序列的某些实施方案中,每个hvr是未改变的,或含有仅仅一个、两个或三个氨基酸取代。
用于鉴定抗体和/或结合多肽的可针对诱变靶向的残基或区域的有用方法被称为“丙氨酸分区诱变”,如cunningham和wells(1989)science,244:1081-1085所述的。在该方法中,残基或一组靶残基(例如,带电荷的残基,如arg、asp、his、lys和glu)被鉴定和被中性或带负电荷的氨基酸(例如,丙氨酸或多丙氨酸(polyalanine))置换,以确定抗体-抗原的相互作用是否受到影响。进一步的取代可在显示对最初取代的功能敏感性的氨基酸位置引入。可选地,或另外,测定抗原-抗体复合体的晶体结构以鉴定抗体和抗原之间的接触点。这种接触残基和邻近残基可作为取代的候选物被靶向或消除。变体可经筛选以确定它们是否含有期望的性质。
氨基酸序列插入包括长度从1个残基到包含一百或更多个残基的多肽变化的氨基-和/或羧基-末端融合物,以及单个或多个氨基酸残基的序列内(intrasequence)插入。末端插入的实例包括具有n-末端甲硫氨酰残基的抗体。抗体分子的其它插入变体包括抗体的n-或c-末端融合至酶(例如,对于adept)或增加抗体的血清半衰期的多肽。
在某些实施方案中,本文提供的抗体和/或结合多肽可进一步修饰以含有本领域已知的且容易获得的另外的非蛋白部分。适合于衍生抗体和/或结合多肽的部分包括但不限于水溶性聚合物。水溶性聚合物的非限制性实例包括但不限于聚乙二醇(peg)、乙二醇/丙二醇的共聚物、羧基甲基纤维素、葡聚糖、聚乙烯醇、聚乙烯吡咯烷酮、聚-1,3-二氧杂环戊烷、聚-1,3,6-三氧杂环已烷、乙烯/马来酐共聚物、聚氨基酸(均聚物或无规共聚物)、和葡聚糖或聚(n-乙烯吡咯烷酮)聚乙二醇、丙二醇(propropyleneglycol)均聚物、聚环氧丙烷/环氧乙烷共聚物、聚氧乙基化多元醇(例如,甘油)、聚乙烯醇和其混合物。聚乙二醇丙醛由于其在水中的稳定性可具有制造中的益处。聚合物可具有任何分子量且可以是分支的或未分支的。附着至抗体和/或结合多肽的聚合物的数目可改变,且如果附着超过一个聚合物,则它们可以是相同的或不同的分子。通常,用于衍生的聚合物的数目和/或类型可基于以下考虑来确定,包括但不限于待改进的抗体和/或结合多肽的特定性质或功能,无论抗体衍生物和/或结合多肽衍生物是否将在限定的条件下用于疗法中。
d.小分子拮抗剂
在其它方面,待根据本文描述的方法和用途使用的actriib拮抗剂是小分子(actriib拮抗剂小分子)或小分子拮抗剂的组合。actriib拮抗剂小分子或小分子拮抗剂的组合可以抑制例如一种或多种actriib配体(例如,激活蛋白、gdf11、gdf8、gdf3、bmp6和/或bmp10)、i型受体(例如,alk4、alk5和/或alk7)、ii型受体(例如,actriib)和/或共同受体。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制由一种或多种actriib配体介导的信号传导,例如,如在基于细胞的测定、如本文所述的那些中所测定的。如本文所述的,可以单独或与一种或多种支持疗法或活性剂组合使用actriib拮抗剂小分子,以治疗、预防骨髓纤维化或降低其进展速率和/或严重性,特别是治疗、预防一种或多种骨髓纤维化相关并发症(例如,脾肿大、髓外造血、贫血和纤维化)或降低其进展速率和/或严重性,和/或治疗用janus激酶抑制剂治疗的患者。
在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少gdf11,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少gdf8,任选地进一步抑制gdf11、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少激活蛋白(激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be),任选地进一步抑制gdf8、gdf11、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少激活蛋白b,任选地进一步抑制gdf8、gdf11、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少bmp6,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、gdf3、gdf11、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少gdf3,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp15、bmp6、gdf11、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少bmp10,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp15、bmp6、gdf11、gdf3、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少actriib,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp15、bmp6、gdf11、gdf3、bmp10、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少alk4,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp15、bmp6、gdf11、gdf3、actriib、bmp10、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少alk5,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp15、bmp6、gdf11、gdf3、actriib、alk4、bmp10和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂小分子或小分子拮抗剂的组合抑制至少alk7,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp15、bmp6、gdf11、gdf3、actriib、alk4、alk5和bmp10中的一种或多种。在一些实施方案中,如本文所公开的actriib拮抗剂小分子或小分子拮抗剂的组合不抑制或基本上不抑制bmp9。在一些实施方案中,如本文所公开的actriib拮抗剂小分子或小分子拮抗剂的组合不抑制或基本上不抑制激活蛋白a。
actriib拮抗剂小分子可以是直接或间接抑制剂。例如,间接小分子拮抗剂或小分子拮抗剂的组合可以抑制至少一种或多种actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白b、激活蛋白bc、激活蛋白ae或激活蛋白be)、gdf11、bmp10、bmp9、bmp6、bmp5、gdf3和/或gdf8]、i型受体(例如,alk4、alk5和/或alk7)、ii型受体(例如,actriib)、共同受体和/或一种或多种下游actriib信号传导组分(例如,smads)的表达(例如,转录、翻译、细胞分泌或其组合)。可选地,直接小分子拮抗剂或小分子拮抗剂的组合可以直接结合和抑制例如一种或多种一种或多种actriib配体[例如,激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白b、激活蛋白bc、激活蛋白ae或激活蛋白be)、gdf11、bmp10、bmp9、bmp6、bmp5、gdf3和/或gdf8]、i型受体(例如,alk4、alk5和/或alk7)、ii型受体(例如,actriib)、共同受体和/或一种或多种下游actriib信号传导组分(例如,smads)。一种或多种间接和一种或多种直接actriib拮抗剂小分子的组合可以根据本文公开的方法使用。
本公开内容的结合小分子拮抗剂可使用已知的方法鉴定和化学合成(参见,例如,pct公开号wo00/00823和wo00/39585)。通常,本公开内容的小分子拮抗剂通常大小小于约2000道尔顿,可选地,大小小于约1500、750、500、250或200道尔顿,其中这种有机小分子能够结合、优选地特异性结合如本文所述的多肽。这些小分子拮抗剂可使用众所周知的技术在没有过度实验的情况下鉴定。在这方面,注意用于针对能够结合多肽靶的分子筛选有机小分子文库的技术是本领域众所周知的(参见,例如,国际专利公开号wo00/00823和wo00/39585)。
本公开内容的结合有机小分子可以是例如,醛、酮、肟、腙、缩氨基脲、卡巴肼、伯胺、仲胺、叔胺、n-取代的肼、酰肼、醇、醚、硫醇、硫醚、二硫化物、羧酸、酯、酰胺、脲、氨基甲酸酯、碳酸酯、缩酮、酮缩硫醇、缩醛、硫缩醛、芳基卤、芳基磺酸酯、烷基卤、烷基磺酸酯、芳族化合物、杂环化合物、苯胺、链烯、炔、二醇、氨基醇、噁唑烷、噁唑啉、噻唑烷、噻唑啉、烯胺、磺酰胺、环氧化物、氮丙啶、异氰酸酯、磺酰氯、重氮化合物和酰基氯。
e.多核苷酸拮抗剂
在其它方面,待根据本文公开的方法和用途使用的actriib拮抗剂是多核苷酸(actriib拮抗剂多核苷酸)或多核苷酸的组合。actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合可以抑制例如一种或多种actriib配体(例如,激活蛋白、gdf11、gdf8、gdf3、bmp6和/或bmp10)、i型受体(例如,alk4、alk5和/或alk7)、ii型受体(例如,actriib)、共同受体和/或下游信号传导组分(例如,smads)。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制由一种或多种actriib配体介导的信号传导,例如,如在基于细胞的测定、如本文所述的那些中所测定的。如本文所述的,可以单独或与一种或多种支持疗法或活性剂组合使用actriib拮抗剂多核苷酸,以治疗、预防骨髓纤维化或降低其进展速率和/或严重性,特别是治疗、预防一种或多种骨髓纤维化相关并发症(例如,脾肿大、髓外造血、贫血和纤维化)或降低其进展速率和/或严重性,和/或治疗用janus激酶抑制剂治疗的患者。
在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少gdf11,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少gdf8,任选地进一步抑制gdf11、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少激活蛋白(激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be),任选地进一步抑制gdf8、gdf11、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少激活蛋白b,任选地进一步抑制gdf8、gdf11、gdf3、bmp6、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少bmp6,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、gdf3、gdf11、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少gdf3,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp6、gdf11、bmp10、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少bmp10,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp6、gdf11、gdf3、actriib、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少actriib,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp6、gdf11、gdf3、bmp10、alk4、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少alk4,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp6、gdf11、gdf3、actriib、bmp10、alk5和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少alk5,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp6、gdf11、gdf3、actriib、alk4、bmp10和alk7中的一种或多种。在一些实施方案中,actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合抑制至少alk7,任选地进一步抑制gdf8、激活蛋白(例如,激活蛋白a、激活蛋白b、激活蛋白c、激活蛋白e、激活蛋白ab、激活蛋白ac、激活蛋白bc、激活蛋白ae和/或激活蛋白be)、bmp6、gdf11、gdf3、actriib、alk4、alk5和bmp10中的一种或多种。在一些实施方案中,如本文所公开的actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合不抑制或基本上不抑制bmp9。在一些实施方案中,如本文所公开的actriib拮抗剂多核苷酸或多核苷酸拮抗剂的组合不抑制或基本上不抑制激活蛋白a。
在一些实施方案中,本公开内容的多核苷酸拮抗剂可以是反义核酸、rnai分子[例如,小干扰rna(sirna)、小-发夹rna(shrna)、微rna(mirna)]、适体和/或核酶。人gdf11、gdf8、激活蛋白(激活蛋白a、激活蛋白b、激活蛋白c和激活蛋白e)、bmp6、gdf3、actriib、alk4、alk5、alk7和bmp10的核酸和氨基酸序列是本领域已知的。此外,生成多核苷酸拮抗剂的许多不同方法是本领域众所周知的。因此,根据本公开内容使用的多核苷酸拮抗剂可由本领域技术人员基于本领域的知识和本文提供的教导常规制备。
反义技术可用于通过反义dna或rna或通过三股螺旋形成来控制基因表达。反义技术讨论于例如,okano(1991)j.neurochem.56:560;oligodeoxynucleotidesasantisenseinhibitorsofgeneexpression,crcpress,bocaraton,fla.(1988)。三股螺旋形成讨论于例如,cooney等(1988)science241:456;和dervan等,(1991)science251:1300。该方法基于多核苷酸与互补dna或rna的结合。在一些实施方案中,反义核酸包含单链的rna或dna序列,其与本文公开的基因的rna转录物的至少一部分互补。然而,绝对互补性尽管是优选的,但不是必需的。
本文提及的“与rna的至少一部分互补的”序列是指具有足够的互补性以能够与rna杂交、形成稳定的双链体的序列;在本文公开的基因的双链反义核酸的情况下,可因此测试双链体dna的单链,或可测定三链体形成。杂交能力将取决于互补性的程度和反义核酸的长度两者。通常,杂交核酸越长,其可含有且仍形成稳定的双链体(或根据具体情况,三链体)的与rna的碱基错配越多。本领域技术人员可通过使用确定杂交的复合体的解链温度的标准程序来确定可允许的错配程度。
与信使(message)的5'端、例如直至和包括aug起始密码子的5'-非翻译序列互补的多核苷酸应在抑制翻译中最有效地起作用。然而,与mrna的3'-非翻译序列互补的序列已显示也有效抑制mrna的翻译[参见,例如,wagner,r.,(1994)nature372:333-335]。因此,与本公开内容的基因的5'-或3'-非翻译、非编码区互补的寡核苷酸可用于反义方法中以抑制内源mrna的翻译。与mrna的5'-非翻译区互补的多核苷酸应包括aug起始密码子的互补序列(complement)。与mrna编码区互补的反义多核苷酸是较不有效的翻译抑制剂,但可以根据本公开内容的方法使用。无论是设计为与本公开内容的mrna的5'-、3'-还是编码区杂交,反义核酸长度都应为至少6个核苷酸且优选为长度从6到约50个核苷酸变化的寡核苷酸。在具体方面,寡核苷酸为至少10个核苷酸、至少17个核苷酸、至少25个核苷酸或至少50个核苷酸。
在一个实施方案中,本公开内容的反义核酸通过从外源序列转录在细胞内产生。例如,载体或其部分经转录,产生本公开内容的基因的反义核酸(rna)。这种载体将含有编码期望的反义核酸的序列。这种载体可保持附加型或成为染色体整合的,只要其可被转录以产生期望的反义rna。这种载体可通过本领域标准的重组dna技术方法构建。载体可以是用于在脊椎动物细胞中复制和表达的质粒、病毒或本领域已知的其它载体。编码本公开内容的期望的基因或其片段的序列的表达可通过本领域已知的在脊椎动物、优选地人细胞中起作用的任何启动子。这种启动子可以是诱导型或组成型的。这种启动子包括但不限于sv40早期启动子区[参见,例如,benoist和chambon(1981)nature290:304-310]、在劳斯肉瘤病毒的3'长-末端重复序列中含有的启动子[参见,例如,yamamoto等(1980)cell22:787-797]、疱疹胸苷启动子[参见,例如,wagner等(1981)proc.natl.acad.sci.u.s.a.78:1441-1445]和金属硫蛋白基因的调节性序列[参见,例如,brinster,等(1982)nature296:39-42]。
在一些实施方案中,多核苷酸拮抗剂是干扰rna(rnai)分子,其靶向以下中的一种或多种的表达:gdf11、gdf8、激活蛋白(激活蛋白a、激活蛋白b、激活蛋白c和激活蛋白e)、bmp6、actriib、gdf3、alk4、alk5、alk7和bmp10。rnai是指干扰靶向的mrna的表达的rna的表达。具体而言,rnai通过与特定的mrna通过sirna(小干扰rna)相互作用来沉默靶向的基因。dsrna复合体然后被靶向用于由细胞降解。sirna分子是长度10-50个核苷酸的双链的rna双链体,其干扰足够互补(例如,与该基因具有至少80%同一性)的靶基因的表达。在一些实施方案中,sirna分子包含与靶基因的核苷酸序列具有至少85、90、95、96、97、98、99或100%同一性的核苷酸序列。
额外的rnai分子包括短发夹rna(shrna);以及短干扰发夹和微rna(mirna)。shrna分子含有通过环连接的来自靶基因的有义和反义序列。shrna从细胞核转运至细胞质并且其与mrna一起降解。对于rnai,poliii或u6启动子可用于表达rna。paddison等[genes&dev.(2002)16:948-958,2002]已经使用折叠成发夹的小的rna分子作为实现rnai的工具。因此,这种短发夹rna(shrna)分子也有利地用于本文所述的方法中。功能性shrna的茎和环的长度不同;在不影响沉默活性的情况下,茎长度可从约25到约30nt的任何地方变化,且环大小可从4到约25nt变化。尽管不希望受任何特定理论束缚,但认为这些shrna类似于dicerrna酶的双链rna(dsrna)产物,并且在任何情况下都具有相同的抑制特定基因表达的能力。shrna可从慢病毒载体表达。mirna是长度约10-70个核苷酸的单链rna,其最初转录为特征在于“茎-环”结构的前-mirna,其在通过risc进一步加工后,随后被加工成成熟mirna。
介导rnai的分子,包括但不限于sirna,可通过化学合成(hohjoh,febslett521:195-199,2002)、dsrna的水解(yang等,procnatlacadsciusa99:9942-9947,2002),通过用t7rna聚合酶体外转录(donzeet等,nucleicacidsres30:e46,2002;yu等,procnatlacadsciusa99:6047-6052,2002)和通过使用核酸酶如大肠杆菌rna酶iii的双链rna水解(yang等,procnatlacadsciusa99:9942-9947,2002)体外产生。
根据另一个方面,本公开内容提供了多核苷酸拮抗剂,其包括但不限于诱饵dna、双链dna、单链dna、复合dna、被囊的(encapsulated)dna、病毒dna、质粒dna、裸rna、被囊的rna、病毒rna、双链rna、能够产生rna干扰的分子或其组合。
在一些实施方案中,本公开内容的多核苷酸拮抗剂是适体。适体是核酸分子,包括双链dna和单链rna分子,其结合和形成特异性结合靶分子的三级结构。适体的产生和治疗用途是本领域充分确立的(参见,例如,美国专利号5,475,096)。关于适体的额外信息可见于美国专利申请公开号20060148748。核酸适体使用本领域已知的方法选择,例如通过指数富集配体系统进化(systematicevolutionofligandsbyexponentialenrichment)(selex)方法。selex是具有与靶分子高度特异性结合的核酸分子的体外进化的方法,如描述于例如,美国专利号5,475,096;5,580,737;5,567,588;5,707,796;5,763,177;6,011,577和6,699,843中的。鉴定适体的另一种筛选方法描述于美国专利号5,270,163。selex方法基于核酸形成多种二维和三维结构的能力,以及核苷酸单体内充当与实际上任何化合物(无论是单体还是聚合的,包括其它核酸分子和多肽)的配体(形成特异性结合对)的可用化学多功能性。任何大小或组成的分子都可充当靶。selex方法牵涉从候选寡核苷酸的混合物的选择,和使用相同的通用选择方案逐步重复结合、分开和扩增,以实现期望的结合亲和力和选择性。从可包含随机化序列的区段的核酸的混合物开始,selex方法包括以下步骤:使混合物与靶在有利于结合的条件下接触;使未结合的核酸与已经特异性结合至靶分子的那些核酸分开;解离核酸-靶复合体;扩增从核酸-靶复合体解离的核酸以得到配体富集的核酸混合物。结合、分开、解离和扩增的步骤重复如所需要的那么多循环,以得到以高亲和力和特异性结合靶分子的核酸配体。
一般,将这种结合分子单独施用于动物[参见,例如,o'connor(1991)j.neurochem.56:560],但这种结合分子也可从宿主细胞摄取的多核苷酸体内表达、和体内表达[参见,例如,oligodeoxynucleotidesasantisenseinhibitorsofgeneexpression,crcpress,bocaraton,fla.(1988)]。
f.促滤泡素抑制素和flrg拮抗剂
在其它方面,actriib拮抗剂是促滤泡素抑制素或flrg多肽。如本文所用的,促滤泡素抑制素和/或flrg多肽可单独或与一种或多种支持疗法或活性剂组合,以治疗、预防骨髓纤维化或降低其进展速率和/或严重性,特别是治疗、预防一种或多种骨髓纤维化相关并发症(例如,脾肿大、髓外造血、贫血和纤维化)或降低其进展速率和/或严重性,和/或治疗用janus激酶抑制剂治疗的患者。
术语“促滤泡素抑制素多肽”包括包含促滤泡素抑制素的任何天然存在的多肽以及其保留有用活性的任何变体(包括突变体、片段、融合物和肽模拟物形式)的多肽,且进一步包括促滤泡素抑制素的任何功能单体或多聚体。在某些优选实施方案中,本公开内容的促滤泡素抑制素多肽结合和/或抑制激活蛋白活性、特别是激活蛋白a。促滤泡素抑制素多肽的保留激活蛋白结合性质的变体可以基于先前的牵涉促滤泡素抑制素和激活蛋白相互作用的研究鉴定。例如,wo2008/030367公开了特定的促滤泡素抑制素结构域(“fsd”),其显示对于激活蛋白结合是重要的。如在下文seqidno:65-67中所示的,促滤泡素抑制素n-末端结构域(“fsnd”seqidno:65)、fsd2(seqidno:67)和较少程度上fsd1(seqidno:66)代表对于激活蛋白结合是重要的促滤泡素抑制素内的示例性结构域。此外,用于制备和测试多肽文库的方法在上文的actrii多肽的上下文中进行描述,且这种方法还涉及制备和测试促滤泡素抑制素的变体。促滤泡素抑制素多肽包括衍生自任何已知促滤泡素抑制素的序列的多肽,其具有与促滤泡素抑制素多肽的序列具有至少约80%同一性和任选地至少85%、90%、95%、96%、97%、98%、99%或更大同一性的序列。促滤泡素抑制素多肽的实例包括成熟的促滤泡素抑制素多肽或人促滤泡素抑制素前体多肽的较短的同种型或其它变体(seqidno:63),如描述于例如wo2005/025601中的。
人促滤泡素抑制素前体多肽同种型fst344如下:
(seqidno:63;ncbi参考号np_037541.1)
信号肽加下划线;上文加下划线的还有最后27个残基,其代表区分该促滤泡素抑制素同种型与下文所示的较短的促滤泡素抑制素同种型fst317的c-末端延伸。
人促滤泡素抑制素前体多肽同种型fst317如下:
信号肽加下划线。
促滤泡素抑制素n-末端结构域(fsnd)序列如下:
fsd1和fsd2序列如下:
在其它方面,用于根据本文公开的方法使用的药剂是促滤泡素抑制素-样相关基因(flrg),也称为促滤泡素抑制素-相关蛋白3(fstl3)。术语“flrg多肽”包括包含flrg的任何天然存在的多肽以及其保留有用活性的任何变体(包括突变体、片段、融合物和肽模拟物形式)的多肽。在某些优选实施方案中,本公开内容的flrg多肽结合和/或抑制激活蛋白活性、特别是激活蛋白a。flrg多肽的保留激活蛋白结合性质的变体可以使用测定flrg和激活蛋白相互作用的常规方法鉴定(参见,例如,us6,537,966)。此外,用于制备和测试多肽文库的方法在上文的actrii多肽的上下文中进行描述,且这种方法还涉及制备和测试flrg的变体。flrg多肽包括衍生自任何已知flrg的序列的多肽,其具有与flrg多肽的序列具有至少约80%同一性和任选地至少85%、90%、95%、97%、99%或更大同一性的序列。
人flrg前体(促滤泡素抑制素-相关蛋白3前体)多肽如下:
信号肽加下划线。
在某些实施方案中,促滤泡素抑制素多肽和flrg多肽的功能变体或修饰形式包括融合蛋白,其具有促滤泡素抑制素多肽或flrg多肽的至少一部分、和一个或多个融合结构域如例如促进多肽的分离、检测、稳定化或多聚化的结构域。合适的融合结构域在上文参考actriib多肽详细论述。在一些实施方案中,本公开内容的拮抗剂药剂是包含融合至fc结构域的促滤泡素抑制素多肽的激活蛋白-结合部分的融合蛋白。在另一个实施方案中,本公开内容的拮抗剂药剂是包含融合至fc结构域的flrg多肽的激活蛋白-结合部分的融合蛋白。
3.筛选测定
在某些方面,本公开内容涉及主题actriib多肽及其变体(例如,gdf8捕获物)鉴定为actriib多肽的激动剂或拮抗剂的化合物(药剂)的用途。可以测试通过该筛选鉴定的化合物,以评估例如在动物模型中它们治疗骨髓纤维化的能力。
存在许多筛选用于通过靶向actriib信号传导(例如,smad信号传导)治疗骨髓纤维化的治疗剂的方法。在某些实施方案中,可进行化合物的高通量筛选以鉴定在选择的细胞系上干扰actriib-介导的作用的药剂。在某些实施方案中,进行该测定以筛选和鉴定特异性抑制或减少actriib多肽与其结合配偶体如actriib配体(例如,激活蛋白a、激活蛋白b、激活蛋白ab、激活蛋白c、gdf8、gdf3、gdf11或bmp10)的结合的化合物。可选地,该测定可用于鉴定增强actrii多肽与其结合配偶体如actriib配体的结合的化合物。在进一步实施方案中,化合物可通过其与actriib多肽相互作用的能力来鉴定。
多种测定形式将是足够的,并且根据本公开内容,本文未明确描述的那些将仍然被本领域普通技术人员所理解。如本文所述的,本发明的测试化合物(药剂)可通过任何组合化学方法产生。可选地,主题化合物可以是体内或体外合成的天然存在的生物分子。待测试其充当组织生长的调制剂的能力的化合物(药剂)可例如,由细菌、酵母、植物或其它生物产生(例如,天然产物),化学产生(例如,小分子,包括肽模拟物)或重组产生。本发明预期的测试化合物包括非肽基有机分子、肽、多肽、肽模拟物、糖、激素和核酸分子。在某些实施方案中,测试试剂是具有小于约2,000道尔顿的分子量的小的有机分子。
本公开内容的测试化合物可作为单一的离散实体提供,或在较大复杂性的文库(如通过组合化学制备的)中提供。这些文库可包含,例如,醇、烷基卤、胺、酰胺、酯、醛、醚和其它类型的有机化合物。测试化合物至测试系统的呈递可以为分离的形式或作为化合物的混合物,尤其是在最初筛选步骤中。任选地,化合物可任选地用其它化合物衍生,且具有促进化合物的分离的衍生基团。衍生基团的非限制性实例包括生物素、荧光素、洋地黄毒苷、绿色荧光蛋白、同位素、多组氨酸、磁珠、谷胱甘肽s-转移酶(gst)、光可活化的交联剂或其任何组合。
在测试化合物和天然提取物的文库的许多药物-筛选程序中,期望高通量测定以使在给定的时间段内调查的化合物的数目最大化。在无细胞系统中进行的测定,如可用纯化或半纯化的蛋白衍生的,作为“初级”筛选经常是优选的,这是因为它们可经产生以允许由测试化合物介导的分子靶中的改变的快速发展和相对容易检测。此外,测试化合物的细胞毒性或生物利用率的影响在体外系统中通常可忽略,该测定而是主要聚焦于药物对分子靶的影响,如可以在actriib多肽与其结合配偶体(例如,actriib配体)之间的结合亲和力的改变中显现的。
仅仅为了举例说明,在本公开内容的示例性筛选测定中,如对于测定的目的合适的,将目标化合物与分离和纯化的通常能够结合actriib配体的actriib多肽接触。然后向化合物和actriib多肽的混合物中加入含有actriib配体(例如,gdf11)的组合物。actriib/actriib-配体复合体的检测和定量提供了用于测定化合物抑制(或加强)actriib多肽和其结合蛋白之间的复合体形成的功效的手段。化合物的功效可通过从使用各种浓度的测试化合物获得的数据产生剂量-反应曲线来评估。此外,也可进行对照测定以提供基线用于比较。例如,在对照测定中,分离和纯化的actriib配体被加入包含actriib多肽的组合物,并在没有测试化合物的情况下定量actriib/actriib配体复合体的形成。将理解的是,通常,其中可混合反应物的顺序可改变,且可同时混合。此外,代替纯化的蛋白,细胞提取物和裂解物可用于提供合适的无细胞测定系统。
actriib多肽及其结合蛋白之间的复合体形成可通过多种技术检测。例如,复合体形成的调节可以使用例如,可检测标记的蛋白如放射性标记的(例如,32p、35s、14c或3h)、荧光标记的(例如,fitc)或酶促标记的actriib多肽和/或其结合蛋白,通过免疫测定或通过层析检测来定量。
在某些实施方案中,本公开内容预期荧光偏振测定和荧光共振能量转移(fret)测定在直接或间接测量actriib多肽及其结合蛋白之间相互作用的程度中的用途。此外,其它检测模式,如基于光波导(参见,例如,pct公开wo96/26432和美国专利号5,677,196)、表面等离振子共振(spr)、表面电荷传感器和表面力传感器的那些,与本公开内容的许多实施方案相容。
此外,本公开内容预期相互作用捕获物测定、也称为“双杂交测定”用于鉴定破坏或加强actriib多肽及其结合配偶体之间相互作用的药剂的用途。参见,例如,美国专利号5,283,317;zervos等(1993)cell72:223-232;madura等(1993)jbiolchem268:12046-12054;bartel等(1993)biotechniques14:920-924;和iwabuchi等(1993)oncogene8:1693-1696)。在具体实施方案中,本公开内容预期反向双杂交系统鉴定解离actrii多肽或gdf捕获物及其结合蛋白之间相互作用的化合物(例如,小分子或肽)的用途[参见,例如,vidal和legrain,(1999)nucleicacidsres27:919-29;vidal和legrain,(1999)trendsbiotechnol17:374-81;和美国专利号5,525,490;5,955,280;和5,965,368]。
在某些实施方案中,主题化合物通过其与actriib多肽相互作用的能力来鉴定。在化合物和actriib多肽之间的相互作用可以是共价或非共价的。例如,这种相互作用可在蛋白水平上使用体外生物化学方法,包括光交联、放射性标记的配体结合和亲和层析鉴定[参见,例如,jakobywb等(1974)methodsinenzymology46:1]。在某些情况下,化合物可在基于机制的测定(如检测结合actriib多肽的化合物的测定)中筛选。这可包括固相或液相结合事件。可选地,编码actriib多肽的基因可与报道系统(例如,β-半乳糖苷酶、萤光素酶或绿色荧光蛋白)转染至细胞中,且针对文库优选地通过高通量筛选或以文库的个别成员进行筛选。可使用其它基于机制的结合测定;例如,检测自由能中的变化的结合测定。结合测定可用靶进行,所述靶固定至孔、珠或芯片,或通过固定的抗体捕获,或通过毛细管电泳分离(resolved)。结合的化合物可通常使用比色终点(colorimetricendpoints)或荧光或表面等离振子共振检测。
4.示例性治疗用途
如在本公开内容的实施例中描述的,已经发现,actriib拮抗剂(抑制剂)可用于治疗骨髓纤维化患者,特别是改善疾病的各种并发症,包括例如脾肿大、髓外造血和纤维化。特别地,本文呈现的数据显示,gdf捕获物多肽在骨髓纤维化的jak2v617f模型中减少脾肿大、髓外造血和纤维化。因此,在某些方面,在本公开内容涉及用于治疗骨髓纤维化、特别是治疗或预防骨髓纤维化的一种或多种并发症(脾肿大、髓外造血、贫血和纤维化)的组合物和方法,其通过向有需要的患者施用有效量的一种或多种actriib拮抗剂、任选地与用于治疗骨髓纤维化的一种或多种其它支持疗法或活性剂组合实施。
如本文所用,“预防”病症或状况的治疗剂是指化合物,其在统计学样品中相对于未治疗的对照样品减少治疗样品中病症或状况的发生、或相对于未治疗的对照样品延迟病症或状况的一种或多种症状的发作或降低其严重性。如本文所用的术语“治疗”包括一旦其已经确立,则改善或消除状况。在任一情况下,预防或治疗可在由内科医生或其它卫生保健提供者提供的诊断和施用治疗剂的预期结果中辨别。
通常,本公开内容中描述的疾病或状况的治疗或预防通过施用有效量的actriib拮抗剂来实现。药剂的有效量是指在必需的剂量和时间段有效实现期望的治疗或预防结果的量。本公开内容的药剂的治疗有效量可根据因素如个体的疾病状态、年龄、性别和体重以及药剂在个体中引出期望的反应的能力而改变。预防有效量是指在必需的剂量和时间段有效实现期望的预防结果的量。
术语“主体”、“个体”或“患者”在整个说明书中是可互换的,并且通常是指哺乳动物。哺乳动物包括但不限于,家畜(例如,牛、羊、猫、狗和马)、灵长类动物(例如,人和非人灵长类动物如猴)、兔和啮齿类动物(例如,小鼠和大鼠)。
骨髓纤维化是造血作用的克隆性肿瘤病症,其一般特征在于进行性骨髓纤维化,导致越来越无效的造血、髓外造血、各种炎性并发症和缩短的存活[mascarenhas等.(2012)currmedchem19:4399-4413;和vannucchi等.(2011)hematolamsochematoleducprog2011:222-230]。它是产生过量细胞的骨髓的骨髓增生性病症之一。由异常造血细胞克隆产生细胞因子例如成纤维细胞生长因子导致通过胶原纤维化由结缔组织替代骨髓的造血组织。造血组织的减少损害了患者产生新血细胞的能力,导致进行性全血细胞减少症(所有血液类型的短缺)。然而,增殖和成纤维细胞和胶原蛋白沉积是次要现象,并且成纤维细胞本身不是异常细胞克隆的一部分。作为骨髓进行性瘢痕形成或纤维化的结果,因为造血细胞被迫迁移到其它区域,特别是肝和脾,患者发生髓外造血。这导致这些器官的扩大。在肝中,这种情况称为肝肿大。脾的扩大称为脾肿大,这也促成全血细胞减少症,特别是血小板减少症和贫血。也有在肺和淋巴结中发生的髓外造血的报道。髓外造血的另一个并发症是存在形状异常红细胞的异型红细胞症。骨髓纤维化的常见临床表现包括进行性肝脾肿大、血液计数异常和虚弱症状例如疲劳、体重减轻、盗汗、发热、瘙痒症、骨痛、早饱、腹痛或不适、关节痛、肌痛、感觉异常、恶病质、脾梗塞和出血。直到最近,对疾病进展有明确证明的影响的唯一治疗是异基因造血干细胞移植allohsct,但与治疗相关的死亡率高,且只有少数患者有资格进行这种强化疗法[gupta等(2012)blood120:1367–1379]。
在某些方面,actriib拮抗剂可单独使用或与一种或多种支持疗法或活性剂组合使用,以治疗、预防骨髓纤维化(例如,原发性骨髓纤维化、真性红细胞增多症后骨髓纤维化和特发性血小板增多症后骨髓纤维化)或降低其进展速率和/或严重性。特别地,actriib拮抗剂可单独使用或与一种或多种支持疗法或活性剂组合使用,以治疗、预防骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性,所述并发症包括例如无效造血、贫血、炎症、纤维化(例如骨髓纤维化、脾纤维化和肝纤维化)、全血细胞减少症、血小板减少症、髓外造血(例如脾髓外造血、肝髓外造血、肺髓外造血和淋巴髓外造血)、肝肿大、脾肿大、骨硬化症、骨髓纤维化、异型红细胞症、疲劳、体重减轻、盗汗、发热、瘙痒症、骨痛、早饱、腹痛或不适、关节痛、肌痛、感觉异常、恶病质、脾梗塞和出血。
原发性骨髓纤维化(pmf)的目前诊断是基于世界卫生组织(who)的标准,并且牵涉临床和实验室特征的综合评估[tefferia等.(2007)blood.110:1092–1097]。who诊断主要标准有三个:1)巨核细胞增殖和异型性(小至大的巨核细胞,且核/细胞质比率异常,和含染色质多的和不规则折叠的核和密集簇集),伴有网硬蛋白和/或胶原纤维化;或在不存在网硬蛋白纤维化的情况下,巨核细胞变化必须伴随髓细胞性增多、粒细胞增殖并且通常红细胞生成减少(即前纤维化原发性骨髓纤维化),2)不符合who关于慢性髓细胞性白血病、真性红细胞增多症、骨髓增生性综合征或其它髓样肿瘤的标准,和3)显示jak2v617f或其它克隆性标记物或没有反应性骨髓纤维化的证据。此外,who诊断次要标准有四个:1)成白红细胞增多病(leukoerythroblastosis),2)血清ldh水平升高,3)贫血,4)可触及的脾肿大。外周血成白红细胞增多病(即,存在有核红细胞、未成熟粒细胞和泪细胞(dacryocyte))是pmf的典型但不恒定的特征;前纤维化pmf可能不显示明显的成白红细胞增多病[kvasnicka等.(2010)amjhematol.85:62–69]。pmf中的骨髓纤维化通常与jak2v617f或突变型calr、或mpl、三体性9或del(13q)相关[hussein等.(2009)eurjhaematol.82:329–338]。因此,在与骨髓纤维化相关的髓样肿瘤存在的情况下,这些遗传标志物的存在强烈支持诊断pmf。在某些方面,本公开内容涉及actriib拮抗剂治疗、预防原发性骨髓纤维化或降低其进展速率和/或严重性,特别是治疗、预防原发性骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法和用途。
真性红细胞增多症后骨髓纤维化(post-pvmf)和原发性血小板增多症后骨髓纤维化(post-etmf)的目前诊断是基于国际mpn研究和治疗工作组(internationalworkinggroupformpnresearchandtreatment,iwg-mrt)发布的标准[barosig等.(2008)leukemia.22:437–438]。对于post-pvmf有两个iwg-mrt主要标准:1)按who标准定义的真性红细胞增多症的先前诊断的证明文件,和2)骨髓纤维化等级2-3(在0-3量表上)或等级3-4(在0-4量表上)。根据欧洲分类等级2-3:弥漫性、通常粗纤维网络且没有胶原化迹象(阴性三色染色)或弥漫性、粗纤维网络、具有胶原化区域(阳性三色染色)[thiele等.(2005)haematologica.90:1128–1132]。根据标准分类等级3-4:具有广泛交叉的网硬蛋白弥漫性和密集性增加,偶尔仅有局灶性的胶原束和/或局灶性骨硬化症,或具有广泛交叉的网硬蛋白弥漫性和密集性增加,具有粗糙胶原束,通常伴随明显的骨硬化症[manoharan等.(1979)brjhaematol43:185–190]。此外,iwg-mrt诊断性次要标准还有四个,其中两个必须连同post-pvmf诊断的iwg-mrt主要标准在患者中检测:1)在不存在细胞减灭性疗法的情况下贫血或持续失去对静脉切开放血术的要求,2)成白红细胞增多的外周血图片,3)脾肿大增加,定义为≥5cm的可触及的脾肿大增加或出现新的可触及的脾肿大,4)发生下列3个全身症状中的≥1个:6个月内体重丢失>10%,盗汗,不明原因的发热。post-etmf有两个iwg-mrt主要标准:1)由who标准定义的真性红细胞增多症的先前诊断的证明文件,2)骨髓纤维化等级2-3(在0-3量表上)或等级3-4(在0-4量表上)。此外,iwg-mrt诊断次要标准有五个,其中两项必须连同post-etmf诊断的iwg-mrt主要标准在患者中检测:1)贫血和≥2g/dl的从基线血红蛋白水平降低,2)成白红细胞增多的外周血图片,3)脾肿大增加,定义为≥5cm的可触及的脾肿大增加或出现新的可触及的脾肿大,4)乳酸脱氢酶增加,和5)发生下列3个全身症状中的≥1个:6个月内体重丢失>10%,盗汗,不明原因的发热。在某些方面,本公开内容涉及actriib拮抗剂治疗、预防真性红细胞增多症后骨髓纤维化或降低其进展速率和/或严重性,特别是治疗、预防真性红细胞增多症后骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法和用途。在某些方面,本公开内容涉及actriib拮抗剂治疗、预防原发性血小板增多症后骨髓纤维化或降低其进展速率和/或严重性,特别是治疗、预防血小板增多症后骨髓纤维化的一种或多种并发症或降低其进展速率和/或严重性的方法和用途。
骨髓纤维化的稳健预后建模始于2009年国际预后评分系统(ipss)的开发[cervantesf等.(2009)blood113:2895–2901]。骨髓纤维化的ipss适用于初次诊断时评估的患者,并使用5个独立的低存活预测因素:年龄>65岁,血红蛋白<10g/dl,白细胞计数>25×109/l,循环母细胞(blast)≥1%,并存在全身症状。0、1、2和≥3个不利因素的存在分别定义低、中等-1、中等-2和高风险疾病。相应的中值存活分别为11.3、7.9、4和2.3年。在某些方面,本公开内容涉及actriib拮抗剂治疗、预防根据ipss具有低、中等-1、中等-2或高风险骨髓纤维化的患者中的骨髓纤维化或降低其进展速率和/或严重性的方法和用途。在一些实施方案中,本公开内容涉及actriib拮抗剂预防或延迟根据ipss的骨髓纤维化风险进展(例如,根据ipss预防或延迟从低至中等-1风险、中等-1至中等-2风险和中等-2至高风险的风险进展)的方法和用途。在一些实施方案中,本公开内容涉及actriib拮抗剂促进或增加根据ipss的骨髓纤维化风险消退(例如,根据ipss促进或增加从高至中等-2风险、中等-2至中等-1风险和中等-1至低风险的消退)的方法和用途。
iwg-mrt随后开发了动态预后模型(动态国际预后评分系统[dipss]),该模型使用ipss中使用的相同预后变量,但可以在疾病过程中随时应用[passamontif等.(2010)blood.115:1703–1708]。dipss为血红蛋白<10g/dl分配两个而不是一个不利点,并相应修改风险分类:低(0个不利点),中等-1(1或2个点),中等-2(3或4个点),高(5或6个点)。未达到相应的中值存活,14.2、4和1.5年。在某些方面,本公开内容涉及actriib拮抗剂治疗、预防根据dipss具有低、中等-1、中等-2或高-风险骨髓纤维化的患者中的骨髓纤维化或降低其进展速率和/或严重性的方法和用途。在一些实施方案中,本公开内容涉及actriib拮抗剂预防或延迟根据dipss的骨髓纤维化风险进展(例如,根据dipss防止或延迟从低至中等-1风险、中等-1至中等-2风险和中等-2至高风险的风险进展)的方法和用途。在一些实施方案中,本公开内容涉及actriib拮抗剂促进或增加根据dipss的骨髓纤维化风险消退(例如,根据dipss促进或增加从高至中等-2风险、中等-2至中等-1风险和中等-1至低风险的消退)的方法和用途。
用于骨髓纤维化中存活的ipss-和dipss-独立的风险因素随后被鉴定并包括不利的核型(即,复杂的核型或单一或两种异常,包括+8,−7/7q−,i(17q),inv(3),−5/5q−,12p−或11q23重排)[hussein等.(2010)blood.115:496–499]、红细胞输入需求[tefferi等.(2009)amjhematol.85:14–17]和血小板计数<100×109/l[patnaik等.(2010)eurjhaematol.84:105–108]。因此,通过并入这另外三个dipss独立的风险因素将dipss修改为dipss-plus:血小板计数<100×109/l,红细胞输入需求和不利的核型。基于上述八个风险因素的四个dipss-plus风险类别为低(无风险因素)、中等-1(一个风险因素)、中等-2(两个或三个风险因素)和高(四个或更多个风险因素),具有15.4、6.5、2.9和1.3年的各自中值存活。在某些方面,本公开内容涉及actriib拮抗剂治疗、预防根据dipss-plus具有低、中等-1、中等-2或高-风险骨髓纤维化的患者中的骨髓纤维化或降低其进展速率和/或严重性的方法和用途。在一些实施方案中,本公开内容涉及actriib拮抗剂预防或延迟根据dipss-plus的骨髓纤维化风险进展(例如,根据dipss-plus防止或延迟从低至中等-1风险、中等-1至中等-2风险和中等-2至高风险的风险进展)的方法和用途。在一些实施方案中,本公开内容涉及actriib拮抗剂促进或增加根据dipss-plus的骨髓纤维化风险消退(例如,根据dipss-plus促进或增加从高至中等-2风险、中等-2至中等-1风险和中等-1至低风险的消退)的方法和用途。
自dipss-plus公布以来,已经公布了几个研究,其提示额外的预后信息。例如,通过单体核型,inv(3)/i(17q)异常,或循环母细胞>9%、白细胞≥40×109/l或其它不利核型中的任何两种,预测骨髓纤维化中的2年死亡率>80%[tefferi等.(2011)blood.118:4595–4598.]。类似地,骨髓纤维化中较差的存活与jak246/1单倍型的缺合子性、低jak2v617f等位基因负荷,或存在idh、ezh2、srsf2或asxl1突变有关[tefferi,ayalew(2014)am.j.hematol.89:916-925]。相反,jak2v617f、mpl或tet2突变的存在或不存在似乎不影响存活。骨髓纤维化中的存活也受到增加的血清il-8和il-2r水平以及游离血清轻链水平的影响,二者均独立于dipss-plus。最近,tefferi等研究了254名具有骨髓纤维化的患者,并报告了jak2的突变频率为58%、calr的突变频率为25%、mpl的突变频率为8%和对于所有三种突变9%野生型(即三重阴性)[tefferi等.(2014)leukemia.预发表为doi10.1038/leu.2014.3]。jak2/mpl-未突变病例中calr突变频率为74%。calr突变与更年轻的年龄、更高的血小板计数和更低的dipss-plus评分相关。calr突变的患者也不太可能贫血、需要输血或显示白细胞增多。在calr突变的患者中,剪接体突变并不常见。在随后的570例患者的国际研究中,作者报道calr+asxl1-患者中的存活最长(中值10.4年),calr-asxl1+患者中的存活最短(中值2.3年)[tefferi等.(2014)leukemia.预发表为doi10.1038/leu.2014.57]。calr+asxl1+和calr-asxl1-患者具有相似的存活,并被一起归入中等风险类别(中值存活5.8年)。随着总存活逐渐变得明显,携带某些突变(包括idh和srsf2)的患者中的无白血病存活也显著降低[tefferi等.(2012)leukemia.26:475–480;lasho等.(2012)blood.120:4168–4171]。另外,lnk和thpo中的突变也与骨髓纤维化相关。
janus激酶2(jak2)功能获得性突变jak2v617f的发现导致了引起骨髓纤维化的生物学的理解的显著改善,以及鲁索利替尼的开发,鲁索利替尼是jak2抑制剂,其为由fda批准用于治疗骨髓纤维化的第一个药物[baxter等(2005)lancet365:1054–1061;jamesc.等(2005)nature434:1144–1148;kralovics等(2005)nengljmed.352:1779–1790;和levine等(2005)cancercell7:387–397]。受体酪氨酸激酶的janus激酶家族包括四种不同的蛋白(jak1、jak2、jak3和tyk2),并且已知该家族蛋白在骨髓和淋巴细胞生长和发育中起关键作用。特别地,它们介导来自细胞因子受体的细胞内相互作用,导致信号转导转录激活子(stat)因子的激活和调节细胞增殖及分化的基因的下游促进[quintas-cardama等(2011)natrevdrugdiscov10:127–140]。jak2v617f突变导致jak2的组成性激活,并且因此促进骨髓细胞增殖和分化。正在进行临床试验的其它janus激酶抑制剂包括,例如,fedratinib(sar302503)、monoelotinib(cyt387)、帕克替尼、来他替尼、azd-1480、bms-911543、ns-018、ly2784544、sep-701、xl019和at-9283。
在某些方面,本公开内容涉及actriib拮抗剂治疗、预防具有以下一种或多种的患者中的骨髓纤维化或降低其进展速率和/或严重性的方法和用途:单体核型、inv(3)/i(17q)异常、循环母细胞>9%和/或白细胞≥40×109/l、对于jak246/1单倍型的缺合子性、jak2v617f突变、idh1突变、idh2突变、ezh2突变、srsf2突变、asxl1突变、增加的血清il-8水平、增加的血清il-2r水平、增加的游离轻链水平、jak1突变、jak2突变、jak3突变、tyk2突变、mpl突变、calr突变、calr+asxl1-、calr-askl1+、calr+askl1+、calr-askl1-、tet2突变、thpo突变和lnk突变。
贫血的管理可为治疗具有骨髓纤维化的患者的最具挑战性的方面之一[tefferia.(2011)blood117(13):3949-3504;barosi等.(2011)expertopinpharmacother12(10):1597-1611]。输血(全血或红细胞输入)是症状性贫血的骨髓纤维化患者的标准疗法。除输血外,还有多种常规药剂用于治疗这些患者中的贫血。例如,红细胞生成刺激剂[例如esa如促红细胞生成素(epo)及其衍生物]、雄激素(如庚酸睾酮和氟甲睾酮)、泼尼松、达那唑、沙利度胺、泼尼松和来那度胺常用于治疗骨髓纤维化患者中的贫血。一般来说,esa用于具有中度、非输血依赖性贫血和低血清促红细胞生成素水平的患者中。反应率在20-60%变化,且对于达贝泊汀-α比常规重组促红细胞生成素没有明确支持。esa反应通常是短暂的(约1年)。如果esa不起作用或疗效差,达那唑或雄激素制剂通常用于治疗贫血患者,且反应率为约20%。与减量(tapering)泼尼松联合的小剂量沙利度胺已在约20-40%的患者中产生贫血中的反应[thapaliya等.(2011)amjhematol86(1):86-98]。然而,沙利度胺治疗通常耐受性差,具有周围神经病变、便秘和嗜睡,导致在大多数患者中停止药物。在具有del(5q31)相关性贫血的骨髓纤维化患者中,来那度胺是推荐的一线疗法,因为已经报道了显著的改善,且贫血消除和偶尔证实的分子缓解[tefferi等.(2007)leukemia21(8):1827-1828]。在某些方面,本公开内容涉及actriib拮抗剂在具有贫血的患者中治疗、预防骨髓纤维化或降低其进展速率和/或严重性的方法和用途。在一些实施方案中,本公开内容涉及actriib拮抗剂治疗、预防骨髓纤维化患者中的贫血或降低其进展速率和/或严重性的方法和用途。在一些实施方案中,本公开内容涉及在有需要的患者中治疗、预防骨髓纤维化或降低其进展速率和/或严重性的方法,包括与一种或多种选自以下的另外的活性剂联合施用一种或多种actriib拮抗剂:红细胞生成刺激剂[例如esa如促红细胞生成素(epo)及其衍生物]、雄激素(例如庚酸睾酮和氟甲睾酮)、泼尼松、达那唑、沙利度胺、泼尼松和来那度胺。在一些实施方案中,本公开内容涉及治疗、预防有需要的骨髓纤维化患者中的贫血或降低其进展速率和/或严重性的方法,包括与一种或多种选自以下的另外的活性剂联合施用一种或多种actriib拮抗剂:促红细胞生成剂[例如esa如促红细胞生成素(epo)及其衍生物]、雄激素(如庚酸睾酮和氟甲睾酮)、泼尼松、达那唑、沙利度胺、泼尼松和来那度胺。在一些实施方案中,本公开内容涉及治疗、预防有需要的骨髓纤维化患者中的贫血或降低其进展速率和/或严重性的方法,包括与输血(全血或红细胞输入)联合施用一种或多种actriib拮抗剂。
当监测人中血红蛋白和/或血细胞比容水平时,对于适当年龄和性别类别的低于正常水平可能指示贫血,尽管考虑到个体差异。例如,在健康成人中血红蛋白水平为10-12.5g/dl且通常约为11.0g/dl被认为在正常范围内,尽管就治疗而言,较低的目标水平可能导致较少的心血管副作用。参见例如jacobs等(2000)nephroldialtransplant15,15-19。可选地,血细胞比容水平(由细胞占据的血液样本的体积百分比)可以用作贫血的量度。健康个体的血细胞比容水平从成年男性约41-51%、成年女性35-45%变化。在某些实施方案中,患者可以用给药方案治疗,所述给药方案旨在使患者恢复至红细胞、血红蛋白和/或红细胞比容的目标水平,或允许减少或消除红细胞输入(减少输入负荷),同时保持红细胞、血红蛋白和/或血细胞比容的可接受水平。由于血红蛋白和血细胞比容水平因人而异,最佳地,目标血红蛋白和/或血细胞比容水平可针对每个患者个体化。
在接受全血或红细胞的频繁输入的患者中,铁稳态的正常机制可能不堪重负,最终导致重要组织如心脏、肝和内分泌腺体中铁的毒性和潜在致命的累积。定期的红细胞输入需要暴露于各种血液供体单元,且因此更高的同种免疫风险。应用血管通路的困难、应用铁螯合作用的可用性和依从性以及高成本是限制红细胞输入次数可能有益的一些原因。
在某些方面,任选地与epo受体激活剂组合的一种或多种actriib拮抗剂可以与一种或多种铁螯合分子组合使用,以促进尿和/或便中的铁排泄并由此预防或逆转骨髓纤维化患者中的组织铁超载。有效的铁螯合剂应该能够选择性地结合和中和三价铁,这是非转铁蛋白结合的铁的氧化形式,其可能通过催化产生羟基自由基和氧化产物而导致大多数铁毒性[参见例如esposito等.(2003)blood102:2670-2677]。这些药剂在结构上是多样的,但都具有氧或氮供体原子,能够以1:1(六齿剂)、2:1(三齿)或3:1(二齿)化学计量形式与各个铁原子形成中和性八面体配位络合物[kalinowski等.(2005)pharmacolrev57:547-583]。通常,有效的铁螯合剂也具有相对低的分子量(例如小于700道尔顿),且在水和脂质中都具有溶解性,而能够接近受影响的组织。铁螯合分子的具体实例包括去铁胺,需要每日肠胃外施用的细菌来源的六齿剂,和口服活性合成剂去铁酮(二齿)和地拉罗西(三齿)。由同一天施用两种铁螯合剂组成的联合疗法在对螯合单药疗法没有反应的患者中显示出希望,并且也在克服应用单独去铁胺的患者依从性差的问题中显示出希望[cao等.(2011)pediatrrep3(2):e17;和galanello等.(2010)annnyacadsci1202:79-86]。
本公开内容的一种或多种actriib拮抗剂可与epo受体活化剂组合使用以实现红细胞的增加,特别是在较低剂量范围。这可能有益于减少已知的脱靶效应和与高剂量epo受体活化剂相关的风险。esa的主要不良作用包括例如血细胞比容或血红蛋白水平的过度增加和红细胞增多症。升高的血细胞比容水平可导致高血压(更特别是高血压的加重)。其中一些涉及高血压的已经报道的esa的其它不良作用是头痛、流感样综合征、分流阻塞、心肌梗塞和由于血栓形成的脑痉挛、高血压脑病和红细胞血细胞再生障碍。参见,例如,singibarti(1994)j.clininvestig72(suppl6),s36-s43;horl等(2000)nephroldialtransplant15(suppl4),51-56;delanty等(1997)neurology49,686-689;和bunn(2002)nengljmed346(7),522-523)。在某些实施方案中,本公开内容提供了治疗或预防骨髓纤维化患者中的贫血的方法,其通过向患者施用治疗有效量的一种或多种actriib拮抗剂和epo受体活化剂实施。在某些实施方案中,本公开内容的actriib拮抗剂可与epo受体活化剂组合使用,以降低这些活化剂在易受esa不良作用影响的患者中的所需剂量。这些方法可用于患者的治疗性和预防性治疗。
如果本公开内容的actriib拮抗剂通过与esa不同的机制起作用,这些拮抗剂可用于在对esa或其它epo受体活化剂不充分反应的患者中增加红细胞和血红蛋白水平。例如,本公开内容的actriib拮抗剂可能对下列患者有益,其中给予正常至增加的(>300iu/kg/周)剂量的esa不导致血红蛋白水平增加直至目标水平。对esa的不充分反应可以是组成型的(在第一次用esa治疗时观察到)或获得型的(在用esa重复治疗时观察到)。
细胞减灭剂(cytoreductiveagent)一直是用于大多数具有症状性脾肿大的患者的治疗选择。羟基尿素(羟基脲,hc)是最常用的细胞减灭剂,其在较高剂量通常产生适度的反应。然而,hc通常可以加重血细胞减少,且因此通常不很好地耐受。据报道,高达35%的用hc治疗的患者中的脾尺寸减小25%-50%[martínez-trillos等.(2010)annhematol.89(12):1233–1237]。在对hc不反应的患者中,可使用白消安或美法仑,尤其是在老年患者中,因为有证据表明这些药剂可增加白血病转化的频率。应用低剂量沙利度胺的脾反应低(<20%)。然而,来那度胺已显示在包括一些对在先沙利度胺治疗失败的患者的研究中导致33%的反应率。在大的顽固性脾肿大的情况下,每月静脉注射克拉屈滨疗程产生高达50%的反应,且严重但可逆的血细胞减少是主要毒性[faoro等.(2005)eurjhaematol74(2):117–120]。在最近的研究中,鲁索利替尼已被证明优于hc,并且因此正成为控制症状性或进行性脾肿大的一线药剂。不幸的是,鲁索利替尼的常见副作用是骨髓纤维化患者中贫血的发展或恶化。因此,尽管jak抑制剂可用于治疗脾肿大,它们实际上可加重骨髓纤维化的其它并发症,特别是贫血和贫血相关病症。
除了jak2抑制之外,正在研究用于治疗骨髓增生性病症的其它几种治疗策略,包括免疫调节药物(例如,pomalidomide)、mtor途径的哺乳动物靶标的抑制剂(例如,雷帕霉素、西罗莫司、deforolimus、依维莫司、temsirolimus、nvp-bez235、bgt226、sf1126、pk1-587、ink128、azd8055和azd2014)和表观遗传因子调节剂(例如,组蛋白脱乙酰酶抑制剂如givinostat(itf2357)、panobinostat(lbh589)和pracinostat)[mascarenhas等(2013)haematologica98(10):1499-1509]。
本公开内容进一步考虑actriib拮抗剂与一种或多种其它治疗方式组合在本文所述的患者治疗中的用途,例如,可将actriib拮抗剂与细胞毒素、免疫抑制剂、放射性毒性剂和/或治疗性抗体组合施用。本发明考虑的具体的共治疗剂包括但不限于类固醇类(例如皮质甾类,例如泼尼松)、免疫抑制和/或抗炎剂(例如γ-干扰素、环磷酰胺、硫唑嘌呤、甲氨蝶呤、青霉胺、环孢菌素、秋水仙碱、抗胸腺细胞球蛋白、麦考酚酸酯和羟氯喹)、细胞毒性药物、钙通道阻断剂(例如硝苯地平)、血管紧张素转化酶抑制剂(ace)抑制剂、对-氨基苯甲酸(paba)、二甲亚砜、转化生长因子β(tgfβ)抑制剂、白介素-5(il-5)抑制剂和泛胱天蛋白酶抑制剂。可与actriib拮抗剂联用的其它药剂包括但不限于凝集素(如描述于例如美国专利号:7,026,283,其完整内容通过引用并入本文中),以及wynn等(2007,jclininvest117:524-529)描述的抗纤维化剂。例如,其它抗纤维化剂和疗法包括但不限于各种抗炎药/免疫抑制药/细胞毒性药(包括秋水仙碱、硫唑嘌呤、环磷酰胺、泼尼松、沙利度胺、己酮可可碱和茶碱)、tgfβ信号传导调节剂(包括松弛素、smad7、hgf和bmp7以及tgfβl、tβri、tβrii、egr-i和ctgf抑制剂)、细胞因子和细胞因子受体拮抗剂(il-lβ、il-5、il-6、il-13、il-21、il-4r、il-13rαl、gm-csf、tnf-α、制癌蛋白m、wlsp-i和pdgf的抑制剂)、细胞因子和趋化因子(ifn-γ、ifn-α/β、il-12、il-10、hgf、cxcll0和cxcl11)、趋化因子拮抗剂(cxcll、cxcl2、cxcl12、ccl2、ccl3、ccl6、ccl17和ccl18的抑制剂)、趋化因子受体拮抗剂(ccr2、ccr3、ccr5、ccr7、cxcr2和cxcr4的抑制剂)、tlr拮抗剂(tlr3、tlr4和tlr9的抑制剂)、血管生成拮抗剂(vegf特异性抗体和腺苷脱氨酶替代疗法)、抗高血压药(β阻断剂和ang11、ace和醛固酮的抑制剂)、血管活性物质(et-1受体拮抗剂和bosetan)、合成和加工胶原的酶的抑制剂(脯氨酰羟化酶抑制剂)、b细胞拮抗剂(利妥昔单抗)、整联蛋白/粘附分子拮抗剂(阻断αlβl和αvβ6整联蛋白的分子,以及整联蛋白相关激酶的抑制剂,和icam-i和vcam-i的特异性抗体)、靶向成肌纤维细胞的促凋亡药物、mmp抑制剂(mmp2、mmp9和mmp12的抑制剂)和tlmp抑制剂(timp-1的特异性抗体)。
在某些实施方案中,本公开内容的actriib拮抗剂可以单独用于治疗有需要的患者。可选地,actriib拮抗剂可与针对治疗或预防本文所述的增殖性疾病的常规治疗方法组合使用,所述方法包括例如手术(例如,脾切除术)、细胞毒性剂、牵涉辐射或施用放射性物质的放射治疗、化学治疗剂、抗激素剂、生长抑制剂、抗瘤组合物、和用本文所列和本领域已知的抗癌药治疗或其组合。
通常,细胞毒性剂是指抑制或防止细胞的功能和/或引起细胞破坏的物质。该术语旨在包括:放射性同位素(例如at211、i131、i125、y90、re186、re188、sm153、bi212、p32和lu的放射性同位素),化学治疗剂例如甲氨蝶呤、阿霉素、长春花属生物碱(长春新碱、长春碱、依托泊苷)、多柔比星、美法仑、丝裂霉素c、苯丁酸氮芥、柔红霉素或其它嵌入剂,酶和其片段例如溶核酶,抗生素和毒素例如小分子毒素或细菌、真菌、植物或动物源的酶促活性毒素,包括其片段和/或变体,以及下文公开的各种抗肿瘤剂或抗癌剂。下面描述了其它细胞毒性剂。杀肿瘤剂引起肿瘤细胞的破坏。
通常,“化学治疗剂”是可用于治疗癌症的化合物。化学治疗剂的实例包括:烷化剂,例如塞替派和cytoxan®环磷酰胺;烷基磺酸酯,例如白消安、英丙舒凡和哌泊舒凡;吖丙啶类,例如苯佐替派(benzodopa)、卡波醌、美妥替哌(meturedopa)和乌瑞替派(uredopa);乙烯亚胺和methylamelamines,包括六甲蜜胺、曲他胺、三乙烯磷酰胺(trietylenephosphoramide)、三乙烯硫代磷酰胺和三羟甲蜜胺;acetogenins(尤其是bullatacin和bullatacinone);δ-9-四氢大麻酚(屈大麻酚、marinol®);β-lapachone;拉帕醇;秋水仙碱;桦木酸;喜树碱(包括合成类似物托泊替康(hycamtin®)、cpt-11(伊立替康、camptosar®)、乙酰基喜树碱、东莨菪亭和9-氨基喜树碱);苔藓抑素;callystatin;cc-1065(包括其阿多来新、卡折来新和比折来新合成类似物);鬼臼毒素;鬼臼酸;替尼泊苷;念珠藻环肽(特别是念珠藻环肽1和念珠藻环肽8);多拉司他汀;duocarmycin(包括合成类似物、kw-2189和cbl-tml);艾榴素;pancratistatin;匍枝珊瑚醇;海绵素;氮芥,例如苯丁酸氮芥、萘氮芥、环磷酰胺、雌莫司汀、异环磷酰胺、氮芥、盐酸氧氮芥、美法仑、新氮芥、苯芥胆甾醇(phenesterine)、泼尼莫司汀、曲磷胺、乌拉莫司汀;亚硝基脲,例如卡莫司汀、氯脲菌素、福莫司汀、洛莫司汀、尼莫司汀和雷莫司汀;抗生素,例如烯二炔类抗生素(例如卡奇霉素、特别是卡奇霉素γll和卡奇霉素ωll(参见例如agnew,chemintl.ed.engl.,33:183-186(1994));烯二炔蒽环类抗生素,包括烯二炔蒽环类抗生素a;埃斯波霉素;以及新制癌菌素发色团和相关色蛋白烯二炔抗生素发色团、阿克拉霉素、放线菌素、authramycin、偶氮丝氨酸、博来霉素、放线菌素c、carabicin、去甲柔红霉素、嗜癌霉素、chromomycinis、放线菌素d、柔红霉素、地托比星、6-重氮基-5-氧代-l-正亮氨酸、adriamycin®多柔比星(包括吗啉代-多柔比星、氰基吗啉代-多柔比星、2-吡咯啉子基(pyrrolino)-多柔比星和去氧多柔比星)、表柔比星、依索比星、伊达比星、马赛罗霉素、丝裂霉素(例如丝裂霉素c)、麦考酚酸、诺拉霉素、橄榄霉素、培洛霉素、紫菜霉素、嘌罗霉素、三铁阿霉素、罗多比星、链黑霉素、链佐星、杀结核菌素、乌苯美司、净司他丁、佐柔比星;抗代谢物,例如甲氨蝶呤和5-氟尿嘧啶(5-fu);叶酸类似物,例如二甲叶酸、甲氨蝶呤、蝶罗呤、三甲曲沙;嘌呤类似物,例如氟达拉滨、6-巯基嘌呤、thiamiprine、硫鸟嘌呤;嘧啶类似物,例如安西他滨、阿扎胞苷、6-氮尿苷、卡莫氟、阿糖胞苷、二脱氧尿苷、去氧氟尿苷、依诺他滨、氟尿苷;雄激素,例如卡鲁睾酮、屈他雄酮丙酸酯、环硫雄醇、美雄烷、睾内酯;抗肾上腺素药(anti-adrenals),例如氨鲁米特、米托坦、曲洛司坦;叶酸补充剂,例如亚叶酸;醋葡醛内酯;醛磷酰胺糖苷;氨基酮戊酸;恩尿嘧啶;安吖啶;bestrabucil;比生群;依达曲沙;秋水仙胺;地吖醌;elfornithine;依利醋铵;埃坡霉素;依托格鲁;硝酸镓;羟基脲;香菇多糖;氯尼达明;美坦生类化合物,例如美登素和安丝菌素;米托胍腙;米托蒽醌;莫哌达醇(mopidanmol);尼曲吖啶(nitraerine);喷司他丁;phenamet;吡柔比星;洛索蒽醌;2-乙基酰肼;丙卡巴肼;psk®多糖复合体(jhsnaturalproducts,eugene,or);雷佐生;利索新;西佐喃;锗螺胺;细交链孢菌酮酸;三亚胺醌;2,2',2"-三氯三乙胺;单端孢菌霉素(尤其是t-2毒素、verracurina、杆孢菌素a和anguidine);乌拉坦;长春地辛(eldisine®、fildesin®);达卡巴嗪;甘露莫司汀;二溴甘露醇;二溴卫矛醇;哌泊溴烷;gacytosine;阿拉伯糖苷c(“ara-c”);塞替派;紫杉醇类,例如taxol®紫杉醇(bristol-myerssquibboncology,princeton,n.j.)、abraxane™cremophor-free、紫杉醇的白蛋白工程化纳米粒制剂(americanpharmaceuticalpartners,schaumberg,illinois)和taxotere®doxetaxel(rhόne-poulencrorer,antony,france);苯丁酸氮芥;吉西他滨(gemzar®);6-硫鸟嘌呤;巯基嘌呤;甲氨蝶呤;铂类似物,例如顺铂和卡铂;长春碱(velban®);铂;依托泊苷(vp-16);异环磷酰胺;米托蒽醌;长春新碱(oncovin®);奥沙利铂;leucovovin;长春瑞滨(navelbine®);诺安托;依达曲沙;道诺霉素;氨基蝶呤;伊班膦酸盐;拓扑异构酶抑制剂rfs2000;二氟甲基鸟氨酸(dmyelofibrosiso);类视黄醇,例如视黄酸;卡培他滨(xeloda®);上述任一种的药学上可接受的盐、酸或衍生物;以及上述两种或更多种的组合,例如chop,其为环磷酰胺、多柔比星、长春新碱和泼尼松龙组合疗法的缩略语,以及folfox,其为应用与5-fu和leucovovin组合的奥沙利铂(eloxatin™)的治疗方案的缩略语。
还有起调节、降低、阻断或抑制可促进癌生长的激素的作用,且常常呈系统或全身治疗形式的抗激素药。它们本身可以是激素。实例包括:抗雌激素和选择性雌激素受体调节剂(serm),包括例如他莫昔芬(包括nolvadex®他莫昔芬)、evista®雷洛昔芬、屈洛昔芬、4-羟基他莫昔芬、曲沃昔芬、keoxifene、lyl17018、奥那司酮和fareston®托瑞米芬;抗黄体酮;雌激素受体下调剂(erd);起抑制或中断卵巢作用的药剂,例如促性腺素释放素(lhrh)激动剂,例如lupron®和eligard®醋酸亮丙立德、醋酸戈舍瑞林、醋酸布舍瑞林和曲普瑞林(tripterelin);其它抗雄激素,例如氟他胺、尼鲁米特和比卡鲁胺;以及抑制酶芳香酶(其调节肾上腺中的雌激素产生)的芳香酶抑制剂,例如4(5)-咪唑、氨鲁米特、megase®醋酸甲地孕酮、aromasin®依西美坦、福美坦、法倔唑、rivisor®伏氯唑、femara®来曲唑和arimidex®阿那曲唑。另外,化学治疗剂的这类定义包括二膦酸盐,例如氯膦酸盐(例如bonefos®或ostac®)、didrocal®依替膦酸、ne-58095、zometa®唑来膦酸/唑来膦酸盐、fosamax®阿伦膦酸盐、aredia®帕米膦酸盐、skelid®替鲁膦酸盐或actonel®利塞膦酸盐;以及曲沙他滨(1,3-二氧杂环戊烷核苷胞嘧啶类似物);反义寡核苷酸,特别是抑制参与异常细胞增殖的信号转导途径中的基因表达的那些,如例如pkc-α、raf、h-ras和表皮生长因子受体(egf-r);疫苗,例如theratope®疫苗和基因疗法疫苗,例如allovectin®疫苗、leuvectin®疫苗和vaxid®疫苗;lurtotecan®拓扑异构酶1抑制剂;abarelix®rmrh;托西拉帕替尼(erbb-2和egfr双重酪氨酸激酶小分子抑制剂,亦称gw572016);和上述任一种的药学上可接受的盐、酸或衍生物。
生长抑制剂通常指体外或体内抑制细胞生长的化合物或组合物。因此,生长抑制剂可以是显著降低s期中细胞的百分比的生长抑制剂。生长抑制剂的实例包括阻断细胞周期进展(处于s期以外的位置)的药剂,例如引起gl停滞和m期停滞的药剂。经典的m期阻断剂包括长春花属生物碱(vinca)(长春新碱和长春碱)、紫杉烷类和拓扑异构酶ii抑制剂,例如多柔比星、表柔比星、柔红霉素、依托泊苷和博来霉素。阻滞gl的那些药剂也波及到s期停滞,例如dna烷化剂,例如他莫昔芬、泼尼松、达卡巴嗪、氮芥、顺铂、甲氨蝶呤、5-氟尿嘧啶和ara-c。更多的信息可见于themolecularbasisofcancer,mendelsohn和israel编辑,第1章,murakami等标题为“cellcycleregulation,oncogenes,andantineoplasticdrugs”(wbsaunders:philadelphia,1995),尤其第13页。紫杉烷类(紫杉醇和多西他赛)是均来源于紫杉树的抗癌药。来源于欧洲紫杉的多西他赛(taxotere®,rhone-poulencrorer)是紫杉醇(taxol®,bristol-myerssquibb)的半合成类似物。紫杉醇和多西他赛促进微管从微管蛋白二聚体的装配,并通过防止解聚稳定微管,这导致在细胞中抑制有丝分裂。
actriib拮抗剂和另外的活性剂(例如,共治疗剂)可以在相同的制剂中施用或单独施用。在单独施用的情况下,actriib拮抗剂可以在另外的活性剂之前、之后或与其同时施用。一种药剂可通过几分钟到几周变化的间隔先于或后于另一药剂的施用。在将两种或更多种不同类型的治疗剂单独应用于主体的实施方案中,将通常确保在每次递送的时间之间相当长的一段时间不到期,使得这些不同种类的药剂将仍然能够对靶组织或细胞发挥有利的组合效应。
在某些实施方案中,本公开内容提供了用于通过测量患者中的一种或多种血液学参数来管理患者的方法,所述患者已经用一种或多种本公开内容的actriib拮抗剂药剂治疗、或者是待用其治疗的候选者。血液学参数可用于评价对其为待用本公开内容的拮抗剂治疗的候选者的患者的适当给药、监控治疗期间的血液学参数、评价在用一种或多种本公开内容的拮抗剂治疗期间是否调整剂量、和/或评价一种或多种本公开内容的拮抗剂的适当维持剂量。如果血液学参数中的一种或多种在正常水平之外,则可以减少、延迟或终止一种或多种actriib拮抗剂的给药。
可以根据本文提供的方法测量的血液学参数包括,例如,使用本领域公认的方法,红细胞水平、血压、铁储备(ironstore)和在体液中发现的与增加的红细胞水平相关的其它因子。这种参数可以使用来自患者的血液样品来测定。红细胞水平、血红蛋白水平和/或血细胞比容水平的增加可以引起血压的增加。
在一个实施方案中,如果一种或多种血液学参数在其为用一种或多种actriib拮抗剂治疗的候选者的患者中的正常范围之外或在正常高侧(highside)上,则可以延迟一种或多种本公开内容的拮抗剂的施用的开始,直到血液学参数自然或经由治疗干预恢复至正常或可接受的水平。例如,如果候选患者是高血压的或高血压前的(pre-hypertensive),则可以用降血压剂治疗患者以降低患者的血压。可以使用适合于个体患者的状况的任何降血压剂,包括例如利尿剂、肾上腺素能抑制剂(包括α受体阻滞剂和β受体阻滞剂)、血管扩张剂、钙通道阻滞剂、血管紧张素转化酶(ace)抑制剂或血管紧张素ii受体阻滞剂。可选地,可以使用膳食和运动方案来治疗血压。类似地,如果候选患者具有低于正常或在正常低侧(lowside)上的铁储备,则患者可以用适当的膳食和/或铁补充剂的方案治疗,直到患者的铁储备已恢复至正常或可接受的水平。对于具有高于正常红细胞水平和/或血红蛋白水平的患者,则可以延迟施用一种或多种本公开内容的拮抗剂,直到所述水平已恢复至正常或可接受的水平。
在某些实施方案中,如果一种或多种血液学参数在其为用一种或多种actriib拮抗剂治疗的候选者的患者的正常范围之外或正常高侧上,则可以不延迟施用的开始。然而,一种或多种本公开内容的拮抗剂的剂量或给药频率可以设置在这样的量,其将降低施用一种或多种本公开内容的拮抗剂时出现的血液学参数的不可接受的增加的风险。可选地,可以为患者开发治疗方案,其将一种或多种actriib拮抗剂与处理不期望的血液学参数水平的治疗剂组合。例如,如果患者具有升高的血压,则可以设计治疗方案,其牵涉施用一种或多种actriib拮抗剂药剂和降血压剂。对于具有低于期望的铁储备的患者,可以开发治疗方案,其牵涉一种或多种本公开内容的actriib拮抗剂和铁补充。
在一个实施方案中,可以为其为待用一种或多种本公开内容的actriib拮抗剂治疗的候选者的患者确立一种或多种血液学参数的基线参数(一种或多种),并且基于所述基线值(一种或多种)为该患者确立适当的给药方案。可选地,基于患者的病史确立的基线参数可用于为患者告知适当的拮抗剂给药方案。例如,如果健康患者具有高于定义的正常范围的确立的基线血压读数,则在用一种或多种本公开内容的拮抗剂治疗之前,可能没有必要使患者的血压进入对于一般人群被认为是正常的范围中。在用一种或多种本公开内容的actriib拮抗剂治疗之前患者的一种或多种血液学参数的基线值也可以用作相关比较值,用于监控用一种或多种本公开内容的拮抗剂治疗期间血液学参数的任何变化。
在某些实施方案中,在正在用一种或多种actriib拮抗剂治疗的患者中测量一种或多种血液学参数。血液学参数可用于在治疗期间监控患者,并允许调节或终止用一种或多种本公开内容的拮抗剂给药或用另一种治疗剂额外给药。例如,如果施用一种或多种actriib拮抗剂导致血压、红细胞水平或血红蛋白水平的增加或铁储备的减少,则可以在量或频率方面减少一种或多种本公开内容的拮抗剂的剂量,以减少一种或多种本公开内容的拮抗剂对一种或多种血液学参数的作用。如果施用一种或多种actriib拮抗剂导致对患者不利的一种或多种血液学参数的变化,则一种或多种本公开内容的拮抗剂的给药可以暂时终止,直到血液学参数(一种或多种)恢复至可接受的水平,或永久终止。类似地,如果在减少一种或多种本公开内容的拮抗剂的施用剂量或频率后,未使一种或多种血液学参数在可接受的范围内,则可以终止给药。作为减少或终止用一种或多种本公开内容的拮抗剂给药的替代方案或另外地,患者可以用额外的治疗剂给药,所述治疗剂处理血液学参数(一种或多种)中的不希望的水平,如例如降血压剂或铁补充剂。例如,如果用一种或多种actriib拮抗剂治疗的患者具有升高的血压,则用一种或多种本公开内容的拮抗剂给药可以在相同水平继续并且将降血压剂添加至治疗方案中,可以减少用一种或多种本公开内容的拮抗剂的给药(例如,在量和/或频率方面)并将降血压剂添加至治疗方案中,或者可以终止用一种或多种本公开内容的拮抗剂的给药并且可以用降血压剂治疗患者。
如本文所用,“与......组合”,“……的组合”或“结合”施用是指任何形式的施用,使得额外的疗法(例如,第二、第三、第四等)在体内仍然有效(例如,多种化合物在患者中同时有效,其可包括那些化合物的协同作用)。有效性可能与血液、血清或血浆中可测量的药剂浓度无关。例如,不同的治疗化合物可以在相同的制剂中或在单独的制剂中同时或依次施用,并且可以在不同的时间表上施用。因此,接受这种治疗的个体可以受益于不同疗法的组合效果。本公开内容的一种或多种actriib拮抗剂或此类多肽的组合可以与一种或多种其它另外的药剂或支持疗法同时、在其之前或之后施用。通常,每种治疗剂将以针对该特定药剂确定的剂量和/或时间表施用。在方案中使用的特定组合将考虑本公开内容的拮抗剂与疗法和/或期望的相容性。
5.药物组合物
本文所述的治疗剂(例如,actriib拮抗剂)可以配制于药物组合物中。用于根据本公开内容使用的药物组合物可以使用一种或多种生理学上可接受的载体或赋形剂以常规方式配制。按照大多数管理要求,这种制剂将通常基本上无致热原。
在某些实施方案中,本公开内容的治疗方法包括全身性施用组合物或作为植入物或设备局部施用组合物。当施用时,用于本公开内容中的治疗组合物呈无致热原、生理学上可接受的形式。除了actriib信号传导拮抗剂以外的治疗上有用的药剂(其也可任选地包括在如上所述的组合物中)可在本文公开的方法中与主题化合物(例如,actriib多肽)同时或序贯施用。
一般,本文公开的蛋白治疗剂将肠胃外、且特别是静脉内或皮下施用。适合于肠胃外施用的药物组合物可包含一种或多种actriib拮抗剂与一种或多种药学上可接受的无菌等渗水溶液或非水溶液、分散体、悬浮液或乳剂、或可恰好在使用前重构成无菌可注射溶液或分散体的无菌粉末的组合,其可含有抗氧化剂、缓冲剂、抑菌剂、使制剂与预期受体的血液等渗的溶质或悬浮剂或增稠剂。可用于本公开内容的药物组合物中的合适的水性和非水性载体的实例包括水、乙醇、多元醇(诸如,甘油、丙二醇、聚乙二醇等)及其合适的混合物、植物油(如,橄榄油)和可注射有机酯(如,油酸乙酯)。正确的流动性可例如,通过使用包被材料(如,卵磷脂)、在分散体的情况下通过维持需要的粒度、且通过使用表面活性剂来维持。
如果期望,所述组合物和制剂可以在包或分配器设备中呈现,所述包或分配器设备可以含有一种或多种含有活性成分的单位剂型(unitdosageform)。所述包可以例如包括金属或塑料箔,诸如泡罩包(blisterpack)。所述包或分配器设备可以附带有关于施用的说明书。
此外,所述组合物可以递送至靶组织部位的形式被包入胶囊内或注射。在某些实施方案中,本发明的组合物可包括能够递送一种或多种治疗化合物(例如,actriib多肽)至靶组织部位、为发育中的组织提供结构、且最佳地能够再吸收至体内的基质。例如,基质可提供actriib拮抗剂的缓慢释放。这种基质可由目前用于其它植入的医学应用的材料形成。
基质材料的选择基于生物适合性、生物降解力、机械性质、美容外观和界面性质。主题组合物的特定应用将定义合适的制剂。用于组合物的潜在基质可以是生物可降解的和化学成分确知的硫酸钙、磷酸三钙、羟基磷灰石、聚乳酸和聚酐。其它潜在的材料是生物可降解的和生物学上充分确定的,诸如骨或皮肤胶原。其它基质包含纯的蛋白或细胞外基质组分。其它潜在的基质是非-生物可降解的和化学成分确知的,诸如烧结的羟基磷灰石、生物玻璃(bioglass)、铝酸盐或其它陶瓷。基质可包含任何上述类型的材料(诸如聚乳酸和羟基磷灰石或胶原和磷酸三钙)的组合。生物陶瓷可在组成(例如,钙-铝酸盐-磷酸盐)和加工方面改变,以改变孔径、粒度、颗粒形状和生物降解力。
在某些实施方案中,本发明的方法可经口施用,例如,以胶囊、扁囊剂(cachet)、丸剂、片剂、锭剂(使用调味基底(flavoredbasis),通常为蔗糖和阿拉伯胶(acacia)或西黄蓍胶)、粉剂、颗粒、或作为水性或非水性液体中的溶液或悬浮液、或作为水包油或油包水液体乳剂、或作为酏剂或糖浆、或作为软锭剂(使用惰性基质,如明胶和甘油,或蔗糖和阿拉伯胶)和/或作为口腔洗剂等的形式,各自含有预定量的作为活性成分的药剂。药剂还可作为推注剂、药糖剂或糊剂施用。
在用于经口施用的固体剂型(胶囊、片剂、丸剂、糖锭剂、粉剂、颗粒等)中,一种或多种本发明的治疗化合物可与一种或多种药学上可接受的载体混合,所述载体如柠檬酸钠或磷酸二钙,和/或以下中的任一种:(1)充填剂或膨胀剂,如,淀粉、乳糖、蔗糖、葡萄糖、甘露糖醇和/或硅酸;(2)结合剂,如,例如,羧基甲基纤维素、藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和/或阿拉伯胶;(3)湿润剂,如,甘油;(4)崩解剂,如,琼脂、碳酸钙、马铃薯或木薯淀粉、藻酸、某些硅酸盐和碳酸钠;(5)溶解阻滞剂,如,石蜡;(6)吸收加速剂,如,季铵化合物;(7)润湿剂,如,鲸蜡醇和甘油单硬脂酸酯;(8)吸收剂,如,高岭土和膨润土;(9)润滑剂,如,例如,滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、月桂基硫酸钠及其混合物;和(10)着色剂。在胶囊、片剂和丸剂的情况下,药物组合物还可包含缓冲剂。类似类型的固体组合物也可作为填充物用于软和硬填充明胶胶囊中,其使用赋形剂如乳糖(lactose)或乳糖(milksugar)以及高分子量聚乙二醇等。
用于经口施用的液体剂型包括药学上可接受的乳剂、微乳、溶液、悬浮液、糖浆和酏剂。除了活性成分以外,液体剂型可含有本领域常用的惰性稀释剂,如,水或其它溶剂、增溶剂和/或乳化剂,如,乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、油(具体而言,棉籽油、花生油、玉米油、胚芽油(germoil)、橄榄油、蓖麻油和芝麻油)、甘油、四氢呋喃基甲醇、聚乙二醇和脱水山梨糖醇的脂肪酸酯和其混合物。除了惰性稀释剂以外,经口组合物还可包括佐剂,如润湿剂、乳化剂和悬浮剂、甜味剂、调味剂、着色剂、芳香剂和防腐剂。
悬浮液,除了活性化合物以外,可含有悬浮剂,如,乙氧基化异十八烷醇、聚氧乙烯山梨糖醇和脱水山梨糖醇酯、微晶纤维素、偏氢氧化铝(aluminummetahydroxide)、膨润土、琼脂和西黄蓍胶及其混合物。
本发明的组合物还可以含有佐剂,如防腐剂、润湿剂、乳化剂和分散剂。微生物的作用的预防可通过包括各种抗菌剂和抗真菌剂(例如对羟基苯甲酸酯、氯丁醇、苯酚山梨酸等)来确保。可期望在组合物中包括等渗剂如糖、氯化钠等。此外,可通过包括延迟吸收的试剂如单硬脂酸铝和明胶导致可注射药物形式的延长吸收。
应理解,剂量方案将由主治医师考虑各种因素来确定,所述因素改变本发明的主题化合物(例如,tβrii多肽)的作用。各种因素包括但不限于患者的年龄、性别和膳食,疾病严重性,施用的时间和其它临床因素。任选地,剂量可以随着重构中使用的基质类型和组合物中化合物的类型而变化。向最终组合物中添加其它已知的生长因子也可以影响剂量。可以通过定期评估骨生长和/或修复来监控进展,例如,x-射线(包括dexa)、组织形态度量测定和四环素标记。
在某些实施方案中,本发明还提供了用于体内产生actriib拮抗剂的基因疗法。这种疗法将通过将actriib多核苷酸序列引入具有上文列出的病症的细胞或组织来实现其治疗效果。actriib多核苷酸序列的递送可使用重组表达载体如嵌合病毒或胶态分散系统来实现。actriib多核苷酸序列的治疗递送优选使用靶向的脂质体。
如本文教导的可用于基因疗法的各种病毒载体包括腺病毒、疱疹病毒、牛痘或优选rna病毒(如,逆转录病毒)。优选地,逆转录病毒载体是鼠或禽逆转录病毒的衍生物。其中可插入单一外源基因的逆转录病毒载体的实例包括但不限于:莫洛尼鼠类白血病病毒(momulv)、harvey鼠肉瘤病毒(hamusv)、鼠类乳腺肿瘤病毒(mumtv)和劳斯肉瘤病毒(rsv)。许多额外的逆转录病毒载体可并入多种基因。所有这些载体都可转移或并入用于选择标记物的基因,从而可鉴定和产生转导的细胞。通过附着例如,糖、糖脂或蛋白,可使得逆转录病毒载体为靶特异性的。优选的靶向通过使用抗体实现。本领域技术人员将认识到,特定的多核苷酸序列可插入逆转录病毒基因组或附着至病毒包膜以允许含有actriib多核苷酸的逆转录病毒载体的靶特异性递送。在优选实施方案中,所述载体被靶向至骨或软骨。
另一方面,组织培养细胞可通过常规磷酸钙转染,用编码逆转录病毒结构基因gag、pol和env的质粒直接转染。然后这些细胞用含有目标基因的载体质粒转染。所得细胞将逆转录病毒载体释放至培养基中。
用于actriib拮抗剂多核苷酸的另一种靶向的递送系统是胶态分散系统。胶态分散系统包括大分子复合体、纳米胶囊(nanocapsules)、微球体、珠和基于脂质的系统,包括水包油乳剂、微团、混合微团和脂质体。本发明的优选的胶态系统是脂质体。脂质体是人工膜小泡,其可体外和体内用作递送载体。rna、dna和完整的病毒体可被囊化在水性内部中且以生物活性形式递送至细胞(参见,例如,fraley等,trendsbiochem.sci.,6:77,1981)。使用脂质体载体的用于有效基因转移的方法是本领域已知的,参见,例如,mannino,等,biotechniques,6:682,1988。脂质体的组合物通常是磷脂的组合,通常与类固醇、特别是胆固醇组合。也可以使用其它磷脂或其它脂质。脂质体的物理特征取决于ph、离子强度和二价阳离子的存在。
脂质体生产中有用的磷脂的实例包括磷脂酰化合物,如,磷脂酰甘油、磷脂酰胆碱、磷脂酰丝氨酸、磷脂酰乙醇胺、鞘脂、脑苷脂和神经节苷脂。举例说明性磷脂包括卵磷脂酰胆碱、二棕榈酰磷脂酰胆碱和二硬脂酰磷脂酰胆碱。脂质体的靶向还可能基于例如,器官-特异性、细胞-特异性和细胞器-特异性,并且是本领域已知的。
本公开内容提供了制剂,其可以被改变以包括调节ph的酸和碱;和将ph保持在狭窄范围内的缓冲剂。
实施例
本发明已总体上进行了描述,其参考以下实施例将更容易理解,所述实施例仅为举例说明本发明的某些实施方案起见包括在内,且不意图限制本发明。
实施例1:actriib-fc融合蛋白的生成
申请人构建了可溶性actriib融合蛋白,其具有与人或小鼠fc结构域融合的人actriib的细胞外结构域,其之间具有最小接头(3个甘氨酸氨基酸)。所述构建体分别被称为actriib-hfc和actriib-fc。
actriib-hfc如下显示为从cho细胞系纯化(seqidno:24):
actriib-hfc和actriib-fc蛋白在cho细胞系中表达。考虑了三种不同的前导序列:(i)蜜蜂蜂毒肽(hbml):mkflvnvalvfmvvyisyiya(seqidno:21),ii)组织纤溶酶原激活物(tpa):mdamkrglccvlllcgavfvsp(seqidno:22),和(iii)天然:mgaaaklafavfliscssga(seqidno:23)。
选择的形式采用tpa前导序列且具有以下未加工的氨基酸序列(seqidno:25):
该多肽由以下核酸序列(seqidno:26)编码:
cho细胞产生的材料的n-末端测序揭示–grgeae(seqidno:27)的主要序列。值得注意的是,文献中报道的其它构建体以–sgr…序列开始。
纯化可以通过一系列柱层析步骤实现,包括例如,以任何顺序的以下的三种或更多种:a蛋白层析、q琼脂糖凝胶层析、苯基琼脂糖凝胶层析、尺寸排阻层析和阳离子交换层析。纯化可以用病毒过滤和缓冲液更换完成。
actriib-fc融合蛋白也在hek293细胞和cos细胞中表达。尽管来自所有细胞系和合理培养条件的材料都提供了在体内具有肌肉锻炼(muscle-building)活性的蛋白,但观察到效力的可变性,其可能与细胞系选择和/或培养条件相关。
申请人在actriib的细胞外结构域中生成了一系列突变,并将这些突变蛋白产生为细胞外actriib和fc结构域之间的可溶性融合蛋白。背景actriib-fc融合物(fusion)具有seqidno:24的序列。
将各种突变(包括n-和c-末端截短)引入背景actriib-fc蛋白中。基于本文呈现的数据,预期这些构建体如果用tpa前导序列表达,将缺乏n-末端丝氨酸。通过pcr诱变在actriib细胞外结构域中生成突变。在pcr后,将片段通过qiagen柱纯化,用sfol和agel消化并凝胶纯化。将这些片段连接至表达载体paid4(参见wo2006/012627)中,从而使得在连接时其产生与人igg1的融合嵌合体。转化入大肠杆菌dh5α中时,挑取菌落并分离dna。对于鼠构建体(mfc),用鼠igg2a取代人igg1。验证所有突变体的序列。通过瞬时转染在hek293t细胞中产生所有突变体。总之,在500ml旋转器中,将hek293t细胞在250ml体积的freestyle(invitrogen)培养基中以6x105个细胞/ml设置并生长过夜。第二天,将这些细胞用dna:pei(1:1)复合体以0.5μg/ml最终dna浓度处理。4小时后,添加250ml培养基,并使细胞生长7天。通过离心(spinningdown)细胞来收获条件培养基并浓缩。
将突变体使用多种技术(包括例如a蛋白柱)纯化,并用低ph(3.0)甘氨酸缓冲液洗脱。中和后,将这些针对pbs透析。
还通过类似方法在cho细胞中产生突变体。在引入本文作为参考的wo2008/097541和wo2006/012627中描述的结合测定和/或生物测定中测试突变体。在一些情况下,用条件培养基而不是纯化的蛋白进行测定。actriib的额外变异描述于美国专利号7,842,663中。
申请人生成了actriib(25-131)-hfc融合蛋白,其包含具有n-末端和c-末端截短(天然蛋白seqidno:1的残基25-131)的人actriib细胞外结构域,其在n-末端与取代天然actriib前导序列的tpa前导序列融合且在c-末端经由最小接头(三个甘氨酸残基)与人fc结构域融合(图12)。编码该融合蛋白的核苷酸序列显示于图13。申请人修饰了密码子并发现了编码actriib(25-131)-hfc蛋白的变体核酸,其提供了最初转化体的表达水平的显著改善(图14)。
成熟蛋白具有如下氨基酸序列(通过n-末端测序证实的n-末端)(seqidno:28):
氨基酸1-107来自actriib。
表达的分子使用一系列柱层析步骤纯化,包括例如,以任何顺序的以下的三种或更多种:a蛋白层析、q琼脂糖凝胶层析、苯基琼脂糖凝胶层析、尺寸排阻层析和阳离子交换层析。纯化可以用病毒过滤和缓冲液更换完成。
用biacore™仪器在体外评价几种配体对actriib(25-131)-hfc及其全长对应物actriib(20-134)-hfc的亲和力,且结果总结于下表中。由于复合体的非常快速的缔合和解离,kd值通过稳态亲和拟合获得,这防止了kon和koff的准确测定。actriib(25-131)-hfc以高亲和力结合激活蛋白a、激活蛋白b和gdf11。
actriib-hfc形式的配体亲和力:
实施例2:gdf捕获物的生成
申请人如下构建gdf捕获物。具有修饰的actriib的细胞外结构域(具有l79d取代的seqidno:1的氨基酸20-134)的多肽(其相对于gdf11和/或肌肉生长抑制素具有大大降低的激活蛋白a结合(由于seqidno:1中位置79的亮氨酸至天冬氨酸取代),与人或小鼠fc结构域融合,其之间具有最小接头(3个甘氨酸氨基酸)。所述构建体分别被称为actriib(l79d20-134)-hfc和actriib(l79d20-134)-fc。在位置79具有谷氨酸而不是天冬氨酸的可选形式表现类似(l79e)。还生成在下面的就seqidno:44而言的位置226处具有丙氨酸而不是缬氨酸的可选形式,并且其在所有测试的方面表现相同。在位置79(相对于seqidno:1,或相对于seqidno:29的位置60)的天冬氨酸在下面用双下划线表示。相对于seqidno:29的位置226处的缬氨酸在下面也通过双下划线表示。
gdf捕获物actriib(l79d20-134)-hfc如下显示为从cho细胞系纯化(seqidno:29)。
gdf捕获物的actriib衍生的部分具有下文所示的氨基酸序列(seqidno:30),并且该部分可以用作单体或作为单体、二聚体或更高级(greater-order)复合体的非fc融合蛋白。
gdf捕获物蛋白在cho细胞系中表达。考虑了三种不同的前导序列:
(i)蜜蜂蜂毒肽(hbml),(ii)组织纤溶酶原激活物(tpa),和(iii)天然。
选择的形式采用tpa前导序列且具有以下未加工的氨基酸序列:
该多肽由以下核酸序列(seqidno:32)编码:
纯化可以通过一系列柱层析步骤实现,包括例如,以任何顺序的以下的三种或更多种:a蛋白层析、q琼脂糖凝胶层析、苯基琼脂糖凝胶层析、尺寸排阻层析和阳离子交换层析。纯化可以用病毒过滤和缓冲液更换完成。在纯化方案的实例中,将细胞培养基在a蛋白柱上经过,在150mmtris/nacl(ph8.0)中洗涤,然后在50mmtris/nacl(ph8.0)中洗涤,并用0.1m甘氨酸,ph3.0洗脱。将低ph洗脱物在室温保持30分钟作为病毒清除步骤。然后将洗脱物中和并在q-琼脂糖凝胶离子交换柱上经过,并在50mmtrisph8.0,50mmnacl中洗涤,并在具有150mm-300mm的nacl浓度的50mmtrisph8.0中洗脱。然后将洗脱物更换到50mmtrisph8.0,1.1m硫酸铵中并在苯基琼脂糖凝胶柱上经过,洗涤,并在具有150-300mm的硫酸铵的50mmtrisph8.0中洗脱。将洗脱物透析并过滤以供使用。
额外的gdf捕获物(经修饰以降低激活蛋白a结合相对于肌肉生长抑制素或gdf11结合的比率的actriib-fc融合蛋白)描述于引入本文作为参考的wo2008/097541和wo2006/012627中。
实施例3:gdf11和激活蛋白介导的信号传导的生物测定
使用a-204报道基因测定来评价actriib-fc蛋白和gdf捕获物对通过gdf-11和激活蛋白a的信号传导的影响。细胞系:人横纹肌肉瘤(衍生自肌肉)。报道载体:pgl3(caga)12(描述于dennler等,1998,embo17:3091-3100)。caga12基序存在于tgf-β响应基因(例如,pai-1基因)中,所以该载体通常用于通过smad2和3信号传导的因子。
第1天:将a-204细胞分至48孔板中。
第2天:用10ugpgl3(caga)12或pgl3(caga)12(10ug)+prlcmv(1µg)和fugene转染a-204细胞。
第3天:添加因子(稀释至培养基+0.1%bsa中)。在添加至细胞之前,抑制剂需要与因子预温育1小时。6小时后,将细胞用pbs冲洗并裂解。
这随后为萤光素酶测定。在不存在任何抑制剂的情况下,激活蛋白a显示报道基因表达的10-倍刺激和ed50~2ng/ml。gdf-11:16倍刺激,ed50:~1.5ng/ml。
actriib(20-134)是该测定中激活蛋白a、gdf-8和gdf-11活性的有效抑制剂。如下所述,还在该测定中测试actriib变体。
实施例4:actriib-fc变体,基于细胞的活性
如上所述在基于细胞的测定中测试actriib-fc蛋白和gdf捕获物的活性。结果总结于下表中。在不同的c-末端截短构建体中测试一些变体。如上文所讨论的,5或15个氨基酸的截短引起活性降低。gdf捕获物(l79d和l79e变体)显示激活蛋白a抑制的基本丧失,同时保留gdf-11的几乎野生型抑制。
可溶性actriib-fc与gdf11和激活蛋白a的结合:
+差的活性(大致1x10-6ki)
++中等活性(大致1x10-7ki)
+++良好(野生型)活性(大致1x10-8ki)
++++大于野生型活性。
在大鼠中针对血清半衰期评估几个变体。actriib(20-134)-fc具有大约70小时的血清半衰期。actriib(a24n20-134)-fc具有大约100-150小时的血清半衰期。上述测试的变体中的任一种可以与gdf捕获物分子组合。
实施例5:gdf-11和激活蛋白a结合。
在biacoretm测定中测试某些actriib-fc蛋白和gdf捕获物与配体的结合。
使用抗-hfc抗体将actriib-fc变体或野生型蛋白捕获至系统上。注射配体并使其流过捕获的受体蛋白。结果总结于下表中。
配体结合特异性iib变体。
这些在无细胞测定中获得的数据证实了基于细胞的测定数据,证明a24n变体保留与actriib(20-134)-hfc分子的那种类似的配体结合活性,且l79d或l79e分子保留肌肉生长抑制素和gdf11结合,但显示显著降低的与激活蛋白a的结合(不可定量)。
已经生成和测试了其它变体,如wo2006/012627(其整体引入本文作为参考)中所报道的。参见例如第59-60页,其使用与设备偶联的配体并使受体流过偶联的配体。值得注意的是,相对于野生型k74分子,k74y、k74f、k74i(并且推测起来k74处的其它疏水取代,如k74l)和d80i引起激活蛋白a(acta)与gdf11结合的比率降低。下面重现了关于这些变体的数据表:
可溶性actriib-fc变体与gdf11和激活蛋白a的结合(biacore™测定)
*没有观察的结合
--<1/5wt结合
-~1/2wt结合
+wt
++<2x增加的结合
+++~5x增加的结合
++++~10x增加的结合
+++++~40x增加的结合。
实施例6:具有截短的actriib细胞外结构域的gdf捕获物的生成
通过tpa前导序列n-末端融合至含有亮氨酸至天冬氨酸取代(在seqidno:1中的残基79处)的actriib细胞外结构域(seqidno:1中的残基20-134)和人fc结构域利用最小接头(三个甘氨酸残基)的c-末端融合,生成被称为actriib(l79d20-134)-hfc的gdf捕获物(图3)。对应于该融合蛋白的核苷酸序列显示于图4。
通过tpa前导序列n-末端融合至含有亮氨酸至天冬氨酸取代(在seqidno:1中的残基79处)的截短的细胞外结构域(seqidno:1中的残基25-131)和人fc结构域利用最小接头(三个甘氨酸残基)的c-末端融合,生成被称为actriib(l79d25-131)-hfc的具有截短的actriib细胞外结构域的gdf捕获物(图5,seqidno:50)。编码该融合蛋白的一种核苷酸序列(seqidno:51)显示于图6中,而编码完全相同的融合蛋白的可选核苷酸序列(seqidno:55)显示于图9中。
实施例7:通过具有双截短的actriib细胞外结构域的gdf捕获物的选择性配体结合
用biacore™仪器在体外评价gdf捕获物和其它actriib-hfc蛋白对几种配体的亲和力。结果总结于下表中。由于复合体的非常快速的缔合和解离,kd值通过稳态亲和拟合获得,这防止了kon和koff的准确测定。
actriib-hfc变体的配体选择性:
具有截短的细胞外结构域的gdf捕获物,actriib(l79d25-131)-hfc,等于或超过较长变体actriib(l79d20-134)-hfc所展示的配体选择性,与缺乏l79d取代的actriib-hfc对应物相比,具有激活蛋白a结合的显著丧失,激活蛋白b结合的部分丧失,以及gdf11结合的几乎完全保留。请注意,单独的截短(没有l79d取代)不改变此处展示的配体中的选择性[比较actriib(l7925-131)-hfc与actriib(l7920-134)-hfc]。actriib(l79d25-131)-hfc还保留了与smad2/3信号传导配体gdf8和smad1/5/8配体bmp6和bmp10的强至中等程度结合。
实施例8:衍生自actriib5的gdf捕获物
其他人已经报道了actriib的可选的可溶形式(称为actriib5),其中包括actriib跨膜结构域的外显子4已经被不同的c-末端序列置换(参见例如,wo2007/053775)。
没有其前导序列的天然人actriib5的序列如下:
亮氨酸至天冬氨酸取代或其它酸性取代可以如所述在天然位置79(加下划线的)处进行,以构建变体actriib5(l79d),其具有以下序列:
该变体可以用tggg接头(单下划线)连接至人fc(双下划线),以生成具有以下序列的人actriib5(l79d)-hfc融合蛋白:
该构建体可以在cho细胞中表达。
实施例9:gdf捕获物在jak2v617f动物模型中的作用
转基因jak2v617f突变小鼠[如xing等(2008)blood111:5109-5117中所述的a系]用于理解actriib(l79d25-131)-fc对骨髓纤维化的作用。
为了理解骨髓纤维化疾病的发作和进展,将jak2v617f小鼠中的全血细胞计数和纤维化程度在不同年龄与从对照动物(年龄匹配的野生型小鼠)获得的数据比较。与野生型相比,红细胞(rbc)和血小板水平在所有年龄的jak2v617f小鼠中升高,且突变动物中的水平在2至5个月之间呈上升趋势,随后在8至12个月之间逐渐减少。从约5个月开始,jak2v617f小鼠的骨髓中可检测到纤维化,其随着年龄而恶化。jak2v617f小鼠在约3至4个月也显示脾肿大,其也随着年龄而恶化。
对于gdf捕获物研究,在12月龄开始治疗,这对应于晚期骨髓纤维化。将小鼠置于两组中的一组:i)用actriib(l79d25-131)-fc以10mg/kg的给药方案每周两次治疗jak2v617f小鼠;和ii)每周两次用载体(tbs)治疗jak2v617f小鼠(即对照动物)。10周后,与对照动物相比,actriib(l79d25-131)-fc治疗的动物显示降低的脾尺寸(-12.5%)。与该观察结果一致,组织病理学显示,与对照动物相比,actriib(l79d25-131)-fc治疗的小鼠的脾中的髓外造血减少。组织病理学还显示,与对照动物相比,actriib(l79d25-131)-fc治疗的小鼠中减少的骨髓纤维化。
因此,在这种jak2v617f模型中,用gdf捕获剂治疗有效改善骨髓纤维化的各种并发症,特别是在减少脾肿大、髓外造血和纤维化方面。因此,这些数据表明actriib拮抗剂可用于治疗骨髓纤维化。例如,actriib拮抗剂可特别用于治疗骨髓纤维化的各种并发症,包括例如减少脾肿大、减少髓外造血、增加红细胞水平和/或减少纤维化(例如,骨髓纤维化)。
实施例10:鲁索利替尼治疗动物中gdf捕获物的效应
鲁索利替尼是janus激酶抑制剂,其已被批准用于治疗中或高风险骨髓纤维化。特别地,鲁索利替尼在减少脾尺寸和改善骨髓纤维化患者中与脾肿大相关的症状中显示显著效果。然而,在用鲁索利替尼治疗的患者中观察到各种血液学副作用,包括例如贫血。使用9个月大的c57bl/6小鼠来理解鲁索利替尼治疗的小鼠中actriib(l79d25-131)-fc治疗对各种血液学参数的效应。
对于该研究,治疗开始于6-7个月龄。将小鼠置于四组中的一组:i)用actriib(l79d25-131)-fc以10mg/kg的给药方案每周两次治疗;ii)用鲁索利替尼以60mg/kg的给药方案每日两次治疗;iii)用actriib(l79d25-131)-fc以10mg/kg的给药方案每周两次、和鲁索利替尼以60mg/kg的给药方案每日两次治疗;和iv)用载体(tbs)每周两次治疗(即对照动物)。治疗4周后,与对照(tbs治疗)小鼠相比,观察到actriib(l79d25-131)-fc小鼠具有增加的红细胞(~15%)和血红蛋白(~13%)水平,证明actriib(l79d25-131)-fc增加c57bl/6小鼠中的红细胞生成活性。与之相比,与对照动物相比,鲁索利替尼治疗导致红细胞(~4%)和血红蛋白(~4%)水平的减少。与对照动物相比,actriib(l79d25-131)-fc和鲁索利替尼结合治疗的小鼠显示出红细胞(~8%)和血红蛋白(~5%)水平的增加。
这些数据证明,actriib(l79d25-131)-fc可以逆转正常健康小鼠中鲁索利替尼诱导的贫血。因此,数据表明actriib拮抗剂可用于减轻多种患者群体中的janus激酶抑制剂诱导的贫血,所述患者包括例如,已经或正在接受一种或多种janus激酶抑制剂治疗的骨髓纤维化患者。因此,actriib拮抗剂可用作与janus激酶抑制剂的结合治疗的一部分,以治疗多种患者群体,包括例如,已经或正在接受一种或多种janus激酶抑制剂治疗的骨髓纤维化患者,特别是呈现贫血的那些。
通过引用并入
本文提及的所有出版物和专利均特此以其整体引入本文作为参考,就像每个个别出版物或专利具体而个别被指明引入作为参考一样。
尽管已经论述了主题的具体实施方案,但上述说明书是举例说明性的而非限制性的。在仔细研究本说明书和随附权利要求书时,许多变化形式对本领域技术人员将变得显而易见。应参考权利要求连同其等同内容的整个范围和说明书连同这种变化形式来确定本发明的整个范围。
- 还没有人留言评论。精彩留言会获得点赞!