一种pH和还原双重响应型载药纳米颗粒的制作方法
本发明涉及一种ph和还原双重响应型载药纳米颗粒,尤其是一种基于微生物发酵产生的高分子聚谷氨酸和胱氨酸、壳聚糖制备的ph和还原双重响应型载药纳米颗粒,属于生物材料和癌症治疗等领域。
背景技术:
癌症是危害人类健康的主要疾病之一,主要治疗方式为化疗药物治疗,然而抗肿瘤药物阿霉素,紫衫醇,喜树碱等在体内对人体其他正常细胞组织具有较大的毒性,药物副作用较大,严重影响人体的其他组织正常代谢。所以寻求一种能提高药物靶向治疗肿瘤,减少对其他组织的损害及其减少药物的浪费是目前需要解决的问题。
聚合物纳米颗粒可以携带药物穿越免疫系统的屏障,到达肿瘤部位,减少药物的浪费。正常生理环境ph为7.4左右,肿瘤微环境ph为6.5-5.0左右,还比正常生理组织具有较强的还原性,利用此性能,研究者们专注研究具有ph和还原性能的药物输送系统,以减少药物对正常组织的损害,提高抗肿瘤药物的靶向释放。2014年中国专利cn103965420b公布了将聚己内酯和n-(2-羟丙基)甲基丙烯酰胺制备的共聚物胶束,但是该体系制备条件复杂,只具有还原响应型,生物相容性差。2017年中国专利cn107412195a利用二氧化硅包裹金纳米粒制备金纳米棒具有ph响应性能,金纳米粒在体内不易降解,且原料价格昂贵,无法普及。
技术实现要素:
针对以上问题,本发明利用生物相容性良好的聚谷氨酸(γ-pga)和胱氨酸,壳聚糖等物质,利用静电自组装、氢键作用等制备了具有ph和还原双重响应性能的纳米颗粒,生物相容性良好,可以实现药物在血液环境中低释放,减轻对正常细胞的损伤,在肿瘤微环境下可以实现药物的大量释放,提高抗肿瘤活性。基于此,本发明还制备了一种具有肿瘤微环境ph还原响应型的阿霉素(dox)药物载体。
本发明提供了制备具有ph和还原双重响应性能的药物载体的方法,包括以下步骤:
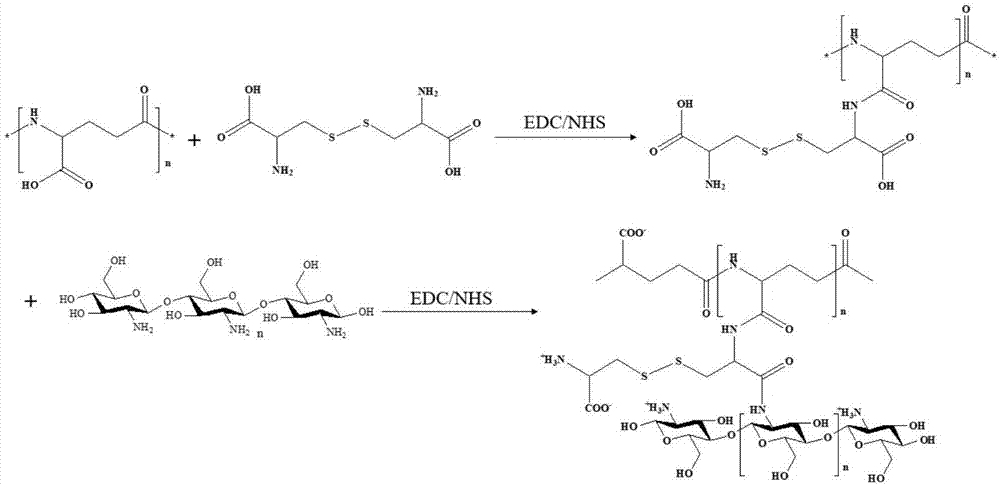
(1)γ-pga-cys的制备:将γ-pga加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和n-羟基琥珀酰亚胺(nhs)中,活化一段时间,加入胱氨酸(cys),搅拌;
(2)将步骤(1)制得的γ-pga-cys添加到壳聚糖中,搅拌,得到药物载体γ-pga-cys–cs。
在本发明的一种实施方式中,步骤(1)γ-pga-cys的制备:取10-50ml0.6-6g/l的γ-pga水溶液加入0.1-0.5g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和0.1-0.5gn-羟基琥珀酰亚胺(nhs)活化2-8h,加入10-60ml0.2-0.6g/l的胱氨酸(cys)水溶液,室温搅拌48h。
在本发明的一种实施方式中,步骤(2)γ-pga-cys-cs纳米颗粒(nps)的制备:用微量注射泵按照2-10ml/h的速度将γ-pga和cys混合液滴加到0.1-0.6g/l的壳聚糖水溶液中,室温搅拌。
在本发明的一种实施方式中,所述聚谷氨酸(γ-pga)的分子量为500万左右。
本发明还提供了应用所述药物载体制备盐酸阿霉素载药纳米颗粒的方法,是配置1-6g/l的dox水溶液,将其加入到γ-pga-cys-cs水溶液中,室温、避光、600-800rpm搅拌24h左右,置于透析袋中(mwco=8000-14000),透析至透析液中检测不到dox的紫外吸收。利用冷冻干燥来获得γ-pga-cys-cs-dox载药纳米颗粒s。
为了减少药物的浪费提高药物的利用率,减缓抗肿瘤药物(dox)对正常细胞的损伤,提高药物对肿瘤细胞的药效等问题,本发明提供了一种载药纳米颗粒,使其在血液生理环境条件下稳定、在肿瘤微环境(弱酸和还原环境)下裂解释放大量药物,从而减少药物在血液循环中对正常细胞的损伤,提高药物对肿瘤细胞的药效。本发明采用上述方案后,具有以下
有益效果:
(1)γ-pga-cys-cs-doxnps在生理条件ph7.4下形态良好,为单一均匀的球形结构。
(2)γ-pga-cys-cs-doxnps在生理条件ph7.4下抗蛋白吸附能力强,生物相容性良好。
(3)γ-pga-cys-cs-doxnps在生理条件下ph7.4时释放量低,在肿瘤微环境及溶酶体微环境下释放量高。
(4)载体γ-pga-cys-csnps对nih3t3细胞没有毒性,γ-pga-cys-cs-doxnps能减少对nih3t3细胞的毒性。
(5)载体γ-pga-cys-csnps对肿瘤细胞hela细胞没有毒性,γ-pga-cys-cs-doxnps能提高对hela细胞的抑制作用。
附图说明
图1γ-pga-cys-csnps制备机理图
图2γ-pga-cys-cs-doxnps在生理条件ph7.4下的tem图
图3γ-pga-cys-cs-doxnps在肿瘤微环境ph5.0(5mmgsh)下的tem图
图4γ-pga-cys-cs-doxnps的傅里叶光谱图
图5γ-pga-cys-cs-doxnps的x-rd图
图6γ-pga-cys-cs-doxnps及其游离dox的细胞摄取图。dox代表药物的红色荧光,dapi为细胞核染色剂呈现蓝色荧光,merge为两者的混合通道,即展示两者的混合荧光。
具体实施方式
实施例1微生物发酵制备高分子量聚谷氨酸(γ-pga)
将甘油管保存的枯草芽孢杆菌hb-7接种于30mllb种子培养基,37℃,110rpm活化12h,按照10%的接种量接种至30ml发酵培养基(还原糖60g/l,胰蛋白胨30g/l,一水谷氨酸钠40g/l,mgso4-7h2o0.5g/l,cacl20.5g/l,nacl10g/l),37℃,110rpm培养48h后,收集发酵液,12000rpm离心30min去除菌体,加入4倍体积的乙醇,4℃冰箱过夜沉淀聚谷氨酸,12000rpm离心30min去除上清液(培养基成分),沉淀用去离子水重悬溶解,再次用乙醇沉淀,离心后沉淀再次用去离子水重悬,置于透析袋中(8000-14000)透析3-5天,冷冻干燥成γ-pga纯品。采用凝胶色谱柱测试γ-pga分子量为500万左右。
实施例2γ-pga-cysnps的制备
取10-50ml0.6-6g/l的γ-pga水溶液加入0.1-0.5g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)和0.1-0.5gn-羟基琥珀酰亚胺(nhs)活化2-8h,加入10-60ml不同浓度的胱氨酸(cys)水溶液制备不同
表1:
实施例3γ-pga-cys-csnps的制备
将按照实施例2制备的
表2:不同ph对γ-pga-cys-csnps粒径和电位的影响
实施例4γ-pga-cys-cs-doxnps的制备
将按照实施例3制备的γ-pga-cys-csnps纳米颗粒与0.5-5g/ldox水溶液混合,dox与γ-pga-cys-cs的质量比为2:3,600-800rpm搅拌48h左右,透析(mwco=8000-14000)除去未包埋的药物。用2m盐酸和2m氢氧化钠调节ph至2.5,4.0,5.0,6.5,7.4,采用马尔文纳米粒径仪(dls)测定不同ph下的粒径和电位。
结果如表3所示,载药后的纳米颗粒γ-pga-cys-cs-doxnps和载药前的纳米颗粒γ-pga-cys-cs一样,具有ph响应性能,粒径随着ph的减小而增大。
采用透射电镜(tem)表征γ-pga-cys-cs-doxnps在生理条件(ph7.4)下和肿瘤微环境(ph5.0+5mmgsh)下的大小和形态。结果显示:生理条件(ph7.4)下载药纳米颗粒γ-pga-cys-cs-doxnps具有良好的形态,粒径较小(图2)。在肿瘤微环境(ph5.0+5mmgsh)下(图3)粒径明显增大,形态依旧保持圆球形,证明γ-pga-cys-cs-doxnps具有ph和还原双重敏感性能。
图4展示了γ-pga-cys-csnps的红外分析图,证明cys通过二硫键连接到γ-pga上。
图5展示了载药纳米颗粒γ-pga-cys-cs-doxnps与空白纳米颗粒γ-pga-cys-csnps的吸收峰的不同,证明药物dox确实包埋于载体内部。载药率为68%(dox/载体(w/w))。
表3:载药纳米颗粒在不同ph下的粒径和电位变化
实施例5γ-pga-cys-cs-doxnps生物相容性实验
按照实施4方法制备的载药纳米颗粒γ-pga-cys-cs-dox分别用2mhcl和/或2mnaoh调解ph,得到ph5.0、ph6.5、ph7.4的溶液,然后向ph5.0、ph6.5的溶液中分别添加终浓度5mm的谷胱甘肽。取10ml不同ph和还原环境下的γ-pga-cys-cs-doxnps溶液,与10ml0.5g/l的牛血清蛋白溶液混合,置于37℃110rpm摇床反应,间隔48h,取出1ml混合溶液,12000rpm离心5min,取上清液,稀释10-20倍,用考马斯亮蓝法测定未吸附蛋白含量。结果显示在生理条件下(ph7.4)抗蛋白吸附能力良好。
表4:γ-pga-cys-cs-doxnps在不同ph和还原环境下对蛋白的吸附率(48h)
注:(蛋白吸附率=牛血清蛋白总质量-未吸附到γ-pga-cys-cs-doxnps上的蛋白的质量)/牛血清蛋白总质量×100%
实施例6γ-pga-cys-cs-doxnps在不同ph和还原环境下药物释放
γ-pga-cys-cs-doxnps的药物释放实验在体外模拟肿瘤微环境ph和还原环境下进行,所述体外模拟肿瘤微环境ph和还原环境,包括ph5.0的含5mmgsh的柠檬酸缓冲液、ph6.5的含5mmgsh的柠檬酸缓冲液和ph为7.4的磷酸钠缓冲液。
取5ml制备好的γ-pga-cys-cs-doxnps水溶液,置于透析袋中(mwco=8000-14000),浸入20ml所述不同ph和还原力的体外模拟肿瘤微环境ph和还原环境中,37℃,110rpm摇床开始透析,间隔一定时间取5ml透析液,同时补加5ml新鲜的缓冲液使得总释放介质体积不变,置于480nm处测定其吸光度,根据标准曲线算出不同时刻的药物浓度,从而计算不同时间段的dox累积释放量。每个ph下设置3个平行对照,取其平均值为最终结果。
其中,v0为总释放介质的体积,ci为第i次取样的药物(dox)浓度(mg/l),v为每次取样的体积,m为透析袋内的总载药量。载药量为纳米颗粒内部的药物总浓度,取1ml载药纳米颗粒冻干,用dmso溶解,在480nm下可以测定出来吸光度,根据标准曲线计算药物浓度,即载药纳米颗粒的内部药物浓度。
结果显示γ-pga-cys-cs-doxnps在ph7.4下40h-70h时间内dox累积释放率为20%,在ph6.5(5mmgsh)下释放90%,在ph5.0(5mmgsh)下释放98%。
实施例7γ-pga-cys-cs和γ-pga-cys-cs-doxnps对正常细胞nih3t3细胞的毒性
取对数期生长的nih3t3细胞,调整细胞悬液浓度,每孔加入200μl,按照细胞密度8×103每孔铺板,5%co2,37℃孵育,过夜培养24h至细胞单层铺满孔底(96孔平底板)。
每孔加入50μl一定浓度的按照实施例4方法制备的载药纳米颗粒溶液(根据药物浓度确定,即0.05、0.5、1.0、2.0μg/ml),游离药物(0.05、0.5、1.0、2.0μg/ml)和空白药物载体(2、10、50、200、500、1000μg/ml),每个浓度设6个复孔。同时设置未添加载药纳米颗粒溶液、游离药物、空白药物载体的细胞为空白对照组。将实验组、空白对照组于5%co2,37℃孵育48小时。每孔加入20μlmtt溶液(5mg/ml,即0.5%mtt),继续培养4h,小心吸去孔内培养液。每孔加入150μl二甲基亚砜(dmso),置摇床上低速振荡10min,使蓝紫色结晶物充分溶解。在酶联免疫检测仪od490nm处测量各孔的吸光值。
细胞存活率(%)=(实验组od490/空白对照组od490)×100%
结果显示高达1000μg/ml的载体γ-pga-cys-cs对nih3t3细胞无毒,细胞存活率高达89%以上。如表6所示,高达1000μg/ml的载体对细胞的毒性依旧很低。
表5:γ-pga-cys-cs-doxnps和游离dox对nih3t3细胞的毒性实验
注:表中dox浓度包括了载药纳米颗粒中药物浓度和游离药物浓度,表5是测定了载药纳米颗粒中药物浓度和游离药物浓度相同时,相应浓度下的细胞存活率。
表6:不同浓度的载体γ-pga-cys-cs对正常细胞的细胞毒性
实施例8γ-pga-cys-cs和γ-pga-cys-cs-doxnps抗肿瘤hela活性测试
按照实施例7的方法检测γ-pga-cys-cs和γ-pga-cys-cs-doxnps对hela细胞生长的抑制作用。结果显示,1000μg/ml的载体γ-pga-cys-cs对hela细胞无毒,细胞存活率高达96%以上。如表7所示,γ-pga-cys-cs-doxnps抗肿瘤性能良好,特别之处在于,载药颗粒抑制肿瘤细胞生长的能力强于游离药物。
表7γ-pga-cys-cs-doxnps和游离dox对hela细胞的生长抑制作用
注:表中dox浓度包括了载药纳米颗粒中药物浓度和游离药物浓度,表7是测定了载药纳米颗粒中药物浓度和游离药物浓度相同时,相应浓度下hela细胞的细胞存活率。
表8:不同浓度的载体γ-pga-cys-csnps对hela细胞的毒性
实施例9
将hela细胞按照每孔105个细胞接种到含有圆玻片的6孔板中,每孔含有1ml培养液,将培养板放入培养箱中培养12-24h,待细胞贴壁后,移除培养液,分别加入终浓度为5μg/ml的γ-pga-cys-cs-dox和dox,培养箱继续培养4h,移除培养液,用pbs洗涤3-5次,加入含有dapi的4%的多聚甲醛,室温固定染色5-10min,pbs洗涤2-3次,自然晾干,加少量防淬灭剂封片,激光共聚焦观察拍照。
如图6所示,在hela细胞摄取相同时间时(4h),载药纳米颗粒γ-pga-cys-cs-doxnps相比游离药物dox具有更明显的红色荧光,证明γ-pga-cys-cs-doxnps使得药物更容易进入细胞。
虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
- 还没有人留言评论。精彩留言会获得点赞!