一种白藜芦醇纳米混悬液及其制备方法与流程
本发明属于药物制剂
技术领域:
,涉及一种白藜芦醇纳米混悬液处方及制备方法。
背景技术:
:白藜芦醇(resveratrol)为非黄酮类多酚化合物,又称为芪三酚,化学名称为3,5,4′-三羟基二苯乙烯,具有抗肿瘤、抗心脑血管疾病、抗突变、抗氧化、抗菌消炎、保护肝脏、诱导细胞凋亡、雌激素样作用及降低血糖等多种生物药理活性。白藜芦醇自然资源丰富,加之具有较高的安全性,故在医药、食品、化妆品等行业中有着广阔的应用前景。白藜芦醇难溶于水,口服吸收较差,生物利用度较低。为克服白藜芦醇稳定性差和溶解度低的问题、提高其生物利用度技术的研究,体外研究发现,壳聚糖交联的微球、环糊精纳米囊,脂质体,mpeg-pcl纳米粒,酵母细胞包合的白黎芦醇和其它纳米输送系统,可提高白黎芦醇的溶解度、体外稳定性和体外释放等性能。这些技术在改善白黎芦醇的溶解度、稳定性和体外释放性能或生物利用度问题方面也显示出了一定程度的成功,但总体上,生物利用度只得到了有限提高,进一步研究表明,白藜芦醇口服生物利用度低的主要原因是因为葡萄糖醛酸化和硫酸化所引起的ⅱ相代谢,单纯提高溶解度、稳定性或肠道通透性只能部分提高生物利用度。由于其在肠道存在广泛的ⅱ相代谢。如何研究开发有效制剂手段调控肠道ⅱ相代谢、提高白藜芦醇生物利用度对这一类天然产物的新药制剂开发具有重要的理论与应用价值。纳米混悬剂是“纯的”药物纳米粒子的胶态分散体系。与传统意义上的基质骨架型纳米体系不同,纳米混悬剂无需载体材料,它是通过表面活性剂的稳定作用,将纳米尺度的药物粒子分散在水中形成的稳定体系。由于纳米混悬剂的特性,其在各种给药途径中都体现出独特的优势:如处方简单、制备快速、有利于降低活性化合物的筛选成本、提高药物溶出度和生物利用度、摒除附加成分造成的刺激性和毒副作用以及较低的给药体积等。技术实现要素:基于以上
背景技术:
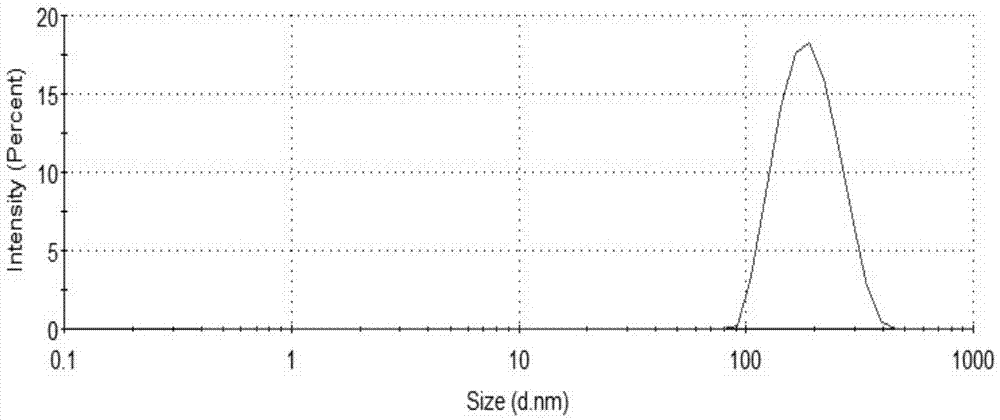
,针对目前白藜芦醇剂型的不足,本发明的目的是提供一种白藜芦醇纳米混悬液处方及制备方法,通过改进稳定剂的选择,优化处方设计,以期促进白藜芦醇的溶出和体内吸收,提高生物利用度。发明人通过在单因素考察的基础上,应用bbd-效应面法优化白藜芦醇纳米混悬液的制备工艺,确定最佳制备工艺。以最佳的制备工艺得到白藜芦醇纳米混悬液,然后通过冷冻干燥进行固化来对该制剂进行了全面的体外评价,包括粒径及粒径分布、zeta电位、透射电子显微镜(tem)、x-射线衍射(xrd)、差示扫描量热法(dsc)、体外溶出度分析、药动实验,旨在生产一种更为安全、稳定、生物利用度高、适于工业化生产的白藜芦醇纳米制剂。本发明采用的技术方案是:一种白藜芦醇纳米混悬液,由白藜芦醇,稳定剂和水组成。稳定剂为聚氧乙烯氢化蓖麻油rh40和聚维酮k30的组合物。所述的白藜芦醇纳米混悬液中,各组分的质量浓度为:聚氧乙烯氢化蓖麻油rh40为0.2%-0.9%,聚维酮k30为0.15%-0.25%;白藜芦醇为0.1%-0.2%,余量为水。其中,聚氧乙烯氢化蓖麻油rh40与聚维酮k30的质量比为:6:1-1:1,优选为:3:2-2:1。作为优选,当聚氧乙烯氢化蓖麻油rh40与聚维酮k30的质量比为:3:2-2:1时,制备的纳米混悬剂的粒径为100-300nm,稳定性好,生物利用度高。本发明还提供了所述白藜芦醇纳米混悬液的制备方法,包括以下步骤:(1)将稳定剂聚氧乙烯氢化蓖麻油rh40和聚维酮k30溶于水形成水性分散介质。放置在冰水浴中控制温度在4-10℃。(2)将白藜芦醇溶于无水乙醇形成白藜芦醇乙醇溶液。(3)在搅拌条件下将白藜芦醇乙醇溶液快速加入含有稳定剂的水溶液中,继续搅拌10-15min,得到白藜芦醇纳米混悬液。作为优选,所述步骤(1)分散介质中稳定剂聚氧乙烯氢化蓖麻油rh40的质量体积浓度为0.2%-0.9%(2-3mg/ml);聚维酮k30的质量体积浓度为0.15%-0.25%(1.5-2.5mg/ml);所述步骤(2)药物的质量体积浓度为0.1%-0.2%(20-40mg/ml);所述步骤(3)转速为1000-2500r/min。所述纳米混悬剂的粒径在100nm-1000nm,优选为100nm-300nm。本发明经过筛选发现,在稳定剂聚氧乙烯氢化蓖麻油rh40的质量浓度为0.2%-0.9%;聚维酮k30的质量浓度为0.15%-0.25%,药物的质量浓度为0.1%-0.2%时,制备成的白藜芦醇纳米混悬液,具有良好的粒径分布和溶出速率,可供口服用于疾病的治疗。本发明的优点在于:(1)白藜芦醇纳米混悬液的粒径小,分布窄,能增加药物的溶出速率,体内生物利用度也有显著提高。(2)所使用的稳定剂聚氧乙烯氢化蓖麻油rh40具有抑制葡萄糖醛酸转移酶的作用,进而可以抑制白藜芦醇的肠道ⅱ相代谢,从而提高口服生物利用度。(3)该纳米混悬剂的处方及制备工艺简单,载药量大,所得制剂安全有效,成本较低。(4)本发明的白藜芦醇纳米混悬液可以进一步加工固化成固体制剂。如冷冻干燥可长期保存。附图说明图1白藜芦醇纳米混悬液的粒径分布图;图2白藜芦醇纳米混悬液的透射电镜形貌图;图3聚氧乙烯氢化蓖麻油rh40浓度,聚维酮k30浓度和白藜芦醇浓度对白藜芦醇纳米混悬液粒径的预测效应图图4聚氧乙烯氢化蓖麻油rh40浓度,聚维酮k30浓度和白藜芦醇浓度对白藜芦醇纳米混悬液粒径分布pdi的预测效应图图5白藜芦醇原料药和白藜芦醇纳米混悬液的冷冻干燥粉末的溶出曲线图;图6白藜芦醇原料药和白藜芦醇纳米混悬液的血药浓度图。具体实施方式实施例1粒径和粒径pdi为指标,进行稳定剂的筛选,操作如下。将稳定剂溶于水形成稳定剂的浓度为5mg/ml的水性分散介质;放置在冰水浴中控制温度在4℃。将白藜芦醇溶于无水乙醇形成白藜芦醇乙醇溶液,其浓度为20mg/ml。在1500r/min搅拌条件下将白藜芦醇乙醇溶液快速加入含有稳定剂的水分散介质中,继续搅拌10-15min,得到白藜芦醇纳米混悬液。所采用的稳定剂和制得的混悬液的粒径和pdi列于表1中。由表可知稳定剂为f68和聚维酮k30(1:1)和rh40和聚维酮k30(1:1)制得的混悬液粒径最小且最均匀,室温放置7天仍然稳定。表1不同稳定剂制备混悬液的粒径和粒径分布实施例2单因素筛选制备过程为:将稳定剂(pvpk30或/和rh40)溶于水形成一定浓度的稳定剂的水性分散体系;放置在水浴中控制一定温度。将白藜芦醇溶于无水乙醇形成白藜芦醇一定浓度的乙醇溶液。在一定搅拌速度下将白藜芦醇乙醇溶液快速加入含有稳定剂的水分散介质中,继续搅拌10-15min,得到白藜芦醇纳米混悬液。固定稳定剂的水性分散体系中pvpk30浓度为20mg/10ml,白藜芦醇乙醇溶液为10mg/ml,水浴温度为15℃,在1200r/min搅拌条件下将白藜芦醇乙醇溶液快速加入含有稳定剂的水分散介质中,采用不同的水性分散体系中rh40浓度,所制得混悬液的粒径和pdi结果如下。rh40浓度(mg/10ml)306090粒径(nm)273.39307.46325.7pdi0.260.2130.158固定稳定剂的水性分散体系中rh40浓度为20mg/10ml,白藜芦醇乙醇溶液为10mg/ml,水浴温度为15℃,在1200r/min搅拌条件下将白藜芦醇乙醇溶液快速加入含有稳定剂的水分散介质中,不同的水性分散体系pvpk30浓度所制得混悬液的粒径和pdi结果如下。聚维酮k30浓度(mg/10ml)102040粒径(nm)488.39167.64505.7pdi0.3850.1240.457固定稳定剂的水性分散体系中rh40浓度为30mg/10ml、pvpk30浓度为20mg/10ml,水浴温度为15℃,在1200r/min搅拌条件下将白藜芦醇乙醇溶液快速加入含有稳定剂的水分散介质中,在不同白藜芦醇乙醇溶液浓度条件下,所制得混悬液的粒径和pdi结果如下。白藜芦醇浓度(mg/10ml)102030粒径(nm)158.77287.56505.7pdi0.0850.2540.467固定稳定剂的水性分散体系中rh40浓度为30mg/10ml、pvpk30浓度为20mg/10ml,白藜芦醇乙醇溶液为10mg/ml,在1200r/min搅拌条件下将白藜芦醇乙醇溶液快速加入含有稳定剂的水分散介质中,在不同水浴温度下所制得混悬液的粒径和pdi结果如下。固定稳定剂的水性分散体系中rh40浓度为30mg/10ml、pvpk30浓度为20mg/10ml,白藜芦醇乙醇溶液为10mg/ml,水浴温度为15℃,在搅拌条件下将白藜芦醇乙醇溶液快速加入含有稳定剂的水分散介质中,在不同搅拌速度所制得混悬液的粒径和pdi结果如下。转速(rpm/min)40012002400粒径(nm)182.8169.35166.73pdi0.2040.1690.133综合以上单因素筛选,聚氧乙烯氢化蓖麻油rh40的质量浓度,聚维酮k30质量浓度,以及白藜芦醇药物的质量浓度对白藜芦醇纳米混悬剂的粒径和分布具有较明显的影响。其中聚氧乙烯氢化蓖麻油rh40质量浓度为0.3%-0.9%,聚维酮k30质量浓度为0.15%-0.35%,白藜芦醇药物的质量浓度为0.1%-0.3%。实施例3box-behnken中心组合设计试验优选白藜芦醇纳米混悬液制备处方在稳定剂筛选和单因素筛选的基础上,选择对白藜芦醇纳米混悬液制备工艺影响显著的3个因素,即稳定剂聚氧乙烯氢化蓖麻油rh40浓度(a)、聚维酮k30浓度(b)、白藜芦醇浓度(c)为考察因素,以粒径大小及多分散系数pdi为响应值进行box-behnken中心组合设计(见表2和表3),建立数学模型优化处方。本实验以白藜芦醇纳米混悬液的粒径和pdi为响应值,聚氧乙烯氢化蓖麻油rh40浓度(a)、聚维酮k30浓度(b)、白藜芦醇浓度(c)为考察因素,采用box-behnken效应面法优化白藜芦醇纳米混悬液制备处方,并进行预测分析。聚氧乙烯氢化蓖麻油rh40浓度,聚维酮k30浓度和白藜芦醇浓度对白藜芦醇纳米混悬液粒径和粒径分布的预测效应图分别见图3和图4。实验结果通过软件分析并结合回归模型的数学分析得到白藜芦醇纳米混悬液最优处方:表2box-behnken中心组合设计实验为检验响应面法的可靠性,采用上述最优处方进行白藜芦醇纳米混悬液的制备,重复试验3次。试验表明采用box-behnken设计-响应面优化得到的处方准确可靠,重现性好。表3box-behnken中心组合设计实验分析结果综合以上的实验结果确定白藜芦醇纳米混悬液的最优条件为:将67mg聚氧乙烯氢化蓖麻油rh40和23mg聚维酮k30加入约10ml蒸馏水中,搅拌溶解,放入冰水浴中温度在4-10℃左右,制成稳定剂水溶液。称取15mg的白藜芦醇原料药,溶于0.5ml的无水乙醇中,制成白藜芦醇乙醇溶液。将白藜芦醇乙醇溶液在搅拌下快速加入稳定剂水溶液中,继续搅拌10min,即得白藜芦醇纳米混悬液。实施例4白藜芦醇纳米混悬液的制备处方:制备方法:将聚氧乙烯氢化蓖麻油rh40和聚维酮k30加入约10ml蒸馏水中,搅拌溶解,放入冰水浴中温度在4-10℃左右,制成稳定剂水溶液。称取处方量的白藜芦醇原料药,溶于0.5ml的无水乙醇中,制成白藜芦醇乙醇溶液。将白藜芦醇乙醇溶液在1000-2500r/min搅拌下快速加入稳定剂水溶液中,继续搅拌10min,即得白藜芦醇纳米混悬液。该方法制备的白藜芦醇纳米混悬液的平均粒径为134.5nm,pdi为0.093。取上述白藜芦醇纳米混悬液加入冻干保护剂进行冷冻干燥,得到白藜芦醇纳米混悬液冻干粉末。实施例5白藜芦醇纳米混悬液的制备处方:制备方法:将聚氧乙烯氢化蓖麻油rh40和聚维酮k30加入约10ml蒸馏水中,搅拌溶解,放入冰水浴中温度在4-10℃左右,制成稳定剂水溶液。称取处方量的白藜芦醇原料药,溶于0.5ml的无水乙醇中,制成白藜芦醇乙醇溶液。将白藜芦醇乙醇溶液在1000-2500r/min搅拌下快速加入稳定剂水溶液中,继续搅拌10min,即得白藜芦醇纳米混悬液。该方法制备的白藜芦醇纳米混悬液的平均粒径为184.5nm,pdi为0.103。制得纳米混悬剂记为纳米混悬剂1,测定粒径分布图如图1,测得透射电镜照片如图2b。取上述白藜芦醇纳米混悬液加入冻干保护剂进行冷冻干燥,得到白藜芦醇纳米混悬液冻干粉末。实施例6白藜芦醇纳米混悬液的制备处方:制备方法:将聚氧乙烯氢化蓖麻油rh40和聚维酮k30加入约10ml蒸馏水中,搅拌溶解,放入冰水浴中温度在4-10℃左右,制成稳定剂水溶液。称取处方量的白藜芦醇原料药,溶于0.5ml的无水乙醇中,制成白藜芦醇乙醇溶液。将白藜芦醇乙醇溶液在1000-2500r/min搅拌下快速加入稳定剂水溶液中,继续搅拌10min,即得白藜芦醇纳米混悬液。该方法制备的白藜芦醇纳米混悬液的平均粒径为263.5nm,pdi为0.127。取上述白藜芦醇纳米混悬液加入冻干保护剂进行冷冻干燥,得到白藜芦醇纳米混悬液冻干粉末。实施例7白藜芦醇纳米混悬液的制备由于f68和聚氧乙烯氢化蓖麻油rh40都是非离子型表面活性剂,二者物理化学性质相似,可以尽量减小因二者的差异性引起的白藜芦醇在肠道吸收的不同。以此处方作为对照研究聚氧乙烯氢化蓖麻油rh40的对白藜芦醇大鼠体内药物动力学的影响。因此按照据文献处方制备一种如下混悬剂作为药物动力学对照研究。制备方法:将泊洛沙姆f68和聚维酮k30加入约10ml蒸馏水中,搅拌溶解,放入冰水浴中温度在4-10℃,制成稳定剂水溶液。称取处方量的白藜芦醇原料药,溶于0.5ml的无水乙醇中,制成白藜芦醇乙醇溶液。将白藜芦醇乙醇溶液在1000-2500r/min搅拌下快速加入稳定剂水溶液中,继续搅拌10min,即得白藜芦醇纳米混悬液。该方法制备的白藜芦醇纳米混悬液的平均粒径为175.7nm,pdi为0.154。制得纳米混悬剂记为纳米混悬剂2,测定的透射电镜图片如图2b。取上述白藜芦醇纳米混悬液加入冻干保护剂进行冷冻干燥,得到白藜芦醇纳米混悬液冻干粉末。实施例8白藜芦醇纳米混悬液体外溶出度研究溶出度测定法:取适量样品(相当于白藜芦醇5mg)照溶出度测定法(中国药典2015版)以250ml水为溶出介质,转速为100r/min,经5,10,15,30,45,60,90,120min时,取溶液5ml(同时补加5ml溶出介质),0.22μm滤膜过滤,取续滤液作为供试品溶液,采用紫外分光光度法,在306nm波长处分别测定吸光度,计算溶出量,其溶出曲线图5,其中实施例3为白藜芦醇纳米混悬剂1,实施例7为白藜芦醇纳米混悬剂2表明纳米混悬剂能显著提高白藜芦醇的溶出速度和程度。实施例9白藜芦醇纳米混悬液体内药物动力学研究取sd大鼠15只,体重为200g±20g,随机分成三组,每组5只,给药前禁食12小时,自由饮用生理盐水。给药前称重标号,两组大鼠分别按照50mg/kg的剂量口服白藜芦醇原料药,实施例3白藜芦醇纳米混悬剂1,和实施例7白藜芦醇纳米混悬剂2分别于给药后5,15,30,60,90,120,180,240,360,480min后眼眶取血0.5ml,并置于肝素钠浸润干燥后的离心管中,将血液以4000rpm离心10min取上层血浆。用移液枪精密吸取血浆样品100μl,加入内标卡马西平溶液25μl混合30s后,用300μl乙腈涡旋提取5min,12000r/min离心10min,取上层并用氮气吹干,残留物加入100μl流动相溶解后进样,用hplc进行测定。记录各个时间点样品峰与内标峰的面积as、ai,以r=as/ai代入标准曲线方程计算测定浓度。通过计算,白藜芦醇原料药及白藜芦醇口服纳米混悬剂药时曲线图如图6,计算的药物动力学参数如表4。白藜芦醇纳米混悬剂1的auc分别是白藜芦醇混悬液和白藜芦醇纳米混悬剂2的5.67倍和1.73倍,可以看出聚氧乙烯氢化蓖麻油rh40作为稳定剂的白藜芦醇纳米混悬剂能够显著增加白藜芦醇口服生物利用度。表4白藜芦醇及其口服纳米混悬剂药物动力学参数表当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1