一种逆转肺纤维化纳米制剂及其制备方法与流程
本发明涉及一种循环纤维细胞介导的负载双药和/或单药逆转肺纤维化纳米制剂,特别涉及一种肺纤维化体内循环纤维细胞靶向的负载双药和/或单药纳米制剂的制备及其应用。
背景技术:
肺纤维化是一种进行性,致死率极高的肺间质病变疾病,生存期为3-5年。近些年,由于环境污染造成空气中粒子(pm2.5)过高,导致肺泡上皮细胞ⅰ(at1)、ⅱ(at2)损伤。其中,at1细胞胞内结构简单,主要负责肺泡氧气的吸入与二氧化碳的呼出;at2细胞被称为肺组织的干细胞样细胞,有自我更新能力。当at2受到损伤后,肺泡的增殖能力会受到严重破坏,出现肺泡功能不可逆的破坏后,分泌大量炎症因子,激活成纤维细胞向肌成纤维细胞转化,活化的肌成纤维细胞是损伤部位胶原蛋白分泌的主要来源,在肺纤维化的病理中发现,生成的胶原对肌成纤维细胞存在正反馈的调节,从而造成上皮细胞损伤部位的胶原大量堆积,细胞间隙被胶原挤压填充,即形成肺纤维化。目前,经fda批准了两种抗肺纤维化的口服药物,分别为吡非尼酮与尼达尼布。但是仅能达到延缓疾病进程,不能修复受损肺组织实现逆转肺纤维化的目的。
at2肺泡上皮细胞ⅱ在肺纤维化的发展中起着至关重要的作用。在肺纤维化发展进程中,受损伤的at2会招募大量的炎症细胞迁移到肺部,包括巨噬细胞,中性粒细胞,嗜酸性细胞及嗜碱性细胞,这些细胞在肺纤维化微环境的刺激下,会分泌大量的炎症因子,包括tnf-β,il-4,il-13,il-1β等,炎症反应进一步加剧,并招募大量骨髓来源的循环纤维细胞及肺成纤维细胞向肌成纤维细胞转化,活化的肌成纤维细胞分泌大量胶原并蓄积,进而加速纤维化的进程。因而,在肺纤维化的治疗中,修复受损伤的at2是能够逆转肺纤维化疾病的关键治疗靶点。
纳米制剂在疾病治疗中得到越来越广泛的关注,但纳米制剂在肺部疾病递送中仍存在靶向性差、递送效率低的缺点。
技术实现要素:
目的:为了克服现有肺纤维化治疗中存在的缺陷,本发明提供一种高效靶向递送的逆转肺纤维化纳米制剂。
技术方案:为解决上述技术问题,本发明采用的技术方案为:
一种用于负载抗肺纤维化药物的纳米制剂载体,其特征在于:所述纳米制剂载体为x-peg-mal,修饰具有循环纤维细胞受体y靶向的靶向肽、抗体、趋化因子e5,和/或,修饰具有肺泡上皮细胞ⅱ靶向的多肽z;其中x为疏水段,x选自plga、pla、pga、pcl;y为循环纤维细胞高表达受体,包括cxcr4、ccr2、ccr7;多肽z包括crgd、rgdf(c)、rgd。
进一步的,所述的纳米制剂载体,其特征在于:包括仅修饰有e5的载体ppe、仅修饰有多肽z的载体ppr、同时修饰有e5和多肽z的载体pper。
进一步的,所述的纳米制剂载体,其特征在于:e5包括cxcr4受体的靶向肽、抗体、趋化因子,ccr7受体的靶向肽、抗体或趋化因子及ccr2受体的靶向肽、抗体或趋化因子;更优选的,使用巯基修饰的e5。多肽z包括crgd、rgdf(c)、rgd。
本发明中,所述抗肺纤维化药物为抗氧化剂、抑制剂中的一种或几种,抗氧化剂为缓解细胞水平氧化应激的药物或生物活性分子,抑制剂为抑制成纤维细胞活化的药物或生物活性分子。负载的抗肺纤维化药物可以同时包括抗氧化剂、抑制剂,或选自抗氧化剂、抑制剂中的一种。负载的抗肺纤维化药物均具有一定疏水性,通过双亲性嵌段共聚物中的疏水段x实现对具有一定抗肺纤维化药物负载,通过peg实现聚合物胶束在体内的长循环,通过修饰的e5特异性靶向体内的循环纤维细胞,实现肺部高效递送。通过多肽z能够特异性靶向受损伤的at2,实现了抗肺纤维化药物对受损伤at2高效的靶向递送。
更优选的,所述抗氧化剂为虾青素,抑制剂为曲美替尼。所述逆转肺纤维化纳米制剂同时负载有曲美替尼和虾青素。同时采用双药协同调控肺纤维化微环境,为抗肺纤维化药物的高效递送及逆转肺纤维化的药物设计提供了一种新的途径和策略。
本发明还提供一种逆转肺纤维化纳米制剂,其特征在于:为上述的纳米制剂载体负载有抗肺纤维化药物,包括pper/药物,ppe/药物,ppr/药物。其中,负载抗肺纤维化药物可以同时包括抗氧化剂、抑制剂,或选自抗氧化剂、抑制剂中的一种。抗氧化剂为缓解细胞水平氧化应激的药物或生物活性分子,抑制剂为抑制ctgf表达的药物或生物活性分子。
1)抗氧化剂:
抗氧化药物:大黄、三七、银杏、陈皮、荷叶、桑叶、何首乌、丹参、黄芪、大蒜、川芎、红景天、鹿茸等中药提取物,普罗布考、吲达帕胺、维拉帕米。
抗氧化活性成分:维生素e、类胡萝卜素及其衍生物(虾青素、角黄素、叶黄素、β-胡萝卜素)、金枪鱼黄素、角黄质、人参总皂苷、黄酮甙类和萜烯内酯类、枸杞多糖、联苯环辛烯类木脂素如五味子酚、五味子乙素、五味子丙素、绞股蓝、藻类多糖、菌类多糖等植物多糖、丁基羟基茴香醚(bha)、二丁基羟基甲苯(bht)、没食子酸丙酯(pg)、特丁基对苯二酚(tbhq);
2)成纤维细胞活化抑制剂:曲美替尼、尼达尼布、吡非尼酮、尼洛替尼、水飞蓟宾、姜黄素、白藜芦醇、丹参酮a、黄连素、五味子素、丹酚酸a,b、木犀草素、没食子儿茶素、川芎嗪等。
所述抗肺纤维化药物包括缓解细胞水平氧化应激的药物或生物活性分子,抑制成纤维细胞活化抑制剂的药物或生物活性分子。
具体的,pper/药物的制备方法:
步骤(1)首先将抗肺纤维化药物与x-peg-mal混合,通过薄膜分散法、直接滴定法或反向溶剂法制备负载抗肺纤维化药物的纳米粒;
步骤(2)将负载抗肺纤维化药物的纳米粒与巯基修饰的e5和巯基修饰的多肽z反应,通过巯基和纳米粒外壳暴露的mal反应,在纳米粒的外端共价修饰e5和多肽z;纳米粒通过共价修饰的e5和多肽z,实现循环纤维细胞和肺泡上皮细胞ⅱ靶向的目标。
反应中,加入的聚合物纳米粒、巯基修饰的e5质量比为30:1~12:1;更优选为15:1。
反应中,加入的聚合物纳米粒、巯基修饰的多肽z质量比为50:1~35:1;更优选为40:1。
ppe/药物的制备方法如下:
步骤(1)首先将抗肺纤维化药物与x-peg-mal混合,通过薄膜分散法、直接滴定法或反向溶剂法制备负载抗肺纤维化药物的纳米粒;
步骤(2)将负载抗肺纤维化药物的纳米粒与巯基修饰的e5反应,通过巯基和纳米粒外壳暴露的mal反应,在纳米粒的外端共价修饰e5;纳米粒通过共价修饰的e5,实现循环纤维细胞靶向的目标。
反应中,加入的聚合物纳米粒、巯基修饰的e5质量比为30:1~12:1;更优选为15:1。
ppr/药物的制备方法如下:
步骤(1)首先将抗肺纤维化药物与x-peg-mal混合,通过薄膜分散法、直接滴定法或反向溶剂法制备负载抗肺纤维化药物的纳米粒;
步骤(2)将负载抗肺纤维化药物的纳米粒与巯基修饰的多肽z反应,通过巯基和纳米粒外壳暴露的mal反应,在纳米粒的外端共价修饰多肽z;纳米粒通过共价修饰的多肽z,实现肺泡上皮细胞ⅱ靶向的目标。
反应中,加入的聚合物纳米粒、巯基修饰的多肽z质量比为50:1~35:1;更优选为40:1。
作为对照,pp/药物的制备方法如下:
步骤(1)首先将抗肺纤维化药物溶于dmso,x-peg-mal与药物的配比100:1~5:1,更优选方案10:1,包封率为82.4%,载药量为7.2%;
步骤(2)与x-peg-mal混合,通过薄膜分散法、直接滴定法或反向溶剂法制备负载抗肺纤维化药物的纳米粒。
作为优选方案,所述的逆转肺纤维化纳米制剂,其特征在于:x-peg-mal中,其中x的分子量范围为1000-50000,peg的分子量范围为200-10000。更优选的使用分子量为2000的peg。
优选地,所述逆转肺纤维化纳米制剂的载药量在2%-20%之间,粒径大小在20nm-500nm之间。
本发明要求上述纳米制剂载体、逆转肺纤维化纳米制剂在制备治疗肺纤维化疾病药物中的应用。
本发明为一种以体内循环纤维细胞作为递送载体高效递送纳米双药/单药达到逆转肺纤维化的目的。特点是该载体包括化学药物负载成份,循环纤维细胞靶向成份及受损伤at2靶向成份。所述化学药物负载成份为末端具有马来酰亚胺修饰的两亲性聚合物,循环纤维细胞靶向成份为巯基化的多肽,受损伤at2靶向的成份为修饰了多肽z的peg。
本发明的还制备了没有e5和多肽z修饰的制剂pp/药物,仅有e5修饰的载体材料ppe/药物,仅有多肽z修饰的载体材料ppr/药物,这些载体材料的制备方式与上述方法相同。
有益效果:本发明提供的以循环纤维细胞作为递送载体包载双药/单药的纳米制剂,与现有技术相比,具有以下优点:载体中的x-peg-mal(x为疏水段,x为plga、pla、pga、pcl)可以很好的实现脂溶性的药物的包载,载体中的peg可延长载体在血液中的循环时间,载体中的修饰的e5可以很好的实现体内循环纤维细胞的特异性靶向,载体中的多肽z能够特异性的实现受损伤at2的特异性靶向。此载体的应用可实现纳米药物的高效肺递送,通过特异性靶向受损伤及修复at2,抑制关键蛋白ctgf,可有效抑制成纤维细胞活化,从而达到逆转肺纤维化的目的。本发明的e5及多肽z修饰的纳米制剂,利用e5特异性靶向体内循环纤维细胞,利用多肽z能够特异性靶向受损伤at2,实现高效的抗肺纤维化双药/单药递送,从而达到逆转肺纤维化目的。本发明首次创新利用体内循环纤维细胞作为递送载体,实现抗肺纤维化药物的高效肺递送,以受损伤at2作为治疗靶点并特异性靶向双药/单药纳米药物制剂,为肺纤维化药物制剂高效递送及逆转治疗提供了一种新的途径。本发明中,首次创新利用肺纤维化过程中,在体内大量增殖的循环纤维细胞靶向作为递送体系,以e5和多肽z同时负载双药/单药的纳米药物制剂从而实现逆转肺纤维化的目的。目前,利用双亲性嵌段共聚物中的疏水嵌段负载疏水性药物进行递送是常见的方法之一,plga(聚乳酸-聚羟基乙酸)、pla(聚乳酸)、pga(聚乙交酯)、pcl(聚己内酯)是常见的具有良好生物相容性的疏水嵌段,常在双亲性嵌段共聚物中作为疏水性内核,对大多数的疏水性药物具有较好的亲和力。
在本发明中,我们利用e5及多肽z修饰的x-peg(x为疏水段,x为plga、pla、pga、pcl)纳米粒,通过双亲性嵌段共聚物中的疏水段实现对具有一定疏水性的双药/单药负载,或通过反向溶剂法可以制备负载亲水性药物的纳米粒,通过peg实现聚合物胶束在体内的长循环,通过修饰的e5特异性靶向体内的循环纤维细胞,实现肺部高效递送。通过多肽z能够特异性靶向受损伤的at2,实现了抗纤维化双药/单药对受损伤at2高效的靶向递送。
附图说明
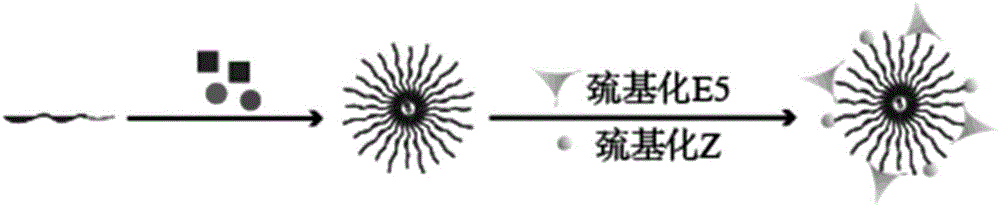
图1是本发明纳米制剂制备的流程示意图;
图2是本发明中所制备的纳米制剂的各成份最佳投料比;
图3是本发明最佳制剂(pper/药物)的纳米制剂粒径分布;
图4是本发明最佳制剂(pper/药物)的纳米制剂透射电镜图;
图5是本发明制剂(pper/药物)的纳米制剂透射电镜图(r=crgd);
图6是本发明制剂(pper/药物)的纳米制剂透射电镜图(r=rgd);
图7是本发明所制备纳米制剂在细胞水平的摄取实验,证明rgdf(c)可以特异性靶向at2,增加纳米制剂的摄取;
图8是本发明所制备的纳米载体在体内水平考察不同载体pper,ppe,ppr,pp,其利用循环纤维细胞作为递送体系的肺递送能力并特异性靶向受损伤at2实现纳米制剂的准确定位;
图9是本发明所制备的纳米载体在体内水平考察不同时间点其利用循环纤维细胞作为递送体系中,纳米制剂在肺内的蓄积变化;
图10是本发明所制备包覆荧光染料(dir)的纳米制剂在造模3周的肺纤维化小鼠中纳米制剂在肺中蓄积的小动物活体成像图片及不同脏器的定量分析。
图11是本发明所制备的纳米载体在体内水平考察不同纳米制剂在逆转肺纤维化的效果分析。
具体实施方式
下面结合附图和具体实施例对本发明作更进一步的说明。
实施例1纳米制剂成份的合成及制备,如图1所示:
一、包载双药/单药的plga-peg-mal纳米粒的制备
采用薄膜分散法,直接滴定法及反向溶剂法均可制备负载抗肺纤维化药物或荧光染料(作为代替药物的模型,用于制剂追踪)的聚合物纳米粒。本发明优选的采用直接滴定法制备包载抗纤维化药物双药/单药(曲美替尼和/或虾青素)的plga-peg-mal纳米粒。具体制备方法如下:
称取100mgplga-peg-mal和10mg双药/单药分别溶于2mldmso溶液中,超声溶解。在搅拌条件下,将dmso溶液滴加至100ml纯水中,室温下继续搅拌搅拌2h后,2500rpm/min离心20min除去未被包载的游离药。使用分子量10000的超滤管浓缩纳米粒至体积为500μl。
二、具有e5及rgdf(c)修饰的聚合物纳米粒制备
e5包括cxcr4受体的靶向肽、抗体、趋化因子,ccr7受体的靶向肽、抗体或趋化因子及ccr2受体的靶向肽、抗体或趋化因子;更优选的,使用巯基修饰的e5。多肽z包括crgd、rgdf(c)、rgd。
抗肺纤维化药物包括:
抗氧化药物及活性成分:
抗氧化药物:大黄、三七、银杏、陈皮、荷叶、桑叶、何首乌、丹参、黄芪、大蒜、川芎、红景天、鹿茸等中药提取物,普罗布考、吲达帕胺、维拉帕米。
抗氧化活性成分:维生素e、类胡萝卜素及其衍生物(虾青素、角黄素、叶黄素、β-胡萝卜素)、金枪鱼黄素、角黄质、人参总皂苷、黄酮甙类和萜烯内酯类、枸杞多糖、联苯环辛烯类木脂素如五味子酚、五味子乙素、五味子丙素、绞股蓝、藻类多糖、菌类多糖等植物多糖、丁基羟基茴香醚(bha)、二丁基羟基甲苯(bht)、没食子酸丙酯(pg)、特丁基对苯二酚(tbhq);
成纤维细胞活化抑制剂:曲美替尼、尼达尼布、吡非尼酮、尼洛替尼、水飞蓟宾、姜黄素、白藜芦醇、丹参酮a、黄连素、五味子素、丹酚酸a,b、木犀草素、没食子儿茶素、川芎嗪等。
1.具有循环纤维细胞受体cxcr4靶向肽及多肽z修饰的聚合物纳米粒制备
e5的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的多肽6.5mg,在纯水溶液中4℃摇床中反应过夜,其中e5为循环纤维细胞受体cxcr4的靶向多肽;
多肽z的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的多肽rgdf(c)2.5mg,在纯水溶液中4℃摇床中反应过夜;利用10000rpm/min离心重悬三次,收集所制备的纳米粒,除去未反应的巯基化的e5和z。
利用本法所制备的pp/(曲美替尼和/或虾青素),ppe/(曲美替尼和/或虾青素),ppr/(曲美替尼和/或虾青素)及pper/(曲美替尼和/或虾青素)的载药量在2%-10%之间,粒径大小在50nm-500nm之间。本发明最佳制剂(pper/(曲美替尼和/或虾青素))的纳米制剂粒径分布,透射电镜图如图3、图4所示,该纳米制剂粒径分布均匀,形态均一,电镜图显示核壳结构明显。
2.具有循环纤维细胞受体ccr7靶向抗体及多肽z修饰的聚合物纳米粒制备
e5的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的抗体6.5mg,在纯水溶液中4℃摇床中反应过夜,其中e5为循环纤维细胞受体ccr7的靶向抗体;
多肽z的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的多肽rgdf(c)2.5mg,在纯水溶液中4℃摇床中反应过夜;利用10000rpm/min离心重悬三次,收集所制备的纳米粒,除去未反应的巯基化的e5和z。
利用本法所制备的pp/(曲美替尼和/或虾青素),ppe/(曲美替尼和/或虾青素),ppr/(曲美替尼和/或虾青素)及pper/(曲美替尼和/或虾青素)的载药量在2%-10%之间,粒径大小在50nm-500nm之间。本发明最佳制剂(pper/(曲美替尼和/或虾青素))的纳米制剂粒径分布均匀,形态均一。
3.具有循环纤维细胞受体ccr2靶向趋化因子及多肽z修饰的聚合物纳米粒制备
e5的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的趋化因子6.5mg,在纯水溶液中4℃摇床中反应过夜,其中e5为循环纤维细胞受体ccr7的靶向抗体;
多肽z的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的多肽z2.5mg,在纯水溶液中4℃摇床中反应过夜;利用10000rpm/min离心重悬三次,收集所制备的纳米粒,除去未反应的巯基化的e5和z。
利用本法所制备的pp/(曲美替尼和/或虾青素),ppe/(曲美替尼和/或虾青素),ppr/(曲美替尼和/或虾青素)及pper/(曲美替尼和/或虾青素)的载药量在2%-10%之间,粒径大小在50nm-500nm之间。本发明最佳制剂(pper/(曲美替尼和/或虾青素))的纳米制剂粒径分布均匀,形态均一。
三、具有e5及crgd或rgd修饰的聚合物纳米粒制备
e5的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的e56.5mg,在纯水溶液中4℃摇床中反应过夜;
多肽crgd或rgd的修饰:将负载药物的plga-peg-mal纳米粒与巯基化的多肽crgd或rgd2.5mg,在纯水溶液中4℃摇床中反应过夜;利用10000rpm/min离心重悬三次,收集所制备的纳米粒,除去未反应的巯基化的e5和crgd或rgd。
利用本法所制备的pp/(曲美替尼和/或虾青素),ppe/(曲美替尼和/或虾青素),ppr/(曲美替尼和/或虾青素)及pper/(曲美替尼和/或虾青素)的载药量在2%-10%之间,粒径大小在50nm-500nm之间。本发明最佳制剂(pper/(曲美替尼和/或虾青素))的纳米制剂粒径分布,透射电镜图如图5、图6所示,该纳米制剂粒径分布均匀,形态均一,电镜图显示核壳结构明显。
实施例2纳米制剂在a549细胞水平的摄取分析及流式细胞仪定量分析
按照实施例1所述制备pp/香豆素6、ppe/香豆素6、ppr/香豆素6及pper/香豆素6纳米制剂。将a549细胞分别以5×105/ml接种于24孔板中,于37℃,5%c02细胞培养箱中贴壁生长24h后,吸去培养基,加入无血清稀释的tgf-β(5ng/ml)刺激24h后,分别加入无血清培养基稀释的游离香豆素6、pp/香豆素6、ppr/香豆素6、ppc/香豆素6及ppcr/香豆素6,各孔香豆素6浓度为1μg/ml,500μl,每组别设置三个副孔。继续培养4h,使用pbs清洗三次,
(1)激光共聚焦lsm-700拍摄细胞对纳米粒及游离香豆素6的摄取情况;
(2)胰酶消化,1500rpm离心沉淀细胞,用不含血清的培养基重悬细胞,利用流式细胞仪对摄取的香豆素6进行定量检测。
本实施例所测得的细胞摄取数据如图7所示,体内水平评价的a549细胞属于腺癌肺泡基底上皮细胞,可模拟体内受损伤肺泡上皮细胞at2对纳米粒的摄取情况。在tgf-β(5ng/ml)24h后,肺泡上皮细胞受到损伤,细胞膜表面高表达整合素受体αvβ6,多肽crgd、rgdf(c)、rgd与αvβ6可以特异性结合。共聚焦结果显示,ppr/香豆素6的摄取明显高于pp/香豆素6和香豆素6的摄取,证明crgd、rgdf(c)、rgd的结合有利于增加a549细胞对纳米制剂的特异性摄取;在未被tgf-β刺激的a549细胞中,细胞膜表面整合素受体αvβ6不会高表达,结果显示其对纳米粒及游离香豆素6的摄取并无明显差异。
实施例4包覆荧光染料(dir)的纳米制剂在肺纤维化小鼠的肺部特异性递送分析
按照实施例1所述制备pp/dir、ppe/dir、ppr/dir及pper/dir纳米制剂。
首先采用6-8周龄的雄性c57bl/6小鼠进行肺纤维化模型的造模试验,造模时应用气管插管法对小鼠肺部直接造模。造模时应用盐酸博来霉素作为小鼠肺纤维化诱导剂,浓度为2usp/kg,三周以后待小鼠肺纤维化成型则继续进行纳米粒示踪实验。对于判断小鼠肺纤维化模型的成模时间,大量文献报道三周开始小鼠肺纤维化处于极速发展期,体内循环纤维细胞增殖最为明显。将造模三周的小鼠随机分配为4组,每组4只,分别通过尾静脉注射游离dir、pp/dir、ppe/dir、ppr/dir及pper/dir,以所注射的dir为1μg/g小鼠体重为标准。在尾静脉注射后的1h、4h、8h、12h、24h利用小动物活体成像仪对小鼠进行活体成像。
本实施例中所制备包覆荧光染料(dir)的纳米制剂在盐酸博来霉素造模后形成肺纤维化小鼠肺脏蓄积的小动物活体成像图片及其定量分析如图8所示;纳米制剂在肺脏的蓄积程度如下:pper/dir>ppe/dir>ppr/dir>pp/dir,证明了e5及多肽z(crgd、rgdf(c)、rgd)的修饰有利于纳米制剂被靶向递送到肺并实现高蓄积。
实施例5包覆荧光染料(dii)的纳米制剂在肺纤维化小鼠中,纳米粒与体内循环纤维细胞的贴附情况、肺部蓄积时间及递送机制。
按照实施例1所述制备pp/dii、ppe/dii、ppr/dii及pper/dii纳米制剂。
首先采用6-8周龄的雄性c57bl/6小鼠进行肺纤维化模型的造模试验,造模时应用气管插管法对小鼠肺部直接造模。造模时应用盐酸博来霉素作为小鼠肺纤维化诱导剂,浓度为2usp/kg,三周以后待小鼠肺纤维化成型则继续进行纳米粒递送机制实验。对于判断小鼠肺纤维化模型的成模时间,大量文献报道三周开始小鼠肺纤维化处于极速发展期,体内循环纤维细胞增殖最为明显。将造模三周的小鼠随机分配为4组,每组3只,分别通过尾静脉注射游离dii、pp/dii、ppe/dii、ppr/dii及pper/dii,以所注射的dii为1μg/g小鼠体重为标准。在尾静脉注射后的30min、1h、2h、4h,取小鼠肺组织进行肺组织免疫染色实验。结果如图9,图10。其中dapi为细胞核蓝色标记,α-sma为循环纤维细胞膜蛋白绿色标记,dii为纳米粒自带红色标记。结果显示,纳米粒自带红光标记与绿色标记的循环纤维细胞贴附情况明显,并且红色荧光随着给药时间的增加,在肺组织蓄积随之增加。证明纳米粒可以通过循环纤维细胞介导的纳米粒递送体系被高效递送至肺组织,实现靶向递送的目的。
实施例6纳米制剂ppater在治疗过逆转肺纤维化的效果分析。
按照实施例1所述制备方法制备纳米制剂pp/a、pp/t、pp/at、ppr/at、ppe/at、ppe/a、ppe/t、及pper/at、pper/a、pper/t。a代表抗氧化剂如虾青素,t代表成纤维细胞活化抑制剂如曲美替尼。
首先采用6-8周龄的雄性c57bl/6小鼠进行肺纤维化模型的造模试验,造模时应用气管插管法对小鼠肺部直接造模。造模时应用盐酸博来霉素作为小鼠肺纤维化诱导剂,浓度为2usp/kg,三周以后待小鼠肺纤维化成型则继续进行纳米制剂在治疗过逆转肺纤维化的效果分析。将造模三周的小鼠随机分配为8组,每组5只,分别通过尾静脉注射游离pp/a、pp/t、pp/at、ppr/at、ppe/at、ppe/a、ppe/t、及pper/at、pper/a、pper/t和生理盐水,以所注射的tra为2μg/g小鼠体重为标准。在治疗4周后,对于不同纳米制剂逆转肺纤维化效果通过h&e染色进行分析结果如图11,可以发现,最终制剂ppe/at、ppe/a、ppe/t、及pper/at、pper/a、pper/t组与blm组相比较,肺纤维化程度明显减弱,其中,pper/at组、ppe/at组效果尤为的好,优于ppr/at组、pp/at组、ppe/t组及pp/a组。更重要的是,最终制剂组pper/at及单靶头ppe/at组与正常组肺切片较为一致,可以看出清晰的肺泡结构,表明通过介导循环纤维细胞的纳米制剂递送体系可以实现高效的肺部靶向及双药联合治疗可以有效的逆转肺纤维化。
plga(聚乳酸-聚羟基乙酸)、pla(聚乳酸)、pga(聚乙交酯)、pcl(聚己内酯)是常见的具有良好生物相容性的疏水嵌段,常在双亲性嵌段共聚物中作为疏水性内核,对大多数的具有一定疏水性的药物具有较好的亲和力,或通过反向溶剂法可以制备负载亲水性药物的纳米粒。在上述实施例中,利用pla-peg-mal,pga-peg-mal,pcl-peg-mal嵌段共聚物代替plga-peg-mal嵌段共聚物,同样可以负载具有一定疏水性的药物,或通过反向溶剂法可以制备负载亲水性药物的纳米粒,形成聚合物胶束的目的,对于本领域技术人员来说,是清楚的。
以上所述仅是本发明的优选实施方式,应当指出:对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!