光敏感材料/海藻酸钙核壳纳米胶囊分散体及其制备方法与流程
本发明公开了一种稳定光敏感材料的制备方法,可以防止光敏材料的降解。
背景技术:
在个人护理产品中常添加维生素、氨基酸、酶、激素等活性物质,以滋养皮肤,抵抗衰老;同时,也会添加一定量的防晒剂,使皮肤免受紫外线的伤害。但是,有些活性成分对光较为敏感,受到光照时会失活,如维生素e等。维生素e对酸、热稳定,而暴露于紫外线环境下会遭到破坏,直接添加到化妆品中,能起到的抗氧化作用非常有限。另外,维生素e是油溶性的粘稠液体,肤感较为黏腻。提高油溶性的活性物质的稳定性,使其能够添加到水性产品中,是个人护理领域的一个非常重要的研究方向。
目前,将油溶性的活性成分直接配成乳液,使其更易于添加到水性产品中已有研究,如cn201711288702.4专利公开了一种维生素e纳米乳的制备方法。其主要做法是维生素e、油相、主表面活性剂、助表面活性剂和水混合制备成30~60nm的乳液,此种方法虽然操作简便,但是维生素e含量较低,在3~9%范围内,对维生素e的保护能力较差,不能解决其易氧化的问题。cn201610033759.9专利公开了一种用脂质体包裹维生素a棕榈酸酯的制备方法,其制备方法是将维生素a棕榈酸酯、磷脂、固态乳化剂、固体脂质及液态脂质熔融并分散均匀得到油相,将无机盐、去离子水混合加热得到水相,搅拌下加入油相,经超声、冷却后加防腐剂,制备固体脂质载体。脂质体包裹维生素a棕榈酸酯可促进维生素a棕榈酸酯的吸收,维生素a棕榈酸酯含量在1~15%之间,但是脂质体的价格较为昂贵,且制备方式较为复杂,得到的产品成本较高。
海藻酸钠(sa)是一种天然的亲水性生物多糖,是由α-l-古洛糖醛酸(g)和β-d-甘露糖醛酸(m)组成。sa可与二价或二价以上的金属阳离子反应,生成在高温下不可逆的凝胶。海藻酸钠具有较好的生物降解性,其安全性已得到美国fda的认证。海藻酸钠疏水改性包括羟基反应法和羧基反应法,羧基反应法工艺简便,且不会引起海藻酸钠分子链的断裂,同时保留了海藻酸钠的生物相容性和可降解性,应用较为广泛。
技术实现要素:
本发明提供一种光敏感材料/海藻酸钙核壳纳米胶囊分散体的制备方法,通过该方法将光敏感材料制成光敏感材料/海藻酸钙核壳纳米胶囊分散体,能稳定和控释光敏感材料,具有工艺简单,同时还具有安全可靠的特点。
本发明为达到其目的,采用的技术方案如下:
本发明一方面提供一种光敏感材料/海藻酸钙核壳纳米胶囊分散体的制备方法,包括如下步骤:
1)将油相溶液加入水相溶液中乳化得到乳液,其中所述油相溶液中含有光敏感材料;或者直接将纯光敏感材料加入水相溶液中乳化得到乳液;所述水相溶液通过将海藻酸钠和/或改性海藻酸钠、乳化剂溶解在水中得到,作为壁材溶液;
2)向所述乳液中加入固化剂水溶液进行搅拌,凝胶海藻酸钠的壳,得到光敏感材料/海藻酸钙核壳纳米胶囊分散体,所述固化剂水溶液选自乳酸钙和/或氯化钙水溶液。
本发明的制备方法得到的微胶囊分散体对光敏感材料具有较好的保护作用,而现有其他方法得到的微胶囊例如囊壁材料为壳聚糖的微胶囊,对光敏感材料的保护作用有限。本发明得到的胶囊分散体中,由于海藻酸钙的糖苷基团受到紫外光照射时会发生断裂,能吸收部分的紫外光,也可对囊芯起到保护作用。本发明提供的制备方法,采用乳化-凝胶的方式,制备工艺简单,且是物理过程,不涉及化学反应,可最大程度的避免残留对人体有害的物质,更为安全可靠,同时还能达到较高的光敏感材料包裹率。
本发明所用的所述海藻酸钠并无特别限定,例如为从褐藻类的海带或马尾藻中提取的天然多糖,粘度可以在50~200cp(测试标准gb1886.243-2016)之间,优选m段含量高于g段质量含量的海藻酸钠。更优选粘度小于100cp的海藻酸钠,此类海藻酸钠对体系的粘度影响较小,在固化过程中不会产生较大的海藻酸钙凝胶。例如采用青岛明月海藻集团或山东结晶集团生产的粘度为80-100cp的海藻酸钠等。
一些实施方式中,可以采用改性海藻酸钠,优选为疏水改性海藻酸钠;可以采用现有改性方法得到的疏水改性海藻酸钠或现有疏水改性海藻酸钠产品,例如通过酯化法制备的海藻酸胆固醇酯及酰胺化法得到侧链接枝型的海藻酸钠,例如庚胺改性的海藻酸钠和/或辛胺改性海藻酸钠,优选为通过酰胺化法将辛胺接枝到海藻酸钠的主链的辛胺改性海藻酸钠,接枝率优选为20-25%。使用疏水改性的海藻酸钠可减缓光敏感活性物质的释放,调节活性物质的释放速率。
一些实施方式中,在制备所述分散体的过程中,所述海藻酸钠或所述改性海藻酸钠的用量与水相溶液质量的比值为>0,且≤5%,例如0.05%、0.1%、0.5%、3%、5%等等,优选为0.001~5%,进一步优选0.5~1%。
本发明的制备方法中,所述乳化剂可以为各种能吸附或结合于油水界面的水包油(o/w)表面活性剂,乳化剂在分散体系中主要起到乳化作用,作用在胶囊和水的界面,亲水端在水中,疏水端在胶囊中,使胶囊稳定的分散在水相中,避免胶囊之间相互接触发生团聚;在实际应用中,可以根据需求调节乳化剂的种类和添加量。本发明优选方案中,在所述分散体中,所述乳化剂的用量与水相溶液质量的比值为>0,且≤40%,例如0.5%、1%、5%、10%、20%等等,优选为1~30%,进一步优选5~20%。
本发明中,所用的所述水包油表面活性剂的具体种类并无特别限定,优选所述水包油表面活性剂的hlb值为8~20。所述水包油表面活性剂可以是含有主剂和/或助剂的亲水亲油平衡值(hlb)介于8~20的表面活性剂。本发明中,可以选用≥200的o/w表面活性剂,例如数均分子量为200~2000000,优选为200~200000,此类高分子表面活性剂可以大面积地与囊壁材料接触,紧密地缠绕在胶囊表面。
所述水包油表面活性剂可选自阴离子表面活性剂、两性离子表面活性剂或非离子表面活性剂中的一种或几种的组合。其中,阴离子表面活性剂可以是但不限于硬脂酸钠、木质素磺酸盐等中的一种或多种。两性离子表面活性剂可以是但不限于卵磷脂、甜菜碱等中的一种或多种。非离子表面活性剂可以是但不限于聚乙烯醇、聚乙烯吡咯烷酮、硬脂醇聚醚-2、聚山梨酯(吐温)系列、失水山梨醇脂肪酸酯(司盘)、烷基葡糖苷、脂肪酸酯类(如脂肪酸甘油酯、丙二醇脂肪酸酯等)、壬基酚聚氧乙烯醚、硬脂酸酯类(如硬脂酸甘油酯)、烷基聚醚、脂肪醇聚氧乙烯醚等中的一种或多种。在主表面稳定剂和辅助表面稳定剂的组合使用的实施方案中,例如主表面稳定剂选自聚山梨酯系列、聚乙烯醇、脂肪酸酯类中的一种;所述辅助表面稳定剂选自聚山梨酯系列、聚乙烯醇、硬脂酸酯类、烷基磺酸盐中的一种或多种;采用该优选方案,其主表面稳定剂可紧密的吸附或结合于囊壁材料表面,且主表面稳定剂和辅助表面稳定剂的组合可以达到很好的协同乳化作用。
在本发明一些优选具体实施方式中,所述水包油表面活性剂选自pva、吐温20、吐温80中的一种或两种以上的组合;优选使用海藻酸钠为囊壁材料。
一些优选实施方式中,本发明制得的分散体中,胶囊的囊芯材料、囊壁材料的质量比为(20~100):1,固化剂为浓度0.6~1wt%的氯化钙,乳化剂选用吐温20,浓度例如为水相质量的1~10%,所制得的胶囊分散体不仅具有较高的包裹率,而且具有较小的粒径分布,同时还有很好的分散体稳定性。
本发明的优选方案中,优选乳化剂中还含有能吸附在油滴表面形成pickering乳液的亲水性固体纳米粒子;通过使用亲水性固体纳米粒子形成pickering乳液,可减少表面活性剂的使用,添加到化妆品中可降低表面活性剂对皮肤的刺激,另外,固体粒子做稳定剂可进一步散射紫外光,减少活性物质与光照的接触面积,降低油相和紫外光、氧气等的接触面积,延长活性物质的保存期限,使活性物质更加稳定。本领域技术人员所知晓的,由固体纳米粒子吸附在油水界面上形成的乳液称为pickering乳液。所述亲水性固体纳米粒子的具体种类并无特别限定,优选其粒径为20~200nm能够形成水包油乳液的粒子,进一步优选粒径为20~40nm。所述亲水性固体纳米粒子例如为无机纳米粒子或有机纳米粒子中的一种或两种以上的组合,所述无机纳米粒子包括但不限于二氧化钛、二氧化硅、氧化锌等中的一种或两种以上的组合,所述有机纳米粒子例如但不限于纳米纤维素颗粒、玉米淀粉晶体、甲壳素晶体、乳清蛋白等中的一种或两种以上的组合。优选为氧化锌粒子,特别是粒径在20~40nm的氧化锌粒子,该粒子粒径较小,分布均匀,可更好的吸附在界面上,同时,可吸收紫外光,进一步保护活性物质,例如为厦门市纳诺泰克有限公司的dnano133w,平均粒径为20nm的水分散型的氧化锌粒子。
优选本发明所述光敏感材料为疏水性活性物质;所涉及的光敏感材料的具体种类并无特别限制,可为市场上常见的各种光敏感材料,所述光敏感材料例如但不限于维生素、光敏感探针、防晒剂中的一种或两种以上的组合。其中,所述维生素例如为维生素a、维生素e、维生素d和/或维生素k等;所述光敏感探针例如为标记氨基酸的极性敏感探针和/或电压敏感探针等;所述防晒剂例如选自二苯酮-3、二苯酮-4、4-丁基-4-甲氧基-二苯甲酰甲烷、4-甲基-4-乙氧基苯甲酰甲烷、双乙基己氧基苯酚、对甲氧基苯基三嗪、乙基己基三嗪酮、二乙氨羟苯甲酰基苯甲酸己酯、甲酚三唑三硅氧烷、苯基苯、甲基肉桂酸辛酯、甲氧基肉桂酸辛酯、水杨酸辛酯、n,n-二甲基对氨基苯甲酸辛酯、2-氰基-3,3二苯基丙烯酸辛酯、氰双苯丙烯酸辛酯、二乙氨羟苯甲酰基苯甲酸己酯、n,n-二甲基对氨基甲酸戊酯、邻氨基苯甲酸薄荷酯、水杨酸薄荷酯、水杨酸苯酯、水杨酸苄酯、对氨基苯甲酸、对氨基苯甲酸甘油酯、乙基-4-双(羟丙基)氨基苯甲酸酯等中的一种或两种以上的组合。
本发明优选的一些实施方式中,在进行乳化之前,可以使用油性溶剂溶解光敏感材料,制成油相溶液,从而可以稀释光敏感的活性物质,降低光敏感活性物质的粘度或溶解固体的光敏感活性物质,使其在分散过程中更加均匀。其中,所述油相溶液中所用的油性溶剂优选选自矿物油、中链甘油三酯(mct)、橄榄油、鳄梨油、聚二甲基硅氧烷、环五聚二甲基硅氧烷等中的一种或两种以上的组合,采用优选油性溶剂具有粘度低,对油性活性物质的溶解性好,且不与活性物质发生反应的特点。在一些实施方式中,优选所述油性溶剂为中链甘油三酯,光敏感材料和中链甘油三酯的质量比优选为1:1~1:3。在另一些实施方式中,所述油性溶剂优选为聚二甲基硅氧烷和环五聚二甲基硅氧烷的混合溶剂,光敏感材料:聚二甲基硅氧烷:环五聚二甲基硅氧烷的质量比值优选为1:1:4~1:1:5之间。采用这些优选方案得到的包裹材料用于个人护理领域可得到较好的肤感。
一些实施方式中,在所述胶囊分散体中,所述光敏感材料和油性溶剂(如有的话)的用量之和与水相溶液质量的比值为>0,且≤100%,例如0.5%、1%、3%、10%、30%、40%、50%、60%、70%、80%等,优选为水相溶液质量的30~90%,进一步优选60~80%。
本发明中,所述氯化钙或乳酸钙水溶液是用来固化交联胶囊的壳,ca2+与海藻酸钠上的g段发生交联,形成“蛋壳结构”,一些优选实施方式中,步骤2)中所述固化剂水溶液中固化剂的质量浓度为0.6%~1%,例如0.6%、0.8%、1%等,固化剂水溶液的用量与所述乳液质量的比值为1:5~1:20,例如1:5、1:8、1:10、1:15、1:18、1:20等。
利用本发明的方法获得的胶囊包裹效果好,囊芯材料的包裹率高,利用本发明的方法制得的胶囊,其囊芯材料和囊壁材料的质量比可达到质量比100:1的水平;优选的,可以将囊芯材料和囊壁材料的质量比控制在100:1~20:1,例如,可以将囊芯材料和囊壁材料的质量比控制在100:1、50:1、20:1、10:1等。
步骤1)中,所述乳化的具体乳化方式并无特别限定,可以采用现有的常用乳化方式,优选为如下乳化方式中的一种或两种以上的联用:搅拌、分散、超声或均质;更优选采用分散或者分散和均质联合使用,更进一步优选为分散和均质联合使用,可获得粒子平均粒径更小且尺寸更均匀的分散体,且分散性更为稳定。在一些实施方式中,将分散和均质联合使用,同时使用主剂和助剂组合的水包油表面活性剂组合物,可获得更佳的分散稳定性,以及更细化和均匀的胶囊尺寸。
本领域技术人员所知晓的,乳化方式中所述的分散,其分散过程指用分散机在溶液局部形成很强的紊流,强劲的离心力将溶液从径向甩入定、转子之间狭窄精密的间隙中,同时受到离心挤压、液层摩擦、液力撞击等综合作用力,在强烈的液力剪切、液层磨擦、撕裂碰撞等作用下被充分分散破碎,同时通过定子槽高速射出。溶液不断地从径向高速射出,在物料本身和容器壁的阻力下改变流向,与此同时在转子区产生的上、下轴向抽吸力的作用下,又形成上、下两股强烈的翻动紊流。溶液经过数次循环,最终完成分散过程。
本领域技术人员所知晓的,均质过程指用高压均质仪使粒子粒径变小,尺寸均匀。高压均质机主要由高压均质腔和增压机构成,在增压机构的作用下,高压溶液快速的通过均质腔,物料会同时受到高速剪切、高频震荡、空穴现象和对流撞击等机械力作用和相应的热效应,由此引发的机械力及化学效应可诱导物料大分子的物理、化学结构发生变化,最终达到均质的效果。
本发明的制备方法得到的分散体中,可以得到较窄的胶囊粒径分布,平均粒径能控制在100nm~1.5μm之间。
本发明第二方面提供一种光敏感材料/海藻酸钙核壳纳米胶囊或胶囊分散体,采用上文所述的制备方法制备。
本发明第三方面提供一种稳定和控释光敏感材料的方法,将所述光敏感材料制备成光敏感材料/海藻酸钙核壳纳米胶囊分散体,其中,所述光敏感材料/海藻酸钙核壳纳米胶囊分散体采用上文所述的制备方法制得。该方法提供了一种稳定光敏感活性物质的方式,将光敏感活性物质包裹在海藻酸钙纳米胶囊中,在制备胶囊分散体过程中,加入ca2+后,相邻的海藻酸钠分子链从自然伸展的卷曲状态向整齐排列的带状结构转变,形成三维网状凝胶结构。三维网状的凝胶结构对囊芯可以起到显著的保护作用。此外,海藻酸钙的糖苷基团受到紫外光照射时会发生断裂,吸收了部分的紫外光,也可对囊芯起到保护作用。同时,通过该方法能实现活性物质可控释放,将活性物质包裹在海藻酸钙纳米胶囊中,在使用过程中,随水分的蒸发,海藻酸钙纳米胶囊收缩,将活性物质缓慢释放出来。在制备所述胶囊分散体时,优选使用改性海藻酸钠为囊壁材料,和/或在乳化剂中引入亲水性固体纳米粒子做乳化剂,可进一步延缓活性物质的释放速率。另外,海藻酸钙是一种凝胶结构,受到压力时,也会释放其中的活性物质。活性物质缓慢释放在个人护理中具有非常重要的应用,如可将维生素e包裹在海藻酸钙纳米胶囊中,将其用于化妆品配方,可以使其缓慢的释放到皮肤表面,渗透到皮肤中,充分发挥其抗氧化和抗衰老的作用。
本发明还提供一种应用,上文所述的光敏感材料/海藻酸钙核壳纳米胶囊或胶囊分散体或上文所述的方法在护理产品领域中应用,例如化妆品中应用。
本发明提供的技术方案具有如下有益效果:
1、本发明提供的核壳纳米胶囊分散体的制备方法,所形成的光敏感材料/海藻酸钙核壳纳米胶囊对囊芯材料例如防晒剂、维生素等光敏感活性物的包裹效果较好,在一些实施方式中包裹率甚至可达到90%以上。
2、本发明提供的核壳纳米胶囊分散体的制备方法,在优选方案中,可以获得胶囊分散更好、保持稳定的胶囊分散体,胶囊不会发生明显团聚,且具有较窄的粒径分布,胶囊粒子粗细较为均匀。粒径调节灵活,根据需要对乳化剂的种类和用量进行调节,可以获得胶囊平均粒径稳定在100nm~1.5μm中的某一粒径范围。
3、本发明提供的核壳纳米胶囊分散体的制备方法,跟其它类似乳化或乳化-凝胶技术对比,可以明显防止光敏感材料的降解。相较于现有的稳定光敏感材料的方法,如通过壳聚糖包裹及油包水乳液等,通过海藻酸钠包裹光敏感材料在光照下更稳定。
4、本发明提供的核壳纳米胶囊分散体的制备方法,可通过干燥的方法释放光敏感的活性物质,另外还可以通过海藻酸钠疏水改性,使用纳米粒子做表面活性剂的方法控制活性物质的释放。这使得纳米胶囊分散体的应用范围更加广泛,如可应用于个人护理领域,将光敏感的活性物质包裹在海藻酸钙的胶囊中,可使其在产品中更加稳定,同时涂抹在皮肤上时,随水的挥发,活性物质可缓慢释放在皮肤表面,发挥作用。
附图说明
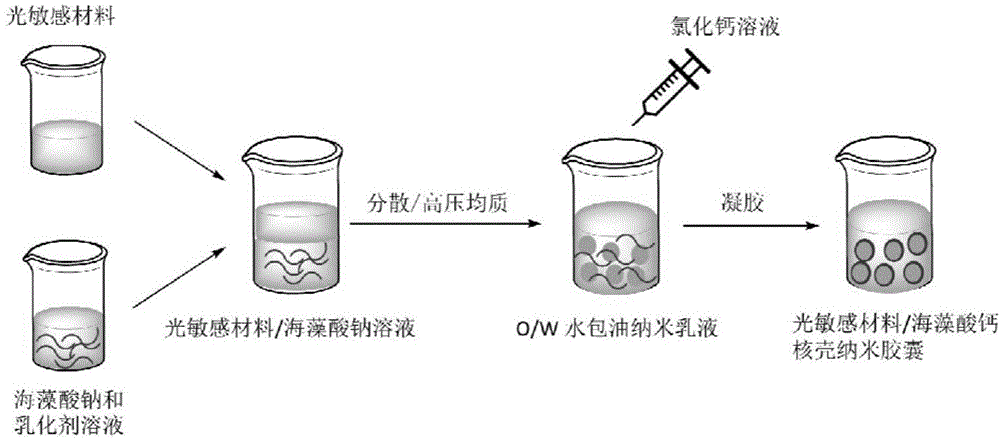
图1示出了一种实施方式的用于稳定光敏感材料的海藻酸钙核壳胶囊的工艺流程图;
图2示出了实施例1中包裹光敏感物质,粒径为1126μm的海藻酸钙微胶囊的显微镜图;
图3示出了实施例2中包裹维生素e的海藻酸钙纳米胶囊的tem图。插入的图片是一个放大的纳米胶囊的tem图,其中内核是维生素e(溶解在矿物油中),外壳是海藻酸钙;
图4示出了实施例2中的dls图来表征海藻酸钙纳米胶囊在放置60天时间内的粒径变化;
图5示出了改变乳化剂吐温20的用量(5-20wt%,tween20/水),海藻酸钙纳米胶囊的粒径变化;
图6示出了实施例2中的包裹维生素e海藻酸钙纳米胶囊在紫外光照射2小时后维生素e含量的变化;
图7示出了实施例7和对比例中包裹omc的海藻酸钙纳米胶囊在紫外光照射两小时后omc的保留率;
图8示出了干燥后,光敏感的活性物质维生素e从海藻酸钙纳米胶囊中释放出来。
具体实施方式
为了更好的理解本发明的技术方案,下面结合实施例进一步阐述本发明的内容,但本发明的内容并不仅仅局限于以下实施例。
以下百分比或浓度若未特别说明,均指质量百分比。
以下实施例或对比例中涉及的部分原料来源说明如下:
海藻酸钠(sa):青岛明月海藻集团,粘度80-100cp;
壳聚糖(cs):阿拉丁,粘度200-400cp;
三聚磷酸钠(tpp):阿拉丁,分析纯;
醋酸:阿拉丁,30%水溶液;
氯化钙:阿拉丁,化学纯;
甲氧基肉桂酸辛酯(omc):unipromasunsafe;
聚乙烯醇(pva):sigmaaldrich,重均分子量89000-98000;
聚山梨酯20(吐温20):沪试(化学纯);
维生素e(ve):阿拉丁,纯度>96%;
矿物油:阿拉丁,25cst(40℃);
辛胺改性sa:青岛明月海藻集团,接枝率20%;
甘油三酯(mct):上海高鸣化工;
环五聚二甲基硅氧烷:斯洛柯;
乳酸钙:阿拉丁,usp级。
以下实施例或对比例中涉及的测试方法说明如下:
(1)动态光散射(dls)测量所用仪器为马尔文仪器zetasizernanozs90;测量步骤或测试条件为:
将胶囊分散体取出少量,用水稀释至接近透明;滴加到dls样品池,25℃下dls测试出纳米胶囊的粒径和粒径分布系数(pdi)。
(2)光学显微镜测量所用仪器为上海上光sg1000;测量步骤或测试条件为:
取出少量胶囊分散体,用等体积水稀释;通过计算机成像系统观察显微镜下的胶囊分散体形貌。
(3)透射电子显微镜(tem)测量所用仪器为jem-1200ex;测量步骤或测试条件为:
将胶囊滴在铜网,使其在通风橱下干燥30分钟,在100kv电压下tem成像。
(4)紫外分光光度计测量所用仪器为上海谱元alpha1500;胶囊分散体对囊芯材料的包裹率测量步骤或测试条件为:
取定量分散体,稀释n倍,经过离心、过滤后去清液,用紫外分光光度计测量清液里的囊芯材料含量,计算出分散体中的游离囊芯材料质量和囊芯材料被囊壁材料包裹的包裹率:
例如,对于含x(g)囊芯材料的y(ml)纳米胶囊分散体。取1ml分散体,加水至100ml混合液;离心后,取上清液进行紫外分光光度计测量,测量到囊芯材料的浓度为z(g/ml);经计算,游离在纳米胶囊外的囊芯材料质量为100×z×y(g),囊芯材料被囊壁材料包裹的包裹率为:
光敏感材料在海藻酸钙纳米胶囊里的稳定性测量步骤或测试条件为:取适量胶囊分散体分散于水溶液中,纯光敏感材料溶解于乙醇溶液中,太阳光下照射2小时,用紫外分光光度计测试照射前后光敏感材料的吸收峰值,进行强度对比,得到光敏感材料的损失率。
实施例1:
将0.4gsa(海藻酸钠)、0.4gpva(乳化剂)溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20ml矿物油中,形成ve溶液(维生素e溶液);
将维生素e溶液倒入sa水溶液中,用分散机分散(ikaultraturraxt-18,10,000r/min,5min),得到ve乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入ve乳液中,搅拌15min,得到维生素e/海藻酸钙胶囊分散体。
动态光散射测量表明,维生素e/海藻酸钙微胶囊的粒径为1126nm,pdi为0.258。紫外分光光度计测量表明,维生素e的包裹率为95%。所得维生素e/海藻酸钙胶囊的光学显微镜图像如图2所示,核壳胶囊大小均匀。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e并未降解。
实施例2:
将0.4gsa(海藻酸钠)、2g吐温20(乳化剂)溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20ml矿物油中,形成ve溶液;
将维生素e溶液倒入sa水溶液中,用分散机(ikaultraturraxt-18)分散5min中,剪切速率为10,000r/min,之后用高压均质机(avestinemulsiflexc-5)均质10min得到ve乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入ve乳液中,搅拌15min,得到维生素e/海藻酸钙胶囊分散体。
动态光散射测试结果如图5所示,测试结果表明,维生素e/海藻酸钙纳米胶囊的粒径为348nm,pdi为0.159。紫外分光光度计测量表明,维生素e的包裹率为94%。所得维生素e/海藻酸钙胶囊的透射电子显微镜图像如图3所示,核壳结构明显,胶囊大小均匀。图4证明,60天后,所得的维生素e/海藻酸钙胶囊分散体依然稳定,粒径和pdi不变。图6证明,在紫外光照射下,2h后,包裹在海藻酸钙纳米胶囊中的维生素e并未降解,而直接暴露在紫外光下的维生素e降解了20%左右,证明海藻酸钙纳米胶囊的壳可以保护光敏感的维生素e。图8证明,干燥后,光敏感的活性物质维生素e从海藻酸钙纳米胶囊中释放出来,当涂抹于皮肤时,随水分的挥发,维生素e可以缓慢的被皮肤吸收。
实施例3:
将0.4gsa(海藻酸钠)、4g吐温20(乳化剂)溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20ml矿物油中,形成ve溶液;
将维生素e溶液倒入sa水溶液中,用分散机(ikaultraturraxt-18)分散5min中,剪切速率为10,000r/min,之后用高压均质机(avestinemulsiflexc-5)均质10min得到ve乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入ve乳液中,搅拌15min,得到维生素e/海藻酸钙胶囊分散体。
动态光散射测试如图5所示,测试结果表明,维生素e/海藻酸钙纳米胶囊的粒径为210nm,pdi为0.118。紫外分光光度计测量表明,维生素e的包裹率为96%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e并未降解。
实施例4:
将0.4gsa、8g吐温20溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20ml矿物油中,形成ve溶液;
将维生素e溶液倒入sa水溶液中,用分散机(ikaultraturraxt-18)分散5min中,剪切速率为10,000r/min,之后用高压均质机(avestinemulsiflexc-5)均质10min得到ve乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入ve乳液中,搅拌15min,得到海藻酸钙胶囊。
动态光散射测试结果如图5所示,结果表明,维生素e/海藻酸钙纳米胶囊的粒径为136nm,pdi为0.092。紫外分光光度计测量表明,维生素e的包裹率为98%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e并未降解。
实施例2、实施例3、实施例4的测试结果表明,随乳化剂用量的增大,海藻酸钙微胶囊的粒径减小。
实施例5:
将0.4gsa、1.6g吐温20及0.4gpva溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20ml矿物油中,形成ve溶液;
将维生素e溶液倒入sa水溶液中,用分散机(ikaultraturraxt-18)分散5min中,剪切速率为10,000r/min,之后用高压均质机(avestinemulsiflexc-5)均质10min得到ve乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入ve乳液中,搅拌15min,得到维生素e/海藻酸钙胶囊分散体。
动态光散射测量表明,维生素e/海藻酸钙纳米胶囊的粒径为405nm,pdi为0.174。紫外分光光度计测量表明,维生素e的包裹率为96%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e降解约4%。
实施例6:
将0.04gsa或0.2gsa、1.6g吐温20及0.4gpva溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20ml矿物油中,形成ve溶液;
将维生素e溶液倒入sa水溶液中,用分散机(ikaultraturraxt-18)分散5min中,剪切速率为10,000r/min,之后用高压均质机(avestinemulsiflexc-5)均质10min得到ve乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入ve乳液中,搅拌15min,得到维生素e/海藻酸钙胶囊。
动态光散射测量表明,当海藻酸钠质量为0.04g时,维生素e/海藻酸钙纳米胶囊的粒径为311nm,pdi为0.114;紫外分光光度计测量表明,维生素e的包裹率为95%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e并未降解。当海藻酸钠质量为0.2g时,维生素e/海藻酸钙纳米胶囊的粒径为386nm,pdi为0.175,紫外分光光度计测量表明,维生素e的包裹率为97%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e并未降解。
实施例7:
将0.4gsa、2gtween20溶解于40ml水中,形成sa水溶液;
将30gomc倒入sa水溶液中,用分散机分散(ikaultraturraxt-18,10,000r/min,5min),得到omc乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入omc乳液中,搅拌15min,得到omc/海藻酸钙胶囊分散体。
动态光散射测量表明,omc/海藻酸钙纳米胶囊的粒径382nm,pdi为0.178。图7证明,经过两小时光照后,包裹在海藻酸钙中的omc降解率小于10%,而omc溶液降解了20%。
实施例8:
将0.2gsa、2gtween20溶解于20ml水中,形成sa水溶液;
将20gomc倒入sa水溶液中,之后用分散机分散(ikaultraturraxt-18,11,000r/min,5min),得到omc乳液;
将0.06g氯化钙溶解于8ml水中,逐滴加入omc乳液中,搅拌15min,得到海藻酸钙胶囊。
动态光散射测量表明,omc/海藻酸钙纳米胶囊的粒径257nm,pdi为0.086。紫外分光光度计测量表明,omc的包裹率为92%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的omc降解约5%。
实施例9:
将0.4g辛胺改性sa(接枝率20%)、1.6g吐温20及0.4gpva溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20ml环五聚二甲基硅氧烷中,形成ve溶液;
将维生素e溶液倒入sa水溶液中,用分散机(ikaultraturraxt-18)分散5min中,剪切速率为10,000r/min,之后用高压均质机(avestinemulsiflexc-5)均质10min得到ve乳液;
将0.12g乳酸钙溶解于6ml水中,逐滴加入ve乳液中,搅拌15min,得到维生素e/海藻酸钙胶囊分散体。
动态光散射测量表明,维生素e/海藻酸钙纳米胶囊的粒径为400nm,pdi为0.135。紫外分光光度计测量表明,维生素e的包裹率为98%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e并未降解。
实施例10:
将0.4gsa、0.6gpva溶解于40ml水中,形成sa水溶液;
将7.5gve溶解于20mlmct油中,形成ve溶液;
将维生素e溶液倒入sa水溶液中,用分散机分散(ikaultraturraxt-18,10,000r/min,5min),得到ve乳液;
将0.12g乳酸钙溶解于6ml水中,逐滴加入ve乳液中,搅拌15min,得到维生素e/海藻酸钙胶囊分散体。
动态光散射测量表明,维生素e/海藻酸钙微胶囊的粒径为873nm,pdi为0.213。紫外分光光度计测量表明,维生素e的包裹率为97%。紫外光照射下,包裹在海藻酸钙纳米胶囊中的维生素e并未降解。
对比例1:
将0.2gcs、1gtween20溶解于20ml1%醋酸溶液中,形成cs水溶液;将20gomc倒入cs水溶液中,用分散机分散(ikaultraturraxt-18,11,000r/min,5min),得到omc乳液;将2ml质量分数为1%的tpp溶液逐滴加入omc乳液中,搅拌15min,得到omc/壳聚糖纳米胶囊。
动态光散射测量表明,omc/壳聚糖纳米胶囊的粒径580nm,pdi为0.077。图7证明,经过两小时光照后,包裹在cs中的omc(即对应于图7中omc包裹在壳聚糖纳米胶囊里的实验结果)降解率约为20%,相较于海藻酸钙纳米胶囊包裹omc而言,使用壳聚糖包裹omc,omc的降解率较高。
对比例2:
将1gtween20溶解于20ml水中,形成tween20水溶液;将20gomc倒入tween20水溶液中,之后用分散机分散(ikaultraturraxt-18,11,000r/min,5min),得到omc纳米乳液。动态光散射测量表明,omc纳米乳液的粒径386nm,pdi为0.186。图7证明,经过两小时光照后,omc纳米乳液(即对应于图7中omc/吐温20的乳液的实验结果)的降解率约为25%,相对于海藻酸钙包裹omc而言,乳液对omc的保护能力很弱。
本领域技术人员可以理解,在本说明书的教导之下,可对本发明做出一些修改或调整。这些修改或调整也应当在本发明权利要求所限定的范围之内。
- 还没有人留言评论。精彩留言会获得点赞!