一种具有靶向功能的自组装纳米粒的制备方法及其应用与流程
本发明属于生物医药技术领域,具体涉及一种具有靶向功能的自组装纳米粒的制备方法及其应用。
背景技术:
熊果酸(ursolicacid,ua)又名乌苏酸,广泛存在于山楂、乌梅、夏枯草等植物中,是一种三萜类化合物,具有抗炎、抗溃疡、抗氧化、抗菌、抗糖尿病、降低血糖等广泛的生物学效应。此外,ua还具有明显的抗肿瘤功能,因而其此作用被国内外药学工作者所重视。下式为熊果酸化学结构式。
表没食子儿茶素没食子酸酯(epigallocatechingallate,egcg)是茶多酚中最有效的活性成分,主要分布在绿茶中,属于儿茶素,但其性质在酸性环境中易分解。近年来研究发现,egcg具有抗菌、抗病毒、抗血管增生、抗氧化、抗动脉硬化、抗血栓形成、抗炎以及抗肿瘤作用。比如egcg与维甲酸a合用对子宫颈癌细胞具有协同效应,并大大增强了其抗癌效果;同时egcg对人的肺癌细胞a549也具有抑制活性,egcg是凋亡基因p53的强烈诱导剂,引起肺癌细胞凋亡,且乙酰半胱氨酸与egcg合用时,能够增强egcg的抗肺癌活性。总之,egcg对前列腺癌、肝癌、肺癌、乳腺癌、咽喉癌及膀胱癌等肿瘤亦具有较强的显著效果。下式为表没食子儿茶素没食子酸酯化学结构式。
核酸适配体(aptamer)是一种单链dna,具有识别分子靶标的特殊结构。它可作用于蛋白质、金属离子、小分子化合物、细胞膜表面受体等靶标。该寡核苷酸序列可以是rna也可以是dna,较其他识别分子而言,适配体具有性质稳定、易合成、易标记、分子量较小和目标分子广泛等优势。其结合能力可与抗体相当甚至更强,并可结合各种药物及载体构建成多元复合靶向给药系统用于肿瘤靶向治疗。
本发明构建ua和egcg的自组装纳米载药体系,兼具ph响应和epcam受体靶向性,因此本发明涉及的纳米给药系统创新性地利用自组装技术将ua、egcg和aptamer共制,制备过程简单易行,为肿瘤治疗提供了一个新的研究方向。
技术实现要素:
本发明是一种基于egcg和ua自组装并具备aptamer靶向肿瘤细胞epcam的纳米给药系统ua@egcg-apt,使用溶剂交换法制备自组装纳米,靶向输送抗肿瘤药物至肿瘤部位,ph响应释放,发挥抗肿瘤作用。
本发明涉及的一种具有靶向功能的自组装纳米粒(ua@egcg-aptnps),组成成分包括熊果酸、表没食子儿茶素没食子酸酯和核酸适配体。
具有靶向功能的自组装纳米粒的制备方法,包括以下步骤:在室温下将熊果酸溶于100µl的良溶剂溶液中,在超声条件下,缓慢逐滴滴加入1ml的不良溶剂中,挥发不良溶剂,然后加入100µl表没食子儿茶素没食子酸酯水溶液,超声45分钟后,得到ua@egcg自组装纳米复合物,之后再加入1µl10mm的核酸适配体水溶液,在摇床震荡4-6小时,室温静置后即可得到具有靶向功能的自组装纳米粒ua@egcg-aptnps。
所述熊果酸与表没食子儿茶素没食子酸酯的物质的量比为1:1-20:1。
所述良溶剂为甲醇。
所述不良溶剂为水。
所述核酸适配体是一种具有靶向功能的dna分子。
所述具有靶向功能的dna分子序列为:
5’-cactacagaggttgcgtctgtcccacgttgtcatggggggttggcctg-cy5-3’
进一步地,将上述具有靶向功能的自组装纳米粒应用于制备抗肿瘤药物中。
本发明的优点在于:
(1)本发明所制备的ua@egcg-aptnps通过溶剂交换法制得,制备过程操作简便易行。
(2)本发明所构建的小分子自组装纳米载药系统可以使egcg包裹ua纳米粒,这种抗肿瘤药物具有ph响应,并在酸性条件下药物释放量更多。
(3)本发明所构建的小分子自组装纳米载药系统可以包载ua这种抗肿瘤药物并能够靶向epcam基因高度表达肿瘤细胞,可特异性地输送更多治疗药物至肿瘤部位发挥药效,有明显的治疗优势。
(4)本发明所制备的ua@egcg-apt小分子自组装纳米给药系统,靶向治疗非小细胞肺癌,不仅可以为肿瘤治疗提供了一个新方法,也为靶向载药系统研究指明了一种新思路。
附图说明
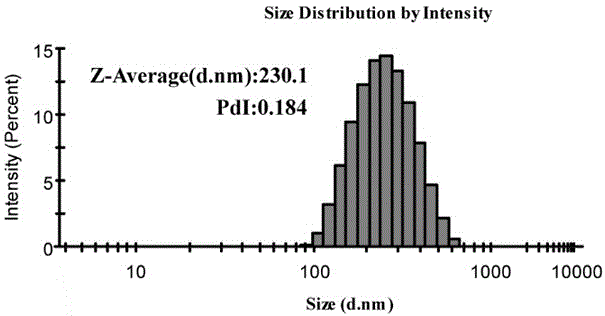
图1为基于egcg和ua自组装纳米给药系统ua@egcg纳米复合物物质的量比为5:1时纳米的粒径大小。
图2为基于egcg和ua自组装纳米给药系统ua@egcg纳米复合物物质的量比5:1时纳米的电势大小。
图3为基于egcg和ua自组装并具备aptamer靶向肿瘤细胞epcam的纳米给药系统ua@egcg-apt纳米复合物的dna琼脂糖电泳图。
图4为基于egcg和ua自组装并具备aptamer靶向肿瘤细胞epcam的纳米给药系统ua@egcg-apt纳米复合物和单独的ua在不同ph条件下的释放曲线。
图5为基于egcg和ua自组装并具备aptamer靶向肿瘤细胞epcam的纳米给药系统ua@egcg-apt纳米复合物cck-8法检测hela细胞毒性结果。
图6为基于egcg和ua自组装并具备aptamer靶向肿瘤细胞epcam的纳米给药系统ua@egcg-apt纳米复合物cck-8法检测hepg2细胞毒性结果。
具体实施方式
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
实施例1具有靶向功能的自组装纳米粒ua@egcg-aptnps的制备
在室温下分别取100µl的20、10、5、1mm的熊果酸甲醇溶液,在超声条件下,分别缓慢逐滴滴加入1ml的水中,将甲醇完全挥发,然后加入100µl1mm的egcg水溶液,超声45分钟后,得到ua@egcg自组装纳米复合物,再加入10µl10μm的核酸适配体水溶液,在摇床震荡4-6小时,室温静置后即可得到具有靶向功能的自组装纳米粒ua@egcg-aptnps。
实施例2ua@egcg自组装纳米复合物的粒径和电位分析检测
使用马尔文粒径仪测量通过物质的量比制备的纳米复合物的粒径分布及zeta电位。
表1不同物质的量比的ua@egcg自组装纳米复合物粒径分布
用“溶剂交换法”制备ua@egcg自组装纳米复合物,物质的量比是影响ua@egcg纳米复合物粒径的重要因素,pdi值则能反应纳米粒径的分布,ua@egcg纳米复合物的最佳物质的量比为10:1(表1)。当物质的量比为1:1时,ua@egcg纳米复合物的平均粒径为358.1nm,pdi为0.376,电势为-27.3mv;当物质的量比为5:1时,ua@egcg纳米复合物的平均粒径为230.1nm,pdi为0.184,电势为-15.8mv(图1、2);当物质的量比为20:1时,ua@egcg纳米复合物的平均粒径为358.1nm,pdi为0.678,电势为-24.8mv。
实施例3琼脂糖电泳实验
为了验证靶向肿瘤细胞epcam的aptamer是否可以吸附上纳米给药系统ua@egcg自组装纳米复合物,为此进行了琼脂糖电泳实验。
(1)0.5g琼脂糖加入50ml0.5×tbe电泳缓冲液中,摇匀。在微波炉中加热1min至琼脂糖溶解,取出后,手动摇匀后,继续在微波炉中加热30s至琼脂糖完全溶解,制成1%的琼脂糖凝胶。
(2)待溶解的琼脂糖冷却到60℃左右,倒到已经插好梳子的琼脂糖凝胶模具中,室温冷却凝固,小心垂直向上拔出梳子。
(3)将凝胶置入电泳槽中,在电泳槽中加入0.5×tbe电泳缓冲溶液至液面覆盖凝胶1-2mm。
(4)样品处理:8μldna样品+2μlsybrgreen+2μlloadingbuffer。
(5)使用移液枪吸取样品到点样孔中,打开电源开关,调节电压至80v,可见带有溴酚蓝的dna条带向正极端缓慢移动。
(6)持续电泳时间30min左右后,待dna片段移动至琼脂糖凝胶下半部分时,关闭电源,终止电泳。取出琼脂糖凝胶,放置到凝胶成像系统成像,得到结果(图3)。从中可以发现具备靶向肿瘤细胞epcam的适配体aptamer已经吸附到ua@egcg自组装纳米复合物,为ua@egcg-aptnps具备靶向性提供了有效依据。
实施例4熊果酸在不同ph值下的释放实验
将1mlua和ua@egcg纳米复合物溶液移至透析袋(mwco=1000)内,然后转移到49mlpbs(ph7.4/ph5.5)的透析介质中,在37℃温度条件下恒温磁力搅拌,进行熊果酸及其纳米复合物在不同ph值下的释放实验。预先设定的时间点为0.5、1、2、4、6、8、12、24、48h,于设定的时间点取样,每次取2ml的透析液,然后再补加2ml新鲜透析介质,取出后利用紫外分光光度计测定每个时间点样品的吸光度,根据ua的标准曲线,计算出每个时间点的的累积释放量,绘制出熊果酸在不同ph值下随时间变化的释放曲线(图4)。
实施例5cck-8法检测细胞毒性
cck-8法检测载ua的纳米给药系统对肝癌细胞株hepg2细胞和宫颈癌细胞株hela细胞的增殖抑制作用。
(1)取对数生长期的肿瘤细胞一瓶,消化后制成6×104cell/ml的细胞悬液。
(2)以每孔6×103cell,在96孔板中的配置100μl细胞悬液,将培养板置于37℃,5%co2培养箱中培养24h。
(3)移去培养基,ua单药组、ua@egcgnps和ua@egcg-apt自组装纳米复合物组按照浓度梯度(1、10、20、30、50µm)与细胞培养基混合加入,每孔100μl。作用24h后,于每孔中加入10μlcck-8溶液,继续孵育1-4h。
(4)到达孵育时间后,使用酶标仪检测各孔光吸收值(od值),吸收波长为570nm,并计算细胞的存活率:细胞存活率(%)=(加药组平均od值a1-空白对照组平均od值a2)/(正常组平均od值a3-空白对照组平均od值a2)×100%,其中加药组具有细胞、细胞培养基、cck-8溶液和不同药物溶液;空白组具有培养基和cck-8溶液而没有细胞;正常组具有细胞、细胞培养基、cck-8溶液但没有药物溶液。最后用graphpadprism软件进行数据处理。从图5、6中可知,ua@egcg-apt对两株细胞均表现出极高的细胞毒性,均超过单独所用ua的细胞毒性,并且对hepg2细胞的细胞毒性比对hela细胞的细胞毒性更强,靶向性作用更强。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
sequencelisting
<110>福州大学
<120>一种具有靶向功能的自组装纳米粒的制备方法及其应用
<130>1
<160>1
<170>patentinversion3.3
<210>1
<211>48
<212>dna
<213>人工序列
<400>1
cactacagaggttgcgtctgtcccacgttgtcatggggggttggcctg48
- 还没有人留言评论。精彩留言会获得点赞!