细胞间隙连接通讯调节剂及其在糖尿病性眼病治疗中的应用的制作方法
本发明涉及细胞间隙连接通讯(gjic)调节剂及其在治疗或预防糖尿病性眼病中的应用,更具体地涉及其在治疗或预防糖尿病性视网膜病和糖尿病性黄斑水肿中的应用。本发明进一步涉及适于将细胞间隙连接通讯调节剂递送至眼的药物组合物。
背景技术:
本领域越来越认识到,胞间通讯对于细胞内稳态、增殖和分化至关重要。据认为,这种通讯由间隙连接促进。据认为,这些结构是关联细胞并允许“串扰”的途径。间隙连接之间的串扰称为“细胞间隙连接通讯(gapjunctionalintercellularcommunication)”(gjic)。通常,间隙连接是细胞膜中包含数百至数千个直接连接两个相邻细胞的细胞质的紧密堆积通道簇的专门区域。间隙连接通道由两个相邻细胞各自提供的两个半通道或连接子(connexon)组成。每个连接子又由称为连接蛋白的六种蛋白质组成。
糖尿病性视网膜病是工作年龄成人的视力丧失和失明的主要原因。视网膜血管细胞损失是早期糖尿病性视网膜病的特征标志。众所周知,视网膜血管细胞损失加速至少部分是由于高葡萄糖诱发的细胞凋亡。
这些病症的一个特殊问题在于,糖尿病性视网膜病的早期阶段通常症状有限或没有症状。因此,这种疾病通常会逐渐恶化直至影响视力。异常的视网膜血管出血可导致出现“漂浮”斑点。这些斑点有时会自身清除。这意味着,如果不及时治疗,出血经常会复发,从而增加永久性视力丧失的风险。如果出现糖尿病性黄斑水肿(dme),可能会导致视力模糊。另一个问题是,由于糖尿病性视网膜病而失去的视力可能是不可逆的。
晚期糖尿病性视网膜病或dme可以通过几种疗法(单独使用或联合使用)治疗。通常,这些疗法靶向在晚期糖尿病性视网膜病中产生的生长因子。这些疗法包括抗vegf注射疗法,其中将抗vegf药物注射到玻璃体凝胶中,以阻断称为血管内皮生长因子(vegf)的蛋白质,该蛋白质可刺激异常血管生长并渗漏流液。阻断vegf可以减缓(破坏)异常血管生长并减少视网膜中的流液。可用的抗vegf药物包括avastin(贝伐单抗)、lucentis(兰尼单抗)和eylea(阿波西普),所有这三种药物对于治疗大多数dme患者都是安全有效的。但是,大多数患者在治疗的前六个月需要每月注射抗vegf。此后,注射的频率降低:通常在治疗的后六个月中需要注射三到四次,在治疗的第二年中注射约四次,第三年注射两次,第四年注射一次,而在第五年则不需要注射。随着疾病的稳定,可能不需要频繁进行散瞳眼科检查。但是,所有这些治疗都需要由眼保健专业人员进行,并且需要通过注射进行。
因此,本领域中需要糖尿病性眼病、尤其是早期糖尿病性视网膜病和糖尿病性黄斑水肿的其它治疗方法。
技术实现要素:
广义上讲,本发明涉及作为细胞间隙连接通讯(gjic)调节剂的化合物,其用于治疗或预防通常在人类患者中的糖尿病性眼病、特别是治疗或预防糖尿病性视网膜病和糖尿病性黄斑水肿的方法。在一些优选的方面,本发明特别涉及早期糖尿病性视网膜病的治疗或预防。
尽管在各种组织中已经广泛研究了细胞间隙连接通讯(gjic)的作用,但是本发明关注的是其与糖尿病性视网膜中的凋亡细胞死亡和周细胞迁移的相关性。间隙连接通道允许离子、营养物质和其他信号分子(最多1kd)在相邻细胞之间通过。重要的是,连接蛋白43(cx43)介导的gjic在调节视网膜中的细胞生长、血管紧密度和细胞死亡中起着关键作用,因此是维持视网膜血管内稳态的重要因素。cx43在视网膜中的表达丰富,这表明大量的间隙连接偶联。然而,在高葡萄糖和糖尿病状况下,cx43表达下调并且其功能受损,由此损害了视网膜血管细胞中的gjic活性。此外,高葡萄糖和糖尿病诱导的cx43下调和gjic活性降低在表现出脱细胞毛细血管数目显著增加且周细胞损失的糖尿病性小鼠、大鼠和人类的视网膜中的血管细胞死亡增加中起关键作用。
在本文所述的实验中,我们示出了间隙连接调节剂达那肽(danegaptide)(2s,4r)-1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸的施用(j.med.chem.52(4):908-911,2009),可防止在高葡萄糖条件下细胞间gj解偶联,并防止高葡萄糖诱导的视网膜血管细胞凋亡。本文所述的实验进一步研究了体外观察到的这些保护作用是否可转化到糖尿病的体内模型中。特别地,本申请中公开的结果研究了达那肽的施用是否可以预防糖尿病性大鼠视网膜中脱细胞毛细血管的生长和周细胞损失。测试了三种不同的体外系统,这些系统显示了细胞偶联和渗透性来替代血管紧密度/血管渗漏和凋亡。
此外,已知血管(包括眼中存在的血管)由两种相互作用的细胞类型组成,参见song等,neuro-oncology,2005年7月,453-464。因此,内皮细胞形成血管壁的内衬,而周细胞围绕血管管部的表面,支持并维持血管的生长并有助于抑制血管渗漏。因此,周细胞在功能上很重要,因为当血管失去周细胞时,其会变得出血和过度扩张,从而导致诸如水肿和糖尿病性视网膜病等病症,最终导致失明。除了gjic调节剂对视网膜内皮细胞的作用之外,本申请显示,通过施用gjic调节剂,可以显著减少大鼠糖尿病性视网膜病模型中的周细胞损失。
此外,在玻璃体内注射途径和使用渗透泵的全身递送途径中确定了达那肽的递送模式的功效。
因此,在第一方面,本发明提供了如本文所述的gjic调节剂化合物,其用于治疗或预防人类受试对象的糖尿病性眼病的方法,所述方法包括向受试对象施用治疗有效量的所述gjic调节剂化合物;或其药学上可接受的盐。
优选地,gjic调节剂化合物选自(2s,4r)-1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸和ac-dtyr-dpro-dhyp-gly-dala-gly-nh2;或其药学上可接受的盐或水合物。
优选地,gjic调节剂化合物用于治疗或预防早期糖尿病性视网膜病和糖尿病性黄斑水肿。这是有利的,因为许多当前形式的糖尿病性视网膜病的治疗都集中于例如增生性糖尿病性视网膜病(pdr)等疾病的晚期治疗,其中视网膜分泌的生长因子触发新血管的增殖。因此,本发明提供了一种在该病症的晚期阶段之前的时间点治疗或预防糖尿病性眼病的方法。
在另一方面,本发明提供了适于将gjic调节剂化合物递送至眼的药物组合物。
本文所述的gjic调节剂化合物可使细胞在糖尿病性眼病期间保护自身。不希望受任何特定理论的束缚,本发明人推测,化合物可能对细胞具有稳定作用,降低了线粒体渗漏的趋势和/或降低了细胞形成渗漏的外细胞膜的趋势和/或改善了细胞的细胞间偶联。这些化合物可能会使细胞之间的偶联更好,使细胞能够共享可用能量(atp),并能够进行细胞间信号传导,包括钙信号传导。
在另一方面,本发明提供选自(2s,4r)-1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸和ac-dtyr-dpro-dhyp-gly-dala-gly-nh2的化合物或其药学上可接受的盐或水合物在制备用于治疗或预防人类受试对象的早期糖尿病性眼病或糖尿病性黄斑水肿的药物中的应用,该方法包括向受试对象施用治疗有效量的化合物,或其药学上可接受的盐或水合物。
在另一方面,本发明提供了一种治疗或预防人类受试对象的早期糖尿病性眼病或糖尿病性黄斑水肿的方法,该方法包括向人类受试对象施用治疗有效量的化合物或其药学上可接受的盐或水合物,其中,所述化合物选自:(2s,4r)-1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸和ac-dtyr-dpro-dhyp-gly-dala-gly-nh2;或其药学上可接受的盐或水合物。
在另一方面,本发明提供了包含本文所述的gjic调节剂化合物的药物组合物,其用于本文所述的方法,所述药物组合物包含所述gjic调节剂化合物和药学上可接受的赋形剂。优选地,gjic调节剂以滴眼剂的形式、经隐形眼镜、或经鼻喷雾剂或注射(例如玻璃体内注射)施用。还可以全身施用,例如通过使用片剂或胶囊剂。
现在将通过示例而非限制的方式,参照附图描述本发明的实施方式。然而,本发明的各种其他方面和实施方式在本公开的基础上对于本领域技术人员而言将是明显可见的。
在本文中使用的“和/或”应视为两个指定的特征或部件中各自的具体公开(独立或与另一个一起)。例如,“a和/或b”将视为具体公开了(i)a、(ii)b和(iii)a和b中的每一种,就像它们在本文中分别列出一样。
除非上下文另外指示,否则以上阐述的特征的描述和定义不限于本发明的任何特定方面或实施方式,并且等同地适用于所描述的所有方面和实施方式。
附图说明
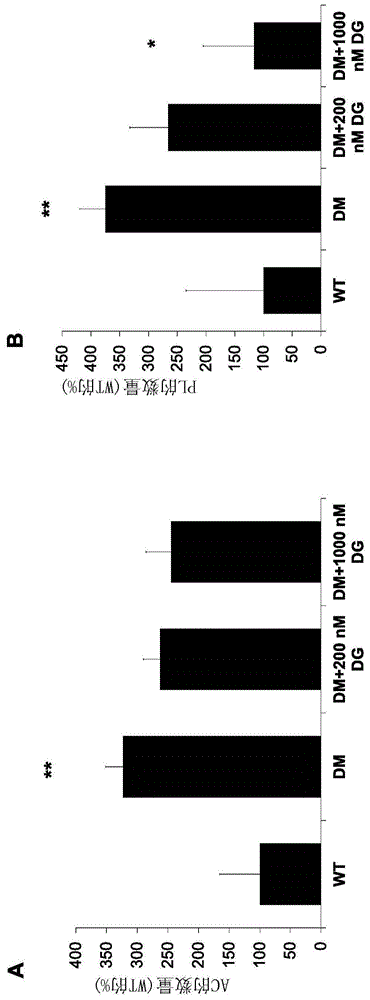
图1.200nm或1000nm达那肽(dg)的玻璃体内注射对糖尿病性大鼠眼中ac和pl生长的影响。与非糖尿病性大鼠视网膜相比,糖尿病性大鼠视网膜中(a)ac和(b)pl的数量明显增加(**=p<0.01)。与未治疗的糖尿病性大鼠视网膜相比,糖尿病性大鼠视网膜的玻璃体内注射1000nm达那肽显著降低了pl的数量(*=p<0.05)。在达那肽治疗组中,ac的数量减少,但由于动物数量少(n=3)而缺乏统计学意义。
图2.达那肽(dg)对糖尿病性大鼠视网膜的ac和pl发展的影响。代表性图像显示了(a)wt、(b)dm、(c)dm+玻璃体内注射(iv)1000nmdg、(d)dm+ivdh2o、(e)dm+渗透泵(op)dg和(f)dm+opdh2o大鼠的视网膜血管网络。ac(箭头);pl(空心箭头)。显示了累积rtd数据的图形化图示表明,与非糖尿病性大鼠视网膜相比,糖尿病性大鼠视网膜中(g)ac和(h)pl的数量明显增加。重要的是,与作为对照组的糖尿病性大鼠视网膜的玻璃体内(iv)注射水相比,iv注射达那肽显著减少了ac和pl的数量。而且,与经渗透泵(op)在糖尿病性大鼠视网膜中全身递送水相比,经op全身递送达那肽明显减少了ac和pl的数量。在达那肽治疗的视网膜中,细胞间偶联的改善防止了ac和pl的发展(**=p<0.001;*=p<0.01;n=6~9只动物/组)。
图3.达那肽(dg)对视网膜血管渗漏的影响。显示累积ivp数据的图形图示表明,与非糖尿病性大鼠视网膜相比,糖尿病性大鼠视网膜的视网膜血管渗漏明显增加。重要的是,与作为对照组的糖尿病性大鼠视网膜的玻璃体内(iv)注射水相比,iv注射dg显著减少了血管渗漏。此外,与经渗透泵(op)在糖尿病性大鼠视网膜中全身递送水相比,经op全身递送dg明显减少了血管渗漏。在dg治疗的视网膜中,细胞间偶联的改善防止了糖尿病诱导的血管渗漏(**=p<0.001;n=8~10只动物/组)。
图4.达那肽(dg)对视网膜血管渗透性的影响。视网膜整装铺片的代表性图像显示出(a)野生型(wt)、(b)糖尿病性(dm)、(c)dm+玻璃体内注射(iv)1000nmdg、(d)dm+ivdh2o、(e)dm+渗透泵(op)dg和(f)dm+opdh2o大鼠的毛细管网络。在dg治疗的视网膜中,细胞间偶联的改善防止了糖尿病诱发的血管渗漏。比例尺=50μm。
图5.采用noiseqbio时达那肽在4h逆转了基因表达的一些变化。深灰色条表示转录物的下调。浅灰色条表示转录物的上调。阈值:padj<0.05。
图6:采用deseq2时达那肽在4h(左)和1d(右)逆转了基因表达的一些变化。黑色条表示下调的基因。白色条表示上调的基因。阈值:padj<0.05。
具体实施方式
定义
除非另有说明,否则为特定术语提供以下定义。
在本说明书和权利要求书中,使用了天然氨基酸的标准三字母和一字母代码。本文中的术语“肽”表示通过肽键连接的两个以上氨基酸部分(氨基酸残基)的链。通常,肽可包含一种或多种天然存在的氨基酸和/或一种或多种非天然存在的氨基酸。
在本文中,术语“天然存在的氨基酸”是指以下20种氨基酸之一:ala(a)、cys(c)、ser(s)、thr(t)、asp(d)、glu(e)、asn(n)、gin(q)、his(h)、arg(r)、lys(k)、ile(i)、leu(l)、met(m)、val(v)、phe(f)、tyr(y)、trp(w)、gly(g)和pro(p)。在天然存在的肽分子中,这些氨基酸(除缺乏手性中心的gly外)通常以l-氨基酸残基的形式存在,不过适用于本发明的化合物包括包含d-氨基酸残基的肽(例如ac-dtyr-dpro-dhyp-gly-dala-gly-nh2)。
氨基酸三字母代码如本领域中所使用。hyp是指4-羟基脯氨酸。
用于本发明的化合物可以包含两个以上不对称原子(也称为手性中心),从而可能存在非对映异构体。适用于本发明的化合物包括这样的非对映异构体。
如本文所用,术语“血管细胞”包括内皮细胞和周细胞。
糖尿病性眼病
糖尿病性眼病是影响糖尿病患者的一组眼病况。这些病症包括糖尿病性视网膜病变、糖尿病性黄斑水肿(dme)、白内障和青光眼。各种形式的糖尿病性眼病都有可能导致严重的视力丧失和失明,因此是糖尿病的严重并发症。糖尿病性视网膜病涉及视网膜血管的变化,其可能导致视网膜血管出血或渗漏流液,从而使视觉失真。糖尿病性视网膜病是糖尿病患者视力丧失的最常见原因,也是工作年龄成人失明的主要原因。dme是糖尿病性视网膜病的后果,其导致称为黄斑的视网膜区域肿胀。
糖尿病引起的慢性高血糖与视网膜细小血管的损伤有关,导致糖尿病性视网膜病。视网膜检测到光并将其转换为信号,该信号通过视神经发送到大脑。糖尿病性视网膜病可导致视网膜血管漏液或出血(流血),使视力失真。在最晚期,新的异常血管在视网膜表面增生(数量增加),这可能导致视网膜上形成瘢痕和细胞丢失。
普遍接受的是,糖尿病性视网膜病的发展经历四个阶段,参见https://nei.nih.gov/health/diabetic/retinopathy:
1.轻度非增生性视网膜病。在视网膜的微细血管中,气球状肿胀的小区域(称为微动脉瘤)出现在该疾病的最早阶段。这些微动脉瘤可能会使流液渗入视网膜。
2.中度非增殖性视网膜病。随着疾病的恶化,滋养视网膜的血管可能会肿胀和扭曲。其还可能失去运输血液的能力。两种病症都会引起视网膜外观的特征性变化,并可能导致dme。
3.重度非增生性视网膜病。更多的血管发生阻塞,向视网膜区域的血液供应丧失。这些区域分泌向视网膜传递信号以生长新血管的生长因子。
4.增生性糖尿病性视网膜病(pdr)。在这个晚期阶段,视网膜分泌的生长因子会触发新血管的增殖,这些血管沿着视网膜的内表面生长并进入玻璃体凝胶,即充满眼的流液。新血管易破碎,这使得更容易泄漏和出血。伴随的疤痕组织可能收缩并引起视网膜脱离,从而将视网膜从下面的组织中拉出,就像墙纸从墙壁上剥落一样。视网膜脱离可导致永久性视力丧失。
由于本发明针对间隙连接的作用,因此在优选的方面,本发明关注患有早期糖尿病性视网膜病(即上述第1至3阶段,更优选的是上述第1和2阶段,还更优选上述第1阶段)的患者的治疗或预防,或作为具有发展为糖尿病性眼病风险的1型或2型糖尿病患者的预防性治疗,这些风险发生在释放出实质水平的在增生性糖尿病视网膜病的第4和/或3阶段中触发新血管的增殖的生长因子之前。
糖尿病性黄斑水肿(dme)是在称为黄斑的视网膜区域中积液(水肿)。黄斑对于用于阅读、辨识面部和驾驶的清晰、直接的视觉非常重要。dme是糖尿病性视网膜病患者视力丧失的最常见原因。糖尿病性视网膜病患者中约有一半会发展为dme。尽管其更可能随着糖尿病性视网膜病恶化出现,但dme可以在疾病的任何阶段发生。
有糖尿病性眼病风险的糖尿病患者包括患有所有类型的糖尿病(1型、2型和妊娠型)的患者。患糖尿病的时间越长,发展为糖尿病性眼病的风险就会增加。举例来说,40%至45%的被诊断出患糖尿病的美国人患有某种阶段的糖尿病性视网膜病,但是仅有约一半的人意识到这一点。怀孕期间发展为糖尿病或患有糖尿病的妇女可能会迅速发作或恶化为糖尿病性视网膜病。因此,本发明可用于治疗所有这些患者类型。
另外,本发明的医学应用和方法可以用于进行血糖控制的患者的预防性应用。在这种治疗中,当将具有长期高血糖水平的患者进行血糖控制时,眼组织可能已经习惯于高葡萄糖的可用性,并且随着达到正常的葡萄糖水平而变得紧张。因此,当患者处于血糖控制时,本发明可以用作保护性治疗。
这些患者处于经历糖尿病性视网膜病恶化的风险,并且由于血糖得到控制而可以得到保护。
糖尿病性视网膜病的早期通常没有症状。这种疾病通常会逐渐恶化直至影响视力。异常的视网膜血管出血可导致出现“漂浮”斑点。这些斑点有时会自身清除。这些斑点有时会自己清除。但是,如果不及时治疗,出血常常会复发,从而增加永久性视力丧失的风险。如果发生dme,则可能导致视力模糊。
糖尿病性视网膜病和dme可能会在全面的散瞳眼科检查中检测到,这种检查可能包括视力测试(使用视力表测试来衡量人在不同距离处的视能力),眼压测量(测量眼内压力),瞳孔散大(其中滴在眼表面的滴液会扩张(扩大)瞳孔,使医师可以检查视网膜和视神经)和/或光学相干断层扫描(oct),该技术类似于使用光波代替声波来捕获体内组织图像的超声技术。oct提供了可以由光线穿透的组织(例如眼)的详细图像。全面的散瞳眼科检查还使医生能够检查视网膜是否有血管变化、血管渗漏、或血管渗漏的警告信号,例如脂肪沉积、黄斑肿胀(dme)、晶状体改变和/或神经组织受损。如果怀疑血管渗漏dme或严重的糖尿病性视网膜病,可以使用荧光素血管造影检查受损或渗漏的血管。在此测试中,通常将荧光染料注射到血液中,通常注射到手臂静脉中。当染料到达眼时,对视网膜血管进行拍照。我们在大鼠中生成的血管渗漏数据之间存在紧密的转译联系,并且这种相同的方法可用于诊断人类的血管渗漏。
可以结合本发明的方法采用各种施用途径,包括但不限于眼内注射、全身施用、口服施用、鼻喷雾剂、滴眼剂或隐形眼镜。
就此而言,可能合意的是,所施用化合物(或其药学上可接受的盐或水合物)的浓度在受试对象的血浆中达到50nm至5μm。本文提供的体外研究表明,当gjic调节剂化合物在视网膜血管的微环境中达到50nm至100nm的浓度时,可观察到最佳效果。举例来说,当通过渗透泵或通过局部注射在眼中实现50nm至100nm的血浆浓度,以在玻璃体中实现较高浓度从而能够朝向视网膜血管形成浓度梯度时,可以实现该浓度。这些数据教导了要施用的有效剂量以在视网膜组织的微环境中达到50nm至100nm。
适用于本发明的化合物
非常适用于本发明的化合物的实例是1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸,例如其(2s,4r)非对映异构体[即,(2s,4r)-1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸]或其药学上可接受的盐或水合物。该化合物的替代名称的一个实例是(2s,4r)-1-(2-氨基乙酰基)-4-苯甲酰氨基吡咯烷-2-甲酸。
后一种化合物的其他非对映异构体(即2s4s、2r4r、2s4r或2r4s非对映异构体)可用于本发明。
适用于本发明的另一种化合物(肽)是ac-dtyr-dpro-dhyp-gly-dala-gly-nh2(见上)。
这些化合物的特定形式也可以分别称为达那肽(danegaptide)和罗替加肽(rotigaptide)。
达那肽的药学上可接受的盐包括达那肽盐酸盐。
除上述化合物外,其他适用于本发明的化合物包括某些其他gjic调节化合物,例如抗心律失常肽aap(aonuma等,chem.pharm.bull.(tokyo),28,3332-3339(1980))、aap10(dhein等,naunynschmiedebergsarchpharmacol.,350,174-184(1994);muller等,eur.j.pharmacol.,327,65-72(1997))、hp5(美国专利4,775,743号公开)和其他抗心律不齐肽,如wo02/077017或wo2007/078990所公开的。
应当理解,本文所述的化合物可以组合使用。例如,可以在本文描述的方法中同时或依次施用多于一种gjic调节剂化合物。
药学上可接受的盐
适用于本发明的具有酸性部分的化合物的药学上可接受的盐可以使用有机或无机碱形成。
与碱形成的合适的盐包括金属盐,例如碱金属或碱土金属盐,例如钠、钾或镁盐;氨盐和有机胺盐,例如与吗啉、硫代吗啉、哌啶、吡咯烷、一元、二元或三元低级烷基胺(例如乙基叔丁基胺、二乙基胺、二异丙基胺、三乙基胺、三丁基胺或二甲基丙基胺)、或一元、二元或三元羟基低级烷基胺(例如单、二或三乙醇胺)形成的那些。也可以形成内盐。当适用于本发明的化合物包含碱性部分时(如在例如1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸及其列举的非对映异构体的情况下),盐可以使用有机或无机酸形成。例如,盐可以由以下酸形成:乙酸、丙酸、乳酸、柠檬酸、酒石酸、琥珀酸、富马酸、马来酸、丙二酸、扁桃酸、苹果酸、邻苯二甲酸、盐酸、氢溴酸、磷酸、硝酸、硫酸、甲磺酸、萘磺酸、苯磺酸、甲苯磺酸或樟脑磺酸。也可以使用其他已知的药学上可接受的酸。如已经提到的(见上),1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸的(2s,4r)非对映异构体的优选盐形式是一水合盐酸盐。
本教导还可以扩展到本文公开的适用于本发明的化合物的前药的应用。如本文所用,“前药”是指当施用于哺乳动物受试对象、特别是人类受试对象时,将产生、生成或释放所公开类型之一的化合物的部分。前药可以通过修饰化合物中存在的官能团来制备,其方式使得修饰可以通过常规操作或在体内从母体化合物上裂解下来。前药的实例包括本文公开的化合物,其包含一个或多个附接(键合)至该化合物的羟基、氨基、巯基或羧基上的分子部分,并且当施用于待治疗的受试对象时,其在体内裂解分别形成游离的羟基、氨基、巯基或羧基。前药的实例包括但不限于可用于本发明的本文公开的化合物中的醇和胺官能团的乙酸酯、甲酸酯和苯甲酸酯衍生物。优选的前药的实例包括噁唑烷酮或咪唑烷酮前药。酯前药可以与低级醇如c1-6醇形成。前药的制备和应用论述于以下文献中:t.higuchi和v.stella,“pro-drugsasnoveldeliverysystems”,a.c.s.symposiumseries,第14卷;以及edwardb.roche编,“bioreversiblecarriersindrugdesign”,americanpharmaceuticalassociationandpergamonpress,1987年。
药物组合物
本发明使用的化合物或其药学上可接受的盐或水合物可以以合适的药物组合物的形式施用,其可以通过本领域已知的任何可接受的方法单独或组合施用。
本文相关的药物组合物可包含与一种或多种药学上可接受的载体、稀释剂、载剂或赋形剂混合的本文公开的用于本发明的化合物。通常,本发明使用的药物组合物可以适于将该化合物以滴眼剂、隐形眼镜、鼻喷雾剂的形式经玻璃体内施用或者全身性(例如通过以片剂或胶囊剂的形式)施用。
有用的制剂可以包括可提供本教导化合物的持续释放的制剂。这些对于后续施用(第一次施用后)特别有用。组合物优选为液体制剂形式,其制备方法一般描述于“remington'spharmaceuticalsciences”,第17版,alfonsor.gennaro(编),markpublishingcompany,easton,pa,美国,1985年。此类组合物通常包含有效量的本教导的一种或多种活性化合物以及合适的载体,以便以与所选的施用途径相容的形式提供剂量。优选地,载体为载剂、稀释剂、缓冲剂、肌肉弹性调节剂、防腐剂和/或稳定剂的形式。构成载体的赋形剂必须与活性药物成分相容,并且优选地能够稳定化合物而不对所治疗的受试对象有害。
可以使用储存型或缓释制剂的形式,以便在施用化合物或组合物(例如通过皮肤注射或沉积)后在许多小时或几天内将治疗有效量的制剂递送到血流中。适于缓释的制剂可包含生物可降解性聚合物,例如l-乳酸、d-乳酸、dl-乳酸、乙交酯、乙醇酸及其异构体。类似地,载体或稀释剂可以包括本领域已知的任何缓释材料,例如单硬脂酸甘油酯或二硬脂酸甘油酯,其单独使用或与蜡混合。
其他缓释制剂可包括但不限于以下制剂,其包含与脂质体、微球、乳剂或胶束和液体稳定剂组合的本文公开的至少一种化合物。
理想的治疗效果所需的本发明的化合物和组合物的剂量将取决于该化合物的效力、所使用的特定组成、以及所选择的施用途径。一般地,化合物以每位患者每天约0.001g至10g的范围施用。例如,化合物可以以每位患者每天约1mg至约1000mg、每位患者每天约10mg至约100mg或每位患者每天约50mg的范围施用。
本发明的化合物(或其药学上的盐或水合物)的施用可以以单次单位剂型(例如以大丸剂的形式)进行或作为连续疗法以随时间的多次剂量的形式进行。作为另选,可以采用连续输注系统或缓释长效制剂。可以同时或以任何顺序相继地共同施用可用于本发明的两种以上化合物(或其药物组合物)。另外,出于预防目的,例如如果糖尿病患者被认为有发展成糖尿病性视网膜病或糖尿病性黄斑水肿的风险,可以以相似的方式施用化合物和组合物。最终,最佳的给药方案将由主治医师为每个患者单独确定。
治疗应用
根据本发明,使用本文指定的化合物可以治疗或预防的病症包括糖尿病性眼病,例如糖尿病性视网膜病(特别是早期糖尿病性视网膜病)和糖尿病性黄斑水肿,特别是人类受试对象中的所述病症。
根据本发明,可以以治疗有效量将一种或多种化合物或其药学上可接受的盐或水合物(例如以适当的药物组合物的形式)施用给有需要的个体。
如本文所用,“治疗有效量”是指下述的量,其能够减轻给定的脑血管病况或病理的症状,并且优选地能够部分或完全地使具有该病况或病理的受试对象的生理响应正常化。症状的减轻或生理响应的正常化可以使用本领域已知的方法来确定,并且可以随着给定的病况或病理而变化。有效量将由技术人员考虑诸如药物的效力、患者的年龄和体质、体重、药物的药代动力学特征等因素来确定,并且通常将针对每个患者或患者组来开具药物。
化合物的有效量可以是至少约10μg/kg体重/天,例如至少约100μg/kg体重/天,至少约300μg/kg体重/天,和至少约1000μg/kg体重/天。另一方面,化合物或二聚体的有效量可以是至多约100mg/kg体重/天,例如至多约50mg/kg体重/天和至多约10mg/kg体重/天。预期该化合物的有效量将为约100μg/kg体重/天,约300μg/kg体重/天或约1000μg/kg体重。
在本文所述的体外系统中提供的实验(在体外系统(细胞偶联检验/sldt)中的剂量发现)表明,在微环境中的最佳浓度为50nm至100nm,而体内先导研究表明100nm注射优于200nm注射。
实验例
gjic调节剂化合物
用于本发明的化合物(肽)可以适当地通过固相或液相合成来合成。在这种情况下,可以参考例如fields等,“principlesandpracticeofsolid-phasepeptidesynthesis”,syntheticpeptides(2002,第二版)。
关于1-(2-氨基乙酰基)-4-苯甲酰基氨基-吡咯烷-2-甲酸(例如其(2s,4r)非对映异构体)的制备,其合成和纯化的合适方法描述于wo2007/078990,其中该(2s,4r)异构体表示为“化合物2”(wo2007/078990通过引用整体并入)。
(2s,4r)非对映异构体的有用盐形式的实例是一水合盐酸盐,其制备描述于wo2008/079266,并且在本说明书中也称化合物x(wo2008/079266通过引用整体并入)。
关于ac-dtyr-dpro-dhyp-gly-dala-gly-nh2,其固相合成和纯化描述于wo01/62775(其中该化合物表示为“化合物2”)。wo01/62775通过引用整体并入。
动物
所有动物研究均根据“针对眼科和视觉研究中的动物使用的arvo声明”进行。在确定达那肽的最佳浓度的初步研究中,使用了12只sprague-dawley雄性大鼠,每只重200g。12只大鼠中有9只经腹膜内注射链脲佐菌素(stz)(55mg/kg体重)以诱导糖尿病,持续6周。其余3只动物用作非糖尿病对照。糖尿病6周后,将动物处死并分离视网膜。在确定1000nm达那肽对ac和pl数量的影响的后续研究中,使用了36只sprague-dawley雄性大鼠,每只重200g。在36只大鼠中,30只注射了stz来诱导糖尿病,持续15周。其余6只动物用作非糖尿病对照。糖尿病15周后,将动物处死并分离视网膜。注射stz后2或3天后检查血液和尿液中的葡萄糖浓度,以确认动物的糖尿病状态。对个每只动物,每周测量血糖水平2至3次并在死亡时测量血糖水平。糖尿病组代表血糖水平>350mg/dl的大鼠。糖尿病性大鼠根据需要接受nph胰岛素注射以维持血糖水平。
视网膜胰蛋白酶消化
摘除的眼在10%福尔马林中放置至少24小时。然后用刀片将眼切成两半,并分离视网膜并将其放入0.5m甘氨酸中,保持24至48小时。如kuwabara&cogan(studiesofretinalvascularpatterns.i.normalarchitecture.archivesofophthalmology1960;64:904-911)中所述进行rtd。每个视网膜都经过3%胰蛋白酶的一系列洗涤,并去除了视网膜的非血管物质。然后分离出视网膜毛细血管网络,并将其铺展在涂有硅烷的载玻片上。
脱细胞毛细血管和周细胞损失的评估
如bobbie等(reducedconnexin43expressionanditseffectonthedevelopmentofvascularlesionsinretinasofdiabeticmice.investigativeophthalmology&visualscience2010;51:3758-3763)所述,rtd用高碘酸schiff和苏木精染色。使用连接到显微镜的数码相机对10个代表性视野照相,并对图像的ac和pl进行分析。根据显著的组织学特征(包括基底膜突出为空壳)将凋亡的周细胞鉴定为pl。缺乏周细胞和内皮细胞的毛细血管被认为是ac。
结果
达那肽保留gjic并减少大鼠视网膜内皮细胞的凋亡
将大鼠视网膜内皮细胞(rrec)在正常(n;5mm)或hg(30mm)培养基中生长3、5和7天。平行地,将在hg培养基中生长的细胞暴露于100nm达那肽(dg,一种aap10类似物,其可稳定cx43介导的细胞偶联)中3、5和7天。另外,用抑制gj偶联的cx43阻断剂(阴性对照)或保护gjic的阳性对照aap10处理在n培养基中生长的细胞。为了确定gjic,在三个时间点进行了刮擦式染料转移(sldt)检验。类似地,分别通过差异化染料染色检验和体外透过率检验评估细胞的凋亡和细胞单层渗透率。
用达那肽处理的rrec保留了gjic,降低了细胞死亡,并降低了细胞单层渗透性。sldt检验表明,在hg条件下生长并暴露于达那肽3、5和7天的细胞保留了gjic。类似地,达那肽在所有三个时间点都从hg诱导的细胞凋亡中拯救了细胞。另外,到第5天时,细胞单层渗透性显著降低。当在n培养基中生长的细胞暴露于对照aap10时,未观察到凋亡或渗透性变化。暴露于降低细胞偶联的cx43阻断剂的细胞显示出过度的凋亡和细胞单层渗透性。
这些发现表明,避免hg介导的受损细胞间偶联可能是抑制与糖尿病性视网膜病相关的细胞凋亡和血管渗透性过大的有用策略。
达那肽防止了脱细胞毛细血管(ac)和周细胞损失(pl)的发展
图1和图2所示的结果表明,cx43间隙连接偶联剂达那肽的施用可防止糖尿病性大鼠视网膜中ac和pl的发展。通过玻璃体内注射或全身递送达那肽,gjic调节剂化合物所促进的细胞间偶联的改善可防止糖尿病性大鼠视网膜中视网膜血管细胞死亡。
这项研究的发现表明,间隙连接偶联剂的施用可保护视网膜中视网膜血管细胞死亡。而且,结果表明,如在糖尿病性视网膜病中观察到的那样,在糖尿病视网膜中减少的细胞间偶联和受损的gjic活性至少部分地导致了视网膜血管细胞死亡增加。因此,本申请的结果表明,改善细胞间偶联可以用作治疗或预防与糖尿病性视网膜病或糖尿病性黄斑水肿的发病机理相关的视网膜血管细胞损失的策略。
gjic调节剂化合物防止视网膜细胞死亡
在糖尿病性视网膜病(dr)中,细胞间偶联似乎受到损害,导致视网膜血管细胞死亡和视网膜血管病变的发展。这项研究评估了在糖尿病性大鼠的视网膜中施用间隙连接调节剂是否对视网膜血管细胞死亡有保护作用。
为了确定达那肽(dg)的最佳浓度,通过玻璃体内注射在链脲佐菌素(stz)诱导的糖尿病性大鼠中测试了cx43间隙连接偶联剂的两种浓度(200nm或1000nm)。通过stz诱导糖尿病,持续6周,研究结束时,摘除眼球,对视网膜进行视网膜胰蛋白酶消化(rtd)以分离毛细血管网络,并用苏木精和高碘酸schiff(pas)试剂染色以分析脱细胞毛细血管数量(ac)和周细胞损失(pl)。基于该初步研究,在后续研究中经玻璃体内注射1000nm达那肽,以确定改善的细胞偶联对视网膜血管细胞死亡的影响。另外,使用渗透泵全身施用达那肽。在该研究中使用的每组大鼠数量为至少6只。总体上,将大鼠分为6组:野生型(wt)对照大鼠,stz诱导的糖尿病性大鼠,经玻璃体内注射达那肽的糖尿病性大鼠,经玻璃体内注射水的糖尿病性大鼠,全身递送达那肽的糖尿病性大鼠和全身递送水的糖尿病性大鼠。经stz诱导糖尿病,持续15周,在研究结束时,分离视网膜并进行rtd以分析ac和pl。
与糖尿病性大鼠相比(对照组的296±26%,p<0.001),经玻璃体内注射或全身施用达那肽治疗的糖尿病性大鼠的视网膜血管系统显示出ac的发展显著降低(分别为对照组的134±28%,p<0.01和对照组的133±37%,p<0.001)。同样,与糖尿病性大鼠相比(对照组的335±40%,p<0.005),经玻璃体内或全身施用达那肽治疗的糖尿病性大鼠的视网膜毛细血管显示出pl数目明显减少(分别为对照组的112±62%,p<0.01和对照组的103±65%,p<0.005)。这项研究的发现表明,改善的细胞间偶联对与糖尿病性视网膜病相关的视网膜血管细胞死亡有保护作用。
在糖尿病性视网膜病动物模型中确定达那肽预防视网膜血管病变的治疗潜力
为了确定对cx43介导的细胞间隙连接通讯(gjic)的改善是否能预防视网膜血管细胞死亡和视网膜血管渗透性过大,在大鼠中经玻璃体内或渗透泵施用达那肽。将60只雄性sprague-dawley大鼠随机分为6组,每组由10只构成:非糖尿病性大鼠,糖尿病性大鼠,经玻璃体内注射dg(浓度为1000nm)的糖尿病性大鼠,经玻璃体内注射无菌水作为空载剂的糖尿病性大鼠,经渗透泵全身施用dg(70mg/ml,以达到100nm血浆dg浓度)治疗的糖尿病性大鼠,和经渗透泵全身施用无菌水治疗糖尿病性大鼠(作为对照)。诱导糖尿病持续15周,在研究结束时检查所有动物并随后处死,并对其视网膜分别检查:(i)体内渗透性(ivp),(ii)rtd和(iii)光学相干断层扫描(oct)以分析血管渗漏、ac和pl以及视网膜厚度。
体内渗透性数据
为了确定在高血糖应激下改善的细胞间偶联对视网膜血管渗透性的影响,在处死动物前不久进行fitc-右旋糖酐尾静脉注射,其后评估视网膜毛细血管中fitc-右旋糖酐的外渗。与非糖尿病性大鼠相比,糖尿病性大鼠的视网膜毛细血管网络显示出血管渗漏增加(对照组的214±17%,相比对照组的100±22%,p<0.001)。重要的是,与经玻璃体内施用水治疗的糖尿病性大鼠(作为对照)相比,经玻璃体内施用dg治疗的糖尿病性大鼠的视网膜毛细血管网络显示出血管渗漏的明显减少(对照组的149±22%,相比对照组的241±14%,p<0.001)(图3和4)。同样,与全身施用水治疗的糖尿病性大鼠(作为对照)相比,经全身施用dg治疗的糖尿病性大鼠的视网膜毛细血管网络显示出血管渗漏的明显减少(对照组的143±14%,相比对照组的224±14%,p<0.001)(图3和4)。此外,经玻璃体内注射dg治疗的糖尿病性大鼠与全身施用dg治疗的糖尿病性大鼠之间的血管渗漏没有明显差异。
达那肽在体外糖尿病性视网膜病模型中的转录组学效应
研究了达那肽在体外糖尿病性视网膜病模型中的转录组学作用,从而:1)揭示在存在或不存在达那肽的糖尿病样病症中的转录组变化,2)将先前观察到的功能作用与转录组修饰相关联,以及3)确定达那肽对糖尿病样病症下的相关细胞的影响所涉及的途径。将大鼠的原生视网膜内皮细胞在正常葡萄糖培养基(ng)、高葡萄糖培养基(hg)、高葡萄糖培养基+达那肽100nm(hg_dg100)和高葡萄糖培养基+达那肽1000nm(hg_dg1000)四个实验条件下进行体外平板实验。在四个时间点(点板后4小时、点板后1天、点板后3天和点板后5天)评估样品。
这些实验表明,与ng条件相比,达那肽诱导hg细胞中基因表达变化,并且对于某些基因逆转了hg诱导的变化。实验还证实了,与正常葡萄糖条件相比,达那肽可诱导暴露于高葡萄糖下的细胞中基因表达的变化,并且达那肽可逆转高葡萄糖条件下差异化表达的某些基因的表达(图5和6)。这些图采用了两种不同的分析方法(deseq2和noiseqbio)描述了4小时(4h)和1天的转录变化。数据显示出转录变化的模式随时间改变。特别是,实验发现,fscn3(在hg中相比ng下调的肌动蛋白捆绑蛋白,被达那肽逆转)通常在暴露于高葡萄糖的细胞中下调,与肌球蛋白和钙粘蛋白相关,并与糖尿病性视网膜病中改变的glcnac过程有关。而且,tpcn2(一种可能在人类糖尿病中起作用的基因)在hg中相比ng下调,在4h时被达那肽逆转,并与参与sp3依赖性糖尿病性视网膜病变途径的esr1相互作用。几种转录物如dnm1l、nucb2和trmt10a等在1天的hg条件下均下调,并且达那肽总体上增加了这些转录物的表达,这表明可能的针对hg应激的保护作用(图6)。在1天时,实验发现cacybp基因在hg中相比ng下调,并被达那肽逆转。该基因与sin3a在功能上相互作用,而sin3a是高血糖诱导的ang2途径(导致糖尿病性视网膜病)的主要上游调节因子。
本文引用或随本申请一起提交的所有出版物、专利和专利申请(包括作为信息披露声明的一部分提交的参考文献)均通过引用将其全文并入。
- 还没有人留言评论。精彩留言会获得点赞!