具有抗炎症及抗菌效果的A.C.C.提取物及包含其作为有效成分的组合物的制作方法
具有抗炎症及抗菌效果的a.c.c.提取物及包含其作为有效成分的组合物
技术领域
1.本发明涉及具有抗炎症及抗菌效果的提取物、抗菌及抗炎症组合物。
背景技术:
2.在体内引起的炎症反应是受到伤口或细菌感染之类的物理、化学刺激时恢复受损部位的重要的身体防御机制之一,当受到刺激时,血管活性物质局部游离,致使血管透过性增加,诱发炎症。并且,炎症反应是根据外部刺激在生物体内形成的恢复体系,临床上伴随红肿、发热、肿胀、疼痛等而出现。炎症反应相关的细胞有巨噬细胞、单核细胞、淋巴细胞、肥大细胞、成纤维细胞、血小板等,巨噬细胞(machrophage)是引起炎症反应的主要细胞,这些受到刺激时或者被免疫细胞中分泌的细胞因子(cytokine)激活而生成一氧化氮(no,nitric oxide)和细胞因子,对生物体防御起到重要作用。并且,炎症反应时,生成及释放组织胺、血清素、花生四烯酸(arachidonic acid)代谢物、活性氧、细胞因子等之类的炎症介质因子。
3.反复的炎症反应在炎症细胞中引起活性氧簇和活性氧簇的过多生成来导致永久性的转基因,从而还导致不可逆的病变。即,虽然炎症反应是在生物体内引起的防御机制,但持续引起炎症反应时,促进粘膜损伤,最终引起浮肿、痛症、红肿、发热等,可导致心血管疾病、类风湿性关节炎、支气管炎及癌症之类的慢性炎症相关疾病。
4.大体上说,一氧化氮合酶(nos,nitric oxide synthase)中的诱导型一氧化氮合酶(inos)与炎症反应相关,因干扰素
‑
γ(interferon
‑
γ)、炎症性细胞因子及脂多糖(lps)的刺激而表达。众所周知,体内的no在抗菌和肿瘤切除中担当重要功能,但由诱导型一氧化氮合酶形成的no增加血管透过性,引起浮肿等反应,并促进炎症介质物质的合成来使炎症加重。
5.众所周知,脂多糖(lps,lipopolysaccharide)为革兰氏阴性菌的细胞外膜中的内毒素,这刺激巨噬细胞或单核细胞来刺激肿瘤坏死因子
‑
α(tnf
‑
α,tumor necrosis factor
‑
α)、白细胞介素
‑
1β(il
‑
1β,int erleukin
‑
1β)及白细胞介素
‑
6(il
‑
6)等炎症介质性细胞因子的分泌,催化炎症反应。肿瘤坏死因子
‑
α为在体内的巨噬细胞、淋巴细胞及白细胞等生成的细胞因子,在正常状态下未生成,当巨噬细胞受到刺激时,合成而分泌。白细胞介素
‑
6为代表性的促炎性细胞因子(pro
‑
inf lammatory cytokine)的一种,从包含单核细胞的多种细胞中分泌,在初期免疫反应中起到重要作用。众所周知,白细胞介素
‑
1β与白细胞介素
‑
6及肿瘤坏死因子
‑
α一同表示代表性的炎症性细胞因子之一,是生成no的介质物质,其为引起局部炎症,并使t细胞激活、b细胞成熟及自然杀伤细胞(nk cell)激活的细胞因子。据报道,这种炎症介质性物质的合成与利用环氧化酶(cox,cyclooxygenase)将花生四烯酸转换为白三烯(leukotriene)、前列腺素(prostaglandin)、血栓素(thromboxane)等的过程及一氧化氮(no)的生成相关,最终对宿主带来致命性结果。尤其,no为反应性高的物质,并且是对细菌、病毒、菌及寄生虫之类的病原菌执行先天免疫反应所需的作用的物质,
其利用一氧化氮合酶(nos,no synthase)由l
‑
精氨酸(l
‑
arginine)制备而成,一氧化氮合酶分为结构型一氧化氮合酶(cnos,constitutive nos)和诱导型一氧化氮合酶(inos,inducible nos)。其中,据悉,诱导型一氧化氮合酶当受到外部刺激或促炎性细胞因子等的刺激时,生产大量的no来引起血管透过性及浮肿等,诱发炎症反应,严重的情况下,还蔓延到类风湿性关节炎及自身免疫性疾病之类的免疫性疾病。与此相关地,需要一起开发具有抗菌及抗炎症活性的天然物提取物和有效的抗炎症治疗剂。
技术实现要素:
6.技术问题
7.本发明提供利用天然物中药材来具有抗菌及抗炎效果的提取物,尤其,其目的在于,确认蒸馏提取包含黄柏的共14种中药材来得到的a.c.c.提取物的抗炎症活性,并确认临床效果。
8.本发明的另一目的在于,确认a.c.c.提取物为一起具有抗炎症效果与强效抗菌效果的有效的成分。
9.并且,其目的在于,确认a.c.c提取物在临床上也是通过抗炎症及抗菌作用缓解尿布疹及痱子等症状的物质,从而确认a.c.c提取物可用作对炎症性疾病有效的治疗剂。
10.解决问题的方案
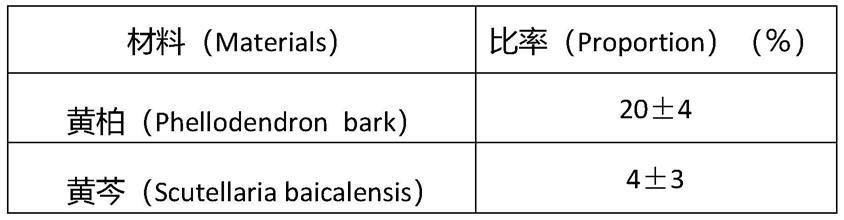
11.为了解决上述问题,本发明提供由黄柏(phellodendron bark)、黄芩(scutellaria baicalensis)、芍药(paeonia lactiflora pall)、白鲜(dictamnus dasycarpus turcz)、知母(anemarrhena asphodeloides)、白矾(alumen)、龙脑香(dryobalanops aromatica gaertner)、薄荷(mentha arvensis var.piperascens)、土木香(inula helenium)、朝鲜野丁香(syringa velutina var.kamibayashii)、刻叶紫堇(coryda lis incisa)、鳢肠(eclipta prostrata)、忍冬(lonicera japonica)及甘草(glycyrrhiza uralensis)中药材配合而成的a.c.c.提取物。
12.尤其,其特征在于,用于制备上述提取物的中药材的配方分别为16~24重量百分比的黄柏、1~7重量百分比的黄芩、5~11重量百分比的芍药、5~11重量百分比的白鲜、1~7重量百分比的知母、4~12重量百分比的白矾、1~7重量百分比的龙脑香、1~7重量百分比的薄荷、1~7重量百分比的土木香、1~7重量百分比的朝鲜野丁香、1~7重量百分比的刻叶紫堇、1~7重量百分比的鳢肠、1~7重量百分比的忍冬、1~7重量百分比的甘草。
13.上述提取物的特征在于,蒸馏提取包含黄柏(黄柏)的共14种中药材来得到的样品(a.c.c.提取物)具有抗菌及抗炎症活性。在相关实验中,确认被脂多糖(lps,lipopolysaccharide)刺激的raw 264.7细胞中细胞释放的一氧化氮(no)生成量和作为炎症性细胞因子的肿瘤坏死因子(tnf,tumor necrosis factor)
‑
α、白细胞介素(il,interleukin)
‑
1β(il
‑
1β)及白细胞介素
‑
6生成量的变化。其结果,a.c.c.提取物在无细胞毒性的情况下强效抑制被脂多糖生成的no和炎症性细胞因子的生成。
14.并且,本发明的a.c.c.提取物的特征在于,对绿脓杆菌(pseudo monas aeruginosa)、金黄色葡萄球菌(staphylococcus aureus)、耐甲氧西林金黄色葡萄球菌(mrsa,methicillin
‑
resistant staphylococcu s aureus)、白色念球菌及变形链球菌(streptococcus mutans)起到抗菌作用。a.c.c.提取物在上述细菌中呈现99.9%的强效细
lps.con;control,lps 1μg/ml;1μg/ml lipopolysaccharide,ao;lps 1μg/ml,a1;a.c.c.1μg/ml,a5;a.c.c.5μg/ml,a10;a.c.c.10μg/ml.
29.图5为表示使用a.c.c.提取物之后尿布疹及痱子等症状变化的图表。(n=18).*,p<0.05,and***,p<0.001compared to 0week
具体实施方式
30.以下,通过实施例更详细说明本发明。但是,这些实施例只不过是本发明的例示性记载内容,而本发明的范围并不局限于这些实施例。
31.实施例1.材料的挑选及a.c.c.提取物的准备
32.基于本草学进行文献调查,总共挑选出14种的中药材。中药材购买了由韩国首尔药令市的ck(株)出品的包装为生药制剂而销售的产品。达尔伯克改良伊格尔培养基(dmem,dulbecco
′
s modified eagle
′
s medium)、胎牛血清(fbs,fetal bovine serum)购买于海克隆(hyclone)(logan,ut,usa)。青霉素(penicillin)(100u/ml)、链霉素(streptomycin)(100μg/ml)购买于gibco(生命技术有限公司,盖瑟斯堡,md,usa(life technology inc.,gaithersburg,md,usa))。脂多糖、3
‑
(4,5
‑
二甲基噻唑
‑2‑
基)
‑
2,5
‑
二苯基四氮唑溴盐(mtt,3
‑
(4,5
‑
dimethylthiazol
‑2‑
yl)
‑
2,5
‑
diphenyl tetrazolium bromide)、亚硝酸钠(sodium nitrite)、二甲基亚砜(dmso,dimethyl sulfoxide)购买于西格玛化工公司(sigma chemical co.)(st.louis,mo,usa)。nitric oxide(no)检测试剂盒(detection kit)购买于内含子(intron)来利用,酶联免疫吸附测定分析试剂盒(elisa assay kit)购买于赛默飞世尔科技公司(thermo fisher scientific)。
33.根据各个比率,配合除了黄柏之外的13种中药材,并将40l的第三蒸馏水作为溶剂来在80℃温度下蒸馏提取11小时(参照图1、表1)。
34.表1
35.材料及a.c.c.提取物中的比率
36.[0037][0038]
实验例1:基于mtt assay的细胞毒性测定
[0039]
raw 264.7细胞的培养
[0040]
raw 264.7细胞购买于韩国细胞株银行。使用含有青霉素/链霉素100unit/ml和10%胎牛血清的dmem培养基,在37℃、5%co2培养箱(incubator)中培养,隔3天一次进行继代培养。
[0041]
raw 264.7细胞生存率测定,将96孔板(well plate)调节为2
×
104cells/well的浓度之后,培养24小时,进行稳定化。24小时之后,全部去除孔(well)的培养基。以a.c.c.提取物的最终浓度为1、5、10μg/ml的方式稀释于培养液,并处理在细胞株之后,培养3小时。3小时之后,除了对照组之外的孔处理1μg/ml脂多糖。24小时之后,全部去除培养基之后,在各孔添加mtt溶液(0.2μg/ml的无酚红(in phenol red free)dmem)100μl,并在37℃、5%co2培养箱中反应2小时,来使mtt还原。之后,在各孔添加二甲基亚砜(dmso)溶液来溶解所
生成的甲臜(formazan)。利用酶标仪(microp late reader)在545nm下测定吸光度。
[0042]
实验例2:一氧化氮(nitric oxide)生成量的测定
[0043]
以1
×
105cells/well的浓度,在6孔板中添加raw 264.7细胞。在37℃、5%co2培养箱中保管24小时之后,在raw 264.7细胞处理1、5、10μg/ml的a.c.c.提取物,3小时之后,处理1μg/ml脂多糖来培养24小时。利用基于格里斯反应(griess reaction)的nitric oxide(no)检测试剂盒(intron)来分析nitric oxide。在细胞培养上清液中放入格里斯试剂(griess reagent)并混合,在常温下反应10分钟之后,利用酶标仪在520nm吸光度下测定。基于亚硝酸钠(sodium ni trite)的不同浓度标准曲线,适用于式中,来确定培养液内的no浓度。
[0044]
实验例3:炎症相关细胞因子分泌量的测定
[0045]
为了测定作为炎症引起细胞因子的肿瘤坏死因子
‑
α、白细胞介素
‑
6及白细胞介素
‑
1β生成量,在6孔板中添加1
×
105的cells/well的浓度的raw 264.7细胞。24小时之后,用1、5、10μg/ml的a.c.c.提取物处理,3小时之后,将1μg/ml的脂多糖处理于除了对照组之外的所有孔。培养24小时之后,利用elisa kit(thermo fisher scie ntific)来分析分泌于培养基的肿瘤坏死因子
‑
α、白细胞介素
‑
6及白细胞介素
‑
1β。利用酶标仪在450nm下测定。
[0046]
实验例4:抗菌活性的测定
[0047]
为了察看a.c.c.提取物的抗菌活性,使用纸盘(paper disc)测定抗菌力。试验之前培养的试验菌株,以1.0
×
104以上接种在各培养基。在灭菌的纸盘(paper disk)中装载100μl的a.c.c.之后,干燥30分钟,以备用。在接种试验菌株的培养基上,按间隔放置装载有a.c.c.的纸盘之后,在培养箱中培养24~48小时。测定纸盘周边的抑制圈,来进行结果判定及分析。
[0048]
实验例5:临床研究
[0049]
通过公告招募的被试者,根据对象的特性,由代理人(监护人)制作“预先问卷”。通过预先问卷调查,掌握症状、皮肤状态等之后,提供组合物,研究员指导被试者每天同样时间,以每天1cc的量涂布5~10次,如此涂布14天。并且,为了客观的研究结果,拍照患处来比较分析涂布前与涂布后,此时,图片中除外如脸部一样可识别个人的部位。涂布14天之后,代理人制作“试验问卷”。资料的保管期间根据生命伦理法从研究结束的时间点起保管3年,信息保护期间之后,个人信息及图片会通过不可复原的方法永久删除。
[0050]
实验例6:统计分析
[0051]
所有测定值由平均
±
标准偏差值表示,适当地通过两侧独立样品t检验(t
‑
test)或方差分析检验(anova test)执行统计分析。在各组之间的组平均值呈现相当大的差异时,通过事后测试方法scheff
′
s方法,适用该分析。
[0052]
实验结果
[0053]
1.a.c.c.提取物对raw 264.7细胞引起的细胞毒性
[0054]
为了确认a.c.c.提取物对raw 264.7细胞引起的影响,按不同浓度(1、5、10μg/ml)对a.c.c.提取物进行预处理之后,处理1μg/ml的脂多糖。培养24小时之后,利用mtt assay方法确认细胞毒性。其结果确认,细胞生存率分别为98.47、90.91、92.23%,对细胞生存不呈现显著意义的高生存率(图2)。
[0055]
2.a.c.c.提取物对raw 264.7细胞的no生成抑制带来的效果
[0056]
利用脂多糖刺激巨噬细胞时,表达诱导型一氧化氮合酶(inos),从而生成过量的no。据悉,生成的no促进炎症反应来诱发组织损伤。因此,察看a.c.c.提取物是否抑制no之类的炎症性介质物质。其结果确认,利用脂多糖处理raw 264.7细胞时,与对照组相比,no生成从0.45增加到3.15,即,增加7倍。当以1、5、10μg/ml处理a.c.c.提取物来测定no的生长抑制效果时,其结果确认,在raw264.7细胞中因脂多糖诱导而增加的no生成因a.c.c.提取物而浓度依赖性地被抑制(参照图3)。
[0057]
3.a.c.c.提取物对raw 264.7细胞的细胞因子生成抑制带来的效果
[0058]
在诱导炎症反应的过程中,伴随着no及pge2之类的炎症介质物的生成与通过免疫反应的炎症性细胞因子的生成。代表性的细胞因子有肿瘤坏死因子
‑
α、白细胞介素
‑
1β及白细胞介素
‑
6。为了察看a.c.c提取物对炎症介质性细胞因子带来何种影响,通过elisa assay方法来测定肿瘤坏死因子
‑
α、白细胞介素
‑
1β及白细胞介素
‑
6的变化量。用脂多糖处理raw 264.7细胞时,与对照组相比,肿瘤坏死因子
‑
α、白细胞介素
‑
1β及白细胞介素
‑
6增加得相当多(图4)。但是,处理10μg/ml的a.c.c.提取物时,减少得相当多。通过这种结果确认,a.c.c.提取物抑制在raw 264.7细胞中诱导炎症的细胞因子,由此具有抗炎症效果。
[0059]
4.a.c.c.提取物的抗菌活性效果
[0060]
已知,诱发瘙痒症、小儿出疹的主要病原菌有a群链球菌(化脓性链球菌(streptococcus pyogenes))及金黄色葡萄球菌(staphylococcus aureus)。并且,女性阴道炎(varginal candidiasis)、出疹、瘙痒感的主要病原真菌有白色念球菌(candida albicans),由此,当男性的大腿根等皮肤折叠而容易潮湿的部位被霉菌感染时,有可能发生股藓或念珠菌性间擦疹之类的皮肤感染症。在本实验中,通过如下列表的方法对绿脓杆菌、金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌、白色念球菌及变形链球菌进行实验,a.c.c.提取物在共5种菌株中呈现99.9%的强效的细菌减少率(%)(表2)。
[0061]
表2
[0062]
a.c.c.提取物的抗菌活性效果
[0063][0064][0065]
因此,可知a.c.c.提取物是对上述5种菌具有强效的抗菌效果的有效成分。
[0066]
5.a.c.c.提取物对婴
·
幼儿的尿布疹、痱子带来的影响
[0067]
将患有尿布疹、瘙痒症、痱子症状的婴
·
幼儿作为对象,涂布a.c.c提取物时,临床上确认出疹、过敏性皮肤、溃烂、瘙痒症、痱子等症状是否得到改善。临床试验前,以出疹、过敏性皮肤、溃烂、瘙痒症及痱子等共5种项目,制作预先问卷。满分为共4分,出疹项目为2.61
±
1.1分,最高,其次分数高的痱子项目为2.41
±
1.1分。制作预先问卷之后,每天在同样的时间,一天5~10次涂布1cc量,如此涂布14天,经过14天之后,制作试验问卷。其结果,使用后分数均为1.5分以下,呈现整体上得到改善的形态。使用前最高的出疹和痱子均分别为1.39
±
0.70、1.35
±
0.70分,确认到减少得相当多的结果(图5、表3)。并且,比较婴
·
幼儿的临床试验前与将a.c.c.提取物涂布1周之后以及将a.c.c.提取物涂布2周之后的经过来进行观察。其结果,皮肤的痱子经过2周时,可确认到消失得相当多。因此,a.c.c.提取物被视为对尿布疹及痱子等症状有效果。
[0068]
表3
[0069]
a.c.c.提取物对婴
·
幼儿的尿布疹、痱子带来的影响
[0070][0071]
由本发明的上述实验结果可确认a.c.c.提取物在作为小鼠巨噬细胞的raw 264.7细胞中不具有细胞毒性(图2),这意味着a.c.c.提取物在细胞中呈现的效果是与细胞的生存率的变化无关的固有的效果。为了确认a.c.c.提取物的抗炎症效果,以不同浓度将a.c.c.提取物预处理在raw 264.7细胞3小时,用1μg/ml脂多糖处理24小时之后,测定细胞中作为炎症性因子的no的生成变化。其结果,因脂多糖而增加的no生成量被a.c.c.提取物浓度依赖性地减少(图3)。
[0072]
这种结果表明a.c.c.提取物在因脂多糖而进行的炎症过程中抑制重要介质因子no的形成,由此具有抗炎症作用。
[0073]
并且,当开始炎症反应时,炎性反应的转录因子nf
‑
kb被激活,调节肿瘤坏死因子
‑
α、白细胞介素
‑
1β及白细胞介素
‑
6之类的重要炎症促进蛋白质的基因表达,据悉,这些调节诱导型一氧化氮合酶的激活而对炎症反应起到重要作用。因此,确认对作为炎症的重要指标的炎症介质性细胞因子(肿瘤坏死因子
‑
α、白细胞介素
‑
1β及白细胞介素
‑
6)带来的a.c.c.提取物的效果。用脂多糖处理raw 264.7而诱发炎症,此时,确认a.c.c.提取物如何改变肿瘤坏死因子
‑
α、白细胞介素
‑
1β及白细胞介素
‑
6的生成量,其结果可见,a.c.c.提取物浓度依赖性地强效减少被脂多糖诱导的炎症因子(图4)。
[0074]
通过这种结果明确得知,a.c.c.提取物减少肿瘤坏死因子
‑
α、白细胞介素
‑
1β及白细胞介素
‑
6的生成,呈现调节诱导型一氧化氮合酶的表达来抑制no生成的抗炎症效果。并且,a.c.c.提取物对绿脓杆菌、金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌、白色念球菌及变形链球菌呈现99.9%的强效细菌减少率(%)(表1)。其表明a.c.c.提取物是呈现抗炎症效果和抗菌作用的协同效果的有效的炎症治疗剂。为了明确地确认这些,将患有尿布疹、瘙痒症、痱子症状的婴
·
幼儿作为对象,评价了涂布a.c.c.时是否有出疹、过敏性皮肤、溃烂、瘙痒症、痱子等症状的改善效果。评价预先问卷的结果显示,在满分4分中,出疹项目为
2.61
±
1.1分,最高,使用14天之后,分数为1.39
±
0.70分,与使用前相比减少得相当多(图5)。并且,观察婴
·
幼儿的临床试验前、后的经过的结果可确认,将a.c.c.提取物使用2周时,皮肤的痱子缓解得相当不错。这明确表明a.c.c.提取物在临床上也是通过抗炎症及抗菌作用缓解尿布疹及痱子等症状的物质。因此,具有抗炎症及抗菌效果的a.c.c.提取物及将其作为主原料的产品可作为对炎症性疾病有效的备选方案。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1