一种无创血糖测量装置与方法与流程
本发明属于医疗器械
技术领域:
,具体涉及一种无创血糖测量装置与方法。
背景技术:
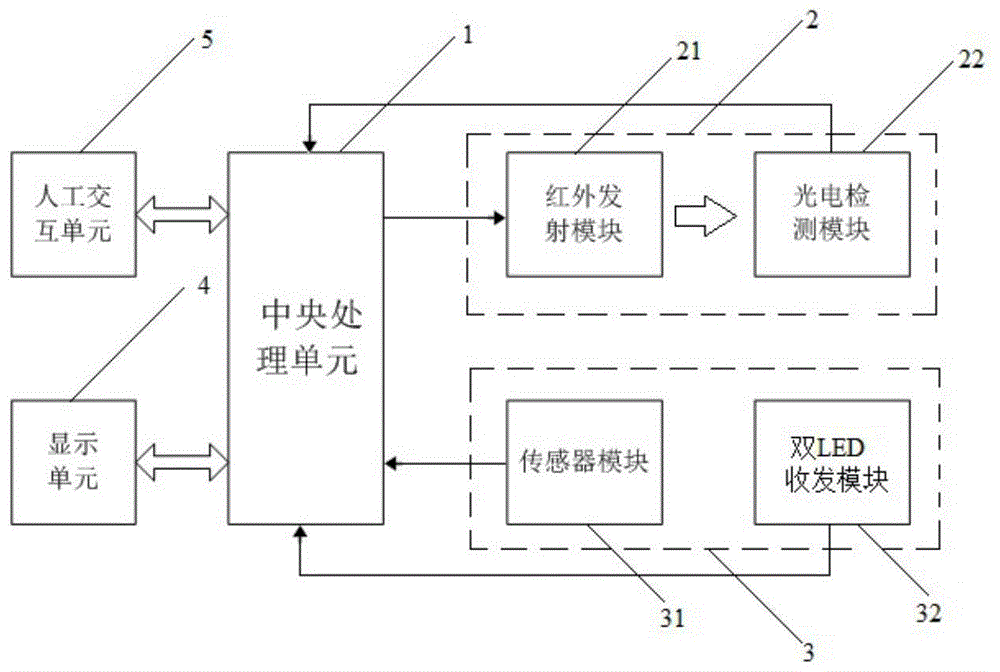
:自我血糖浓度监测一般需要采集血样,容易引起患者的生理疼痛并伴有感染的危险,因此,有创测量方法在很大程度上限制了血糖测定的频率,不利于实现精准管理。无创血糖浓度测量方法可以减少患者每次采血测量的痛苦、提高测量次数、提高血糖控制精确度、降低单次测量的成本。目前,血糖浓度的无创检测方法主要包括红外光谱法、能量代谢守恒法、偏振法等光学方法、离子电渗透法等。光学无创血糖检测技术在快速测量、实时监测、信息多维化等方面比较突出。在无创性血糖检测中应用最广的是红外光谱分析方法,通过对一束红外光透过人体组织或者由其反射的光谱信号分析,确定组织内葡萄糖的含量。红外光谱技术的优点是分析速度快、对人体无创、操作和维护简单、测量具有一定的精度等优点。缺点是采集信号为微弱生理信号导致干扰因素较多,在测量过程中产生包括噪声和其它干扰成分的复杂背景,采用现有的常规方法解析图谱,很难解决复杂背景对光谱分析的影响,从而影响血糖测量精度。另外,由于水的红外波段的吸收强度对溶解物的浓度和温度敏感,导致测量数据不稳定,同样影响血糖测量精度。能量代谢守恒法的原理是,理论上代谢产生的热量是血糖水平和氧容量的函数,而氧容量是动脉血氧饱和度以及血液流速的函数,脉搏跳动率以及血容量具有一定相关性,可对结果进行修正,因此利用代谢产生的热量、血氧饱和度、血流速度和脉率就可以计算出血糖的浓度。此方法的优点是可以使用通用传感器并且便于集成化,小巧轻便无创,成本较低、容易实施,缺点是对环境以及人体表温度和湿度比较敏感,容易导致偏差较大。而目前采用此技术实现的无创血糖检测仪,大多没有解决温度及湿度敏感性问题,导致测试数据不准。技术实现要素:为了解决现有技术中存在的上述问题,本发明提出一种无创血糖测量装置与方法。为实现上述目的,本发明采用如下技术方案:本发明提供一种无创血糖测量装置,包括中央处理单元和红外光法测血糖单元。红外光法测血糖单元包括与中央处理单元相连的红外发射模块和光电检测模块。红外发射模块用于产生波长为λ1和λ2的红外光,λ1为对血糖值变化不敏感的红外光波长,λ2为葡萄糖分子吸收较低、水分子干扰弱的红外光波长;光电检测模块用于接收透过检测部位(一般为手指)和/或经检测部位反射后的红外光,并将其转换为电压信号后送至中央处理单元;中央处理单元用于通过对由光电检测模块输入的电压信号进行信号数据处理,计算红外透射法血糖值(即葡萄糖浓度)bg1和/或红外反射法血糖值bg2。本发明还提供一种应用所述装置进行无创血糖测量的方法,包括以下步骤:步骤1,控制红外发射模块周期交替发射波长为λ1和λ2的红外光,获取透过检测部位波长为λ1的红外光经光电检测模块后输出的电压信号与波长为λ2的红外光直接经光电检测模块后输出的电压信号的差值,并根据所述差值计算红外透射法血糖值bg1;λ1为对血糖值变化不敏感的红外光波长,λ2为葡萄糖分子吸收较低、水分子干扰弱的红外光波长;步骤2,控制红外发射模块同时发射波长为λ1和λ2的红外光,获取由检测部位反射后的红外光经光电检测模块后输出的电压信号,并对所述电压信号进行信号数据处理,计算红外透射法血糖值bg2;步骤3,控制双led收发模块工作,获取由双led收发模块和传感器模块输出的电压信号,并对所述电压信号进行信号数据处理,根据能量守恒定律计算能量守恒法血糖值bg3;步骤4,对bg1、bg2和bg3进行融合,计算最终的血糖值bg。与现有技术相比,本发明具有以下有益效果:本发明通过将透过检测部位或经检测部位反射,对血糖值变化不敏感的波长的红外光信号和葡萄糖分子吸收较低、水分子干扰弱的波长的红外光信号转换成电压信号,并对所述电压信号进行信号数据处理计算血糖值,能够有效地抑制背景干扰信号的影响,消除由于水分子对近红外光的吸收作用引起的测量数据不稳定现象,从而提高无创血糖测量的精度。本发明通过将红外透射法、红外反射法和能量守恒法测得的血糖值进行融合得到最终的血糖值,使三种测量方法互补,进一步提高了血糖测量精度。附图说明图1为本发明实施例一种无创血糖测量装置的组成框图;图2为采用红外透射法测血糖的示意图;图3为采用红外反射法测血糖的示意图。图中:1-中央处理单元,2-红外光法测血糖单元,21-红外发射模块,22-光电检测模块,3-能量守恒法测血糖单元,31-传感器模块,32-双led收发模块,4-显示单元,5-人工交互单元。具体实施方式下面结合附图对本发明作进一步详细说明。本发明实施例一种无创血糖测量装置,如图1所示,所述装置包括中央处理单元1和红外光法测血糖单元2。红外光法测血糖单元2包括与中央处理单元1相连的红外发射模块21和光电检测模块22。红外发射模块21用于产生波长为λ1和λ2的红外光,λ1为对血糖值变化不敏感的红外光波长,λ2为葡萄糖分子吸收较低、水分子干扰弱的红外光波长;光电检测模块22用于接收透过检测部位和/或经检测部位反射后的红外光,并将其转换为电压信号后送至中央处理单元1;中央处理单元1用于通过对由光电检测模块22输入的电压信号进行信号数据处理,计算红外透射法血糖值bg1和/或红外反射法血糖值bg2。在本实施例中,所述装置主要由中央处理单元1和红外光法测血糖单元2组成,红外光法测血糖单元2主要由与中央处理单元1相连的红外发射模块21和光电检测模块22组成。红外发射模块21产生一定波长的红外光照射检测部位,经检测部位反射或透过检测部位的红外光被光电检测模块22接收,经光电检测模块22转换成电压信号后送到中央处理单元1,中央处理单元1通过对所述电压信号进行信号数据处理,计算血糖值。人体血液中的糖类主要由葡萄糖构成,其化学分子式为c6h12o6,包含多个能被红外光吸收的羟基o-h和甲基c-h官能团。由葡萄糖分子的红外光谱特征分析可知,葡萄糖分子在900~1200nm对红外光有二阶倍频吸收,在1400~1800nm对红外光有一阶倍频吸收;水的强吸收区域是1440~1470nm和960nm。根据以上特性,通过对光电检测模块22输出的电压信号进行信号数据处理,就能得到血糖值即血糖浓度。但是,在测量过程中存在复杂背景(包括噪声和其它成分信息),采用现有的常规方法很难消除复杂背景对光谱分析的影响。其中,由于红外谱区吸收峰的分布范围较宽,同一种血液中的基团可以在不同倍频区出现吸收峰;同时由于皮下血液在同一红外谱区内常有不同分子、多种基团的谱峰重叠在一起,导致光谱信息的分布范围广。如何有效地抑制背景信号对待测量结果的影响,从而提高测量精度,是本实施例所要解决的技术问题。经过理论推导以及反复实验,得出葡萄糖对红外光不敏感的波长λ1,以及葡萄糖分子吸收较低、水分子干扰弱的波长λ2。以波长为λ1的红外光检测信号作为测量基准信号,以波长为λ2的红外光检测信号作为参考信号,可以消除背景信号变化的影响。因此,本实施的红外透射法和反射法测血糖均采用上述两个波长的红外光。值得说明的是,本实施例所述的红外光,确切地说应该是近红外光,只是为了叙述简便这里统称为红外光。在本实施例中,检测部位选为手指。以手指作为血糖测量的检测部位,不仅因为操作方便,还由于手指毛细血管丰富,对于人体热代谢的反映也相对充分;同时因为手指皮肤厚度的原因,可以使测量点的测量厚度降低,从而使红外光源发出的光尽可能多地穿透皮肤、组织并被光电检测模块22接收。在所述装置的结构设计中,专门设计了用于放置检测部位的指夹盒或测试盒。作为一种可选实施例,所述装置还包括与中央处理单元1相连的显示单元4和人工交互单元5。在本实施例中,设置显示单元4主要用于显示各种实验参数、工作状态、测量结果等;设置人工交互单元5主要用于输入各种命令、设置参数等。人工交互单元5主要由功能键、操作键等组成。另外,所述装置还包括与中央处理单元1相连的数据存储单元和数据通信单元(图1中未画出)。数据存储单元主要由存储器芯片组成,用于存储实验数据;数据通信单元主要包括各种数据接口及无线通信模块,主要用于数据传输。作为一种可选实施例,所述红外发射模块21主要包括2个分别产生波长为λ1=1550nm和λ2=1310nm的红外光led光源。本实施例给出了红外发射模块21的一种具体技术方案。红外发射模块21主要由2个红外光led光源组成,一个产生波长为λ1=1550nm的红外光,另一个产生波长为λ2=1310nm的红外光。本实施例选用发光二极管作为光源,利用了其结构尺寸小、光源稳定且发光功率高,光谱宽度比较窄等优点。为了节省硬件开支,透射法和反射法可共用一个红外发射模块21;为了同时进行透射法测量和反射法测量,透射法和反射法也可以分别采用一个红外发射模块21。图2、3分别示出了透射法和反射法测血糖的示意图。透射法如图2所示,两个led光源分别发出1310nm和1550nm的红外光。两个自聚焦透镜将led发出的散射光聚焦为平行光,平行光经过光纤分路器后被分成两束能量相同的光,其中一束光透过检测部位后进入传导光纤,再照射到光电检测模块22的光电二极管上;另一束光则直接进入传到光纤,再照射在光电二极管上。反射法如图3所示,与透射法不同的是增加了一个测量探头。测量探头中设有两路传导入射光的光纤和两路传导漫反射光的光纤,并利用自聚焦透镜对入射光准直、增加反射光光强,以此保证入射光的垂直入射,使漫反射光强能够在最大范围内被光电二极管接收。另外,反射法中的两个led周期性交替工作。作为一种可选实施例,所述光电检测模块22主要包括依次相连的ingaas光电二极管、电流/电压转换电路和滤波放大电路。本实施例给出了光电检测模块22的一种具体技术方案。光电检测模块22主要由ingaas光电二极管、电流/电压转换电路和滤波放大电路组成。光电二极管用于将光信号转换为电流信号;电流/电压转换电路用于将所述电流信号转换为电压信号;所述电压信号十分微弱,滤波放大电路用于对其进行滤波放大,最终输出0-5v的电压,并送到中央处理单元1内部的a/d电路转换成数字信号。ingaas光电二极管性能良好,效率高,而且自身电容低、频带宽、暗电流小,响应速度快,噪声小,探测范围为900~1700nm,满足检测波长的需求。作为一种可选实施例,所述装置还包括能量守恒法测血糖单元3,能量守恒法测血糖单元3包括与中央处理单元1相连的传感器模块31,以及用于测量脉率和血氧饱和度的双led收发模块32。所述传感器模块31包括:用于测量环境温度的第一温度传感器,用于测量检测部位前端、中间和末端表面温度的第二温度传感器、第三温度传感器和第四温度传感器,用于测量环境辐射温度的第一辐射温度计,用于测量检测部位表面辐射温度的第二辐射温度计;用于测量环境湿度的第一湿度传感器,用于测量检测部位湿度的第二湿度传感器;所述双led收发模块32包括1个波长为660nm的红光led、一个波长为940nm的红外光led及光电检测电路。中央处理单元1通过对由传感器模块31和双led收发模块32输入的电压信号进行信号数据处理,计算能量守恒法血糖值bg3,并对bg1、bg2和bg3进行融合得到最终的血糖值bg。本实施例给出了能量守恒法测血糖单元3的技术方案。顾名思义,能量守恒法测血糖单元3是根据能量守恒定律测量血糖值。人体产热散热是一个动态平衡的过程,产热量与散热量相对相等。人体散热的主要方式是蒸发、对流和辐射,一般平静状态下人体不对外做功,而且人体代谢产热量与血糖值和血液中的氧含量之间存在相关关系;同时血液中的氧含量与血氧饱和度、血红蛋白浓度和血流速度有关,并且短时间内,人体代谢产生的热量供给其他生物反应所需能量很少,可以忽略不计,因而人体产热量与血糖值、脉率、血流速度和血氧饱和度相关。也就是说,血糖值可以看作是人体代谢产生的热量、脉率、血流速度和血氧饱和度的函数,通过分别求解人体代谢产生的热量、脉率、血流速度和血氧饱和度就可以计算血糖值。为此,能量守恒法测血糖单元3设置了传感器模块31和双led收发模块32。传感器模块31用于测量检测部位表面生理指标参数,双led收发模块32用于测量脉率和血氧饱和度。传感器模块31由8个传感器组成,分别为4个温度传感器、2个辐射温度计和2个湿度传感器。其中,第一温度传感器用于测量检测部位周围的环境温度;第二~四温度传感器分别用于测量检测部位前端、中间和末端的表面温度。现有技术一般只采用1个温度传感器测量检测部位表面温度,并将该表面温度用作表面平均温度。本实施例采用3个温度传感器分别测量检测部位3个不同位置的表面温度然后求平均值作为表面平均温度,更能反映真实的平均温度,从而提高血糖测量精度;第一辐射温度计用于测量环境辐射温度;第二辐射温度计用于测量检测部位表面辐射温度;第一湿度传感器用于测量环境湿度;第二湿度传感器用于测量检测部位湿度。双led收发模块32由发射部分和接收部分组成,发射部分包括1个波长为660nm的红光led和一个波长为940nm的红外光led;接收部分为光电检测电路,电路结构与前述的光电检测模块22相同。测量血氧饱和度时,所述两个波长的led均照射检测部位(透射),通过测量两个波长的吸收比(光电检测电路输出电压之比)计算血氧饱和度,即利用血液中氧合血红蛋白hbo2与脱氧血红蛋白hb对特定波段(通常指660nm~940nm)的红外光的吸收量的不同来检测血液中的血氧饱和度;测量脉率时,通过任意一个波长的led照射检测部位(透射)获得脉动信号,从而计算脉率。中央处理单元1通过对由传感器模块31和双led收发模块32输入的电压信号进行信号数据处理,计算能量守恒法血糖值bg3,并对bg1、bg2和bg3进行融合得到最终的血糖值bg。通过对三种不同方法得到的血糖值进行数据融合,可以取长补短进一步提高血糖测量精度。本发明另一实施例利用所述装置进行无创血糖测量的方法,包括以下步骤:s101、控制红外发射模块21周期交替发射波长为λ1和λ2的红外光,获取透过检测部位波长为λ1的红外光经光电检测模块22后输出的电压信号与波长为λ2的红外光直接经光电检测模块22后输出的电压信号的差值,并根据所述差值计算红外透射法血糖值bg1;λ1为对血糖值变化不敏感的红外光波长,λ2为葡萄糖分子吸收较低、水分子干扰弱的红外光波长;s102、控制红外发射模块21同时发射波长为λ1和λ2的红外光,获取由检测部位反射后的红外光经光电检测模块22后输出的电压信号,并对所述电压信号进行信号数据处理,计算红外透射法血糖值bg2;s103、控制双led收发模块32工作,获取由双led收发模块32和传感器模块31输出的电压信号,并对所述电压信号进行信号数据处理,根据能量守恒原理计算能量守恒法血糖值bg3;s104、对bg1、bg2和bg3进行融合,计算最终的血糖值bg。在本实施例中,步骤s101主要用于测量红外透射法血糖值bg1,步骤s102主要用于测量红外反射法血糖值bg2,步骤s103主要用于测量能量守恒法血糖值bg3,步骤s104主要用于通过对3种不同方法得到的血糖值bg1、bg2、bg3进行数据融合得到最终的血糖值bg。本实施例的通过将血糖值变化不敏感的波长的红外光信号和葡萄糖分子吸收较低、水分子干扰弱的波长的红外光信号转换成电压信号,并对所述电压信号进行信号数据处理计算血糖值bg1、bg2,能够有效地抑制背景干扰信号的影响,消除由于水分子对近红外光的吸收作用引起的测量数据不稳定现象,从而提高无创血糖测量的精度。本实施例通过将红外透射法、红外反射法和能量守恒法测得的血糖值bg1、bg2和bg3进行融合得到最终的血糖值bg,使三种测量方法互补,进一步提高了血糖测量精度。作为一种可选实施例,所述bg1的计算公式为:bg1=-1.5702×u+11.2435(1)其中,u=u参考-u透射,u参考为波长为1310nm的红外光led光源发射的红外光经光电检测模块22后输出的电压信号;u透射为波长为1550nm的红外光led光源发射的红外光透过检测部位后经光电检测模块22输出的电压信号;u的单位为v(伏);bg1的单位为mmol/ml(毫摩尔/毫升)。本实施例给出了一种测量bg1的技术方案。本实施例根据电压u=u参考-u透射按照式(1)计算bg1。u参考为没有经检测部位透射直接经光电检测模块22输出的电压信号,u透射为透过检测部位经光电检测模块22输出的电压信号。u参考对应波长为1310nm的红外光,u透射对应波长为1550nm的红外光,二者对应的波长可以互换,只需将式(1)中第一项的符号由负变为正即可。作为一种可选实施例,所述bg2的计算公式为:bg2=δ1×i1+δ2×i2+ω(2)其中,i1、i2分别为波长为1550nm和1310nm的红外光的反射率;δ1、δ2分别为i1、i2的校正系数,ω为反射光修正因子,δ1、δ2和ω的值通过理论推导和反复实验确定;bg2的单位为mmol/ml。本实施例给出了一种测量bg2的技术方案。本实施例通过测量检测部位对两个波长的红外光的反射率i1、i2,根据式(2)计算bg2。反射率等于反射光强与入射光强的比,与光电检测模块22输出的电压成正比,因此可以通过对光电检测模块22输出的电压进行数据处理得到。式(2)中,δ1、δ2和ω的值通过理论推导和反复实验确定,在本实施例中,取δ1=2.5931,δ2=2.3563,ω=3.4598。作为一种可选实施例,所述bg3的计算方法包括:根据式(3)~(7)计算当前测量时间检测部位代谢产热量q:q=e+r+c(3)e=3.0542×(0.2561×ts-pe×we-3.371)+16.7×ws×hc×(ps-0.7344×pe×we)(4)hc=1.4826×|ts-te|-0.0303×|trs-tre|+6.5539(5)其中,e为检测部位蒸发换热量;hc为人体与空气之间的总的对流换热系数;ts为检测部位表面平均温度,等于第二温度传感器、第三温度传感器和第四温度传感器测得的温度值的平均值;te为环境温度,由第一温度传感器测得;trs为检测部位辐射温度,由第二辐射温度计测得;tre为环境辐射温度,由第一辐射温度计测得;we为环境湿度,由第一湿度传感器测得;ws为检测部位湿度,由第二湿度传感器测得;r为检测部位辐射换热量;ε为人体表面黑度,ε=0.96;σ是波尔兹曼常数;c为检测部位对流换热量;为对流换热的有效散热面积,等于放置检测部位的测量盒内表面积的0.4326倍;pe和ps分别为环境温度下和检测部位表面平均温度下空气中水蒸气的饱和分压力,将t=te和t=ts分别代入式(8)得到的p即为pe和ps:其中,c1~c7为常数,通过理论推导和反复实验确定;根据式(9)计算每分钟脉动的次数即脉率hr:其中,f为采样频率;n为光电信号采样次数;m为采样到的脉动峰值的个数。根据式(10)计算血流速度bv:其中,γ为修正系数,γ=1.0125+|ws-we|/ws;t3、t1分别为检测部位前端和末端的表面温度;c1为血液比热容;ρ1为血液比重;δt为接触时间即当前测量时间。根据式(11)计算血氧饱和度spo2:其中,为氧合血红蛋白的质量分数,为脱氧血红蛋白的质量分数,均为常数,n34为检测部位对波长为λ3和λ4的红外光的吸光度之比,λ3=660nm,λ4=940nm。根据式(12)计算bg3:其中,分别为q、hr、bv、spo2的归一化值;α0为修正因子,α1、α2、α3、α4为拟合系数,α0、α1、α2、α3、α4的值通过理论推导和反复实验确定。本实施例给出了一种测量bg3的技术方案。本实施例根据能量守恒定律测量bg3。首先分别计算检测部位的代谢产热量q、脉率hr、血流速度bv、血氧饱和度spo2,然后根据式(12)计算bg3。式(8)中的c1~c7通过理论推导和反复实验确定,在本实施例中,t的单位为k(开氏温标)时,取c1=-5.6745359e+03,c2=6.3925247,c3=-9.677843e-03,c4=6.2215701e-07,c5=2.0747825e-09,c6=-9.4840240e-13,c7=4.1635019。式(12)中的α0、α1、α2、α3、α4的值通过理论推导和反复实验确定,本实施例取α0=0.5554,α1=1.3145,α2=1.6235,α3=1.4569,α4=1.2108。作为一种可选实施例,所述步骤s104具体包括:建立由微创法测得的血糖数据构成的训练数据集bg1(i)、bg2(i)和bg3(i),i=1,2,…,n,n为样本数据个数;以bg1、bg2和bg3为输入参数,以无创血糖值bg为输出参数,以无创血糖值与微创血糖值的误差被作为目标函数,建立bp神经网络模型:bgi=f(ε1i×bg1,ε2i×bg2,ε3i×bg3)(13)其中,i表示血糖类别,i=h,m,l,分别表示高血糖、中血糖和低血糖;ε1i、ε2i、ε3i分别为对应血糖类别i的bg1、bg2和bg3的计算因子,是多层神经网络中各层阈值的整体体现;根据当前检测量测得到的bg1或bg2或bg3,调用已构建好的随机森林算法中的多棵决策树模型,判断血糖类别;根据所述血糖类别和bg1、bg2、bg3,按照式(13)计算无创血糖值bg。本实施例给出了步骤s104的一种具体实现方法。首先,利用微创法测得的血糖数据建立训练数据集。然后,基于所述数据集建立以3种不同血糖值bg1、bg2和bg3为输入、以最终的无创血糖值bg为输出的bp神经网络模型,如式(13)。为了提高血糖计算精度,针对不同的血糖类别(高、中、低)分别建立模型,具体体现在不同血糖类别模型的bg1、bg2和bg3的计算因子ε1i、ε2i和ε3i也不同。有了构建好的模型就可以根据本次测量的bg1、bg2和bg3计算最终的血糖值bg了,具体方法是:根据本次测得的bg1或bg2或bg3,调用已构建好的随机森林算法中的多棵决策树模型,判断血糖类别;根据所述血糖类别按照式(13)计算无创血糖值bg。为了验证本发明无创血糖测量方法的有效性,进行了小规模临床试验。表1、表2分别是采用本发明的无创血糖测量方法(简称无创法)测得的血糖值,与利用标准仪器采用生化法和微创法测得的血糖值的对比数据。表1、表2中各血糖值的单位均为mmol/ml。表2中,序号为1~10的血糖值小于6,血糖类别为l(低);序号为11~20的血糖值在6~9之间,血糖类别为m(中);序号为21~30的血糖值大于9,血糖类别为h(高)。由表1可知,本发明所述方法与生化法相比,平均相对差在10%以内,完全满足《gb/t19634-2005体外诊断检验系统自测用血糖监测系统通用技术条件》所规定的要求,且数据的线性趋势基本相近,充分证明了本发明所述方法的准确性与稳定性。由表2可知,本发明所述方法与微创法相比较,平均相对误差在5%以内,且数据的线性趋势基本相同,充分说明本发明所述方法能够替代微创法实现血糖的无创测量。表1无创法和生化法测得的血糖值的对比序号无创法生化法误差相对误差14.914.560.357.68%24.244.65-0.41-8.82%33.403.69-0.29-7.86%47.077.46-0.39-5.23%54.204.67-0.47-10.06%66.255.770.488.32%75.104.590.5111.11%83.783.590.195.29%95.155.63-0.48-8.53%105.274.750.5210.95%114.565.05-0.49-9.70%126.325.830.498.40%134.304.78-0.48-10.04%146.435.950.488.07%155.354.860.4910.08%165.125.57-0.45-8.08%174.755.22-0.47-9.00%186.446.91-0.47-6.80%194.374.79-0.42-8.77%204.894.410.4810.88%表2无创法和微创法测得的血糖值的对比上述仅对本发明中的几种具体实施例加以说明,但并不能作为本发明的保护范围,凡是依据本发明中的设计精神所做出的等效变化或修饰或等比例放大或缩小等,均应认为落入本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1