治疗具有抗药性的癌症的医药组合物的制作方法
[0001]
本发明有关于一种化合物2,3,5,4
’-
四羟基二苯乙烯(tg-1,2,3,5,4
’-
tetrahydroxy-trans-stilbene),该医药组合物具有治疗抗药性的癌症的新用途。
背景技术:
[0002]
细胞表面的蛋白质p-glycoprotein,简写为p-gp,又称为调控多重抗药性相关蛋白mdr1(multidrug resistance protein 1)或三磷酸腺苷结合盒转运子b亚家族成员1abcb1(atp-binding cassette sub-family b member 1),主要为将药物排出细胞外的机制(mechanism),获得能量而利用药物帮浦(药物载体,drug efflux pump,药物流程泵)将药物排出细胞外,导致药物在细胞内的浓度不够,无法毒杀细胞,因而造成抗药性。目前发现至少有15种这样的蛋白质,可以产生对抗癌药物的抗药性,常见的有:p-glycoprotein、mrp1、abcg2等,由于这种蛋白质可以与许多种药物作结合,包括蒽环霉素类(anthracycline)、长春花属生物碱(vinca alkaloids)、稳定微管的药物(microtubule stabilizing drug),会产生交叉抗药,故又称为「多重抗药性」(multidrug resistance,mdr)蛋白。在临床上已经证实,许多肿瘤如果过度表现这种多重抗药性蛋白,将使得对治疗的反应变差,存活率下降。临床上,学者也利用所谓的mdr(multidrug resistance,多药耐药性)抑制剂,如唯律脉必利(verapamil)、奎尼丁(quinidine)、环孢素(cyclosporine),试图来逆转多重抗药性,但可惜的是,到目前为止,都没有很成功的试验。
[0003]
细胞在dna受到破坏时,会启动dna修补路径(dna repair pathway)的机制,来减少细胞的死亡,但是若无法修补,则将启动细胞凋亡程序。假设肿瘤细胞因修补系统发生突变,使得修补系统过度活跃,则即使肿瘤细胞受到化疗药物伤害,细胞凋亡程序受到抑制无法进行,故化疗药物便无法毒杀肿瘤细胞,抗药性因而产生。如用于多形恶性神经胶质瘤(gbm,glioblastoma multiforme)的药物temozolomide(替莫唑胺),当dna修补蛋白
─
mgmt突变,则受到temozolomide破坏的肿瘤细胞便受到保护,于是便对temozolomide产生了抗药性。
[0004]
绝大多数的肿瘤多少都有缺氧(hypoxia)的部位,肿瘤缺氧的状态下会刺激产生hif(hypoxia-inducible factor,缺氧诱导因子),hif会造成许多影响,而使肿瘤细胞延长存活、产生抗药性;这些影响包括:代谢功能改变、多重抗药性蛋白质的过度表现、细胞凋亡的抑制等。另外缺氧可能也与疾病进展或远程转移有关联,因为hif可以影响上皮细胞转型成间质细胞(epithelialto-mesenchymal transition,emt)、细胞迁移(cell migration)、建立有利于转移的前转移微环境(pre-metastatic niche)。另外,微环境中也存在着许多不同的基质细胞(stromal cells),其中不得不提的是肿瘤相关巨噬细胞(tumor-associated macrophage,tam),肿瘤相关巨噬细胞存在于肿瘤的血管周边或是缺氧区域,它会驱动着血管增生(angiogenesis)、淋巴血管增生(lymphangiogenesis)、免疫抑制与肿瘤转移。另外肿瘤相关巨噬细胞及肿瘤相关纤维母细胞(cancerassociated fibroblasts,caf)所分泌的细胞激素、生长因子也都参与上述过程,因而产生肿瘤恶化、抗药性。
[0005]
肿瘤干细胞(cancer stem cells,csc)一开始是在血癌中发现的,而后陆续在许多的固态肿瘤也有看到,一般认为这是发展为肿瘤最为原始的细胞。它的定义是,具有自我更新(selfrenewal)、分化(differentiate)的能力,且打入生物体内具有可以再生、传播的能力,生成新的肿瘤。肿瘤干细胞与正常的干细胞一样,高度表达p-glycoprotein(p糖蛋白)、abcg2等多重抗药性蛋白,它的状态处在相对静止期,具活化的dna修补能力,以及对细胞凋亡具有抵抗性,也由于以上这些特性,让肿瘤干细胞具有很强的药物抗药性。
[0006]
不论是致癌基因的活化性(activating mutation of oncogenes)突变或是肿瘤抑制基因得去活化性突变(inactivating mutation of tumor suppressor genes),都会造成讯息传导路径(信号传导路径)的不受控制,因而造成细胞不正常的大量生长。重要的致癌基因讯息传导路径有:pi3k/akt/mtor、ras/raf/mapk、nf-κb等;重要的肿瘤抑制基因有:rb、pten。临床上许多标靶治疗,包括表皮生长因子抑制剂、血管生成抑制剂、酪胺酸激酶抑制剂、mtor抑制剂等,都是想办法阻断这些讯息传导路径,来达到抑制肿瘤的效果。然而这些讯息传导路径是错综复杂的,肿瘤细胞有各种不同的机转,常常逃避抑制,因而产生抗药性。
[0007]
综合上述,肿瘤细胞透过抗药性机制(mechanism)使肿瘤产生抗药性,然而化疗又是目前不可或缺的一种治疗癌症的方法,依统计目前癌症死亡的患者中,90%以上与肿瘤细胞的抗药性有关,而且往往是对多种化疗药物都有抗药性。因此,在治疗癌症的过程中,如何对抗肿瘤细胞的耐药性是一个重要的问题,尤其在第一个机制药物自细胞排出(drug efflux)的蛋白质p-glycoprotein,简写为p-gp,又称为mdr1(multidrug resistance protein 1),到目前为止,都没有很成功的试验,因此,业界亟需开发一种医药组合物具有治疗抗药性的癌症的用途。
技术实现要素:
[0008]
有鉴于此,本发明提供一种用于制备治疗具有抗药性癌症的医药组合物的用途,所述医药组合物包含一化合物,该化合物如式i所示:
[0009][0010]
本发明提供一种用于制备治疗具有抗药性癌症的药物的用途,所述药物包含如式i所示的化合物;及一药学上可接受的载体、佐剂或媒剂。
[0011]
本发明提供的所述医药组合物治疗的癌症,所述癌症的癌细胞相较于一般正常细胞具有高度表达p-glycoprotein(p-gp)蛋白质的活性。
[0012]
本发明提供的所述具有抗药性的癌症的医药组合物的用途,所述癌症为一固态肿瘤癌。
[0013]
本发明治疗的所述固态肿瘤癌,其中包括乳腺癌、大肠癌、直肠癌或肺癌。
[0014]
本发明提供的所述具有抗药性的癌症的医药组合物的用途,所述医药组合物是用
于抑制癌细胞中p-glycoprotein蛋白质的活性。
[0015]
本发明提供一种用于制备治疗具有抗药性的癌症的医药组合物的用途,所述医药组合物包含:(a)一种如上述式(i)所述的化合物,与(b)一抗癌药物;及一药学上可接受的载体、佐剂或媒剂。
[0016]
本发明上述的用途,所述具有抗药性的癌症的癌细胞相较于一般正常细胞具有高度表达p-glycoprotein蛋白质的活性。
[0017]
本发明上述的用途,所述具有抗药性的一癌症为一固态肿瘤癌。
[0018]
本发明上述的用途,所述具有抗药性的一癌症为一固态肿瘤癌,该固态肿瘤癌包含乳腺癌、大肠癌、直肠癌或肺癌。
[0019]
本发明上述的用途,所述癌症治疗药物包含欧洲紫杉醇(docetaxel,dtx)或阿霉素(doxorubicin)。
[0020]
本发明上述的用途,所述抗癌药物包含欧洲紫杉醇(docetaxel,dtx)或阿霉素(doxorubicin)。
[0021]
本发明上述的用途,所述医药组合物是用于抑制癌细胞中p-glycoprotein蛋白质的活性。
[0022]
为达到上述及其它目的,以下对本发明一个或多个具体实施例进行说明。本发明的其它特征或优点以实施例及请求项详细描述。
附图说明
[0023]
图1显示将何首乌水萃取物的活性成分四羟基二苯乙烯-2-o-β-d葡萄糖苷(thsg,2,3,5,4'-tetrahydroxyl-stilbene-2-o-beta-d-glucoside)修饰其官能基后的产物tg-1(2,3,5,4'-tetrahydroxy-trans-stilbene,2,3,5,4
’–
四羟基二苯乙烯)和白藜芦醇(resveratrol,rsv)的化学式。
[0024]
图2a及2b显示将产物tg-1(2,3,5,4'-tetrahydroxy-trans-stilbene)溶于meod中〈约0.4毫升〉,置入核磁共振测量管内,室温下于dpx-200核磁共振仪上进行测定的1h-nmr、13c-nmr谱图。
[0025]
图3显示四羟基二苯乙烯-2-o-β-d葡萄糖苷(thsg)、tg-1、白藜芦醇(resveratrol)在不同浓度的细胞存活率,取得三种不同药物的ic
50
值(即毒杀50%的乳腺癌细胞的浓度值),其结果显示四羟基二苯乙烯-2-o-β-d葡萄糖苷(thsg)需要较高的药物浓度方能毒杀50%的乳腺癌细胞,与tg-1和白藜芦醇(resveratrol)所需的药物浓度差距甚大,约有3.5倍。
[0026]
图4为显示tg-1(2,3,5,4'-tetrahydroxy
–
trans-stilbene)和抗癌药物欧洲紫杉醇(docetaxel)合并使用具有加乘作用,结果显示当数据显示当抗癌药物与tg-1的比例为1:5、1:10、1:20下皆具有拮抗作用的效果,其中在1:5与1:10的比例下所计算出的combination index(ci,联合用药指数)低于0.6,表示两种药物以上述两种比例合并使用时,具有较好的加乘作用。
[0027]
图5显示将抗癌药物欧洲紫杉醇(docetaxel,dtx)分别与四羟基二苯乙烯-2-o-β-d葡萄糖苷(thsg)、tg-1、白藜芦醇(resveratrol)合并使用,并且以dtx:thsg、dtx:tg-1、dtx:resveratrol为1:5的比例于浓度的组别(a组:dox(阿霉素,doxorubicin)为0.25um、b
组:dox为0.5um、c组:dox为1um)下相互比较的细胞存活率试验,即a,b,c组分别加入不同浓度阿霉素(dox)促进癌细胞产生抗药性,再以抗癌药物dtx与thsg,tg1,resveratrol用1:5的比例合并治疗,测定细胞存活率。
[0028]
图6显示将抗癌药物欧洲紫杉醇(docetaxel)分别与四羟基二苯乙烯-2-o-β-d葡萄糖苷(thsg)、tg-1、白藜芦醇(resveratrol)合并使用结果,显示抗癌药物dox合并tg-1在1:5的比例下所计算出的combination index(ci)皆低于0.5且皆优于其他两种分子,表示此抗癌药物合并tg-1合并使用上更具有优势及进步性。
[0029]
图7显示将抗癌药物欧洲紫杉醇(docetaxel)分别与四羟基二苯乙烯-2-o-β-d葡萄糖苷(thsg)、tg-1、白藜芦醇(resveratrol)合并使用,并且以dtx:thsg、dtx:tg-1、dtx:resveratrol为1:10的比例于浓度的组别(d组:dox(阿霉素)为0.25um、e组:dox为0.5um、f组:dox为1um)下相互比较的细胞存活率试验,即d,e,f组分别加入不同浓度阿霉素(dox)促进癌细胞产生抗药性,再以抗癌药物dtx与thsg,tg1,resveratrol用1:10的比例合并治疗,测定细胞存活率。
[0030]
图8显示将抗癌药物欧洲紫杉醇(docetaxel)分别与四羟基二苯乙烯-2-o-β-d葡萄糖苷(thsg)、tg-1(2,3,5,4'-tetra hydroxy-trans-stilbene)、白藜芦醇(resveratrol)合并使用结果,显示抗癌药物dox合并tg-1在1:10的比例下的combination index(ci)更是低于0.3且皆优于其他两种分子,表示此抗癌药物dox与tg-1合并使用,更具有优势及进步性。
[0031]
图9a至9c显示针对乳腺癌细胞(mcf-7)合并使用tg-1和抗癌药物的细胞存活率测试与药物合并指数(ci)计算结果。
[0032]
图10a至10c显示针对抗药性乳腺癌细胞(mcf-7/adr)合并使用tg-1和抗癌药物的细胞存活率测试与药物合并指数(ci)计算结果。
[0033]
图11a至11b显示针对抗药性乳腺癌细胞(mcf-7/adr)合并使用tg-1和抗癌药物的p-glycoprotein(p-gp)药物帮浦表达量测试结果。
[0034]
图12显示针对抗药性肺癌细胞(a549)合并使用tg-1和抗癌药物的细胞存活率测试结果。
[0035]
图13显示针对抗药性大肠癌细胞(sw480)合并使用tg-1和抗癌药物的细胞存活率测试结果。
[0036]
图14a显示tg-1抑制乳腺癌细胞产生抗药性试验。乳腺癌细胞分别加入抗癌药物欧洲紫杉醇(dtx)、欧洲紫杉醇(dtx)及100nm tg1、欧洲紫杉醇(docetaxel,dtx)及200nm tg1,作用1周后,抗药性帮浦蛋白p-gp(运输蛋白,p-glycoprotein pumps)表达量。
[0037]
图14b显示tg-1抑制乳腺癌细胞产生抗药性试验。乳腺癌细胞分别加入抗癌药物欧洲紫杉醇(dtx)、欧洲紫杉醇(dtx)及100nm tg1、欧洲紫杉醇(dtx)及200nm tg1,作用2周后,抗药性帮浦蛋白p-gp(p-glycoprotein pumps)表达量。
[0038]
图14c显示tg-1抑制乳腺癌细胞产生抗药性试验。乳腺癌细胞分别加入抗癌药物欧洲紫杉醇(dtx)、欧洲紫杉醇(dtx)及100nm tg1、欧洲紫杉醇(dtx)及200nm tg1,作用3周后,抗药性帮浦蛋白p-gp(运输蛋白p-glycoprotein pumps)表达量。
[0039]
图14d显示tg-1抑制乳腺癌细胞产生抗药性试验结果。
具体实施方式
[0040]
实施例1tg-1(2,3,5,4'-tetrahydroxy-trans-stilbene)的合成方法
[0041]
在本发明一范畴中,本发明提供一医药组合物,如式i所示。
[0042][0043]
如图1,tg-1(2,3,5,4'-tetrahydroxy-trans-stilbene)的合成方法为将何首乌水萃取物的活性成分thsg(2,3,5,4'-tetrahydroxystilbene-2-o-beta-d-glucoside)修饰其官能基后的产物tg-1,相关的合成方法如步骤(1)-(3)所示。
[0044]
(1)在圆底烧瓶中将thsg〈2.06g,5.62mmol〉溶于乙醇〈50ml〉,加入盐酸〈1.0m,75ml〉,回流加热至摄氏70℃,反应18小时。(2)冷却至常温后使用回旋浓缩仪除去乙醇,水溶液使用乙醚进行萃取,取出乙醚后使用无水硫酸镁除去乙醚中残留的水,过滤去除硫酸镁后使用回旋浓缩仪将乙醚抽干。(3)使用正相管柱层析法纯化产物〈展开溶液为二氯甲烷/甲醇体积比14:1
→
13:1
→
12:1的混合溶液〉,得到最终产物634.2mg,产率为51%。
[0045]
实施例2、使用核磁共振测定tg-1(2,3,5,4'-tetra hydroxy-trans-stilbene)
[0046]
将实施例1制备的产物溶于meod中〈约0.4毫升〉,置入核磁共振测量管内,室温下于dpx-200核磁共振仪上进行测定。1h nmr(200mhz,meod)δppm:7.31,6.72(dt,j=8.5,2.9,1.8hz;j=8.7,2.8,2.0hz 2h;2h,h-2’,h-6’,h-3’,h-5’),7.21,6.90(d,j=16.5hz;j=16.4hz,1h;1h,h-7,h-8),6.45,6.20(d,j=2.7hz;j=2.7hz,1h;1h,h-3,h-5);13c nmr(50mhz,meod)δppm:157.1,150.3,146.5,136.4(c2,c4,c6,c4’),130.1,126.0(c 1,c 1’),128.1,120.7(c7,c8),127.7,115.4(c2’,c3’,c4’,c5’),102.1,101.9(c3,c5)(如图2a及2b所示)。
[0047]
实施例3、tg-1(2,3,5,4'-tetrahydroxy-trans-stilbene)对乳腺癌细胞的影响
[0048]
mcf-7为普遍用于细胞实验的乳腺癌细胞,mcf-7/adr为从mcf-7细胞株培养的具有抗药性的乳腺癌细胞,mcf-7/adr相比于mcf-7细胞株,p-gp药物帮浦有过度表达的现象。
[0049]
实验方法:
[0050]
1)前一天先将乳腺癌细胞培养于24或48孔盘上24小时,细胞数为104cells/well,使癌细胞完全贴附于孔盘
[0051]
2)抽取培养液,加入含有不同浓度的药物的培养液,让细胞与药物在培养箱作用24小时
[0052]
3)抽取培养液,加入含有10%mtt(3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐,噻唑蓝)的培养液,使其在培养箱中且避光反应4小时后取出
[0053]
4)抽取培养液,加入dmso,使紫色结晶溶解呈色,以波长570nm测量其吸光值
[0054]
5)藉由不同组别的吸光值来对比控制组(即不添加任何药物的处理组)的数值,计算出该药物的细胞存活率与ic50
[0055]
实验结果:
[0056]
比较三种不同药物(thsg、tg-1、resveratrol)的ic50,结果显示thsg需要较高的药物浓度才能毒杀50%的乳腺癌细胞,与tg-1和resveratrol所需的药物浓度差距甚大,约有3.5倍之多(如表1和图3所示),thsg经由修饰官能基之后的产物tg-1,对于癌细胞的毒杀能力有其进步性。
[0057]
表1三种不同药物(thsg、tg-1、resveratrol)的ic
50
值。
[0058]
药物ic
50
thsg703.77umtg-1190umresveratrol181um
[0059]
实施例4、tg-1(2,3,5,4'-tetrahydroxy-trans-stilbene)和抗癌药物合并使用的combination index(ci)计算
[0060]
实验方法:
[0061]
1)前一天先将癌细胞培养于24或48孔盘上24小时,细胞数为104cells/well,使癌细胞完全贴附于孔盘
[0062]
2)抽取培养液,加入含有不同浓度的药物的培养液,让细胞与药物在培养箱作用24小时
[0063]
3)抽取培养液,加入含有10%mtt的培养液,使其在培养箱中且避光反应4小时后取出
[0064]
4)抽取培养液,加入dmso,使紫色结晶溶解呈色,以波长570nm测量其吸光值
[0065]
5)藉由不同组别的吸光值来对比控制组(即不添加任何药物的处理组)的数值,计算出该药物的细胞存活率与ic50
[0066]
6)藉由不同组别的吸光值来对比控制组的数值,计算出该比例下合并药物的细胞存活率与ic50
[0067]
7)利用药物合并指数定理(the combination index theorem)公式计算出该药物合并指数(combination index)
[0068]
实验结果:
[0069]
1984年经由周廷潮及塔式(talalay)所提出的药物合并指数定理the combination index theorem,可将药物合并作用分为协同作用(ci<1)、相加作用(ci=1)及拮抗作用(ci>1)。
[0070]
药物合并指数定理的公式如下:
[0071]
d1、d2表示各别药物剂量,p、q分别代表药物与药物间的比例,ed50代表着细胞被毒杀至50%所需的有效药物剂量。
[0072][0073]
[0074][0075]
此定理与公式可应用于癌症治疗上合并多种药物进行分析与讨论,因此我们可以藉由此公式计算出抗癌药物合并tg-1使用上是否具有协同作用,数据显示当抗癌药物与tg-1的比例为1:5、1:10、1:20下皆具有协同作用的效果,其中,在1:5与1:10的比例下所计算出的combination index(ci)低于0.6,表示两种药物合并使用,在上述两种比例下,具有较好的协同作用,使用效果好,(如图4所示)。
[0076]
将抗癌药物欧洲紫杉醇(docetaxel)分别与tg-1、thsg、resveratrol合并使用,并且以1:5与1:10的比例(如表2和表3所示浓度比)下相互比较,结果显示抗癌药物合并tg-1在1:5和1:10的比例下所计算出的combination index(ci)皆低于0.5,且皆优于其他两种分子,在1:10比例下的combination index(ci)更是低于0.3(如图5至图8所示),表示此抗癌药物合并tg-1合并使用更具有优势及进步性。
[0077]
不仅如此,当抗癌药物合并tg-1合并使用能减低抗癌药物的使用剂量,由结果显示,若合并使用tg-1作为治疗,抗癌药物的剂量能够降为原本的二分之一,换句话说,在同样的治疗效果下,将能大幅减轻对人体造成的毒性及副作用。
[0078]
表2.抗癌药物欧洲紫杉醇(docetaxel)分别与tg-1、thsg、resveratrol合并使用,并且以1:5的比例的浓度值。
[0079]
组别docetaxel(简称dtx)thsg/tg-1/rsva0.25um1.25umb0.5um2.5umc1um5um
[0080]
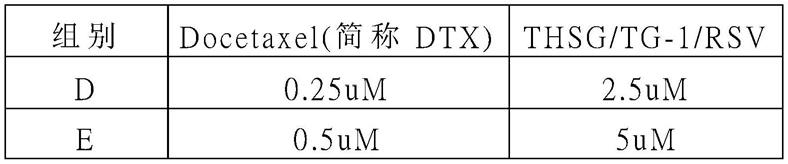
表3.抗癌药物欧洲紫杉醇(docetaxel)分别与tg-1、thsg、resveratrol合并使用,并且以1:10的比例的浓度值。
[0081][0082][0083]
实施例5、针对乳腺癌细胞(mcf-7)合并使用tg-1和抗癌药物的细胞存活率测试与药物合并指数(ci)计算
[0084]
藉由mtt试验结果显示,抗癌药物欧洲紫杉醇(docetaxel,dtx)、阿霉素(doxorubicin,dox),分别与tg-1作合并治疗(摩尔浓度比=1:3),分别与乳腺癌细胞进行反应24小时后的细胞存活率皆大幅度降低,以药物的ic
50
浓度来分析,欧洲紫杉醇
(docetaxel)的浓度能大幅下降至原始ic
50
浓度的25%(如图9a所示),阿霉素(doxorubicin)的浓度亦能下降至原始ic
50
浓度的50%(如图9b所示),以药物合并指数的观点来分析,两者数值均低于0.5,意味着有强烈的协同效应(如图9c所示)。
[0085]
实施例6、针对抗药性乳腺癌细胞(mcf-7/adr)合并使用tg-1和抗癌药物的细胞存活率测试与药物合并指数(ci)计算
[0086]
藉由mtt试验结果显示,抗癌药物欧洲紫杉醇(docetaxel)、阿霉素(doxorubicin),分别与tg-1作合并治疗(摩尔浓度比=1:3),分别与抗药性乳腺癌细胞反应24小时后的细胞存活率皆大幅度降低,相较于先前乳腺癌细胞(mcf-7)的测试结果,使细胞存活率降低的效果更加显著,以药物合并指数的观点来分析,两者数值均低于0.5,意味着有强烈的协同效应(如图10a至10c所示)。
[0087]
实施例7、针对抗药性乳腺癌细胞(mcf-7/adr)合并使用tg-1和抗癌药物的p-glycoprotein(p-gp)药物帮浦表达量测试
[0088]
藉由western blotting分析结果,比较对照组的抗药性乳腺癌细胞与实验组的乳腺癌细胞内p-glycoprotein(p-gp)药物帮浦表达量的差异,结果显示,实验组相较于对照组的药物帮浦表达量较低,证明tg-1有抑制p-glycoprotein(p-gp)药物帮浦表达的效果(如图11a与11b)。
[0089]
实施例8、针对肺癌细胞(a549)合并使用tg-1和抗癌药物的细胞存活率测试
[0090]
藉由mtt试验结果显示,抗癌药物阿霉素(doxorubicin)与tg-1作合并治疗(摩尔浓度比=1:3),与具有p-gp(p-glycoprotein)药物帮浦表达的肺癌细胞(a549)进行反应24小时后的细胞存活率皆明显降低(如图12所示)。
[0091]
实施例9、针对大肠癌细胞(sw480)合并使用tg-1和抗癌药物的细胞存活率测试
[0092]
藉由mtt试验结果显示,抗癌药物irinotecan(伊立替康)与tg-1作合并治疗(摩尔浓度比=1:3),与具有p-glycoprotein(p-gp)药物帮浦表达的大肠癌细胞(sw480)进行反应24小时后的细胞存活率皆明显降低(如图13所示)。
[0093]
实施例10、tg-1(2,3,5,4'-tetrahydroxy-trans-stilbene)抑制癌细胞产生抗药性的功效测试
[0094]
为了证明tg-1具有能够抑制抗药性的功效,利用低剂量的抗癌药物(5nm欧洲紫杉醇(docetaxel,dtx))诱导乳腺癌细胞株(mcf-7)药物帮浦蛋白量的表达,同时加上不同摩尔浓度的tg-1作为培养抗药性细胞的条件。
[0095]
细胞培养:实验组别分别为控制组、5nm欧洲紫杉醇组、5nm欧洲紫杉醇+100nm tg-1组及5nm欧洲紫杉醇+200nm tg-1组,持续细胞培养一周、二周及三周之后藉由西方墨点法(western blotting)方式检测其药物帮浦的表达量多寡。
[0096]
西方墨点法(western blotting):首先,收集各组实验组别的细胞,细胞数至少1
×
106cells/ml,以1500rpm离心3分钟,移出上清液并加入适量体积的细胞裂解缓冲液(cell lysis buffer)于冰上作用0.5~1小时,以12000rpm,4℃离心3分钟后,收集上清液作为后续的蛋白质定量步骤。
[0097]
利用蛋白质定量法(bio-rad protein assay)来定量每组组别的蛋白质,配制五个0.2~0.9mg/ml牛血清蛋白(bovine serum albumin,bsa)作为标准品,描绘出标准曲线;配制适量的样品染料试剂缓冲液(dye reagent buffer)(染料试剂缓冲液:去离子水=1:
4),每组加入1μl的样品与500μl染料试剂缓冲液至微管中混和均匀5分钟,从中再取200μl至96-well孔盘中以酶联免疫检测仪(elisa reader)量测吸光值(595nm),利用标准曲线定量各组蛋白质。
[0098]
配制每一组20μg蛋白质,加入适量去离子水使总体积为7μl,再加入3μl样品缓冲液(sample buffer),混和后放入煮沸的水中10分钟,置于冰上冷却;电泳槽中放置好电泳胶片与加入适量体积的电泳缓冲液(running buffer),每一组样品加入10μl到电泳胶片中,加入5μl双色标准指示标记(dual color standard)到电泳胶片中,以160伏特,作用1小时为电泳的条件。
[0099]
为了使蛋白质与特定抗体进行专一性结合,须利用电流把电泳胶片转渍(转膜)到聚偏氟乙烯膜(pvdf membrane)上。方法为将电泳胶片取出,依据电流方向,配置转渍器(transfer sandwich、转膜器),转渍器中加入适量体积转膜缓冲液(transfer buffer)与冰柱,以0.3安培,在冰上作用1小时为转渍的条件。
[0100]
转膜完成后的聚偏氟乙烯膜再浸泡于5%牛血清蛋白进行封闭(blocking)1小时,随后再浸泡于各适当体积的抗体浓度中搅拌,并于4℃环境中隔夜,隔天再以清洗缓冲液(wash buffer)清洗后接上二级抗体(secondary antibody)
[0101]
为了使影像能够侦测到抗体,聚偏氟乙烯膜须先加上冷光呈色剂(chemiluminescent substrate)进行拍照及影像撷取,再以量化数据软件(image j)作为量化数据的分析。
[0102]
图14a至14c显示了tg-1抑制乳腺癌细胞产生抗药性试验,实验组别包括乳腺癌细胞分别加入抗癌药物欧洲紫杉醇(dtx)、欧洲紫杉醇(dtx)及100nm tg1、欧洲紫杉醇(dtx)及200nm tg1,观测tg1作用1、2以及3周后,抗药性帮浦蛋白p-glycoprotein(p-gp)的表达量。
[0103]
图14d显示乳腺癌细胞株(mcf-7)给予5nm欧洲紫杉醇的药物刺激之后,的确诱导p-gp药物帮浦蛋白的表达量提升,随著作用时间增长,药物帮浦蛋白p-gp表达更明显。而添加100nm与200nm tg-1的组别会抑制p-gp药物帮浦蛋白的表达,尤其在200nm tg-1的组别更是能将p-gp药物帮浦蛋白降低到原始mcf-7乳腺癌细胞株未使用药物刺激的表达量。此外,作用三周的结果显示200nm tg-1的组别能有效抑制p-gp药物帮浦蛋白表达,意味着tg-1具有预防乳腺癌细胞产生抗药性的功效。
[0104]
发明所揭露的所有特征应可以任何结合方式实现。本发明所揭露的每一特征应可以相同、均等或相似目的的取代物所取代。因此,除非有明确的指定,否则所揭露的每一个特征仅仅只是均等物或相似特征的一个种类的一实施例。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1