一种抗肝纤维化的药物组合物及其应用的制作方法
本发明涉及医药技术领域,具体涉及抗肝纤维化的药物组合物及其应用。
背景技术:
世界上有超过10%的人患有慢性肝病,其中肝纤维化患者超过1亿人,每年因肝纤维化死亡的患者超过100万例。肝纤维化是慢性病毒性肝炎、胆汁淤积、药物性肝损伤、寄生虫感染、慢性酒精性肝病及自身免疫性肝炎等病因作用于肝脏,是其炎症损伤再修复过程中的一种代偿反应,是进展至肝硬化的必经之路。肝纤维化被认为具有可逆性的阶段,故成为临床药物干预逆转的最佳时期,延缓、阻止、甚至逆转肝纤维化,对于改善患者肝功能,延缓肝硬化及其并发症的形成,提高患者生活质量,延长患者生存期都有重要的意义。
迄今为止,国内外尚缺乏对肝纤维化治疗的理想方案,还没有一个通过美国食品药品监督管理局(fda)审批的抗肝纤维化药物。由于肝纤维化的分子机制复杂,涉及多条分子通路,单一靶点的药物很难有好的药效。实现肝纤维化的多靶点治疗仍是亟待解决的问题。
技术实现要素:
本发明克服了现有技术中由于肝纤维化的分子机制复杂,涉及多条分子通路,单一靶点的药物很难有好的药效的技术问题,提供天然产物药物组合物在治疗肝纤维化中的应用,通过多靶点作用肝纤维化通路,提高肝脏细胞抗氧化、抗炎、抗纤维化的能力,延缓或逆转肝纤维化进程,从而达到治疗肝纤维化的目的。
为解决上述问题,本发明采取如下技术方案:
一种抗肝纤维化的药物组合物,该组合物是由以下重量份的原料药制备而成的制剂:chitosan1-5份,genistein2-10份,egcg3-15份,taurine20-100份。
原料药中的chitosan(壳聚糖)、genistein(染料木素)、egcg(没食子儿茶素没食子酸酯)和taurine(牛磺酸)均是天然产物;其中,chitosan为从甲壳类动物的表皮中提取的活性成分经脱乙酰作用得到,genistein为槐角、山豆根中提取的活性成分,egcg为从茶叶中提取的活性成分,taurine为从海鱼中提取的活性成分,也可以较经济地化学合成;上述原料药的提取方式是:醇提。
本发明中,进一步地,所述组合物是由以下重量份的原料药制备而成的制剂:chitosan2-4份,genistein4-8份,egcg6-12份,taurine40-80份。
本发明中,进一步地,所述组合物是由以下重量份的原料药制备而成的制剂:chitosan3份,genistein6份,egcg9份,taurine60份。
本发明中,进一步地,所述组合物是由原料药为活性成分,加上药学上常用的辅料或辅助性成分制备而成的适合于临床应用的各种剂型;该制剂包括但不限于:颗粒剂、胶囊剂、片剂、口服液、注射液。
本发明中,进一步地,所述组合物通过以下方法制备而得:
s1:按重量份称取原料药;
s2:取原料药为活性成分,加上药学上常用的辅料或辅助性成分制成适合于临床应用的各种剂型。
本发明的另一目的还在于保护上述一种以抗肝纤维化的药物组合物为活性成分的药物制剂在制备抗肝纤维化药物中的应用。
本发明所述药学上可接受的辅料,是指除活性成分以外包含在剂型中的物质,包括但不仅限于填充剂(稀释剂)、润滑剂(助流剂或抗粘着剂)、分散剂、湿润剂、粘合剂、调节剂、增溶剂、抗氧剂、抑菌剂、乳化剂、崩解剂等。粘合剂包含糖浆、阿拉伯胶、明胶、山梨醇、黄芪胶、纤维素及其衍生物(如微晶纤维素、羧甲基纤维素钠、乙基纤维素或羟丙甲基纤维素等)、明胶浆、糖浆、淀粉浆或聚乙烯吡咯烷酮等;填充剂包含乳糖、糖粉、糊精、淀粉及其衍生物、纤维素及其衍生物、无机钙盐(如硫酸钙、磷酸钙、磷酸氢钙、沉降碳酸钙等)、山梨醇或甘氨酸等;润滑剂包含微粉硅胶、硬脂酸镁、滑石粉、氢氧化铝、硼酸、氢化植物油、聚乙二醇等;崩解剂包含淀粉及其衍生物(如羧甲基淀粉钠、淀粉乙醇酸钠、预胶化淀粉、改良淀粉、羟丙基淀粉、玉米淀粉等)、聚乙烯吡咯烷酮或微晶纤维素等;湿润剂包含十二烷基硫酸钠、水或醇等;抗氧剂包含亚硫酸钠、亚硫酸氢钠、焦亚硫酸钠、二丁基苯酸等;抑菌剂包含0.5%苯酚、0.3%甲酚、0.5%三氯叔丁醇等;调节剂包含盐酸、枸橼酸、氢氧化钾(钠)、枸橼酸钠及缓冲剂(包括磷酸二氢钠和磷酸氢二钠)等;乳化剂包含聚山梨酯-80、没酸山梨坦、普流罗尼克f-68,卵磷酯、豆磷脂等;增溶剂包含吐温-80、胆汁、甘油等。
所述药学上可接受的辅助性成分,它具有一定生理活性,但该成分的加入不会改变上述化合物或衍生物在疾病治疗过程中的主导地位,而仅仅发挥辅助功效,这些辅助功效仅仅是对该成分已知活性的利用,是医药领域惯用的辅助治疗方式。若将上述辅助性成分与本发明化合物配合使用,仍然应属于本发明保护的范围。
申请人根据多年医学工作经验结合无数次医学试验,将本申请药物组分的效果以及于本申请中治疗肝纤维的作用原理简述如下:
chitosan(壳聚糖),作为生物材料具有生物相容性,无毒且无免疫原性,可不同程度地抑制瘢痕形成,参与胆汁酸代谢,降低机体对胆汁酸的吸收,减轻肝脏细胞脂质过氧化对线粒体膜完整性的破坏,保护肝细胞膜,抑制肝细胞凋亡,修复大鼠肝损伤,从而减轻肝纤维化。
genistein(染料木素),具有抗氧化、抑制免疫激活和肝星状细胞增殖的作用,可以浓度依赖性减少由tgf-β1刺激的星状细胞内胶原的合成和细胞外基质的沉积,通过增加肝脏抗氧化酶的活性及表达协同消除自由基,降低α-sma的表达,阻断纤维化细胞因子pdgf的表达,具有体外抗纤维化作用。
egcg(没食子儿茶素没食子酸酯),通过清除hsc细胞内的ros和lpo来降低氧化应激,且egcg通过抑制rho信号通路抑制hsc的生长,egcg能抑制胶原的产生和胶原酶的活性来抑制胶原的合成,egcg还可降低mmps的表达,从而抑制肝纤维化。
taurine(牛磺酸),是一种含硫β-氨基酸,是名贵中药牛黄的主要成分之一,体内广泛存在的自身抗损伤物质,牛磺酸可以促进胆汁排泄,在体外抑制大鼠肝星状细胞,抑制成纤维细胞的增殖和胶原合成,抑制大鼠肝脏细胞外基质的沉积从而减轻肝纤维化程度。有研究表明牛磺酸通过调节no信号传导通路来降低肝内血管阻力,从而调节肝脏血液微循环,改善肝功能从而抑制肝纤维化。
由于采用了上述技术方案,本发明至少包括以下有益效果:
(1)本发明的药物组合物从纤维化的主要病理机制切入,选用chitosan(壳聚糖)、genistein(染料木素)、egcg(没食子儿茶素没食子酸酯)和taurine(牛磺酸)四种天然产物组合,以达到多通路多靶点治疗肝纤维化的目的;其中,chitosan具有降低胆固醇、抑菌、预防和控制高血压以及良好的生物相容性。genistein具有大豆异黄酮的雌激素样作用,抗氧化、抗肿瘤、抑菌、降血脂、抗肝纤维化等药效。egcg是绿茶儿茶素类提取物中最有效的活性成分,是一种含有多个酚羟基的化合物,具有抗病毒、抗氧化、抗动脉硬化、抗血栓形成、抗血管增生、抗菌、抗炎以及抗肿瘤等多重药效,其抗氧化性强于抗坏血酸。taurine是一种由含硫氨基酸转化而来的氨基酸,具有抗炎、降压、降糖、抗心律失常、抗菌、增强免疫功能、利胆、强肝等药效;经研究证实,将chitosan、genistein、egcg和taurine制成复方,通过药物的抗炎、抗坏死和保护肝细胞等方面协同作用,抑制贮脂细胞的增生,减少胶原的合成,促进肝脏修复,调节肝脏血液微循环,达到抗肝纤维化的目的。
(2)本发明的独特性在于,多靶点作用肝纤维化通路,提高肝脏细胞抗氧化、抗炎、抗纤维化的能力,延缓或逆转模型动物的肝纤维化进程,无明显肝毒性,质量稳定可控,来源广泛等特点,在抗肝纤维化上有良好的应用前景。
(3)本发明的药物组合物应用于治疗肝纤维化过程中时,可与其他药物或者药物载体复合制成颗粒剂、胶囊剂、片剂、口服液、注射液等药剂,组成该药剂的各组分的配比具有协同增效效果,功效成分含量高,使用和携带方便,口服吸收迅速,生物利用度高,经过动物试验验证表明防治效果明显。
附图说明
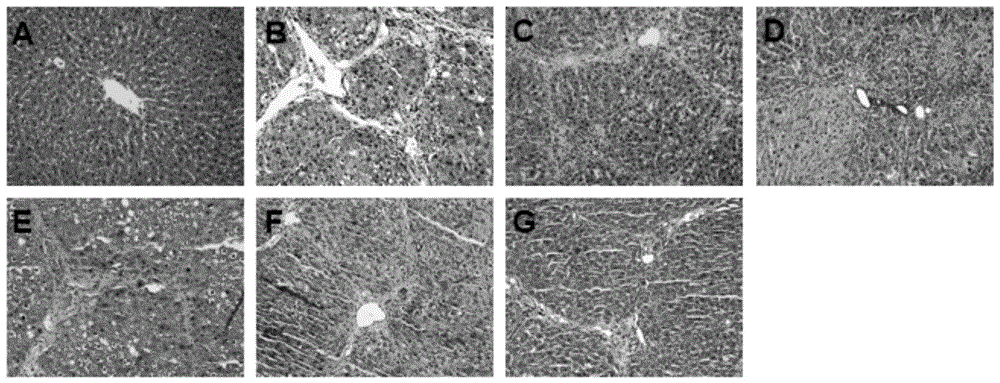
图1为通过七组大鼠肝组织切片he染色观察cget对肝纤维化大鼠肝组织病理结构及肝纤维化程度的影响;
图2为通过七组大鼠肝组织切片siriusred染色观察cget对肝纤维化大鼠肝组织病理结构及肝纤维化程度的影响。
图中,a为对照组,b为模型组,c为药物低剂量a组,d为药物低剂量b组,e为药物低剂量c组,f为药物中剂量组,g为药物高剂量组。
具体附图分析见实验方法。
具体实施方式
下面结合实施例和试验对本发明作进一步说明。
实施例1
本实施例提供一种抗肝纤维化的药物组合物,该组合物是由以下重量份的原料药制备而成的制剂:chitosan1份,genistein2份,egcg3份,taurine20份。
其制备方法,包括如下步骤:
s1:按重量份称取原料药;
s2:取原料药为活性成分,加上药学上常用的辅料或辅助性成分制成适合于临床应用的各种剂型。
本实施例还提供上述一种以抗肝纤维化的药物组合物为活性成分的药物制剂在制备抗肝纤维化药物中的应用。
实施例2
本实施例提供一种抗肝纤维化的药物组合物,该组合物是由以下重量份的原料药制备而成的制剂:chitosan3份,genistein6份,egcg9份,taurine60份。
其制备方法,包括如下步骤:
s1:按重量份称取原料药;
s2:取原料药为活性成分,加上药学上常用的辅料或辅助性成分制成适合于临床应用的各种剂型。
本实施例还提供上述一种以抗肝纤维化的药物组合物为活性成分的药物制剂在制备抗肝纤维化药物中的应用。
实施例3
本实施例提供一种抗肝纤维化的药物组合物,该组合物是由以下重量份的原料药制备而成的制剂:chitosan5份,genistein10份,egcg15份,taurine100份。
其制备方法,包括如下步骤:
s1:按重量份称取原料药;
s2:取原料药为活性成分,加上药学上常用的辅料或辅助性成分制成适合于临床应用的各种剂型。
本实施例还提供上述一种以抗肝纤维化的药物组合物为活性成分的药物制剂在制备抗肝纤维化药物中的应用。
本发明通过如下实验,说明本发明的药物组合物(以下简称cget药物)具有治疗肝纤维化疾病的作用。
1.实验材料
实验动物:6周龄spf级sd大鼠,雄性♂,体质量180-220g,由广西医科大学实验动物中心提供,合格证号:scxk桂2009-0002,使用许可证号:syxk桂2014-0003。安置于湿度50%-70%,温度25±1℃,12小时光照的环境,入实验室适应一周后进行实验。
化学试剂:ccl4、生理盐水;
检测试剂盒:总胆红素(totalbilirubin,tbil)、血清碱性磷酸酶(alkalinephosphatase,alp)、丙氨酸氨基转移酶(alanineaminotransferase,alt)、天冬氨酸氨基转移酶(aspartictransaminase,ast)购自美国abbott公司,委托桂林医学院附属医院检验科检测。
2.实验方法
2.1大鼠肝纤维化造模与给药治疗
随机分为7组,即对照组、模型组(ccl4)、药物低剂量a组(1.25、2.5、3.75、25mg/kg·d)、药物低剂量b组(2.5、5、7.5、50mg/kg·d)、药物低剂量c组(5、10、15、100mg/kg·d)、药物中剂量组(10、20、30、200mg/kg·d)、药物高剂量组(20、40、60、400mg/kg·d);
除正常组给予等体积的生理盐水外,其余6组大鼠均经口灌胃40%四氯化碳(溶于玉米油)连续8周,每周2次,复制大鼠肝纤维化模型。造模后第二天开始灌胃,其中,药物低剂量a组给予chitosan:1.25mg/kg·d、genistein:2.5mg/kg·d、egcg:3.75mg/kg·d、taurine:25mg/kg·d;药物低剂量b组给予chitosan:2.5mg/kg·d、genistein:5mg/kg·d、egcg:7.5mg/kg·d、taurine:50mg/kg·d;药物低剂量c组给予chitosan:5mg/kg·d、genistein:10mg/kg·d、egcg:15mg/kg·d、taurine:100mg/kg·d;药物中剂量组给予chitosan:10mg/kg·d、genistein:20mg/kg·d、egcg:30mg/kg·d、taurine:200mg/kg·d;药物高剂量组给予chitosan:20mg/kg·d、genistein:40mg/kg·d、egcg:60mg/kg·d、taurine:400mg/kg·d;同时模型组和空白组给予等体积的生理盐水,连续8周。
2.2血清肝功能检测
于末次给药及生理盐水后24h,水合氯醛麻醉大鼠,之后腹主动脉取血后处死大鼠,分离血清,分装后置于-80℃冰箱中,供生化指标分析。取大鼠血清,分别用谷丙转氨酶(alt)、谷草转氨酶(ast)、血清碱性磷酸酶(alp)生化试剂盒检测各组alt、ast、alp的水平,并取平均值。
2.3肝脾指数及胶原面积百分比检测
a.计算肝脏、脾脏指数
于末次给药及生理盐水后24h,麻醉大鼠,称重之后处死大鼠,完整剥离肝脏、脾脏,将肝脏、脾脏分别置于冷的生理盐水中清洗后,称重;分别计算各组每次测得的肝脏指数、脾脏指数,并取平均值;
上述,肝指数=肝脏湿质量/体质量×100%;脾指数=脾脏湿质量/体质量×100%;
b.计算胶原面积百分比
取经上述方式处死后的大鼠肝右叶,于4%多聚甲醛溶液中固定,石蜡包埋,切片行siriusred染色,切片扫描,aperioimagescope12.3计算胶原面积百分比并取平均值;
上述,胶原面积百分比=切片中胶原染色面积/切片中肝脏组织面积×100%。
2.4肝组织病理学观察
取部分肝组织用4%多聚甲醛固定,将其切成约3mm×5mm×5mm大小,用石蜡包埋,4μm连续切片。用二甲苯脱蜡,用乙醇梯度脱水处理后用自来水、蒸馏水漂洗至水化。he染色,水洗,脱水透明封片;于光学显微镜下观察组织结构。
3.实验结果
注:统计学处理:数据用平均值±标准差的形式表示,结果使用方差分析,显著性检验均使用spss19.0中的t检验,以p<0.05为有显著性差异。
3.1血清肝功能检测
七组大鼠血清alt、ast及alp水平如表1所示:
表1各组大鼠血清中alp、alt、ast含量测定结果(x±s)
注:*与对照组对比,p<0.05
#与模型组对比,p<0.05
根据表1可知,模型组alp、alt和ast水平较空白组均明显上升,差异有统计学意义(p<0.05);随着cget药物量的增加,alp呈下降趋势。而alt和ast指标中,药物量过大过小,下降均不明显。表明在药物低剂量c组、药物中剂量组、药物高剂量组剂量下cget药物降低ccl4模型大鼠的alp值较模型组有统计学意义(p<0.05)。五组药物均可降低大鼠的alt指标,且与ccl4比较有统计学意义。在药物低剂量c组和药物中剂量组剂量下,cget药物降低ccl4模型大鼠的ast值较模型组有统计学意义(p<0.05);表示cget药物能够降低大鼠血清alt,ast,alp水平,有助于减轻大鼠肝损伤。
3.2肝脾指数及胶原面积百分比检测
七组大鼠肝脏指数(liverindex)、脾脏指数(spleenindex)及胶原蛋白面积百分比如表2所示:
表2各组大鼠肝脾指数及胶原面积百分比(x±s)
注:*与对照组对比,p<0.05
#与模型组对比,p<0.05
ccl4大鼠模型中肝脏指数以下降为主,加用cget后肝脏指数升高,药物低剂量c组、药物中剂量组、药物高剂量组与对照组比较,差异无统计学意义(p>0.05);其中药物低剂量c组和药物高剂量组与模型组比较,差异有统计学意义(p<0.05);
ccl4大鼠模型中脾脏指数以上升为主,加用cget后脾脏指数升高,药物低剂量a组、药物低剂量b组、药物低剂量c组与对照组比较,差异无统计学意义(p>0.05);
根据全切片扫描软件计算染色区域纤维化的面积,模型组胶原面积显著升高,较对照组差异有统计学意义(p<0.05),所有cget组胶原面积均有所下降,较模型组对比,差异均有统计学意义(p<0.05),表2。
3.3肝组织病理学观察
如图1所示,对各组肝组织he染色观察,a组肝小叶结构完整,无细胞变性及炎性细胞浸润;b、c肝小叶结构紊乱,胶原增生形成假小叶,大量肝细胞变性,中性粒细胞浸润;d-g肝小叶结构略紊乱,肝细胞变性较模型组显著减少,胶原增生未见假小叶,有肝细胞变性,较b、c组减少,有少量炎细胞浸润。
如图2所示,对各组肝组织进行siriusred染色观察,a肝小叶结构完整,无胶原增生;b、c肝小叶结构紊乱,大量胶原(红色)增生形成假小叶且胶原面积大;d-g肝小叶结构略紊乱,胶原增生面积较b、c组明显减少。
根据图1-2综合分析可知:cget药物给药组(c-g组)肝细胞变性明显减轻,少量纤维增生,炎细胞浸润减少,无明显假小叶形成。表明cget药物对肝纤维化有明显改善作用。而由于c组剂量过低导致改善效果不明显。
上述说明是针对本发明较佳可行实施例的详细说明,但实施例并非用以限定本发明的专利申请范围,凡本发明所提示的技术精神下所完成的同等变化或修饰变更,均应属于本发明所涵盖专利范围。
- 还没有人留言评论。精彩留言会获得点赞!