一种基于液态金属的可视化载药栓塞微球及其制备方法与流程
本发明属于医用材料技术领域,特别涉及一种基于液态金属的可视化载药栓塞微球及其制备方法。
背景技术:
介入治疗是近年来发展起来的新兴领域,它是在影像设备引导下的一种微创医疗技术,具有创伤小、恢复快、疗效好等特点。经导管动脉栓塞术是介入治疗的重要技术,它是将栓塞材料有控制的注入到病变器官的供应血管中,以此阻止血液流动,导致肿瘤组织部分缺少氧气和养料供应,以达到治疗肿瘤及清除病变器官的目的。
目前,临床上常用的栓塞微球主要有dcbead、hepasphere、callispheres等,但是,他们普遍存在显影效果差、载药量小、载药单一等问题。
技术实现要素:
为了克服上述现有技术的缺点,解决目前载药栓塞微球存在的问题,本发明的目的在于提供一种基于液态金属的可视化载药栓塞微球及其制备方法,其通过液态金属和壳聚糖和抗肿瘤药物的优化组合,可以经导管注入血管中,有效堵塞血管中血液的流动,并且微球中包载的抗肿瘤药物在肿瘤治疗中具有一定的辅助作用。此外,本发明的可视化载药栓塞微球具有dsa或ct下显影的特性,有利于实时观测微球在血管中的栓塞效果。
为了实现上述目的,本发明采用的技术方案是:
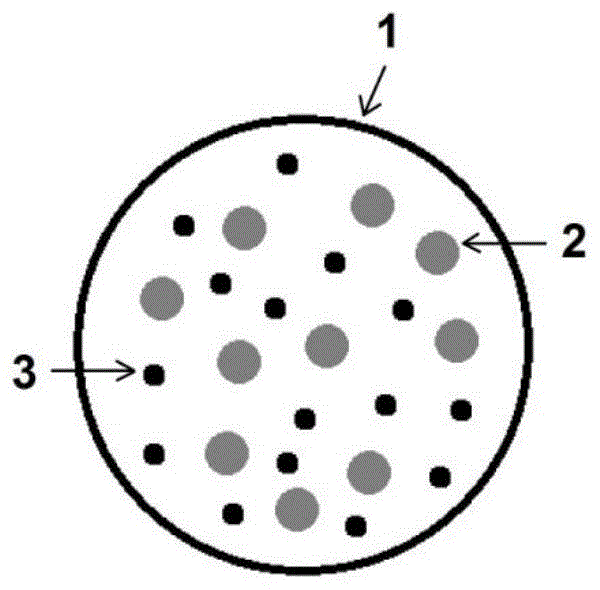
一种基于液态金属的可视化载药栓塞微球,包括壳聚糖材料1和被壳聚糖材料1包裹的液态金属纳米颗粒2和抗肿瘤药物3。壳聚糖材料1生物相容性好,载药能力强,载药谱广,而以镓为代表的液态金属纳米颗粒2具有不低于一般金属的x射线吸收系数,因此在dsa拍摄或ct扫描中,基于液态金属的载药栓塞微球会与周围组织形成鲜明对比,达到优异的显影效果,有利于对栓塞效果的实时评估,因此该可视化载药栓塞微球可用于肿瘤辅助治疗中的血管栓塞,且具有良好的缓释效果。
所述液态金属纳米颗粒2、壳聚糖材料1和抗肿瘤药物3的质量比为1:(10~100):(0.5~2)。
所述抗肿瘤药物3为小分子抗肿瘤药物、抗肿瘤血管生成药物或免疫治疗药物,所述小分子抗肿瘤药物为阿霉素、甲氨蝶呤或吉西他滨;所述抗肿瘤血管生成药物为贝伐珠单抗、雷莫芦单抗、阿帕替尼、索拉非尼、舒尼替尼、阿西替尼或帕唑帕尼;所述免疫治疗药物为pd-1免疫治疗剂、ido抑制剂、精氨酸酶抑制剂、腺苷a2a受体拮抗剂、rorγt激动剂、趋化因子受体抑制剂、转化生长因子β(tgf-β)、t细胞活化的免疫球蛋白抑制v型结构域(vista)抑制剂、sting激动剂、toll样受体激动剂中的一种或多种。
所述液态金属选择熔点临近室温的液态金属,如熔点在15~30℃的液态金属,优选金属镓单质或基于金属镓的合金,如镓铟合金。
本发明还提供了所述基于液态金属的可视化载药栓塞微球的制备方法,包括如下步骤:
(1)制备液态金属纳米颗粒溶液:在壳聚糖水溶液中加入液态金属,超声分散,离心去除大颗粒,制得纳米形式的均匀分散的液态金属纳米颗粒溶液;
(2)制备基于液态金属的可视化载药栓塞微球:先将壳聚糖水溶液和分散剂加入油相中搅拌,再加入均匀分散好的液态金属纳米颗粒溶液和抗肿瘤药物进行搅拌,最后加入溶解在水相中的交联剂反应即得。
所述步骤(1)中,超声分散10min以上,得到纳米级的液态金属颗粒,粒径大小直径500-800nm;所述(2)中,设置温度30~40℃,搅拌速率100~1000rpm,加入交联剂后反应0.5~2h。
所述步骤(1)和(2)中,壳聚糖水溶液的质量浓度均为1~5%,用量之比为1:2~4,整个流程中所用的液态金属纳米颗粒(2)、壳聚糖材料(1)和抗肿瘤药物(3)的质量比为1:(10~100):(0.5~2)。
所述步骤(2)中,设置温度30~40℃,搅拌速率100~1000rpm,加入交联剂后反应0.5~2h。
所述(2)中,分散剂为失水山梨糖醇脂肪酸酯,用量约为0.1重量份;所述交联剂为三聚磷酸钠、京尼平或β-甘油磷酸钠,浓度为0.1g/ml,用量0.1~1重量份。
在所述步骤(2)之后,将得到的微球经离心去除反应溶剂,再经多次水、乙醚、乙醇等溶剂洗涤,去除交联剂和分散剂,并烘干备用。
本发明用于肿瘤辅助治疗中的血管栓塞的方法,包括:使用上述的可视化载药栓塞微球,在肿瘤血管中经导管注射堵塞肿瘤血管,从而阻止血液流动对肿瘤组织的氧气和养料供应。该可视化载药栓塞微球具有dsa或ct下显影的特性,有利于实时观测微球在血管中的栓塞效果。
与现有技术相比,本发明采用壳聚糖作为液态金属和抗肿瘤药物的包裹材料,制备的微球具有优良的生物相容性,更重要的是液态金属具有dsa或ct下显影的特性,更有利于判断微球使用过程中在血管中的位置、分布情况以及栓塞的效果等。
附图说明
图1为本发明所述的可视化载药栓塞微球的结构示意图。
图中:1为壳聚糖材料,2为液态金属纳米颗粒,3为抗肿瘤药物。
具体实施方式
下面结合附图和实施例详细说明本发明的实施方式,但不用来限制本发明的范围。
一种基于液态金属的可视化载药栓塞微球,由如下重量份的组分制得:液态金属(egain,金属镓与金属铟的质量比为75.5:24.5)1份,壳聚糖水溶液50份,抗肿瘤药物1份,所得产品为固体粉末,如图1所示,液态金属纳米颗粒2和抗肿瘤药物3由固态的壳聚糖材料1包裹。
其制备方法,包括:
(1)制备液态金属纳米溶液:在壳聚糖水溶液50ml中加入液态金属1g,超声分散,离心去除大颗粒,制得纳米形式的均匀分散的液态金属纳米颗粒溶液,其中液态金属浓度为0.02g/ml。
(2)制备基于液态金属的可视化载药栓塞微球:先将壳聚糖水溶液和分散剂加入油相中搅拌,设置温度30℃,搅拌速率100rpm,再将均匀分散好的液态金属纳米颗粒溶液和抗肿瘤药物阿霉素加入溶液中搅拌,设置温度30℃,搅拌速率100rpm,最后将交联剂溶解在水相中加入上述溶液中,设置温度30℃,搅拌反应1h。
(3)将步骤(2)得到的微球经离心去除反应溶剂,再经多次水、乙醚、乙醇等溶剂洗涤,去除交联剂和分散剂,37℃烘干48h,备用。
在上述方法中,采用了物理交联法,利用壳聚糖和交联剂进行交联形成微球,该方法制备条件温和,操作简单,所得可视化载药栓塞微球的粒径为10~700μm,可通过微球制备过程中的搅拌速率控制微球尺寸。
使用制备所得的可视化载药栓塞微球,在兔子肝癌模型中经导管注射到肿瘤血管中,一方面,微球可进行血管栓塞,阻止血液流动对肿瘤组织的氧气和养分供应;另一方面,微球中包载的抗肿瘤药物可以缓慢释放到肿瘤组织中,杀死肿瘤细胞。该微球可以起到肿瘤栓塞治疗和化疗协同治疗的作用。经该微球治疗后,可以导致部分肿瘤细胞被杀死或肿瘤组织缺血性坏死。
并且,该可视化载药栓塞微球具有dsa透视或ct下显影的特性,有利于实时观测微球在血管中的栓塞位置和栓塞情况,以及时评估疗效,补充栓塞。同时,载药微球可以在血管中缓慢释放抗肿瘤药物,协助肿瘤的栓塞治疗。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!