预测前列腺癌发生和转移发生的装置的制作方法
本发明涉及一种用于预测前列腺癌发生和预测前列腺癌淋巴转移发生的装置,属于生物医疗领域。
背景技术:
在世界范围内,前列腺癌的发病率和死亡率在男性中跃居第一和第二位,占据主要地位。而在前列腺癌的早期筛查中往往会经历三个阶段:1)psa+直肠指诊,2)经直肠超声、ct、多参数磁共振(mpmri)等影像学检查,3)超声引导下的前列腺穿刺活检。在nccn指南及acp临床指南指出,穿刺活检往往会带来一些血尿,感染等并发症,风险较高。因此,对于前列腺穿刺活检在早期可疑前列腺癌病人筛查中的应用需持谨慎态度。
中国专利文献cn102968558b(申请号:201210457389.3)是一种预测初诊前列腺癌骨转移风险的装置,其通过临床分期变量、gleason评分变量、psa(前列腺特异抗原)值变量以及年龄变量计算前列腺癌会发生骨转移的预测风险值。
近年研究提示,脂肪组织尤其前列腺周围脂肪与前列腺癌的进展密切相关,《naturecommunication》杂志一文中提及前列腺周围脂肪组织可能作为一种驱动因子促进前列腺癌的发生发展,但是前列腺周围脂肪形状并不规则,无法直接作为早期辅助诊断前列腺癌的工具。
技术实现要素:
本发明要解决的技术问题是,提供一种无需穿刺活检,即可预测前列腺癌发生和转移发生的装置。
本发明为解决上述技术问题提出的一种技术方案是:一种预测前列腺癌发生和转移发生的装置,包括医学影像成像装置、处理装置和输出装置;
所述医学影像成像装置,拍摄人体前列腺和膀胱处的立体图像;
所述处理装置,连接所述医学影像成像装置,选择矢状面图像中经过膀胱底部的层面,获得该层面处的横断面图像,在所述横断面图像中识别前列腺周围脂肪外轮廓和前列腺外轮廓,计算前列腺周围脂肪面积ppfa=前列腺周围脂肪外轮廓内的面积-前列腺外轮廓内的面积,计算前列腺面积pa=前列腺外轮廓内的面积,获得前列腺周围脂肪面积与前列腺面积的比值ppfa/pa;
所述输出装置,连接所述处理装置,输出前列腺周围脂肪面积与前列腺面积的比值ppfa/pa,前列腺癌发生和转移发生的风险值与比值ppfa/pa成正比。
上述处理装置基于年龄变量,直肠指诊变量,家族遗传史变量,前列腺影像报告和数据系统评分变量,psa值变量,前列腺周围脂肪面积与前列腺面积的比值变量,根据公式计算得到初诊患前列腺癌的风险值,所述输出装置输出初诊患前列腺癌的风险值,所述公式如下:
logit(p)=in(p/(1-p))=1.037*age+coefdre+coefhistory+1.033*psa+coefpirads+1.066*(ppfa/pa),
其中,p表示患前列腺癌风险预测值,age表示年龄变量,coefdre表示直肠指诊变量,coefhistory表示家族遗传史变量,coefpirads表示前列腺影像报告和数据系统评分变量,psa表示前列腺特异抗原值变量,ppfa/pa表示前列腺周围脂肪面积与前列腺面积的比值变量。
上述处理装置基于术前依据mri诊断淋巴结转移可能性变量,前列腺影像报告和数据系统评分变量,前列腺周围脂肪面积与前列腺面积的比值变量,gleason评分变量,病理t分期变量,psa值变量,ki-67表达水平变量,根据公式计算得到前列腺癌患者淋巴结转移的风险值,所述输出装置输出前列腺癌患者淋巴结转移的风险值,所述公式如下:
logit(p)=in(p/(1-p))=coefpre-lnm+coefpirads+coefratio+coefgs+coefpt-stage+1.008*psa+1.152*ki-67,
其中,p表示患前列腺癌淋巴结转移风险预测值,coefpre-lnm表示术前依据mri诊断淋巴结转移可能性变量,coefpirads表示前列腺影像报告和数据系统评分变量,coefratio表示前列腺周围脂肪面积与前列腺面积的比值变量,coefgs表示gleason评分变量,coefpt-stage表示病理t分期变量,psa表示psa值变量,coefki-67表示ki-67表达水平变量。
上述矢状面是正中矢状面。
上述医学影像成像装置是核磁共振成像装置。
本发明要解决的技术问题是,提供一种预测前列腺癌发生的生物标志物。
本发明为解决上述技术问题提出的一种技术方案是:前列腺周围脂肪面积与前列腺面积的比值ppfa/pa作为前列腺癌发生的生物标志物的应用。
本发明为解决上述技术问题提出的另一种技术方案是:前列腺周围脂肪面积与前列腺面积的比值ppfa/pa联合年龄参数、直肠指诊参数、家族遗传史参数、psa值参数、pirads评分参数作为预测前列腺癌发生的应用。
本发明要解决的技术问题是,提供一种预测前列腺癌转移发生的参数。
本发明为解决上述技术问题提出的一种技术方案是:前列腺周围脂肪面积与前列腺面积的比值ppfa/pa作为预测前列腺癌转移发生的参数的应用。
本发明为解决上述技术问题提出的另一种技术方案是:前列腺周围脂肪面积与前列腺面积的比值ppfa/pa联合pre-lnm参数、pirads评分参数、psa值参数、gleason评分参数、pt-stage参数和ki-67表达水平参数作为预测前列腺癌转移发生的应用。
本发明具有积极的效果:本发明通过测量特殊位置处,前列腺周围脂肪和前列腺的面积,得到前列腺周围脂肪面积与前列腺面积比值ppfa/pa,该比值可以单独作为预测前列腺癌发生和前列腺癌转移发生风险的可靠指标,可以联合年龄、直肠指诊、家族遗传史、psa值、pirads等参数提高预测前列腺癌发生风险的准确度,可以联合pre-lnm、psa值、gleason评分、pt-stage等级和ki-67表达水平等参数提高预测前列腺癌转移发生风险的准确度。本发明仅通过影像学资料,识别图像轮廓,计算相应的面积,即可得到有助于预测前列腺癌发生和前列腺癌转移发生风险的指标,减少不必要的穿刺,进而减少穿刺相关并发症血尿、感染等发生风险。ppfa/pa与psa联用能显著提高前列腺癌的检出率,对临床上前列腺癌的早期诊断和监控病情发展具有很好的参考价值。以ppfa/pa为重要组成参数建立前列腺癌的预测模型,较好的避免穿刺带来的风险,可达到节约医疗资源的目的,可为临床决策提供辅助信息。
附图说明
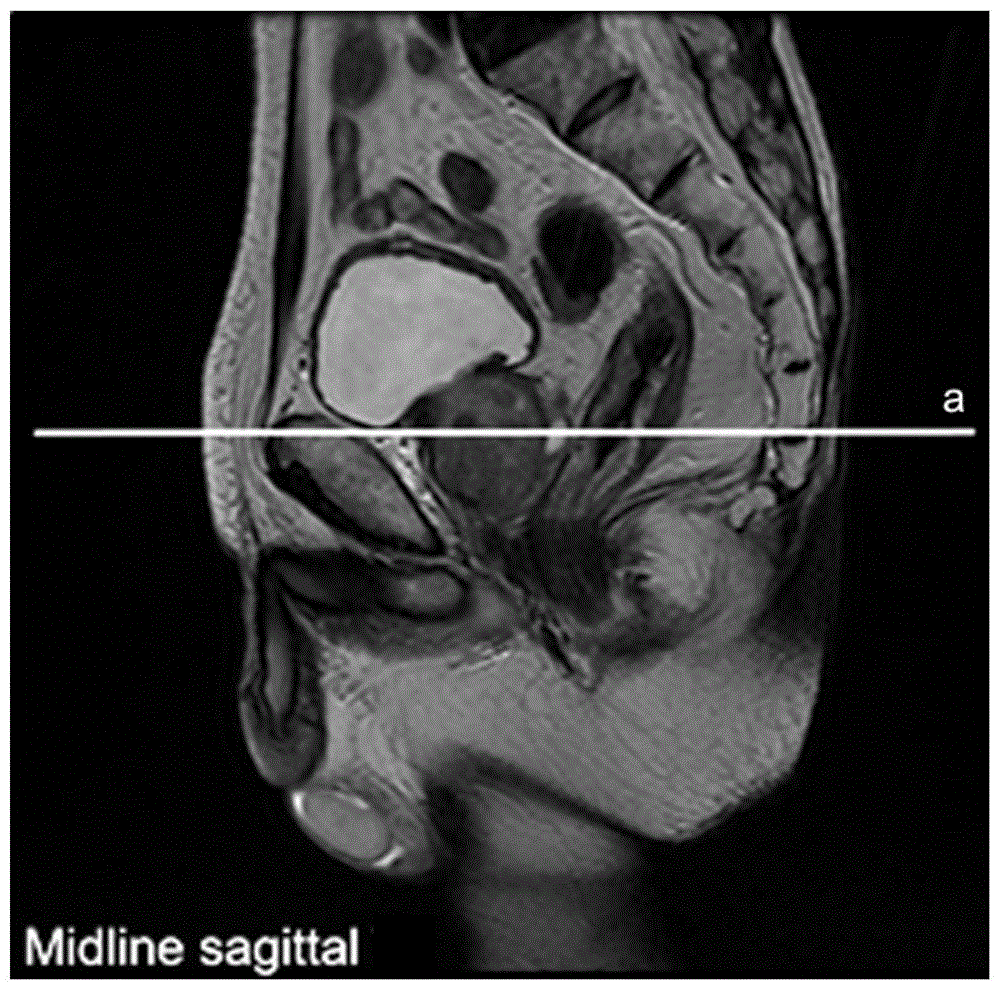
图1为本发明实施例的660例患者中的某一位的磁共振成像图;
图2为图1中的水平层面a的磁共振成像图;
图3为660例患者的ppfa与前列腺癌恶性程度的相关性分析图;
图4为660例患者的ppfa/pa与前列腺癌恶性程度的相关性分析图;
图5为343例前列腺癌患者的ppfa与gleason评分的相关性分析图;
图6为343例前列腺癌患者的ppfa/pa与gleason评分的相关性分析图;
图7为模型a、b、c、d预测前列腺癌发生的效应曲线;
图8为模型a、b、c、d预测有意义的前列腺癌发生的效应曲线;
图9为ppfa/pa联合其他指标预测前列腺癌发生的nomogrm图;
图10为前列腺癌发生预测模型的准确度的校正曲线;
图11为前列腺癌发生预测模型的准确度的roc曲线;
图12为前列腺癌发生预测模型预测风险的效应决策曲线;
图13为179例患者ppfa/pa与gleason评分的相关性分析图;
图14为179例患者ppfa/pa与t分期的相关性分析图;
图15为ppfa/pa在前列腺癌淋巴结转移和非淋巴结转移组间的差异性分析图;
图16为ppfa/pa在前列腺癌骨转移与非骨转移组间的差异性分析图;
图17为ppfa指标单独预测前列腺癌转移发生的效应曲线;
图18为ppfa/pa指标单独预测前列腺癌转移发生的效应曲线;
图19为ppfa/pa联合其他指标预测前列腺癌转移发生的nomogrm图;
图20为前列腺癌转移发生预测模型的准确度的校正曲线;
图21为前列腺癌转移发生预测模型的准确度的roc曲线;
图22为前列腺癌转移发生预测模型预测风险的效应决策曲线。
具体实施方式
下面通过实施例对本发明进行具体的描述,有必要在此指出的是以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,该领域的技术人员可以根据上述本发明内容对本发明作出一些非本质的改进和调整。除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。age表示年龄;dre表示直肠指诊;history表示家族遗传史;psa表示前列腺特异抗原;pca表示前列腺癌;bmi表示身体质量指数;chd表示冠心病;htn表示高血压;psa表示前列腺特异抗原;pv表示前列腺体积;ppfa表示前列腺周围脂肪面积;pa表示前列腺面积;pirads表示前列腺影像报告和数据系统评分;bph表示良性前列腺增生;pin表示前列腺上皮内瘤变;cs-pca表示有临床意义的前列腺癌;lnm表示淋巴结转移;pre-lnm表示依据mri诊断的前列腺癌转移可能性;gs表示gleason评分;ihc表示免疫组化;auc表示roc曲线下的面积;ratio表示前列腺周围脂肪面积与前列腺面积的比值ppfa/pa;pt-stage表示病理t分期。
实施例
本实施例对上海市第十人民医院以及克拉玛依中心医院共660例疑似前列腺癌患者的病例进行分析,其中179例进行前列腺癌根治手术。
mri检查方法如下:采用德国西门子2.0t磁共振扫描仪,t1wi快速自旋回波fse加权成像矩阵250×250,层厚3mm,fov220mm。如图1所示,选取的mri层面为矢状面图像中经过膀胱底部的层面a。与之对应的横断面图像如图2所示,图2中的前列腺周围脂肪外轮廓b是前列腺周围脂肪的外轮廓,前列腺外轮廓c是前列腺面积pa的外轮廓。优选的技术方案是采用自动图像识别软件,根据各轮廓边缘的灰度值不同,自动识别。或者通过软件手动进行选取。
手动选取的计算方法如下:影像系统中下载该层面对应dicom格式的mri图像,用图像处理软件imagejversion1.51k(nationalinstituteforhealth,bethesda,md)打开图像,使用“polygonselections”功能分别勾画相应ppfa和pa外轮廓,然后点击“analyze”→“measure”功能分别计算两者外轮廓内的面积。
图2中的外轮廓线b内的面积为35.9cm2,外轮廓线c内的面积为18.7cm2,所以前列腺周围脂肪面积(ppfa)=35.9–18.7=17.2cm2,前列腺面积(pa)=18.7cm2。
所有患者均施行经直肠超声前列腺穿刺活检。每次均由同一医师执行,细针穿刺12针后送病理科行病理检查,经过固定、脱水、浸腊、包埋、切片、封片等过程,将所收集的组织制作成病理切片,由两名以上的病理医师对所取组织的病理性质进行诊断。最后通过两位病理科医生判断,根据直肠穿刺结果确定患者类型并分为未患前列腺癌组、前列腺癌组和增生组。
统计学分析方法如下:采用spss20.0软件进行统计学分析,计量资料用mean±sd表示,两组比较采用t检验,计数资料用例数表示,组间比较用χ2检验。进一步用logistic回归对差异性因素进行多因素分析,筛选出潜在的独立影响因素。同时,建立roc曲线,分析ppfa与psa单独诊断前列腺癌的价值。同时进一步利用logistic回归建立联合诊断模型,探索联合诊断前列腺癌的价值。以p<0.05被认为差异具有统计学意义。
患者入院时,详细记录患者的临床基线资料并建立档案,记录患者的身高、体重、年龄、既往病史。660例疑似前列腺癌病例的临床基线资料如表1所示。
表1660例疑似前列腺癌病例的临床基线资料
其中*除特殊说明外各指标均以人数(占总人数百分比)表示,
在660例患者中,将前列腺癌的343例分为一组,其余的317例分为另一组。对单因素分析存在统计学的意义的因素进行进一步的多因素分析,将年龄、psa值、测量的前列腺周围脂肪面积等都纳入分析。logistic回归分析结果如表2所示。
表2影响前列腺癌的logistic回归分析数据表
其中*除特殊说明外各指标均以人数(占总人数百分比)表示,
在660例患者中,343例为前列腺癌,52例为前列腺上皮内瘤变,265例为良性前列腺增生。其前列腺周围脂肪面积ppfa与前列腺癌恶性程度的相关性如图3所示,其前列腺周围脂肪面积与前列腺面积的比值ppfa/pa与前列腺癌恶性程度的相关性如图4所示,显示ppfa和ppfa/pa都与前列腺癌恶性程度具有一定的相关性。
在343例前列腺癌患者的gleason评分与前列腺周围脂肪面积ppfa的相关性如图5所示,ppfa与gleason评分相关性不显著。与前列腺周围脂肪面积与前列腺面积的比值ppfa/pa的相关性如图6所示,ppfa/pa与gleason评分具有一定的相关性。
分别建立前列腺癌和有临床意义的前列腺癌的各自模型a、b、c、d,如图7和图8所示建立roc曲线,分析ppfa/pa与psa单独诊断前列腺癌和联合其他指标诊断前列腺癌的价值。前列腺癌和有临床意义的前列腺癌的各自模型a、b、c、d预测前列腺癌发生准确度的对比数据如表3所示。
表3各模型预测前列腺癌发生的准确度数据表
模型a为psa,模型b为ppfa/pa,模型c为psa+病史(年龄、直肠指诊、家族史、pirads),模型d为ppfa/pa+psa+病史(年龄、直肠指诊、家族史、pirads)。通过对比模型a和模型b,发现ppfa/pa单独诊断前列腺癌的准确度较高,可用于单独诊断前列腺癌,ppfa/pa联合其他指标可以有效提高诊断前列腺癌的准确度。
根据现有的nomogrm绘制原理,以及表2中有统计学意义的各变量参数,绘制前列腺癌发生预测模型图如图9所示,计算初诊患前列腺癌的风险值的公式如下:logit(p)=in(p/(1-p))=1.037*age+coefdre+coefhistory+1.033*psa+coefpirads+1.066*(ppfa/pa),其中,p表示患前列腺癌风险预测值,age表示年龄变量,coefdre表示直肠指诊变量,coefhistory表示家族遗传史变量,coefpirads表示前列腺影像报告和数据系统评分变量,psa表示前列腺特异抗原值变量,ppfa/pa表示前列腺周围脂肪面积与前列腺面积的比值变量。
通过如图10所示的校正曲线可以显示该前列腺癌发生预测模型的准确度。通过图11所示的roc曲线验证该前列腺癌发生预测模型的准确度。该前列腺癌发生预测模型预测前列腺癌发生风险的效应决策曲线如图12所示。
660例患者中有179例接受了前列腺癌根治手术,这179例前列腺癌根治手术病例的临床基线资料如表4所示。
表4179例前列腺癌根治手术病例的临床基线资料
其中*除特殊说明外各指标均以人数(占总人数百分比)表示,
在179例患者中,将发生淋巴结转移的29例分为一组,其余的150例分为另一组。对单因素分析存在统计学的意义的因素进行进一步的多因素分析,将年龄、psa值、测量的前列腺周围脂肪面积,gleason评分,pirads,ihc免疫组化等都纳入分析。logistic回归分析结果如表5所示。
表5影响前列腺癌恶性化程度的logistic回归分析数据表
其中*除特殊说明外各指标均以人数(占总人数百分比)表示,
179例前列腺癌根治手术病例的前列腺周围脂肪面积与前列腺面积的比值ppfa/pa与前列腺癌的gleason评分如图13所示具有一定的相关性,与前列腺癌的t分期如图14所示具有一定的相关性。前列腺周围脂肪面积与前列腺面积的比值ppfa/pa在前列腺癌淋巴结转移和非淋巴结转移组间如图15所示具有一定的差异性,前列腺周围脂肪面积与前列腺面积的比值ppfa/pa在前列腺癌骨转移与非骨转移组间如图16所示具有一定的差异性。
如图17、18所示,建立ppfa和ppfa/pa两个指标的roc曲线,分析pre-lnm、ppfa和ppfa/pa预测前列腺癌淋巴结转移发生准确度的数据如表6所示。
表6预测前列腺癌淋巴结转移发生的准确度数据表
pre-lnm,lnmpossililitybypie-biopsymri.
根据现有的nomogrm绘制原理,以及表5中有统计学意义的各变量参数,绘制前列腺癌转移发生预测模型图如图19所示,前列腺癌患者淋巴结转移风险值公式如下:logit(p)=in(p/(1-p))=coefpre-lnm+coefpirads+coefratio+coefgs+coefpt-stage+1.008*psa+1.152*ki-67,其中,p表示患前列腺癌淋巴结转移风险预测值,coefpre-lnm表示术前依据mri诊断淋巴结转移可能性变量,coefpirads表示前列腺影像报告和数据系统评分变量,coefratio表示前列腺周围脂肪面积与前列腺面积的比值变量,coefgs表示gleason评分变量,coefpt-stage表示病理t分期变量,psa表示psa值变量,coefki-67表示ki-67表达水平变量。
通过如图20所示的校正曲线可以显示该前列腺癌转移发生预测模型的准确度。通过图21所示的roc曲线验证该前列腺癌移发生预测模型的准确度。该前列腺癌移发生预测模型预测前列腺癌发生风险的效应决策曲线如图22所示。
显然,上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而这些属于本发明的精神所引伸出的显而易见的变化或变动仍处于本发明的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!