用于检测室性颤动的设备和方法与流程
本发明涉及一种医疗设备,尤其涉及一种植入式医疗设备,以及一种用于检测室性颤动的方法和软件。
背景技术:
由室性心律失常引起的心源性猝死仍然是发达国家的主要死亡原因。快速检测此类发作对于能够立即作出反应和提供适当的处理至关重要。室性心律失常的幸存者的心脏状况在医院通常使用ecg监测系统进行密切监测。监测心脏活动以检测室性心律失常通常涉及使用电生理信号,诸如心电图(ecg)或电描记图(egm)。这些信号提供心脏功能的电信息并被用于检测诸如室性颤动之类的室性心律失常的发生。
尽管基于医院的ecg监测是一种可行的、短期的、成本有效的替代方法,但对于有心源性猝死风险的患者可能建议各种长期的处理选择。这些处理选择包括药物处理和/或植入除颤器。植入式自动除颤器包括记录egm的电极。皮下植入式除颤器能够记录ecg。这些egm/ecg在设备中通过算法被处理以检测心律,其可指示例如存在室性颤动。然而,这些算法可能会引起假阳性,通常是由其他电生理噪声源引起的。假阳性对应于对诸如电噪声、肌电势、宽qrs的双重检测、t波检测、室上性心律失常或不对应于室性心律失常但被不适当地检测到的任何其他电生理现象之类的现象的检测。实际上,电生理背景噪声的频繁出现降低了信噪比。例如,在植入式心脏复律除颤器中,假阳性会导致适当的电击,这可能是创伤性的或甚至是有害的,因为这会诱发室性心律失常。
us2004/225332a1涉及一种用于基于心脏壁运动的机械信号和心脏去极化电信号来检测和辨别心脏心律不齐的系统和方法。us2004/225332a1的算法将检测到的机械信号与检测到的电信号进行比较和验证,以对心率进行分类。因此,除了电生理信号之外,us2004/225332a1还使用心脏机械活动信号来检测室性心律不齐,而室性心律不齐通常仅从电生理信号中检测。但是,us2004/225332a1的算法不适用于改善对室性颤动的检测,因为它始终基于电生理信号,但电生理信号由于存在来自其他源的电生理噪声(例如由于肌电势)而常常会导致假阳性。
除了检测电生理信号的一系列电极之外,us2011/0098587a1还涉及对非电生理传感器(诸如加速度计或声学传感器)的使用,这些传感器被皮下地植入以检测室性心律失常和其他方面。然而,根据us2011/0098587a1,作为非电生理信号的经记录的信号(例如由皮下加速度计记录)被用于通过“盲信号分离”处理(bss)来选择一系列电生理信号的最佳可能输出信号。由bss产生的输出信号被用于对心律进行分类并检测例如室性心律失常。因此,us2011/0098587a1的方法取决于用于对心律进行分类的电生理信号。但是,此类信号如果被噪声污染(诸如肌电势在分离过程期间未被抑制),则可能会导致检测出假阳性。因此,us2011/0098587a1的设备不适用于改善对室性颤动的检测。
本发明的目的是改善心脏事件,特别是室性颤动的辨别特异性,并减少假阳性检测结果的发生,即,对诸如电噪声、肌电势、宽qrs的双重检测、t波检测、室上性心动过速或不对应于室性心律失常但被不适当地检测到的任何其他电生理现象之类的现象的检测。
技术实现要素:
本发明的目的通过一种医疗设备,特别是一种植入式医疗设备被实现,包括被配置成检测心脏血液动力学信号的至少一个植入式或非植入式血液动力学传感器;被配置成通过将由下式定义的teager能量算子(teo)应用于检测到的血液动力学心脏信号和/或从检测到的血液动力学心脏信号导出的信号来处理和分析所述信号的控制器:teo{x(n)}=ψ(n)=x2.(n-1).x(n-2).x(n),其中“x(n)”是心脏血液动力学信号,“ψ(n)”是输出的血液动力学信号且“n”是指预定样本;所述控制器进一步包括至少一个算法,该至少一个算法被配置成考虑至少一个输出的血液动力学信号来确定除颤操作的必要性。
与正常窦性心律相比,室性颤动期间由心脏生成的机械能大大降低。本发明的设备利用这一事实来根据检测到的血液动力学信号或它们的导出信号来检测室性颤动发作。通过应用teo算子进行转换使得能够提高输出信号的信噪比,并从而提供检测到的信号或从检测到的信号中导出的信号的表示,从中可以更容易地确定是否存在心音(即是否存在机械心脏活动)。实际上,通过teo算子处理信号使得将心脏的声音基本上压缩在单个峰值中成为可能。
关于假阳性结果,本发明的设备能够执行与用于检测室性颤动的电活动有关的电生理信号,诸如心电图(ecg)或电描记图(egm),心电图(ecg)或电描记图(egm)通常被用于检测心律失常但往往会产生假阳性检测结果,尤其是在室性颤动的情况下。因此,由于teo表示,对室性颤动发作的检测可被更容易地执行,同时减少了假阳性检测结果的发生。
本发明涉及可通过以下实施例被进一步改善的医疗设备。
根据一个实施例,至少一个血液动力学传感器可以是能够检测血液动力学心脏信号,特别是心音,的植入式或非植入式加速度计、话筒、压电传感器或压力传感器。加速度计被配置成检测血液动力学心脏信号,并且可被皮下地植入心脏或被外部地附接到皮肤。可被用于实施根据本发明的设备的血液动力学传感器可因此是植入式或非植入式(皮下或皮上)传感器。结果,血液动力学传感器可位于患者身体内和/或患者身体上的不同位置处。
根据一个实施例,控制器的至少一个算法可被配置成在输出的血液动力学信号的至少一个特征在比与室性颤动发作相关联的持续时间长的持续时间内不超过预定阈值的情况下确定除颤操作的必要性。此外,输出的血液动力学信号的至少一个特征可以是振幅、能量,所述信号的平均值或中值、或均方根值。因此,本发明依赖于不存在活动,而非依赖于存在增加的活动,其中电生理噪声伪影会影响心脏机械活动信号。而且,即使信号中存在类似的机械伪影,它们也不会产生假阳性。
根据一个实施例,在预定时间段内的输出的血液动力学心脏信号的振幅、和/或每个输出的血液动力学心脏信号以升序或降序穿过预定阈值的次数、和/或每个信号的超过预定阈值的峰值的个数可在确定是否存在室性颤动时被考虑。teo处理允许提高信号的清晰度,并从而提高峰值的清晰度,有助于与阈值相比确定室性颤动。
根据一个实施例,医疗设备可进一步包括除颤器,特别是植入式除颤器,其被配置成生成电除颤器信号;以及通过导线被连接到所述除颤器的至少一个电极,该导线被配置成当借助于医疗设备的控制器确定有必要触发除颤操作时,将所述电除颤信号传递给患者。因此,此设备还被配置成在借助于除颤器在检测到室性颤动发作之后处理室性颤动。
根据一个实施例,控制器可被配置成通过将输出的血液动力学信号与借助于至少一个电极相较于心脏血液动力学信号而言独立地检测到的电生理信号进行比较来确定发起除颤操作的必要性。考虑并比较彼此独立地检测的不同(电生理和血液动力学)性质的信号的这一事实使得验证并改善结果的可靠性(存在或不存在室性颤动发作)成为可能。
根据一个实施例,控制器可被配置成通过仅考虑血液动力学心脏信号来确定除颤操作的必要性。该设备可因此免于对电生理信号进行检测和处理,这简化了对室性颤动的检测。
根据一个实施例,控制器可被配置成在1至100hz,特别是从7.5至49hz的范围内对检测到的心脏血液动力学信号和/或从检测到的血液动力学心脏信号导出的信号进行带通滤波。在此窄频带中对血液动力学信号进行滤波消除了低频呼吸贡献和高频声学心波的贡献。另外,这限制了运动伪影可能对心脏信号产生的影响。这在植入有此类设备的患者移动并且例如进行体育锻炼时尤其重要。
根据一个实施例,控制器可进一步被配置成通过应用窗口函数,特别是汉明窗口,来滤波输出信号。汉明窗口可以使输出信号的峰值相对于噪声更大,但也有助于对输出信号的处理和分析,因为它降低了双重检测的风险(即若干峰值彼此靠近并可能会被误认为单个峰值)。
根据一个实施例,控制器可被配置成根据预定义的静态阈值、或者根据从心脏血液动力学信号的一个或多个特征或从其采用teager能量算子的表示周期性地重新计算并导出的动态阈值来确定除颤操作和/或发起除颤操作的必要性。因此,预定阈值的值可以是被事先定义的恒定值。替换地,用于确定是否存在室性颤动的动态阈值更为具体,并因此使得有可能改进对室性颤动发作的检测。
各实施例可以组合以形成本发明的较有利的替换实施例。
本发明的目的还可通过处理由医疗设备,特别是植入式医疗设备,的至少一个血液动力学传感器检测到的血液动力学心脏信号的方法来实现,包括处理检测到的血液动力学信号和/或从检测到的血液动力学心脏信号导出的信号的至少一个步骤,该步骤包括应用由下式定义的teager能量算子(teo):teo{x(n)}=ψ(n)=x2.(n-1).x(n-2).x(n),其中“x(n)”是检测到的血液动力学心脏信号,“ψ(n)”是输出的血液动力学心脏信号且“n”是指预定样本;并进一步包括其中通过考虑输出的血液动力学心脏信号来相对于预定阈值确定是否存在室性颤动的步骤。
与正常窦性心律相比,室性颤动期间由心脏生成的机械能大大降低。本发明的方法利用这一事实来根据检测到的血液动力学心脏信号或其导出的信号来检测室性颤动发作。通过应用teo算子进行转换可以提高输出信号的信噪比,并从而提供检测到的信号或从检测到的信号中导出的信号的表示,从中可以更容易地确定是否存在心音(即是否存在机械心脏活动)。
借助于以下各实施例可进一步改善与一种方法有关的本发明。
关于假阳性结果,本发明的方法能够执行与用于检测室性颤动的电活动有关的电生理信号,诸如心电图(ecg)或电描记图(egm),心电图(ecg)或电描记图(egm)通常被用于检测心律失常但可能会产生假阳性检测结果,尤其是在室性颤动的情况下。因此,由于teo表示,对室性颤动发作的检测可被更容易地执行,同时减少了假阳性检测结果的发生。
根据一个实施例,在信号处理步骤之前可以有信号预处理步骤,在信号预处理步骤处对检测到的心脏血液动力学信号和/或从检测到的血液动力学心脏信号导出的信号进行带通滤波,特别是在1至100hz,更特别是从7.5至49hz的范围内。在此窄频带中对血液动力学信号进行滤波消除了低频呼吸贡献和高频声学心波的贡献。另外,这限制了运动伪影可能对心脏信号产生的影响。这在配备有和/或植入有此类设备的患者移动并且例如进行体育锻炼时尤其重要。
根据一个实施例,信号处理步骤之后可以是信号后处理步骤,在该信号后处理步骤处通过应用窗口函数,特别是通过应用汉明窗口来对输出的血液动力学信号进行滤波。汉明窗口可以使输出信号的峰值相对于噪声更大,但也有助于对输出信号的处理和分析,因为它降低了双重检测的风险(即若干峰值彼此靠近并可能会被同化为单个峰值)。
根据一个实施例,至少一个血液动力学传感器可以是能够检测血液动力学心脏信号,特别是心音,的植入式或非植入式n-轴加速度计(n≥1)、话筒、压电传感器或压力传感器。加速度计被配置成检测血液动力学心脏信号,并且可被皮下地植入心脏或被外部地附接到皮肤。
根据一个实施例,由n轴加速度计检测到的n个心脏信号可沿着轴n+1被组合成新信号,轴n+1被确定成使得新信号的振幅和/或信噪比和/或稳定性和/或相关生理参数沿n+1轴最大。以此方式,信号可被组合以产生不同的信号,该不同的信号更因患者而异和/或使得诸如振幅、信噪比和/或稳定性之类的检测到的血液动力学信号的特性最大化。
根据一个实施例,预定阈值可以是预定的静态阈值或者从心脏血液动力学信号的一个或多个特征或从其采用teager能量算子的表示周期性地重新计算并导出的动态阈值。因此,预定阈值的值可以是恒定值,并且该恒定值被事先定义。替换地,用于确定是否存在室性颤动的动态阈值更为具体,并因此使得有可能改进对室性颤动发作的检测。
根据一个实施例,在预定时间段内的振幅、和/或每个输出的血液动力学信号以升序或降序穿过预定阈值的次数、和/或每个信号的超过预定阈值的峰值的个数可以/可能在确定是否存在室性颤动时被考虑。因此,相对于阈值的室性颤动的确定被促进,因为teo处理使得能够改善峰值的锐度,从而改善信号的锐度。
根据一个实施例,可通过仅考虑血液动力学心脏信号来确定是否存在室性颤动。因此,该方法可免于检测、处理以及与电生理信号比较,从而简化了用于检测室性颤动的方法。
替换地,可通过将输出的血液动力学信号与借助于医疗设备的电极检测到的至少一个电生理信号进行比较来确定是否存在室性颤动。考虑并比较不同性质(电生理和血液动力学)的信号的这一事实允许验证并改善结果的可靠性(存在或不存在室性颤动发作)。
本发明的目的还可通过处理由医疗设备,特别是植入式医疗设备的至少一个血液动力学传感器检测到的心脏血液动力学信号的软件来实现,其特征在于,其包括当由医疗设备执行时能够执行以下各项的指令:通过应用由下式定义的teager能量算子(teo)处理检测到的血液动力学信号和/或从检测到的血液动力学心脏信号导出的信号:teo{x(n)}=ψ(n)=x2.(n-1).x(n-2).x(n),其中“x(n)”是检测到的血液动力学信号,“ψ(n)”是输出信号且“n”是指预定样本;以及将输出信号的至少一个特征与预定阈值进行比较;以及当输出信号的至少一个特征未超过预定阈值达预定时间段时触发警报。
与正常窦性心律相比,室性颤动期间由心脏生成的机械能大大降低。本发明的软件基于这一事实来根据检测到的血液动力学信号或它们的导出信号来检测室性颤动发作。通过teo算子进行转换使得可以提高输出信号的信噪比,并从而提供原始信号的表示,从中可以更容易地确定是否存在心音(即是否存在机械心脏活动)。此外,与诸如小波滤波之类的其他方法和算法不同,teo算子不需要先验信号信息或学习算法。
通过以下各实施例可进一步改善与软件有关的本发明。
根据一个实施例,软件可进一步包括通过带通滤波对检测到的血液动力学心脏信号和/或从检测到的心脏血液动力学信号导出的信号进行预处理,特别是在1至100hz,更特别是从7.5至49hz的范围内。在此窄频带中对血液动力学信号进行预滤波,消除了低频呼吸贡献和高频声学心波的贡献。另外,这限制了运动伪影可能对心脏信号产生的影响。这在植入有此类设备的患者移动并且例如进行体育锻炼时尤其重要。
根据一个实施例,软件可进一步包括通过应用窗口函数,特别是汉明窗口来对输出信号进行后处理。汉明窗口可以使输出信号的峰值相对于噪声更大,但也有助于对输出信号的处理和分析,因为它降低了双重检测的风险(即若干峰值彼此靠近并可能会被同化为单个峰值)。
附图说明
将在以下藉由优选实施例并且特别是依赖于以下附图来更详细地解释本发明及其优点,其中
图1a表示根据本发明的第一实施例的包括血液动力学心脏传感器的医疗设备。
图1b表示根据本发明的第二实施例的包括血液动力学心脏传感器的医疗设备。
图1c表示根据本发明的第三实施例的包括心脏血液动力学传感器的医疗设备。
图1d表示根据本发明的第四实施例的包括血液动力学心脏传感器的组装件。
图2表示室性颤动期间的血液动力学信号。
图3表示三轴加速度计。
图4a表示根据本发明的第一实施例的算法。
图4b表示根据本发明的第二实施例的算法。
图4c表示根据本发明的第三实施例的算法。
图4d表示根据本发明的第四实施例的算法。
具体实施方式
现在将通过使用示例性方法中的有利实施例并且参考附图来更详细地描述本发明。所描述的实施例仅是可能的配置,并且应当铭记,在实现本发明时如上所述的个体特征可以彼此独立地提供或者可以一起被省略。
根据本发明,血液动力学信号由至少一个心脏血液动力学传感器(诸如加速度计)记录,根据各种实施例(参见图1a-1c),其可被集成在除颤器壳体,特别是植入式自动除颤器内或被集成在被连接到除颤器的导线内。根据替换实施例,心脏血液动力学传感器可以不同于除颤器,也就是说不与除颤器相关联,不与除颤器相集成或不与除颤器相结合(参见图1d)。
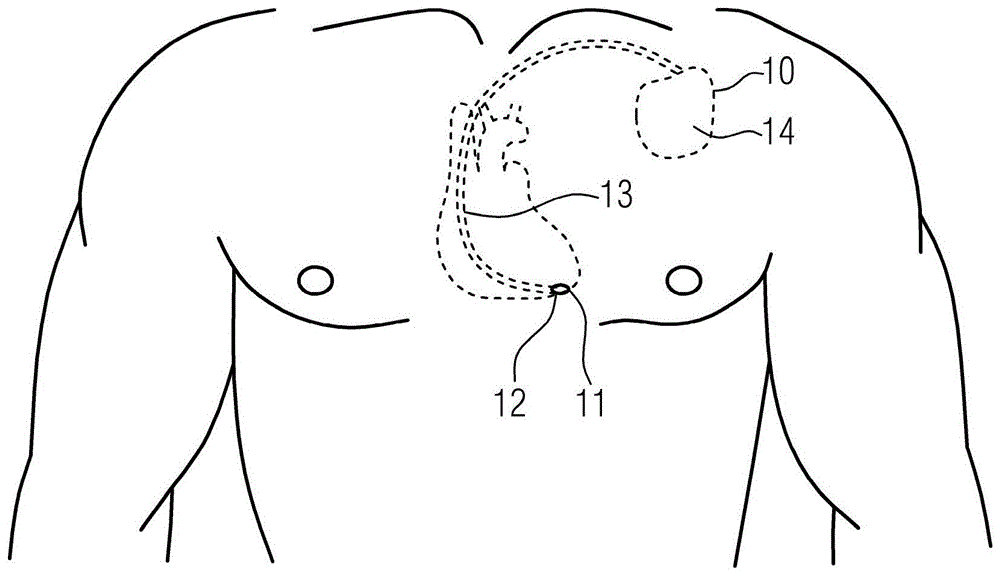
图1a例示了皮下地被植入的医疗设备10,特别是根据第一实施例的植入式自动除颤器10,其中单轴或多轴加速度计11被集成在除颤器10的心内刺激导线13的远端12处。心内刺激导线13还可包括用于记录电生理信号的一个或多个电极(未示出)。被连接到心内刺激导线13的植入式自动除颤器10被适配成将微控制器和相关联的电子电路(未示出)容纳在壳体14中。
医疗设备10包括控制器(未示出),该控制器具有被配置成通过考虑由加速度计11检测到的心脏血液动力学信号来检测室性颤动的算法。根据本发明,控制器的所述算法不使用由电极或心内刺激导线13检测到的电生理信号。实际上,医疗设备10的控制器能够通过仅考虑血液动力学信号来检测室性颤动发作。
另外,根据本发明的第一实施例,医疗设备10的控制器还包括被配置成通过考虑血液动力学信号来触发除颤操作的算法。因此,设备10还被配置成借助于由除颤器10,特别是由除颤器10的心内刺激导线13,传递的除颤信号在检测到室性颤动发作之后处理室性颤动。
图1b例示了医疗设备20,特别是根据第二实施例的植入式自动除颤器20,其壳体21被皮下地植入在患者的腋下。设备20的壳体21包括微控制器和相关联的电子电路(未示出),并在胸骨旁区域中被连接到皮下导线22,该导线22本身具有一个或多个电极(未示出)。诸如加速度计23之类的心脏血液动力学传感器可被集成在设备20的壳体21中和/或被集成到皮下导线22。
医疗设备20包括控制器(未示出),该控制器具有被配置成通过考虑由加速度计23检测到的心脏血液动力学信号来检测室性颤动的算法。根据本发明,所述控制器算法不使用由导线22的(一个或多个)电极检测到的电生理信号。实际上,医疗设备20的控制器能够通过仅考虑血液动力学信号来检测室性颤动发作。
另外,根据本发明的第二实施例,医疗设备20的控制器还包括被配置成通过考虑血液动力学信号来触发除颤操作的算法。因此,设备20还被配置成借助于由除颤器20传递的除颤信号,在检测到室性颤动发作之后处理室性颤动。
类似地,图1c例示了医疗设备30,特别是根据第三实施例的植入式自动除颤器30,其壳体31被皮下地植入在胸腔中。除颤器30的壳体31包括微控制器和相关联的电子电路(未示出)。壳体31在胸骨旁区域中被连接到皮下刺激导线32,该导线32本身具有一个或多个电极(未示出)。在刺激导线32的远端34处集成有血液动力学心脏传感器,这里是加速度计33。
医疗设备30包括控制器(未示出),该控制器具有被配置成通过考虑由加速度计33检测到的心脏血液动力学信号来检测室性颤动的算法。根据本发明的第三实施例,控制器的所述算法不使用由刺激导线32的(一个或多个)电极检测到的电生理信号。实际上,医疗设备30的控制器能够通过仅考虑血液动力学信号来检测室性颤动发作。
根据替换实施例,控制器将相较于血液动力学心脏信号而言独立地检测到的电生理信号考虑在内,以便将这两种类型的信号(电生理和血液动力学)相互比较,以提高检测室性颤动发作的可靠性。
另外,根据本发明的第三实施例,医疗设备30的控制器还包括被配置成通过考虑血液动力学信号来触发除颤操作的算法。因此,设备30还被配置成借助于由除颤器30,特别是刺激导线32传递的除颤信号在检测到室性颤动发作之后处理室性颤动。
图1d例示了第四实施例,其中心脏血液动力学传感器40,特别是加速度计,被并入粘贴在患者胸部的绷带41的中心。此绷带41还可包括一个或多个电极(未示出)、微控制器和相关的电子电路(未示出)。在此第四实施例中,当通过绷带41的心脏血液动力学传感器40检测到室性颤动时,外部除颤器(自动或手动的)可被用于除颤操作。替换地,心脏血液动力学传感器40既不同于除颤器(即,例如,其未集成或连接至除颤器和/或其起搏导线之一),也不与除颤器结合使用。
因此,根据本发明的各种实施例,血液动力学信号借助于诸如加速计11、23、33、40之类的至少一个血液动力学传感器来检测,该加速计11、23、33、40要么被植入心脏内(11),要么被植入皮下(23,33)或附接在病人的胸部表皮上(40)。
在另一实施例中,血液动力学传感器可以是话筒、压电传感器、压力传感器等。
另外,根据本发明的变型,对血液动力学信号的记录可由同一类型的若干血液动力学传感器(例如若干加速计)或不同类别的若干血液动力学传感器(例如植入式传感器和皮肤传感器)的组合来完成,这些传感器将被定位在患者身体的不同点处。
根据本发明的实施例,每个血液动力学传感器可以与或可以不与除颤器,特别是植入式除颤器结合使用。
无论本发明的实施例是什么,本发明都考虑到生成心脏血液动力学信号所需的能量,例如由加速计记录信号以便将该信号转换为显著地促进对室性颤动的检测的替换表示的能量。能量的这种表示是通过在心脏血液动力学信号上应用teo(即“teager能量算子”)来提供的。
teager能量算子(以下为teo)由以下公式定义:
teo{x(n)}=ψ(n)=x2(n-1).x(n-2).x(n),其中“x(n)”是输入信号(在此示例中是心脏血液动力学信号),而“ψ(n)”是算子的输出信号。“n”是指特定样本。
teo算子(即“teager能量算子”)是一种数学算子,其可被集成到使用血液动力学传感器(诸如加速计)的植入式心脏设备(诸如植入式自动除颤器)的软件或硬件中以记录心脏血液动力学信号。传感器可以是心内的、皮下的或外部的(即,传感器被附接到患者的皮肤)。
图2以图形表示在室性颤动发作之前(s)的正常窦性心律信号和在室性颤动发作期间(p)的几秒钟。曲线图a例示了由加速度计(a)获取并被滤波的信号,曲线图b例示了teo输出信号,而曲线图c例示了经平滑的teo输出信号。
由teo算子对信号进行的转换会产生对其用于生成输入信号所需的能量的实时估计。此能量是原始信号的振幅和频率的函数。特别地,能量对应于原始信号的振幅和频率的加权乘积。在正常窦性心律期间,来自如图1a-d所描绘的心脏血液动力学加速度计的信号的teo输出呈现出与心音一致的一系列清晰且锐利的尖峰,如图2的曲线图a所示。通常,第一心音(通常称为s1声音)比第二心音或s2声音具有更大的振幅。结果,对应于第一心音s1的te0输出信号的峰值显著大于对应于第二心音s2的te0输出信号的峰值。
在心音s1,s2之间,teo输出信号是平坦的,如图2中的曲线图b和c所示。这是由于背景噪声相对于心音s1,s2而言通常具有较低的振幅和频率的事实。因此,利用teo算子对信号进行的转换,可以大大提高信号的信噪比,其中所述信噪比信号对应于心音s1(由在心收缩开始时二尖瓣和三尖瓣关闭引起的湍流引起),而信号的其余部分对应于噪声。结果,本发明使得能够改善心脏事件,特别是室性颤动的辨别的特异性。
实际上,在室性颤动期间,心室的同步和协调收缩被无序或混乱的震颤所代替。心脏机械性能严重受损,心室的收缩能量与正常运作时不同。这被反映在心脏血液动力学信号的teo输出信号中,该心脏血液动力学信号具有接近零的长而平的平顶形状,并在图2中用双箭头p表示。不存在反映心音s1,s2的高振幅特征峰(请参见双箭头s)。
如图2的曲线图a所例示的,在10-50hz频率范围内使用例如具有0.05%通带波纹滤波器的四阶tchebychev模拟滤波器对用诸如单轴或多轴加速度计之类的心脏血液动力学传感器在n轴(其中n≥1)处记录的信号进行第一次带通滤波(如在weinberg,louis,slepian,paul(1960年6月)的文章“takahasi'sresultsontchebycheffandbutterworthladdernetworks(takahasi在tchebycheff和butterworth阶梯网络上的结果)”,电路理论的ire交易:88-101中描述的)。在此窄频带中对血液动力学信号进行预滤波,消除了低频呼吸贡献和高频声学心波的贡献。另外,这限制了运动伪影可能对心脏信号产生的影响。这在植入有此类设备的患者移动并且例如进行体育锻炼时尤其重要。
滤波后,可对由心脏血液动力学传感器记录的信号执行其他预处理。例如,信号可被独立地分析并按值的顺序分类。此类分类可考虑响应于血液动力学变化的振幅、频率、信噪比、稳定性或信号敏感性。对信号的选择也可被考虑。根据排序标准的最佳信号被选择以供后续处理。
替换地,可以以某种方式组合信号以产生用于检测室性颤动的不同的,更特定的信号。
图3表示3轴(x,y,z)加速度计50,其可被集成在设备10、20、30之一中或可以为血液动力学传感器40。如图3所示,心脏心缩机械轴m是平行于正常收缩期间由心脏生成的最大力矢量的轴。沿x,y,z轴的原始血液动力学信号的分量沿此心脏心缩机械轴m投影并相加以生成新信号。沿此轴m记录的心脏血液动力学信号指示可由诸如加速度计之类的血液动力学传感器记录的最大振幅并基本上指示最大信噪比,例如,在图3所例示的位置处,沿此心脏机械轴m的信号实质上是比简单地沿前后轴记录的信号更具生理性、患者特异性并因此不那么任意的信号。
在滤波和预处理之后,血液动力学信号用作teo的输入信号。根据算法的一些实施例,在能够检测诸如室性颤动的室性心律失常之前,利用例如汉明窗口对teo输出信号进行平滑处理,如图2的曲线图c所示。汉明窗口可以使输出信号的峰值与噪声相比更大,但也有助于算法的几个实施例对输出信号的处理,因为它降低了双重检测的风险(即若干峰值彼此靠近并可能会被误认为单个峰值)。
在滤波、预处理和平滑之后,经平滑的teo输出信号用作算法的输入,该算法考虑到teo输出信号的频率和/或振幅以便检测诸如室性颤动之类的室性心律失常。下文描述这些算法的几个实施例。
图4a例示了算法100的第一实施例。
在步骤101,接收由血液动力学传感器记录的血液动力学信号的样本n。血液动力学传感器可以是加速度计、话筒、压电传感器、压力传感器等。另外,根据本发明的变型,对血液动力学信号的记录可由同一类型的若干血液动力学传感器(例如若干加速计)或不同类别的若干血液动力学传感器(例如植入式传感器和皮肤传感器)的组合来完成,这些传感器将被定位在患者身体的不同点处。
在步骤102中,在10-50hz频率范围内对血液动力学信号进行带通滤波以消除低频呼吸贡献和高频声学心波贡献。
在步骤103中,对信号进行预处理以使得它们与室性颤动的检测更加相关。已经参考图2和3描述了这种预处理。例如,在血液动力学传感器是n轴加速度计的情况下,沿n轴的血液动力学信号的分量可沿n+1轴(尤其是沿心缩心脏机械轴m)被投射并被添加以产生其振幅被最大化的新信号。替换地或组合地,在10-50hz频率范围内使用例如具有0.05%带通波纹滤波器的四阶tchebychev模拟滤波器对信号进行带通滤波。
经滤波和预处理的心脏血液动力学信号然后被用作teo算子中的输入信号。在步骤104处,通过应用teo算子来转换血液动力学信号,该teo算子提供产生这些信号所需能量的实时估计。此能量是原始信号的振幅和频率的函数。特别地,能量对应于原始信号的振幅和频率的加权乘积。
在步骤105中,例如通过应用汉明窗口来平滑teo输出信号。
在步骤106中,将经平滑的teo输出信号与阈值107进行比较。阈值107可以是静态值(即,事先计算并定义的单个恒定值)或动态值(即,其使用原始或处理后的信号的各种值被规律地重新计算)。根据其中若干心脏血液动力学信号被不同的血液动力学传感器(例如被第一植入式传感器和被第二皮肤传感器)记录的实施例,阈值可通过交叉比对和验证第一和第二血液动力学传感器的血液动力学信号来计算。在其中心脏血液动力学信号由n轴血液动力学传感器记录的另一实施例中(参见图3所示的示例),阈值可通过交叉比对和检查分别沿着每个轴记录的血液动力学信号来计算。
如果teo输出信号大于阈值107,则在步骤108中不采取任何动作,并且准备好考虑经平滑的teo输出信号的下一个样本。然而,如果teo输出信号小于阈值107,则在步骤109中计算当前样本与大于阈值107的最近样本之间的经过的时间“δt”。
如果经过的时间“δt”小于室性颤动所特有的特定时间极限(图4a中的“极限持续时间vf”),则在步骤110处不采取任何动作,并且期望接收teo输出信号的下一个n+1样本。
但是,如果经过的时间“δt”大于或等于“极限持续时间vf”,则在步骤111中检测到室性颤动并触发警报。与阈值类似,“vf极限持续时间”的特定值也可以是静态值(即,单一的、不变的和确定的事先值)或动态值(即,其根据原始信号或输出信号被规律地重新计算)。
图4b例示了算法200的第二实施例。
在类似于算法100的方法中,在步骤201中接收由血液动力学传感器记录的血液动力学信号的样本n。血液动力学传感器可以是加速度计、话筒、压电传感器、压力传感器等。另外,根据本发明的变型,对血液动力学信号的记录可由同一类型的若干血液动力学传感器(例如若干加速计)或不同类别的若干血液动力学传感器(例如植入式传感器和皮肤传感器)的组合来完成,这些传感器将被定位在患者身体的不同点处。
然后,在步骤202处,在10-50hz频率范围内对血液动力学信号进行带通滤波以消除低频呼吸贡献和高频声学心波贡献。
在步骤203中,对信号进行预处理以使得它们与室性颤动的检测更加相关。已经参考图2、3和4a描述了这种预处理。在步骤204处,通过应用teo算子来转换血液动力学信号。
根据第二实施例,在步骤205中,通过应用滑动窗口滤波器对teo输出信号进行滤波,该滑动窗口滤波器的“窗口”长度可以是静态值(即,事先计算并定义的单个不改变的值)或动态值(即,其使用原始或输出信号被规律地重新计算)。
“窗口”在teo输出信号的最近样本上滑动(即,移至下一个或上一个样本,而不会像“跳跃窗口”那样一次“跳跃”多个样本),该teo输出信号在步骤206处使用例如汉明窗口被平滑。
在步骤207处,在“窗口”内将经平滑的teo输出信号与阈值208进行比较。阈值208可以是静态值(即,事先计算并定义的单个不改变的值)或动态值(即,其使用经平滑的输出信号teo被规律地重新计算)。在步骤207中,计算在“窗口”内以升序或降序穿过阈值208的次数x,或超过阈值208的峰值的个数x。
如果次数x大于特定极限次数(图4b中的“极限vf”),则在步骤209中不采取动作,并且期望接收下一个n+1信号样本。
如果次数x小于特定极限次数“极限vf”,则在步骤210中检测到室性颤动并触发警报。与阈值208类似,次数“极限vf”的特定值也可以是静态值(即,单一的、不变的和确定的事先值)或动态值(即,其根据原始信号或输出信号被规律地重新计算)。
根据其中若干心脏血液动力学信号被不同的血液动力学传感器(例如被第一植入式传感器和被第二皮肤传感器)记录的实施例,阈值可通过交叉比对和验证第一和第二血液动力学传感器的血液动力学信号来计算。
根据其中心脏血液动力学信号由n轴血液动力学传感器记录的另一实施例中(参见图3所示的示例),阈值可通过交叉比对和验证分别沿着每个轴记录的血液动力学信号来计算。
图4c例示了算法300的第三实施例。
在算法200的类似方法中,在步骤301中接收由血液动力学传感器记录的血液动力学信号的样本n。血液动力学传感器可以是加速度计、话筒、压电传感器、压力传感器等。另外,根据本发明的变型,对血液动力学信号的记录可由同一类型的若干血液动力学传感器(例如若干加速计)或不同类别的若干血液动力学传感器(例如植入式传感器和皮肤传感器)的组合来完成,这些传感器将被定位在患者身体的不同点处。
然后,在步骤302中,在10-50hz频率范围内对血液动力学信号进行带通滤波以消除低频呼吸贡献和高频声学心波贡献。
在步骤303中,对信号进行预处理以使得它们与室性颤动的检测更加相关。已经参考图2、3和4a描述了这种预处理。
根据第三实施例,在步骤304中,在带通滤波和预处理之后,“窗口”的心脏血液动力学信号的最近样本被存储在存储器中。此窗口是“跳跃窗口”类型,且“窗口”的长度可以是静态值(即,事先计算并定义的单个不改变的值)或动态值(即,其使用原始或输出信号被规律地重新计算)。
在步骤305处,通过应用teo算子来转换血液动力学信号。在步骤305中,在当前“窗口”中计算teo输出信号。
在步骤306处,使用例如汉明窗口在当前“窗口”中平滑teo输出信号。
在步骤307处,在“窗口”内将经平滑的teo输出信号与阈值308进行比较。阈值308可以是静态值(即,事先计算并定义的单个不改变的值)或动态值(即,其使用经平滑的teo输出信号被规律地重新计算)。
根据其中若干心脏血液动力学信号被不同的血液动力学传感器(例如被第一植入式传感器和被第二皮肤传感器)记录的实施例,阈值可通过交叉比对和验证第一和第二血液动力学传感器的血液动力学信号来计算。
根据其中心脏血液动力学信号由n轴血液动力学传感器记录的另一实施例中(参见图3所示的示例),阈值可通过交叉比对和检查分别沿着每个轴记录的血液动力学信号来计算。
在步骤307中,计算在“窗口”内以升序或降序穿过阈值308的次数x,或超过阈值308的峰值的个数x。
如果次数x大于特定极限值(图4c中的“极限vf”),则未检测到室性颤动:在步骤309,算法300在考虑处理下一窗口之前等待特定数量的“样本跳跃”。同时,在步骤304处经预处理的信号仍被记录并保存在存储器中,以便在下一窗口中被考虑。
如果次数x小于特定极限次数“极限vf”,则在步骤310中检测到室性颤动并触发警报。与阈值308类似,“极限vf”次数的特定值也可以是静态值(即,单一的、不变的和确定的事先值)或动态值(即,其根据原始信号或输出信号被规律地重新计算)。
算法300允许比算法100和200的计算成本低的计算成本,因为它仅针对所有“样本跳跃”而不是连续地计算窗口内的teo输出信号。
图4d例示了算法400的第四实施例。
与先前的算法100、200、300不同,算法400考虑了在“滑动窗口”或“跳跃窗口”中超过阈值的峰值的个数及其振幅。
在步骤401,接收由血液动力学传感器记录的血液动力学信号的样本n。血液动力学传感器可以是加速度计、话筒、压电传感器、压力传感器等。另外,根据本发明的变型,对血液动力学信号的记录可由同一类型的若干血液动力学传感器(例如若干加速计)或不同类别的若干血液动力学传感器(例如植入式传感器和皮肤传感器)的组合来完成,这些传感器将被定位在患者身体的不同点处。
在步骤402处,在10-50hz频率范围内对血液动力学信号进行带通滤波以消除低频呼吸贡献和高频声学波贡献。
在步骤403中,对信号进行预处理以使得它们与室性颤动的检测更加相关。已经参考图2、3和4a描述了这种预处理。
在步骤404处,通过应用teo算子来转换血液动力学信号。
根据第四实施例,在步骤405中,在“滑动”窗口中考虑输出信号teo。窗口的长度的值可以是静态值(即,事先计算并定义的恒定值)或动态值(即,其使用原始或处理后的信号被规律地重新计算)。
在步骤406中,使用例如汉明窗口在所述窗口中平滑teo输出信号。
在步骤407中,确定窗口中超过teo阈值408的经平滑的teo输出信号的峰值及其振幅。阈值408可以是静态值(即,事先计算并定义的单个不改变的值)或动态值(即,其使用经平滑的输出信号teo被规律地重新计算)。
根据其中若干心脏血液动力学信号被不同的血液动力学传感器(例如被第一植入式传感器和被第二皮肤传感器)记录的实施例,阈值可通过交叉比对和验证第一和第二血液动力学传感器的血液动力学信号来计算。
根据其中心脏血液动力学信号由n轴血液动力学传感器记录的另一实施例中(参见图3所示的示例),阈值可通过交叉比对和检查分别沿着每个轴记录的血液动力学信号来计算。
具有特别大振幅的峰值被怀疑是外部和寄生噪声并因此可能会误导信号处理。因此,在步骤409中,忽略其振幅超过特定值(图4d中的“噪声极限”)的所有峰值。“噪声极限”的值可以是静态值(即,事先计算并定义的单个恒定值)或动态值(即,其使用经平滑的teo输出信号被规律地重新计算)。
在步骤410中,剩余峰值的振幅被相加以仅给出称为“窗口能量”的一个值。
如果“窗口能量”的值大于称为“极限能量vf”的特定值,则在步骤411中不采取动作,并且期望接收下一个n+1信号样本。
如果“窗口能量”的值小于所述特定值“极限能量vf”,则在步骤412处检测到室性颤动并触发警报。与阈值408类似,“极限能量vf”次数的特定值也可以是静态值(即,单一的、不变的和确定的事先值)或动态值(即,其根据原始或输出信号被规律地重新计算)。此阈值“极限能量vf”可被解释为确保足够的全身性输注(即,脑和身体中的血液循环)所需的最小能量。
根据本发明的设备和方法100、200、300、400的不同实施例可进一步被配置成在检测到室性颤动之后按照“室性颤动检测警报”111、210、310、412的步骤,特别是借助于手动或自动除颤器触发除颤操作。另外,本发明的方法和设备可被配置成验证除颤操作是否有效,即,在除颤操作之后心脏的机械活动是否已经恢复。为此,在允许除颤操作后恢复正常心率的预定时间流逝后,血液动力学心脏信号借助于血液动力学传感器被检测,并特别地通过应用teo算子被处理,如参考图4a至4d所描述的。因此定义了“后处理”输出的血液动力学心脏信号。在与参考图4a至4d中的至少一者描述的相同的方法中,将所述“后处理”输出的血液动力学心脏信号与预定阈值进行比较,以确定除颤操作是否已经有效地处理了室性颤动。在否定的情况下,新的除颤操作可被发起,在此期间将处理性除颤信号(电击)传递给患者。
所描述的实施例仅是可能的配置,并且应当铭记,不同的实施例的各个特征可以彼此组合或彼此独立地提供。
另外,算法100、200、300、400中的每一者可在参考图4a、4b、4c和4d描述的各步骤之前、之间或之后包括附加的步骤。
- 还没有人留言评论。精彩留言会获得点赞!