一种冲击波心脏瓣膜介入治疗输送系统的制作方法
本申请属于医疗技术领域,具体涉及一种冲击波心脏瓣膜介入治疗输送系统。
背景技术:
心脏瓣膜钙化是心脏瓣膜狭窄和返流等主要的病理表现,通常发生于老年人群;血管钙化是动脉粥样硬化、高血压、糖尿病血管病变、血管损伤、慢性肾病和衰老等普遍存在的共同的病理表现。
目前,针对心脏瓣膜钙化和血管钙化的治疗方法包括:药物治疗、外科手术置换或介入手术置换等方法。
本申请的发明人在长期的研发过程中发现,现有的药物治疗效果十分有限,而现有的外科手术或介入手术置换的方式存在对患者本身创伤大且耗时长等缺点。
技术实现要素:
本申请提供一种冲击波心脏瓣膜介入治疗输送系统,能够将能量传递并转化到冲击波发射器上,通过冲击波软化钙化部位,能够快速有效完成对钙化部位的治疗。
为解决上述技术问题,本申请采用的一个技术方案是:一种冲击波心脏瓣膜介入治疗输送系统,包括:外层编织管,为中空结构;内管,为中空结构,位于所述外层编织管内部,与所述外层编织管间形成预制通道;传导电极线缆,在所述预制通道内延伸,用于传导电压/电流脉冲。
根据本申请一实施方式,所述外层编织管从外到内依次包括外层管、金属编织层和内层管,其中,所述外层管采用嵌段聚醚酰胺树脂材料,所述金属编织层由金属丝或金属线编织而成,所述内层管采用聚四氟乙烯、氟化乙烯丙烯共聚物、热塑性弹性体橡胶、聚酰亚胺或聚酰胺材料。
根据本申请一实施方式,所述金属编织层的编织密度为30-75ppi。
根据本申请一实施方式,所述金属编织层端部固定有显影环,所述显影环至少设置于所述金属编织层靠近冲击波发射器一端。
根据本申请一实施方式,所述传导电极线缆设置有若干条,且在所述外层编织管和所述内管之间呈圆周阵列设置。
根据本申请一实施方式,所述传导电极线缆包括间隔设置的正极导体和负极导体,包裹所述正极导体和所述负极导体的内绝缘层,以及包裹所述内绝缘层的外绝缘层。
根据本申请一实施方式,所述正极导体为银包铜线,所述负极导体包括绝缘外层和导体芯,所述导体芯包括铜线或者铜包钢线。
根据本申请一实施方式,所述内绝缘层为绝缘材料,所述输送系统可输送3-7kv的电压。
根据本申请一实施方式,所述内管的内径大于或等于0.035英寸。
根据本申请一实施方式,所述内管采用聚醚醚酮、聚乙烯或聚酰胺材料;或者,所述内管为具有编织结构的管体。
根据本申请一实施方式,所述预制通道用于输送电解质液体。
本申请的有益效果是:通过本申请的输送系统,可以使治疗心脏瓣膜钙化的冲击波装置将能量传递并转化到冲击波发射器上,从而将瓣膜狭窄和返流的僵硬瓣叶或瓣环软化,改善工作时瓣叶开合的状态,达到治疗的效果,可避免植入人工瓣膜术中和术后的风险。还可与现有手术治疗相结合,解决手术过程中遇到的瓣膜钙化严重,无法精确放置心脏瓣膜的问题,即有效避免手术过程中人工瓣膜定位和固定困难、人工瓣膜释放不合适及难以取出等风险,且可减少周漏,并缩短手术时间,大大改善了手术操作和预后。
附图说明
为了更清楚地说明本申请实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本申请的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图,其中:
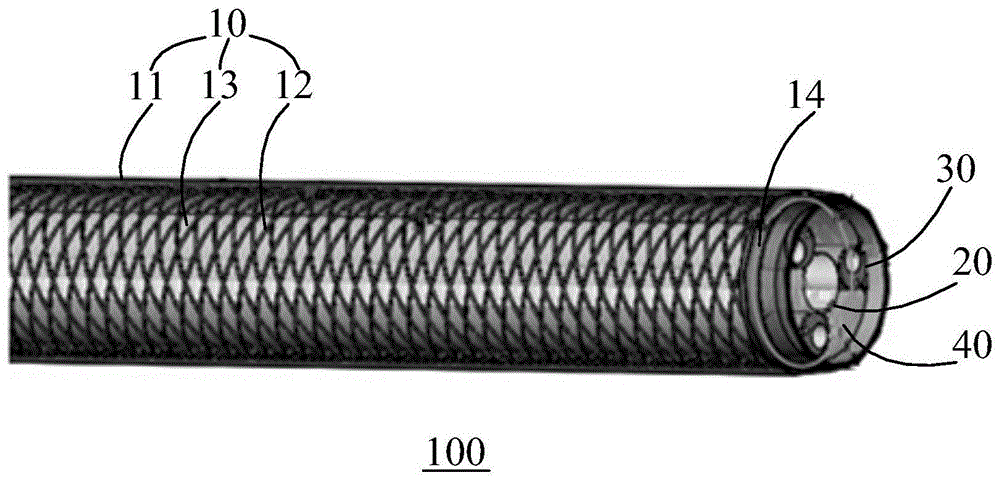
图1是本申请的冲击波心脏瓣膜介入治疗输送系统一实施例的立体结构示意图;
图2是本申请的冲击波心脏瓣膜介入治疗输送系统一实施例的剖面结构示意图。
具体实施方式
下面将结合本申请实施例中的附图,对本申请实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本申请的一部分实施例,而不是全部的实施例。基于本申请中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本申请保护的范围。
请参阅图1至图2,图1是本申请的冲击波心脏瓣膜介入治疗输送系统一实施例的立体结构示意图;图2是本申请的冲击波心脏瓣膜介入治疗输送系统一实施例的剖面结构示意图。
本申请一实施例提供了一种冲击波心脏瓣膜介入治疗输送系统100,如图1所示,包括外层编织管10、内管20和传导电极线缆30。外层编织管10为中空结构,内管20位于外层编织管10内部,与所述外层编织管10间形成预制通道40,传导电极线缆30在预制通道40内延伸,用于传导电压/电流脉冲。外层编织管10承担介入器械通路的建立的作用;传导电极线缆30传导电压/电流脉冲至冲击波发射器上;内管20具有隔绝传导电极线缆30和形成内部导丝(外部器械)通过的通路的功能。通过本申请的输送系统100,可以使治疗心脏瓣膜钙化的冲击波装置将能量传递并转化到冲击波发射器上,从而将瓣膜狭窄和返流的僵硬瓣叶或瓣环软化,改善工作时瓣叶开合的状态,达到治疗的效果,可避免植入人工瓣膜术中和术后的风险。还可与现有手术治疗相结合,解决手术过程中遇到的瓣膜钙化严重,无法精确放置心脏瓣膜的问题,即有效避免手术过程中人工瓣膜定位和固定困难、人工瓣膜释放不合适及难以取出等风险,且可减少周漏,并缩短手术时间,大大改善了手术操作和预后。
在一实施例中,如图1所示,外层编织管10从外到内依次包括外层管11、金属编织层12和内层管13。外层管11采用pebax材料(嵌段聚醚酰胺树脂材料),具有一定柔软性和可变形能力,外层管11选用的pebax材料可根据实际所需采用不同硬度。金属编织层12由金属丝或金属线交叉编织而成,其具有一定的支撑性能和通过性能,金属编织层12具有可变的编织密度,可根据实际所需做出调整,具体地,金属编织层12的编织密度为30-75ppi,例如30ppi、40ppi、45ppi、50ppi、60ppi或者75ppi等。内层管13可采用ptfe(聚四氟乙烯)、fep(氟化乙烯丙烯共聚物)、tpe(热塑性弹性体橡胶)、pi(聚酰亚胺)或者pa(聚酰胺)等高分子材料制成,其具有一定的延展性和润滑性。具体地,金属编织层12在内管20外部编织而成。
进一步地,如图1所示,金属编织层12端部固定有显影环14,由于金属编织层12由金属丝或金属线编织而成,其端部存在杂乱的丝线头端,显影环14起到固定金属编织层12端部丝线的作用,防止散乱的丝线头端对其他结构造成损伤。显影环14至少位于金属编织层12靠近冲击波发射器一端,或者显影环14可位于金属编织层12两端,此处不作限定。显影环14在x光下可显影,起到一定的定位作用。
在一实施例中,如图2所示,传导电极线缆30可设置有若干条,且在外层编织管10和内管20之间呈圆周阵列设置。由于传导电极线缆30需要传导高电压/电流,从而阵列设置的传导电极线缆30间保持一定的距离,避免相互干扰,将电能传送到远端电极发生器上,保证发生器可以正常放电,将能量转化成声波传递至瓣膜钙化位置。在本实施例中,传导电极线缆30设置有三条,在其他实施例中,传导电极线缆30还可以设置有一条、两条、四条或者更多条,从而本申请的输送系统100可以安装一组或多组电极。
进一步地,如图2所示,传导电极线缆30包括间隔设置的正极导体31和负极导体32,包裹正极导体31和负极导体32的内绝缘层33,以及包裹内绝缘层33的外绝缘层34。正极导体31为银包铜线,负极导体32为有绝缘外层的漆包线,具体地,负极导体32包括绝缘外层和导体芯,导体芯为铜线或者铜包钢线,绝缘外层为聚酰亚胺或其他绝缘材料,绝缘外层的颜色可以为红色、黄色或黑色等。通过多层绝缘设计,本申请的输送系统100可承受更高的电压,具体地,本申请的输送系统100可承受3-7kv的电压。
在一实施例中,如图2所示,内管20可采用peek(聚醚醚酮)、pe(聚乙烯)、pa(聚酰胺)等高分子材料制成,其具有一定的延展性和润滑性。在其他实施例中,内管20还可以是具有编织结构的管体,结构类似外层编织管10,此处不再阐述。
在一实施例中,如图2所示,内管20的内径大于或等于0.035英寸,从而其可通过最大直径为0.035inch尺寸的导丝。
在一实施例中,如图1和图2所示,外层编织管10和内管20间的预制通道40与球囊(包裹于冲击波发射器外)连通,用于输送电解质液体,从而球囊内的电解质液可通过预制通道40流入。
总而言之,区别于现有技术的情况,治疗心脏瓣膜钙化的冲击波装置依靠本申请的输送系统100将冲击波发生器产生的脉冲信号传递给冲击波发射器,然后电极放电将心脏瓣膜钙化位置软化或将粘连部位变松弛,从而改善、治疗心脏瓣膜狭窄和返流病患。该装置可以通过介入方式进行治疗,或与“外科手术的方法置换自体瓣膜手术方法”结合的方式,有效提高手术的成功率。
本申请的输送系统100的工作状态可将高频电压/电流脉冲进行输出,且可承受不同电流/电压的脉冲强度、重复频率,保证多次的放电后不衰减。本申请的输送系统100可以通过股动脉入路,并有良好的支撑性和通过性,并有较强的过弓能力。
以上所述仅为本申请的实施例,并非因此限制本申请的专利范围,凡是利用本申请说明书及附图内容所作的等效结构或等效流程变换,或直接或间接运用在其它相关的技术领域,均同理包括在本申请的专利保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!