用于治疗实体瘤的靶向鹅膏毒素缀合物的制作方法
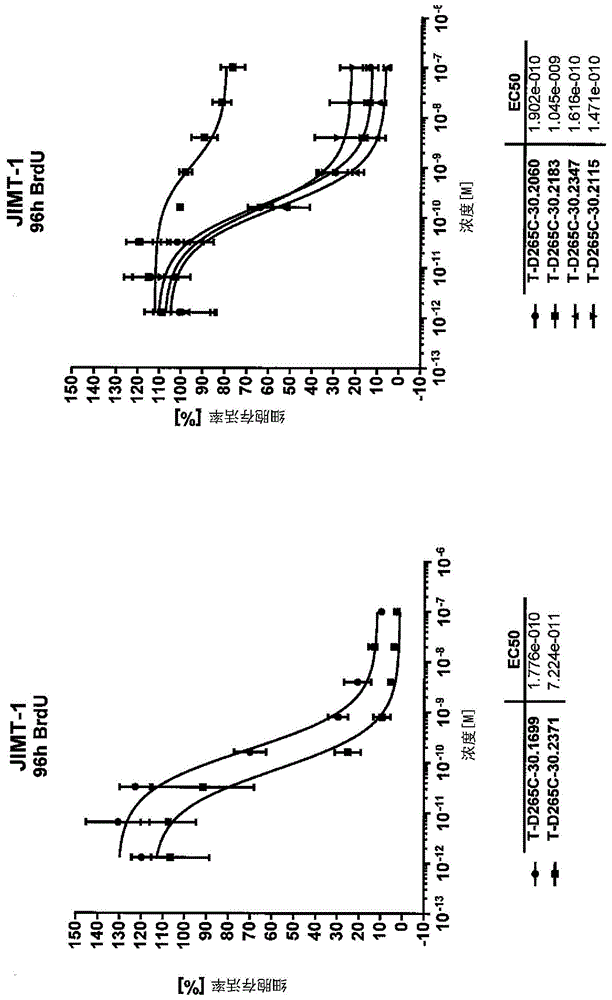
发明领域本申请涉及用于治疗实体瘤的靶向鹅膏毒素缀合物。发明背景实体瘤的治疗是一个持续的挑战,在过去的几十年中进展甚微。尽管最近已经开发了相当多新的治疗方式,但是仍然需要进一步的改进,以增加患有实体瘤的患者的存活率并改善其生活质量。一种有前途的治疗方式是抗体药物缀合物,其中具有杀死细胞能力的高毒性实体与使毒素穿梭到疾病部位的靶结合实体偶联。申请人在过去已经开发了所谓的atac,即,抗体靶向的鹅膏蕈碱缀合物,其中鹅膏蕈碱毒素与高度靶特异性抗体偶联。鹅膏蕈碱是八个氨基酸的双环肽,其天然存在于蘑菇的鹅膏属的数个物种中,一种是死帽蕈(鬼笔鹅膏(amanitaphalloides))。鹅膏蕈碱具有以下一般结构:鹅膏毒素以非常高的亲和力与rna聚合酶ii结合,导致分裂细胞和静止细胞的蛋白质合成急剧下降,并最终导致细胞凋亡(cochet-meilhac和chambon,1974;cochet-meilhac等人,1974)。α-鹅膏蕈碱仅与rna聚合酶iii轻微结合,并显示出与rna聚合酶i没有结合。当与rna聚合酶ii结合时,鹅膏蕈碱抑制酶在rna和dna上的易位,因此转录速率会减慢1000倍以上,最终导致细胞凋亡。当前正在开发的一种atac称为hdp101,并且公开在pct申请pct/ep2017/084431中。它包含鹅膏毒素,该鹅膏毒素具有6′-脱氧位置的氨基酸4(上图中=r4);和s-脱氧位置的氨基酸8。连接基是pabvalala连接基。该鹅膏毒素经由氨基酸1和与其缀合的可裂解连接基与称为j22.9-isy的抗bcma结合抗体缀合。hdp101中使用的鹅膏毒素连接基缀合物的结构称为30.2115,并示于本文下表中。该atac在恶性血液病,特别是淋巴瘤的治疗中显示出非常好的效力。这种恶性血液病在本文中也称为“液体瘤”。但是,申请人已经意识到,在实体瘤的治疗方面仍然有改进的空间,实体瘤是比液体瘤更具挑战性的ataca的靶标。因此,本发明的一个目的是提供实体瘤的新治疗选择。本发明的另一个目的是改善atac在实体瘤中的效力。这些和其他目的通过根据本发明的独立权利要求的方法和手段来实现。从属权利要求涉及特定实施方案。发明概述本申请提供用于治疗实体瘤的靶向鹅膏毒素缀合物。下面将详细讨论本发明及其特征的一般益处。附图简要说明以下列表给出附图及其内容的概述:发明详述在详细描述本发明之前,应当理解,本发明不限于所描述的设备的特定组成部分或所描述的方法的过程步骤,因为这样的设备和方法可以变化。还应理解,本文所使用的术语仅出于描述特定实施方案的目的,而无意于进行限制。必须注意,如说明书和所附权利要求书中所使用的,单数形式“a”,“an”和“the”包括单数和/或复数所指对象,除非上下文另外明确指出。此外要理解的是,在给出由数值界定的参数范围的情况下,该范围被认为包括这些限制值。还应理解,本文中所公开的实施方案并不意味着应理解为彼此不相关的单个实施方案。关于一个实施方案讨论的特征也旨在公开结合本文中所示的其他实施方案。如果在一种情况下,特定特征没有被一个实施方案公开,但是被另一个实施方案公开,则本领域技术人员会理解这不一定意味着所述特征没有意图被所述其他实施方案公开。本领域技术人员会理解,针对其他实施方案也公开所述特征是本申请的主旨,但是仅仅为了清楚的目的并且将说明书保持在可管理的大小,这尚未进行。此外,本文中引用的现有技术文件的内容通过援引加入。尤其是对于公开标准或常规方法的现有技术文件而言。在那种情况下,通过援引加入的主要目的是提供足够的使能公开,并避免冗长的重复。根据第一方面,提供式(i)的包含鹅膏毒素的鹅膏毒素-连接基构建体其中:·r1和r2各自为-oh·r3是nh2,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基,·r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基,·r5不存在或为=o,其中r3和r4不能相同。所述构建体提供用于制备用于治疗实体瘤的结合部分-毒素缀合物。这些构建体的关键特征之一是在分子的氨基酸4(trp)的吲哚环中4位上的-or4取代基。发明人令人惊讶地表明,包含这样的鹅膏毒素连接基构建体的结合部分-毒素缀合物对实体瘤或其中包含的细胞具有优异的效力。当与结构相似的结合部分-毒素缀合物(在4位上不具有-or4,而是具有氢取代基)相比时特别如此。有趣的是,如在pct申请pct/ep2017/084431中所公开的,如果两个变体都具有相当的效力,则在液体瘤的治疗中不可观察到这种明显的差异。如本文所用,术语“实体瘤”涉及影响除了血液、骨髓和淋巴系统之外的身体组织或器官的所有癌症类型。如本文所用,术语“液体瘤”涉及在患者的体液(例如血液,骨髓或淋巴)中发生的任何癌症或恶性肿瘤,包括白血病、淋巴瘤和骨髓瘤。重要的是要理解,-or4可以是-oh或-o-连接基。特别地,如果连接基是可裂解连接基或自降解(selfimmolative)连接基,则所述连接基会随着时间而降解,并且降解的最后步骤将会导致-o-连接基键水解,从而释放-oh。由于这个原因,裂解/降解会提供6-oh-trp。根据一个实施方案,所述连接基是可裂解连接基和/或自降解连接基。如本文所用,术语“可裂解连接基”涉及通常在细胞内条件下易于裂解的连接基。合适的可裂解连接基包括,例如,可被细胞内蛋白酶诸如溶酶体蛋白酶或核内体蛋白酶理解的肽连接基。在示例性实施方案中,所述连接基可以是二肽连接基,诸如缬氨酸-瓜氨酸(val-cit)、缬氨酸-丙氨酸(val-ala)、苯丙氨酸-赖氨酸(phe-lys)连接基,或马来酰亚胺基己酸-缬氨酸-瓜氨酸-对氨基苄氧基羰基(mc-val-cit-paba)连接基。这样的连接基例如公开在美国专利号6214345中。另一连接基是磺基琥珀酰亚胺基-44n-马来酰亚胺基甲基]环己烷-1-羧酸酯(smcc)。磺基-smcc缀合是通过马来酰亚胺基团进行的,所述基团与巯基(硫醇,-sh)反应,而其磺基-nhs酯则对伯胺(如赖氨酸和蛋白质或肽n端所存在的)具有反应性。又一种连接基是马来酰亚胺基己酰基(mc)。其他合适的连接基包括在特定ph或ph范围下可水解的连接基,诸如腙连接基。其他合适的可裂解连接基包括二硫化物连接基。连接基可以与抗体共价结合至使得抗体必须在细胞内降解以便药物释放的程度,例如mc连接基等。ep3130587中公开了包括环状亚苄基缩醛连接基的其他ph敏感性可裂解连接基。如本文所用,术语“自降解连接基”涉及在发生初始反应后自发降解的连接基。自降解连接基的一个实例是对氨基苄醇(pab),其通常经由芳香胺基团与可裂解二肽如缬氨酸-瓜氨酸(val-cit)或缬氨酸-丙氨酸(val-ala)缀合,并且经由氨基甲酸酯基团与毒素的伯胺或仲胺缀合。用合适的蛋白酶裂解二肽触发pab的1,6-消除和pab中的二氧化碳,以及游离毒素的伴随释放。对氨基苄基部分也可以通过烷基化直接与毒素的氨基、羟基或酚基偶联。然后通过苄胺或苄醚键的1,6-消除至断裂,伴随毒素的释放来产生二肽的裂解。通过以下例示(但不限于)用于该基于pab的自降解体系的其他蛋白酶触发器:可被基质金属蛋白酶(mmpii)裂解的甘氨酸-脯氨酸-亮氨酸-甘氨酸(gly-pro-leu-gly)起动力(motive),或可被弹性蛋白酶裂解的丙氨酸-丙氨酸-脯氨酸-缬氨酸(ala-ala-pro-val)起动力。自降解连接基的另一实例由对羟基苯甲醛醇与葡糖醛酸的β-糖苷表示。毒素可以经由芳族环的间位通过上述基团和靶结合部分与苄基碳原子缀合。当β-葡糖醛酸糖苷酶裂解糖苷键时,毒素通过1,6-消除过程释放。根据一个实施方案,所述连接基可被选自下列中的至少一种物质裂解:·半胱氨酸蛋白酶·金属蛋白酶·丝氨酸蛋白酶·苏氨酸蛋白酶·天冬氨酸蛋白酶半胱氨酸蛋白酶(也称为硫醇蛋白酶)是降解蛋白质的酶。这些蛋白酶具有共同的催化机制,所述机制涉及催化三联体或二联体中的亲核半胱氨酸硫醇。半胱氨酸蛋白酶常见于包括番木瓜、菠萝、无花果和猕猴桃的水果中。merops蛋白酶分类系统具有在c下的半胱氨酸蛋白酶。金属蛋白酶是其催化机理涉及金属的蛋白酶。大多数金属蛋白酶需要锌,但有些使用钴。金属离子经由三个配体与蛋白质配位。配位金属离子的配体可随组氨酸、谷氨酸、天冬氨酸、赖氨酸和精氨酸而变化。第四配位位置由不稳定的水分子占据。丝氨酸蛋白酶是裂解蛋白质中的肽键的酶,其中丝氨酸在(酶的)活性位点充当亲核氨基酸。在真核生物和原核生物中都普遍发现它们。丝氨酸蛋白酶根据其结构分为两大类:胰凝乳蛋白酶样(胰蛋白酶样)或枯草杆菌蛋白酶样。merops蛋白酶分类系统具有在s下的半胱氨酸蛋白酶。苏氨酸蛋白酶是在活性位点内携带苏氨酸(thr)残基的蛋白水解酶家族。这类酶的原型成员是蛋白酶体的催化亚单位,然而,酰基转移酶趋同地演化出相同的活性位点几何结构和机理。天冬氨酸蛋白酶是一种催化类型的蛋白酶,其使用与一个或多个天冬氨酸残基结合的活化水分子来催化其肽底物。通常,它们在活性位点中具有两个高度保守的天冬氨酸,并且在酸性ph下具有最佳活性。胃蛋白酶抑制剂抑制几乎所有已知的天冬氨酰蛋白酶。merops蛋白酶分类系统具有在a下的半胱氨酸蛋白酶。在特定的实施方案中,所述连接基可被选自下列中的至少一种物质裂解:·组织蛋白酶a或b·基质金属蛋白酶(mmp)·弹性蛋白酶·β-葡糖醛酸糖苷酶·β-半乳糖苷酶根据又一个实施方案,所述连接基包含选自下列的基序:·valala·valcit·vallys·valarg·phelysglyproleugly·alaalaproval·β-葡糖苷酸·β-半乳糖苷。根据又一个实施方案,所述连接基中的反应性基团y为选自下列中的至少一种:·马来酰亚胺·3,4-二苯基硫基-马来酰亚胺·4,5-双(2-吡啶基-硫烷基)-1,2-二氢哒嗪-3,6-二酮·dbco·dibo·hips·2-(4-羟苯基)-5-(甲基磺酰基)-1,3,4-噁二唑·apn·琥珀酰亚胺·琥珀酰亚胺基氨基甲酸酯·溴乙酰胺·碘乙酰胺根据又一个实施方案,所述连接基包含对氨基苯valala马来酰亚胺基丙基基序。根据又一个实施方案,鹅膏毒素-连接基构建体中的连接基是不可裂解连接基。术语“稳定的连接基”和“不可裂解连接基”在本文可互换使用。通常,在结合部分(即毒素连接基构建体所缀合的单克隆抗体)在细胞内(例如在溶酶体中)降解后,不可裂解连接基释放药物。代表性的不可裂解连接基是马来酰亚胺烷烃连接基:另一代表性的不可裂解连接基是ado-曲妥珠单抗emtansine(t-dm1)中使用的smcc连接基。在一个实施方案中,r3不是不可裂解连接基。在另一个实施方案中,r3是可裂解连接基,优选地是自降解连接基。在另一个实施方案中,r4是不可裂解连接基、可裂解连接基或自降解连接基。根据又一个实施方案,所述鹅膏毒素-连接基构建体具有选自下列的式:a)b)c)d)表1:这四种鹅膏毒素-连接基构建体的一些分子特征。根据又一个实施方案,提供用于制备用于治疗实体瘤的结合部分-毒素缀合物的所述鹅膏毒素-连接基构建体,其中所述实体瘤对其中鹅膏毒素在吲哚的6’-位不包含-or4取代基的结合部分-毒素缀合物有抗性。根据本发明的另一方面,提供结合部分-毒素缀合物,所述缀合物用于治疗(i)对实体瘤进行诊断,(ii)患有实体瘤,或(iii)处于发生实体瘤的风险的人或动物个体,所述缀合物包含:(a)以上描述的鹅膏毒素-连接基构建体,和(b)靶结合部分;且其中所述连接基连接所述鹅膏毒素和所述靶结合部分。根据本发明的另一方面,提供这样的结合部分-毒素缀合物,其用于制备用于治疗(i)对实体瘤进行诊断,(ii)患有实体瘤,或(iii)处于发生实体瘤的风险的人或动物个体的药物。根据本发明的另一方面,提供用于治疗或预防实体瘤的方法,所述方法包括向需要其的个体给药有效量的这样的结合部分-毒素缀合物。根据本发明的一个实施方案,所述靶结合部分是抗体、抗体片段、基于抗体的结合蛋白或抗体模拟物,它们都保留靶结合特性。如本文所用,“抗体”优选是单克隆抗体。如本文所用,术语“单克隆抗体(mab)”应指具有均一抗体群的抗体组合物,即,由完整免疫球蛋白或其保留靶结合能力的片段或衍生物组成的均一群。特别优选的是,这样的抗体选自igg、igd、ige、iga和/或igm,或其保留靶结合能力的片段或衍生物。如本文所用,术语“抗体片段”应指保留靶结合能力的这样的抗体的片段,例如,·cdr(互补决定区)·高变区·可变域(fv)·igg重链(由vh、ch1、铰链、ch2和ch3区组成)·igg轻链(由vl和cl区组成),和/或·fab和/或f(ab)2。其他实施方案包括骆驼抗体、鲨鱼抗体、由vh和ch1结构域组成的fab(fd)片段的重链部分;可变片段(fv)片段;结构域抗体(dab)片段,其包含单个可变结构域、单链fv片段(scfv);(viii)双抗体;线性抗体,其包含与互补性轻链多肽一起形成一对抗原结合区的一对串联fv片段(vh-ch1-vh-ch1);以及免疫球蛋白重链和/或轻链的其他非全长部分,或其突变体、变体或衍生物,单独的或任何组合。如本文使用的基于抗体的结合蛋白在其他非免疫球蛋白或非抗体衍生组分的情况下包含至少一种抗体衍生的vh、vl或ch免疫球蛋白结构域。如本文所用的抗体模拟物是一种有机化合物,其与抗体一样可以特异性结合抗原,但在结构上与抗体不相关。该定义涵盖例如锚蛋白重复蛋白、c型凝集素、金黄色葡萄球菌(s.aureus)的a结构域蛋白、转铁蛋白、脂质运载蛋白、纤连蛋白的第10种iii型结构域、kunitz结构域蛋白酶抑制剂、泛素衍生的结合物、γ晶体蛋白衍生的结合物、半胱氨酸结或结蛋白(knottin)、基于硫氧还蛋白a支架的结合物、核酸适配子、通过聚合物分子印迹产生的人工抗体、细菌基因组的肽库、sh-3结构域、stratobody、通过二硫键和ca2+稳定化的膜受体的“a结构域”、基于ctla4的化合物、fynsh3和适配子。根据一个实施方案,所述靶结合部分结合选自下列中的至少一种靶:·her2,和/或·psma。根据本发明的一个实施方案,所述靶结合部分为选自下列中的至少一种抗体:·曲妥珠单抗,和/或·h3/f11。发明人发现,当皮下施用时,诸如raji或raji-luc的肿瘤细胞生长为具有界定的结构和结缔组织的均一实体瘤。这些皮下植入的肿瘤细胞指示实体瘤,因为给出了实体瘤的重要特性,诸如穿透障碍和扩散障碍。此外,皮下模型通常是旨在用于治疗癌症的新药物临床前开发的先决条件。然而,当静脉内注射时,raji或raji-luc会发展成液体瘤(例如白血病)的表型。由于这个原因,raji或raji-luc是用以显示所要求保护的毒素连接基缀合物在治疗实体瘤对液体瘤中的不同作用的合适的模型。抗体h3/f11的cdr序列在ep2363486中公开,其内容通过援引加入。根据本发明的一个实施方案,所述实体瘤为选自下列中的至少一种:a)肉瘤,b)母细胞瘤,和/或c)癌。根据本发明的一个实施方案,所述实体瘤对其中鹅膏毒素在吲哚的6’-位不包含-or4取代基的结合部分-毒素缀合物有抗性。根据本发明的一个实施方案,所述抗体或其片段或衍生物包含工程化的半胱氨酸残基。在一个实施方案中,连接基与所述半胱氨酸的游离sh基团缀合。因为半胱氨酸是人为地引入抗体的氨基酸序列中,所以将其用作缀合位点不会影响抗体的链内和链间二硫桥的形成,因此其稳定性不受影响。优选地,将这样的半胱氨酸引入抗体的恒定结构域,以不影响抗体的靶结合。该缀合方法的原理在junumla等人(2008)中公开,其内容通过援引加入。根据本发明的一个实施方案,根据edelman等人,proc.natl.acad.sci.usa;63(1969)78-85的eu编号系统,所述半胱氨酸残基选自重链118cys、重链239cys和重链265cys。本实验中使用的抗体在两个fc结构域中均包含d265c置换,以提供具有这样的游离sh基团的半胱氨酸残基。各自技术公开在转让给本申请人的wo2016142049a1中(其内容通过援引加入),并提供具有为2的固定药物与抗体的比率(“dar”)和位点特异性缀合的均一产物。发明人进一步表明,使用d265c作为缀合具有额外效果,因为d265参与抗体fc区与一种或多种fc[γ]受体的结合相互作用,导致与一种或多种fc[γ]受体的受损结合。这样的抗体或抗体鹅膏毒素缀合物在个体中可表现出降低的免疫调节应答(如adcc、adcp和/或cdc应答,这是由与fc[γ]受体结合的抗体引起的),并因此可有助于减少不良副作用。根据本发明的一个实施方案,提供缀合物,其用于治疗(i)对实体瘤进行诊断,(ii)患有实体瘤,或(iii)处于发生实体瘤的风险的人或动物个体,其中所述实体瘤对其中鹅膏毒素在吲哚的6’-位不包含-or4取代基的结合部分-毒素缀合物有抗性。根据本发明的又一方面,提供药物组合物,其用于治疗(i)对实体瘤进行诊断,(ii)患有实体瘤,或(iii)处于发生实体瘤的风险的人或动物个体,所述组合物包含如上所述的结合部分-毒素缀合物。根据本发明的另一方面,提供这样的组合物用于制备用于治疗(i)对实体瘤进行诊断,(ii)患有实体瘤,或(iii)处于发生实体瘤的风险的人或动物个体的药物。根据本发明的另一方面,提供了用于治疗或预防实体瘤的方法,所述方法包括向需要其的个体给药有效量的这样的组合物。实施例尽管已经在附图和前面的描述中详细地说明和描述了本发明,但是这样的说明和描述应被认为是说明性或示例性的而不是限制性的;本发明不限于所公开的实施方案。通过研究附图、公开内容和所附权利要求书,本领域技术人员在实施所要求保护的发明时可以理解和实现所公开的实施方案的其他变体。在权利要求书中,单词“包含”不排除其他元素或步骤,并且不定冠词“a”或“an”不排除多个。在互不相同的从属权利要求中记载某些方案的事实并不表示不能有利地使用这些方案的组合。权利要求中的任何参考标志都不应被解释为限制范围。本文公开的所有氨基酸序列均显示为从n末端到c末端;本文公开的所有核酸序列均显示为5’->3’。材料和方法1.鹅膏毒素连接基缀合物在本文所述的实验中,使用了四种靶向鹅膏毒素连接基缀合物,它们落在本发明的范围内,这意味着它们具有与连接基未缀合或缀合的6-ohtrp残基,如式(i)中r4所提及。此外,使用了两种靶向鹅膏毒素连接基缀合物,它们不落在本发明的范围内,因为它们包含缺少6-or取代基的trp。这些分子被用作基准以证明所要求保护的构建体和缀合物在实体瘤的治疗中的效力增加。以下显示本研究中使用的六种鹅膏毒素连接基缀合物:2.抗体以下抗体与鹅膏毒素连接基缀合物缀合曲妥珠单抗和h3/f11已经在上面进行了描述。chibce19已在lüttgau等人2013中使能地公开。3.缀合技术借助于所谓的thiomab技术使抗体与鹅膏毒素连接基缀合物缀合。在该方法中,缀合是通过毒素连接基构建体的马来酰亚胺残基与抗体中的半胱氨酸残基的游离sh基缀合而进行的,如以下反应路线所示:该缀合方法的原理在junutula等人(2008)中公开,其内容通过援引加入。本实验中使用的抗体在两个fc结构域中包含d265c置换,以提供具有这样的游离sh基团的半胱氨酸残基。各自的技术公开在转让给本申请人的wo2016142049a1中(其内容通过援引加入),并提供具有为2的固定药物与抗体的比率(“dar”)和位点特异性缀合的均一产物。3.测定3.1.细胞存活率测定使用靶-阳性肿瘤细胞系和化学发光brdu掺入法(rochediagnostics)在体外评估抗psma和抗her2鹅膏毒素缀合物的细胞毒活性。通过在bmglabtechoptima酶标仪中用抗brdu-hrp抗体测量固定和透化的细胞,在37℃和5%co2下用不同浓度的缀合物孵育96小时后,测定细胞存活率。通过graphpadprism4.0软件计算剂量响应曲线的ec50值。通过96孔组织培养板中的celltiter-glo2.0发光细胞存活率测定(promega,madison,wi)评估抗cd19鹅膏毒素缀合物对靶阳性细胞的细胞毒活性。在37℃和5%co2下用不同浓度的缀合物孵育96小时后,测定细胞存活率。数据分析使用graphpadprism7(graphpadsoftware,inc,lajolla,ca)软件进行,以绘制曲线拟合并进行统计分析。非线性可变斜率曲线拟合绘制为log[adc]相对于响应,并生成ec50值。3.2.异种移植物/肿瘤体积lncap异种移植物模型:对雄性cb17scid小鼠在右侧腹部中,每只小鼠皮下接种2.5x106个lncap前列腺癌细胞。在~150mm3的平均肿瘤体积下,在第0天将动物分配到各组。在同一天,动物接受单次静脉内剂量的基于鹅膏蕈碱的抗psma抗体药物缀合物(adc)。每周两次测定肿瘤体积和体重。jimt-1异种移植物模型:对雌性nmri裸鼠在右侧腹部中,每只小鼠皮下接种5x106个jimt-1乳腺癌细胞。在~120mm3的平均肿瘤体积下,在第0天将动物分配到各组。在同一天,动物接受单次静脉内剂量的基于鹅膏蕈碱的抗her2抗体药物缀合物(adc)。每周两次测定肿瘤体积和体重。raji异种移植物模型:对雌性cb17scid小鼠在右侧腹部中,每只小鼠皮下接种2.5x106个raji伯基特淋巴瘤细胞。在~80mm3的平均肿瘤体积下,在第0天将动物分配到各组。在同一天,动物接受单次静脉内剂量的基于鹅膏蕈碱的抗cd19抗体药物缀合物(adc)。每周两次测定肿瘤体积和体重。通过卡尺测量来监测肿瘤生长。根据以下公式计算肿瘤大小:体积=w2xlx0.5(l=长度,w=肿瘤的垂直宽度,l>w)。3.3.异种移植物/存活率静脉内nalm-6异种移植物模型:对雌性cb17scid小鼠,每只小鼠用2.5x106raji伯基特淋巴瘤细胞接种到尾静脉中。在第0天将动物分配到各组。注射肿瘤细胞后的第3天,动物接受单次静脉内剂量的基于鹅膏蕈碱的抗cd19抗体药物缀合物(adc)。每周两次测定体重。每天监测存活率。静脉内raji异种移植物模型:对雌性cb17scid小鼠,每只小鼠用5x106nalm-6b细胞前体白血病细胞接种到尾静脉中。在第0天将动物分配到各组。注射肿瘤细胞后的第3天,动物接受单次静脉内剂量的基于鹅膏蕈碱的抗cd19抗体药物缀合物(adc)。每周两次测定体重。每天监测存活率。3.4.缀合物chibce19-d265c-30.2115的合成3.4.1.hdp30.2060与10mgchibce19-d265c的缀合pbs缓冲液中的10mgthiomabchibce19-d265c会用于与hdp30.2060缀合。·将抗体溶液调节至1mmedta:ο2ml抗体溶液(10.0mg)+20μl100mmedta,ph8.0ο抗体量:10mg=6.8x10-8mol3.4.2.通过抗体与40当量tcep反应使半胱氨酸解封端:·2ml抗体溶液(6.8x10-8mol)+54.5μl50mmtcep溶液(2.72x10-6mol)·在摇床上于37℃下孵育3小时。·在slide-a-lyzer透析盒20′000mwco中,在2.0i1xpbs、1mmedta,ph7.4中于4℃下进行两次连续透析,第一次透析约4小时,第二次透析过夜·使用amicon超离心过滤器50′000mwco,浓缩至约4.0ml3.4.3.通过抗体与20当量脱氢抗坏血酸(dhaa)的反应进行氧化:·约2ml抗体溶液(6.8x10-8mol)+27.2μl新鲜的50mmdhaa溶液(1.36x10-6mol)·在摇床上于室温下孵育3小时。3.4.4.使用6当量hdp30.2060与鹅膏蕈碱缀合,并用25当量n-乙酰基-l-半胱氨酸淬灭:·使0.7mghdp30.2060溶解在70μldmso=10μg/μl中ο约2ml抗体溶液(=9.5mg;6.46x10-8mol)+50.9μlhdp30.2060(=509μg;3.88×10-7mol)。ο在室温下孵育1小时。ο通过加入16μl100mmn-乙酰基-l-半胱氨酸(1.62x10-6mol)进行淬灭。ο在室温下孵育15分钟(或在4℃下过夜)。ο利用1xpbs,ph7.4平衡的pd-10柱来纯化各反应混合物。用封口膜上的bradford试剂鉴定含蛋白质的馏分,并将含蛋白质的馏分聚集在一起。ο在2.0ipbs,ph7.4和slide-a-lyzer透析盒20′000mwco中于4℃下过夜来透析各抗体溶液。3.4.5.使用调节至相同蛋白质浓度的裸抗体相对于adc通过紫外光谱(在280nm和310nm处的吸收)测定蛋白质浓度和药物-抗体比率(dar)。3.4.6.将蛋白质浓度调节至5.0mg/ml(3.4x10-5m),并通过过滤使其达到无菌条件。储存在4℃下。4.细胞系使用了以下细胞系her2阳性psma阳性cd19阳性jimt-1lncaprajiskbr-322rv1rajilucbt474mda-pca2bnalm-6nci-n87c4.2mec-2除了raji、nalm-6和mec-2细胞系,所使用的细胞系来自实体瘤,而raji是造血来源的第一连续的人细胞系。非常重要的是,当静脉注射到小鼠中时,cd19阳性的raji细胞发展成白血病表型,而当皮下注射到小鼠中时,发展成实体瘤表型。结果1.与曲妥珠单抗缀合的毒素-连接基构建体将细胞存活率测定用于jimt-1细胞,所述jimt-1细胞用与曲妥珠单抗(药库条目:db00072)(在fc结构域中具有d265c置换)缀合的上文讨论的毒素-连接基构建体进行处理。jimt-1是衍生自乳腺导管腺癌的实体癌细胞。结果示于图1中。6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)30.1699、30.2371、30.2060和30.2347显示出相当的效力,而trp变体30.2115显示出略微降低的效力,并且trp变体30.2183显示出显著降低的效力。用均表达不同程度的her2的衍生自实体瘤的三个其它癌细胞系(skbr-3、bt474和nci-n87)重复图1所示的实验。在所有细胞系中观察到几乎相同的模式。在所有情况下,6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)显示出比trp变体(其中鹅膏蕈碱的trp残基中的6位被h基团取代)更高的细胞毒性潜力。表2:不同细胞系上的缀合物的ec50值[m]缀合物特征jimt-1skbr-3bt474nci-n87t-d265c-30.1699so;6-oh-w;aa41.8x10-109.9x10-126.8x10-111.2x10-11t-d265c-30.2371s;6-oh-w;aa47.2x10-111.6x10-124.6x10-119.5x10-12t-d265c-30.2060so;6-oh-w;aa11.9x10-10(10%)2.6x10-111.1x10-101.6x10-11t-d265c-30.2347s;6-oh-w;aa11.6x10-107.9x10-126.4x10-113.7x10-11t-d265c-30.2115s;w;aa11.5x10-10(25%)5.8x10-125.6x10-115.1x10-11t-d265c-30.2183so;w;aa1nfb4.2x10-114.2x10-102.4x10-10粗体印刷:最高的细胞毒性潜力;斜体:最低的细胞毒性潜力。“so”意指式(i)的鹅膏蕈碱的r5=o,“s”意指式(i)的鹅膏蕈碱的r5不存在,“6-oh-w”意指具有or4的式(i)中所示的实施方案,“w”是意指其中鹅膏蕈碱的trp残基中的6位被h基团取代的不是根据本发明的实施方案,并且“aa4/aa1”意指与连接基缀合的鹅膏蕈碱中的氨基酸残基。“nfb”意指:具有>50%残余细胞存活率的非全面爆发细胞毒性潜力。然后利用jimt细胞的肿瘤异种移植物进行生长抑制实验,该jimt细胞的肿瘤异种移植物然后用与曲妥珠单抗(药库条目:db00072)(在fc结构域中具有d265c置换)缀合的上文讨论的毒素-连接基构建体进行处理。结果示于图2中。6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)30.1699、30.2371、30.2060和30.2347显示出强的肿瘤收缩活性(图2),而trp变体30.2115和30.2183显示出显著降低的肿瘤收缩活性(图2b)。2.与抗psma抗体缀合的毒素-连接基构建体将细胞存活率测试用于lncap细胞,所述lncap细胞用与抗psma抗体h3/f11(在fc结构域中具有d265c置换)缀合的上文讨论的毒素-连接基构建体进行处理。lncap是衍生自左锁骨上淋巴结转移瘤的实体前列腺腺癌细胞系。结果示于图3中。6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)30.1699、30.2371、30.2060和30.2347显示出相当的效力,而trp变体30.2115和30.2183显示出显著降低的效力。用均表达不同程度的psma的三个其它实体癌细胞系(22rv1、mda-pca2b和c4.2)来重复图3所示的实验。在所有细胞系中观察到几乎相同的模式。在所有情况下,6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)显示出比trp变体(其中鹅膏蕈碱的trp残基中的6位被h基团取代)更高的细胞毒性潜力。表3:不同细胞系上的缀合物的ec50值[m]粗体印刷:最高的细胞毒性潜力;斜体:最低的细胞毒性潜力。“so”意指式(i)的鹅膏蕈碱的r5=o,“s”意指式(i)的鹅膏蕈碱的r5不存在,“6-oh-w”意指具有or4的式(i)中所示的实施方案,“w”是意指其中鹅膏蕈碱的trp残基中的6位被h基团取代的不是根据本发明的实施方案,并且“aa4/aa1”意指与连接基缀合的鹅膏蕈碱中的氨基酸残基。“nfb”意指:具有>50%残余细胞存活率的非全面爆发细胞毒性潜力。(x%)意指残余存活率。然后利用lncap细胞的肿瘤异种移植物进行生长抑制实验,该lncap细胞的肿瘤异种移植物然后利用与抗psma抗体h3/f1(在fc结构域中具有d265c置换)缀合的上文讨论的毒素-连接基构建体进行处理。结果示于图4中。6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)30.1699、30.2371、30.2060和30.2347显示出强的肿瘤收缩活性(图4a、b),而trp变体30.2115和30.2183显示出显著降低的肿瘤收缩活性(图4c)。3.与抗cd19抗体缀合的毒素-连接基构建体将细胞存活率测试用于raji细胞,该raji细胞用与抗cd19抗体chibce19(在fc结构域中具有d265c置换)缀合的上文讨论的毒素-连接基构建体进行处理。raji是衍生自伯基特淋巴瘤的细胞系。在该情况下,6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)30.1699、30.2371、30.2060和30.2347以及trp变体30.2115和30.2183均显示相当的效力。用均表达不同程度的cd19的两个其它癌细胞系(raji-luc和mec-2)来重复图5所示的实验。在所有细胞系中观察到几乎相同的模式。在所有情况下,6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)显示出与trp变体(其中鹅膏蕈碱的trp残基中的6位被h基团取代)相当的细胞毒性潜力。表4:不同细胞系上的缀合物的ec50值[m]粗体印刷:最高的细胞毒性潜力;斜体:最低的细胞毒性潜力。“so”意指式(i)的鹅膏蕈碱的r5=o,“s”意指式(i)的鹅膏蕈碱的r5不存在,“6-oh-w”意指具有or4的式(i)中所示的实施方案,“w”是意指其中鹅膏蕈碱的trp残基中的6位被h基团取代的不是根据本发明的实施方案,并且“aa4/aa1”意指与连接基缀合的鹅膏蕈碱中的氨基酸残基。“nfb”意指:具有>50%残余细胞存活率的非全面爆发细胞毒性潜力。(x%)意指残余存活率。然后用通过各自细胞的静脉内给药获得的raji细胞(有或没有转染的荧光素酶)或nalm-6细胞的肿瘤异种移植物研究存活率。然后用单次静脉注射剂量的与抗cd19抗体chibce19(在fc结构域中具有d265c置换)缀合的上文讨论的毒素-连接基构建体来处理小鼠。raji是衍生自伯基特淋巴瘤的细胞系,nalm-6是衍生自急性淋巴细胞白血病(all)的细胞系。结果示于图6的kaplan-meier曲线中。当静脉内给药时,raji以及nalm-6细胞发展出模拟白血病(即,液体瘤)的表型,而当皮下给药时,仅raji细胞发展出模拟实体瘤的表型,而nalm-6细胞仍然发展成液体瘤。利用静脉注射的rajiluc(图6a)或nalm6(图6b)进行存活率实验。在所有情况下,结果是具有6-ohtrp(30.1699)的变体具有比trp变体30.2115更低的效力。然后利用皮下注射入小鼠的raji细胞的肿瘤异种移植物进行生长抑制实验。该方法产生模拟实体瘤表型的肿瘤。用与抗cd19抗体chibce19(在fc结构域中具有d265c置换)缀合的上文讨论的毒素-连接基构建体进行处理。6‘-羟基-trp变体(其中式(i)的r4是h,或带有用于将所述鹅膏毒素连接至靶结合部分的反应性基团y的连接基)30.1699、30.2371、30.2060和30.2347显示出强的肿瘤收缩活性(图7a),而trp变体30.2115和30.2183显示出显著降低的肿瘤收缩活性(图7b)。*不是根据本发明的鹅膏毒素连接基构建体。mtd:最大耐受剂量,hnstd:最高的非严重毒性剂量,cyno:食蟹猴,dig:不与宿主靶交叉反应的地高辛抗体参考文献:junutula等人,nat.biotechnol.26(8),925-932(2008)lüttgau等人,antibodies(2013)2,338-352当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1