具有对医学病症的严重性预测和可视化的患者监测系统和方法与流程
背景技术:
本公开整体涉及包括测量两个或更多个生理参数的患者监测系统和方法,并且更具体地,涉及基于所测量的生理数据参数的参数数据来跟踪、可视化和预测特定医学病症的严重性的方法和系统。
在医学领域中,医师通常希望持续监测其患者的多种生理特性。通常,对多种生理特性或参数的此类监测涉及同时使用若干监测设备,诸如脉搏血氧计、血压监测器、心脏监测器、温度监测器等。这些监测设备可以是位于较大的多功能患者监测设备内的单独设备或元件。另外的监测、治疗和/或配套设备和系统还可连接到患者或与患者相关联,诸如用于递送流体、药物、麻醉、呼吸辅助、患者请求的辅助、实验室/成像结果、emr/ehr通知/警示等,或者分析各种患者相关数据以确定病症或患者状态并警示临床医生该病症或患者状态(例如,败血症方案、apache评分、预警评分)。这些设备和系统中的每一者可生成一个或多个告警以向临床医生警示问题,该问题可能是患者的生理或健康状况的问题,或者可能是监测和/或护理递送设备的技术问题。因此,在任何给定时间,一个或多个设备可生成需要引起临床医生注意的告警。
技术实现要素:
提供本发明内容是为了介绍将在下面的具体实施方式中进一步描述的一系列概念。本发明内容不旨在识别要求保护的主题的关键或必要特征,也不旨在用于帮助限制要求保护的主题的范围。
对患者的特定医学病症进行监测的计算机实现的方法的一个实施方案包括:接收至少两个生理参数中的每一者的时间同步参数数据的长时间间隔,以及将长时间间隔划分为多个区段,其中每个区段包含参数数据的预定义时间增量。基于每个区段中的所述参数数据确定所述区段的一组特征值,其中所述一组特征值包括与所述特定医学病症相关的所述预定义的一组特征中的每个特征的特征值。利用训练的机器学习模型,将权重分配给所述预定义的一组特征中的每个特征,然后基于所述一组特征值和权重计算所述长时间间隔内所述特定医学病症的风险严重性指数。
在一个实施方案中,患者监测系统包括一个或多个患者监测器和处理系统,该一个或多个患者监测器测量来自患者的至少两个生理参数以及生成所述至少两个所测量的生理参数中的每一者的参数数据。所述处理系统被配置为接收所述至少两个生理参数中的每一者的时间同步参数数据的长时间间隔,并将所述长时间间隔划分为多个区段,每个区段包含所述参数数据的预定义时间增量。基于每个区段中的所述参数数据确定长时间间隔内的一组特征值,其中所述一组特征值包括与特定医学病症相关的预定义的一组特征中的每个特征的特征值。训练的机器学习模型,诸如逻辑回归模型,为特征值中的每一者分配权重,以根据一组特征值计算长时间间隔内特定医学病症的风险严重性指数。
在对患者的特定医学病症进行监测的计算机实现的方法的另一个实施方案中,接收时间同步参数数据的长时间间隔,包括至少两个生理参数中的每一者的参数数据。时间同步参数数据的长时间间隔被划分为多个区段,其中每个区段包含参数数据的预定义时间增量。确定每个区段中的至少两个生理参数中的每一者的参数数据的斜率。然后基于参数数据的斜率对每个区段进行分类。然后基于每个区段的分类和其中的参数数据确定区段的一组特征值,其中该组特征值包括与特定医学病症相关的预定义的一组特征中的每个特征的特征值。然后基于分类将可视化代码分配给每个区段,并且生长时间序列内描绘每个时间区段的可视化代码的进展图。然后将进展图显示在显示设备上。
从以下结合附图的描述中,本发明的各种其他特征、目的和优点将变得显而易见。
附图说明
参考以下附图描述本公开。
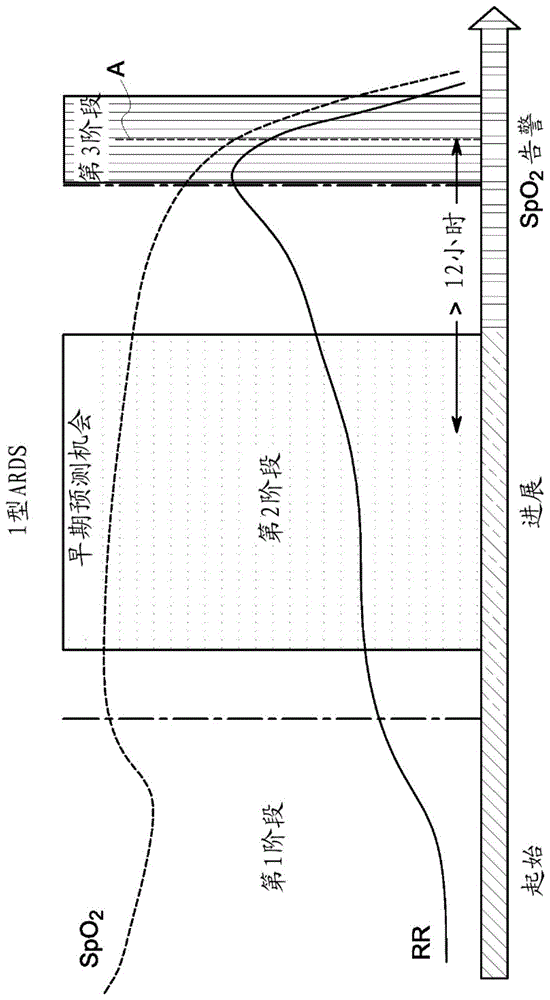
图1为示出急性呼吸窘迫综合征进展期间的两个生理参数包括spo2和呼吸速率的图。
图2是根据本公开的一个实施方案的示例性患者监测系统的示意图。
图3a至图3c为示例性进展图,其示出了基于两个监测到的生理参数的示例性医学病症的进展和严重性。
图4是示出根据本公开的实现训练的机器学习模块的方法的一个实施方案的流程图。
图5是示出训练机器学习模型以接收一组特征值并将权重分配给特征值中的每一者以便生成特定医学病症的风险严重性指数的示例性方法的流程图。
图6是示出根据本公开的预处理原始参数数据的一种示例性方法的流程图。
图7a至图7d为示出在图6中识别的预处理步骤的曲线图。
图8为示出根据本公开的一个实施方案的用于识别示例性的一组特征值的步骤的流程图。
具体实施方式
当前的监测系统和方法在监测特定生理参数的数据时或在监测模式内有效地通知临床医生告警事件的发生。然而,当前的患者监测系统和方法通常不评估或提供关于跨不同生理参数和/或监测模态的比较变化的信息。此外,目前可用的患者监测方法和系统通常无法分析和/或说明生理数据的长期模式或变化,包括在12、24或48小时内发生的较小幅度变化的模式,经单独评估,这些变化不会升高到触发告警的水平。
图1示出了特定医学病症,即1型急性呼吸窘迫综合征(ards)的一个示例,其中早期检测和干预对于改善患者结果而言极其重要。该曲线图示出了外周血氧饱和度值(spo2)和呼吸速率值(rr)。在所示实施方案中,spo2和rr参数数据可表征为与1型ards的进展相关的三个阶段。在第一阶段ards中,spo2正在下降并且rr正在增加。在第二阶段ards中,spo2相对稳定并且rr正在增加。在第三阶段ards中,spo2和rr均快速减小。到生成spo2告警时(虚线a),患者病症已经迅速下降并且患者病症非常严重。
发明人已经认识到存在早期预测机会,诸如图1所示,其中可在医学病症进展到严重状态之前检测到1型ards的进展。鉴于ards像许多医学病症一样在相对较长的时间段内缓慢发展,发明人已经认识到对患者监测数据的长期评估可用于预测某些医学病症的严重性。在所示实施方案中,spo2和rr的进展在大于12小时并且甚至可大于24小时的长时间间隔内发生。因此,发明人已经认识到,需要用于监测和比较来自多个参数的参数数据以便检测与特定医学病症相关联的模式的系统和方法。此外,发明人已经认识到,可利用机器学习模型来识别与特定医学病症最相关的参数数据中的特定特征的模式。在本文所讨论的一个例示性示例中,spo2和rr在24小时时间间隔内用于评估1型ards。
在另一个示例中,医学病症诸如低血容量性休克、内出血和/或动脉瘤休克可基于包括收缩压和心率的生理参数通过风险严重性指数来量化。当血管内容量减小到心血管受损点时发生低血容量性休克,并且低血容量性休克可能是由于通过多种机制的严重脱水导致或由于失血导致。出血可为外出血或内出血。在一些情况下,内出血在低血容量性休克患者中检测不到,从而导致健康状况恶化到危重病症和死亡。低血容量性休克的严重性可通过收缩压的降低和心率随时间推移的相应升高来确定。发明人已经认识到,hr与sysbp之间的这种关系可被视为休克期临床事件,并且用于通过将其视为根据本文提供的公开内容的机器学习模型的特征来量化严重性。
发明人已经认识到,可基于对两个或更多个生理参数的患者监测数据的长期比较分析来早期识别并预测大量的医学病症,并且此类检测和预测可在患者生理状况发生严重变化之前发生。此类早期检测在当前系统中是不可用的,当前系统通常依赖于触发告警条件以便分析患者的生理状况并相应地警示临床医生。然而,患者生理状况的此类显著变化通常指示紧急情况,并且此时对医学病症的识别通常太晚而无法提供预防性或早期治疗,因为医学病症通常已经严重。因此,发明人已经认识到,需要改进的系统和方法来分析患者监测数据,包括多个生理参数的参数数据,以便提供患者医学病症的早期检测。如本文所公开,发明人已开发出利用机器学习模型以基于参数数据的长时间间隔来计算特定医学病症的风险严重性指数的预测算法。该方法涉及在长时间间隔(诸如24小时或更长)内分析至少两个不同的生理参数中的每一者的参数数据。在一个实施方案中,该方法和系统利用机器学习模型,诸如逻辑回归,该逻辑回归被训练为将权重分配给预定义的一组特征中的每个特征,以便计算特定医学病症的风险严重性指数。
图2示出了包括多个感测设备3a-3c的患者监测系统1的示例性实施方案,每个感测设备测量来自患者的不同的生理参数。如本领域普通技术人员将知道的,多参数患者监测构造在患者监测的相关领域中是常见的,诸如其中多个感测设备(例如,3a-3c)将从患者测量的参数数据传送到中心设备或集线器15,或传送到主机网络30。同样为人们所熟知的是,参数数据到集线器15或主机网络30的此类传送可通过有线或无线方式进行。在各种实施方案中,患者监测系统1可监测任一组两个或更多个生理参数,并且各种此类多参数监测构造也是为人们所熟知的。
在图2的示例中,患者监测系统1包括与集线器15通信的三个感测设备3a-3c。每个感测设备3a-3c包括用于测量患者的生理参数的一个或多个传感器9a-9c,并且还包括数据采集设备10a-10c,该数据采集设备接收由传感器9a-9c记录的生理参数测量,并且经由通信链路11a-11c将基于这些测量的参数数据集传输到集线器设备15。在各种实施方案中,通信链路11a-11c可经由有线或无线方式来实现,所述有线或无线方式的示例是人们所熟知的。传感器9a-9c可通过有线或无线方式连接到相应的数据采集设备10a-10c。传感器9a-9c可为本领域中可用于感测或检测患者的生理信息的任何传感器、导联或其他设备,其可包括但不限于电极、导联线或可用的生理测量设备,诸如压力传感器、血压袖带、脉搏血氧仪传感器等。
在所示实施方案中,第一感测设备3a是ecg感测设备,其具有作为ecg电极的传感器9a。第二感测设备3b是非侵入式血压(nibp)感测设备,其具有传感器9b,该传感器为包括其中结合有压力传感器的血压袖带。第三感测设备3c是外周血氧饱和度(spo2)监测仪,其具有作为脉搏血氧仪传感器的传感器9c,诸如被配置用于放置在患者指尖上的标准红外脉搏血氧仪传感器。应当理解,本公开的患者监测系统1不限于所提供的感测设备的示例,但可被配置并且用来感测和监测患者的任何生理参数。本文所提供的示例是出于说明示例性实施方案的目的,并且不应被认为是限制性的。
每个示例性感测设备3a-3c的数据采集设备10a-10c可包括模数(a/d)转换器,其可为能够使由相关的传感器9a-9c所记录的模拟生理信号数字化的任何设备或逻辑集。例如,a/d转换器可为模拟前端(afe)设备。每个数据采集设备10a-10c还可包括处理单元12a-12c,该处理单元从a/d转换器接收数字生理数据并创建生理参数数据以用于传输至集线器设备15和/或主机网络30。每个数据采集设备10a-10c可根据感测设备的类型和功能以不同方式配置,并且可被配置为执行各种信号处理功能和/或传感器控制功能。仅举几例,ecg感测设备3a中的处理单元12a可被配置为对来自ecg传感器9a的数字信号进行滤波以去除伪影和/或基于所记录的心脏数据,诸如心率、qrs间期、st段/间期等来执行各种计算和确定。nibp监测器3b中的处理单元12b可被配置为例如处理由血压袖带中的传感器9b记录的生理数据以计算患者的收缩压值、舒张压值和平均血压值。spo2感测设备3c的处理单元12c可被配置为基于从脉搏血氧仪传感器9c接收的数字化信号来确定患者的血氧合值。
因此,每个处理单元12a-12c可开发生理参数数据,除了所记录的生理数据之外,该生理参数数据还包括从所记录的生理数据测量和/或计算的值。然后,相应的处理单元12a-12c可控制相关感测设备3a-3c中的接收器/发射器5a-5c,以经由通信链路11a-11c将生理参数数据传输到集线器设备15。从相应感测设备3a-3c传输的生理参数数据可包括原始数字化生理数据、过滤后的数字化生理数据和/或指示关于从患者测量的相应生理参数的信息的处理数据。另外,数据采集设备10a-10c中的一个或多个数据采集设备可以被配置为将生理参数数据与一个或多个告警阈值进行比较,以确定告警条件的存在,即,基于生理参数数据检测告警事件。
在相应感测设备3a-3c检测到告警事件时,告警可由感测设备3a-3c(例如,经由扬声器发出的听觉告警和/或经由显示器发出的视觉告警)或集线器15(例如,经由扬声器18和/或显示器16)在移动设备50处(例如,经由扬声器53和/或显示器52)和/或在网络接入点处(诸如中央监测站或护士站的计算机终端)生成。告警的通知可从相应的感测设备3a-3c传输到集线器15,或者可在第一实例中在集线器15处检测到,如上所述。此外,该系统可以各种方式被配置用于临床医生将相应的告警静音,该告警可以经由相应的感测设备3a-3c、在集线器15处或在一些其他位置处诸如经由移动设备50提供。
感测设备3a-3c可与中心集线器15(其可另选地为主要感测设备或其它中心设备)联网,该中心集线器分析参数数据并且调节网络中的各种感测设备3a-3c。在某些实施方案中,集线器15可与主机网络30通信,诸如医疗护理机构的中心网络。感测设备3a-3c可将参数数据传送至主机网络30,诸如间接地通过集线器15。例如,集线器可用作放大器和/或路由器以便在感测设备3a-3c与主机网络30之间通信。在其他实施方案(其可包括或可不包括集线器15)中,感测设备3a-3c可与主机网络30直接通信,诸如通过经由无线网络协议和基础结构将由相应感测设备记录的参数数据直接传输到主机网络30。在各种实施方案中,每个感测设备3a-3c可处理其自身的生理参数数据并确定其自身的告警条件,或者此类功能可在主机网络30的层级执行。
根据本公开,相关领域的普通技术人员应当理解,所公开的患者监测方法和系统可由结合到集线器15中(即,在床边患者监测系统处)的计算系统执行,或者可由结合到主机网络30中的计算系统执行。在所示的示例中,集线器设备15包括具有处理系统139和存储系统141的计算系统135。集线器设备15可用于控制感测设备3a-3c,并且因此可经由通信链路11a-11c将操作命令传输到相应的感测设备3a-3c以控制它们的监测操作。集线器15可包含监测调节模块23,该监测调节模块为存储在存储系统141的存储器中并且可由处理系统139执行的软件指令集,以评估由感测设备3a-3c收集的生理参数数据,诸如以检测告警事件并且根据监测需要控制相应的感测设备3a-3c。例如,可通过将由一个或多个感测设备3a-3c收集的生理参数数据与相应的告警限值进行比较来确定告警事件,以确定是否应生成告警来向临床医生警示患者的病症。
同样,主机网络30的计算系统235包括可通信地连接到存储系统241以便加载和执行计算机可读指令的处理系统239。虽然本文所提供的描述涉及计算系统135、235和处理系统139、239,但是应当认识到,可使用一个或多个处理器来执行此类系统的具体实施,这些处理器可通信地连接,并且此类具体实施被认为在描述的范围内。每个处理系统139、239可在单个处理设备内实现,但也可分布在多个处理设备或子系统上,这些处理设备或子系统在执行程序指令时协作。每个存储系统141、241可以包括可由处理系统139、239读取并且能够存储软件的任何存储介质或存储介质组,每个存储系统各自存储可包括严重性预测模块24的软件。存储系统141、241可以包括以用于存储信息的任何方法或技术实现的易失性和非易失性、可移除和不可移除介质,所述信息诸如是计算机可读指令、数据结构、程序模块或其它数据。每个存储系统141、241可以实现为单个存储设备,但是也可以在多个存储设备或子系统上实现。同样,存储介质可以与处理系统139、239一起容纳在本地,或者可以分布在一个或多个服务器中,这些服务器可以位于多个位置并联网,诸如在云计算应用和系统中。
系统1包括严重性预测模块24,所述严重性预测模块为计算机可读指令集,所述计算机可读指令存储在一个或多个存储系统141、241上并且可如本文所述执行,以根据两个或更多个生理参数的参数数据的长时间间隔来计算特定医学病症的风险严重性指数。严重性预测模块24可以在患者监测系统1内的任何计算系统上执行,例如在集线器15的计算系统135上或在主机网络30的计算系统235上安装和执行。在其他实施方案中,严重性预测模块24可以安装在移动设备50上并可在其上执行,诸如智能电话或由临床医生操作的其他移动计算设备。在某些实施方案中,严重性预测模块24可以安装在整个患者监测系统1内的多个计算系统上并可由其执行,或者严重性预测模块的各部分可以在整个系统1内的各个计算系统(例如135和235)之间划分。在所示实施方案中,严重性预测模块24设置在主机网络的计算系统235(即,24a)处和集线器15的计算系统135(即,24b)上。每个严重性预测模块24a、24b可以执行本文所述的全部功能,或者每个模块可以执行本文所述的一部分功能。
在各种实施方案中,对患者的特定医学病症进行监测的计算机实现的方法和系统包括接收至少两个生理参数中的每一者的时间同步参数数据的长时间间隔,以及使用训练的机器学习模型处理参数数据的长时间间隔,以识别由模型学习的模式,并且基于在参数数据中识别的一组特征值来计算特定医学病症的风险严重性指数。该组特征基于特定医学病症来定义,如将在下文更详细所述。在一个实施方案中,参数数据的长时间间隔被划分为多个区段,其中每个区段包含参数数据的预定义时间增量。为了提供一个示例,可将两个或更多个生理参数的时间同步参数数据的24小时划分为1小时的时间区段。在另一个示例中,可以将的参数数据的12小时划分为30分钟的区段。在另一个实施方案中,两个或更多个生理参数的时间同步参数数据的五小时可被划分为30分钟的时间区段,这在低血容量性休克是被监测的医学病症的情况下可能特别有用。
图3a至图3c提供了时间同步的参数数据的示例性长时间间隔的可视化描绘,这些长时间间隔被划分为预定义增量的区段并相应地进行分析。图3a和图3b提供了示出spo2和rr的时间同步参数数据的24小时时间间隔的窗口32a、32b,以及指示特定医学病症(在这种情况下为1型ards)的特征值和风险严重性的进展图。窗口32a例示了其中患者未表现出1型ards的任何迹象的24小时时间间隔,并且窗口32b示出了其中表现出1型ards的参数数据的24小时时间间隔。
将时间同步参数数据(此处为spo2和rr数据)的24小时划分为一小时的区段33,并相应地分析该数据。数据的每个区段被单独评估,诸如基于区段中的参数数据是超过告警阈值还是超过较小阈值。此外,可分析每个区段33中的每个参数数据集的斜率。例如,斜率可被分类为图1所例示的ards的上述三个阶段之一—其中spo2正在下降并且rr正在增加的第一阶段,其中spo2相对稳定并且rr正在增加的第二阶段,以及其中spo2和rr两者均显著下降的第三阶段。根据基于参数数据的幅值或斜率的预定义的一组特征来评估每个区段以及作为整体的24小时长的间隔。
然后可基于其中的参数数据,诸如基于数据的幅值或斜率或基于分类器,为每个区段分配可视化代码。在所示的示例中,可视化代码是色码,其中根据特征值中的一者或多者为每个区段33分配色码。更具体地,在所示的示例中,每个参数数据和区段分类由颜色编码的进展图39汇总,包括spo2趋势条34、rr趋势条36和分类器趋势条38。每个趋势条被分成区段33,区段33根据其中的相关值被分配色码。在参数数据稳定的情况下,在窗口32a中例示,为每个区段分配色码(例如,绿色),其表示参数数据是正常的并且不满足任何阈值幅值或斜率或不满足ards阶段分类标准。例如,在spo2和rr数据的斜率满足第一阶段的要求的情况下,分类器趋势条38的相对区段33被分配第一颜色(例如,粉色)。在区段中的参数数据满足ards评估的第二阶段的要求的情况下,趋势条38的相关区段33被着色为第二颜色(例如,橙色)。如果区段中的参数数据满足ards评估的第三阶段的要求,则趋势条的与该区段33对应的相关部分被分配第三颜色(例如,红色或紫色)。类似地,每个参数的趋势条34、36可根据相应生理参数的每个区段中的数据值进行颜色编码。例如,spo2趋势条34可根据其中的值的大小或斜率进行颜色编码,诸如spo2的相对于一个或多个低spo2阈值的大小。同样,rr趋势条36可根据相关区段33中的参数数据的大小或斜率,诸如相对于一个或多个高呼吸阈值的rr数据值进行颜色编码。低spo2阈值和高rr阈值可包括作为极端阈值的告警阈值,并且还可包括另外的中等阈值,其中色码与每个阈值相关联并被相应地分配。
在未检测到或不存在ards的窗口32a中,趋势条34a、36a、38a在整个24小时时间间隔内始终为绿色。相比之下,在ards的风险严重性指数高的窗口32b中,趋势条34b、36b、38b显示出与较高风险相关联的多个着色区段。然而,如从图3c中的示例可以看出,风险严重性指数可检测参数数据中的某些模式,这些模式单独地通过查看参数数据原本不可见。图3c中的进展图39的spo2趋势条34c和rr趋势条36c通常示出单独评估的spo2和rr参数值不越过指示问题的相关阈值。然而,基于spo2斜率与rr斜率的比较的分类器趋势条38基于表征ards的第一阶段、第二阶段和第三阶段的比较斜率值来识别多个有问题的区段33。因此,在长时间间隔内比较这些参数数据的这种长期评估方法可以提供单独检查任何单个参数所无法提供的信息。同样,检查参数数据的任何短时间段也不能提供早期检测某些医学病症诸如ards所需的信息类型。
在每个时间窗口32a-32c的底部是风险严重性指数的示例性视觉指示器40。如本文所述,可基于时间同步参数数据的长时间间隔的一组特征值来计算特定医学病症的风险严重性指数。在一个示例中,风险严重性指数是基于该组特征值计算的特定医学病症的概率。例如,风险严重性值可以是介于0和1之间的指示医学病症的对应概率(0%-100%)的值,其中更靠近1的较高概率值指示特定医学病症的较高风险严重性,并且更靠近0的概率值指示较低严重性风险。
如所示实施方案所示,风险严重性指数基于长时间间隔诸如参数数据的24小时来计算。在图3b中,计算所示的spo2和rr参数数据的24小时间隔内的风险严重性指数,并且由风险严重性视觉指示器40指示该风险严重性指数。风险严重性视觉指示器与24小时长时间间隔的最后一个区段对齐,因为其是基于整个时间间隔数据计算的。
风险严重性指数是预定义的一组特征值的函数,该组特征值是使用机器学习模型进行加权的临床相关特征,这将在下文更详细地描述。图3c处的窗口32c示出了多个风险严重性指数,这些风险严重性指数被计算用于在参数数据的超过100小时内滑动24小时时间间隔。进展图39示出了在参数数据的24小时之后开始并在其后每小时进行更新的风险严重性视觉指示器40。该特定示例示出了发展为严重的1型ards并且其直到生成spo2告警(在第47行处表示)才被检测到的患者的数据集,此时治疗已经太晚并且已无法预防严重医疗事件(在这种情况下对于患者而言已经为晚期)。
然而,使用本文所公开的方法和系统本可以对ards病症进行早期检测。在早期检测时,本可以施加医疗干预并且有可能预防严重ards的发作。即,对风险严重性指数的评估,例如在预定义时间量内的评估,可产生对医学病症(例如ards)的早期指示。例如,如果至少阈值数量的最近风险严重性指数值大于阈值,则可生成告警。例如,如果连续四个小时的风险严重性指数等于或高于80%,则可生成告警,指示对特定医学病症的检测和对医疗干预的需求。在所示的示例中,箭头49指示告警生成,其中风险严重性指数在连续四个小时内大于或等于80%。这仅仅是一个示例,并且其他阈值和时间段可能在临床上更相关。作为另外一种选择或除此之外,如果风险严重性指数超过高阈值以进行甚至一次性间隔计算,例如超过90%的高阈值,则可生成告警。
图4示出了对患者的特定医学病症进行监测的计算机实现的方法100的一个实施方案。例如,流程图表示由严重性预测模块24在一个或多个计算系统(例如,计算系统135和集线器15或者计算系统235和主机网络30)上执行的步骤。在步骤120处接收长时间间隔内的原始参数数据。如上所述,长时间间隔可以是足以检测特定医学病症的任何时间段。例如,1型ards的长时间间隔可为介于30分钟与48小时之间的任何值。对于许多医学病症,长时间间隔将为至少六小时,并且通常为12小时或24小时。
一旦在步骤120处接收到至少两个参数的原始参数数据的第一长时间间隔,就在步骤122处预处理原始参数数据,以便准备用于特征值评估的数据。在步骤124处,识别长时间间隔内的一组特征值。特征值基于特定医学病症的所识别的临床模式来定义,诸如基于参数数据的幅值或斜率评估。下面更详细地描述示例性医学病症的示例性多组特征值。然后在步骤126中,使用训练的机器学习模型来计算风险严重性指数,以将权重分配给特征值。在步骤128处生成可视化,诸如图3a至图3c所示。然后,严重性预测模块24等待在步骤130处接收的原始参数数据的下一个时间增量。预定义时间增量限定参数数据的区段,其必须小于长时间间隔值。一般来讲,预定义时间增量介于一分钟与一小时之间,但可长于1小时。在图3a至图3c处所示的示例中,预定义时间增量为一小时,并且长时间间隔为24小时。然而,可根据检测与所评估的特定医学病症相关的模式所需的时间量来使用其他时间间隔和时间增量。
图5示出了用于训练机器学习模型以接收一组特征值并将权重分配给其中的特征值中的每一者以便计算特定医学病症的风险严重性指数的示例性步骤。如相关领域的普通技术人员将理解的,可利用不同类型的机器学习模型。在一个示例中,机器学习模型是逻辑回归模型,其基于包括参数数据的标记的长时间间隔的数据集来训练。标记的长时间间隔针对特定医学病症被标记为阳性或针对特定医学病症被标记为阴性。逻辑回归模型具有简单且透明的模型的有益效果,从而为进行观察的临床医生提供对所计算的风险严重性指数的逻辑理解,因为可以确定分配给每个特征(临床事件)的权重。然而,可利用其他机器学习模型来计算风险严重性指数,诸如支持向量机(svm)、多层感知器(mlp)、卷积神经网络(cnn)、线性判别分析(lda)、套袋法和随机森林集成算法或朴素贝叶斯分类器。在步骤102处接收标记数据,并且在步骤104处对数据进行排序以识别相关训练数据,诸如选择长度等于针对特定医学病症被标记为阳性或阴性的长时间间隔的参数数据记录。一旦识别出训练数据集,就在步骤106处—即,基于针对特定医学病症的阳性和阴性标记,将其分成阳性和阴性训练集。在步骤108处,在每个患者数据集的每个长时间间隔内识别预定义的一组特征值。然后使用该组特征值和阳性/阴性标记来训练机器学习模型。在步骤110处用阳性数据集训练机器学习模型,并在步骤112用阴性数据集训练机器学习模型,并且所得的训练的机器学习模型能够将权重分配给该组特征值中的每一者,以便计算特定医学病症的风险严重性指数。在步骤114处存储训练的机器学习模型。然后利用所存储的机器学习模型来计算风险严重性指数。例如,使用训练的逻辑回归模型,将严重性指数表示为该组特征值的函数,具体如下:
其中h(x)是严重性指数(特定医学病症的概率),f是预定义的一组特征,并且θt是由最佳训练的逻辑回归模型返回的系数。
在一个实施方案的开发中,发明人利用来自模拟数据集的数据集,该模拟数据集是由mitlab开发的用于计算生理学的多于40,000名重症护理患者的公开可用数据集。这是用于训练逻辑回归模型的标记数据(步骤102)。从标记数据中,利用特定医学病症的相关标记来识别数据集(步骤104),在该实施方案中,该相关标记是用于1型ards的阳性标记和阴性标记。此外,还基于数据的时间间隔来评估数据集,其中训练数据集包含至少数据的长时间间隔,使得可以适当地确定风险严重性指数。在各种实施方案中,也可能需要数据集的其他特征来识别训练数据集。例如,在训练用于ards检测的逻辑回归模型时,可能优选的是将训练数据限制为患者未配戴呼吸机情况下的参数数据集。
图6表示用于预处理原始参数数据的一组方法步骤,既用于训练目的又用于实施所公开的风险严重性计算。在步骤130处接收到由感测设备记录的原始参数数据。可在步骤132处对参数数据进行下采样,或者可应用其他数值来以非常低的采样速率(诸如一次采样/分钟)生成波形数据的表示。考虑到长期趋势的分析,较低的采样速率可能更适合风险严重性指数计算。然而,在其他实施方案中,可使用全波形数据(诸如240次采样/分钟)。
然后在步骤134处使用异常值剔除来过滤下采样的原始参数数据,以减少参数数据中存在的噪声。例如,可利用针对异常值剔除的chauvenet剔除准则,之后是使用回填来重新采样到下采样频率(例如,一次采样/分钟)进行的内插。例如,chauvenet准则的异常值剔除可利用2.5的最大允许偏差。图7a和图7b的比较展示了异常值剔除的有益效果,其中图1a中的原始参数数据是嘈杂的,诸如由于患者移动、光学干涉、传感器放置问题等。图7b示出异常值剔除之后的相同参数数据,这表明大部分伪影被消除。
返回图6,在步骤136处使用平滑算法使参数数据平滑化。例如,可使用局部估计回归散点平滑法(loess)或局部加权回归散点平滑法(lowess)局部多项式回归来使参数数据平滑化。从而,将分段二次多项式拟合到数据值以使数据平滑化。该方法具有优于最小二乘回归的通用框架的明显优点,所述最小二乘回归概括了具有单一函数的整个时间序列的平滑化。与使用24小时时间间隔和以一次采样/分钟的速率进行采样的1小时区段的ards检测实施方案相关,可使用三小时的窗口尺寸进行平滑化。在该示例中,由于采样速率是一次采样/分钟,因此单段二次多项式覆盖180个采样点。图7c示出了使用具有3小时窗口尺寸的loess进行平滑后的参数数据。
重新参考图6,然后用分段线性回归(plr)拟合去噪且平滑的参数数据。plr有助于将时间序列建模成单独的区段,从而为每个区段提供线性近似。在所示的示例中,1小时区段被定义用于线性回归拟合,因为这有助于捕获长时间间隔(例如,24小时)中的长期趋势。plr将一条线拟合到每个1小时区段中的参数数据。假设一次采样/分钟的样本速率,则每个1小时区段将一条线拟合到60个样本点。因此,该区段的斜率可针对陡度进行量化并用于特征值检测,诸如被分类为针对特定医学病症定义的各个阶段。图7d是表示plr之后的示例性参数数据的曲线图。
在参数数据已被预处理之后,可相对于预定义的一组特征对其进行分析,以便生成将由训练的机器学习模型分析的该组特征值。图8表示用于相对于被确定为与检测ards临床相关的预定义的一组特征来分析参数数据的步骤。ards检测的示例性预定义的一组特征包括以下各项:
·rr破坏是否在长时间间隔内发生
·spo2破坏是否在长时间间隔内发生
·rr高于rr阈值的区段的数量
·spo2低于spo2阈值的区段的数量
·第1阶段ards的发生次数
·第2阶段ards的发生次数
·第3阶段ards的发生次数
为了生成上面列出的预定义的一组特征的一组特征值,可以执行图8所示的步骤。在步骤140处确定每个区段中的参数数据的斜率,该步骤140由上述分段线性回归得出。然后在步骤142处根据上述阶段定义对每个区段进行分类。然后可对其中存在ards的第一阶段、第二阶段和第三阶段中的每个阶段的区段的数量进行计数。在步骤144处,评估长时间间隔内的参数数据以识别是否存在告警阈值破坏。例如,在呼吸速率超过25次循环/分钟的情况下可识别rr破坏,并且在spo2参数数据小于90的情况下可识别spo2破坏。还执行步骤以识别参数数据在阈值范围(其包括与告警阈值不同且不太极端的一个或多个阈值)之外的区段的数量。如上文相对于图3a至图3c所述,可设置多个阈值以用于在步骤146处评估参数数据的幅值。在各种实施方案中,可识别除上文列出的那些特征之外的附加特征。在步骤148处表示另外的示例,其中将每个参数数据区段中的斜率的大小与相关生理参数的阈值斜率进行比较。类似于幅值阈值,可提供多个斜率阈值以产生相关生理参数的变化的详细分类和进展跟踪。
在计算风险严重性指数以监测低血容量性休克的示例中,生理参数(包括心率和收缩压)的趋势可随时间推移而被监测并用于量化休克的严重性。另外,高呼吸速率(例如,在成人群体中大于20次呼吸/分钟)、严重低血压(收缩压<90mmhg)和明显心动过速(心率>120bpm)可有助于量化严重性。在该临床场景中,5小时长时间间隔和以一次采样/分钟进行采样的30分钟区段,以及一个半小时(3*30分钟)的窗口尺寸可用于平滑化。在该示例中,由于采样速率是一次采样/分钟,因此单段二次多项式覆盖90个采样点。在参数数据已被预处理之后,可相对于预定义的一组特征对其进行分析,以便生成将由训练的机器学习模型分析的该组特征值。例如,该临床场景中的一组特征可包括:
·rr高于rr阈值的区段的数量
·hr高于hr阈值的区段的数量
·sysbp高于sysbp阈值的区段的数量
·rr破坏是否在长时间间隔内发生
·hr破坏是否在长时间间隔内发生
·sysbp破坏是否在长时间间隔内发生
·低血容量性休克的休克期临床事件的发生次数
该书面描述使用示例来公开本发明,包括最佳模式,并且还使得本领域技术人员能够执行和使用本发明。为了简洁、清楚和易于理解而使用了某些术语。除了现有技术的要求之外,不应从中推断出不必要的限制,因为此类术语仅用于描述目的并且旨在被广义地理解。本发明的专利范围由权利要求书限定,并且可包括本领域的技术人员想到的其他示例。如果这些其他示例具有与权利要求书的字面语言没有不同的特征或结构元件,或者如果它们包括与权利要求书的字面语言无实质差别的等效特征或结构元件,则这些其他示例旨在在权利要求书的范围内。
- 还没有人留言评论。精彩留言会获得点赞!