一种小米复合发酵产品及其制备方法和应用与流程
本公开涉及发酵
技术领域:
,尤其涉及一种小米复合发酵产品及其制备方法和应用。
背景技术:
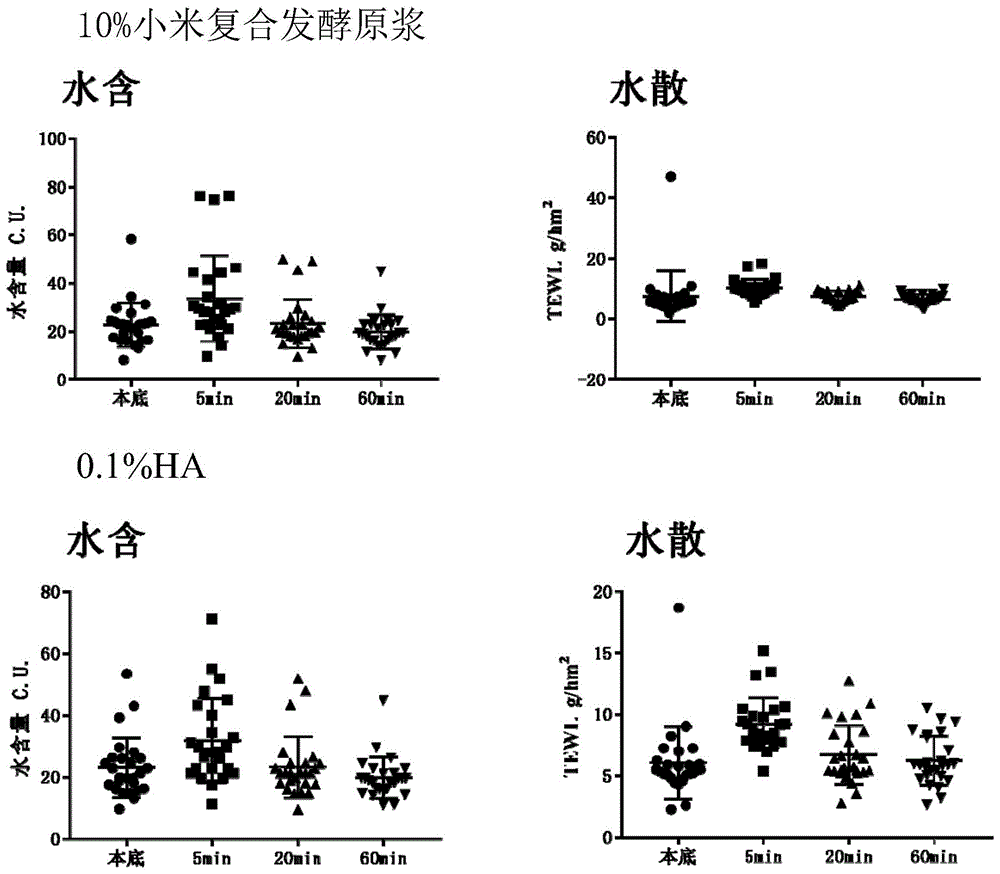
:小米(setariaitalicavar.germanica(mill.)schred.),又称为粟,谷子。小米营养价值高,营养全面均衡,主要含有碳水化合物、蛋白质及氨基酸、脂肪及脂肪酸、维生素、矿物质等;其中,碳水化合物含量为72.0%~79.5%,主要成分是淀粉(约为59.4%~70.2%),其中80%~85%为支链淀粉;蛋白质含量为4.88%~15.58%,小米蛋白是甲硫氨酸、异亮氨酸、亮氨酸、苯丙氨酸和其他必需氨基酸的丰富来源;小米中含有丰富的vb1、vb2和烟酸;矿物质的含量约为2.5%~3.5%,如钠、钙、镁、磷、钾;小米中含有机硒。小米有清热、消渴的功效,可以缓解脾胃气弱、食不消化等症状。小米还可以治疗口臭,一定程度上缓解脚气。另外,小米也具有美容功效。槐角为我国常用中药材,豆科植物槐(sophorajaponical.)的果实,别名:槐实、槐子、槐豆、天豆、槐连豆。主要成分包括黄酮及异黄酮类、生物碱、三萜皂苷类、氨基酸、磷脂类化合物等;其中,黄酮及异黄酮类化合物是槐角中的主要活性成分之一。大豆肽是从大豆中提取的一种多功能肽类物质,它除具有一般的蛋白质营养作用外,还具有良好的营养特征、生理功能和加工特性,是一种非常有前途的功能性食品原料。由于其独特的加工性能,在食品生产等诸多领域有着广泛的应用前景。比如用于医疗食品、蛋白饮料、老年及营养强化食品、运动营养食品和减肥食品,同时还可以作为发酵促进剂,此外,还可以用于营养性化妆品。发酵指人们借助微生物在有氧或无氧条件下的生命活动来制备微生物菌体本身、或者直接代谢产物或次级代谢产物的过程,在食品工业、生物和化学工业中均有广泛应用。对采用发酵技术提取营养物质已多有报道,但是根据发酵底物和发酵工艺条件的不同,提取效果差别很大。有赖于研究人员继续探索更多发酵底物组合及发酵方法制备出更多、更优功效的产品以,满足消费者需求。目前尚未有采用小米、槐角和大豆肽一同进行发酵提取产物应用于化妆品的报道。技术实现要素:在下文中给出了关于本公开的简要概述,以便提供关于本公开的某些方面的基本理解。应当理解,这个概述并不是关于本公开的穷举性概述。它并不意图确定本公开的关键或重要部分,也不意图限定本公开的范围。其目的仅仅是以简化的形式给出某些概念,以此作为稍后论述的更详细描述的前序。鉴于现有技术的上述缺陷,本公开的目的是提供小米复合发酵产品及其制备方法和应用,本公开提供的小米复合发酵产品具有良好的抗敏性能。根据本公开的一个方面,提供了一种小米复合发酵产品的制备方法,包括:将发酵菌接种至由小米提取物、槐角和大豆肽组成的发酵底物中进行发酵培养,然后进行灭菌处理,得到所述小米复合发酵产品。本公开中采用的发酵菌为益生菌,可以维持新的皮肤环境,有益于改善皮肤的生态平衡和舒适度,强化微生物保护膜,促进皮肤微循环。优选地,所述益生菌为乳酸菌;具体选自如下一种或以上:布氏乳杆菌(lactobacillusbuchneri,cgmcc1.15607)、德氏乳杆菌保加利亚亚种(lactobacillusdelbruechiisubsp.bulgaricus,cgmcc1.16075)和两歧双歧杆菌(bifidobacteriumbifidum,cgmcc1.5029);优选用于接种至发酵底物的乳酸菌种子液的浓度为107-1010cfu/ml(比如108cfu/ml、109cfu/ml)。本公开中发酵底物由槐角、大豆肽和小米提取物混合后灭菌制成。即用该小米提取物替代常规发酵底物所采用的水。本公开中采用的小米提取物,为采用热水浸提法对小米进行处理得到的清液或其干粉;优选地,本公开中采用的小米提取物的制备方法如下:将适量小米加入水中,小米与水的质量比为1:25~1:100(比如1:25、1:30、1:40、1:50、1:60、1:70、1:80、1:90等),加热至90-100℃(比如92℃、94℃、96℃、98℃等)提取1.5-2.5h(比如1.8h、2h、2.2h等),然后分离取上清液,即为本公开所用小米提取物,小米提取物富含从小米中提取的活性成分低聚肽,可以提升肌肤健康,优选用量为99.2~99.89wt.%,即小米提取物用量占发酵底物总重量的99.2%~99.89%。上述小米提取物制备方法中,优选小米与水的质量比为1:25~1:50(比如1:30、1:35、1:40、1:45等)。上述小米提取物制备方法中,优选采用离心分离,离心速度为4000-6000r/min(比如4200r/min、4500r/min、5000r/min、5500r/min、5800r/min等)、离心20-40min(比如22min、25min、30min、35min、38min等)。本公开中采用的槐角为豆科植物槐的干燥成熟果实。槐果含有芸香甙、槐花二醇、葡萄糖与葡萄糖醛酸和鞣质等许多微量元素,可以提高皮肤对过敏和刺激的免疫力;优选用量为0.1-0.3%,即槐角占发酵底物总重量的0.1-0.3%(比如0.15%、0.2%、0.25%等)。实验证明,槐角用量比过低不能体现应有的功效,槐角用量比过高得到的发酵液整体颜色较深,色素沉着于皮肤且容易造成皮肤过敏反应。本公开中采用的大豆肽是利用生物技术酶将大分子的大豆蛋白质分解成由2到10个氨基酸组成的小分子片段,具有抗氧化、促进细胞增殖、美容养颜的作用。优选用量为0.01~0.5%,即大豆肽占发酵底物总重量的0.01~0.5%(比如0.05%、0.1%、0.2%、0.3%、0.4%、0.45%等)。实验证明,大豆肽用量比过低不能体现应有的功效,用量比过高效果提升有限,且成本提高。上述小米复合发酵产品的制备方法中,作为一种优选实施方式,所述发酵菌为德氏乳杆菌保加利亚亚种(lactobacillusdelbruechiisubsp.bulgaricus)。进一步地,所述种子液的制备方法包括如下步骤:活化:将菌种接种至mrs液体培养基的试管中,35~37℃活化20~48h;纯化:取活化后的液体菌种梯度稀释后,接种于mrs固体培养基平板中,35~37℃静置培养40~48h;液体培养:取所述平板中的单菌落2~3环,接种于100mlmrs液体培养基中,35~37℃活化20~48h;扩大培养:以10%接种量取上述液体培养步骤得到的菌液,接入到mrs液体培养基中(菌液和培养基的体积比10:100),35~37℃培养10~14h左右,当菌体量达到107-1010cfu/ml时,得到种子液。其中,上述mrs液体培养基配方为:蛋白胨10.0g,牛肉膏10.0g,酵母粉5.0g,葡萄糖20.0g,k2hpo4·7h2o2.0g,醋酸钠·3h2o5.0g,柠檬酸三铵2.0g,mgso4·7h2o0.05g,吐温801.0ml,ph6.2,补足水分至1000ml;上述mrs固体培养基为往上述mrs液体培养基中添加1.5%琼脂粉;培养基灭菌条件为:115~121℃灭菌15~20min。上述小米复合发酵产品的制备方法中,作为一种优选实施方式,所述发酵菌的接种比例,即所述种子液与所述发酵底物的体积比为1%~3%(比如1.2%、1.5%、2%、2.5%、2.8%等)。上述小米复合发酵产品的制备方法中,作为一种优选实施方式,所述发酵培养的温度为30-50℃(比如31℃、32℃、33℃、34℃、35℃、36℃、37℃、38℃、39℃、40℃、41℃、42℃、43℃、44℃、45℃、46℃、47℃、48℃、49℃等),时间为6-10h(比如6.5h、7h、8h、9h、9.5h等)。上述小米复合发酵产品的制备方法中,作为一种优选实施方式,所述灭菌处理的温度是115~121℃(比如116℃、117℃、118℃、119℃、120℃),时间是15-20min(比如16min、17min、18min、19min等)。上述小米复合发酵产品的制备方法中,作为一种优选实施方式,所述灭菌处理前,还包括分离处理,最终得到所述小米复合发酵产品,即小米复合发酵原浆。更优选地,所述离心处理的速度是3500-8000r/min(比如4000r/min、4500r/min、5000r/min、5500r/min、6500r/min、7000r/min、7500r/min等),时间是20-60min(比如25min、30min、40min、50min、55min等)。上述小米复合发酵产品的制备方法中,作为一种优选实施方式,所述灭菌处理后,还包括干燥处理,最终得到所述小米复合发酵产品,即小米复合发酵干粉。上述小米复合发酵产品的制备方法中,作为一种优选实施方式,所述干燥处理可以是喷雾干燥、真空冷冻干燥等。根据本公开的又一个方面,还提供了一种采用上述制备方法制备的小米复合发酵干粉。根据本公开的又一个方面,还提供了一种采用上述制备方法制备的小米复合发酵原浆。根据本公开的又一个方面,还提供了一种上述小米复合发酵干粉在制备化妆品的应用。根据本公开的又一个方面,还提供了一种上述小米复合发酵原浆在制备化妆品的应用。上述化妆品可以是面膜、精华液或爽肤水等。上述根据本公开实施例的技术方案,通过对小米提取物、槐角、大豆肽组成的发酵底物中进行复合发酵,制得了一种新型小米复合发酵原浆,具有良好的抗过敏效果,hacat角质形成细胞抗炎舒缓效果。通过以下结合附图对本公开的最佳实施例的详细说明,本公开的这些以及其他优点将更加明显。附图说明本公开可以通过参考下文中结合附图所给出的描述而得到更好的理解。所述附图连同下面的详细说明一起包含在本说明书中并且形成本说明书的一部分,而且用来进一步举例说明本公开的优选实施例和解释本公开的原理和优点。其中:图1示出了使用实施例1制备的小米复合发酵原浆和0.1%透明质酸(0.1%ha)进行皮肤水分含量(简称“水含”)和皮肤水分流失量(即经皮水分散失,简称“水散”)测试所得结果;图2示出了使用实施例1制备的小米复合发酵原浆和0.1%透明质酸(0.1%ha)进行皮肤水分含量(简称“水含”)测试所得结果,其中,a表示使用后不同时间点与各区域使用前水分含量的变化百分比变化趋势,b表示不同时间点不同区域的水分含量中位数变化趋势;图3示出了使用实施例1制备的小米复合发酵原浆和0.1%透明质酸(0.1%ha)进行皮肤水分流失量(即经皮水分散失,简称“水散”)测试所得结果,其中,a表示使用后不同时间点与各区域使用前tewl值的变化百分比变化趋势,b表示不同时间点不同区域的tewl值中位数变化趋势;图4示出了使用实施例1制备的小米复合发酵原浆进行透皮吸收性实验所得结果;图5示出了使用实施例1制备的小米复合发酵原浆进行抗氧化清除abts自由基测试所得结果;图6示出了一个志愿者使用实施例1制备的小米复合发酵原浆后进行皮肤皱纹及粗糙度测试所拍摄的照片,其中,从上至下依次为分析细纹、皱纹的照片,从左至右依次为使用样品前、使用样品后5min、20min、60min拍摄的照片;图7示出了图6所示志愿者使用实施例1制备的小米复合发酵原浆前后测试部位的皮肤细纹平均深度;图8示出了图6所示志愿者使用实施例1制备的小米复合发酵原浆前后测试部位的皮肤皱纹平均深度。具体实施方式在下文中将结合附图对本公开的示范性实施例进行描述。下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。下述实施例中的小米来自市面销售。下述实施例中的槐角购于安徽省亳州市何欢堂农副产品购销有限公司。下述实施例中的大豆肽来自乳山市华隆生物科技股份有限公司。下述实施例中的发酵菌为乳酸菌,具体为:德氏乳杆菌保加利亚亚种(lactobacillusdelbruechiisubsp.bulgaricus),保藏编号为cgmcc1.16075,可从cgmcc购买。还可以根据本申请实施例的内容替换采用布氏乳杆菌(lactobacillusbuchneri,保藏编号为cgmcc1.15607)或两歧双歧杆菌(bifidobacteriumbifidum,保藏编号为cgmcc1.5029)或任意两者或三者的组合实施本公开的方案。实施例1小米复合发酵原浆的制备1、菌种的活化:挑取德氏乳杆菌保加利亚亚种(lactobacillusdelbruechiisubsp.bulgaricus)菌落2环接种至100mlmrs液体培养基的试管中,35℃活化24h。2、菌种纯化:取上述液体菌种梯度稀释后,接种200μl涂布于mrs固体培养基平板中,35℃静置培养48h。3、液体培养:取上述平板中的单菌落3环,接种于100mlmrs液体培养基中,35℃活化48h。4、扩大培养:以10%接种量取上述液体培养所得菌液,接入到100mlmrs液体培养基中,37℃培养12h,当菌体量达到108cfu/ml时,得到种子液。5、发酵底物配制1)小米上清液制备:取小米10g加入500g水中(小米与水质量比为1:50),于95℃搅拌提取2h,期间注意水分保持,提取结束后5000r/min、离心30min,所得上清液即为本公开所用小米上清液;2)取槐角0.6g,大豆肽0.6g,步骤1)制备的小米上清液300g,并将槐角、大豆肽加入至小米上清液,混合均匀,灭菌,得到发酵底物;其中,槐角约占0.2%;大豆肽约占0.2%;小米上清液约占99.6%。6、小米复合发酵原浆的获得将9ml步骤4得到的发酵菌种子液接种到300g发酵底物中,得到发酵体系;将发酵体系在45℃摇床中发酵8小时,得到发酵产物;将发酵产物在5000r/min、离心30min,弃沉淀,收集上清液,于115℃灭菌20min,使菌失活,得到灭菌后的发酵产物,即为小米复合发酵原浆。实施例1所制得的小米复合发酵原浆的外观为微黄色半透明粘稠液体,ph值5.5-6.5,粘度150-300cp,可溶性固含物含量1.5-5.0%,菌落总数小于50cfu/ml,无致病菌检出。根据化妆品卫生标准gb7916-87,化妆品细菌总数不高于1000cfu/ml,所以此发酵提取物符合化妆品质量要求。对该小米复合发酵原浆进行成分分析,其中,蛋白质检测方法参照gb5009.5-2010,粗多糖检测方法参照gb/t5009.8-2008,黄酮检测方法参照gb/t5009.124-2003,总酚检测方法参照gb/t8313-2008;所得结果如下:实施例1制得的小米复合发酵原浆含蛋白质3.193g/kg、粗多糖7.567g/kg、总黄酮0.036g/kg(以芦丁计)、总酚0.021g/kg。实施例2小米复合发酵原浆在作为化妆品的应用一、小米复合发酵原浆的安全性检测人体斑贴试验主要是用于检测化妆品终产品或原料的刺激性。本公开根据《化妆品卫生规范》(2015)对实施例1获得的发酵原浆进行人体封闭式斑贴试验,旨在对其潜在皮肤刺激性进行评估。1、试验对象:本试验选择选择合适的志愿者30人,年龄范围在18-60岁随机选择。2、试验方法:将液体样品(100%小米复合发酵原浆)0.02ml到0.025ml滴加在滤纸片上,再将滤纸片置于斑试器内。每个样品均设置空白对照,在对照斑试器孔内加入与样品等量的样品溶剂(蒸馏水)。测试周期持续24h。为了试验结果的准确、可信和科学,在测试期间志愿者按照要求,不能摘掉斑试器,亦不可使受试部位接触水。24h后去除斑试器,静置30min后,等待压痕消失,观察皮肤的反应。如果试验为阴性,则需要在斑贴试验后24h和48h分别再观察一次。人体斑贴试验皮肤不良反应分级标准参见表1。表1皮肤不良反应分级标准3、试验结果:参见表2。从表中可以看出:志愿者使用实施例1得到的小米复合发酵原浆后都是阴性反应,说明本发明提供的小米复合发酵原浆具有安全性,不会给人体带来不良反应。表2、实施例1获得的小米复合发酵原浆的斑贴试验结果二、小米复合发酵原浆的水含、水散测试对实施例1获得的小米复合发酵原浆的保湿效果进行测试,具体为皮肤水分含量测试、皮肤水分流失量测试,透明质酸(ha)普遍认为是具有较好保湿效果的阳性对照样品,本测试采用10%小米复合发酵原浆(记为10%样品,即用实施例1制备的小米复合发酵原浆配制的体积浓度为10%的水溶液)和0.1%透明质酸(记为0.1%ha,即用透明质酸配制的体积浓度为0.1%的水溶液)进行对比实验。具体如下:1、测试环境:温度:22±1℃;湿度:50%-60%。2、测试区域:皮肤水分含量测试、皮肤水分流失量测试:左右前臂。3、测试时间点:皮肤水分含量测试、皮肤水分流失量测试:使用前、使用后5min、20min、60min。4、实验仪器:cornemeter,cm825、tewameter,tm300。5、测试方法:1)30名符合条件的志愿者参加测试。测试场所无光线直射、无风,室温22~24℃,湿度40%~60%。检测前用洗面奶清洗双侧前臂,静息30min,取受试者双侧前臂内侧用记号笔画出面积为3.5×3.5cm正常皮肤。依次测量在使用前的皮肤水分含量及皮肤水分流失量。2)将浸有样品的面膜分别剪成3×3cm大小,分别贴在前臂相应标记处,15min后取下,轻轻用化妆棉沾干测试部位未干的精华液,并开始计时。3)分别在5min、20min、60min时测试3个部位角质层含水量及tewl值。每个部位测量3次取平均值。6、测试结果:图1是30名志愿者手臂测试皮肤水含和水散的离散图,从图1可以看出10%样品(即10%小米复合发酵原浆)和0.1%ha的水含水散变化趋势较相似,利用t-test分析其显著性发现,使用后5min的水含量显著高于本底(样品p=0.017,vs本底;hap=0.01,vs本底),其他时间点水含量与本底均无显著性差异。进一步对数据进行分析,图2中的a为10%样品和0.1%ha的水含量变化百分比趋势图,b为10%样品和0.1%ha水含量中位数的变化趋势图。从图2中可以看出样品和ha在使用后5min的水含量中位数均达到最大,随着使用后时间的延长,样品和ha的水含量中位数均呈现降低趋势,水含量变化百分比均低于0,表示使用后该时间点的水含量低于本底数据,但是样品和ha数据趋势相似。图3中的a为10%样品和0.1%ha的经皮水分散失变化百分比趋势图,b为10%样品和0.1%ha经皮水分散失量中位数的变化趋势图。由图3可知,样品和ha的经皮水分散失变化规律较为相似,两者均在使用后5min达到最大,是因为此时水含量较大造成经皮水分散失也较大;随着使用后时间的延长,经皮水分散失量逐渐下降,并在使用后60min有所回弹,该时间点下的twel变化百分比均大于0,表示该时间点下的twel高于皮肤本底,这是由于未进一步进行锁水成分(如油脂)的涂抹的原因。可见实施例1制备的小米复合发酵原浆具有良好的补水性能,其10%样品与0.1%ha补水性能相当。三、透皮吸收性实验1、鼠皮的制备将裸鼠脱颈椎处死,迅速将其背部毛用剃须刀剃净,剥离背部皮肤并除去皮下脂肪,血管,用蒸馏水反复冲洗至净,再用生理盐水冲洗数遍,置-80℃冰箱中冷藏备用(在5天内用完)。2、franz扩散池进行体外透皮吸收实验实验过程:向体外渗透扩散装置恒温槽中加入适量水。开启电源和恒温槽磁力搅拌,设定恒温槽中水温为37±0.1℃。将制备好的鼠皮用铁夹子固定在两室扩散池之间,向垂直扩散池的接受池内加入5ml接受液,放入体外渗透扩散装置恒温槽中预热,设定接受池搅拌速度为400r/min。向供给池内分别加入供给液(10%样品,即实施例1制备的小米复合发酵原浆制备成体积百分比为10%的水溶液),以保鲜膜封住上口。开始记时,当样品(即供给液)渗透0、2、4、6、8、12、24小时时(根据实际样品确定具体时间间隔),分别取样500μl置具塞离心管中,每次取样的同时向接受池中补充等量的接受液并排除池中的气泡。将测定样品含量。再根据以下公式计算出累积透过量q(mg/cm2)。其中,扩散池底部直径为1.50cm,样品接触面积为1.77cm2。式中,q为累积透过量,s为透皮扩散面积,v为改进franz扩散池接受室的体积,cn为第n次取样时接受液的浓度,ci为第i次取样时接受液的浓度,0.5为取样量。通过以上公式计算后,做出累积量与时间的曲线图。接受液浓度为0.9%的nacl溶液(生理盐水);供给液为10%样品,即将实施例1制备的小米复合发酵原浆制备成体积百分比为10%的水溶液。3、实验结果实验结果参见图4。从图中可以看出样品0到2h时透过率急速增到0.65mg/cm3,随着时间的延长透过率趋于稳定,表示样品可以顺利透过皮肤。四、hacat炎症细胞模型的修复性能测试建立以lps为诱导剂的hacat炎症模型,具体方法如下:选择生长良好的hacat细胞,控制细胞数为5×105个/ml,铺设于6孔板中,每孔2ml,然后在37℃,5%co2培养箱过夜,选择100mg/l的lps刺激hacat细胞24h。样品分组:细胞建模后,以0.05%样品(即体积浓度为0.05%的小米复合发酵原浆水溶液)进一步作用hacat炎症细胞模型24h,作为样品组;细胞建模后,以无血清细胞培养液dmem进一步作用hacat炎症细胞模型24h,作为模型组;以无血清细胞培养液dmem替代建模过程中的100mg/llps,以新鲜无血清细胞培养液dmem进一步作用细胞24h,作为空白组。检测指标:qrt-pcr检测炎症因子白细胞介素-1α(interleukin-1α,il-1α)表达量。具体方法如下:取经过上述不同处理的细胞,根据trizol总rna抽提试剂说明书进行操作,所提总rna放于-80℃冰箱备用。使用one-stepgdnaremovalandcdnasynthesissupermix反转录试剂盒进行cdna第一条链合成反应。根据ncbi中发布的基因序列,通过primerexpress软件设计引物,以erk1作为内参基因,qrt-pcr检测il-1α相对表达量。根据topgreenqpcrsupermix试剂盒进行操作,总反应体系为20μl,具体试剂与用量参考试剂盒说明书。具体结果见表3。模型组il-1α相对表达量显著高于空白组,表示建模成功;当0.05%样品作用于炎症细胞24h后,il-1α相对表达量显著降低(p<0.05),表示样品具有显著的抗炎效果。表3细胞分组il-1α相对表达量显著性分析空白组1±0.04——模型组6.43±1.04与空白组相比,p<0.01样品组3.23±0.87与模型组相比,p<0.05五、抗氧化清除自由基性能测试1、实验方法配制abts+·储备液:配制2.45mmol/l过硫酸钾,用过硫酸钾溶解abts,配成7mmol/labts储备液,在室温、避光条件下静置12~16h,这种储备液可稳定3~4d。配制abts工作液:将5ml7mmol/labts和88μl140mmol/l过硫酸钾溶液混合,在室温、避光条件下静置过夜,形成abts工作液。使用前用无水乙醇稀释成工作液,使其在734nm下的吸光度在0.70±0.02。实验操作:取4mlabts工作液,加入40μl样品待测液(即事先配置的体积浓度分别为5%、10%、20%、50%、100%的小米复合发酵原浆水溶液),准确震荡30s,测定反应6min后734nm波长下的吸光度a样品。按照下式计算:abts·+清除率/%=(1-a样品/0.700)×1002、实验结果实验结果参见图5。从图中可以看出不同浓度的样品具有不同的abts自由基清除能力,且呈现剂量依赖性,50%的样品清除abts自由基的能力在25%以上。说明实施例1制备的小米复合发酵原浆具有一定的抗氧化性能。六、透明质酸酶抑制实验测试产品的抗过敏性能透明质酸酶i型过敏反应的参与者,透明质酸酶与炎症、过敏有强相关性,研究报道各种肥大细胞释放组胺的药物能调节透明质酸酶活性,一些抗过敏药物有强抑制透明质酸酶活性,因此抑制透明质酸酶活性作为研究抗过敏作用的指标。透明质酸酶抑制实验的实验方法及结果参见下表4和表5。样品待测液(即事先配置的体积浓度分别为5%、10%、20%、50%、100%的小米复合发酵原浆水溶液)。表4透明质酸酶抑制实验的实验方法根据下式计算透明质酸酶抑制率,结果参见表5。透明质酸酶抑制率(%)=(c-d)-(a-b)/(c-d)×100%式中:a—(透明质酸酶+样品+透明质酸钠)试样溶液的od值;b—(醋酸缓冲液+样品+醋酸缓冲液)试样空白的od值;c—(透明质酸酶+去离子水+透明质酸钠)对照溶液的od值;d—(醋酸缓冲液+去离子水+醋酸缓冲液)对照空白的od值。从表5中可以看出,不同浓度的样品具有不同的透明质酸酶抑制能力,且呈现剂量依赖性,50%及以上的样品抑制透明质酸酶的能力在50%以上,说明实施例1制备的小米复合发酵原浆具有良好的透明质酸酶抑制能力。表5五种样品对透明质酸酶抑制能力的结果六、人体皮肤皱纹及粗糙度测试1、测试方法antera3d相机可发射多种波长的平行光,并通过收集所测区域内皮肤表面的反射光波长构建出皮肤图像,根据其内置复杂算法,可以准确测量皮肤皱纹、纹理、色素化程度等参数。选10名符合条件的志愿者参加测试。测试场所无光线直射、无风,室温22~24℃,湿度40%~60%。检测前用洗面奶清洗面部,静息30min,取受试者眼角位置作为测试部位,将浸有样品(实施例1制得的100%小米复合发酵原浆)的面膜分别剪成3×3cm大小,贴在眼角处,15min后取下,轻轻用化妆棉沾干测试部位未干的精华液,并开始计时,在使用前(本底)、5min、20min、60min时通过antera3d面部成像分析。测量在使用前后眼角皮肤细纹、皱纹的变化。2、测试结果测试结果参见图6-图8。图6为其中一位志愿者在使用样品过程中眼角皮肤的变化分析图片,其中,从左至右依次为使用前(本底)、使用样品后5min、20min、60min时的图片;从图中可以看出该志愿者在使用前的细纹、皱纹均较为明显,使用实施例1制得的小米复合发酵原浆后有较为明显的改善。进一步用软件捕捉数据进行变化趋势分析,得到图7~图8。图7为志愿者所分析眼角区域中细纹平均深度的变化趋势,从图中可以看出相同区域本底皮肤细纹平均深度为0.05mm,使用后5min、20min和60min的皮肤细纹平均深度均低于本底,表示该样品具有抗细纹能力。图8为志愿者所分析眼角区域中皱纹平均深度的变化趋势,从图中可以看出相同区域本底皮肤细纹平均深度为0.07~0.08mm,使用后20min和60min的皮肤皱纹平均深度均显著低于本底,表示该样品具有抗皱纹能力。综上,在根据本公开的实施例中,本公开提供了如下技术方案,但不限于此:方案1、一种小米复合发酵产品的制备方法,其特征在于,包括:将发酵菌接种至由小米提取物、槐角和大豆肽组成的发酵底物中进行发酵培养,然后进行灭菌处理,得到所述小米复合发酵产品。方案2、如方案1所述的制备方法,其特征在于,所述发酵菌为乳酸菌。方案3、如方案2所述的制备方法,其特征在于,所述发酵菌选自如下一种或以上:布氏乳杆菌(lactobacillusbuchneri,cgmcc1.15607)、德氏乳杆菌保加利亚亚种(lactobacillusdelbruechiisubsp.bulgaricus,cgmcc1.16075)和两歧双歧杆菌(bifidobacteriumbifidum,cgmcc1.5029)。方案4、如方案1-3中任一项所述的制备方法,其特征在于,所述发酵底物通过将适量槐角、大豆肽加入小米提取物,混合后灭菌制成。方案5、如方案1-4中任一项所述的制备方法,其特征在于,所述小米提取物为采用热水浸提法对小米进行处理得到的清液。方案6、如方案5所述的制备方法,其特征在于,所述小米提取物的制备方法如下:将适量小米加入水中,小米与水的质量比为1:25~1:100,加热至90-100℃提取1.5-2.5h,然后分离取上清液。方案7、如方案6所述的制备方法,其特征在于,所述小米提取物的制备方法中,所述小米与水的质量比为1:25~1:50。方案8、如方案6或7所述的制备方法,其特征在于,所述小米提取物的制备方法中,采用离心分离,离心速度为4000-6000r/min、离心时间为20-40min。方案9、如方案6-8中任一项所述的制备方法,其特征在于,所述小米提取物用量占发酵底物总重量的99.2%~99.89%。方案10、如方案1-9中任一项所述的制备方法,其特征在于,所述槐角占发酵底物总重量的0.1-0.3%。方案11、如方案1-10中任一项所述的制备方法,其特征在于,所述大豆肽占发酵底物总重量的0.01~0.5%。方案12、如方案2-11中任一项所述的制备方法,其特征在于,用于接种至所述发酵底物的乳酸菌种子液的浓度为107-1010cfu/ml,所述种子液与所述发酵底物的体积比为1%~3%。方案13、如方案1-12中任一项所述的制备方法,其特征在于,所述发酵菌为德氏乳杆菌保加利亚亚种(lactobacillusdelbruechiisubsp.bulgaricus)。方案14、如方案13所述的制备方法,其特征在于,所述德氏乳杆菌保加利亚亚种(lactobacillusdelbruechiisubsp.bulgaricus)种子液的制备流程如下:活化:将菌种接种至mrs液体培养基的试管中,35~37℃活化20~48h;纯化:取活化后的液体菌种梯度稀释后,接种于mrs固体培养基平板中,35~37℃静置培养40~48h;液体培养:取所述平板中的单菌落2~3环,接种于100mlmrs液体培养基中,35~37℃活化20~48h;扩大培养:以10%接种量取所述液体培养步骤得到的菌液,接入到mrs液体培养基中,35~37℃培养10~14h,得到种子液。方案15、如方案14所述的制备方法,其特征在于,所述mrs液体培养基配方为:蛋白胨10.0g,牛肉膏10.0g,酵母粉5.0g,葡萄糖20.0g,k2hpo4·7h2o2.0g,醋酸钠·3h2o5.0g,柠檬酸三铵2.0g,mgso4·7h2o0.05g,吐温801.0ml,ph6.2,补足水分至1000ml;所述mrs固体培养基为往上述mrs液体培养基中添加1.5%琼脂粉;所述培养基灭菌条件为:115~121℃灭菌15~20min。方案16、如方案1-15中任一项所述的制备方法,其特征在于,所述发酵培养的温度为30-50℃,时间为6-10h。方案17、如方案1-15中任一项所述的制备方法,其特征在于,所述灭菌处理的温度是115~121℃,时间是15-20min。方案18、如方案1-17中任一项所述的制备方法,其特征在于,所述灭菌处理前,还包括分离处理。方案19、如方案18所述的制备方法,其特征在于,所述离心处理的速度是3500-8000r/min,时间是20-60min。方案20、如方案1-19中任一项所述的制备方法,其特征在于,所述灭菌处理后,还包括干燥处理,最终得到小米复合发酵干粉。方案21、如方案20所述的制备方法,其特征在于,所述干燥处理采用方法至少包括如下一种:喷雾干燥和真空冷冻干燥。方案22、一种小米复合发酵干粉,其特征在于,采用如方案20或21所述的制备方法制备而成。方案23、一种小米复合发酵原浆,其特征在于,采用如方案1-19中任一项所述的制备方法制备而成。方案24、如方案22所述的小米复合发酵干粉在制备化妆品中的应用。方案25、如方案23所述的小米复合发酵原浆在制备化妆品的应用。方案26、如方案24或24所述应用,其特征在于,所述化妆品是面膜、精华液或爽肤水。最后,还需要说明的是,在本公开中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个……”限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。尽管上面已经通过本公开的具体实施例的描述对本公开进行了披露,但是,应该理解,本领域技术人员可在所附方案的精神和范围内设计对本公开的各种修改、改进或者等同物。这些修改、改进或者等同物也应当被认为包括在本公开所要求保护的范围内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1