一种用于膀胱癌诊断与治疗的双靶向纳米团簇、制备方法及应用与流程
[0001]
本发明涉及生物医药领域,特别涉及一种用于膀胱癌诊断与治疗的双靶向纳米团簇、制备方法及应用。
背景技术:
[0002]
膀胱癌是全球第十大最常见的癌症和我国发病率最高的泌尿系统恶性肿瘤。膀胱癌具有复发、进展率高,临床预后差的显著特点。pd-l1是肿瘤细胞表面“找不到我”的信号,是一种适应性免疫检查点,而cd47则是肿瘤细胞表面“不要吃我”的信号,是一种先天性免疫检查点,pd-l1和cd47在膀胱癌细胞表面均高表达。其中,cd47在超过80%的膀胱癌细胞上表达,而其表达水平在膀胱肿瘤干细胞中更高。在蓝光膀胱镜检查中使用荧光标记的cd47抗体诊断膀胱癌的敏感性和特异性分别为82.9%和90.5%,抗cd47单克隆抗体可通过阻断cd47抑制信号使巨噬细胞体外吞噬膀胱癌细胞。因此,将荧光标记的抗cd47单抗与抗pd-l1单抗联用,可用于膀胱癌的诊断,提高诊断效能,而且有希望能有效增强抗pd-l1单抗的疗效,减少膀胱癌的复发和进展,改善膀胱癌患者预后。
[0003]
既往实验研究表明,通过联合使用分别抗pd-l1和cd47的单克隆抗体或者应用抗pd-l1和cd47的融合蛋白,相较于单种抗体,均可显著增强对乳腺癌和结肠癌小鼠模型的抗肿瘤作用。但是,不管是抗体联用还是双特异性融合蛋白,均是单个抗体,瘤内富集程度较低,副作用相对较大,限制了抗体联合治疗的效果。
[0004]
纳米药物可通过增强渗透和滞留效应增加其在肿瘤内的富集,而加载其上的不同抗体则可实现主动靶向和协同抗肿瘤作用。因此,可以通过纳米技术将多个不同的单克隆抗体连接成一个整体,充分发挥不同抗体的抗原靶向诊断和治疗作用。
[0005]
前期,我们团队“新一代多功能抗体纳米团簇的制备及其协同治疗应用”专利中采用pei连接i型和ⅱ型cd20抗体构建了一种纳米团簇用于淋巴瘤的治疗,其效果良好,但是依旧存在着一些弊端,如:其靶向抗原单一,应用病种单一,且无法充分发挥不同抗体抗原结合的联合作用,而且普适性较差。
技术实现要素:
[0006]
本发明的目的在于提供一种用于膀胱癌诊断与治疗的双靶向纳米团簇、制备方法及应用,以解决上述背景技术中提出的问题。
[0007]
为实现上述目的,本发明提供如下技术方案:
[0008]
一种用于膀胱癌诊断与治疗的双靶向纳米团簇,由多个巯基化的抗cd47和pd-l1抗体通过mal-peg-scm偶联到支化型聚乙烯亚胺上。
[0009]
优选的,所述双靶向纳米免疫团簇中的骨架为聚乙烯亚胺pei,铰链为马来酰亚胺-聚乙二醇-琥珀酰亚胺mal-peg-scm。
[0010]
优选的,所述双靶向纳米免疫团簇中所含的抗体为抗cd47抗体和抗pd-l1抗体。
[0011]
优选的,所述双靶向纳米免疫团簇为树枝状,尺寸为100-200nm。
[0012]
本发明还提供了一种用于膀胱癌诊断与治疗的双靶向纳米团簇的制备方法,具体包括以下步骤:
[0013]
s1、通过traut's试剂分别将抗cd47抗体和抗pd-l1抗体实现巯基化;
[0014]
s2、用异官能团修饰剂mal-peg-scm修饰分子量为750kda的支化型pei,获得pei-mal-peg-scm溶液;
[0015]
s3、用巯基化的抗cd47和pd-l1抗体与pei-mal-peg-scm溶液混合反应,制备得到双靶向纳米免疫团簇。
[0016]
优选的,所述s1中将抗cd47抗体、抗pd-l1抗体溶液与traut
’
s试剂分别按照摩尔比(1-2):(18-22)的比例在氮气环境下室温避光反应1h,并在mwco3.5kda透析袋室温透析30min,获得巯基化抗体acd47-sh和apd-l1-sh。
[0017]
优选的,所述s2中将pei溶液与mal-peg-scm溶液按照质量比1:27室温避光反应48h,并在mwco3.5kda透析袋室温透析12h,得到pei-mal-peg-scm溶液。
[0018]
优选的,将pei-mal-peg-scm、acd47-sh、apd-l1-sh按照摩尔比1:3000:3000的比例在氮气条件下4℃避光反应12h,用mwco300kda透析袋室温透析12h,获得的保留液即为双靶向纳米免疫团簇。
[0019]
本发明还提供了一种用于膀胱癌诊断与治疗的双靶向纳米团簇的应用,应用于膀胱癌的诊断和治疗。
[0020]
与现有技术相比,本发明的有益效果是:
[0021]
(1)、本发明所采用的是抗cd47和pd-l1抗体,既能充分发挥不同抗体抗原结合的联合作用,而且具有更好的普适性;
[0022]
(2)、抗cd47和pd-l1双靶向纳米免疫团簇中的抗cd47和pd-l1抗体可靶向结合膀胱癌细胞表面高表达的cd47和pd-l1抗原,其抗原结合能力良好,荧光标记后可用于膀胱癌的诊断;
[0023]
(3)、双靶向纳米免疫团簇与抗原结合后的解离速率慢,可持续作用于膀胱癌细胞发挥协同抗膀胱癌作用;
[0024]
(4)双靶向纳米免疫团簇通过直接抗原抗体结合触发细胞凋亡,表现出良好的抗膀胱癌活性;
[0025]
(5)双靶向纳米免疫团簇在瘤内的富集程度高,可进一步提高联合诊断和治疗的效能;
[0026]
(6)双靶向纳米免疫团簇具有良好的体内抗膀胱癌作用。
附图说明
[0027]
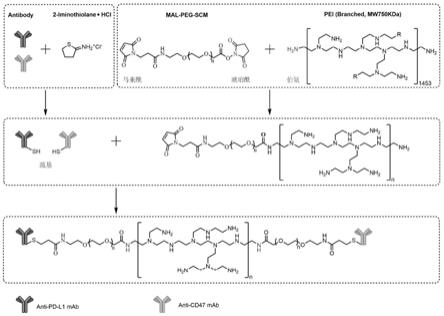
图1为抗cd47和pd-l1双靶向纳米免疫团簇的制备示意图;
[0028]
图2为纳米免疫团簇的表征分析图,其中2a为纳米免疫团簇的粒径,2b为纳米免疫团簇的3d形态;
[0029]
图3为纳米免疫团簇与5637膀胱癌细胞表面抗原的结合能力评价图;
[0030]
图4为纳米免疫团簇与5637膀胱癌细胞表面抗原结合后解离能力评价图;
[0031]
图5为纳米免疫团簇体外抗膀胱癌作用评价图,其中5a为纳米免疫团簇对5637细
胞的杀伤作用图,5b为纳米免疫团簇对5637细胞凋亡的影响图;
[0032]
图6为纳米免疫团簇瘤内富集评价图,其中6a为纳米免疫团簇在荷瘤小鼠活体内的分布,6b为纳米免疫团簇在荷瘤小鼠主要内脏和肿瘤内的分布,6c为比较游离抗体和纳米免疫团簇在肿瘤内的分布;
[0033]
图7为纳米免疫团簇体内抗膀胱癌作用评价图。
具体实施方式
[0034]
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0035]
实施例1
[0036]
一种用于膀胱癌诊断与治疗的双靶向纳米团簇,由多个巯基化的抗cd47和pd-l1抗体通过mal-peg-scm偶联到支化型聚乙烯亚胺上。
[0037]
其中,双靶向纳米免疫团簇中的骨架为聚乙烯亚胺pei,铰链为马来酰亚胺-聚乙二醇-琥珀酰亚胺mal-peg-scm。
[0038]
其中,双靶向纳米免疫团簇中所含的抗体为抗cd47抗体和抗pd-l1抗体。
[0039]
其中,双靶向纳米免疫团簇为树枝状,尺寸为100nm。
[0040]
实施例2
[0041]
参考图2,与实施例1的不同之处在于,还提供了一种用于膀胱癌诊断与治疗的双靶向纳米团簇的制备方法,具体包括以下步骤:
[0042]
s1、通过traut's试剂分别将抗cd47抗体和抗pd-l1抗体实现巯基化;
[0043]
s2、用异官能团修饰剂mal-peg-scm修饰分子量为750kda的支化型pei,获得pei-mal-peg-scm溶液;
[0044]
s3、用巯基化的抗cd47和pd-l1抗体与pei-mal-peg-scm溶液混合反应,制备得到双靶向纳米免疫团簇。
[0045]
其中,s1中将抗cd47抗体、抗pd-l1抗体溶液与traut
’
s试剂分别按照摩尔比1:20的比例在氮气环境下室温避光反应1h,并在mwco3.5kda透析袋室温透析30min,获得巯基化抗体acd47-sh和apd-l1-sh。
[0046]
其中,s2中将pei溶液与mal-peg-scm溶液按照质量比1:27室温避光反应48h,并在mwco3.5kda透析袋室温透析12h,得到pei-mal-peg-scm溶液。
[0047]
其中,将pei-mal-peg-scm、acd47-sh、apd-l1-sh按照摩尔比1:3000:3000的比例在氮气条件下4℃避光反应12h,用mwco300kda透析袋室温透析12h,获得的保留液即为双靶向纳米免疫团簇。
[0048]
实施例3
[0049]
与实施例2的不同之处在于,还提供了一种用于膀胱癌诊断与治疗的双靶向纳米团簇的应用,应用于膀胱癌的诊断和治疗;综合分析可知本发明所采用的是抗cd47和pd-l1抗体,既能充分发挥不同抗体抗原结合的联合作用,而且具有更好的普适性;此外,由于抗cd47和pd-l1双靶向纳米免疫团簇中的抗cd47和pd-l1抗体可靶向结合膀胱癌细胞表面高
表达的cd47和pd-l1抗原,其抗原结合能力良好,荧光标记后可用于膀胱癌的诊断;此外,双靶向纳米免疫团簇与抗原结合后的解离速率慢,可持续作用于膀胱癌细胞发挥协同抗膀胱癌作用;此外,双靶向纳米免疫团簇通过直接抗原抗体结合触发细胞凋亡,表现出良好的抗膀胱癌活性;此外,双靶向纳米免疫团簇在瘤内的富集程度高,可进一步提高联合诊断和治疗的效能;再者,双靶向纳米免疫团簇具有良好的体内抗膀胱癌作用。
[0050]
参考图1至图7,为了验证本用于膀胱癌诊断与治疗的双靶向纳米团簇的具体功能性,分别做了如下实验、观察,具体内容及其结果如下:
[0051]
参考图2,图2为双靶向纳米免疫团簇的表征分析:分析时进行了以下分析内容,(1)用激光光散射仪alv/cgs-3检测粒径;(2)用原子力显微镜观察形态。
[0052]
参考图3,图3为纳米免疫团簇与5637膀胱癌细胞表面抗原的结合能力评价图,其中纳米免疫团簇与5637细胞表面抗原的结合能力评价包括如下内容:收集对数生长期5637细胞8
×
104细胞/ml,用12孔板(1ml/孔)爬片,37℃培养24h;4%多聚甲醛固定15min,1%bsa溶液室温孵育30min,10μg/ml游离抗体溶液、双靶向纳米免疫团簇溶液各500μl4℃孵育过夜,用10μg/ml的fitc标记山羊抗人igg抗体溶液200μl重悬细胞沉淀后室温避光孵育1h,取用载玻片滴加含dapi抗淬灭封片剂50-100μl,封片,荧光显微镜下观察,通过荧光情况间接反映团簇与抗原的结合。
[0053]
参考图4,图4为纳米免疫团簇与5637膀胱癌细胞表面抗原结合后解离能力评价图,其中纳米免疫团簇与5637细胞表面抗原结合后解离能力评价包括如下内容:收集对数生长期5637细胞2
×
105细胞/ml,取用12孔板(1ml/孔)培养37℃培养6h,每孔分别加入10μg/ml的同型对照抗体、抗cd47抗体(c)、抗pd-l1抗体(p)、抗cd47抗体+抗pd-l1抗体(cpb)、纳米团簇(ncpc)1ml,置于37℃孵育2h,换培养基,分别于0h、1.5h、3h、6h、12h、24h时收集细胞,用10μg/ml的fitc标记山羊抗人igg抗体溶液100μl重悬,避光孵育30min,依次上样流式检测细胞表面平均荧光强度(mfi),计算分析各时间点荧光强度相对于0h时的百分比,从而间接评价团簇与抗原结合后的解离能力,具体公式如下:
[0054][0055]
参考图5,图5为纳米免疫团簇体外抗膀胱癌作用评价图,其中纳米免疫团簇体外抗膀胱癌作用评价具体包括以下内容:
[0056]
(1)细胞毒性:收集对数生长期5637膀胱癌细胞8
×
104/ml,取用96孔板每孔加入100μl,37℃培养24h。将c、p、cpb、ncpc配制成0、0.5、1、2、5、10、20、50mg/ml的不同浓度,分别加入对应孔内,37℃孵育24h。每孔加入10%cck-8工作液100μl,空白组(blank)仅加cck-8工作液,37℃孵育1-2h。酶标仪检测450nm处的光密度值(od)。根据od值计算细胞活率,从而评估载体的生物相容性,具体公式如下:
[0057][0058]
(2)细胞凋亡:对数生长期5637膀胱癌细胞,每孔按105(1ml)接种至12孔细胞培养板中37℃培养24h;将cpb、ncpc用rpmi1640完全培养基按照0、5、10、20μg/ml的浓度配制后分别加入对应孔,37℃培养24h;收集上层培养基及pbs漂洗液,与用胰蛋白酶消化收集的细
胞悬液一起1000rpm离心5min,pbs重悬后转移至1.5mlep管,再次离心收集细胞沉淀;弃上清,加入200μl的1
×
bidingbuffer重悬细胞;照组(0μg/ml)设置未染管、单染管、双染管,药物处理组设置双染管,其中未染管仅含1
×
bidingbuffer,单染管中每管需另外分别加入5μl的annexin
ⅴ-
apc或3μl的7-aad;双染管中每管加入5μl的annexin
ⅴ-
apc和3μl的aad;柔涡旋混匀后室温避光孵育20min;用流式细胞仪检测荧光信号。
[0059]
参考图6,图6为纳米免疫团簇瘤内富集评价图,其中纳米免疫团簇瘤内富集程度评价包括以下内容:5周龄balb/c雌性裸鼠麻醉后于右侧腋下注入100μlmbt2小鼠膀胱癌细胞悬液,皮下成瘤,待瘤体长至约200mm3时,将小鼠分成2组,分别予以cy5标记的cpb、ncpc15mg/kg瘤内注射1次。药物注射12h,成瘤小鼠予以异氟烷吸入麻醉,将其置于活体化学发光凝胶成像系统暗室内,拍照记录并收集小鼠体内荧光信号;随后将小鼠通过颈椎脱臼法处死,用无菌解剖器械将小鼠的心脏、肝脏、脾脏、肺脏、肾脏、肿瘤完整取出,按照分组依次摆放整齐,将其置于化学发光凝胶成像系统暗室内,拍照记录并收集小鼠体内荧光信号。
[0060]
参考图7,为纳米免疫团簇体内抗膀胱癌作用评价图,其中纳米免疫团簇体内抗膀胱癌作用具有包括以下内容:6周龄c3h/hen雌性小鼠,麻醉后,麻醉后每只小鼠注入100μlmbt2肿瘤细胞悬液皮下成瘤,待瘤体长至约100-200mm3时,将小鼠随机分成6组:pbs组、ngc(连接同型对照igg的纳米团簇)组、抗cd47单抗组(c)、抗pd-l1单抗组(p)、游离单抗联合组(cpb)、纳米免疫团簇组(ncpc),根据15mg/kg体重的剂量(按照抗体浓度)予以瘤内注射,每3天1次,共注射5次。每3天使用游标卡尺测量肿瘤的长径和短径(单位mm)肿瘤体积计算公式为:
[0061][0062]
综上分析可知,双靶向纳米免疫团簇具有良好的消灭肿瘤的能力,效果突出,为治疗癌症患者提出了更好的方法和思路。
[0063]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1