紫堇灵在防治人巨细胞病毒感染中的新用途的制作方法
[0001]
本发明属于生物医药领域,具体是一种紫堇灵在防治人巨细胞病毒感染中的新用途。
背景技术:
[0002]
人巨细胞病毒(human cytomegalovirus,hcmv)属疱疹病毒β亚科,人群普遍易感,且感染后终身带毒,感染缓解后,病毒长期潜伏在体内,形成潜伏感染,在身体免疫力低下或者器官移植病人中,容易发生继发感染,容易导致神经系统、肝脏、呼吸系统及血液系统等损伤,严重时甚至危及生命;同时,在孕妇中,hcmv的继发感染是造成新生儿先天性疾病的主要病原体,引起黄疸性肝炎、智力低下、失明、耳聋等多器官、多系统病变。因此,对人巨细胞病毒感染进行积极有效治疗,是提高出生人口素质以及提高免疫力低下老年人生活质量的重要手段。目前还没有获批的疫苗上市,临床上对症用药主要是膦甲酸钠、西多福韦、福米韦生等抗病毒药物,但是这些药物具有骨髓抑制、肾毒性和引起电解质紊乱等明显的副作用,而且还会出现耐药性,限制了其在临床上的应用。
[0003]
紫堇灵是来源于罂粟科植物布氏紫堇的一种生物碱类,到目前为止,还没有关于紫堇灵在制备预防和/或治疗hcmv药物中的应用。
技术实现要素:
[0004]
本发明采用商品化的紫堇灵,进行了系列的生物学实验,为紫堇灵防治人巨细胞病毒感染的新用途提供了理论依据。
[0005]
本发明提供了紫堇灵在制备防治人巨细胞病毒感染药物中的新用途。
[0006]
所述的紫堇灵可以抑制hcmv立即早期蛋白ie1/2和早期蛋白ul44的表达,从而发挥抗hcmv感染的作用。
[0007]
所述的紫堇灵形式包括其盐的形式以及药学上可接受的载体结合的形式。
[0008]
所述的防治人巨细胞病毒感染的药物的制剂形式为液体制剂、颗粒剂、片剂、冲剂、胶囊、缓释剂、滴丸剂或注射剂。
[0009]
生物学实验研究的结果表明:
[0010]
1.紫堇灵单独处理hcmv宿主细胞-人胚肺二倍体成纤维细胞wi-38在0-20μm没有表现出明显的细胞毒性;
[0011]
2.紫堇灵具有良好的抗hcmv的作用,具体表现为,显著抑制立即早期蛋白ie1/2和早期蛋白ul44的表达;同时抑制hcmv的核酸复制。
[0012]
本发明的优点及有益效果是通过系列的生物学实验发现并证明,紫堇灵在没有明显细胞毒性的剂量下具有显著的抗hcmv的作用,安全有效,有望将其开发为防治hcmv的药物。
附图说明
[0013]
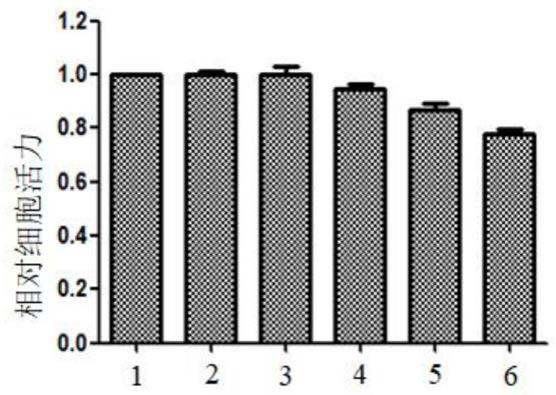
图1:mtt法测定紫堇灵对wi-38细胞活力的影响。
[0014]
其中:纵坐标-细胞活力(设置对照组为1)
[0015]
横坐标:1-对照组(control)
[0016]
2-紫堇灵(1μm)单独处理2天
[0017]
3-紫堇灵(2μm)单独处理2天
[0018]
4-紫堇灵(5μm)单独处理2天
[0019]
5-紫堇灵(10μm)单独处理2天
[0020]
6-紫堇灵(20μm)单独处理2天
[0021]
图2:western-blot法检测紫堇灵对hcmv立即早期蛋白ie1/2和早期蛋白ul44的影响(gapdh为内参)
[0022]
其中图2a:1-hcmv(moi 0.01)接种1天
[0023]
2-紫堇灵(10μm)+hcmv(moi 0.01)接种1天
[0024]
3-dmso+hcmv(moi 0.01)接种1天
[0025]
4-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)接种1天
[0026]
5-hcmv(moi 0.01)接种4天
[0027]
6-紫堇灵(10μm)+hcmv(moi 0.01)接种4天
[0028]
7-dmso+hcmv(moi 0.01)接种4天
[0029]
8-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)接种4天
[0030]
9-hcmv(moi 0.01)接种7天
[0031]
10-紫堇灵(10μm)+hcmv(moi 0.01)接种7天
[0032]
11-dmso+hcmv(moi 0.01)接种7天
[0033]
12-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)接种7天
[0034]
其中图2b:1-hcmv(moi 0.01)
[0035]
2-dmso+hcmv(moi 0.01)
[0036]
3-紫堇灵(10μm)+hcmv(moi 0.01)
[0037]
4-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)
[0038]
*p<0.5,**p<0.05,***p<0.001,与对照组比较
[0039]
图3:ifa法检测紫堇灵对hcmv立即早期蛋白ie1/2表达的影响
[0040]
其中:1-dmso+hcmv(moi 0.01)接种7天
[0041]
2-紫堇灵(1μm)+hcmv(moi 0.01)接种7天
[0042]
3-紫堇灵(5μm)+hcmv(moi 0.01)接种7天
[0043]
4-紫堇灵(10μm)+hcmv(moi 0.01)接种7天
[0044]
5-紫堇灵(20μm)+hcmv(moi 0.01)接种7天
[0045]
6-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)接种7天
[0046]
图4:qpcr法检测紫堇灵对hcmv dna扩增的影响
[0047]
其中:1-hcmv(moi 0.01)接种1天
[0048]
2-dmso+hcmv(moi 0.01)接种1天
[0049]
3-紫堇灵(10μm)+hcmv(moi 0.01)接种1天
[0050]
4-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)接种1天
[0051]
5-hcmv(moi 0.01)接种4天
[0052]
6-dmso+hcmv(moi 0.01)接种4天
[0053]
7-紫堇灵(10μm)+hcmv(moi 0.01)接种4天
[0054]
8-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)接种4天
[0055]
9-hcmv(moi 0.01)接种7天
[0056]
10-dmso+hcmv(moi 0.01)接种7天
[0057]
11-紫堇灵(10μm)+hcmv(moi 0.01)接种7天
[0058]
12-膦甲酸钠(200μg/ml)+hcmv(moi 0.01)接种7天
[0059]
*p<0.5,***p<0.001,与hcmv组比较
具体实施方式
[0060]
本发明所涉及的人胚肺二倍体成纤维细胞株wi-38和人巨细胞病毒(hcmv)towne株均来自于美国模式培养物集存库(american type culture collection,atcc)。
[0061]
实施例1紫堇灵单独处理对wi-38细胞增殖活力的影响
[0062]
通过mtt法检测细胞活力,方法如下:pd30的人胚肺二倍体成纤维细胞wi-38以每孔3000个的细胞密度接种于96孔细胞培养板中,培养24h后加入不同浓度的紫堇灵,每一浓度设3个平行孔,并设不加药物的空白对照组和无细胞的溶剂对照组。在培养箱培养48小时后,每孔加入20μl mtt(5mg/ml,用无血清的dmem培养液配制),37℃、5%co2条件下继续培养4h,然后吸净细胞培养孔内的液体,每孔加150μl dmso,在摇床上轻轻振荡10min,使结晶物充分溶解,而后于570nm处测定光吸收度,计算相对细胞活力,以不加药物的空白对照组细胞活力为100%。实验结果见图1。
[0063]
实施例2紫堇灵处理以及hcmv的接种
[0064]
采用pd30的人胚肺成纤维细胞wi-38细胞,用含10%fbs的培养基按照2
×
104/cm2的细胞量铺板六孔细胞培养板,24小时后更换0.2%fbs的培养基继续培养48小时,通过血清饥饿的方法,使其细胞周期g0/g1同步化,利于hcmv的感染。之后进行hcmv病毒(towne病毒株)的接种,接种剂量为0.01moi(感染复数),继续培养至指定时间进行相关检测。进行紫堇灵抗hcmv活性检测时,提前2小时将一定浓度的紫堇灵加至培养基中,而后接种hcmv(moi 0.01),进而观察病毒蛋白表达和dna扩增等的变化。
[0065]
实施例3western-blot检测紫堇灵对hcmv病毒蛋白表达的影响
[0066]
为了确认紫堇灵的抗hcmv作用,我们检测了紫堇灵对hcmv立即早期蛋白ie1/2和早期蛋白ul44的表达影响,细胞培养和紫堇灵处理以及hcmv接种如上述实施例2。设立不做任何药物处理,只接种hcmv的对照组;溶剂dmso处理,接种hcmv的对照组,接种hcmv和临床用膦甲酸钠(200μg/ml)处理的药物对照组,以及紫堇灵(10μm)处理和接种hcmv不同时间的实验组。接种hcmv后1、4、7天,弃去上清,用pbs洗细胞三次,用中等强度的ripa裂解液裂解细胞后收集细胞样品,用bca试剂盒测定蛋白浓度后采用相应的ie1/2和ul44抗体进行western-blot检测,结果显示紫堇灵可以显著抑制hcmv病毒蛋白ie1/2和ul44的表达(图2a、2b)。
[0067]
实施例4间接免疫荧光法(ifa)检测紫堇灵对hcmv病毒蛋白表达的影响
[0068]
具体实施方法如上述实施例2,在药物处理和hcmv接种后7天,弃去上清,用pbs洗细胞三次,用预冷的甲醇丙酮(1:1)在-20℃固定20分钟,然后弃去固定液,放置通风橱中自然晾干。用针对ie1/2蛋白的抗体进行常规ifa操作,然后在倒置荧光显微镜下观察拍照,结果显示,紫堇灵能够显著降低hcmv立即早期蛋白ie1/2的表达,并且具有剂量依赖性(图3)。
[0069]
实施例5qpcr测定紫堇灵对hcmv dna拷贝数的影响
[0070]
细胞培养、药物处理以及hcmv接种处理同上述实施例2所述。采用qpcr法测定hcmv dna的拷贝数,取10ng总dna,按照iq sybr green supermix kit(bio-rad)试剂盒说明进行,所用引物为:上游5-tctgccaggacatctttctc-3
′
(seq id no.1)和下游5
′-
gtgaccaaggccacgacgtt-3
′
(seq id no.2)。扩增条件:95℃5min,(95℃5sec,60℃30sec)
×
40循环,经法计算,结果显示,紫堇灵能够显著抑制病毒dna的拷贝数(图4)。
[0071]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1