一种可注射组织再生型壳聚糖复合凝胶支架的制备方法与流程
1.本发明属于生物医学材料领域,具体地,本发明涉及一种可注射组织再生型壳聚糖复合凝胶支架的制备方法和应用。
背景技术:
2.长期以来,利用生物材料促进或者引导组织和器官的修复和再生受到人们的广泛关注。生物材料的理化性质,诸如化学基团、粒径、孔径、亲疏水性、降解性等对于组织修复和再生起到重要的调控作用。植入非完全惰性的生物材料后,机体对于材料反应较为复杂,反映在细胞(如巨噬细胞,成纤维细胞,内皮细胞,淋巴细胞等)活动、相关因子释放、相关通路的激活,这也决定了组织修复的进程。
3.壳聚糖是一种天然的碱性多糖,可从资源丰富的虾蟹壳等中进行提取,具有可降解性、良好生物相容性、抗菌性。壳聚糖以及其衍生物在止血、防黏连及软骨组织、骨组织、皮肤、神经等组织修复和再生上有重要的应用。其中,为了达到组织修复和再生的效果,研究人员基于壳聚糖设计出多种类型的支架材料,如静电纺丝纤维支架、多孔海绵支架、水凝胶支架等。专利cn103893835b公开了通过脱钙、脱蛋白、乙酰及手工分层方式得到的壳聚糖生物膜,该膜提供了物理的屏障及多孔结构,可用作引导组织再生膜,促进成骨细胞、骨细胞的黏附和生长。然而,大多数支架为预成型的支架,不具备可注射特性且一般只适合相对规整的伤口及组织部位,对于不规则的待修复区域顺应性差。同时,为了减轻手术创伤和人们的治疗痛苦,加速了伤口的愈合,提高疾病的治愈效率与质量,可注射型水凝胶支架成为该领域新一轮的研究热点。为了解决这个,研究人员探索了可注射性和原位成型的植入性材料。专利cn111068116a公开了一种注射用软骨修复温敏凝胶及其制备方法,该方法以壳聚糖与β-甘油磷酸盐共混的温敏性凝胶为基础,同时加入胶原蛋白和细胞生长因子,利于软骨缺损的修复。但是由于涉及到复杂的合成过程及成分相对复杂,进而不利于后续的临床应用转化。专利wo20200237956a1公开了一种可注射壳聚糖溶液的方法,壳聚糖在ph低于6.2为溶液状态,当注入体内由于体液交换变成不溶性结晶的颗粒,可以作为真皮填充并促进真皮组织的重建,但是酸性溶液对人体产生刺激性,溶液流动性强,短期内无法很好地塑形。本发明创新地对壳聚糖原料的分子结构及其微凝胶粒径进行控制,并将带有负电性粘性多糖作为赋形剂混合壳聚糖微凝胶。所得的壳聚糖复合凝胶支架具有良好的支撑性,通过切力变稀作用破坏壳聚糖微凝胶和负电性多糖间的静电相互作用,可让该支架材料顺畅地通过27g针头,注射后恢复静电相互作用再次形成支架材料,实现支架材料的微创性交付;此外,通过对壳聚糖原料脱乙酰度和微凝胶粒径的控制,所得壳聚糖复合凝胶支架体可诱导正常细胞长入,并同时提供适当的炎症刺激促进新组织的再生形成。该体系材料制备工艺简单,制备工艺操作性强,生物相容性优异,在组织再生领域有广阔应用前景。
技术实现要素:
4.为了克服上述不足,本发明提供一种可注射组织再生型壳聚糖复合凝胶支架的制
备方法,壳聚糖微凝胶尺寸在20-60μm,加入赋型剂后该支架,具有微创注射性,注射后具有良好的支撑性和可降解性;支架为多孔结构并可诱导细胞长入,凝胶支架的ph位于6.8-7.4,与人体正常组织体液ph接近,在骨组织、软骨组织、皮肤等组织再生领域有着广泛应用前景。
5.为了实现上述目的,本实验采用的技术方案如下:
6.一种可注射组织再生型壳聚糖复合凝胶支架制备方法包括:
7.(1)以壳聚糖或者壳聚糖衍生物为原料,经过酸溶得到澄清溶液。
8.(2)加入碱液进行沉淀得到壳聚糖物理凝胶
9.(3)通过制粒机制粒得到壳聚糖微凝胶。
10.(4)将上述微凝胶清洗至中性后,加入具有一定黏度的负电性多糖(附型剂)溶液混合并均质化,得到可注射性壳聚糖复合凝胶支架。
11.为了控制可注射组织再生型壳聚糖复合凝胶支架的炎症水平与组织再生,需要对壳聚糖或者壳聚糖衍生物及赋形剂的选择和壳聚糖微凝胶的尺寸进行严格的控制。
12.所述壳聚糖或者壳聚糖衍生物脱乙酰度在85%-99%。
13.所述的制粒过程包括粉碎、过挤压板、过筛等。
14.所述壳聚糖微凝胶的粒径在20-60μm。
15.所述赋形剂包括透明质酸钠、羧甲基壳聚糖、海藻酸钠、羧甲基纤维素钠中的一种或者多种,黏度在500-14000mpa
·
s。
16.所述可注射组织再生型壳聚糖复合凝胶支架体系中壳聚糖微凝胶浓度为4-10%,赋形剂浓度为1%-5%,ph在6.8-7.4。
17.所述可注射组织再生型壳聚糖复合凝胶支架体系可以通过25g及更细针头,推挤力小于25n。
18.术语说明
19.壳聚糖:壳聚糖为天然多糖甲壳素脱除部分乙酰基的产物,具有生物降解性、生物相容性、无毒性、增强免疫等多种生理功能。
20.脱乙酰度:为将天然多糖甲壳素脱去乙酰基的程度,脱去程度越高,则分子链上胺基(nh2)含量则越多,而且胺基质子化而使壳聚糖在稀酸溶液中带电基团增多,聚电解质电荷密度增加,其结果必将导致其结构,性质和性能上的变化。
21.赋型剂:赋型剂为粘性多糖溶液,溶液中较大的粘性除了可以给壳聚糖微凝胶在注射时提供润滑作用,在注射后通过粘多糖和壳聚糖微凝胶之间的分子间作用力(氢键、静电等相互作用)提供材料稳定的力学性能。
22.组织工程支架:组织工程支架材料是指能与组织活体细胞结合并能植入生物体的不同组织,并根据具体替代组织具备的功能的材料。为了使种子细胞增殖和分化,需要提供一个由生物材料所构成的细胞支架,支架材料相当于人工细胞外基质。
23.本发明的主要优点在于:
24.(1)本发明提出的可注射组织再生型壳聚糖复合凝胶支架,具有良好注射性,可以从25g针头及更小的针头注射,实现微创性。
25.(2)本发明提出的可注射组织再生型壳聚糖复合凝胶支架,具有良好的塑形性和可降解性,该支架内部疏松多孔,可以支持细胞生长,不会产生有毒有害的物质。
26.(3)本发明提出的可注射组织再生型壳聚糖复合凝胶支架,壳聚糖微凝胶的粒径在20-60μm,可以有效地控制炎症水平和促进组织再生。
27.(4)本发明提出的可注射组织再生型壳聚糖复合凝胶支架制备工艺简单易行,适合大规模工业化生产,具有临床应用的潜力。
附图说明
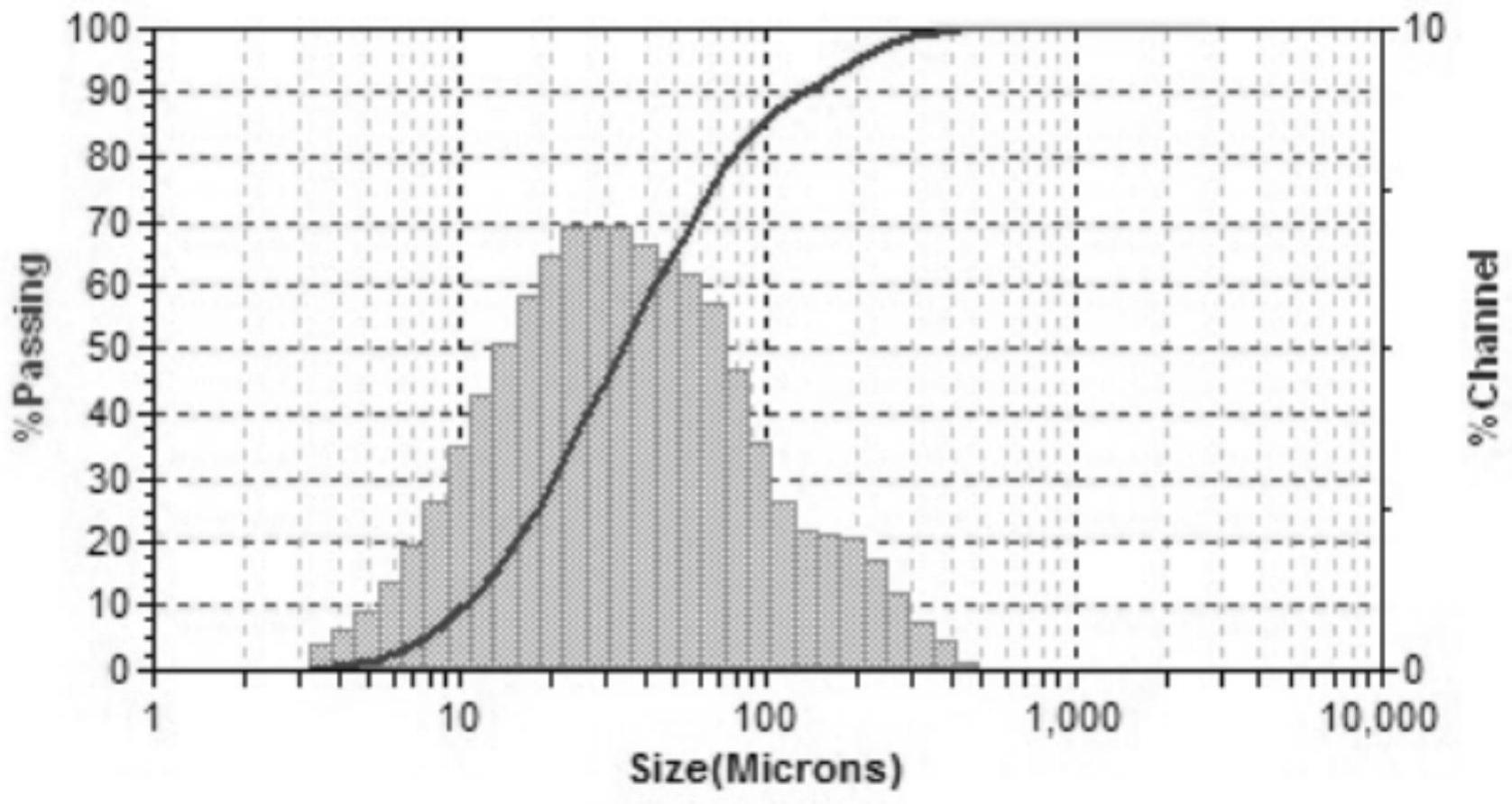
28.图1壳聚糖微凝胶粒径;
29.图2可注射性壳聚糖复合凝胶支架推挤力;
30.图3可注射组织再生型壳聚糖复合凝胶支架皮下植入20天实物图;
31.图4可注射组织再生型壳聚糖复合凝胶支架皮下植后h&e组织染色。
具体实施方式
32.以下通过实施例对本发明特征及其它相关特征作进一步详细说明,以便于同行业技术人员的理解,但不以任何方式限制本发明。本技术领域的技术人员,在本发明的实质范围内,作出的变化、改型、添加或替换,都应属于本发明的保护范围。
33.实施例1
34.将脱乙酰度为90%的壳聚糖溶于1%冰乙酸溶液,得到0.7%壳聚糖溶液,溶解均匀。接着,逐滴加入1m氢氧化钠溶液,析出壳聚糖物理凝胶。待析出完全后,将上述析出物用纯水分散,放置粉碎机进行粉碎,粉碎20min,使用激光粒度仪测试其粒径分布,其粒径中位数为33.71μm,如附图1所示。
35.实施例2
36.将实施例1中的壳聚糖凝胶反复使用纯水清洗,待ph至中性后,使用200μm挤压板进一步制粒均质化,得到壳聚糖物理凝胶。将7%壳聚糖微凝胶与1%的羧甲基纤维素钠(黏度为6000mpa
·
s)溶液混合均匀,过100目绢丝均质化,得到可注射性壳聚糖复合凝胶支架。利用万能拉力机测试其推挤力,推挤速度为30mm/min,测试3次,针头为27g针头(bd hypoint tm,0.4*13mm)。其推挤力如附图2,测试范围内的平均推挤力为9.27n。
37.实施例3
38.将实施例1中的壳聚糖凝胶反复使用纯水清洗,待ph至中性后,使用500μm及200μm挤压板进一步制粒均质化,得到壳聚糖物理凝胶。将8%壳聚糖微凝胶与1.7%的羟丙甲纤维素溶液混合均匀,得到可注射性壳聚糖复合凝胶支架。
39.实施例4
40.将实施例1中的壳聚糖凝胶反复使用纯水清洗,待ph至中性后,得到壳聚糖物理凝胶。将5%壳聚糖微凝胶与1.5%的羧甲基纤维素钠溶液(黏度为1000mpa
·
s)混合均匀,过200μm挤压板均质化得到可注射性壳聚糖复合凝胶支架。
41.实施例5
42.将实施例4中可注射组织再生型壳聚糖复合凝胶支架植入家兔皮下,在植入20天后解剖观察。通过实物图(附图3)可以看出,凝胶支架的颜色较植入前有轻微的发黄,在凝胶支架的表面有血管和组织的形成。h&e可以看出(附图4),在材料表面及内部出现血管壁和血红细胞等,表明血管的形成;在材料与组织的交界处存在成纤维细胞、巨噬细胞及而凝
胶的内部有少量的细胞浸润。新生血管是营养供给的纽带,是组织再生的基础,因而可注射性壳聚糖复合凝胶支架有利于促进组织再生。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1