脂质运载蛋白突变蛋白的吸入施用的制作方法
脂质运载蛋白突变蛋白的吸入施用
1.i.背景
2.通过吸入在气道中的药物递送可以用于局部和/或全身作用,这取决于治疗需要和雾化药物穿过空气-血液屏障的能力。吸入的药物被递送至肺,在肺中良好的血管形成、极大的溶质交换能力、和肺泡上皮的超薄性是可以促进经由肺部施用肽和蛋白质的全身递送的独特特征(agu等,respir res,2001)。然而,本领域中仍然存在许多与分子和施用途径相关的挑战。
3.脂质运载蛋白是能够在大小、形状和化学特性方面适应多种靶标的蛋白骨架(skerra,biochim biophys acta,2000)。脂质运载蛋白共有高度保守的总体折叠结构,其由安装在稳定的β-桶骨架上的四环可变区组成(skerra,febs j,2008)。最近,脂质运载蛋白家族成员已作为靶标结合蛋白而成为研究主题,该研究主题通常在生命科学中具有关键作用,其大部分已被抗体(免疫球蛋白)占据(wo99/16873;wo03/029463;wo03/029471;schlehuber和skerra,biophys chem,2002;skerra,j biotechnol,2001)。脂质运载蛋白突变蛋白是一类基于脂质运载蛋白结构的分子,通过突变其结合位点以进一步增加其可塑性而产生,由此允许这样的突变蛋白结合至所选靶标。
4.目前没有批准的用于吸入递送抗体的系统或批准的吸入的抗体治疗剂。虽然有许多批准的用于吸入的小分子,但它们具有许多缺点,包括低靶向亲和力、脱靶结合和对其它器官的副作用。吸入的生物治疗剂,包括蛋白质(例如抗体和抗体样分子)和肽,可以用作替代物,从而提供增加的靶标结合能力和效力以及减少的脱靶效应。然而,蛋白质和肽的吸入施用对递送装置提出了严格的要求,并且某些屏障,特别是呼吸上皮,损害吸入的蛋白质和肽的吸收和全部与区域(例如,远端肺)沉积。因此,本领域仍然需要通过吸入提供基于蛋白质的疗法诸如抗体或抗体样治疗剂的有效递送。本技术的技术问题是满足所述需要。通过提供权利要求中反映的、说明书中描述的以及随后的实施例和附图中示出的实施方案,解决了技术问题。
5.ii.定义
6.以下列表定义了本说明书中使用的术语、短语和缩写。本文列出和定义的所有术语旨在涵盖所有语法形式。
7.如本文所用,“可检测的亲和力”是指以通常通过kd或ec
50
测量的至多约10-5
m或更低的亲和力结合所选靶标的能力(较低的kd或ec50值反映较好的结合活性)。较低的亲和力通常不再能用普通方法如elisa(酶联免疫吸附试验)测量,因此具有次要的重要性。
8.如本文所用,本公开的蛋白质(例如脂质运载蛋白的突变蛋白)或其融合多肽与选定靶标的“结合亲和力”可通过本领域技术人员已知的多种方法测量(并由此可确定突变蛋白-配体复合物的kd值)。这些方法包括、但不限于荧光滴定、竞争elisa、比色法诸如等温滴定量热法(itc)和表面等离子体共振(spr)。这些方法在本领域中是建立成熟的,并且其实例也在下面详述。
9.还应注意,各种结合剂与其配体之间的复合物形成受许多不同因素影响,诸如相应结合配偶体的浓度、竞争剂的存在、ph和所用缓冲体系的离子强度和用于测定解离常数
kd的实验方法(例如荧光滴定、竞争elisa或表面等离子体共振,仅列举几个)或甚至用于评价实验数据的数学算法。
10.因此,技术人员还清楚的是,kd值(在相应结合剂与其靶标/配体之间形成的复合物的解离常数)可在一定实验范围内变化,这取决于用于测定特定脂质运载蛋白突变蛋白对给定配体的亲和力的方法和实验设置。这意味着,取决于例如kd值是通过表面等离子体共振(spr)、竞争elisa还是通过直接elisa测定地,在所测得的kd值可能存在轻微偏差或可能存在容差范围。
11.如本文所用,“突变蛋白”、“突变的”实体(无论是蛋白质或核酸)或“突变体”是指与天然存在的(野生型)核酸或蛋白质“参照”骨架相比,一个或多个核苷酸或氨基酸的交换、缺失或插入。“参照骨架”优选地是成熟的人泪脂质运载蛋白或成熟的人嗜中性粒细胞明胶酶相关脂质运载蛋白。所述“参照骨架”还包括如本文所述的突变蛋白和变体的片段。
12.如本文所用,“泪脂质运载蛋白”是指人泪脂质运载蛋白(htlc),并且还是指成熟的人泪脂质运载蛋白。术语“成熟(的)”当用于表征蛋白质时,表示基本上不含信号肽的蛋白质。本公开的“成熟htlc”指人泪脂质运载蛋白的成熟形式,其不含信号肽。成熟htlc由以登记号p31025保藏于swiss-prot数据库的序列的残基19-176描述,其氨基酸在seq id no:1中示出。
13.如本文所用,“脂质运载蛋白-2”或“嗜中性粒细胞明胶酶相关脂质运载蛋白”是指人脂质运载蛋白-2(hlcn2)或人嗜中性粒细胞明胶酶相关脂质运载蛋白(hngal),并且还是指成熟hlcn2或成熟hngal。术语“成熟(的)”当用于表征蛋白质时,表示基本上不含信号肽的蛋白质。本公开的“成熟hngal”是指人嗜中性粒细胞明胶酶相关脂质运载蛋白的成熟形式,其不含信号肽。成熟hngal由以登记号p80188保藏于swiss-prot数据库的序列的残基21-198描述,其氨基酸在seq id no:2中示出。
14.如本文与本公开的突变蛋白有关所用的术语“片段”涉及来源于所述突变蛋白的蛋白质或肽,诸如全长成熟人泪脂质运载蛋白(htlc或htlpc)或全长成熟人嗜中性粒细胞明胶酶相关脂质运载蛋白(hngal),其n-端和/或c-端截短,即缺少n-端和/或c-端氨基酸的至少一个。这样的片段可以缺少n-端和/或c-端氨基酸的至多2个、至多3个、至多4个、至多5个、至多10个、至多15个、至多20个、至多25个或至多30个(包括其间的所有数字)。作为一个说明性实例,这样的片段可以缺少一个、两个、三个或四个n-端和/或一个或两个c-端氨基酸,尤其是如果突变蛋白来源于htlc。应当理解,所述片段优选地是全长脂质运载蛋白(突变蛋白)的功能片段,这表示其优选地包含其来源的全长脂质运载蛋白(突变蛋白)的结合口袋。作为一个说明性实例,这样的功能片段可以至少在对应于成熟htlc线性多肽序列的位置5-158、1-156、5-153、5-150、9-148、12-140、20-135或26-133处包含氨基酸。作为另一个说明性实例,这样的功能片段可以至少在对应于成熟hngal线性多肽序列的位置5-168、8-160、13-157、15-150、18-141、20-134、25-134或28-134处包含氨基酸。这样的片段可以包括成熟脂质运载蛋白一级序列的至少10个、更多诸如20或30或更多个连续氨基酸,并且通常在成熟脂质运载蛋白的免疫试验中可检测到。片段可以与蛋白质或多肽的天然序列具有至少约50%、60%、70%、75%、80%、85%、90%、92%、95%或至少约98%氨基酸序列同一性。通常,如本文关于本公开的脂质运载蛋白突变蛋白的对应蛋白靶标所用的术语“片段”涉及n-端和/或c-端缩短的蛋白或肽配体,其保留全长配体被根据本公开的突变蛋白识别
和/或结合的能力。
15.如本文所用,术语“变体”涉及蛋白质或多肽的衍生物,其包括突变,例如通过氨基酸序列或核苷酸序列的取代、缺失、插入和/或化学修饰。在一些实施方案中,这样的突变和/或化学修饰不降低蛋白质或肽的功能性。这样的取代可以是保守的,即,氨基酸残基被化学上相似的氨基酸残基替代。保守取代的实例是下列组的成员之间的替代:1)丙氨酸、丝氨酸、苏氨酸和缬氨酸;2)天冬氨酸、谷氨酸、谷氨酰胺、天冬酰胺和组氨酸;3)精氨酸、赖氨酸、谷氨酰胺、天冬酰胺和组氨酸;4)异亮氨酸、亮氨酸、甲硫氨酸、缬氨酸、丙氨酸、苯丙氨酸、苏氨酸和脯氨酸;和5)异亮氨酸、亮氨酸、甲硫氨酸、苯丙氨酸、酪氨酸和色氨酸。这样的变体包括蛋白质或多肽,其中一个或多个氨基酸已被它们各自的d-立体异构体或被除天然存在的20个氨基酸以外的氨基酸诸如例如鸟氨酸、羟脯氨酸、瓜氨酸、高丝氨酸、羟赖氨酸、正缬氨酸取代。这样的变体还包括例如其中在n-和/或c-端添加或缺失一个或多个氨基酸残基的蛋白质或多肽。通常,变体与天然序列蛋白质或多肽具有至少约50%、60%、70%、75%、80%、85%、90%、92%、95%或至少约98%氨基酸序列同一性。变体优选地保留其衍生的蛋白质或多肽的生物活性,例如结合相同的靶标。
16.如本文所用的术语“诱变”表示选择实验条件使得成熟脂质运载蛋白的给定序列位置处天然存在的氨基酸可以被不存在于相应天然多肽序列中该特定位置处的至少一个氨基酸取代。术语“诱变”还包括通过一个或多个氨基酸的缺失或插入对序列片段的长度的(额外)修饰。因此,例如,在选定序列位置处的一个氨基酸被三个随机突变的区段替代,导致与野生型蛋白质的相应段的长度相比两个氨基酸残基的插入,这在本公开的范围内。这种插入或缺失可以彼此独立地引入本公开中可以进行诱变的肽段的任一个中。在本公开的一个示例性实施方案中,可以将几个突变的插入引入所选脂质运载蛋白骨架的环ab中(参见国际专利公开no.wo2005/019256,其通过引用整体并入本文)。
17.如本文所用,术语“随机诱变”表示在某个序列位置处不存在预定的突变(氨基酸改变),但在诱变过程中至少两个氨基酸可以以某个概率掺入预定的序列位置。
18.如本文所用,术语“序列同一性”或“同一性”是指测量其相似性或关系的序列的性质。如本公开所用,术语“序列同一性”或“同一性”表示在本公开的蛋白质或多肽的序列与所讨论的序列(同源)比对后,相对于这两个序列中较长序列中的残基数目,成对相同残基的百分比。序列同一性通过将相同氨基酸残基的数目除以残基总数并将除数乘以100来测量。
19.如本文所用,术语“序列同源性”或“同源性”具有其通常含义,并且同源氨基酸包括相同氨基酸以及被认为是本公开的蛋白质或多肽(例如,本公开的任何融合蛋白或脂质运载蛋白突变蛋白)的线性氨基酸序列中等同位置处的保守取代的氨基酸。
20.技术人员将认识到用于使用标准参数测定序列同源性或序列同一性的可用的计算机程序,例如blast(altschul等,nucleic acids res,1997)、blast2(altschul等,j mol biol,1990)、tblastn(altschul等,j mol biol,1990)、fasta(pearson和lipman,proc natl acad sci u s a,1988)、gap(wisconsin gcg程序包,acceleers inc)和smith-waterman(smith和waterman,j mol biol,1981)。序列同源性或序列同一性的百分比可以例如使用2002年11月16日2.2.5版的程序blastp(altschul等,nucleic acids res,1997)在本文中测定。在该实施方案中,同源性百分比基于包括前肽序列的整个蛋白质或多肽序
列(矩阵:blosum 62;缺口成本:11.1;截止值设置为10-3
)的比对,优选地使用野生型蛋白质骨架作为成对比较中的参照。它计算为blastp程序输出中显示为结果的“阳性”(同源氨基酸)数目除以程序选择用于比对的氨基酸总数的百分比。
21.具体地,为了确定脂质运载蛋白(突变蛋白)氨基酸序列的氨基酸残基是否与野生型脂质运载蛋白的氨基酸序列中某个位置对应的野生型脂质运载蛋白不同,技术人员可使用本领域熟知的手段和方法,例如手动或通过使用计算机程序诸如blast 2.0(其代表基本局部比对搜索工具)或clustalw或任何其它适于产生序列比对的合适程序进行比对。因此,脂质运载蛋白的野生型序列可以用作“主题序列”或“参考序列”,而与本文所述野生型脂质运载蛋白不同的脂质运载蛋白的氨基酸序列用作“查询序列”。术语“野生型序列”和“参考序列”和“主题序列”在本文中可互换使用。优选的人泪脂质运载蛋白野生型序列是如seq id no:1所示的成熟人泪脂质运载蛋白序列。hngal的优选的野生型序列是如seq id no:2所示的成熟hngal序列。
[0022]“缺口”是比对中由于氨基酸的添加或缺失而产生的空间。因此,完全相同序列的两个拷贝具有100%同一性,但是不那么高度保守并且具有缺失、添加或替代的序列可以具有较低程度的序列同一性。本领域技术人员将认识到,可用用于使用标准参数确定序列同一性的几种计算机程序,例如blast(altschul等,nucleic acids res,1997)、blast2(altschul等,j mol biol,1990)、tblastn(altschul等,j mol biol,1990)、fasta(pearson和lipman,proc natl acad sci u s a,1988)、gap(wisconsin gcg程序包,accelerys inc)和smith-waterman(smith和waterman,j mol biol,1981)。
[0023]
如本文所用,术语“位置”表示本文所述氨基酸序列内的氨基酸的位置或本文所述核酸序列内的核苷酸的位置。应理解,当如本文在一种或多种脂质运载蛋白突变蛋白的氨基酸序列位置的上下文中使用术语“对应”或“相应(的)”时,对应位置不仅由前面的核苷酸或氨基酸的数目决定。因此,由于(突变或野生型)脂质运载蛋白中其它地方氨基酸的缺失或添加,根据本公开的给定氨基酸的绝对位置可以与相应位置不同。类似地,由于突变蛋白或野生型脂质运载蛋白5
’‑
非翻译区(utr)中其它地方的缺失或额外核苷酸,包括启动子和/或任何其它调节序列或基因(包括外显子和内含子),根据本公开的给定核苷酸的绝对位置可以与相应位置不同。
[0024]
根据本公开的“相应位置”可以是在根据本公开的成对或多个序列比对中与其对应的序列位置比对的序列位置。优选地理解的是,对于根据本公开的“相应位置”,核苷酸或氨基酸的绝对位置可以不同于相邻的核苷酸或氨基酸,但是可能已经交换、缺失或添加的所述相邻的核苷酸或氨基酸可以被相同的一个或多个“相应位置”包含。
[0025]
此外,对于基于根据本公开的参考序列的脂质运载蛋白突变蛋白中的相应位置,优选地理解的是,脂质运载蛋白突变蛋白的核苷酸或氨基酸的位置可以在结构上对应于参考脂质运载蛋白(野生型脂质运载蛋白)或另一种脂质运载蛋白突变蛋白中其它地方的位置,即使它们的绝对位置数目可能不同,如本领域技术人员根据脂质运载蛋白中高度保守的总体折叠模式所理解地。
[0026]
如本文所用,“抗体”包括完整抗体或其任何抗原结合片段(即,“抗原结合部分”)或单链。完整抗体是指包含通过二硫键相互连接的至少两条重链(hc)和两条轻链(lc)的糖蛋白。每条重链由重链可变结构域(vh或hcvr)和重链恒定区(ch)组成。重链恒定区由三个结
构域c
h1
、c
h2
和c
h3
组成。每条轻链由轻链可变结构域(v
l
或lcvr)和轻链恒定区(c
l
)组成。轻链恒定区由一个结构域c
l
组成。vh和v
l
区可进一步细分为高变区,称为互补决定区(cdr),其间散布着更保守的区域,称为框架区(fr)。每个vh和v
l
由三个cdr和四个fr组成,从氨基端到羧基端按以下顺序排列:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。重链和轻链的可变区包含与抗原相互作用的结合结构域。抗体的恒定区可以任选地介导免疫球蛋白与宿主组织或因子的结合,包括免疫系统的各种细胞(例如效应细胞)和经典补体系统的第一组分(c1q)。
[0027]
如本文所用,抗体的“抗原结合片段”是指抗体的保留特异性结合抗原(例如gpc3)的能力的一个或多个片段。已经显示抗体的抗原结合功能可以通过全长抗体的片段来执行。包含在术语抗体的“抗原结合片段”内的结合片段的实例包括(i)由vh、v
l
、c
l
和c
h1
结构域组成的fab片段;(ii)包含在铰链区由二硫键连接的两个fab片段的f(ab’)2片段;(iii)由vh、v
l
、c
l
和c
h1
结构域以及c
h1
和c
h2
结构域之间的区域组成的fab’片段;(iv)由vh和c
h1
结构域组成的fd片段;(v)由抗体的单臂的vh和v
l
结构域组成的单链fv片段,(vi)由vh结构域组成的dab片段(ward等,nature,1989);和(vii)分离的互补决定区(cdr)或两个或更多个分离的cdr的组合,其可以任选地通过合成接头连接;(viii)包含使用短接头连接在同一多肽链中的vh和v
l
的“双抗体”(参见,例如,专利文献ep404,097;wo93/11161;和holliger等,proc natl acad sci u sa,1993);(ix)仅含有vh或v
l
的“结构域抗体片段”,其中在一些情况下两个或更多个vh区共价连接。
[0028]
抗体可以是多克隆或单克隆的;异种、同种异体或同基因的;或其修饰形式(例如,人源化、嵌合或多特异性的)。抗体也可以是完全的人的。
[0029]“受试者”是脊椎动物,优选哺乳动物,更优选人。本文所用的术语“哺乳动物”是指归类为哺乳动物的任何动物,包括、但不限于人、家畜和农场动物,以及动物园、运动或宠物动物,例如绵羊、狗、马、猫、牛、大鼠、猪、猿例如食蟹猴(cynomolgous monkey)等,仅举几个说明性实例。优选地,本文的“哺乳动物”是人、小鼠或非人灵长类动物。优选地,所述受试者是人。
[0030]“有效量”是足以产生有益或所需结果的量。有效量可以在一次或多次施用中施用。
[0031]“样品”定义为取自任何受试者的生物样品。生物样品包括、但不限于血液、血清、尿、粪便、精液或组织。
[0032]
如本文所用,“吸入施用”或“通过吸入施用”是指经由呼吸道施用,通常通过口腔吸入或鼻吸入。该物质可以是气体、液体气溶胶、细粉末或液体喷雾的形式。吸入施用可以使用吸入器进行。
[0033]“施用剂量”对应于已经施用给受试者的化合物的剂量。在使用微型喷雾器装置进行气管内施用物质的情况下,“施用剂量”对应于“递送剂量”。
[0034]“计量剂量”或“装置剂量”,特别是在吸入装置的上下文中,涉及装置已经装载的物质的剂量。
[0035]“递送剂量”是指递送给受试者的物质的剂量,即当应用该装置时从吸入装置出来的剂量。例如,喷雾器有时有意过度填充,因为最终总体积将不会雾化。对于喷雾器,递送剂量通常小于标称剂量的50%,该标称剂量是装载到装置中的总活性物质。标称剂量也被称为装置剂量或计量剂量。对于干粉吸入器,递送剂量通常为计量剂量的约85-90%。技术人
员可以通过确定从吸入装置出来的物质的量来容易地确定递送剂量。例如,欧洲药典9.0第2.9.44节提供了用于实验测量“递送剂量”的方法。
[0036]
如本文所用,“局部暴露”或“局部施用”表示没有局部施用物质的实质性部分进入循环系统。优选地,进入循环系统的物质的量在量化限值(blq)以下。在其他情况下,可以测量进入循环系统的物质的量,但其将不被认为是实质性的。在物质的吸入施用的情况下,“局部暴露”或“局部施用”可以表示物质基本上保留在呼吸系统中。由于在一些情况下,特别是如果受试者是人,则难以直接测量保留在呼吸系统中的物质的量,因此优选地通过确定进入循环系统的物质的量来间接地进行“局部暴露”或“局部施用”的确定。
[0037]
如本文所用,“全身暴露”表示局部施用物质的实质性部分进入循环系统,并且任选地,整个身体可能受到该物质的影响。全身暴露可以表示进入循环系统的物质的量是可量化的。全身暴露可等同于进入血流的可定量的物质的浓度。这种暴露可以由物质的血液(血清、血浆或全血)浓度表示,其可以随时间测量并由包括曲线下面积(auc)的一系列参数记录。对物质的全身暴露也可影响生物标志物,其水平可直接与物质浓度相关,并因此与全身暴露相关。当与全身暴露结合使用时,术语“可定量的”或“可检测的”是指由物质的血液(血清、血浆或全血)浓度或由通过本领域已知的一种或多种分析方法可测量的生物标志物的水平表示的暴露。这样的分析方法包括、但不限于elisa、竞争elisa、荧光滴定、比色法、质谱法(ms)和层析法,例如高效液相层析(hplc)。还应理解,使用这样的分析方法进行的测量与检测限值相关联,例如仪器检测限值、方法检测限值和定量限值。
[0038]
如本文所用,药物的“起效”或“作用起效”是指施用后药物效果达到显著所花费的持续时间。在一些实施方案中,在达到例如50%、60%、70%、80%、90%或100%的最大治疗作用时,可以认为药物效果是显著的。在一些实施方案中,当施用药物的受试者的症状减轻时,药物效果可以被认为是显著的。药物的起效可以通过确定从这样的药物的任何施用结束至达到与基线相比药物治疗作用变化的所需水平例如90%或最大水平的时间来定量。在一些具体实施方案中,如实施例4中所述,药物的起效可以被确定为达到与基线相比颈动脉血管阻力50%、60%、70%、80%、90%或甚至更高百分比降低的持续时间。药物的起效可以例如是约1至5分钟、约1至25分钟、约5至25分钟或约10至20分钟。
[0039]
无论在本文何处使用,术语“和/或”都包括“和”、“或”和“由所述术语连接的元件的全部或任何其它组合”的含义。
[0040]
如本文所用,术语“约”或“大约”表示在给定值或范围的20%内、优选地10%内、并且更优选地5%内。然而,该术语也包括具体的数字,例如,“约20”包括20。
[0041]
iii.附图的描述
[0042]
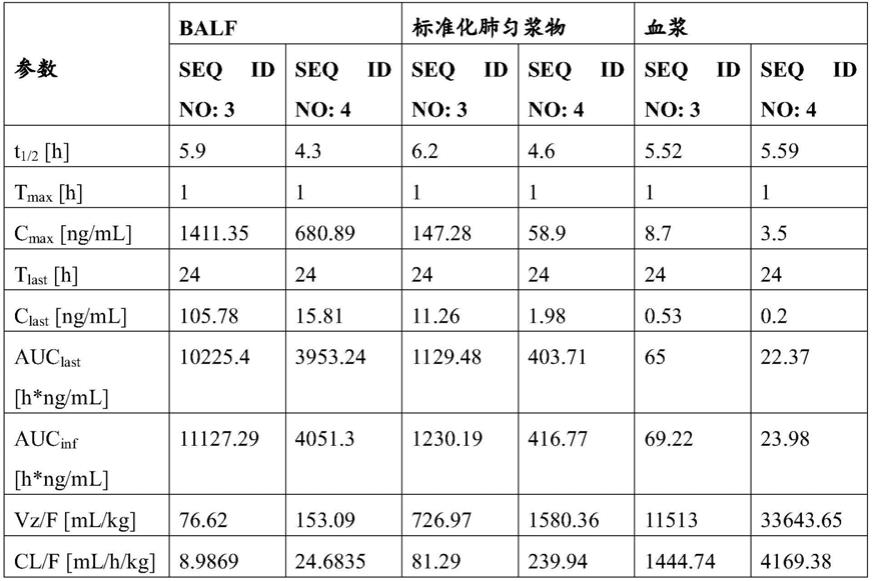
图1:提供了如实施例1所述,seq id no:3(hngal的脂质运载蛋白突变蛋白,图1a)和seq id no:4(htlc的脂质运载蛋白突变蛋白,图1b)的小鼠药代动力学分析结果。以100μg/kg的剂量给小鼠气管内施用测试脂质运载蛋白突变蛋白。使用基于电化学发光(ecl)的试验检测支气管肺泡灌洗液(balf)、标准化肺匀浆物和血浆中的药物水平。脂质运载蛋白突变蛋白在三个区室的每一个中都显示具有相似pk特性(profile)的不同浓度。
[0043]
图2:提供了如实施例2所述,以100μg/小鼠的剂量气管内施用seq id no:3(hngal的脂质运载蛋白突变蛋白,图2a)和seq id no:4(htlc的脂质运载蛋白突变蛋白,图2b)的小鼠药代动力学分析结果。使用基于ecl的试验检测balf、标准化肺匀浆物和血浆中的药物
水平。脂质运载蛋白突变蛋白在三个区室的每一个中都显示相似pk特性。两种脂质运载蛋白突变蛋白在所有三个区室中都显示浓度的时间依赖性降低,但如通过auc
inf
所测量地,balf中具有比肺中高的暴露水平,而肺中比血浆中高。
[0044]
图3:提供了如实施例3所述,以2mg/kg的剂量静脉内注射seq id no:3(hngal的脂质运载蛋白突变蛋白)和seq id no:4(htlc的脂质运载蛋白突变蛋白)的小鼠药代动力学分析结果。使用基于ecl的试验检测血清药物水平。两种脂质运载蛋白突变蛋白显示相似的pk谱。
[0045]
图4:提供了以1mg/kg的剂量静脉内施用、以5mg/kg的剂量皮下施用、以5mg/kg的剂量气管内施用、或以5mg/kg的剂量气管内施用富马酰基二酮哌嗪(fdkp)后用示例性脂质运载蛋白突变蛋白(seq id no:47)处理的大鼠中感觉神经介导的血管舒张结果。作为对照,还经由静脉内施用测试了参照抗cgrp抗体(seq id nos:204和205),如实施例4所述。在脂质运载蛋白突变蛋白处理的动物中,神经刺激后大鼠后爪背内侧皮肤中的皮肤血流与未处理动物中观察到的相比显著降低,最大变化与参照抗cgrp抗体观察到的相当,表明通过阻断cgrp的血管收缩增加。气管内施用的脂质运载蛋白突变蛋白与皮下施用的脂质运载蛋白突变蛋白相比显示更快的起效,并且与静脉内施用的脂质运载蛋白突变蛋白或参照抗体相比显示相当的或甚至更快的起效。
[0046]
图5:提供了如实施例4所述,以2.5mg/kg、5mg/kg或10mg/kg的剂量气管内施用(图5a)或以1mg/kg、2.5mg/kg、5mg/kg或10mg/kg的剂量静脉内施用(图5b)后用示例性脂质运载蛋白突变蛋白(seq id no:47)处理的大鼠中感觉神经介导的血管舒张结果。作为对照,还经由静脉内施用测试了参照抗cgrp抗体(seq id nos:204和205)。在脂质运载蛋白突变蛋白处理的动物中,神经刺激后大鼠后爪背内侧皮肤的皮肤血流与未处理动物中观察到的相比显著降低,表明通过阻断cgrp的血管收缩增加。气管内施用的脂质运载蛋白突变蛋白seq id no:47在两小时研究期间显示抑制血管舒张的快速起效(数分钟内)和持久效力。
[0047]
图6:提供了如实施例4所述,以2.5mg/kg、5mg/kg或10mg/kg的剂量气管内施用(图6a)或以1mg/kg、2.5mg/kg、5mg/kg或10mg/kg的剂量静脉内施用(图6b)后用示例性脂质运载蛋白突变蛋白(seq id no:47)处理的大鼠中血浆脂质运载蛋白突变蛋白浓度。
iv.具体实施方式
[0048]
本发明基于通过吸入施用的脂质运载蛋白突变蛋白导致呼吸道中、特别是肺中的局部暴露的惊人发现。吸入的药物通常允许与全身递送(口服或注射)所需相比的更低剂量,因此具有更低的风险特征,具有更少和严重性更小的副作用的可能性(bodier-montagutelli等,expert opin drug deliv,2018)。吸入的药物的其它优点包括更容易的自我施用和更好的患者依从性(与注射相比)和更快的作用模式。在一些情况下,局部递送后的全身扩散也会发生,并提供治疗益处。本发明还基于通过吸入施用的脂质运载蛋白突变蛋白也可导致全身暴露的惊人发现。不希望受理论的束缚,据信脂质运载蛋白突变蛋白是否进入全身循环或是否可检测到全身暴露尤其取决于施用或递送至肺的脂质运载蛋白突变蛋白的剂量。
[0049]
本发明还基于通过吸入全身施用脂质运载蛋白突变蛋白能够使脂质运载蛋白突变蛋白快速递送至循环系统的惊人发现。已经令人惊讶地发现,在脂质运载蛋白突变蛋白
的施用后约0.1至约10小时、优选地在施用后约0.5小时至约5小时、优选地在施用后约1小时至约2小时之后,可达到血浆中脂质运载蛋白突变蛋白的最大浓度。
[0050]
本发明还基于通过这样的脂质运载蛋白突变蛋白的吸入施用可实现脂质运载蛋白突变蛋白的高全身暴露水平(递送剂量的一位或两位数百分比)的惊人发现。这样的高水平是令人惊讶的,因为wo2013/087660公开了在施用后一小时在血液中仅检测到0.2%的已气管内施用给小鼠的脂质运载蛋白突变蛋白的实验。
[0051]
本发明还基于取决于脂质运载蛋白突变蛋白的剂量,也可实现对肺的局部施用而无可检测的脂质运载蛋白突变蛋白的全身暴露的令人惊讶的发现。如果脂质运载蛋白突变蛋白的治疗效果在肺中局部实现并且不需要或甚至不期望对脂质运载蛋白突变蛋白的全身暴露,则这是特别有利的。
[0052]
因此,本发明涉及给受试者施用脂质运载蛋白突变蛋白的方法,其中所述方法包括通过吸入施用脂质运载蛋白突变蛋白,其中所述施用提供在呼吸道中对脂质运载蛋白突变蛋白的局部暴露。
[0053]
本发明还涉及用于在受试者的疗法中使用的脂质运载蛋白突变蛋白,其中所述使用包括通过吸入施用脂质运载蛋白突变蛋白,其中所述施用提供在呼吸道中对脂质运载蛋白突变蛋白的局部暴露。
[0054]
本发明还涉及脂质运载蛋白突变蛋白用于制备用于吸入施用的药物的用途,其中吸入施用提供在呼吸道中对脂质运载蛋白突变蛋白的局部暴露。
[0055]
本发明还涉及给受试者施用脂质运载蛋白突变蛋白的方法,其中所述方法包括通过吸入施用脂质运载蛋白突变蛋白,其中所述施用提供对脂质运载蛋白突变蛋白的全身暴露。
[0056]
本发明还涉及用于在受试者的疗法中使用的脂质运载蛋白突变蛋白,其中所述使用包括通过吸入施用脂质运载蛋白突变蛋白,其中所述施用提供对脂质运载蛋白突变蛋白的全身暴露。
[0057]
本发明还涉及脂质运载蛋白突变蛋白用于制备用于吸入施用的药物的用途,其中吸入施用提供对脂质运载蛋白突变蛋白的全身暴露。
[0058]
a.本公开的脂质运载蛋白突变蛋白
[0059]
如本文所用,“脂质运载蛋白”定义为重量约18-20kda的单体蛋白,其具有圆柱形β折叠片超二级结构区,所述结构区包含通过多个(优选四个)环在一端成对连接的多个(优选八个)β链,由此限定结合袋。正是本应刚性的脂质运载蛋白骨架中环的多样性在脂质运载蛋白家族成员中产生了多种不同的结合模式,每种能够适应不同大小、形状和化学特性的靶标(例如在skerra,biochim biophys acta,2000,flower等,biochim biophys acta,2000,flower,biochem j,1996中综述)。实际上,脂质运载蛋白家族蛋白质天然进化为结合广谱配体,共有异常低水平的总体序列保守性(通常具有小于20%序列同一性),但仍保留高度保守的总体折叠模式。各种脂质运载蛋白中位置之间的对应性是本领域技术人员熟知的(参见,例如,美国专利no.7,250,297)。
[0060]
如上所述,脂质运载蛋白是由其超二级结构定义的多肽,所述结构即圆柱形β折叠片超二级结构区,其包含八个β链,所述β链通过在一端的四个环成对连接,由此限定结合袋。本公开不限于本文具体公开的脂质运载蛋白突变蛋白。在这方面,本公开涉及具有圆柱
形β折叠片超二级结构区的脂质运载蛋白突变蛋白,所述结构区包含通过一端的四个环成对的八个β链,由此限定结合袋,其中所述四个环中至少三个的每一个的至少一个氨基酸与参照序列相比已突变,并且其中所述脂质运载蛋白以可检测的亲和力有效结合其靶标。
[0061]
根据本公开的脂质运载蛋白突变蛋白可以是任何脂质运载蛋白的突变蛋白。可以使用其突变蛋白的合适的脂质运载蛋白(有时也称为“参照脂质运载蛋白”、“野生型脂质运载蛋白”、“参照蛋白质骨架”或简称为“骨架”)的实例包括、但不限于泪脂质运载蛋白(脂质运载蛋白-1、tlc或von ebner腺蛋白)、视黄醇结合蛋白、嗜中性粒细胞脂质运载蛋白型前列腺素d合酶、β-乳球蛋白、后胆色素结合蛋白(bbp)、载脂蛋白d(apod)、嗜中性粒细胞明胶酶相关脂质运载蛋白(ngal)、α2-微球蛋白相关蛋白(a2m)、24p3/子宫运载蛋白(24p3)、von ebner腺蛋白1(vegp 1)、von ebner腺蛋白2(vegp 2)和主要变应原can f 1(all-1)。在相关的实施方案中,脂质运载蛋白突变蛋白源自由人泪脂质运载蛋白(htlc)、人嗜中性粒细胞明胶酶相关脂质运载蛋白(hngal)、人载脂蛋白d(hapod)和大菜粉蝶(pieris brassicae)后胆色素结合蛋白组成的脂质运载蛋白组。
[0062]
当相较于与另一种脂质运载蛋白(也见上文)的序列同一性时,根据本公开的脂质运载蛋白突变蛋白的氨基酸序列与其来源的参照(或野生型)脂质运载蛋白(例如,htlc或hngal)相比可具有高序列同一性。在该一般背景下,根据本公开的脂质运载蛋白突变蛋白的氨基酸序列至少基本上类似于相应的参照(野生型)脂质运载蛋白的氨基酸序列,条件是在比对中可能存在由于氨基酸添加或缺失而产生的缺口(如本文所定义)。在一些实施方案中,与相应的参照(野生型)脂质运载蛋白的序列基本上相似的本公开的脂质运载蛋白突变蛋白的相应序列与相应的脂质运载蛋白的序列具有至少60%、至少65%、至少70%、至少75%、至少80%、至少82%、至少85%、至少87%、至少90%同一性,包括至少95%同一性。在这方面,本公开的脂质运载蛋白突变蛋白当然可以含有如本文所述的取代,其使得脂质运载蛋白突变蛋白能够结合所选靶标。
[0063]
通常,脂质运载蛋白突变蛋白在包含配体结合袋并限定配体结合袋入口的开放端的四个环中包含一个或多个突变的氨基酸残基——相对于野生型或参照脂质运载蛋白的氨基酸序列,例如htlc和hngal(见上文)。如上所述,这些区域在确定脂质运载蛋白突变蛋白对所需靶标的结合特异性中是必需的。在一些实施方案中,本公开的脂质运载蛋白突变蛋白还可含有四个环之外的突变的氨基酸残基区域。在一些实施方案中,本公开的脂质运载蛋白突变蛋白可在连接脂质运载蛋白封闭端的β链的三个肽环(命名为bc、de和fg)中的一个或多个中含有一个或多个突变的氨基酸残基。在一些实施方案中,源自泪脂质运载蛋白、ngal脂质运载蛋白或其同源物的突变蛋白可以在n-端区和/或在β-桶结构端部排列的三个肽环bc、de和fg中的任何序列位置处具有1、2、3、4或更多个突变的氨基酸残基,所述β-桶结构端部位于天然脂质运载蛋白结合口袋的对面。在一些实施方案中,与野生型泪脂质运载蛋白序列相比,源自泪脂质运载蛋白、ngal脂质运载蛋白或其同源物的突变蛋白在β-桶结构端部排列的肽环de中可没有突变的氨基酸残基。
[0064]
设想了任何类型和数量的突变,包括取代、缺失和插入,只要提供的脂质运载蛋白突变蛋白保留其结合其靶标的能力,和/或其与参照(野生型)脂质运载蛋白例如成熟htlc或成熟hngal的氨基酸序列具有为至少60%,例如至少65%、至少70%、至少75%、至少80%、至少85%或更高同一性的序列同一性。在一些实施方案中,取代是保守取代。在一些
实施方案中,取代是非保守取代。
[0065]
具体地,为了确定不同于参照(野生型)脂质运载蛋白的脂质运载蛋白突变蛋白的氨基酸序列的氨基酸残基是否对应于所述参照(野生型)脂质运载蛋白的氨基酸序列中的某个位置,技术人员可使用本领域熟知的手段和方法,例如,手动或通过使用计算机程序进行比对,所述计算机程序诸如blast2.0(其代表基本局部比对搜索工具)或clustalw或任何其它适于产生序列比对的合适程序。因此,参照(野生型)脂质运载蛋白的氨基酸序列可用作“主题序列”或“参照序列”,而脂质运载蛋白突变蛋白的氨基酸序列用作“查询序列”(也见上文)。
[0066]
保守取代通常是以下取代,其根据待突变的氨基酸列出,每个后跟着一个或多个可以被认为是保守的替代:ala
→
ser、thr或val;arg
→
lys、gln、asn或his;asn
→
gln、glu、asp或his;asp
→
glu、gln、asn或his;gln
→
asn、asp、glu或his;glu
→
asp、asn、gln或his;his
→
arg、lys、asn、gln、asp或glu;ile
→
thr、leu、met、phe、val、trp、tyr、ala或pro;leu
→
thr、ile、val、met、ala、phe、pro、tyr或trp;lys
→
arg、his、gln或asn;met
→
thr、leu、tyr、ile、phe、val、ala、pro或trp;phe
→
thr、met、leu、tyr、ile、pro、trp、val或ala;ser
→
thr、ala或val;thr
→
ser、ala、val、ile、met、val、phe、pro或leu;trp
→
tyr、phe、met、ile或leu;tyr
→
trp、phe、ile、leu或met;val
→
thr、ile、leu、met、phe、ala、ser或pro。其它取代也是允许的,并且可以凭经验或根据其它已知的保守或非保守取代来确定。作为进一步的方向,以下组各自含有通常可用于定义彼此保守取代的氨基酸:(a)丙氨酸(ala)、丝氨酸(ser)、苏氨酸(thr)、缬氨酸(val);(b)天冬氨酸(asp)、谷氨酸(glu)、谷氨酰胺(gln)、天冬酰胺(asn)、组氨酸(his);(c)精氨酸(arg)、赖氨酸(lys)、谷氨酰胺(gln)、天冬酰胺(asn)、组氨酸(his);(d)异亮氨酸(ile)、亮氨酸(leu)、甲硫氨酸(met)、缬氨酸(val)、丙氨酸(ala)、苯丙氨酸(phe)、苏氨酸(thr)、脯氨酸(pro);和(e)异亮氨酸(ile)、亮氨酸(leu)、甲硫氨酸(met)、苯丙氨酸(phe)、酪氨酸(tyr)、色氨酸(trp)。
[0067]
如果这种取代导致生物活性的变化,则可以引入更实质的变化,例如以下或如下面关于氨基酸类别进一步描述的变化,并且筛选产物的所需特征。这种更实质的变化的实例是:ala
→
leu或phe;arg
→
glu;asn
→
ile、val或trp;asp
→
met;cys
→
pro;gln
→
phe;glu
→
arg;his
→
gly;ile
→
lys、glu或gln;leu
→
lys或ser;lys
→
tyr;met
→
glu;phe
→
glu、gln或asp;trp
→
cys;tyr
→
glu或asp;val
→
lys、arg、his。
[0068]
在一些实施方案中,通过选择取代来实现脂质运载蛋白(突变蛋白)的物理和生物性质的实质性修饰,所述取代在它们对维持以下方面的作用中显著不同:(a)取代区域中多肽主链的结构,例如,作为片状或螺旋状构象,(b)靶标位点处的分子的电荷或疏水性,或(c)侧链的体积。
[0069]
天然存在的残基基于共同的侧链性质被分成以下的组:(1)疏水性:甲硫氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸;(2)中性亲水性:半胱氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺;(3)酸性:天冬氨酸、谷氨酸;(4)碱性:组氨酸、赖氨酸、精氨酸;(5)影响链取向的残基:甘氨酸、脯氨酸;和(6)芳香性:色氨酸、酪氨酸、苯丙氨酸。在一些实施方案中,取代可能需要将这些类别之一的成员与另一类别交换。
[0070]
非保守取代将需要将这些类别之一的成员交换为另一类别。任何不参与维持相应脂质运载蛋白的正确构象的半胱氨酸残基也可以通常用丝氨酸取代,以改善分子的氧化稳
定性并防止异常交联。相反,可以将半胱氨酸键加入脂质运载蛋白以改善其稳定性。
[0071]
任何不参与维持相应脂质运载蛋白的正确构象的半胱氨酸残基也可以通常用丝氨酸取代,以改善分子的氧化稳定性并防止异常交联。相反,可以将半胱氨酸键加入脂质运载蛋白以改善其稳定性。
[0072]
在一些实施方案中,本文公开的脂质运载蛋白突变蛋白可以是或包含成熟人泪脂质运载蛋白(htlc)的突变蛋白。成熟htlc的突变蛋白在本文中可命名为“htlc突变蛋白”。在一些其它实施方案中,本文公开的脂质运载蛋白突变蛋白是成熟人嗜中性粒细胞明胶酶相关脂质运载蛋白(hngal)的突变蛋白。成熟hngal突变蛋白在本文中可称为“hngal突变蛋白”。
[0073]
任何突变,包括如上文所讨论的插入,都可以使用已建立的标准方法在核酸例如dna水平上非常容易地完成。氨基酸序列的改变的示例性实例是插入或缺失以及氨基酸取代。此外,代替替代单个氨基酸残基,也可以插入或缺失脂质运载蛋白(突变蛋白)的一级结构的一个或多个连续氨基酸,只要这些缺失或插入产生稳定的折叠/功能性突变蛋白。
[0074]
氨基酸序列的修饰包括单个氨基酸位置的定向诱变,以便通过掺入用于某些限制酶的切割位点来简化突变的脂质运载蛋白基因或其部分的亚克隆。此外,也可掺入这些突变以进一步提高脂质运载蛋白突变蛋白对给定靶标的亲和力。此外,如果需要,可以引入突变以便调节突变蛋白的某些特征,例如以改善折叠稳定性、血清稳定性、蛋白抗性或水溶性,或以降低聚集趋势。例如,天然存在的半胱氨酸残基可以突变为其它氨基酸以防止二硫键形成。也可以将其它氨基酸序列位置故意突变成半胱氨酸以便引入新的反应基团,例如用于缀合其它化合物,诸如聚乙二醇(peg)、羟乙基淀粉(hes)、生物素、肽或蛋白质,或用于形成非天然存在的二硫键。产生的硫醇部分可用于peg化或hes化突变蛋白,例如,以便增加相应脂质运载蛋白突变蛋白的血清半衰期。将半胱氨酸残基引入htlc突变蛋白的氨基酸序列的这种突变的示例性可能性包括thr 40
→
cys、glu 73
→
cys、arg 90
→
cys、asp 95
→
cys和glu 131
→
cys的置换。类似地,对于人ngal的突变蛋白,将半胱氨酸残基引入脂质运载蛋白突变蛋白氨基酸序列的示例性可能性包括至少在对应于人ngal野生型序列的序列位置14、21、60、84、88、116、141、145、143、146或158的序列位置中一个处引入半胱氨酸(cys)残基。在任何上述氨基酸位置的侧面处产生的硫醇部分可用于peg化或hes化突变蛋白,例如,以便增加相应脂质运载蛋白突变蛋白的血清半衰期。
[0075]
在另一个实施方案中,为了提供用于将上述化合物之一缀合至根据本公开的脂质运载蛋白突变蛋白的合适的氨基酸侧链,可通过诱变引入人工氨基酸。通常,将这样的人工氨基酸设计成更具反应性,并因此促进与所需化合物的缀合。可经由人工trna引入的这样的人工氨基酸的一个实例为对乙酰基苯丙氨酸。
[0076]
对于本文公开的突变蛋白的几种应用,以融合蛋白的形式使用它们可能是有利的。在一些实施方案中,本公开的脂质运载蛋白突变蛋白在其n-端或其c-端与蛋白质、蛋白质结构域或肽例如信号序列和/或亲和标签融合。
[0077]
亲和标签诸如strep-标签或strep-标签ii(schmidt等,j mol biol,1996)、c-myc-标签、flag-标签、his-标签或ha-标签或蛋白质诸如谷胱甘肽-s-转移酶,允许容易地检测和/或纯化重组蛋白,是合适的融合配偶体的进一步实例。最后,具有生色或荧光性质的蛋白质诸如绿色荧光蛋白(gfp)或黄色荧光蛋白(yfp至少一个)也是用于本公开的脂质
运载蛋白突变蛋白的合适融合配偶体。
[0078]
通常,可以用任何合适的化学物质或酶标记本公开的脂质运载蛋白突变蛋白,其在化学、物理、光学或酶促反应中直接或间接产生可检测的化合物或信号。物理反应和同时的光学反应/标记物的实例是在照射时发射荧光或当使用放射性标记时发射x射线。碱性磷酸酶、辣根过氧化物酶和β-半乳糖苷酶是催化生色反应产物形成的酶标记(和同时的光学标记)的实例。通常,常用于抗体的所有标记(除了仅与免疫球蛋白的fc部分中的糖部分一起使用的那些)也可用于与本公开的脂质运载蛋白突变蛋白缀合。本公开的脂质运载蛋白突变蛋白还可与任何合适的治疗活性剂缀合,例如用于将这样的试剂靶向递送至给定细胞、组织或器官,或用于选择性靶向细胞(例如,肿瘤细胞)而不影响周围的正常细胞。这种治疗活性剂的实例包括放射性核素、毒素、小的有机分子和治疗肽(诸如作为细胞表面受体的激动剂/拮抗剂的肽或竞争给定细胞靶标上的蛋白质结合位点的肽)。然而,本公开的脂质运载蛋白突变蛋白也可与治疗活性核酸诸如反义核酸分子、小干扰rna、微小rna或核酶缀合。这样的缀合物可以通过本领域熟知的方法生产。
[0079]
本公开还涉及用于产生如本文所述的脂质运载蛋白突变蛋白的方法,其中突变蛋白、突变蛋白的片段或突变蛋白与另一多肽的融合蛋白通过基因工程方法的手段从编码突变蛋白的核酸开始产生。该方法可在体内进行,脂质运载蛋白突变蛋白可例如在细菌或真核宿主生物体中产生,然后从该宿主生物体或其培养物中分离。也可以在体外生产蛋白质,例如通过使用体外翻译系统。
[0080]
当体内产生脂质运载蛋白突变蛋白时,通过重组dna技术(如上文已经概述的)的手段将编码这样的突变蛋白的核酸引入合适的细菌或真核宿主生物体。为此目的,首先使用已建立的标准方法用克隆载体转化宿主细胞,所述克隆载体包括编码如本文所述的脂质运载蛋白突变蛋白的核酸分子。然后在允许异源dna表达并因此允许相应多肽合成的条件下培养宿主细胞。随后,从细胞或从培养基中回收多肽。
[0081]
在一些实施方案中,本技术中公开的核酸分子,例如dna,可以“可操作地连接”到本公开的另一个核酸分子,以允许表达本公开的融合蛋白。在这方面,可操作连接是其中第一核酸分子的序列元件和第二核酸分子的序列元件以使融合蛋白能够作为单一多肽表达的方式连接的连接。
[0082]
此外,在用于本公开的htlc突变蛋白的一些实施方案中,可去除cys 61和cys 153之间的天然存在的二硫键。因此,可以在具有还原性氧化还原环境的细胞区室中,例如在革兰氏阴性细菌的细胞质中,产生这样的突变蛋白。
[0083]
在本公开的脂质运载蛋白突变蛋白包括分子内二硫键的情况下,可优选的是使用适当的信号序列将新生多肽引导至具有氧化性氧化还原环境的细胞区室。这样的氧化性环境可以由革兰氏阴性细菌诸如大肠杆菌的周质提供、在革兰氏阳性细菌的细胞外环境中或在真核细胞内质网的内腔中,并且通常有利于结构二硫键的形成。
[0084]
然而,也可以在宿主细胞、优选大肠杆菌的胞质溶胶中产生本公开的突变蛋白。在这种情况下,多肽可以直接以可溶和折叠状态获得,或者以包涵体的形式回收,然后在体外复性。另一种选择是使用具有氧化性细胞内环境特定宿主菌株,其因此可以允许在胞质溶胶中形成二硫键(venturi等,j mol biol,2002)。
[0085]
然而,如本文所述的脂质运载蛋白突变蛋白可能不一定仅通过使用基因工程生成
或产生。相反,这样的突变蛋白也可以通过化学合成诸如merrifield固相多肽合成或通过体外转录和翻译获得。例如可能的是使用分子建模鉴定有希望的突变,体外合成继续这样的突变的多肽,并研究关于其靶标的结合活性和其它期望的性质(例如稳定性)。用于多肽/蛋白质的固相和/或液相合成的方法是本领域熟知的(参见例如,bruckdorfer等,curr pharm biotechnol,2004)。
[0086]
在另一个实施方案中,本公开的脂质运载蛋白突变蛋白可以采用本领域技术人员已知的充分建立的方法通过体外转录/翻译产生。
[0087]
技术人员将理解可用于制备由本公开考虑、但其蛋白质或核酸序列未在本文中明确公开的脂质运载蛋白突变蛋白的方法。总的来说,氨基酸序列的这样的修饰包括,例如,单个氨基酸位置的定向诱变,以便通过掺入用于某些限制酶的切割位点来简化突变的脂质运载蛋白基因或其部分的亚克隆。此外,也可掺入这些突变以进一步改善脂质运载蛋白突变蛋白对其靶标的亲和力。此外,如果需要,可以引入突变以调节突变蛋白的某些特征,以致改善折叠稳定性、血清稳定性、蛋白抗性或水溶性,或以致降低聚集趋势。例如,天然存在的半胱氨酸残基可以被突变为其它氨基酸以防止二硫键形成。
[0088]
本文公开的脂质运载蛋白突变蛋白及其衍生物可用于与抗体或其片段类似的许多领域。例如,脂质运载蛋白突变蛋白可用于标记酶、抗体、放射性物质或具有生物化学活性或确定的结合特征的任何其它基团。通过这样做,可以检测它们各自的靶标或其缀合物或融合蛋白,或使它们与它们接触。此外,本公开的脂质运载蛋白突变蛋白可用于通过已建立的分析方法(例如,elisa或western印迹)的手段或通过显微术或免疫传感器检测化学结构。在这方面,检测信号可通过使用合适的突变蛋白缀合物或融合蛋白直接产生,或通过免疫化学检测经由抗体的结合的突变蛋白间接产生。
[0089]
1.对il4-rα特异性的脂质运载蛋白突变蛋白
[0090]
白介素-4受体α链(il-4rα)是i型跨膜蛋白,其可以结合白介素4和白介素13以调节b细胞中ige抗体的产生。在t细胞中,编码的蛋白质也可以结合白介素4以促进th2细胞的分化。
[0091]
对il-4受体、特别是人il-4rα特异性的脂质运载蛋白突变蛋白公开于国际专利公开wo2008/015239、wo2011/154420和wo2013/087660中。bruns ib、fitzgerald mf、pardali k、gardiner p、keeling dj、axelsson lt、jing f、licklitl j、close dr,吸入il-4rα拮抗剂azd1402/prs-060的人中首次数据(first-in-human data for the inhaled il-4rαantagonist azd1402/prs-060)已经报道了对人il-4rα特异性的脂质运载蛋白突变蛋白的吸入施用,揭示了用于治疗哮喘的有前景的临床特征,在美国胸科协会年会(dallas,tx,usa,2019年5月17-22日)上提出;bruns ib、fitzgerald mf、pardali k、gardiner p、keeling dj、axelsson lt、jiang f、lickliter j、close dr,吸入il-4rα拮抗剂azd1402/prs-060(il-4rα的有效和选择性阻断剂)的1期评价(phase 1evaluation of the inhaled il-4rαantagonist azd1402/prs-060,a potent and selective blocker of the il-4rα),在欧洲呼吸学会国际会议(madrid,spain,2019年9月28日-10月2日)上提出;将二者通过参考引入本文。
[0092]
本公开的il-4rα特异性脂质运载蛋白突变蛋白可以是人泪脂质运载蛋白的突变蛋白。与成熟人泪脂质运载蛋白的线性多肽序列(seq id no:1)相比,这样的突变蛋白可包
含以下突变的氨基酸残基的组之一:
[0093]
(a)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
gly;leu 56
→
gln;ile 57
→
arg;ser 58
→
ile;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0094]
(b)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
lys;leu 56
→
gln;ile 57
→
arg;ser 58
→
asn;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
‑→
gln;
[0095]
(c)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys,glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;leu 56
→
gln;ile 57
→
arg;ser 58
→
arg;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0096]
(d)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
ser;leu 56
→
gln;ile 57
→
arg;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0097]
(e)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
his;leu 33
→
tyr;glu 34
→
ser;leu 56
→
gln;ile 57
→
arg;ser 58
→
ala;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0098]
(f)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
asp;leu 56
→
gln;ile 57
→
arg;ser 58
→
lys;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0099]
(g)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
gly;leu 56
→
gln;ile 57
→
arg;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0100]
(h)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
gly;leu 56
→
gln;ile 57
→
arg;ser 58
→
ile;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0101]
(i)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
a1a;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
lys;leu 56
→
gln;ile 57
→
arg;ser 58
→
asn;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0102]
(j)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys,glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;leu 56
→
gln;ile 57
→
arg;ser 58
→
arg;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0103]
(k)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
ser;leu 56
→
gln;ile 57
→
arg;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0104]
(l)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
his;leu 33
→
tyr;glu 34
→
ser;leu 56
→
gln;ile 57
→
arg;ser 58
→
ala;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;
[0105]
(m)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
asp;leu 56
→
gln;ile 57
→
arg;ser 58
→
lys;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln;或
[0106]
(n)arg 26
→
ser;glu 27
→
arg;phe 28
→
cys;glu 30
→
arg;met 31
→
ala;asn 32
→
tyr;leu 33
→
tyr;glu 34
→
gly;leu 56
→
gln;ile 57
→
arg;asp 80
→
ser;lys 83
→
arg;glu 104
→
leu;leu 105
→
cys;his 106
→
pro;lys 108
→
gln。
[0107]
本公开的il-4rα特异性脂质运载蛋白突变蛋白可包含选自seq id nos:177-194的氨基酸序列或其片段或变体。本公开的il-4rα特异性脂质运载蛋白突变蛋白可与seq id nos:177-194中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0108]
2.对cgrp特异性的脂质运载蛋白突变蛋白
[0109]
降钙素基因相关肽(cgrp)是由中枢和外周神经系统的神经分泌的血管活性神经肽,在该处含cgrp的神经元与血管密切相关。cgrp介导的血管舒张也与神经原性炎症相关,作为导致血浆外渗和微血管舒张的事件级联的一部分,并且存在于偏头痛中。
[0110]
对cgrp特异性的脂质运载蛋白突变蛋白公开于国际专利公开wo2017/097946中。
[0111]
本公开的cgrp特异性脂质运载蛋白突变蛋白可以是hngal的突变蛋白。与成熟hngal的线性多肽序列(seq id no:2)相比,这样的突变蛋白可包含以下突变的氨基酸残基的组之一:
[0112]
(a)gln 28
→
his;leu 36
→
glu;ala 40
→
trp;ile 41
→
gly;gln 49
→
lys;tyr 52
→
ala;ser 68
→
asp;leu 70
→
gln;arg 72
→
ile;lys 73
→
glu;arg 81
→
gly;cys 87
→
ser;asn 96
→
ala;tyr 100
→
glu;leu 103
→
gln;tyr 106
→
asn;lys 125
→
glu;ser 127
→
trp;tyr 132
→
leu;lys 134
→
trp;
[0113]
(b)gln 28
→
his;leu 36
→
phe;ala 40
→
met;ile 41
→
trp;gln 49
→
phe;tyr 52
→
gly;ser 68
→
trp;leu 70
→
trp;arg 72
→
glu;lys 73
→
ala;trp79
→
gly;arg 81
→
asn;cys 87
→
ser;asn 96
→
gly;tyr100
→
pro;leu 103
→
met;tyr 106
→
his;lys 125
→
glu;ser 127
→
phe;tyr 132
→
trp;lys 134
→
trp;
[0114]
(c)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
thr;tyr 52
→
gln;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ser;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;tyr 106
→
ile;lys 125
→
gly;tyr 132
→
ile;lys 134
→
glu:
[0115]
(d)gln 28
→
his;leu 36
→
arg;ile 41
→
glu;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
trp;lys 73
→
gln;asp 77
→
ile;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
thr;tyr 106
→
ala;lys 125
→
val;ser 127
→
arg;tyr 132
→
trp;lys 134
→
glu;
[0116]
(e)gln 28
→
his;leu 36
→
ile;ala 40
→
trp;ile 41
→
trp;gln 49
→
leu;ser 68
→
his;leu 70
→
met;arg 72
→
met;lys 73
→
thr;trp 79
→
thr;cys 87
→
ser;tyr 100
→
ile;leu 103
→
met;tyr 106
→
leu;lys 125
→
phe;ser 127
→
trp;tyr 132
→
trp;lys 134
→
his;
[0117]
(f)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ser;lys 73
→
glu;lys 75
→
arg;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;phe 83
→
ser;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;
tyr 106
→
ile;lys 125
→
gly;tyr 132
→
ile;lys 134
→
glu;
[0118]
(g)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;leu 42
→
arg;asp 47
→
asn;gln 49
→
thr;tyr 52
→
gln;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ser;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;phe 83
→
ser;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;tyr 106
→
ile;lys 125
→
gly;tyr 132
→
ile;lys 134
→
glu;
[0119]
(h)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;asn 65
→
asp;ser 68
→
trp;leu 70
→
tyr;phe 71
→
leu;arg 72
→
ser;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;phe 83
→
ser;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;tyr 106
→
ile;lys 125
→
gly;val 126
→
met;tyr 132
→
ile;lys 134
→
glu;thr 145
→
ala;
[0120]
(i)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;asp 47
→
asn;gln 49
→
thr;tyr 52
→
gln;val 66
→
ala;ser 68
→
trp;leu 70
→
tyr;phe 71
→
leu;arg 72
→
ser;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;phe 83
→
ser;cys 87
→
ser;asn 96
→
thr;ile 97
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;tyr 132
→
ile;lys 134
→
glu;
[0121]
(j)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
ile;lys 62
→
arg;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ser;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
ile;ser 146
→
asn;
[0122]
(k)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
pro;tyr 52
→
gln;lys 62
→
arg;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ser;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;phe 83
→
ser;cys 87
→
ser;asn 96
→
thr;lys 98
→
gln;tyr 100
→
his;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;val 126
→
met;ser 127
→
gly;tyr 132
→
ile;lys 134
→
glu;
[0123]
(1)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
lys;lys 62
→
arg;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
leu;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
ile;ser 146
→
asn;
[0124]
(m)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
lys;lys 62
→
arg;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
ile;ser 146
→
asn;
[0125]
(n)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
lys;lys 62
→
arg;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
ile;ser 146
→
asn;
[0126]
(o)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
lys;lys 62
→
arg;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;asp 77
→
arg;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;tyr 100
→
his;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
ile;ser 146
→
asn;
[0127]
(p)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;
[0128]
(q)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
ile;lys 62
→
arg;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ser;lys 73
→
glu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;val 111
→
met;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
ile;ser 146
→
asn;
[0129]
(r)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
arg;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
phe;
[0130]
(s)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
met;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
tyr;
[0131]
(t)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
leu;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
trp;
[0132]
(u)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
ile;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
glu;
[0133]
(v)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
val;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
tyr;
[0134]
(w)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
arg;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
trp;
[0135]
(x)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
asn;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
leu;
[0136]
(y)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
arg;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
val;
[0137]
(z)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
lys;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
asp;
[0138]
(aa)leu 36
→
trp;ala 40
→
thr;ile 41
→
leu;gln 49
→
ile;tyr 52
→
gln;thr 54
→
met;ser 68
→
trp;leu 70
→
tyr;arg 72
→
ala;lys 73
→
asp;cys 76
→
phe;asp 77
→
asn;trp 79
→
his;arg 81
→
glu;cys 87
→
ser;asn 96
→
thr;leu 103
→
glu;ser 105
→
pro;tyr 106
→
ile;lys 125
→
gly;ser 127
→
asn;tyr 132
→
ile;lys 134
→
glu;thr 136
→
val;ser 146
→
asn;cys 175
→
asp;
[0139]
(bb)gln 28
→
his;leu 36
→
arg;ala 40
→
glu;ile 41
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
ser;lys 73
→
glu;asp 77
→
ile;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
val;tyr 106
→
ala;lys 125
→
val;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;
[0140]
(cc)gln 28
→
his;leu 36
→
arg;ala 40
→
asp;ile 41
→
ala;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;asp 77
→
met;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
val;tyr 106
→
ala;lys 125
→
leu;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;
[0141]
(dd)gln 28
→
his;leu 36
→
arg;gly 38
→
ala;ala 40
→
asp;ile 41
→
arg;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
ser;lys 73
→
arg;asp 77
→
ile;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
thr;tyr 106
→
gly;lys 125
→
val;ser 127
→
gly;tyr 132
→
ser;lys 134
→
glu;
[0142]
(ee)gln 28
→
his;leu 36
→
arg;ala 40
→
asp;ile 41
→
glu;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;asp 77
→
met;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
val;tyr 106
→
gly;lys 125
→
val;ser 127
→
arg;tyr 132
→
leu;lys 134
→
glu;
[0143]
(ff)gln 28
→
his;leu 36
→
arg;ala 40
→
asp;ile 41
→
val;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;lys 75
→
arg;asp 77
→
met;trp 79
→
val;ile 80
→
thr;arg 81
→
his;cys 87
→
ser;lys 98
→
glu;leu 103
→
val;tyr 106
→
ala;asn 114
→
asp;phe 123
→
val;lys 125
→
leu;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;
[0144]
(gg)gln 28
→
his;leu 36
→
arg;gly 38
→
ala;ala 40
→
asp;ile 41
→
val;glu 44
→
asp;lys 46
→
asn;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;asp 77
→
met;trp 79
→
val;ile 80
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
val;tyr 106
→
ala;lys 125
→
leu;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;ile 135
→
val:
[0145]
(hh)gln 28
→
his;leu 36
→
arg;ala 40
→
asp;ile 41
→
thr;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;phe 71
→
leu;arg 72
→
val;lys 73
→
gln;asp 77
→
met;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
val;tyr 106
→
ala;phe 123
→
val;lys 125
→
leu;ser 127
→
lys;asn 129
→
ser;tyr 132
→
leu;lys 134
→
glu;
[0146]
(ii)gln 28
→
his;leu 36
→
arg;ala 40
→
asp;ile 41
→
thr;glu 44
→
lys;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;asp 77
→
met;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
val;tyr 106
→
ala;phe 123
→
val;lys 125
→
leu;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;
[0147]
(jj)gln 28
→
his;leu 36
→
arg;ala 40
→
asp;ile 41
→
ala;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;asp 77
→
met;trp 79
→
val;arg 81
→
his;cys 87
→
ser;leu 103
→
val;tyr 106
→
ala;val 108
→
ile;ser 112
→
asn;phe 123
→
val;lys 125
→
leu;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;
[0148]
(kk)gln 28
→
his;leu 36
→
arg;ala 40
→
asp;ile 41
→
ala;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;phe 71
→
leu;arg 72
→
val;lys 73
→
gln;asp 77
→
met;trp 79
→
val;arg 81
→
his;cys 87
→
gly;leu 103
→
val;tyr 106
→
ala;phe 123
→
val;lys 125
→
leu;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;
[0149]
(ll)leu 36
→
arg;ala 40
→
asp;ile 41
→
val;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;lys 75
→
arg;cys 76
→
leu;asp 77
→
met;trp 79
→
val;ile 80
→
thr;arg 81
→
his;cys 87
→
ser;lys 98
→
glu;leu 103
→
val;tyr 106
→
ala;asn 114
→
asp;phe 123
→
val;lys 125
→
leu;ser 127
→
lys;tyr 132
→
leu;lys 134
→
glu;cys 175
→
ile;ile 176
→
asp;asp 177
→
gly;
[0150]
(mm)leu 36
→
arg;ala 40
→
asp;ile 41
→
val;gln 49
→
glu;tyr 52
→
glu;ser 68
→
asp;leu 70
→
gly;arg 72
→
val;lys 73
→
gln;lys 75
→
arg;cys 76
→
tyr;asp 77
→
met;trp 79
→
val;ile 80
→
thr;arg 81
→
his;cys 87
→
ser;lys 98
→
glu;leu 103
→
val;tyr 106
→
ala;asn 114
→
asp;phe 123
→
val;lys 125
→
leu;ser 127
→
lys;tyr 132
→
212的氨基酸序列或其片段或变体。本公开的cgrp特异性脂质运载蛋白突变蛋白可与seq id nos:6-51和206-212中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0159]
3.对铁调素(hepcidin)特异性的脂质运载蛋白突变蛋白
[0160]
铁调素是一种肽激素,通常以20或25个氨基酸组成的两种形式存在,其由许多细胞应答铁负荷和炎症时表达和分泌。铁调素主要在肝的肝细胞中产生,在铁稳态的调节中起中心作用,充当抗微生物肽,并且直接或间接地参与大多数缺铁/铁超负荷综合征的发展。铁调素的主要作用是内化并降解铁输出蛋白铁转运蛋白,其在所有铁输出细胞上表达。铁调素直接结合铁转运蛋白。因此,高铁调素水平导致肠铁吸收以及铁从巨噬细胞和肝细胞释放的抑制,而低浓度的铁调素导致铁从这些细胞释放加速。
[0161]
对铁调素特异性的脂质运载蛋白突变蛋白公开于国际专利公开wo2012/022742和wo2013/087654中。
[0162]
本公开的铁调素特异性脂质运载蛋白突变蛋白可以是hngal的突变蛋白。与成熟hngal的线性多肽序列(seq id no:2)相比,这样的突变蛋白可在成熟hngal的相应序列位置处包含以下氨基酸残基组之一:
[0163]
(a)ala 36,ser 40,leu 41,met 49,asn 70,gly 72,gly 73,ser 77,leu 79,leu 125,val132;
[0164]
(b)leu 36,arg 40,val 41,gln 49,asp 70,arg 72,thr 73,leu 77,ser 79,thr 125,val 132;
[0165]
(c)leu 36,glu 40,ile 41,leu 49,gln 70,gly 72,glu 73,gly 77,gly 79,phe 125,val 132;
[0166]
(d)leu 36,glu 40,ile 41,met 49,met 70,leu 72,ala 73,glu 77,leu 79,val 125,val 132;
[0167]
(e)leu 36,glu 40,val 41,met 49,met 70,leu 72,ala 73,glu 77,leu 79,thr 125,val 132;
[0168]
(f)leu 36,glu 40,val 41,met 49,met 70,leu 72,ala 73,glu 77,leu 79,val 125,val 132;
[0169]
(g)thr 36,ser 40,ile 41,gln 49,phe 70,glu 72,gly 73,arg 77,val 79,val 125,leu 132;
[0170]
(h)val 36、glu 40、met 41、leu 49、met 70、glu 72、tyr 73、val 77、leu 79、arg 125、val 132;
[0171]
(i)val 36、gly 40、leu 41、leu 49、leu 70、val 72、arg 73、arg 77、tyr 79、met 125、val 132;
[0172]
(j)leu 36,glu 40,val 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,asp 96,ser 100,arg 103,gly 106,thr 125,trp 127,val 132,trp 134;
[0173]
(k)leu 36,glu 40,val 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,gly 96,gly 100,arg 103,gly 106,val 125,trp 127,val 132,和trp 134;
[0174]
(1)leu 36,glu 40,val 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,asp 96,ser 100,arg 103,gly 106,val 125,trp 127,val 132,trp 134;
[0175]
(m)leu 36,glu 40,ile 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,asp 96,ser 100,arg 103,gly 106,val 125,trp 127,val 132,trp 134;
[0176]
(n)leu 36,glu 40,ile 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,asp 96,ser 100,arg 103,gly 106,val 125,trp 127,val 132,trp 134;
[0177]
(o)leu 36,glu 40,val 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,asp 96,ser 100,arg 103,gly 106,val 125,trp 127,val 132,trp 134;
[0178]
(p)leu 36,glu 40,val 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,gly 96,gly 100,arg 103,gly 106,val 125,trp 127,val 132,trp 134;
[0179]
(q)leu 36,glu 40,val 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,asp 96,ser 100,arg 103,gly 106,thr 125,trp 127,val 132,trp 134;或
[0180]
(r)leu 36,glu 40,val 41,met 49,trp 52,ile 68,met 70,leu 72,ala 73,glu 77,leu 79,gln 81,asp 96,ser 100,arg 103,gly 106,val 125,trp 127,val 132,trp 134。
[0181]
本公开的铁调素特异性脂质运载蛋白突变蛋白可包含选自seq id nos:52-65的氨基酸序列或其片段或变体。本公开的铁调素特异性脂质运载蛋白突变蛋白可与seq id nos:52-65中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0182]
4.对pcsk9特异性的脂质运载蛋白突变蛋白
[0183]
人前蛋白转化酶枯草杆菌蛋白酶/kexin 9型(pcsk9)是主要在肾、肝和肠中表达的分泌的蛋白。它具有三个结构域:抑制性前-结构域(氨基酸1-152;包括在氨基酸1-30处的信号序列)、丝氨酸蛋白酶结构域(或催化结构域;在氨基酸153-448处)和c-端结构域(或富含半胱氨酸/组氨酸的结构域)。pcsk9被合成为在内质网中在前结构域和催化结构域之间经历自催化切割的酶原。切割后,前-结构域保持与成熟蛋白结合,并且该复合物被分泌。富含半胱氨酸的结构域可以起到类似于其它弗林蛋白酶/kexin/枯草杆菌蛋白酶样丝氨酸蛋白酶的p-(加工)结构域的作用,其似乎是活化的蛋白酶的折叠和调节所必需的。
[0184]
pcsk9是丝氨酸蛋白酶的蛋白酶k分泌枯草杆菌蛋白酶样亚家族的成员(naureckiene等,arch biochem biophys,2003),并且用作肝低密度脂蛋白受体(ldl-r)的强负调节剂。pcsk9通过控制在血流中循环的低密度脂蛋白(ldl)颗粒的水平在胆固醇代谢中起关键作用。升高的pcsk9水平已显示降低肝脏中的ldl-r水平,从而导致血浆中高水平的低密度脂蛋白胆固醇(ldl-c)和对冠状动脉疾病的易感性增加(peterson等人,j lipid res,2008)。
[0185]
对pcsk9特异性的脂质运载蛋白突变蛋白公开于国际专利公开wo2014/140210中。
[0186]
本公开的pcsk9特异性脂质运载蛋白突变蛋白可以是人泪脂质运载蛋白的突变蛋白。与成熟人泪脂质运载蛋白的线性多肽序列(seq id no:1)相比,这样的突变蛋白可以在成熟人泪脂质运载蛋白的相应序列位置处包含以下残基组之一:
[0187]
(a)glu 27
→
ser,phe 28
→
arg,pro 29
→
gly,glu 30
→
asp,met 31
→
ala,leu 33
→
trp,ile 57
→
tyr,asp 80
→
met,glu 104
→
pro,leu 105
→
tyr,his 106
→
gln,lys 108
→
ala;
[0188]
(b)glu 27
→
gln,phe 28
→
cys,pro 29
→
asp,glu 30
→
thr,met 31
→
gly,leu 33
→
trp,ile 57
→
tyr,leu 105
→
cys,his 106
→
gly,lys 108
→
trp;
[0189]
(c)glu 27
→
glu,phe 28
→
trp,pro 29
→
asn,glu 30
→
gly,met 31
→
his,leu 33
→
tyr,ile 57
→
tyr,asp 80
→
pro,glu 104
→
ser,leu 105
→
trp,his 106
→
pro,lys 108
→
tyr;
[0190]
(d)glu 27
→
thr,phe 28
→
asp,pro 29
→
asn,glu 30
→
ser,met 31
→
pro,leu 33
→
phe,ile 57
→
tyr,asp 80
→
ile,glu 104
→
ala,leu 105
→
glu,his 106
→
arg,lys 108
→
arg;
[0191]
(e)glu 27
→
phe,phe 28
→
lys,pro 29
→
ile,glu 30
→
ala,met 31
→
ser,leu 33
→
pro,ile 57
→
trp,asp 80
→
gln,glu 104
→
asn,leu 105
→
arg,his 106
→
gln,lys 108
→
asp;
[0192]
(f)glu 27
→
lys,phe 28
→
gly,pro 29
→
pro,glu 30
→
thr,met 31
→
pro,leu 33
→
trp,ile 57
→
his,asp 80
→
tyr,glu 104
→
ala,leu 105
→
ser,his 106
→
val,lys 108
→
asn;
[0193]
(g)glu 27
→
glu,phe 28
→
his,pro 29
→
leu,glu 30
→
ala,met 31
→
asp,leu 33
→
ala,ile 57
→
gln,asp 80
→
ile,glu 104
→
ala,leu 105
→
tyr,his 106
→
pro,lys 108
→
ser;
[0194]
(h)glu 27
→
ala,phe 28
→
asp,pro 29
→
met,glu 30
→
gly,met 31
→
asp,leu 33
→
pro,ile 57
→
thr,asp 80
→
thr,glu 104
→
thr,his 106
→
thr,lys 108
→
arg;
[0195]
(i)glu 27
→
arg,phe 28
→
leu,pro 29
→
asp,glu 30
→
asn,met 31
→
glu,leu 33
→
trp,ile 57
→
tyr,asp 80
→
gln,glu 104
→
pro,leu 105
→
arg,his 106
→
asn,lys 108
→
ala;
[0196]
(j)glu 27
→
lys,phe 28
→
asn,pro 29
→
met,glu 30
→
gly,met 31
→
gln,leu 33
→
pro,ile 57
→
arg,asp 80
→
ile,glu 104
→
asp,leu 105
→
arg,his 106
→
leu,lys 108
→
thr;
[0197]
(k)glu 27
→
ser,phe 28
→
arg,pro 29
→
gly,glu 30
→
asp,met 31
→
ala,leu 33
→
trp,ile 57
→
tyr,asp 80
→
met,glu 104
→
pro,leu 105
→
gly,his 106
→
gln,lys 108
→
ala;
[0198]
(1)arg 26
→
phe,glu 27
→
ser,phe 28
→
arg,pro 29
→
gly,glu 30
→
asp,met 31
→
ala,asn 32
→
ile,leu 33
→
trp,glu 34
→
thr,leu 56
→
met,ile 57
→
tyr,ser 58
→
ala,lys 83
→
ser,glu 104
→
pro和lys 108
→
thr;
[0199]
(m)thr 43
→
ile或ala,glu 45
→
gly,asn 48
→
gly,glu 63
→
gly,ala 66
→
val,
glu 69
→
val,lys 70
→
arg,ala 79
→
thr、met或val,asp 80
→
met或ser,gly 82
→
ser,his 84
→
gln,val 85
→
gly,tyr 87
→
ser,ile 88
→
thr或leu,his 92
→
pro,leu 105
→
his、gly或tyr和his 106
→
gln或arg;
[0200]
(n)glu 27
→
phe,phe 28
→
lys,pro 29
→
ile,asn 32
→
trp,leu 33
→
pro,glu 34
→
arg,leu 56
→
asn,ile 57
→
trp,his 106
→
gln和lys 108
→
glu;或
[0201]
(o)glu 43
→
gly或ala,glu 45
→
gly,ser 58
→
trp或arg,glu 63
→
asp,glu 69
→
gly,lys 70
→
arg,asp 80
→
gln、val或thr,gly 82
→
asp,lys 83
→
ser或arg,ala 86
→
glu或ser,phe 99
→
leu,glu 102
→
lys或val,glu 104
→
asn或lys以及pro 106
→
thr。
[0202]
本公开的pcsk9特异性脂质运载蛋白突变蛋白可包含选自seq id nos:66-91的氨基酸序列或其片段或变体。本公开的pcsk9特异性脂质运载蛋白突变蛋白可与seq id nos:66-91中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0203]
5.对绿脓杆菌荧光素(pyoverdine)和绿脓杆菌螯铁蛋白(pyochelin)特异性的脂质运载蛋白突变蛋白
[0204]
绿脓杆菌荧光素(pvd)是肽连接的异羟肟酸和儿茶酚酸盐型配体,绿脓杆菌螯铁蛋白(pch)是水杨酸盐和两分子半胱氨酸的衍生结合物并具有酚、羧酸盐和胺配体官能度。pvd和pch都在铜绿假单胞菌(p.aeruginosa)毒性中发挥作用,并具有一些协同作用的指征——通过使用分泌的铁结合铁载体绿脓杆菌荧光素和绿脓杆菌螯铁蛋白,铜绿假单胞菌能够从宿主环境中清除铁。不能产生任一铁载体的双缺陷突变体比不能仅产生两个铁载体之一的单缺陷突变体在毒力上减弱得多(takase等人,infect immun,2000)。此外,绿脓杆菌荧光素作为信号传导分子发挥作用控制几种毒力因子以及绿脓杆菌螯铁蛋白本身的产生;而已经提出,除了三价铁,绿脓杆菌螯铁蛋白可作为用于获得铜绿假单胞菌致病性的二价金属诸如亚铁和锌的系统的一部分(visca等,appl environ microbiol,1992)。
[0205]
已从几种铜绿假单胞菌菌株中鉴定出三种结构不同的绿脓杆菌荧光素类型或组:来自铜绿假单胞菌atcc 15692(g.等,liebigs ann chem,1989),来自铜绿假单胞菌atcc 27853(tappe等,j prakt chem,1993)和来自天然分离物铜绿假单胞菌r(gipp等,naturforsch,1991)。此外,根据参照菌株,对88个临床分离物和上述两种收集菌株的比较生物学研究揭示了三种不同的菌株特异性绿脓杆菌荧光素介导的铁摄取系统(meyer等,microbiology,1997;comclis等,infect immun,1989):铜绿假单胞菌atcc 15692(i型pvd或pvd i)、铜绿假单胞菌atcc 27853(ii型pvd或pvd ii)和临床分离物铜绿假单胞菌r和pa6(iii型pvd或pvd iii)。
[0206]
对pvd i型、pvd ii型、pvd iii型和pch特异性的脂质运载蛋白突变蛋白公开于国际专利公开wo2016/131804中。
[0207]
本公开的pvd i型特异性脂质运载蛋白突变蛋白可以是hngal的突变蛋白。与成熟hngal的线性多肽序列(seq id no:2)相比,这样的突变蛋白可包含以下突变的氨基酸残基的组之一:
[0208]
(a)gln 28
→
his;leu 36
→
asn;ala 40
→
gly;ile 41
→
trp;gln 49
→
ile;tyr 52
→
met;ser 68
→
val;leu 70
→
gln;arg 72
→
trp;lys 73
→
asp;asp 77
→
leu;trp 79
→
gln;arg 81
→
gln;cys 87
→
ser;asn 96
→
his;tyr 100
→
lys;leu 103
→
his;tyr 106
→
his;lys 125
→
arg;ser127
→
trp;tyr 132
→
trp;lys 134
→
asp;
[0209]
(b)gln 28
→
his;leu 36
→
thr;ala 40
→
gly;ile 41
→
phe;gln 49
→
leu;tyr 52
→
trp;leu 70
→
trp;arg 72
→
ala;lys 73
→
leu;asp 77
→
tyr;trp 79
→
asp;arg81
→
gly;cys 87
→
ser;asn 96
→
ile;tyr 100
→
glu;leu 103
→
his;tyr 106
→
gln;lys 125
→
trp;ser 127
→
asn;tyr 132
→
asn;lys 134
→
gln;
[0210]
(c)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
thr;gln 49
→
pro;tyr 52
→
pro;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
glu;asp 77
→
ser;trp 79
→
ser;arg 81
→
ile;cys 87
→
ser;asn 96
→
gly;tyr 100
→
asn;leu 103
→
lys;tyr 106
→
his;lys 125
→
tyr;ser 127
→
ala;tyr 132
→
gly;lys 134
→
asn;
[0211]
(d)gln 28
→
his;leu 36
→
phe;ala 40
→
asn;ile 41
→
arg;gln 49
→
pro;tyr 52
→
met;ser 68
→
asp;leu 70
→
thr;arg 72
→
glu;lys 73
→
ala;asp 77
→
arg;trp79
→
arg;arg 81
→
ile;cys 87
→
ser;asn 96
→
tyr;tyr 100
→
lys;leu 103
→
pro;tyr 106
→
phe;lys 125
→
ser;ser 127
→
thr;tyr 132
→
trp;lys 134
→
gly;
[0212]
(e)gln 28
→
his;ala 40
→
gly;ile 41
→
trp;gln 49
→
val;tyr 52
→
met;ser 68
→
val;leu 70
→
asp;arg 72
→
glu;lys 73
→
leu;asp 77
→
arg;trp 79
→
met;arg 81
→
glu;cys 87
→
ser;asn 96
→
asp;tyr 100
→
phe;leu 103
→
trp;tyr 106
→
gln;lys 125
→
gly;ser 127
→
tyr;tyr 132
→
trp;lys 134
→
his;
[0213]
(f)gln 28
→
his;leu 36
→
val;ala 40
→
phe;ile 41
→
phe;gln 49
→
ala;tyr 52
→
pro;ser 68
→
glu;leu 70
→
trp;arg 72
→
leu;lys 73
→
asn;asp 77
→
gln;trp 79
→
glu;arg 81
→
his;cys 87
→
ser;asn 96
→
tyr;leu 103
→
tyr;tyr 106
→
his;lys 125
→
val;ser 127
→
his;tyr 132
→
lys;lys 134
→
trp;
[0214]
(g)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
thr;gln 49
→
pro;tyr 52
→
pro;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
glu;asp 77
→
ser;trp 79
→
ser;ile 80
→
thr;arg 81
→
ile;cys 87
→
ser;asn 96
→
gly;tyr 100
→
ser;leu 103
→
gln;tyr 106
→
his;lys 125
→
tyr;ser 127
→
ile;tyr 132
→
gly;lys 134
→
asn;
[0215]
(h)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
thr;gln 49
→
pro;tyr 52
→
pro;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
asp;asp 77
→
ser;trp 79
→
ser;arg 81
→
ile;cys 87
→
ser;asn 96
→
gly;tyr 100
→
asn;leu 103
→
asp;tyr 106
→
his;lys 125
→
tyr;ser 127
→
val;tyr 132
→
gly;lys 134
→
asn;
[0216]
(i)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
thr;gln 49
→
pro;tyr 52
→
pro;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
glu;asp 77
→
thr;trp 79
→
ser;arg 81
→
ile;cys 87
→
ser;asn 96
→
asp;tyr 100
→
asn;leu 103
→
glu;tyr 106
→
his;lys 125
→
tyr;ser 127
→
asp;tyr 132
→
gly;lys 134
→
asn;
[0217]
(j)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
thr;gln 49
→
pro;tyr 52
→
pro;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
asp;asp 77
→
val;trp 79
→
ser;arg 81
→
ile;cys 87
→
ser;asn 96
→
gly;tyr 100
→
asn;leu 103
→
asn;tyr 106
→
his;lys 125
→
tyr;ser 127
→
via;tyr 132
→
gly;lys 134
→
asn;
[0218]
(k)gln 28
→
his;ala 40
→
gly;ile 41
→
trp;gln 49
→
leu;tyr 52
→
met;ser 68
→
val;leu 70
→
asp;arg 72
→
glu;lys 73
→
leu;asp 77
→
arg;trp 79
→
met;arg 81
→
glu;cys 87
→
ser;asn 96
→
asp;tyr 100
→
ser;leu 103
→
trp;tyr 106
→
gln;lys 125
→
gly;ser 127
→
tyr;tyr 132
→
trp;lys 134
→
his;
[0219]
(l)gln 28
→
his;leu 36
→
trp;ala 40
→
thr;ile 41
→
thr;gln 49
→
pro;tyr 52
→
pro;thr 54
→
val;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
glu;lys 75
→
glu;asp 77
→
ser;trp 79
→
ser;ile 80
→
thr;arg 81
→
ile;cys 87
→
ser;asn 96
→
gly;tyr 100
→
ser;leu 103
→
gln;tyr 106
→
his;lys 125
→
tyr;ser 127
→
thr;tyr 132
→
gly;lys 134
→
asn;
[0220]
(m)gln 28
→
his;ala 40
→
gly;ile 41
→
trp;lys 46
→
glu;gln 49
→
leu;tyr 52
→
met;thr 54
→
ala;ile 55
→
via;lys 59
→
arg;ser 68
→
val;leu 70
→
asp;arg 72
→
glu;lys 73
→
leu;lys 74
→
glu;lys 75
→
glu;asp 77
→
arg;trp 79
→
met;ile 80
→
thr;arg 81
→
glu;ser 87
→
asn;asn 96
→
asp;tyr 100
→
ser;leu 103
→
trp;tyr 106
→
gln;lys 125
→
gly;ser 127
→
tyr;tyr 132
→
trp;lys 134
→
his;
[0221]
(n)leu 36
→
trp;asn 39
→
asp;ala 40
→
thr;ile 41
→
thr;gln 49
→
pro;tyr 52
→
pro;thr 54
→
val;asn 65
→
asp;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
glu;lys 75
→
glu;asp 77
→
ser;trp 79
→
ser;ile 80
→
thr;arg 81
→
ile;cys 87
→
ser;asn 96
→
gly;tyr 100
→
ser;leu 103
→
gln;tyr 106
→
his;lys 125
→
tyr;ser 127
→
thr;tyr 132
→
gly;lys 134
→
asn;thr 136
→
ala;
[0222]
(o)leu 36
→
trp;ala 40
→
thr;ile 41
→
ala;gln 49
→
pro;tyr 52
→
pro;thr 54
→
val;asn 65
→
asp;ser 68
→
asp;leu 70
→
gln;arg 72
→
ser;lys 73
→
glu;lys 75
→
glu;asp 77
→
ser;trp 79
→
ser;ile 80
→
thr;arg 81
→
ile;cys 87
→
ser;asn 96
→
gly;tyr 100
→
ser;leu 103
→
gln;tyr 106
→
his;lys 125
→
tyr;ser 127
→
thr;tyr 132
→
gly;lys 134
→
asn;thr 136
→
ala;
[0223]
(p)gln 28
→
his;ala 40
→
gly;ile 41
→
trp;lys 46
→
glu;gln 49
→
leu;tyr 52
→
met;thr 54
→
ala;ile 55
→
via;lys 59
→
arg;asn 65
→
asp;ser 68
→
val;leu 70
→
asp;arg 72
→
glu;lys 73
→
leu;lys 74
→
glu;lys 75
→
glu;asp 77
→
arg;trp 79
→
met;ile 80
→
thr;arg 81
→
glu;ser 87
→
asn;asn 96
→
asp;tyr 100
→
ser;leu 103
→
trp;tyr 106
→
gln;lys 125
→
gly;ser 127
→
tyr;tyr 132
→
trp;lys 134
→
his;或
[0224]
(q)gln 28
→
his;ala 40
→
gly;ile 41
→
trp;lys 46
→
glu;gln 49
→
leu;tyr 52
→
met;thr 54
→
ala;ile 55
→
val;lys 59
→
arg;asn 65
→
gln;ser 68
→
val;leu 70
→
asp;arg 72
→
glu;lys 73
→
leu;lys 74
→
glu;lys 75
→
glu;asp 77
→
arg;trp 79
→
met;ile 80
→
thr;arg 81
→
glu;ser 87
→
asn;asn 96
→
asp;tyr 100
→
ser;leu 103
→
trp;tyr 106
→
gln;lys 125
→
gly;ser 127
→
tyr;tyr 132
→
trp;lys 134
→
his。
[0225]
本公开的pvd ii型特异性脂质运载蛋白突变蛋白可以是hngal的突变蛋白。与成熟hngal的线性多肽序列(seq id no:2)相比,这样的突变蛋白可包含以下突变的氨基酸残基的组之一:
[0226]
(a)gln 28
→
his;leu 36
→
val;ala 40
→
glu;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;ser 68
→
glu;leu 70
→
arg;arg 72
→
his;lys 73
→
asn;asp 77
→
asn;trp 79
→
ser;arg 81
→
glu;cys 87
→
ser;tyr 100
→
asn;leu 103
→
gln;tyr 106
→
met;ser 127
→
lys;tyr 132
→
gly;lys 134
→
trp;
[0227]
(b)gln 28
→
his;ala 40
→
thr;ile 41
→
ile;gln 49
→
gly;tyr 52
→
asn;ser 68
→
asp;leu 70
→
arg;arg 72
→
ile;lys 73
→
met;asp 77
→
his;trp 79
→
tyr;arg 81
→
glu;cys 87
→
ser;asn 96
→
ile;tyr 100
→
asn;leu 103
→
thr;tyr 106
→
gln;lys 125
→
ile;ser 127
→
arg;tyr 132
→
met;lys 134
→
trp;
[0228]
(c)gln 28
→
his;leu 36
→
ile;ala 40
→
thr;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;ser 68
→
glu;leu 70
→
arg;arg 72
→
ala;lys 73
→
pro;asp 77
→
ile;trp 79
→
ser;arg 81
→
ser;cys 87
→
ser;asn 96
→
met;tyr 100
→
ser;leu 103
→
gly;tyr 106
→
ala;lys 125
→
lys;tyr 132
→
val;lys 134
→
trp;
[0229]
(d)gln 28
→
his;ala 40
→
asn;gln 49
→
ala;tyr 52
→
pro;ser 68
→
glu;leu 70
→
arg;arg 72
→
ser;lys 73
→
gln;asp 77
→
met;trp 79
→
ala;arg 81
→
tyr;cys 87
→
ser;asn 96
→
arg;tyr 100
→
pro;leu 103
→
thr;tyr 106
→
ile;lys 125
→
lys;ser 127
→
met;tyr 132
→
phe;lys 134
→
trp;
[0230]
(e)gln 28
→
his;ala 40
→
his;gln 49
→
ala;tyr 52
→
pro;ser 68
→
glu;leu 70
→
asp;arg 72
→
gly;lys 73
→
arg;asp 77
→
his;trp 79
→
trp;arg 81
→
glu;cys 87
→
ser;asn 96
→
arg;tyr 100
→
asp;leu 103
→
met;tyr 106
→
phe;lys 125
→
ala;ser 127
→
asp;tyr 132
→
asn;lys 134
→
trp;
[0231]
(f)gln 28
→
his;leu 36
→
asn;ala 40
→
gly;ile 41
→
arg;gln 49
→
pro;tyr 52
→
trp;ser 68
→
arg;leu 70
→
trp;arg 72
→
asn;lys 73
→
gln;asp 77
→
lys;trp 79
→
asp;arg 81
→
glu;cys 87
→
ser;asn 96
→
asp;tyr 100
→
thr;leu 103
→
trp;tyr 106
→
asn;lys 125
→
asn;ser 127
→
met;tyr132
→
ile;lys 134
→
tyr;
[0232]
(g)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
thr;gln 49
→
gly;tyr 52
→
gly;ser 68
→
glu;leu 70
→
arg;arg 72
→
gly;lys 73
→
arg;asp 77
→
gly;trp 79
→
trp;arg 81
→
glu;cys 87
→
ser;asn 96
→
ala;tyr 100
→
trp;leu 103
→
ile;tyr 106
→
gly;lys 125
→
lys;ser 127
→
asn;tyr 132
→
val;lys 134
→
trp;
[0233]
(h)gln 28
→
his;leu 36
→
val;ala 40
→
glu;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;ser 68
→
glu;leu 70
→
arg;arg 72
→
his;lys 73
→
asn;asp 77
→
asn;trp 79
→
ser;arg 81
→
glu;cys 87
→
ser;asn 96
→
lys;tyr 100
→
asn;leu 103
→
val;tyr 106
→
met;lys 125
→
asn;ser 127
→
lys;tyr 132
→
gly;lys 134
→
trp;
[0234]
(i)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;ser 68
→
glu;leu 70
→
arg;arg 72
→
his;lys 73
→
asn;asp 77
→
asn;trp 79
→
ser;arg 81
→
glu;cys 87
→
ser;leu 103
→
gln;tyr 106
→
met;ser 127
→
lys;tyr 132
→
val;lys 134
→
trp;
[0235]
(j)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;ser 68
→
glu;leu 70
→
arg;arg 72
→
his;asp 77
→
asn;trp 79
→
phe;arg 81
→
glu;cys 87
→
ser;asn 96
→
lys;tyr 100
→
his;leu 103
→
gln;tyr 106
→
met;ser 127
→
lys;tyr 132
→
ala;lys 134
→
trp;
[0236]
(k)gln 28
→
his;leu 36
→
val;ala 40
→
gly;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;ser 68
→
glu;leu 70
→
arg;arg 72
→
his;lys 73
→
asn;asp 77
→
asn;trp79
→
trp;arg 81
→
glu;cys 87
→
ser;tyr 100
→
asn;leu 103
→
his;tyr 106
→
met;ser 127
→
lys;
tyr 132
→
gly;lys 134
→
trp;
[0237]
(l)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
ile;gln 49
→
gly;tyr 52
→
asn;ser 68
→
asp;leu 70
→
arg;arg 72
→
ile;lys 73
→
phe;asp 77
→
his;trp 79
→
tyr;arg 81
→
asp;cys 87
→
ser;leu 103
→
met;tyr 106
→
gln;lys 125
→
ile;ser 127
→
arg;tyr 132
→
ile;lys 134
→
trp;
[0238]
(m)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
ile;gln 49
→
gly;tyr 52
→
asn;ser 68
→
asp;leu 70
→
arg;arg 72
→
ile;lys 73
→
arg;asp 77
→
his;trp 79
→
tyr;arg 81
→
asp;cys 87
→
ser;leu 103
→
thr;tyr 106
→
gln;lys 125
→
ile;ser 127
→
arg;tyr 132
→
ile;lys 134
→
trp;
[0239]
(n)gln 28
→
his;leu 36
→
val;ala 40
→
glu;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;asn 65
→
asp;ser 68
→
glu;leu 70
→
arg;arg 72
→
his;lys 73
→
asn;asp 77
→
asn;trp 79
→
phe;arg 81
→
glu;cys 87
→
ser;asn 96
→
lys;tyr 100
→
asn;leu 103
→
val;tyr 106
→
met;lys 125
→
asn;ser 127
→
lys;tyr 132
→
gly;lys 134
→
trp;
[0240]
(o)gln 28
→
his;leu 36
→
val;ala 40
→
glu;ile 41
→
val;gln 49
→
gly;tyr 52
→
pro;asn 65
→
gln;ser 68
→
glu;leu 70
→
arg;arg 72
→
his;lys 73
→
asn;asp 77
→
asn;trp 79
→
phe;arg 81
→
glu;cys 87
→
ser;asn 96
→
lys;tyr 100
→
asn;leu 103
→
val;tyr 106
→
met;lys 125
→
asn;ser 127
→
lys;tyr 132
→
gly;lys 134
→
trp;
[0241]
(p)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
ile;gln 49
→
gly;tyr 52
→
asn;thr 54
→
ala;asn 65
→
asp;ser 68
→
asp;leu 70
→
arg;arg 72
→
ile;lys 73
→
arg;asp 77
→
his;trp 79
→
tyr;arg 81
→
asp;cys 87
→
ser;leu 103
→
thr;tyr 106
→
gln;lys 125
→
ile;ser 127
→
arg;tyr 132
→
ile;lys 134
→
trp;
[0242]
(q)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
ile;gln 49
→
gly;tyr 52
→
asn;thr 54
→
ala;asn 65
→
gln;ser 68
→
asp;leu 70
→
arg;arg 72
→
ile;lys 73
→
arg;asp 77
→
his;trp 79
→
tyr;arg 81
→
asp;cys 87
→
ser;leu 103
→
thr;tyr 106
→
gln;lys 125
→
ile;ser 127
→
arg;tyr 132
→
ile;lys 134
→
trp;
[0243]
(r)leu 36
→
val;ala 40
→
thr;ile 41
→
ile;gln 49
→
gly;tyr 52
→
asn;thr 54
→
ala;asn 65
→
asp;ser 68
→
asp;leu 70
→
arg;arg 72
→
ile;lys 73
→
arg;asp 77
→
his;trp 79
→
tyr;arg 81
→
asp;cys 87
→
ser;leu 103
→
thr;tyr 106
→
gln;lys 125
→
ile;ser 127
→
arg;tyr 132
→
ile;lys 134
→
trp;或
[0244]
(s)gln 28
→
his;leu 36
→
val;ala 40
→
thr;ile 41
→
ile;gln 49
→
gly;tyr 52
→
asn;asn 65
→
gln;ser 68
→
asp;leu 70
→
arg;arg 72
→
ile;lys 73
→
arg;asp 77
→
his;trp 79
→
tyr;arg 81
→
asp;cys 87
→
ser;leu 103
→
thr;tyr 106
→
gln;lys 125
→
ile;ser 127
→
arg;tyr 132
→
ile;lys 134
→
trp。
[0245]
本公开的pvd iii型特异性脂质运载蛋白突变蛋白可以是hngal的突变蛋白。与成熟hngal的线性多肽序列(seq id no:2)相比,这样的突变蛋白可包含以下突变的氨基酸残基的组之一:
[0246]
(a)gln 28
→
his;leu 36
→
phe;ala 40
→
trp;ile 41
→
met;gln 49
→
his;tyr 52
→
asn;ser 68
→
glu;leu 70
→
lys;arg 72
→
gln;lys 73
→
ala;asp 77
→
ile;trp 79
→
ser;arg 81
→
his;cys 87
→
ser;asn 96
→
ile;tyr 100
→
asn;leu 103
→
gly;tyr 106
→
glu;lys 125
→
trp;ser 127
→
his;tyr 132
→
phe;lys 134
→
gln;
[0247]
(b)gln 28
→
his;leu 36
→
phe;ala 40
→
arg;ile 41
→
trp;gln 49
→
ile;tyr 52
→
tyr;ser 68
→
gln;leu 70
→
asn;arg 72
→
trp;lys 73
→
leu;asp 77
→
ala;trp 79
→
ser;arg 81
→
ser;cys 87
→
ser;asn 96
→
arg;tyr 100
→
ile;leu 103
→
pro;tyr 106
→
glu;lys 125
→
thr;ser 127
→
ile;tyr 132
→
phe;lys 134
→
glu;
[0248]
(c)gln 28
→
his;leu 36
→
phe;ala 40
→
leu;ile 41
→
leu;gln 49
→
arg;tyr 52
→
arg;ser 68
→
asp;leu 70
→
arg;arg 72
→
leu;lys 73
→
tyr;asp 77
→
ile;trp 79
→
ser;arg 81
→
ala;cys 87
→
ser;asn 96
→
gly;tyr 100
→
ala;leu 103
→
phe;tyr 106
→
glu;lys 125
→
trp;ser 127
→
ala;lys 134
→
glu;
[0249]
(d)gln 28
→
his;leu 36
→
phe;ala 40
→
trp;ile 41
→
arg;gln 49
→
pro;tyr 52
→
ser;ser 68
→
asn;leu 70
→
arg;arg 72
→
trp;lys 73
→
pro;asp 77
→
arg;trp 79
→
ser;arg 81
→
ser;cys 87
→
ser;asn 96
→
met;tyr 100
→
pro;leu 103
→
gly;tyr 106
→
glu;lys 125
→
trp;ser 127
→
phe;tyr 132
→
phe;lys 134
→
glu;
[0250]
(e)gln 28
→
his;leu 36
→
phe;ala 40
→
trp;ile 41
→
arg;gln 49
→
pro;tyr 52
→
ser;ser 68
→
asn;leu 70
→
arg;arg 72
→
trp;lys 73
→
pro;asp 77
→
arg;trp 79
→
ser;arg 81
→
ser;cys 87
→
ser;asn 96
→
met;tyr 100
→
pro;leu 103
→
gly;tyr 106
→
glu;lys 125
→
trp;ser 127
→
phe;tyr 132
→
phe;lys 134
→
glu;
[0251]
(f)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;gln 49
→
lys;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
gln;trp 79
→
asp;arg 81
→
ala;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0252]
(g)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;gln 49
→
met;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
gln;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0253]
(h)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
thr;gln 49
→
met;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
arg;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
val;tyr 100
→
asp;leu 103
→
gln;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0254]
(i)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;gln 49
→
met;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0255]
(j)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;gln 49
→
lys;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
tyr;asp 77
→
gln;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→‑
;tyr 100
→
glu;leu 103
→
gln;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0256]
(k)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;leu 42
→
arg;gln 49
→
met;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;ser 105
→
pro;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0257]
(l)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;asp 47
→
asn;gln 49
→
met;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;ser 105
→
pro;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;thr 145
→
pro;
[0258]
(m)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;asp 45
→
gly;lys 46
→
arg;gln 49
→
met;tyr 52
→
met;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;ser 105
→
pro;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0259]
(n)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;leu 42
→
arg;gln 49
→
met;tyr 52
→
met;asn 65
→
asp;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;ser 105
→
pro;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;
[0260]
(o)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;asp 47
→
asn;gln 49
→
met;tyr 52
→
met;asn 65
→
asp;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;ser 105
→
pro;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;thr 145
→
pro;
[0261]
(p)gln 28
→
his;leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;asp 45
→
gly;lys 46
→
arg;gln 49
→
met;tyr 52
→
met;asn 65
→
asp;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;ser 105
→
pro;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp;或
[0262]
(q)leu 36
→
glu;ala 40
→
leu;ile 41
→
ala;leu 42
→
arg;gln 49
→
met;tyr 52
→
met;asn 65
→
asp;ser 68
→
glu;leu 70
→
arg;lys 73
→
his;asp 77
→
lys;trp 79
→
asp;arg 81
→
val;cys 87
→
ser;asn 96
→
leu;tyr 100
→
asp;leu 103
→
gln;ser 105
→
pro;tyr 106
→
glu;ser 127
→
val;tyr 132
→
phe;lys 134
→
trp。
[0263]
本公开的pch特异性脂质运载蛋白突变蛋白可以是hngal的突变蛋白。与成熟hngal的线性多肽序列(seq id no:2)相比,这样的突变蛋白可包含以下突变的氨基酸残基的组之一:
[0264]
(a)gln 28
→
his;ala 40
→
ile;ile 41
→
leu;gln 49
→
his;tyr 52
→
leu;ser 68
→
his;leu 70
→
thr;arg 72
→
lys;lys 73
→
trp;asp 77
→
ile;trp 79
→
ser;arg 81
→
his;cys 87
→
ser;asn 96
→
met;tyr 100
→
asn;leu 103
→
his;tyr 106
→
met;lys 125
→
trp;ser 127
→
asp;tyr 132
→
glu;lys 134
→
leu;
[0265]
(b)gln 28
→
his;leu 36
→
his;ala 40
→
gln;ile 41
→
trp;gln 49
→
arg;tyr 52
→
trp;ser 68
→
asp;leu 70
→
asp;arg 72
→
ala;lys 73
→
ile;asp 77
→
his;trp 79
→
arg;arg 81
→
thr;cys 87
→
ser;tyr 100
→
his;leu 103
→
gly;tyr 106
→
gly;lys 125
→
phe;ser 127
→
ile;tyr 132
→
ala;lys 134
→
phe;
[0266]
(c)gln 28
→
his;leu 36
→
met;ala 40
→
phe;ile 41
→
his;gln 49
→
ser;tyr 52
→
pro;ser 68
→
his;leu 70
→
pro;arg 72
→
trp;lys 73
→
ala;asp 77
→
ala;trp 79
→
lys;arg 81
→
ile;cys 87
→
ser;asn 96
→
ala;tyr 100
→
gly;leu 103
→
met;tyr 106
→
trp;lys 125
→
gly;ser 127
→
trp;tyr 132
→
thru;lys 134
→
val;
[0267]
(d)gln 28
→
his;leu 36
→
val;ala 40
→
tyr;ile 41
→
trp;gln 49
→
ala;ser 68
→
asp;leu 70
→
arg;arg 72
→
trp;lys 73
→
arg;asp 77
→
arg;trp 79
→
asp;arg 81
→
trp;cys 87
→
ser;asn 96
→
pro;tyr 100
→
glu;leu 103
→
gln;tyr 106
→
arg;lys 125
→
leu;ser 127
→
arg;tyr 132
→
ala;lys 134
→
asn;
[0268]
(e)gln 28
→
his;val 34
→
leu;leu 36
→
met;ala 40
→
phe;ile 41
→
his;gln 49
→
ser;tyr 52
→
pro;ser 68
→
his;leu 70
→
pro;arg 72
→
trp;lys 73
→
ala;asp 77
→
ala;trp 79
→
lys;ile 80
→
thr;arg 81
→
ile;cys 87
→
ser;asn 96
→
ala;tyr 100
→
gly;leu 103
→
met;tyr 106
→
trp;phe 123
→
ser;lys 125
→
gly;ser 127
→
trp;tyr 132
→
thru;lys 134
→
val;thr 141
→
ala;
[0269]
(f)gln 28
→
his;leu 36
→
met;ala 40
→
phe;ile 41
→
his;gln 49
→
ser;tyr 52
→
pro;ser 68
→
his;leu 70
→
pro;arg 72
→
trp;lys 73
→
ala;asp 77
→
ala;trp 79
→
lys;ile 80
→
thr;arg 81
→
ile;cys 87
→
ser;asn 96
→
ala;tyr 100
→
gly;leu 103
→
met;tyr 106
→
trp;phe 123
→
ser;lys 125
→
gly;ser 127
→
trp;tyr 132
→
thru;lys 134
→
val;
[0270]
(g)gln 28
→
his;leu 36
→
his;ala 40
→
gln;ile 41
→
trp;asp 45
→
gly;lys 46
→
arg;gln 49
→
arg;tyr 52
→
trp;ser 68
→
asp;leu 70
→
asp;arg 72
→
ala;lys 73
→
ile;asp 77
→
leu;trp 79
→
arg;arg 81
→
thr;cys 87
→
ser;tyr 100
→
his;leu 103
→
gly;tyr 106
→
gly;lys 125
→
phe;ser 127
→
ile;tyr 132
→
ala;lys 134
→
phe;
[0271]
(h)gln 28
→
his;leu 36
→
his;ala 40
→
gln;ile 41
→
trp;glu 44
→
gly;lys 46
→
tyr;gln 49
→
arg;tyr 52
→
trp;ser 68
→
asp;leu 70
→
asp;arg 72
→
ala;lys 73
→
ile;lys 74
→
glu;asp 77
→
his;trp 79
→
arg;arg 81
→
thr;cys 87
→
ser;leu 94
→
phe;tyr 100
→
his;leu 103
→
gly;tyr 106
→
gly;val 108
→
ala;lys 125
→
phe;ser 127
→
ile;tyr 132
→
ala;lys 134
→
phe;或
[0272]
(i)leu 36
→
his;ala 40
→
gln;ile 41
→
trp;asp 45
→
gly;lys 46
→
arg;gln 49
→
arg;tyr 52
→
trp;asn 65
→
asp;ser 68
→
asp;leu 70
→
asp;arg 72
→
ala;lys 73
→
ile;asp 77
→
leu;trp 79
→
arg;arg 81
→
thr;cys 87
→
ser;tyr 100
→
his;leu 103
→
gly;tyr 106
→
gly;lys 125
→
phe;ser 127
→
ile;tyr 132
→
ala;lys 134
→
phe。
[0273]
本公开的pvd i型特异性脂质运载蛋白突变蛋白可包含选自seq id nos:115-131的氨基酸序列或其片段或变体。本公开的pvd i型特异性脂质运载蛋白突变蛋白可与seq id nos:115-131中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。本公开的pvd ii型特异性脂质运载蛋白突变蛋白可包含选自seq id nos:132-150的氨基酸序列或其片段或变体。本公开的pvd ii型特异性脂质运载蛋白突变蛋白可与seq id nos:132-150中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。本公开的pvd iii型特异
性脂质运载蛋白突变蛋白可包含选自seq id nos:151-166的氨基酸序列或其片段或变体。本公开的pvd iii型特异性脂质运载蛋白突变蛋白可与seq id nos:151-166中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。本公开的pch特异性脂质运载蛋白突变蛋白可包含选自seq id nos:167-176的氨基酸序列或其片段或变体。本公开的pch特异性脂质运载蛋白突变蛋白可与seq id nos:167-176中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0274]
6.对其他靶标特异性的脂质运载蛋白突变蛋白
[0275]
本领域已描述了对治疗靶标特异性的其他脂质运载蛋白突变蛋白。wo2011/069992描述了对淀粉样蛋白β和纤连蛋白的额外结构域(extra-domain)b特异性的脂质运载蛋白突变蛋白。淀粉样蛋白β(aβ)是关键涉及于阿尔茨海默病中的肽,作为在阿尔茨海默患者脑中发现的淀粉样蛋白斑的主要成分。所述肽衍生自淀粉样前体蛋白(app),其被β分泌酶和γ分泌酶切割产生aβ。纤连蛋白(fn)是大的、模块的二聚体糖蛋白,其包含多个i、ii和iii型结构域。fn的选择性剪接变体,例如含有额外结构域b(ed-b)的同种型,其掺入fniii7和fniii8结构域之间,以组织特异性和发育阶段依赖性方式表达(zardi等,embo j,1987)。除了在伤口愈合和肿瘤血管形成期间,正常成人组织中不存在ed-b。因此,含有ed-b的纤连蛋白在许多不同的肿瘤类型中大量表达,所述肿瘤类型引起新血管形成并经历异常的血管生成。本公开的淀粉样蛋白β特异性脂质运载蛋白突变蛋白可包含选自seq id nos:195-199的氨基酸序列或其片段或变体。本公开的淀粉样蛋白β特异性脂质运载蛋白突变蛋白可与seq id nos:195-199中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。本公开的对纤连蛋白ed-b特异性的脂质运载蛋白突变蛋白可包含选自seq id nos:200-203的氨基酸序列或其片段或变体。本公开的纤连蛋白ed-b特异性脂质运载蛋白突变蛋白可与seq id nos:200-203中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0276]
wo2014/076321和wo2015/177175描述了对白介素-17a(il-17a或il-17)和白介素-23(il-23)、特别是白介素-23的p19亚基(il-23p19)特异性的脂质运载蛋白突变蛋白。
[0277]
人il-17a(ctla-8,进一步命名为il-17,swiss prot q16552)是一种mr为17,000道尔顿的糖蛋白(spriggs,j clin immunol,1997)。il-17a可以以同二聚体il-17 a/a或以与同系物il-17f复合以形成异二聚体il-17 a/f的异二聚体存在。il-17f(il-24,ml-1)与il-17a共有55%的氨基酸同一性。il-17a和il-17f也共有同一个受体(il-17ra),其在多种细胞上表达,所述细胞包括血管内皮细胞、外周t细胞、b细胞、成纤维细胞、肺细胞、骨髓单核细胞和骨髓基质细胞(moseley等,cytokine growth factor rev,2003;kawaguchi等,j allergy clin immunol,2004;kolls和linden,immunity,2004)。il-17a主要由th17细胞表达,在类风湿性关节炎(ra)患者的滑液中以升高的水平存在,并已显示参与早期ra发展。il-17a也在多发性硬化(ms)患者的脑脊液中过表达。此外,il-17是tnf-α和il-1的诱导剂,后者主要负责骨侵蚀和对于受累患者的非常疼痛的后果(lubberts,cytokine,2008)。此
外,il-17a的不适当或过度产生与各种其它疾病和病症的病理学有关,例如骨关节炎、骨植入物的松动、急性移植排斥(van kooten等,j am soc nephrol,1998;anonyssamy等,j immunol,1999)、败血症、脓毒性或内毒素性休克、过敏、哮喘(molet等,j allergy clin immunol,2001)、骨丢失、牛皮癣(teunissen等,j invest dermatol,1998)、局部缺血、系统性硬化(kurasawa等,arthritis rheum,2000)、中风和其它炎性病症。本公开的对il-17a特异性的脂质运载蛋白突变蛋白可包含选自seq id nos:99-104的氨基酸序列或其片段或变体。本公开的il-17a特异性脂质运载蛋白突变蛋白可与seq id nos:99-104中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0278]
白介素-23(也称为il-23)是一种异二聚体细胞因子,由两个亚基即p19和p40组成(oppmann等,immunity,2000)。p19(swiss prot q9npf7,本文中可互换地称为“il-23p19”)亚基在结构上与il-6、粒细胞集落刺激因子(g-csf)和il-12的p35亚基相关。il-23通过结合由il-23r和il-12β1组成的异二聚体受体介导信号传导。il-12β1亚基是il-12受体所共有的,由il-12β1和il-12β2组成。最近已经描述了转基因p19小鼠显示严重的全身性炎症和嗜中性白细胞增多(wiekowski等,j immunol,2001)。已报道人il-23促进t细胞、特别是记忆t细胞的增殖,并可有助于thi 7细胞的分化和/或维持(frucht,sci stke,2002)。本公开的对il-23p19特异性的脂质运载蛋白突变蛋白可包含选自seq id nos:105-114的氨基酸序列或其片段或变体。本公开的il-23p19特异性脂质运载蛋白突变蛋白可与seq id nos:105-114中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0279]
细胞毒性t淋巴细胞相关蛋白4(ctla-4)是一种蛋白质受体,其作为免疫检查点发挥作用并下调免疫应答。ctla-4在调节性t细胞中组成型表达,但在活化后仅在常规t细胞中上调。ctla-4阻断被认为是抑制免疫系统对肿瘤耐受的一种手段,由此为癌症患者提供了一种潜在有用的免疫治疗策略。对ctla-4特异性的脂质运载蛋白突变蛋白公开于wo2006/056464和wo2012/072806中。本公开的对ctla-4特异性的脂质运载蛋白突变蛋白可包含选自seq id nos:92-98的氨基酸序列或其片段或变体。本公开的ctla-4特异性脂质运载蛋白突变蛋白可与seq id nos:92-98中任一个所示的氨基酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少92%、至少95%、至少97%、至少98%或甚至更高序列同一性。
[0280]
对治疗靶标特异性的其它脂质运载蛋白突变蛋白例如公开于wo2009/095447,其公开了对c-met特异性的脂质运载蛋白突变蛋白;wo2012/065978、wo2013/174783和wo2016/184875,其公开了对磷脂酰肌醇蛋白聚糖-3特异性的脂质运载蛋白突变蛋白;wo2017/009456和wo2018/134274,其公开了对lag-3特异性的脂质运载蛋白突变蛋白;wo2016/177762和wo2018/087108,其公开了对cd137特异性的脂质运载蛋白突变蛋白;wo2016/120307,其公开了对ang-2特异性的脂质运载蛋白突变蛋白;和wo2008/015239,其公开了对1egf特异性的脂质运载蛋白突变蛋白。
[0281]
b.本公开的脂质运载蛋白突变蛋白的施用
[0282]
本公开的脂质运载蛋白突变蛋白可通过吸入施用。用于物质的吸入施用的方法和装置是本领域技术人员已知的,例如在wo94/017784a和elphick等(2015)中公开。这些装置
和设备包括喷雾器、计量剂量吸入器、粉末吸入器和鼻喷雾剂。适于指导脂质运载蛋白突变蛋白的吸入施用的其它手段和装置也是本领域已知的。喷雾器可用于由溶液产生气溶胶,而计量剂量吸入器、干粉吸入器等有效产生小颗粒气溶胶。
[0283]
喷雾器是一种用于以吸入肺部的薄雾形式给药的药物输送装置。不同类型的喷雾器是本领域技术人员已知的,包括喷射喷雾器、超声波喷雾器、振动网技术和软雾吸入器。一些喷雾器提供连续的雾化溶液流,即它们将在长时间段内提供连续的雾化,而不管受试者是否从其吸入,而其他的喷雾器是呼吸致动的,即受试者仅在从其吸入时获得一定剂量。
[0284]
计量剂量吸入器(mdi)是一种以液体雾化药物的短爆发形式将特定量的药物输送到肺部的装置。这种计量剂量吸入器通常由三个主要部件组成:包含待施用的制剂的罐,允许每次致动时分配计量数量的制剂的计量阀,和允许患者操作该装置并将液体气溶胶导入患者肺中的致动器(或接口)。
[0285]
干粉吸入器(dpi)是一种以干粉形式将药物输送到肺部的装置。干粉吸入器是基于气雾剂的吸入器例如计量剂量吸入器的替代物。药物通常保持在用于手动装载的胶囊中或位于吸入器内部的专有泡罩包装中。
[0286]
鼻喷雾剂可用于经鼻给药,通过该鼻喷雾剂将药物通过鼻吹入。鼻喷雾剂可提供药物的极快吸收。
[0287]
脂质运载蛋白突变蛋白可一次、两次、三次、四次、五次、一周一次、一周两次、一周三次、一周四次、一周五次、一周六次、一天一次或一天两次施用。
[0288]
脂质运载蛋白突变蛋白的吸入施用可导致对脂质运载蛋白突变蛋白的局部暴露、全身暴露或局部和全身暴露。据信脂质运载蛋白突变蛋白的剂量对施用是否导致局部或全身暴露具有强烈影响。通常,认为低剂量的脂质运载蛋白突变蛋白倾向于导致局部暴露,而高剂量倾向于导致全身暴露。
[0289]
在一些实施方案中,局部暴露是指脂质运载蛋白突变蛋白的递送剂量的约0.15%或更少、0.1%或更少、0.05%或更少、0.03%或更少、0.02%或更少或0.01%或更少进入循环系统。在一些实施方案中,局部暴露是指没有可检测的脂质运载蛋白突变蛋白的全身暴露。脂质运载蛋白突变蛋白的全身暴露优选在血液中测量,优选在血浆或血清中测量。
[0290]
在一些实施方案中,局部暴露是指递送的脂质运载蛋白突变蛋白的约20%或更多、约30%或更多、约40%或更多、约50%或更多、约60%或更多、约70%或更多、约80%或更多、或约90%或更多保留在呼吸道或肺中,例如在肺组织或上皮内衬流体中。
[0291]
为了实现局部暴露,脂质运载蛋白突变蛋白的递送剂量可以为每次施用约0.05mg至约1000mg,优选每次施用0.05mg至约5mg,优选每次施用约0.1mg至约5mg,优选每次施用约0.1mg至约2mg。脂质运载蛋白突变蛋白的递送剂量可以为每次施用每kg体重约0.05μg至约15mg,优选每次施用每kg体重约0.05μg至约100μg,优选每次施用每kg体重约0.05μg至约50μg,优选每次施用每kg体重约0.1μg至约50μg。通常,脂质运载蛋白突变蛋白的递送剂量可以为每次施用约10mg或更少、约9mg或更少、约8mg或更少、约7mg或更少、约6mg或更少、或约5mg、或约2mg、或约1mg、或约100μg、或约50μg或更少、或约200μg或更少、约180μg或更少、约160μg或更少、约140μg或更少、约120μg或更少、约100μg或更少、约90μg或更少、约80μg或更少、约70μg或更少、约60μg或更少、约50μg或更少、约40μg或更少、约30μg或更少、约20μg或更少、或约10μg或更少。脂质运载蛋白突变蛋白的递送剂量可以为每次施用约0.05mg或
更多、约0.1mg或更多、或约0.2mg或更多,或每次施用每kg体重约0.05μg或更多、约0.1μg或更多、约0.15μg或更多。
[0292]
如果脂质运载蛋白突变蛋白用于治疗呼吸道疾病或病症,则可能需要局部暴露。局部暴露将具有的益处是脂质运载蛋白突变蛋白保持在其发挥作用的位置。此外,保留在呼吸道中的脂质运载蛋白突变蛋白的清除率可能低于全身吸收的脂质运载蛋白突变蛋白。
[0293]
在一些实施方案中,全身暴露是指脂质运载蛋白突变蛋白的递送剂量的约0.3%或更多、约0.4%或更多、约0.5%或更多、约0.6%或更多、约0.7%或更多、约0.8%或更多、约0.9%或更多、约1%或更多、约2%或更多、约3%或更多、约4%或更多、约5%或更多、约6%或更多、约7%或更多、约8%或更多、约9%或更多、约10%或更多、约11%或更多、约12%或更多、约13%或更多、约14%或更多、或约15%或更多进入循环系统。
[0294]
为了实现全身暴露,脂质运载蛋白突变蛋白的递送剂量可以为每次施用约0.05mg至约1000mg,优选每次施用5mg至约1000mg,优选每次施用约6mg至约500mg,优选每次施用约7mg至约300mg,优选每次施用约7mg至约280mg。脂质运载蛋白突变蛋白的递送剂量可以为每次施用每kg体重约0.1μg至约15mg,优选每次施用每kg体重约0.05mg至约8mg,优选每次施用每kg体重约0.1mg至约4mg。通常,脂质运载蛋白突变蛋白的递送剂量可以为每次施用约4mg或更多、约5mg或更多、约6mg或更多、约7mg或更多、约8mg或更多、约9mg或更多、约10mg或更多、约15mg或更多、约20mg或更多、约25mg或更多、约30mg或更多、约50mg或更多、或约100mg或更多,或每次施用每kg体重约50μg或更多、60μg或更多、70μg或更多、80μg或更多、约90μg或更多、约100μg或更多、约120μg或更多、约140μg或更多、约160μg或更多、约180μg或更多、约200μg或更多、约250μg或更多、约300μg或更多、约400μg或更多、约500μg或更多。脂质运载蛋白突变蛋白的递送剂量可以为每次施用约400mg或更少、约300mg或更少、约200mg或更少、约150mg或更少、约120mg或更少、或约100mg或更少,或每次施用每kg体重约6mg或更少、约5mg或更少、约4mg或更少、约3mg或更少、约2.5mg或更少、或约2mg或更少。
[0295]
吸入施用后脂质运载蛋白突变蛋白的全身暴露的特征可在于快速吸收。血浆中脂质运载蛋白突变蛋白的最大浓度可以在施用后约0.1小时至约10小时、优选约0.5小时至约5h后、优选在约1h至约2h后达到。血浆中脂质运载蛋白突变蛋白的最大浓度(c
max
)可以为约1ng/ml或更多、约3ng/ml或更多、约8ng/ml或更多、约10ng/ml或更多、约50ng/ml或更多、约100ng/ml或更多、约600ng/ml或更多、约1,000ng/ml或更多、约1,500ng/ml或更多、或约2,000ng/ml,例如约1ng/ml至约2,000ng/ml、约1ng/ml至约600ng/ml、或约1ng/ml至约100ng/ml。脂质运载蛋白突变蛋白的血清浓度的时间曲线下面积(auc
inf
)可以为约10h*ng/ml或更多、约20h*ng/ml或更多、约70h*ng/ml或更多、约100h*ng/ml或更多、约500h*ng/ml或更多、约1,000h*ng/ml或更多、约5,000h*ng/ml或更多、约10,000h*ng/ml或更多、或约16,000h*ng/ml或更多,诸如约10h*ng/ml至约16,000h*ng/ml、约10h*ng/ml至约5,000h*ng/ml、或20h*ng/ml至约5,000h*ng/ml。脂质运载蛋白突变蛋白的血清半衰期(t
1/2
)可以为约2小时至约10小时,诸如约5小时、约6小时、约7小时、约8小时、约9小时或约10小时。
[0296]
全身暴露可能是期望的,以实现与药物的累加和/或协同效应,所述药物否则将保留在呼吸道中,即以非常低的水平(或在定量限制以下)进入循环系统。如果脂质运载蛋白突变蛋白用于治疗全身性或影响除呼吸系统以外的组织或器官的疾病或病症,则也可能需要全身暴露。例如,对于cgrp特异性脂质运载蛋白突变蛋白的施用,全身暴露可能是期望
的。如本文所用的“全身性疾病”是影响许多器官和组织或影响整个身体的疾病。
[0297]
局部暴露将具有的益处是脂质运载蛋白突变蛋白保持在其发挥作用的位置。此外,保留在呼吸道中的脂质运载蛋白突变蛋白的清除率可能低于全身吸收的脂质运载蛋白突变蛋白。
[0298]
c.制剂
[0299]
用于本发明的脂质运载蛋白突变蛋白通常以药物组合物的形式施用,其可以包含除特异性结合成员之外的至少一种组分。因此,除了活性成分之外,根据本发明使用的药物组合物可以包含药学上可接受的赋形剂、载体、缓冲剂、稳定剂或本领域技术人员熟知的其它材料。这些物质应该是无毒的,并且不应该干扰活性成分的功效。例如,可将根据本发明使用的脂质运载蛋白突变蛋白配制在磷酸盐缓冲盐水(pbs)的水溶液中。
[0300]
在一些实施方案中,根据本发明使用的药物组合物可包含赋形剂。在一些实施方案中,这样的赋形剂可促进吸入的药物,例如本公开的脂质运载蛋白突变蛋白,到达肺深部和/或肺的肺泡区。在一些实施方案中,这样的赋形剂可以增强吸入的药物例如本公开的脂质运载蛋白突变蛋白的全身摄取。在一些实施方案中,这样的赋形剂可促进吸入的药物例如本公开的脂质运载蛋白突变蛋白的更快起效。在一些实施方案中,这样的赋形剂可以有助于吸入的药物例如本公开的脂质运载蛋白突变蛋白的增强的治疗效果。在一些实施方案中,这样的赋形剂可以在溶液中形成微球。在一些实施方案中,根据本发明使用的药物组合物可以包含富马酰基二酮哌嗪(fdkp)。
[0301]
包含脂质运载蛋白突变蛋白的药物组合物可单独施用或与其它治疗同时或依次地组合施用。
[0302]
适合与喷雾器一起使用的制剂通常包含分散在水或液体(通常是含水)介质中的脂质运载蛋白突变蛋白。制剂还可以包括缓冲剂、糖(例如,用于蛋白质稳定和渗透压调节)、(生理量的)盐和/或其它药学上可接受的赋形剂。可以使用的缓冲剂的实例是磷酸盐、乙酸盐、柠檬酸盐和甘氨酸。合适的缓冲液是磷酸盐缓冲盐水(例如1.06mm kh2po4,2.96mm na2hpo4,154mm nacl,ph 7.4)。
[0303]
与计量剂量吸入器装置一起使用的脂质运载蛋白突变蛋白制剂通常包含细分粉末。可通过冻干含有脂质运载蛋白突变蛋白的制剂并研磨至所需粒度来产生该粉末。该制剂还可含有稳定剂如人血清白蛋白(has)。可以向制剂中加入一种或多种糖或糖醇。实例包括乳糖、麦芽糖、甘露醇、山梨醇、山梨糖醇、海藻糖、木糖醇和木糖。然后可任选地借助于表面活性剂将颗粒悬浮在推进剂中。推进剂可以是用于该目的任何常规材料,例如氯氟烃、氢氯氟烃、氢氟烃或烃,包括三氯氟甲烷、二氯二氟甲烷、二氯四氟乙醇和1,1,1,2-四氟乙烷或其组合。合适的表面活性剂包括脱水山梨糖醇三油酸酯和大豆卵磷脂。油酸也可用作表面活性剂。
[0304]
d.疾病的治疗
[0305]
1.呼吸道的疾病或病症
[0306]
呼吸道的疾病或病症是指涉及呼吸系统的任何疾病或病症。可以使用脂质运载蛋白突变蛋白经由吸入施用来治疗这样的疾病或病症。在一些实施方案中,施用可提供在呼吸道中对脂质运载蛋白突变蛋白的局部暴露。局部暴露可能是有益的,允许脂质运载蛋白突变蛋白保留在呼吸道,即其发挥作用的位置。在一些其他实施方案中,施用可以提供对脂
质运载蛋白突变蛋白的全身暴露。与脂质运载蛋白突变蛋白基本上保留在呼吸道中时即当全身暴露非常低(即,在定量限值以下)时相比,这种全身暴露可提供累加和/或协同效应。在一些实施方案中,与全身性施用(约)相同或相当的生物可利用量的脂质运载蛋白突变蛋白相比,脂质运载蛋白突变蛋白的吸入施用提供改善的效果,诸如潜在的更长的作用持续时间。因此,在一些实施方案中,可能需要对吸入的脂质运载蛋白突变蛋白的全身暴露。
[0307]
呼吸道的疾病或病症包括变应性炎症、变应性哮喘、鼻炎、结膜炎、肺纤维化、囊性纤维化、慢性阻塞性肺病、肺泡蛋白沉积症、成人呼吸窘迫综合征或细菌感染,例如铜绿假单胞菌(pseudomonas aeruginosa)感染。呼吸道的疾病或病症可以是肺病,例如(变应性)哮喘、慢性阻塞性肺病(copd)或囊性纤维化(cf)。
[0308]
白介素(il)-4和il-13长期以来与呼吸道的各种疾病或病症相关。这些疾病或病症可以使用il-4rα拮抗剂、例如对il-4rα特异性的脂质运载蛋白突变蛋白治疗。
[0309]
例如,哮喘是一种复杂的、持续性的炎性疾病,其特征在于与气道炎症相关的气道高反应性。研究表明,定期使用高剂量的吸入的皮质类固醇和长效支气管扩张药或奥马珠单抗(一种结合免疫球蛋白e并且经常用作针对不受控于护理治疗标准的患者的递升治疗的人源化单克隆抗体)可能不足以在所有患者中提供哮喘控制,从而突出了一个重要的未满足的需求。白介素-4(il-4)、白介素-13(il-13)和转录因子-6的信号转导和激活剂是哮喘中气道炎症、粘液产生和气道高反应性的发展中的关键组分。在一些优选的实施方案中,变应性哮喘是其中il-4/il-13途径有助于疾病发病的气道炎症。
[0310]
涉及il-4/il-13信号传导途径的其它肺病包括肺部病症。这样的肺部病症包括但不限于肺纤维化,包括慢性纤维化肺病、特征在于il-4诱导的成纤维细胞增殖或胶原在肺中累积的病症、th2免疫应答在其中起作用的肺部病症、特征在于肺中屏障功能降低(例如,由il-4诱导的上皮损伤引起)的病症、或il-4在炎性应答中起作用的病症。
[0311]
囊性纤维化(cf)的特征在于粘液的过量产生和慢性感染的发展。抑制il-4rα和th2应答将减少粘液产生并帮助控制感染,诸如变应性支气管肺曲霉病(abpa)。变应性支气管肺真菌病主要发生在患有囊性纤维化或哮喘的患者中,其中th2免疫应答是占优势的。抑制il-4rα和th2应答将有助于清除和控制这些感染。
[0312]
慢性阻塞性肺病(copd)与粘液分泌过多和纤维化相关。抑制il-4rα和th2应答将减少粘液的产生和纤维状的发展,由此改善呼吸功能和延缓疾病进展。博来霉素诱导的肺病和纤维化以及辐射诱导的肺纤维化是特征在于肺的纤维化的病症,其表现为th2、cd4
+
细胞和巨噬细胞的流入,这些细胞产生il-4和il-13,而il-4和il-13进而介导纤维化的发展。抑制il-4rα和th2应答将减少或预防这些病症的发展。
[0313]
而且,il-4和il-13诱导肺上皮细胞分化成产粘液杯状细胞。因此,il-4和il-13可有助于在亚群或某些情况下粘液产生的增加。粘液产生和分泌有助于copd和cf中的疾病发病机理。因此,优选地,通过本公开的方法,通过应用如本文所述的对il-4rα特异性的脂质运载蛋白突变蛋白,可以治疗、改善或预防与粘液产生或粘液分泌(例如,过量产生或分泌过多)相关的病症。在一些优选的实施方案中,与粘液产生或粘液分泌相关的病症优选是慢性阻塞性肺病(copd)或囊性纤维化(cf)。
[0314]
肺泡蛋白沉积症的特征在于表面活性剂清除的破坏。il-4增加表面活性剂产物。在一些进一步的实施方案中,本文还考虑了il-4rα拮抗剂、诸如本公开的对il-4rα特异性
的脂质运载蛋白突变蛋白减少表面活性剂产生并减少对整个肺灌洗的需要的用途。
[0315]
成人呼吸窘迫综合症(ards)可归因于许多因素,其中之一是对毒性化学物质的暴露。因此,作为优选但非限制性的实例,一个对ards敏感的患者群是使用呼吸器的危重患者,因为ards是这类患者中常见的并发症。在一些进一步的实施方案中,il-4rα拮抗剂诸如本公开的il-4rα特异性脂质运载蛋白突变蛋白,因此可用于通过减少炎症和粘附分子来减轻、预防或治疗ards。
[0316]
结节病的特征在于肉芽肿性病变。在一些进一步的实施方案中,本文还考虑了il-4rα拮抗剂、诸如本公开的il-4rα特异性脂质运载蛋白突变蛋白治疗结节病、特别是肺结节病的用途。
[0317]
il-4诱导的肺中屏障破坏在其中起作用的病症可以用il-4rα拮抗剂治疗。对肺中上皮屏障的损伤可由il-4和/或il-13直接或间接诱导。肺中的上皮作为选择性屏障起作用,其防止肺腔的内容物进入粘膜下层。受损或“渗漏的”屏障允许抗原穿过屏障,这继而引发可引起对肺组织进一步损伤的免疫应答。这种免疫应答可包括例如嗜酸性粒细胞或肥大细胞的募集。可以局部地施用il-4rα拮抗剂以抑制这种不希望的免疫应答刺激。
[0318]
在这点上,il-4rα拮抗剂诸如本公开的il-4rα特异性脂质运载蛋白突变蛋白可用于促进例如哮喘患者肺上皮的愈合,从而恢复屏障功能,或者出于预防目的通过在呼吸系统中局部施用来给药,以预防il-4和/或il-13诱导的肺上皮损伤。
[0319]
呼吸道的疾病或病症也可以是细菌感染,例如由细菌铜绿假单胞菌(p.aeruginosa)引起的感染。铜绿假单胞菌是机会致病菌,其引起急性感染,主要与组织损伤相关。值得注意的是,相同的病原体还与copd、cf、支气管扩张和慢性破坏性肺病中进行性和最终慢性复发性呼吸道感染相关(yum等,tuberc respir dis(seoul),2014)。铜绿假单胞菌感染的发病机理主要取决于其形成生物膜的能力,该生物膜是可覆盖粘膜表面或侵入性装置的结构化细菌群落。生物膜感染难以用常规抗生素疗法治疗。绿脓杆菌荧光素和绿脓杆菌螯铁蛋白是铜绿假单胞菌致病性的关键靶标。因此,细菌感染诸如由铜绿假单胞菌引起的感染进一步代表可以在吸入施用后经由对本公开的脂质运载蛋白突变蛋白的局部暴露而治疗的疾病。因此,对绿脓杆菌荧光素i、ii、iii型或绿脓杆菌螯铁蛋白特异性的脂质运载蛋白突变蛋白可用于治疗这样的感染。
[0320]
癌症治疗是用于实现对脂质运载蛋白突变蛋白的局部暴露的另一应用领域,特别是治疗呼吸道的癌症,诸如肺癌。本文公开了对一系列癌症靶标特异性的脂质运载蛋白突变蛋白,并且本公开考虑了所有这些脂质运载蛋白突变蛋白通过吸入施用在癌症治疗中的用途。这样的脂质运载蛋白突变蛋白包括对ed-b纤连蛋白、ctla-4、c-met、磷脂酰肌醇蛋白聚糖-3、lag-3、cd137、ang-2或vegf特异性的脂质运载蛋白突变蛋白。
[0321]
2.全身性疾病和其他器官或组织的疾病
[0322]
影响除呼吸系统以外的器官或组织的全身性疾病或病症可以使用吸入施用后全身性吸收的脂质运载蛋白突变蛋白来治疗。这样的疾病或病症包括疼痛病症诸如偏头痛、贫血、心血管疾病、神经变性疾病诸如阿尔茨海默病、炎性疾病、变应性疾病、癌症和细菌感染诸如铜绿假单胞菌感染。
[0323]
除了呼吸道的疾病或病症,il-4/il-13途径还涉及于一系列影响除呼吸道以外的其它器官或组织的全身性疾病或病症。这样的疾病或病症的实例是变应性疾病,诸如鼻炎、
结膜炎、皮炎或食物变应性。因此,也有导致全身暴露的吸入施用il-4rα特异性脂质运载蛋白突变蛋白的治疗应用。因此,本公开还考虑经由对il-4rα特异性脂质运载蛋白突变蛋白的全身暴露来治疗或预防疾病和病症。这样的疾病或病症包括变应性疾病,诸如鼻炎、结膜炎、皮炎或食物变应性。
[0324]
疼痛病症可以是偏头痛,其是典型地以中度至重度的复发性头痛为特征的原发性头痛病症。典型地,头痛影响一半的头,本质上是搏动的,并且持续两至72个小时。相关症状可包括恶心、呕吐以及对光、声音或气味的敏感性。据报道,cgrp在偏头痛中起作用,因为cgrp在刺激感觉神经时释放,并具有有效的血管舒张活性(arulmozhi等,vascul pharmacol,2005)。此外,cgrp的释放增加了三叉神经纤维在这些纤维受刺激时神经支配的组织中血管通透性和随后的血浆蛋白渗漏(血浆蛋白外渗)(arulmozhi等,vascul pharmacol,2005)。此外,研究报道在患有偏头痛的患者中输注cgrp已经导致偏头痛样症状(lassen等,cephalalgia,2002)。本公开的cgrp特异性脂质运载蛋白突变蛋白可用于治疗与游离cgrp水平失调相关的疾病或病症。这样的脂质运载蛋白突变蛋白可用于降低游离cgrp的循环水平。优选地,本公开的crgp结合脂质运载蛋白突变蛋白可用于治疗、预防和/或改善parin病症,特别是偏头痛。cgrp特异性脂质运载蛋白突变蛋白的吸入施用具有该方法避免注射和能够自我给药的优点。另一个优点是当通过吸入施用cgrp特异性脂质运载蛋白突变蛋白时治疗功效和全身吸收的快速起效。
[0325]
令人惊讶地,脂质运载蛋白突变蛋白、诸如本文所述的cgrp特异性脂质运载蛋白突变蛋白的吸入施用,可具有优于(即快于)皮下施用的起效。令人惊讶地,脂质运载蛋白突变蛋白、诸如本文所述的cgrp特异性脂质运载蛋白突变蛋白的吸入施用,可具有与直接全身性施用(诸如静脉内施用)相当(即大约一样快)或甚至更快的起效。通过与某些赋形剂如富马酰基二酮哌嗪(fdkp)制剂,可以实现脂质运载蛋白突变蛋白的增加的全身暴露、更快速的起效和/或增强的治疗作用。特别是关于本公开的cgrp特异性脂质运载蛋白突变蛋白(例如包含seq id no:47所示的序列的脂质运载蛋白突变蛋白),其起效可以与参照抗cgrp抗体(seq id nos:204和205)大约一样快或相比甚至更快。当与fdkp配制时,例如以0.4mg/kg,本公开的cgrp特异性脂质运载蛋白突变蛋白可显示更迅速的起效,诸如约1分钟、约2分钟、约3分钟、约4分钟、约5分钟、约10分钟、约15分钟、约20分钟、约25分钟或约30分钟的起效。cgrp特异性脂质运载蛋白突变蛋白的起效可以在感觉神经介导的血管舒张试验中测定。这种试验可以基本上如实施例4中所述进行。
[0326]
本文所述的cgrp特异性脂质运载蛋白突变蛋白(例如包含seq id no:47所示的序列的脂质运载蛋白突变蛋白)的治疗作用(诸如抑制血管舒张)与参照抗cgrp抗体(seq id nos:204和205)相当或优于该参照抗cgrp抗体。当与fdkp配制时,例如以0.4mg/kg,本公开的cgrp特异性脂质运载蛋白突变蛋白的起效可进一步增强。
[0327]
贫血是与血清铁耗竭相关的疾病,其导致血液学参数诸如红细胞(rbc)计数、血细胞比容(ht)、血红蛋白(hb)、血清铁水平和转铁蛋白(tf)饱和度降低。这导致血液中氧水平降低,并与由虚弱、注意力不集中、呼吸短促和呼吸困难描述的生活质量(qol)下降相关。严重的贫血可导致心率加快、心脏增大和心力衰竭。贫血通常与慢性肾病/已形成的慢性肾病(ckd)、癌症贫血(ac)、化疗诱导的贫血(cia)和慢性疾病贫血(acd)相关。
[0328]
缺铁性贫血是铁稳态紊乱,与炎性疾病相关的贫血相比,其易于通过铁施用而治
愈。铁调素是一个能够区分这两种疾病的参数,因为铁调素水平仅在与炎症结合时被上调。
[0329]
铁调素是铁稳态的主要负调控子。铁调素的产生随铁负荷和炎症而增加,在低铁条件和低氧下减少。铁调素经由与唯一已知的哺乳动物细胞铁输出蛋白即铁转运蛋白结合而发挥作用,并诱导其内化和降解。由于铁转运蛋白在十二指肠上皮细胞、脾和肝中表达,铁调素增加,而随后的铁转运蛋白减少,导致十二指肠的铁吸收的抑制,从巨噬细胞释放回收的铁,以及肝中铁储备的动员。铁调素被认为在与炎性疾病相关的贫血的发展中起关键作用。急性或慢性炎性病症导致铁调素表达上调,从而导致缺铁,这可引起与acd、ac、cia相关的贫血和ckd贫血。
[0330]
本公开的铁调素结合脂质运载蛋白突变蛋白可用于治疗具有升高水平的铁调素、铁调素相关病症、铁稳态病症、贫血或与升高水平的铁调素相关的炎性病症的受试者。贫血可以是炎症贫血、慢性炎性贫血、缺铁性贫血、铁负荷贫血、与ckd、ac、cia相关的贫血或与红细胞生成刺激剂(esa)抗性相关的贫血中的任一种。
[0331]
冠状动脉疾病(cad),也称为缺血性心脏病(ihd),涉及由于心脏动脉中斑块的累积而导致的流向心肌的血流减少。它是最常见的心血管疾病。类型包括稳定型心绞痛、不稳定型心绞痛、心肌梗塞和心脏性猝死。本公开的pcsk9结合脂质运载蛋白突变蛋白可用于治疗或预防这样的冠心病。
[0332]
神经变性疾病是可以在吸入施用后经由对脂质运载蛋白突变蛋白的全身暴露而治疗的另一组疾病。阿尔茨海默病(ad)是老年人群中最常见的痴呆形式。与ad相关的是淀粉样前体蛋白的缺陷性加工,这产生潜在神经毒性的包括40-42个残基的淀粉样β肽(aβ)。aβ随后聚集为寡聚体和长原纤维,这在疾病过程中起关键作用,最终形成老年斑(haass和selkoe,nat rev mol cell biol,2007)。本公开的淀粉样蛋白β特异性脂质运载蛋白突变蛋白因此可用于治疗或预防神经变性疾病诸如ad。
[0333]
细菌感染诸如铜绿假单胞菌引起的感染进一步代表可以在吸入施用后经过对本公开的脂质运载蛋白突变蛋白的全身暴露而治疗的疾病。绿脓杆菌荧光素和绿脓杆菌螯铁蛋白是铜绿假单胞菌致病性的关键靶标。因此,对绿脓杆菌荧光素i、ii、iii型或绿脓杆菌螯铁蛋白特异性的脂质运载蛋白突变蛋白可用于治疗这样的感染。
[0334]
炎性疾病和自身免疫疾病是另一组疾病,其可以在吸入施用后经由对本公开的脂质运载蛋白突变蛋白的全身暴露而治疗。il-17a和il-23都是参与炎症和自身免疫疾病的细胞因子。因此,本公开的il-17a特异性或il-23特异性脂质运载蛋白突变蛋白可用于治疗或预防炎性疾病或自身免疫疾病,诸如多发性硬化、类风湿性关节炎、克罗恩氏病和银屑病。
[0335]
癌症治疗是用于实现对脂质运载蛋白突变蛋白的全身暴露的另一应用领域。本文公开了对一系列癌症靶标特异性的脂质运载蛋白突变蛋白,并且本公开考虑了所有这些脂质运载蛋白突变蛋白通过吸入施用在癌症治疗中的用途。这样的脂质运载蛋白突变蛋白包括对ed-b纤连蛋白、ctla-4、c-met、磷脂酰肌醇蛋白聚糖-3、lag-3、cd137、ang-2或vegf特异性的脂质运载蛋白突变蛋白。
[0336]
在研究了以下实施例及其附图后,本公开的其他目的、优点和特征对于本领域技术人员将变得显而易见,所述实施例及其附图不旨在限制。因此,应当理解,尽管本公开通过示例性实施方案和任选特征具体公开,但本领域技术人员可以采用本文公开的本文中实
施的公开的修改和变化,并且这样的修改和变化被认为在本公开的范围内。
[0337]
v.实施例
[0338]
实施例1:气管内施用的脂质运载蛋白突变蛋白在健康小鼠中的药代动力学
[0339]
在健康小鼠中进行示例性脂质运载蛋白突变蛋白(seq id nos:3和4)的药代动力学(pk)分析。
[0340]
使用微型喷雾器(#1a-1c-m,penn century)以100μg/kg或100μg/小鼠的剂量给约8周龄的雌性小鼠气管内施用各自的测试脂质运载蛋白突变蛋白。在1h、4h、6h、12小时和24小时在处死小鼠后获得血浆、支气管肺泡灌洗液(balf)和肺匀浆物样品(n=5只动物/时间点/测试分子),并测定相应的药物水平。
[0341]
在确定的时间点,通过在轻度异氟烷麻醉下心脏穿刺,从实验组中的所有动物抽取血液,放入装有肝素锂作为抗凝剂的管中。然后将样品在eppendorf管中于4℃下以5000
×
rpm离心10分钟,收集血浆(100μl/管)并在-80℃下储存直至进一步使用。balf样品通过用0.5ml盐水洗涤肺三次(总量:1.5ml),然后在4℃下以400
×
g离心10分钟而获得。收集上清液并在-80℃下储存直至进行试验。灌洗后立即用盐水通过右心室灌注肺以冲洗血管内容物,随后冷冻并储存在-20℃下。通过使用ultra turrax匀浆器(ika)将称重的肺在含有蛋白酶抑制剂混合物的1ml pbs中匀浆来获得肺匀浆物。将肺匀浆物等分并在-80℃下储存用于进一步分析。在分析前,使用bca蛋白测定试剂盒定量肺匀浆物中的总蛋白浓度。用pbs将匀浆物样品调节至总蛋白浓度为5mg/ml(标准化肺匀浆物)。
[0342]
使用以下方案分析balf、肺匀浆物和血浆中的药物水平:将抗ngal或抗tlc抗体(pieris)溶解在pbs(1μg/ml)中,并在4℃下在微量滴定板上包被过夜。在每个温育步骤后,用80μl pbs-0.05%t(补充0.05%(v/v)tween 20的pbs)洗涤板五次。将板用含2%bsa(w/v)的pbs-0.1%t(pbs-0.1%t-2%bsa)在室温虾封闭1小时,随后洗涤。将样品在pbs-0.1%t-2%bsa稀释——血浆样品稀释至50%血浆浓度,肺样品稀释至20%肺匀浆物,balf样品稀释至facs缓冲液中20%balf——加入到孔中,并在室温下温育1小时。接着进行另一个洗涤步骤。在用1μg/ml的抗ngal-生物素或抗tlc-生物素和1μg/ml的sulfo-标签链霉抗生物素(meso scale discovery)(每种都在pbs-0.1%t-2%bsa中稀释)温育1小时后,检测所研究的结合的试剂。在另外的洗涤步骤之后,将具有表面活性剂的msd读取缓冲液加入到每个孔中,并且使用meso scale discovery读板仪读取每个孔的电化学发光(ecl)信号。为了进行数据分析和定量,还制备了使用标准蛋白稀释液的校准曲线。
[0343]
在示例性实验中,在气管内施用后测试分子随时间的balf、标准化肺匀浆物和血浆浓度绘制于图1a和1b中。使用phoenix winnonlin 8.1版对数据进行非区室分析,并且将计算的半衰期总结于表1。数据显示在单个气管内肺给药后,在三个区室(balf、肺和血浆)的每一个中观察到了seq id no:3(hngal的脂质运载蛋白突变蛋白)和seq id no:4(htlc的脂质运载蛋白突变蛋白)的类似的pk特性(profile)。
[0344]
表1:脂质运载蛋白突变蛋白气管内施用后的pk参数
[0345][0346]
实施例2:气管内施用的脂质运载蛋白突变蛋白在健康小鼠中的药代动力学
[0347]
用大约8周龄的雄性balb/c小鼠也进行了类似的pk分析,其中使用微型喷雾器给动物以84μg/小鼠的剂量气管内施用脂质运载蛋白突变蛋白seq id no:4(htlc的脂质运载蛋白突变蛋白)和以100μg/小鼠的剂量气管内施用seq id no:3(hngal的脂质运载蛋白突变蛋白)。在1h、2h、4h、6h、24h和48小时(n=5只动物/时间点/测试分子)通过腹膜内注射戊巴比妥钠(200mg/kg体重或200μl 80mg/ml储备液)过量给药处死动物,,收集血浆、balf和肺组织用于pk分析。对于1至6小时之间的时间点,将小鼠气管内注射间隔20分钟;对于24小时和48小时的时间点,间隔5分钟注射小鼠。
[0348]
在气胸外科切除后,通过用注射器将30g针插入心房下的心脏,将约0.5ml的心脏血液抽取到含有20μl 0.5m edta的1.5ml管中。对于血浆分离,然后将血液样品在4℃下以3000
×
g离心10分钟。然后收集血浆并冷冻直至分析。
[0349]
对于balf收集,将balf收获尖端插入小鼠气管以重复注射pbs,然后将balf抽取到无菌管中至25q-300μl并标记为“balf洗液1”。将肺再洗涤7次,每次用300μl pbs,将balf收集到分开的管中作为balf洗液2-8。将balf洗液在-80℃下储存直至进一步分析。
[0350]
为了收获肺组织,将单个叶(叶1:左叶;叶2:下叶;叶3:上叶;叶4:中叶)切割、称重并在干冰上冷冻。使用tissuelyser lt装置(0iagen)在ripa缓冲液(50mm tris-hcl,ph 7.4,1%triton x-100,0.2%脱氧胆酸钠,0.2%十二烷基硫酸钠,具有完全蛋白酶抑制剂混合物)中将肺叶匀浆,并在4℃下以10000
×
g离心10分钟。收集上清液,使用bca蛋白测定试剂盒定量蛋白浓度。匀浆物样品用ripa缓冲液调节至5mg/ml的蛋白质浓度,并储存用于进一步使用(标准化肺匀浆物)。
[0351]
如实施例1所述,使用elisa测定不同区室中的药物水平。绘制balf、肺或血浆中测试分子随时间的平均浓度。示例性实验的结果示于图2a和2b。相应的pk参数总结于表2。
[0352]
数据显示,在所有三个区室——balf、肺组织和血浆中,对于seq id no:4(htlc的
dawley大鼠中大鼠后爪感觉神经介导的皮肤血管舒张的作用的评估。
[0361]
为了研究吸入的脂质运载蛋白突变蛋白的体内作用,使用皮肤血管舒张模型(zeller等人,br j pharmacol,2008),其中用单剂量的示例性脂质运载蛋白突变蛋白(seq id no:47)处理大鼠,并在刺激隐神经后测量皮肤血管舒张。
[0362]
用腹膜内(i.p.)氨基甲酸乙酯注射麻醉雄性sprague dawley大鼠(约300g体重)。将麻醉的大鼠置于体内平衡毯系统上以维持体温,经由气管切开术通气,po2、pco2&ph经由动脉血液气体分析维持(50μl血液样品)。当需要时,进行呼吸机调节。阿托品皮下给药以抑制支气管分泌。
[0363]
在最初的准备之后,经由小切口暴露一个后肢的隐神经,并且放置双极铂电极用于随后的感觉神经纤维的逆向电刺激,所述感觉神经纤维与隐神经一起延伸(神经被切割并且溴苄胺用于阻断交感神经)。在动物和暴露的后肢周围放置松散的覆盖物,以在整个测量期间保持恒定的环境温度。经由置于后爪上的激光多普勒探针测量皮肤血流。
[0364]
在神经刺激前的规定时间点,抗cgrp脂质运载蛋白突变蛋白(seq id no:47)以1mg/kg的剂量静脉内施用,以5mg/kg的剂量皮下施用,经由微型喷雾器装置以5mg/kg的剂量气管内施用,或经由微型喷雾器装置以5mg/kg的剂量与肺渗透增强剂富马酰基二酮哌嗪一起气管内施用。另外,用抗cgrp脂质运载蛋白突变蛋白(seq id no:47)以1mg/kg、2.5mg/kg、5mg/kg或10mg/kg的剂量静脉内施用,或经由微型喷雾器装置以2.5mg/kg、5mg/kg或10mg/kg的剂量气管内施用,进行测试。作为对照,还经由静脉内施用测试了参照抗cgrp抗体(seq id nos:204和205)。
[0365]
除了皮肤血流量之外,经由颈动脉导管测量平均动脉血压(map)和心率(hr)。通过将跨音速超声血流传感器(1mm i.d.,#1prb模型)置于对侧颈动脉上测量颈动脉血管阻力(map/颈动脉流量),其表明药物治疗对基线血流动力学的任何影响(即如果脂质运载蛋白突变蛋白去除内源性cgrp调节以引起血管收缩)。在施用后5分钟、30分钟、60分钟和120分钟采集血液样品,并分析药物的药代动力学。
[0366]
在最后观察点(2小时)后用过量麻醉剂对大鼠实施安乐死。
[0367]
测量的参数——hr、map、颈动脉血管阻力和激光多普勒后爪皮肤血流量——经由连接到计算机的powerlab(chart version 7,ad instruments,sydney,澳大利亚)记录。在每个实验日校准数据采集系统、cobe血压传感器和跨音速血流传感器。
[0368]
结果示于图4和5。抗cgrp脂质运载蛋白突变蛋白(seq id no:47)在抗cgrp脂质运载蛋白突变蛋白处理的动物中的血浆浓度示于图6。在抗cgrp脂质运载蛋白突变蛋白(seq id no:47)处理的动物中,大鼠后爪的背部皮肤中的皮肤血流从未处理的动物中观察到的显著降低,在给药后约5分钟时开始并持续至少2小时,这表明通过阻断cgrp而增加的血管收缩。当与0.4mg/kg富马酰基二酮哌嗪(fdkp)一起配制时,seq id no:47诱导的血管阻力的降低增强。在神经刺激后,seq id no:47的颈动脉血管阻力的最大变化与参照抗cgrp抗体(seq id nos:204和205)观察到的相当。抗cgrp脂质运载蛋白突变蛋白(seq id no:47)的血浆水平与皮肤血管舒张实验中所见的pd效应良好对应。气管内施用的脂质运载蛋白突变蛋白与皮下施用的脂质运载蛋白突变蛋白相比显示更快的起效,并且与静脉内施用的脂质运载蛋白突变蛋白或参照抗cgrp抗体相比显示相当的或甚至更快的起效。
[0369]
在缺少本文没有具体公开的任何一个或多个元件、一个或多个限制的情况下,可
onas aeruginosa atcc 27853.j prakt chem,83-87.
[0395]
24.gipp,s.,hahn,j.,taraz,k.&budzikiewicz,h.1991.zwei pyoverdine aus pseudomonas aeruginosa r.z.naturforsch,534-541.
[0396]
25.meyer,j.m.,stintzi,a.,de vos,d.,cornelis,p.,tappe,r.,taraz,k.&budzikiewicz,h.1997.use of siderophores to type pseudomonads:the three pseudomonas aeruginosa pyoverdine systems.microbiology,143(pt 1),35-43.
[0397]
26.cornelis,p.,hohnadel,d.&meyer,j.m.1989.evidence for different pyoverdine-mediated iron uptake systems among pseudomonas aeruginosa strains.infect immun,57,3491-7.
[0398]
27.zardi,l.,carnemolla,b.,siri,a.,petersen,t.e.,paolella,g.,sebastio,g.&baralle,f.e.1987.transformed human cells produce a new fibronectin isoform by preferential alternative splicing of a previously unobserved exon.embo j,6,2337-42.
[0399]
28.spriggs,m.k.1997.interleukin-17 and its receptor.j clin immunol,17,366-9.
[0400]
29.moseley,t.a.,haudenschild,d.r.,rose,l.&reddi,a.h.2003.interleukin-17 family and il-17receptors.cytokine growth factor rev,14,155-74.
[0401]
30.kawaguchi,m.,adachi,m.,oda,n.,kokubu,f.&huang,s.k.2004.il-17cytokine family.j allergy clin immunol,114,1265-73;quiz 1274.
[0402]
31.kolls,j.k.&linden,a.2004.interleukin-17 family members and inflammation.immunity,21,467-76.
[0403]
32.lubberts,e.2008.il-17/th17 targeting:on the road to prevent chronic destructive arthritis?cytokine,41,84-91.
[0404]
33.van kooten,c.,boonstra,j.g.,paape,m.e.,fossiez,f.,banchereau,j.,lebecque,s.,bruijn,j.a.,de fijter,j.w.,van es,l.a.&daha,m.r.1998.interleukin-17 activates human renal epithelial cells in vitro and is expressed during renal allograft rejection.j am soc nephrol,9,1526-34.
[0405]
34.antonysamy,m.a.,fanslow,w.c.,fu,f.,li,w.,qian,s.,troutt,a.b.&thomson,a.w.1999.evidence for a role of il-17 in organ allograft rejection:il-17 promotes the functional differentiation of dendritic cell progenitors.j immunol,162,577-84.
[0406]
35.molet,s.,hamid,q.,davoine,f.,nutku,e.,taha,r.,page,n.,olivenstein,r.,elias,j.&chakir,j.2001.il-17 is increased in asthmatic airways and induces human bronchial fibroblasts to produce cytokines.j allergy clin immunol,108,430-8.
[0407]
36.teunissen,m.b.,koomen,c.w.,de waal malefyt,r.,wierenga,e.a.&bos,j.d.1998.interleukin-17 and interferon-gamma synergize in the enhancement of proinflammatory cytokine production by human keratinocytes.j invest dermatol,111,645-9.
[0408]
37.kurasawa,k.,hirose,k.,sano,h.,endo,h.,shinkai,h.,nawata,y.,takabayashi,k.&iwamoto,i.2000.increased interleukin-17 production in patients with systemic sclerosis.arthritis rheum,43,2455-63.
[0409]
38.oppmann,b.,lesley,r.,blom,b.,timans,j.c.,xu,y.,hunte,b.,vega,f.,yu,n.,wang,j.,singh,k.,zonin,f.,vaisberg,e.,churakova,t.,liu,m.,gorman,d.,wagner,j.,zurawski,s.,liu,y.,abrams,j.s.,moore,k.w.,rennick,d.,de waal-malefyt,r.,hannum,c.,bazan,j.f.&kastelein,r.a.2000.novel p19 protein engages il-12p40 to form a cytokine,il-23,with biological activities similar as well as distinct from il-12.immunity,13,715-25.
[0410]
39.wiekowski,m.t.,leach,m.w.,evans,e.w.,sullivan,l.,chen,s.c.,vassileva,g.,bazan,j.f.,gorman,d.m.,kastelein,r.a.,narula,s.&lira,s.a.2001.ubiquitous transgenic expression of the il-23 subunit p19 induces multiorgan inflammation,runting,infertility,and premature death.j immunol,166,7563-70.
[0411]
40.frucht,d.m.2002.il-23:a cytokine that acts on memory t cells.sci stke,2002,pel.
[0412]
41.elphick,m.,von hollen,d.,pritchard,j.n.,nikander,k.,hardaker,l.e.&hatley,r.h.2015.factors to consider when selecting a nebulizer for a new inhaled drug product development program.expert opin drug deliv,12,1375-87.
[0413]
42.yum,h.k.,park,i.n.,shin,b.m.&choi,s.j.2014.recurrent pseudomonas aeruginosa infection in chronic lung diseases:relapse or reinfection?tuberc respir dis(seoul),77,172-7.
[0414]
43.arulmozhi,d.k.,veeranjaneyulu,a.&bodhankar,s.l.2005.migraine:current concepts and emerging therapies.vascul pharmacol,43,176-87.
[0415]
44.lassen,l.h.,haderslev,p.a.,jacobsen,v.b.,iversen,h.k.,sperling,b.&olesen,j.2002.cgrp may play a causative role in migraine.cephalalgia,22,54-61.
[0416]
45.haass,c.&selkoe,d.j.2007.soluble protein oligomers in neurodegeneration:lessons from the alzheimer
′
s amyloid beta-peptide.nat rev mol cell biol,8,101-12.
[0417]
46.zeller,j.,poulsen,k.t.,sutton,j.e.,abdiche,y.n.,collier,s.,chopra,r.,garcia,c.a.,pons,j.,rosenthal,a.&shelton,d.l.2008.cgrp function-blocking antibodies inhibit neurogenic vasodilatation without affecting heart rate or arterial blood pressure in the rat.br j pharmacol,155,1093-103.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1