抗CD47抗体、可活化抗CD47抗体及其使用方法与流程
抗cd47抗体、可活化抗cd47抗体及其使用方法
1.相关申请的交叉引用
2.本技术要求2019年9月23日提交的美国临时申请号62/904,534的权益,所述临时申请的内容以引用的方式整体并入本文。
发明领域
3.本发明总体上涉及特异性结合至cd47的抗体、特异性结合至cd47的可活化抗体,以及制备这些抗体和可活化抗体和在各种治疗、预防和诊断环境中使用这些抗体和可活化抗体的方法。
4.对序列表的引用
5.依据美国联邦法规(c.f.r.)第37章第1.821条,以计算机可读形式(cfr)通过efs-web作为文件名“cytx-066-pct_st25”以电子方式随函提交的“序列表”以引用的方式并入本文。序列表的电子副本创建于2020年9月23日,并且磁盘容量为197千字节。
6.发明背景
7.基于抗体的疗法已证实是若干种疾病的有效治疗,但在一些情况下,广泛的靶标表达所致的毒性限制了这些疗法的治疗有效性。此外,基于抗体的治疗剂还表现出其他局限性,如施用后从循环中快速清除。
8.在小分子治疗剂领域,已经开发出提供活性化学实体的前药的策略。此类前药以相对无活性(或活性显著较低)的形式施用。一旦施用,前药在体内代谢成活性化合物。此类前药策略可使药物对其预期靶标的选择性增强以及减少副作用。
9.因此,在基于抗体的治疗剂领域中持续需要模拟小分子前药的期望特性的抗体。
技术实现要素:
10.本文提供了结合至cd47的可活化抗体以及制备这些可活化抗体和在各种治疗、预防和诊断环境中使用这些可活化抗体的方法。在一些实施方案中,可活化抗体结合人和食蟹猴cd47。
11.在本发明的一个方面,本文提供了一种在活化状态下结合cd47的可活化抗体,所述可活化抗体包含:(a)特异性结合至人cd47和食蟹猴cd47的抗体或其抗原结合片段(ab);(b)偶合至ab的掩蔽部分(mm),其中当可活化抗体处于未裂解(未活化状态)状态时,mm抑制ab与cd47的结合,并且其中mm包含选自由seq id no:16-29组成的组的氨基酸序列;和(c)偶合至ab的可裂解部分(cm),其中cm是用作蛋白酶的底物的多肽。
12.在本文提供的另一方面,本文提供的任一种可活化抗体缀合至一种剂,产生缀合的可活化抗体。在一些实施方案中,剂为毒素或其片段。在一些实施方案中,剂为微管抑制剂。在一些实施方案中,剂为核酸损伤剂。在一些实施方案中,剂为可检测部分。在一些实施方案中,可检测部分为诊断剂。在相关方面,本文提供了一种缀合的可活化抗体,所述缀合的可活化抗体包含:在活化状态下结合cd47的抗体或其抗原结合片段(ab);以及通过接头缀合至ab的毒素,其中缀合的可活化抗体包含选自表d中单行的氨基酸序列、接头和毒素,
其中对于给定组合:(a)ab包含含有对应于表d所列单行中的给定组合的重链序列或重链可变结构域序列的氨基酸序列的重链;(b)ab包含含有对应于表d所列单行中的给定组合的轻链序列或轻链可变结构域序列的氨基酸序列的轻链;并且(c)接头和毒素包含对应于表d所列单行中的给定组合的接头和毒素。
13.在另一方面,本文提供了一种药物组合物,所述药物组合物包含本文提供的可活化抗体或缀合的可活化抗体中的任一者;和载体。在一些实施方案中,药物组合物包含另外的剂。在一些实施方案中,另外的剂为治疗剂。
14.在另一方面,本文提供了一种编码本文所述的任一种可活化抗体的分离的核酸分子。在相关方面,本文提供了一种包含分离的核酸分子的载体。在另一相关方面,本文提供了一种产生可活化抗体的方法,所述方法通过在导致所述可活化抗体表达的条件下培养细胞来进行,其中所述细胞包含本文提供的核酸分子或载体。
15.在另一方面,本文提供了一种制造在活化状态下结合cd47的本文提供的任一种可活化抗体的方法,所述方法包括:(a)在导致本文所述的任一种可活化抗体表达的条件下培养包含编码所述可活化抗体的核酸构建体的细胞,以及(b)回收所述可活化抗体。
16.在另一方面,本文提供了一种预防病变细胞表达cd47的病症或疾病或cd47介导的疾病或病症、治疗所述病症或疾病、缓解所述病症或疾病的症状、延迟所述病症或疾病的进展或以其他方式改善所述病症或疾病的方法,所述方法包括向有需要的受试者施用治疗有效量的本文提供的可活化抗体或缀合的可活化抗体中的任一者或其药物组合物。在另一方面,本文提供了一种预防与表达cd47的细胞相关的病症或疾病或cd47介导的疾病或病症、治疗所述病症或疾病、缓解所述病症或疾病的症状、延迟所述病症或疾病的进展或以其他方式改善所述病症或疾病的方法,所述方法包括向有需要的受试者施用治疗有效量的本文提供的可活化抗体或缀合的可活化抗体中的任一者或其药物组合物。在一些实施方案中,所述病症或疾病为癌症。在一些实施方案中,癌症是腺癌、胆管(胆)癌、膀胱癌、骨癌、乳腺癌、三阴性乳腺癌、her2阴性乳腺癌、类癌、宫颈癌、胆管癌、结肠直肠癌、结肠癌、子宫内膜癌、食道癌、神经胶质瘤、头颈癌、头颈鳞状细胞癌、白血病、肝癌、肺癌、非小细胞肺癌、小细胞肺癌、淋巴瘤、黑素瘤、口咽癌、卵巢癌、胰腺癌、前列腺癌、转移性去势抵抗性前列腺癌、肾癌、肉瘤、皮肤癌、鳞状细胞癌、胃癌、睾丸癌、甲状腺癌、泌尿生殖系统癌或尿路上皮癌。
17.在相关方面,本文提供了一种抑制或减少表达cd47的细胞的生长、增殖或转移的方法,所述方法包括向有需要的受试者施用治疗有效量的本文提供的可活化抗体或缀合的可活化抗体中的任一者或其药物组合物。在一些实施方案中,cd47的表达和/或活性是异常的。
18.在另一方面,本文提供了一种抑制、阻断或阻止天然配体与cd47结合的方法,所述方法包括向有需要的受试者施用治疗有效量的本文提供的可活化抗体或缀合的可活化抗体中的任一者或其药物组合物。在一些实施方案中,cd47的表达和/或活性是异常的。
19.在另一方面,本文提供了可活化抗体、缀合的可活化抗体、其药物组合物及其使用方法,其中可活化抗体或缀合的可活化抗体在与cd47结合时阻断cd47与sirpα的相互作用。
附图说明
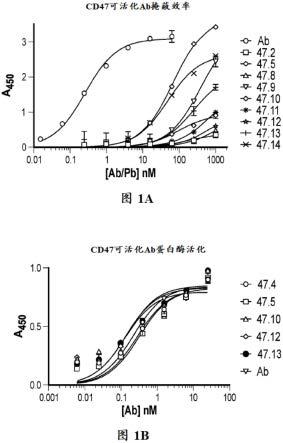
20.图1a和图1b是描绘本公开的抗人cd47可活化抗体结合人cd47抗原的能力的示例
性体外研究的图。
21.图2是描绘本公开的抗人cd47可活化抗体激活抗体依赖性细胞吞噬作用(adcp)的能力的示例性体外研究的图。
22.图3a至图3d是描绘本公开的抗人cd47抗体和抗cd47可活化抗体激活adcp的能力的示例性体外研究的图。
23.图4a至图4c是描绘本公开的抗人cd47抗体激活adcp的能力的示例性体外研究的图。
24.图5a和图5b是描绘抗人cd47抗体在小鼠异种移植模型中的体内功效的示例性研究的图。
具体实施方式
25.cd47,也称为整联蛋白相关蛋白(iap),是一种跨膜糖蛋白,属于免疫球蛋白超家族。cd47已被证明与其他细胞上的膜整联蛋白相互作用。cd47还已被证明与配体血小板反应蛋白-1(tsp-1)和信号调节蛋白α(sirpα)结合。cd47可以通过防止骨髓细胞(如巨噬细胞)消耗细胞来保护癌细胞免受免疫系统的影响。cd47已被证明在人细胞中表达并在许多肿瘤细胞中过表达。
26.阻断靶细胞上的cd47与巨噬细胞或其他吞噬细胞上的sirpα之间的相互作用可以诱导对靶细胞的吞噬作用。在一些情况下,阻断靶细胞上的cd47与巨噬细胞或其他吞噬细胞上的sirpα之间的相互作用可以诱导对靶细胞的吞噬作用以及与吞噬细胞上的fc受体的衔接合。在一些情况下,fc受体的接合可通过cd47结合抗体上的fc结构域进行。
27.cd47是理想的靶标,因为它被证明在多种癌症适应症中过表达。
28.因此,本公开提供了特异性结合哺乳动物cd47的抗体、可活化抗体、缀合的抗体和缀合的可活化抗体,其制备方法和用途。
29.更具体地说,本公开提供了抗哺乳动物cd47抗体及其片段(在本文中可互换地称为cd47抗体或ab)、缀合的cd47抗体、可活化cd47抗体和缀合的可活化cd47抗体,其可用于治疗与表达cd47的细胞相关的疾病或病症、预防所述疾病或病症、延迟所述疾病或病症的进展、改善所述疾病或病症和/或缓解所述疾病或病症的症状的方法中。在一些实施方案中,细胞与正常cd47表达和/或活性相关。在一些实施方案中,细胞与异常cd47表达和/或活性相关。在一些实施方案中,细胞与病变细胞中的cd47表达和/或活性相关。例如,本文所述的任何抗体/可活化抗体可用于治疗癌症或其他赘生性疾患、预防癌症或其他赘生性疾患、延迟癌症或其他赘生性疾患的进展、改善癌症或其他赘生性疾患和/或缓解癌症或其他赘生性疾患的症状的方法中。本文所述的任何抗体/可活化抗体也可用于检测/诊断应用。
30.在本公开的一些实施方案中,抗体和可活化抗体特异性结合人cd47和食蟹猴cd47。在一些实施方案中,抗体和可活化抗体结合人cd47。在一些实施方案中,抗体和可活化抗体结合食蟹猴cd47。在一些实施方案中,抗体和可活化抗体被含cd47的细胞内化。在一些实施方案中,抗体和可活化抗体结合cd47抗原的糖基化和去糖基化形式。
31.在本公开的一些实施方案中,抗体和可活化抗体特异性结合人cd47和食蟹猴cd47并阻断与sirpα的相互作用。在本公开的一些实施方案中,抗体和可活化抗体特异性结合人cd47和食蟹猴cd47并活化抗体依赖性细胞吞噬作用。在本公开的一些实施方案中,抗体和
可活化抗体特异性结合人cd47和食蟹猴cd47并接合fc受体途径。
32.定义:
33.除非另外定义,否则结合本公开使用的科学和技术术语应具有本领域普通技术人员通常所理解的含义。术语“一个/种(a/an)”实体是指一个/种或多个/种所述实体。例如,一种化合物是指一种或多种化合物。因此,术语“一”、“一个”、“一个或多个”和“至少一个”可互换使用。此外,除非上下文另有要求,否则单数术语应包括复数且复数术语应包括单数。一般来说,与本文所述的细胞和组织培养、分子生物学以及蛋白质和寡核苷酸或多核苷酸化学及杂交结合使用的命名法和它们的技术是本领域中众所周知且常用的那些。标准技术用于重组dna、寡核苷酸合成以及组织培养和转化(例如,电穿孔、脂转染)。酶促反应和纯化技术根据制造商的说明书或如本领域中通常所完成或如本文所述来进行。前述技术和程序通常根据本领域中众所周知的常规方法和如在整个本说明书中所引用且论述的各种一般和更具体的参考文献中所述来进行。参见例如sambrook等人molecular cloning:a laboratory manual(第2版,cold spring harbor laboratory press,cold spring harbor,n.y.(1989))。结合本文所述的分析化学、合成有机化学和医药化学所使用的命名法和这些化学领域的实验室程序和技术是本领域中众所周知且常用的那些。标准技术用于化学合成、化学分析、药物制备、配制和递送以及患者的治疗。
34.如根据本公开所用,除非另外指出,否则以下术语应理解为具有以下含义:
35.如本文所用,术语“抗体”是指免疫球蛋白分子和免疫球蛋白(ig)分子的免疫活性部分,其含有特异性结合抗原(与抗原免疫反应)的抗原结合位点的分子。“特异性结合”或“与......免疫反应”或“免疫特异性结合”意指抗体与所需抗原的一个或多个抗原决定簇反应,并且不与其他多肽反应或以低得多的亲和力结合(kd》10-6
)。抗体包括但不限于多克隆抗体、单克隆抗体、嵌合抗体、结构域抗体、单链抗体、fab和f(ab’)2片段、scfv以及fab表达文库。本文提供的抗体可以是igg、igm、iga、ige和igd类别(或其亚类)中的任一种。
36.如本文所用,术语“单克隆抗体”(mab)或“单克隆抗体组合物”是指仅含有由独特轻链基因产物和独特重链基因产物组成的抗体分子的一个分子种类的抗体分子的群体。特别地,单克隆抗体的互补决定区(cdr)在群体的所有分子中是相同的。mab含有能够与抗原的特定表位免疫反应的抗原结合位点,所述表位的特征在于针对所述抗原结合位点的独特结合亲和力。
37.术语“抗原结合位点”或“结合部分”是指免疫球蛋白分子的参与抗原结合的部分。抗原结合位点由重链(“h”)和轻链(“l”)的n末端可变(“v”)区的氨基酸残基形成。在重链和轻链的v区内三个高度相异的链段(称为“高变区”)插在称为“框架区域”或“fr”的更为保守的侧翼链段之间。因此,术语“fr”是指天然存在于免疫球蛋白中的高变区之间并且与高变区相邻的氨基酸序列。在抗体分子中,轻链的三个高变区和重链的三个高变区在三维空间中相对于彼此布置,以形成抗原结合表面。抗原结合表面与结合的抗原的三维表面互补,并且每条重链和轻链的三个高变区称为“互补决定区”或“cdr”。每个结构域的氨基酸分配是根据免疫学感兴趣的蛋白质的kabat序列的定义进行的(national institutes ofhealth,bethesda,md.(1987和1991)),或chothia和lesk j.mol.biol.196:901-917(1987),chothia等人nature342:878-883(1989)。
38.如本文所用,术语“表位”包括能够特异性结合至免疫球蛋白、scfv或t细胞受体的
任何蛋白质决定簇。术语“表位”包括能够特异性结合至免疫球蛋白或t细胞受体的任何蛋白质决定簇。表位决定簇通常由分子的化学活性表面基团(诸如氨基酸或糖侧链)组成,并且通常具有特定三维结构特征以及特定电荷特征。例如,可产生针对多肽的n末端或c末端肽的抗体。当解离常数≤1μm;在一些实施方案中≤100nm并且在一些实施方案中≤10nm时,认为抗体特异性结合抗原。
39.如本文所用,术语“特异性结合”、“免疫结合”和“免疫结合性质”是指在免疫球蛋白分子与所述免疫球蛋白对其具有特异性的抗原之间发生的类型的非共价相互作用。免疫结合相互作用的强度或亲和力可根据相互作用的解离常数(kd)来表示,其中较小的kd表示较大的亲和力。可使用本领域中众所周知的方法来定量所选择的多肽的免疫结合性质。一种此类方法需要测量抗原结合位点/抗原复合物形成和解离的速率的速率,其中那些速率取决于复合物配偶体的浓度、相互作用的亲和力以及在两个方向上同等地影响速率的几何参数。因此,可通过计算浓度以及缔合和解离的实际速率来确定“缔合速率常数”(k
on
)和“解离速率常数”(k
off
)。(参见nature 361:185-87(1993))。k
off
/k
on
的比率能够删去与亲和力无关的所有参数,并且等于解离常数kd。(通常参见davies等人(1990)annual rev biochem 59:439-473)。如通过诸如放射性配体结合测定或本领域技术人员已知的类似测定的测定所测量的,当结合常数(kd)为≤1μm,在一些实施方案中≤为100nm,在一些实施方案中≤为10nm,并且在一些实施方案中≤为100pm至约1pm时,认为本公开的抗体特异性结合至靶标。
40.如本文所用,术语“分离的多核苷酸”应意指基因组、cdna或合成来源或其某种组合的多核苷酸,所述“分离的多核苷酸”根据其来源(1)不与多核苷酸的全部或一部分缔合(其中“分离的多核苷酸”见于自然界中),(2)可操作地连接至其在自然界中不连接的多核苷酸,或(3)不作为较大序列的一部分存在于自然界中。根据本公开的多核苷酸包含编码本文所示的重链免疫球蛋白分子的核酸分子以及编码本文所示的轻链免疫球蛋白分子的核酸分子。
41.本文提及的术语“分离的蛋白质”意指cdna、重组rna或合成来源或其某种组合的蛋白质;所述“分离的蛋白质”根据其来源或衍生来源(1)不与自然界中所见的蛋白质缔合,(2)不含来自相同来源的其他蛋白质,例如不含鼠蛋白质,(3)由来自不同物种的细胞表达,或(4)不存在于自然界中。
42.术语“多肽”在本文中用作通用术语,是指具有多肽序列的天然蛋白质、片段或类似物。因此,天然蛋白质片段和类似物是多肽属的种类。根据本公开的多肽包含本文所示的重链免疫球蛋白分子和本文所示的轻链免疫球蛋白分子,以及通过包含重链免疫球蛋白分子与轻链免疫球蛋白分子的组合形成的抗体分子(诸如κ轻链免疫球蛋白分子,并且反之亦然),以及其片段和类似物。
43.如本文所用,术语“天然存在的”当应用于对象时是指对象可见于自然界中的事实。例如,可从自然界中的来源分离并且不通过人在实验室中有意修饰的存在于生物(包括病毒)中或以其他方式天然存在的多肽或多核苷酸序列为天然存在的。
44.如本文所用,术语“可操作地连接”是指所描述的组分处于容许其以预期的方式起作用的关系中。“可操作地连接”至编码序列的控制序列是以使得在与控制序列相容的条件下实现编码序列的表达的方式连接。
45.如本文所用,术语“控制序列”是指影响与它们连接的编码序列的表达和加工所必
需的多核苷酸序列。此类控制序列的性质根据宿主生物体而不同;在原核生物中,此类控制序列通常包括启动子、核糖体结合位点和转录终止序列;在真核生物中,此类控制序列通常包括启动子和转录终止序列。术语“控制序列”旨在至少包括存在对于表达和加工来说是必需的所有组分,并且还可包括存在是有利的其他组分,例如前导序列和融合配偶体序列。如本文所提及的术语“多核苷酸”是指长度至少为10个碱基的核苷酸,其为核糖核苷酸或脱氧核苷酸或任一类型核苷酸的修饰形式。所述术语包括dna的单链和双链形式。
46.本文提及的术语寡核苷酸包括通过天然存在的和非天然存在的寡核苷酸键联连接在一起的天然存在的和修饰的核苷酸。寡核苷酸是通常包含200个碱基或更少碱基的长度的多核苷酸亚群。在一些实施方案中,寡核苷酸长度为10至60个碱基,并且在一些实施方案中,长度为12个、13个、14个、15个、16个、17个、18个、19个或20个至40个碱基。寡核苷酸通常为单链的,例如用于探针,但是寡核苷酸可为双链的,例如用于构建基因突变体。本公开的寡核苷酸为有义或反义寡核苷酸。
47.本文提及的术语“天然存在的核苷酸”包括脱氧核糖核苷酸和核糖核苷酸。本文提及的术语“修饰的核苷酸”包括具有修饰的或取代的糖基的核苷酸等。本文提及的术语“寡核苷酸键联”包括诸如硫代磷酸酯、二硫代磷酸酯、硒代磷酸酯、二硒代磷酸酯、苯胺硫代磷酸酯(phosphoroanilothioate)、苯胺磷酸酯(phoshoraniladate)、氨基磷酸酯等的寡核苷酸键联。参见例如laplanche等人nucl.acids res.14:9081(1986);stec等人j.am.chem.soc.106:6077(1984),stein等人nucl.acids res.16:3209(1988),zon等人anti cancer drug design 6:539(1991);zon等人oligonucleotides and analogues:a practical approach,第87-108页(f.eckstein,编,oxford university press,oxford england(1991));stec等人美国专利号5,151,510;uhlmann and peyman chemical reviews 90:543(1990)。如果需要,寡核苷酸可包括用于检测的标记。
48.如本文所用,二十种常规氨基酸及其缩写遵循常规用法。参见immunology-asynthesis(第2版,e.s.golub和d.r.green编,sinauer associates,sunderland,mass.(1991))。二十种常规氨基酸的立体异构体(例如d-氨基酸)、非天然氨基酸(诸如α-,α-二取代的氨基酸)、n-烷基氨基酸、乳酸以及其他非常规氨基酸也可为本公开的多肽的合适的组分。非常规氨基酸的实例包括:4-羟基脯氨酸、γ-羧基谷氨酸、ε-n,n,n-三甲基赖氨酸、ε-n-乙酰赖氨酸、o-磷酸丝氨酸、n-乙酰丝氨酸、n-甲酰基甲硫氨酸、3-甲基组氨酸、5-羟基赖氨酸、σ-n-甲基精氨酸以及其他类似氨基酸和亚氨基酸(例如4-羟基脯氨酸)。在本文所用的多肽表示法中,根据标准用法和惯例,左手方向为氨基端方向,并且右手方向为羧基端方向。
49.类似地,除非另外说明,否则单链多核苷酸序列的左手端为5’端,双链多核苷酸序列的左手方向称为5’方向。初生rna转录物的5’至3’添加方向被称为转录方向,在具有与rna相同的序列的dna链上并且是5’至rna转录物的5’端的序列区域被称为“上游序列”,在具有与rna相同的序列的dna链上并且是3’至rna转录物的3’端的序列区域被称为“下游序列”。
50.当应用于多肽时,术语“实质同一性”意指当诸如通过使用默认空位权重的程序gap或bestfit进行最佳比对时,两个肽序列共享至少80%序列同一性,在一些实施方案中共享至少90%序列同一性,在一些实施方案中共享至少95%序列同一性并且在一些实施方
案中共享至少99%序列同一性。
51.在一些实施方案中,不相同的残基位置因保守氨基酸取代而不同。
52.如本文所论述,设想的是本公开涵盖抗体或免疫球蛋白分子的氨基酸序列中的微小变化,条件是氨基酸序列中的变化保持至少75%,在一些实施方案中保持至少80%、90%、95%,并且在一些实施方案中保持99%。特别地,设想保守性氨基酸置换。保守性置换是发生在侧链相关的氨基酸家族内的置换。基因编码的氨基酸一般分为以下家族:(1)酸性氨基酸是天冬氨酸、谷氨酸;(2)碱性氨基酸是赖氨酸、精氨酸、组氨酸;(3)非极性氨基酸是丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、蛋氨酸、色氨酸,以及(4)不带电极性氨基酸是甘氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、丝氨酸、苏氨酸、酪氨酸。亲水性氨基酸包括精氨酸、天冬酰胺、天冬氨酸、谷氨酰胺、谷氨酸、组氨酸、赖氨酸、丝氨酸和苏氨酸。疏水性氨基酸包括丙氨酸、半胱氨酸、异亮氨酸、亮氨酸、甲硫氨酸、苯丙氨酸、脯氨酸、色氨酸、酪氨酸和缬氨酸。其他氨基酸家族包括:(i)丝氨酸和苏氨酸,其为脂肪族羟基家族;(ii)天冬酰胺和谷氨酰胺,其为含有酰胺的家族;(iii)丙氨酸、缬氨酸、亮氨酸和异亮氨酸,其为脂肪族家族;和(iv)苯丙氨酸、色氨酸和酪氨酸,其为芳香族家族。例如,可合理地预期,用异亮氨酸或缬氨酸独立置换亮氨酸,用谷氨酸独立置换天冬氨酸,用丝氨酸独立置换苏氨酸或用结构相关氨基酸类似置换氨基酸对所得分子的结合或特性将不具有重大影响,尤其在置换不涉及在框架位点内的氨基酸的情况下。氨基酸改变是否产生功能性肽可通过测定多肽衍生物的比活性来容易地确定。本文详细描述了测定。本领域普通技术人员可容易地制备抗体或免疫球蛋白分子的片段类似物。片段或类似物的合适的氨基末端和羧基末端出现在功能域的边界附近。可通过将核苷酸和/或氨基酸序列数据与公共或专有序列数据库进行比较来鉴别结构域和功能域。在一些实施方案中,计算机化的比较方法用于鉴别在具有已知结构和/或功能的其他蛋白质中出现的序列基序或预测的蛋白质构象结构域。鉴别折叠成已知三维结构的蛋白质序列的方法是已知的。bowie等人science 253:164(1991)。因此,前述实例证明,根据本公开,本领域技术人员可识别可用于定义结构和功能结构域的序列基序和结构构象。
53.合适的氨基酸取代是以下的那些:(1)降低对蛋白水解的易感性,(2)降低对氧化的易感性,(3)改变用于形成蛋白质复合物的结合亲和力,(4)改变结合亲和力,以及(5)赋予或修饰此类类似物的其他物理化学或功能性质。类似物可包括具有除了天然存在的肽序列以外的序列的各种突变蛋白。例如,单个或多个氨基酸取代(例如保守性氨基酸取代)可在天然存在的序列中(例如,在形成分子间接触的一个或多个结构域外部的多肽部分中)进行。保守性氨基酸取代不应实质上改变亲本序列的结构特征(例如,氨基酸置换不应倾向于破坏亲本序列中存在的螺旋,或破坏表征亲本序列的其他类型的二级结构)。本领域公认的多肽二级结构和三级结构的实例描述于proteins,structures and molecular principles(creighton编,w.h.freeman and company,new york(1984));introduction to protein structure(c.branden和j.tooze编,garland publishing,new york,n.y.(1991));以及thornton等人nature 354:105(1991)。
54.如本文所用,术语“多肽片段”是指如下多肽,其具有氨基端和/或羧基端缺失和/或一个或多个内部缺失,但是其中剩余的氨基酸序列与例如从全长cdna序列推导的天然存在的序列中的相应位置相同。片段长度通常为至少5、6、8或10个氨基酸,在一些实施方案中
长度至少14个氨基酸,在一些实施方案中长度至少20个氨基酸,通常长度至少50个氨基酸,并且在一些实施方案中长度至少70个氨基酸。如本文所用,术语“类似物”是指由至少25个氨基酸的区段组成的多肽,所述区段与推导的氨基酸序列的一部分具有实质同一性并且在合适的结合条件下与靶标具有特异性结合。通常,多肽类似物相对于天然存在的序列包含保守性氨基酸取代(或添加或缺失)。类似物长度通常为至少20个氨基酸,在一些实施方案中长度至少50个氨基酸或更长,并且经常可与全长天然存在的多肽一样长。
55.术语“剂”在本文中用于表示化学化合物、化学化合物的混合物、生物大分子或由生物材料制成的提取物。
56.如本文所用,术语“标记”或“标记的”是指并入可检测的标志物,例如通过并入放射性标记的氨基酸或附接至具有可通过标记的亲和素(例如,含有可通过光学方法或比色方法检测的荧光标志物或酶促活性的链霉亲和素)检测的生物素基部分的多肽。在某些情况下,标记或标志物也可为治疗性的。标记多肽和糖蛋白的各种方法是本领域中已知的并且可使用。用于多肽的标记的实例包括但不限于以下:放射性同位素或放射性核素(例如,3h、
14
c、
15
n、
35
s、
90
y、
99
tc、
111
in、
125
i、
131
i)、荧光标记(例如,fitc、罗丹明、镧系元素磷光体)、酶标记(例如,辣根过氧化物酶、p-半乳糖苷酶、荧光素酶、碱性磷酸酶)、化学发光、生物素基团、由二级报告分子识别的预定多肽表位(例如,亮氨酸拉链对序列、二级抗体的结合位点、金属结合结构域、表位标签)。在一些实施方案中,标记通过具有各种长度的间隔臂附接以降低潜在的空间位阻。如本文所用,术语“药剂或药物”是指当适当施用于患者时能够诱导所需治疗作用的化合物或组合物。
57.本文中的其他化学术语根据本领域中的常规用法使用,如由the mcgraw-hill dictionary of chemical terms(parker,s.编,mcgraw-hill,san francisco(1985))所例示。
58.如本文所用,“基本上纯的”意指目标种类是存在的主要种类(即,在摩尔基础上它比组合物中的任何其他单独种类更丰富),并且在一些实施方案中,基本上纯化的级分是其中目标种类占存在的所有大分子种类的至少约50%(在摩尔基础上)的组合物。
59.一般来说,基本上纯的组合物将占组合物中存在的所有大分子种类的大于约80%,在一些实施方案中大于约85%、90%、95%和99%。在一些实施方案中,目标种类被纯化至必要的均质性(通过常规的检测方法不能检测到组合物中的污染物种类),其中组合物基本上由单一大分子种类组成。
60.术语患者包括人和兽医受试者。
61.cd47抗体
62.本文提供了特异性结合至哺乳动物cd47的抗体及其抗原结合片段(ab)。在一些实施方案中,ab特异性结合人cd47和食蟹猴cd47。
63.本文提供的结合cd47的ab包括单克隆抗体、结构域抗体、单链抗体、fab片段、f(ab’)2片段、scfv、scab、dab、单结构域重链抗体或单结构域轻链抗体。在一些实施方案中,此种结合cd47的ab为小鼠抗体、其他啮齿动物抗体、嵌合抗体、人源化抗体或完全人单克隆抗体。
64.本文还提供了可活化cd47抗体,其包括特异性结合cd47的抗体或其抗原结合片段(ab),所述ab偶合至掩蔽部分(mm),使得mm的偶合降低抗体或其抗原结合片段结合cd47的
能力。在一些实施方案中,所述mm经由包含蛋白酶的底物(可裂解部分,cm)的序列偶合,所述蛋白酶例如是与cd47共定位在受试者的治疗部位的蛋白酶。(本公开的可活化cd47抗体在以下部分中更详细地描述)。
65.本公开的cd47抗体特异性结合哺乳动物cd47靶标,例如像人cd47。本公开中还包括结合至与本公开的抗体和/或本文所述的活化的可活化抗体相同的cd47表位的cd47抗体和ab。本公开中还包括与本文所述的cd47抗体竞争结合至cd47靶标例如人cd47的cd47抗体。本公开中还包括与本文所述的cd47抗体和/或活化的cd47可活化抗体交叉竞争结合至cd47靶标例如人cd47(抑制其结合cd47靶标)的cd47抗体。
66.本公开的抗体和/或可活化抗体特异性结合哺乳动物cd47,例如人cd47和食蟹猴cd47。本公开中还包括与本文所述的任何抗体和/或可活化抗体结合至相同的表位的抗体和/或可活化抗体。本公开中还包括与本文所述的cd47抗体和/或cd47可活化抗体竞争结合至cd47例如人cd47(抑制其结合cd47)的抗体和/或抗体可活化抗体。本公开中还包括与本文所述的cd47抗体和/或cd47可活化抗体交叉竞争结合至cd47例如人cd47(抑制其结合cd47)的抗体和/或抗体可活化抗体。
67.在一些实施方案中,哺乳动物cd47选自由人cd47、鼠cd47、大鼠cd47和食蟹猴cd47组成的组。在一些实施方案中,ab以小于1nm的解离常数特异性地结合至人cd47、鼠cd47或食蟹猴cd47。在一些实施方案中,哺乳动物cd47是人cd47。
68.在一些实施方案中,ab具有以下特征中的一个或多个:(a)ab特异性结合至人cd47;(b)ab特异性结合至人cd47和食蟹猴cd47。
69.在一些实施方案中,ab具有以下特征中的一个或多个:(a)ab特异性结合人cd47和食蟹猕猴cd47;(b)ab抑制cd47的一种或多种天然哺乳动物配体与哺乳动物cd47的结合;(c)ab抑制cd47的一种或多种天然人配体与人cd47的结合;以及(d)ab抑制cd47的一种或多种天然食蟹猴配体与食蟹猴cd47的结合。
70.在一些实施方案中,ab结合cd47的糖基化和去糖基化形式。
71.在一些实施方案中,ab以小于或等于5nm、小于或等于10nm、小于或等于50nm、小于或等于等于100nm、小于或等于500nm和/或小于或等于1000nm的ec
50
阻断天然配体结合至哺乳动物cd47的能力。在一些实施方案中,ab以小于或等于5nm、小于或等于10nm、小于或等于50nm、小于或等于等于100nm、小于或等于500nm和/或小于或等于1000nm的ec
50
阻断天然配体结合至哺乳动物cd47的能力。
72.在一些实施方案中,ab以5nm至1000nm、5nm至500nm、5nm至100nm 5nm至50nm、5nm至10nm、10nm至1000nm、10nm至500nm、10nm至100nm 10nm至50nm、50nm至1000nm、50nm至500nm、50nm至100nm、100nm至1000nm、100nm至500nm、500nm至1000nm的ec
50
阻断天然配体结合至哺乳动物cd47的能力。在一些实施方案中,ab以5nm至1000nm、5nm至500nm、5nm至100nm 5nm至50nm、5nm至10nm、10nm至1000nm、10nm至500nm、10nm至100nm 10nm至50nm、50nm至1000nm、50nm至500nm、50nm至100nm、100nm至1000nm、100nm至500nm、500nm至1000nm的ec
50
阻断天然配体结合至哺乳动物cd47的能力。
73.在一些实施方案中,本公开的ab抑制或减少表达哺乳动物cd47的细胞的生长、增殖和/或转移。在不希望受任何理论束缚的情况下,本公开的ab可通过特异性结合至cd47并且抑制、阻断和/或防止天然配体与哺乳动物cd47的结合而抑制或减少表达哺乳动物cd47
的细胞的生长、增殖和/或转移。
74.在一些实施方案中,ab与哺乳动物cd47结合的解离常数为约100nm或更低。在一些实施方案中,ab与哺乳动物cd47结合的解离常数为约10nm或更低。在一些实施方案中,ab与cd47结合的解离常数为约5nm或更低。在一些实施方案中,ab与cd47结合的解离常数为约1nm或更低。在一些实施方案中,ab与cd47结合的解离常数为约0.5nm或更低。在一些实施方案中,ab与cd47结合的解离常数为约0.1nm或更低。在一些实施方案中,ab与哺乳动物cd47结合的解离常数为0.01nm至100nm、0.01nm至10nm、0.01nm至5nm、0.01nm至1nm、0.01至0.5nm、0.01nm至0.1nm、0.01nm至0.05nm、0.05nm至100nm、0.05nm至10nm、0.05nm至5nm、0.05nm至1nm、0.05至0.5nm、0.05nm至0.1nm、0.1nm至100nm、0.1nm至10nm、0.1nm至5nm、0.1nm至1nm、0.1至0.5nm、0.5nm至100nm、0.5nm至10nm、0.5nm至5nm、0.5nm至1nm、1nm至100nm、1nm至10nm、1nm至5nm、5nm至100nm、5nm至10nm或10nm至100nm。
75.本发明的示例性cd47抗体和可活化cd47抗体可包括为或源自以下所示的重链可变序列和轻链可变序列的重链和轻链(cdr序列以粗体和下划线显示):
76.hu h4l2 h4 vh:
77.qvqlvqsgaevkkpgssvklsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgratltvdkststaymelsslrsedtavyycarggvggmdywgqgtlvtvss(seq id no:1)
78.hu h4l2 l2 vl:
79.dvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik(seq id no:2)
80.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含seq id no:1和57-59中任一者的重链可变区氨基酸序列。
81.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含seq id no:2和76-79中任一者的轻链可变区氨基酸序列。
82.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含seq id no:1的重链可变区氨基酸序列。
83.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含seq id no:2的轻链可变区氨基酸序列。
84.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。
85.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含与seq id no:1的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的重链可变区氨基酸序列。
86.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含与seq id no:2的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的轻链可变区氨基酸序列。
87.在一些实施方案中,cd47抗体/可活化抗体的抗体或其抗原结合片段包含与seq id no:1的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的重链可变区氨基酸序列,和与seq id no:2的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的轻链可变区氨基酸序列。
88.本发明的示例性cd47抗体和可活化抗cd47抗体包括以下的组合:可变重链互补决定区1(vh cdr1,在本文中也称为cdrh1)序列、可变重链互补决定区2(vh cdr2,在本文中也称为cdrh2)序列、可变重链互补决定区3(vh cdr3,在本文中也称为cdrh3)序列、可变轻链互补决定区1(vl cdr1,在本文中也称为cdrl1)序列、可变轻链互补决定区2(vl cdr2,在本文中也称为cdrl2)序列和可变轻链互补决定区3(vl cdr3,在本文中也称为cdrl3)序列,其中至少一个cdr序列选自由以下组成的组:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸序列ridpydvethyaqkfqg(seq id no:6)或氨基酸序列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
89.在一些实施方案中,cd47抗体或其抗原结合片段包含以下的组合:vh cdr1序列、vh cdr2序列、vh cdr3序列、vl cdr1序列、vl cdr2序列和vl cdr3序列,其中至少一个cdr序列选自由以下组成的组:包括与包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr1序列;包括与包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr2序列;包括与包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr3序列;包括与包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr1序列;包括与包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr2序列;以及包括与包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr3序列。
90.在一些实施方案中,cd47抗体或其抗原结合片段包含以下的组合:vh cdr1序列、vh cdr2序列、vh cdr3序列、vl cdr1序列、vl cdr2序列和vl cdr3序列,包括:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
91.在一些实施方案中,cd47抗体或其抗原结合片段包含含有以下的氨基酸序列:包含氨基酸序列gytftny(seq id no:3)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
92.在一些实施方案中,cd47抗体或其抗原结合片段包含含有以下的氨基酸序列:包含氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列ridpydvethyaqkfqg(seq id no:6)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
93.在一些实施方案中,cd47抗体或其抗原结合片段包含以下的组合:vh cdr1序列、vh cdr2序列、vh cdr3序列、vl cdr1序列、vl cdr2序列和vl cdr3序列,包括:包括与包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr1序列;包括与包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr2序列;包括与包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr3序列;包括与包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr1序列;包括与包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr2序列;以及包括与包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr3序列。
94.本公开的合适的cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含seq id no:1和57-59中任一者的重链可变区氨基酸序列和seq id no:2和76-79中任一者的轻链可变区氨基酸序列的cd47抗体结合至人cd47和/或食蟹猴cd47上的相同表位。
95.本公开的合适的cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含重链可变区氨基酸序列seq id no:1和轻链可变区氨基酸序列seq id no:2的cd47抗体结合至人cd47和/或食蟹猴cd47上的相同表位。
96.本公开的合适的cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含以下的cd47抗体结合至人cd47和/或食蟹猴cd47上的相同表位:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)
的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
97.本公开的合适的cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含seq id no:1和57-59中任一者的重链可变区氨基酸序列和seq id no:2和76-79中任一者的轻链可变区氨基酸序列的cd47抗体交叉竞争结合至人cd47和/或食蟹猴cd47(抑制其结合cd47)。
98.本公开的合适的cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含重链可变区氨基酸序列seq id no:1和轻链可变区氨基酸序列seq id no:2的cd47抗体交叉竞争结合至人cd47和/或食蟹猴cd47(抑制其结合cd47)。
99.本公开的合适的cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含以下的cd47抗体交叉竞争结合至人cd47和/或食蟹猴cd47(抑制其结合cd47):包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
100.在一些实施方案中,本公开的cd47抗体包含特异性结合至哺乳动物cd47的分离的抗体或其抗原结合片段(ab),其中ab特异性结合人cd47和食蟹猴cd47。在一些实施方案中,所述抗体或其抗原结合片段包含:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,抗体或其抗原结合片段包含含有seq id no:1的氨基酸序列的重链可变区和含有seq id no:2的氨基酸序列的轻链可变区。
101.在一些实施方案中,分离的抗体或其抗原结合片段与包含以下的分离的抗体结合至人cd47和/或食蟹猴cd47上的相同表位:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt
(seq id no:10)的vl cdr3序列。在一些实施方案中,抗体或其抗原结合片段包含含有seq id no:1的氨基酸序列的重链可变区和含有seq id no:2的氨基酸序列的轻链可变区。
102.在一些实施方案中,分离的抗体或其抗原结合片段与包含以下的分离的抗体交叉竞争(抑制其结合):包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;以及包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,抗体或其抗原结合片段包含含有seq id no:1的氨基酸序列的重链可变区和含有seq id no:2的氨基酸序列的轻链可变区。
103.在一些实施方案中,cd47抗体/可活化cd47抗体包含或源自由杂交瘤制造、分泌或以其他方式产生的抗体,所述杂交瘤例如像美国专利号5,330,896中公开并以保藏号hb 8214保藏在atcc的杂交瘤。
104.在一些实施方案中,cd47抗体/可活化cd47抗体包含或源自由杂交瘤制造、分泌或以其他方式产生的抗体,所述杂交瘤例如像在美国专利号7,736,647中公开并于2005年6月14日以编号cncm i-3449保藏在collection nationale de cultures de microorganismes(cncm)(institut pasteur,paris,france,25,rue du docteur roux,f-75724,paris,cedex 15)的命名为ba120的杂交瘤;在美国专利号7,572,895中公开并以pta-6055保藏在atcc的杂交瘤;在pct公布号wo 2014/020140和wo 2005/111082中公开并于2001年5月10日以编号1-2665保藏在cncm的杂交瘤;在美国专利号4,434,156中公开并以hb-8094保藏在atcc的杂交瘤;在美国专利号5,648,469中公开并以hb-1161和hb-1160保藏在atcc的杂交瘤。
105.在一些实施方案中,cd47抗体/可活化cd47抗体包括重链,所述重链包含或源自美国pct公布号wo 2014/144060、wo 2014/189973、wo 2014/020140;美国专利号8,663,598、8,129,503、7,736,647、7,572,895、4,434,156;美国专利申请公布号us2014114054、us20140212423、us2013177579、us2013045206、us20130216476、us20120282176和/或中国专利号cn16245107b中所示的重链氨基酸序列,每个专利的内容通过引用的方式整体并入本文。
106.本公开还提供了用于通过在导致抗体或其片段表达的条件下培养细胞来产生本公开的cd47 ab的方法,其中所述细胞包含本公开的核酸分子或本公开的载体。
107.在一些实施方案中,cd47抗体或其抗原结合片段由包含编码重链可变区氨基酸序列的核酸序列的核酸序列编码,所述重链可变区氨基酸序列包含seq id no:1的氨基酸序列。在一些实施方案中,抗体或其抗原结合片段由包含编码重链氨基酸序列的核酸序列的核酸序列编码,所述重链氨基酸序列包含选自由seq id no:11-14组成的组的氨基酸序列。
108.在一些实施方案中,cd47抗体或其抗原结合片段由包含编码轻链可变区氨基酸序列的核酸序列的核酸序列编码,所述轻链可变区氨基酸序列包含选自由seq id no:2组成的组的氨基酸序列。在一些实施方案中,抗体或其抗原结合片段由包含编码轻链氨基酸序
列的核酸序列的核酸序列编码,所述轻链氨基酸序列包含seq id no:15的氨基酸序列。
109.在一些实施方案中,cd47抗体或其抗原结合片段由包含与编码重链可变区氨基酸序列的核酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%同一的核酸序列的核酸序列编码,所述重链可变区氨基酸序列包含seq id no:1的氨基酸序列。在一些实施方案中,抗体或其抗原结合片段由包含与编码重链氨基酸序列的核酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%同一的核酸序列的核酸序列编码,所述重链氨基酸序列包含选自由seq id no:11-14组成的组的氨基酸序列。
110.在一些实施方案中,cd47抗体或其抗原结合片段由包含与编码轻链可变区氨基酸序列的核酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%同一的核酸序列的核酸序列编码,所述轻链可变区氨基酸序列包含选自由seq id no:2组成的组的氨基酸序列。在一些实施方案中,抗体或其抗原结合片段由包含与编码轻链氨基酸序列的核酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%同一的核酸序列的核酸序列编码,所述轻链氨基酸序列包含seq id no:15的氨基酸序列。
111.可活化cd47抗体
112.如上文所述,本公开还提供了可活化抗体,其包括特异性结合cd47的抗体或其抗原结合片段,所述抗体或其抗原结合片段偶合至掩蔽部分(mm),使得mm的偶合降低抗体或其抗原结合片段结合cd47的能力。在一些实施方案中,所述mm经由包含蛋白酶的底物(cm,可裂解部分)的序列偶合,所述蛋白酶例如是在病变组织中有活性的蛋白酶和/或与cd47共定位在受试者的治疗部位的蛋白酶。本文提供的可活化cd47抗体在循环中稳定,在治疗和/或诊断的预期部位活化,但在正常例如健康组织或未靶向治疗和/或诊断的其他组织中不稳定,并且在活化时表现出与相应的未修饰抗体(在本文中也称为亲本抗体)至少相当的与cd47的结合。
113.本文所述的可活化cd47抗体克服了抗体治疗剂的限制,特别是已知在体内至少具有某种程度的毒性的抗体治疗剂。靶标介导的毒性构成了开发治疗性抗体的主要限制。本文提供的可活化cd47抗体旨在解决与传统治疗性抗体在正常组织中抑制靶标相关的毒性。这些可活化cd47抗体一直被掩蔽,直到在疾病部位被蛋白水解活化。从作为亲本治疗性抗体的cd47抗体开始,本发明的可活化cd47抗体是通过将抗体与抑制性掩蔽物通过结合了蛋白酶底物的接头偶合而设计的。
114.如本文所用,术语可活化抗体的裂解状态是指在通过至少一种蛋白酶修饰cm后可活化抗体的状况。如本文所用,术语未裂解状态是指在不存在蛋白酶对cm的裂解的情况下可活化抗体的状况。如上所述,术语“可活化抗体”在本文中用于指在其未裂解(天然)状态下以及在其裂解状态下的可活化抗体。对于普通技术人员而言显而易见的是,在一些实施方案中,裂解的可活化抗体可由于蛋白酶对cm的裂解而缺乏mm,从而导致至少mm的释放(例如,其中所述mm未通过共价键(例如,半胱氨酸残基之间的二硫键)连接至可活化抗体)。
115.可活化的或可转换的意指当处于受抑制、掩蔽或未裂解状态(即第一构象)时,可活化抗体表现出与靶标的第一结合水平,并且当可活化抗体处于未受抑制、无掩蔽和/或裂解状态(即第二构象)时,可活化抗体表现出与靶标的第二结合水平,其中第二靶标结合水平大于第一结合水平。一般来说,靶标对可活化抗体的ab的接近在存在能够裂解cm的裂解剂即蛋白酶的情况下比在不存在这种裂解剂的情况下更大。因此,当可活化抗体处于未裂
解状态时,ab与靶标的结合受到抑制并且其靶标结合可受到掩蔽(即,第一构象使得ab不能结合靶标),并且在裂解状态下,ab不受抑制或对靶标结合无掩蔽。
116.选择可活化抗体的cm和ab以使得ab代表给定靶标的结合部分,并且cm代表蛋白酶的底物。在一些实施方案中,蛋白酶与靶标共定位在受试者的治疗部位或诊断部位。如本文所用,共定位是指在相同位置或相对紧密邻近。在一些实施方案中,蛋白酶裂解cm,从而产生结合至位于裂解位点附近的靶标的活化的抗体。本文公开的可活化抗体具有特殊用途,其中例如,能够裂解cm中的位点的蛋白酶(即蛋白酶)在治疗部位或诊断部位的含靶标组织中以比非治疗部位的组织中(例如在健康组织中)相对更高的水平存在。在一些实施方案中,本公开的cm还通过一种或多种其他蛋白酶裂解。在一些实施方案中,正是一种或多种其他蛋白酶与靶标共定位并且在体内负责cm的裂解。
117.在一些实施方案中,如果ab与靶标的结合未被掩蔽或以其他方式抑制,则可活化抗体提供降低的另外可由ab在非治疗位点的结合引起的毒性和/或不良副作用。
118.一般来说,可通过选择目标ab(诸如本文所述的任何cd47抗体或其片段)并构建可活化抗体的剩余部分来设计可活化抗体,以便在构象受限时,mm可掩蔽ab或减少ab与其靶标的结合。可考虑结构设计标准以提供此功能特征。
119.提供了在受抑制的构象对比未受抑制的构象中表现出靶标结合的所需动态范围的可转换表型的可活化抗体。动态范围通常是指(a)在第一组条件下参数的最大检测水平与(b)在第二组条件下参数的最小检测值的比率。例如,在可活化抗体的情况下,动态范围是指(a)在至少一种能够裂解可活化抗体的cm的蛋白酶存在下,靶蛋白与可活化抗体的结合的最大检测水平与(b)在所述蛋白酶不存在下靶蛋白与可活化抗体的结合的最低检测水平的比率。可活化抗体的动态范围可计算为可活化抗体裂解剂(例如,酶)处理的解离常数与可活化抗体裂解剂处理的解离常数的比率。可活化抗体的动态范围越大,可活化抗体的可转换表型就越好。具有相对较高的动态范围值(例如,大于1)的可活化抗体表现出更期望的转换表型,使得在存在能够裂解可活化抗体的cm的裂解剂(例如,酶)的情况下与不存在裂解剂的情况相比,由可活化抗体进行的靶蛋白结合发生的程度更大(例如,主要发生)。
120.如上文所述,本文提供的可活化cd47抗体包含掩蔽部分(mm)。在一些实施方案中,掩蔽部分是偶合或以其他方式连接至cd47抗体并且位于可活化cd47抗体构建体内、以使得所述掩蔽部分降低所述cd47抗体特异性地结合cd47的能力的氨基酸序列。使用多种已知技术中的任一种来鉴定合适的掩蔽部分。例如,使用daugherty等人的pct公布号wo 2009/025846中描述的方法来鉴定肽掩蔽部分,所述专利的内容特此以引用的方式整体并入。
121.如上文所述,本文提供的可活化cd47抗体包含可裂解部分(cm)。在一些实施方案中,所述可裂解部分包含氨基酸序列,所述氨基酸序列是蛋白酶(通常是细胞外蛋白酶)的底物。使用多种已知技术中的任一种来鉴定合适的底物。例如,使用在以下专利中描述的方法来鉴定肽底物:daugherty等人的美国专利号7,666,817;stagliano等人的美国专利号8,563,269;la porte等人的pct公布号wo 2014/026136,所述专利各自的内容以引用的当时整体并入本文。(另见boulware等人“evolutionary optimization of peptide substrates for proteases that exhibit rapid hydrolysis kinetics.”biotechnol bioeng.106.3(2010):339-46)。
122.示例性底物包括但不限于可被表a中所列的以下一种或多种酶或蛋白酶裂解的底
物。
123.表a:示例性蛋白酶和/或酶
124.[0125][0126]
处于活化状态的可活化抗体结合cd47,并且包括:(i)特异性结合至cd47的抗体或其抗原结合片段(ab);(ii)当可活化抗体处于未裂解状态时抑制ab与cd47的结合的掩蔽部分(mm);和(c)偶合至ab的可裂解部分(cm),其中cm是用作蛋白酶的底物的多肽。
[0127]
在一些实施方案中,处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:mm-cm-ab或ab-cm-mm。
[0128]
在一些实施方案中,可活化抗体包含mm与cm之间的连接肽。
[0129]
在一些实施方案中,可活化抗体包含cm与ab之间的连接肽。
[0130]
在一些实施方案中,可活化抗体包含第一连接肽(lp1)和第二连接肽(lp2),并且其中处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:mm-lp1-cm-lp2-ab或ab-lp2-cm-lp1-mm。在一些实施方案中,两个连接肽不需要彼此相同。
[0131]
在一些实施方案中,lp1或lp2中的至少一个包含选自由以下组成的组的氨基酸序列:(gs)n、(ggs)n、(gsggs)n(seq id no:116)和(gggs)n(seq id no:117),其中n为至少1的整数。
[0132]
在一些实施方案中,lp1或lp2中的至少一个包含选自由以下组成的组的氨基酸序列:ggsg(seq id no:118)、ggsgg(seq id no:119)、gsgsg(seq id no:120)、gsggg(seq id no:121)、gggsg(seq id no:122)、and gsssg(seq id no:123)。
[0133]
在一些实施方案中,lp1包含氨基酸序列gssggsggsggsg(seq id no:124)、gssggsggsgg(seq id no:125)、gssggsggsggs(seq id no:126)、gssggsggsggsgggs(seq id no:127)、gssggsggsg(seq id no:128)、gssggsggsgs(seq id no:129)或gggssggs(seq id no:134)。
[0134]
在一些实施方案中,lp2包含氨基酸序列gss、ggs、gggs(seq id no:130)、gssgt(seq id no:131)或gssg(seq id no:132)。
[0135]
在一些实施方案中,结合cd47的抗体或其抗原结合片段为单克隆抗体、结构域抗体、单链、fab片段、f(ab’)2片段、scfv、scab、dab、单结构域重链抗体或单结构域轻链抗体。在一些实施方案中,此种结合cd47的抗体或其抗原结合片段为小鼠抗体、其他啮齿动物抗体、嵌合抗体、人源化抗体或完全人单克隆抗体。
[0136]
在一些实施方案中,处于未裂解状态的可活化抗体以小于或等于1nm、小于或等于5nm、小于或等于10nm、小于或等于15nm、小于或等于20nm、小于或等于25nm、小于或等于50nm、小于或等于100nm、小于或等于150nm、小于或等于250nm、小于或等于500nm、小于或等于750nm、小于或等于1000nm和/或小于或等于2000nm的解离常数特异性地结合至哺乳动物cd47。
[0137]
在一些实施方案中,处于未裂解状态的可活化抗体以在1nm至2000nm、1nm至1000nm、1nm至750nm、1nm至500nm、1nm至250nm、1nm至150nm、1nm至100nm、1nm至50nm、1nm至25nm、1nm至15nm、1nm至10nm、1nm至5nm、5nm至2000nm、5nm至1000nm、5nm至750nm、5nm至500nm、5nm至250nm、5nm至150nm、5nm至100nm、5nm至50nm、5nm至25nm、5nm至15nm、5nm至10nm、10nm至2000nm、10nm至1000nm、10nm至750nm、10nm至500nm、10nm至250nm、10nm至150nm、10nm至100nm、10nm至50nm、10nm至25nm、10nm至15nm、15nm至2000nm、15nm至1000nm、15nm至750nm、15nm至500nm、15nm至250nm、15nm至150nm、15nm至100nm、15nm至50nm、15nm至25nm、25nm至2000nm、25nm至1000nm、25nm至750nm、25nm至500nm、25nm至250nm、25nm至150nm、25nm至100nm、25nm至50nm、50nm至2000nm、50nm至1000nm、50nm至750nm、50nm至500nm、50nm至250nm、50nm至150nm、50nm至100nm、100nm至2000nm、100nm至1000nm、100nm至750nm、100nm至500nm、100nm至250nm、100nm至150nm、150nm至2000nm、150nm至1000nm、150nm至750nm、150nm至500nm、150nm至250nm、250nm至2000nm、250nm至1000nm、250nm至750nm、250nm至500nm、500nm至2000nm、500nm至1000nm、500nm至750nm、500nm至500nm、500nm至250nm、500nm至150nm、500nm至100nm、500nm至50nm、750nm至2000nm、750nm至1000nm或1000nm至2000nm范围内的解离常数特异性地结合至哺乳动物cd47。
[0138]
在一些实施方案中,处于活化状态的可活化抗体以小于或等于0.01nm、0.05nm、0.1nm、0.5nm、1nm、5nm或10nm的解离常数特异性地结合至哺乳动物cd47。
[0139]
在一些实施方案中,处于活化状态的可活化抗体以在0.01nm至100nm、0.01nm至10nm、0.01nm至5nm、0.01nm至1nm、0.01至0.5nm、0.01nm至0.1nm、0.01nm至0.05nm、0.05nm至100nm、0.05nm至10nm、0.05nm至5nm、0.05nm至1nm、0.05至0.5nm、0.05nm至0.1nm、0.1nm至100nm、0.1nm至10nm、0.1nm至5nm、0.1nm至1nm、0.1至0.5nm、0.5nm至100nm、0.5nm至10nm、0.5nm至5nm、0.5nm至1nm、1nm至100nm、1nm至10nm、1nm至5nm、5nm至100nm、5nm至10nm或10nm至100nm范围内的解离常数特异性地结合至哺乳动物cd47。
[0140]
与未用mm修饰的ab的特异性结合或亲本ab与靶标的特异性结合相比,当用mm修饰ab且在存在靶标时,ab与其靶标的特异性结合降低或受到抑制。
[0141]
用mm修饰的ab针对cd47靶标的kd比未用mm修饰的ab或亲本ab针对cd47靶标的kd大至少5、10、25、50、100、250、500、1,000、2,500、5,000、10,000、50,000、100,000、500,000、1,000,000、5,000,000、10,000,000、50,000,000倍或更多倍,或在5-10倍、10-100倍、10-1,
000倍、10-10,000倍、10-100,000倍、10-1,000,000倍、10-10,000,000倍、100-1,000倍、100-10,000倍、100-100,000倍、100-1,000,000倍、100-10,000,000倍、1,000-10,000倍、1,000-100,000倍、1,000-1,000,000倍、1000-10,000,000倍、10,000-100,000倍、10,000-1,000,000倍、10,000-10,000,000倍、100,000-1,000,000倍或100,000-10,000,000倍之间。相反,用mm修饰的ab针对cd47靶标的结合亲和力比未用mm修饰的ab或亲本ab针对cd47靶标的结合亲和力低至少2、3、4、5、10、25、50、100、250、500、1,000、2,500、5,000、10,000、50,000、100,000、500,000、1,000,000、5,000,000、10,000,000、50,000,000倍或更多倍,或在5-10倍、10-100倍、10-1,000倍、10-10,000倍、10-100,000倍、10-1,000,000倍、10-10,000,000倍、100-1,000倍、100-10,000倍、100-100,000倍、100-1,000,000倍、100-10,000,000倍、1,000-10,000倍、1,000-100,000倍、1,000-1,000,000倍、1000-10,000,000倍、10,000-100,000倍、10,000-1,000,000倍、10,000-10,000,000倍、100,000-1,000,000倍或100,000-10,000,000倍之间。
[0142]
mm针对ab的解离常数(kd)通常大于ab针对cd47靶标的kd。mm针对ab的kd可比ab针对cd47靶标的kd大至少5、10、25、50、100、250、500、1,000、2,500、5,000、10,000、100,000、1,000,000或甚至10,000,000倍。相反,mm针对ab的结合亲和力通常比ab针对cd47靶标的结合亲和力低。mm针对ab的结合亲和力可比ab针对cd47靶标的结合亲和力低至少5、10、25、50、100、250、500、1,000、2,500、5,000、10,000、100,000、1,000,000或甚至10,000,000倍。
[0143]
在一些实施方案中,mm针对ab的解离常数(kd)大致等于ab针对cd47靶标的kd。在一些实施方案中,mm针对ab的解离常数(kd)不超过ab针对cd47靶标的解离常数。在一些实施方案中,mm针对ab的解离常数(kd)等于ab针对cd47靶标的解离常数。
[0144]
在一些实施方案中,mm针对ab的解离常数(kd)小于ab针对cd47靶标的解离常数。
[0145]
在一些实施方案中,mm针对ab的解离常数(kd)大于ab针对cd47靶标的解离常数。
[0146]
在一些实施方案中,mm与ab的结合的kd不超过ab与靶标的结合的kd。
[0147]
在一些实施方案中,mm与ab的结合的kd不小于ab与靶标的结合的kd。
[0148]
在一些实施方案中,mm与ab的结合的kd大致等于ab与靶标的结合的kd。
[0149]
在一些实施方案中,mm与ab的结合的kd小于ab与靶标的结合的kd。
[0150]
在一些实施方案中,mm与ab的结合的kd大于ab与靶标的结合的kd。
[0151]
在一些实施方案中,mm与ab的结合的kd比ab与靶标的结合的kd大不超过2、3、4、5、10、25、50、100、250、500或1,000倍。在一些实施方案中,mm与ab的结合的kd比ab与靶标的结合的kd大1-5、2-5、2-10、5-10、5-20、5-50、5-100、10-100、10-1,000、20-100、20-1000或100-1,000倍之间。
[0152]
在一些实施方案中,mm与ab结合的亲和力小于ab与靶标结合的亲和力。
[0153]
在一些实施方案中,mm与ab结合的亲和力不超过ab与靶标结合的亲和力。
[0154]
在一些实施方案中,mm与ab结合的亲和力大致等于ab与靶标结合的亲和力。
[0155]
在一些实施方案中,mm与ab结合的亲和力不小于ab与靶标结合的亲和力。
[0156]
在一些实施方案中,mm与ab结合的亲和力大于ab与靶标结合的亲和力。
[0157]
在一些实施方案中,mm与ab结合的亲和力比ab与靶标结合的亲和力小2、3、4、5、10、25、50、100、250、500或1,000倍。在一些实施方案中,mm与ab结合的亲和力比ab与靶标结合的亲和力小1-5、2-5、2-10、5-10、5-20、5-50、5-100、10-100、10-1,000、20-100、20-1000
或100-1,000倍之间。在一些实施方案中,mm与ab结合的亲和力比ab与靶标结合的亲和力小2至20倍。在一些实施方案中,未与ab共价连接且与ab在等摩尔浓度下的mm不抑制ab与靶标的结合。
[0158]
与未用mm修饰的ab的特异性结合或亲本ab与靶标的特异性结合相比,当用mm修饰ab且在存在靶标时,ab与其靶标的特异性结合降低或受到抑制。当在体内或体外测定中测量时,与未用mm修饰的ab与靶标的结合或亲本ab与靶标的结合相比,当用mm修饰时,ab结合靶标的能力可降低至少50%、60%、70%、80%、90%、92%、93%、94%、95%、96%、97%、98%、99%和甚至100%,持续至少2、4、6、8、12、28、24、30、36、48、60、72、84或96小时或5、10、15、30、45、60、90、120、150或180天或1、2、3、4、5、6、7、8、9、10、11或12个月或更长时间。
[0159]
mm抑制ab与靶标的结合。mm结合ab的抗原结合结构域并抑制ab与靶标的结合。mm可在空间上抑制ab与靶标的结合。mm可变构地抑制ab与其靶标的结合。在这些实施方案中,当在体内或体外测定中测量时,与未用mm修饰的ab、亲本ab或未偶合至mm的ab与靶标的结合相比,当ab被修饰或偶合至mm且在存在靶标时,ab与靶标不结合或基本上不结合,或ab与靶标的结合不超过0.001%、0.01%、0.1%、1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、35%、40%或50%,持续至少2、4、6、8、12、28、24、30、36、48、60、72、84或96小时或5、10、15、30、45、60、90、120、150或180天或1、2、3、4、5、6、7、8、9、10、11或12个月或更长时间。
[0160]
当ab偶合至mm或被mm修饰时,mm“掩蔽”或减少或以其他方式抑制ab与靶标的特异性结合。当ab偶合至mm或被mm修饰时,此种偶合或修饰可引起降低或抑制ab特异性结合其靶标的能力的结构变化。
[0161]
偶合至mm或用mm修饰的ab可由下式(以从氨基(n)端区域到羧基(c)端区域的顺序)表示:
[0162]
(mm)-(ab)
[0163]
(ab)-(mm)
[0164]
(mm)-l-(ab)
[0165]
(ab)-l-(mm)
[0166]
其中mm为掩蔽部分,ab为抗体或其抗体片段,并且l为接头。在许多实施方案中,可能希望将一个或多个接头,例如柔性接头插入组合物中,以提供柔性。
[0167]
在某些实施方案中,mm不是ab的天然结合配偶体。在一些实施方案中,mm不含或基本上不含与ab的任何天然结合配偶体的同源性。在一些实施方案中,mm与ab的任何天然结合配偶体至多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%或80%相似。在一些实施方案中,mm与ab的任何天然结合配偶体不超过5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%或80%同一。在一些实施方案中,mm与ab的任何天然结合配偶体不超过25%相同。在一些实施方案中,mm与ab的任何天然结合配偶体不超过50%相同。在一些实施方案中,mm与ab的任何天然结合配偶体不超过20%相同。在一些实施方案中,mm与ab的任何天然结合配偶体不超过10%相同。
[0168]
在一些实施方案中,可活化抗体包含通过mm修饰的ab,并且还包含一个或多个可裂解部分(cm)。此类可活化抗体表现出与ab的靶标的可活化/可转换结合。可活化抗体通常
包含通过掩蔽部分(mm)修饰或偶合至掩蔽部分的抗体或抗体片段(ab)以及可修饰或可裂解部分(cm)。在一些实施方案中,cm含有充当至少一种蛋白酶的底物的氨基酸序列。
[0169]
排列可活化抗体的元件,使得mm和cm定位成使得在裂解(或相对活性)状态下且在存在靶标的情况下,ab结合靶标,而在可活化抗体处于未裂解(或相对无活性)状态下在存在靶标的情况下,ab与其靶标的特异性结合降低或受到抑制。由于mm对ab特异性结合其靶标的能力的抑制或掩蔽,ab与其靶标的特异性结合可减少。
[0170]
用mm和cm修饰的ab针对cd47靶标的kd比未用mm和cm修饰的ab或亲本ab针对cd47靶标的kd大至少5、10、25、50、100、250、500、1,000、2,500、5,000、10,000、50,000、100,000、500,000、1,000,000、5,000,000、10,000,000、50,000,000倍或更多倍,或在5-10倍、10-100倍、10-1,000倍、10-10,000倍、10-100,000倍、10-1,000,000倍、10-10,000,000倍、100-1,000倍、100-10,000倍、100-100,000倍、100-1,000,000倍、100-10,000,000倍、1,000-10,000倍、1,000-100,000倍、1,000-1,000,000倍、1000-10,000,000倍、10,000-100,000倍、10,000-1,000,000倍、10,000-10,000,000倍、100,000-1,000,000倍或100,000-10,000,000倍之间。相反,用mm和cm修饰的ab针对cd47靶标的结合亲和力比未用mm和cm修饰的ab或亲本ab针对cd47靶标的结合亲和力低至少5、10、25、50、100、250、500、1,000、2,500、5,000、10,000、50,000、100,000、500,000、1,000,000、5,000,000、10,000,000、50,000,000倍或更多倍,或在5-10倍、10-100倍、10-1,000倍、10-10,000倍、10-100,000倍、10-1,000,000倍、10-10,000,000倍、100-1,000倍、100-10,000倍、100-100,000倍、100-1,000,000倍、100-10,000,000倍、1,000-10,000倍、1,000-100,000倍、1,000-1,000,000倍、1000-10,000,000倍、10,000-100,000倍、10,000-1,000,000倍、10,000-10,000,000倍、100,000-1,000,000倍或100,000-10,000,000倍之间。
[0171]
与未用mm和cm修饰的ab或亲本ab与靶标的特异性结合相比,当用mm和cm修饰ab且在存在靶标但不存在修饰剂(例如至少一种蛋白酶)时,ab与其靶标的特异性结合降低或受到抑制。当在体内或体外测定中测量时,与亲本ab与其靶标的结合或未用mm和cm修饰的ab与其靶标的结合相比,当用mm和cm修饰时,ab结合靶标的能力可降低至少50%、60%、70%、80%、90%、92%、93%、94%、95%、96%、97%、98%、99%和甚至100%,持续2、4、6、8、12、28、24、30、36、48、60、72、84或96小时或5、10、15、30、45、60、90、120、150或180天或1、2、3、4、5、6、7、8、9、10、11或12个月或更长时间。
[0172]
可以提供多种结构构型的可活化抗体。下文提供了可活化抗体的示例性式。特别考虑的是,在可活化抗体内,ab、mm和cm的n末端至c末端顺序可颠倒。还特别考虑到,cm和mm可在氨基酸序列中重叠,例如使得cm包含在mm内。
[0173]
例如,可活化抗体可由下式(以从氨基(n)端区域到羧基(c)端区域的顺序)表示:
[0174]
(mm)-(cm)-(ab)
[0175]
(ab)-(cm)-(mm)
[0176]
其中mm为掩蔽部分,cm为可裂解部分,并且ab为抗体或其片段。应注意,尽管在上式中mm和cm被指示为不同的组分,但是在本文公开的所有示例性实施方案(包括式)中,考虑mm和cm的氨基酸序列可重叠,例如以使得cm完全或部分包含在mm中。另外,上式提供了可定位在可活化抗体元件的n末端或c末端的另外的氨基酸序列。
[0177]
在某些实施方案中,mm不是ab的天然结合配偶体。在一些实施方案中,mm不含或基
本上不含与ab的任何天然结合配偶体的同源性。在一些实施方案中,mm与ab的任何天然结合配偶体至多5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%或80%相似。在一些实施方案中,mm与ab的任何天然结合配偶体不超过5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%或80%同一。在一些实施方案中,mm与ab的任何天然结合配偶体不超过50%相同。在一些实施方案中,mm与ab的任何天然结合配偶体不超过25%相同。在一些实施方案中,mm与ab的任何天然结合配偶体不超过20%相同。在一些实施方案中,mm与ab的任何天然结合配偶体不超过10%相同。
[0178]
在许多实施方案中,可能需要将一个或多个接头(例如柔性接头)插入可活化抗体构建体中,以便在mm-cm接点、cm-ab接点或两者处提供柔性。例如,ab、mm和/或cm可能不含足够数量的残基(例如,gly、ser、asp、asn,特别是gly和ser,特别是gly)来提供所需的柔性。因此,此类可活化抗体构建体的可转换表型可受益于一种或多种氨基酸的引入以提供柔性接头。另外,如下文所述,当可活化抗体以构象受限的构建体提供时,可以可操作地插入柔性接头以促进未裂解的可活化抗体中环状结构的形成和维持。
[0179]
例如,在某些实施方案中,可活化抗体包含下式中的一个(其中下式表示在n末端到c末端方向或c末端到n末端方向的氨基酸序列):
[0180]
(mm)-l1-(cm)-(ab)
[0181]
(mm)-(cm)-l2-(ab)
[0182]
(mm)-l1-(cm)-l2-(ab)
[0183]
其中mm、cm和ab如上文所定义;其中l1和l2各自独立且任选地存在或不存在,是包含至少1种柔性氨基酸(例如,gly)的相同或不同的柔性接头。另外,上式提供了可定位在可活化抗体元件的n末端或c末端的另外的氨基酸序列。实例包括但不限于靶向部分(例如,存在于靶组织中的细胞受体的配体)和血清半衰期延长部分(例如,结合血清蛋白的多肽,诸如免疫球蛋白(例如,igg)或血清白蛋白(例如,人血清白蛋白(has))。
[0184]
cm通过至少一种蛋白酶以约0.001-1500x104m-1
s-1
或至少0.001、0.005、0.01、0.05、0.1、0.5、1、2.5、5、7.5、10、15、20、25、50、75、100、125、150、200、250、500、750、1000、1250或1500x104m-1
s-1
的速率特异性地裂解。在一些实施方案中,cm以约100,000m-1
s-1
的速率特异性地裂解。在一些实施方案中,cm以约1x10e2至约1x10e6 m-1
s-1
(即,约1x102至约1x106m-1
s-1
)的速率特异性地裂解。
[0185]
为了通过酶特异性裂解,在酶与cm之间进行接触。当包含偶合到mm的ab和cm的可活化抗体是在存在靶标和足够的酶活性的情况下时,cm可被裂解。足够的酶活性可指所述酶与cm接触并实现裂解的能力。可容易地预见到,酶可能在cm附近,但是由于其他细胞因子或酶的蛋白质修饰而不能裂解。
[0186]
适用于在本文所述的组合物中使用的接头通常是提供修饰的ab或可活化抗体的柔性以促进抑制ab与靶标的结合的接头。此类接头通常被称为柔性接头。合适的接头可容易地选择并且可具有任何合适的不同长度,诸如1个氨基酸(例如,gly)至20个氨基酸、2个氨基酸至15个氨基酸、3个氨基酸至12个氨基酸,包括4个氨基酸至10个氨基酸、5个氨基酸至9个氨基酸、6个氨基酸至8个氨基酸、或7个氨基酸至8个氨基酸,并且长度可为1、2、3、4、5、6、7、8、9、10、3或4、5或6、7、14、15、16、17、18、19或20个氨基酸。
[0187]
示例性柔性接头包括甘氨酸聚合物(g)n、甘氨酸-丝氨酸聚合物(包括例如(gs)n、(gsggs)n(seq id no:116)和(gggs)n(seq id no:117),其中n为至少1的整数)、甘氨酸-丙氨酸聚合物、丙氨酸-丝氨酸聚合物和本领域已知的其他柔性接头。甘氨酸和甘氨酸-丝氨酸聚合物是相对无结构的,并且因此可能能够充当组件之间的中性系链。甘氨酸比甚至丙氨酸接近显著更大的phi-psi空间,并且受到的限制远小于具有较长侧链的残基(参见scheraga,rev.computational chem.11173-142(1992))。示例性柔性接头包括但不限于gly-gly-ser-gly(seq id no:118)、gly-gly-ser-gly-gly(seq id no:119)、gly-ser-gly-ser-gly(seq id no:120)、gly-ser-gly-gly-gly(seq id no:121)、gly-gly-gly-ser-gly(seq id no:122)、gly-ser-ser-ser-gly(seq id no:123)等。普通技术人员将认识到,可活化抗体的设计可包括全部或部分柔性的接头,以使得接头可包括柔性接头以及赋予较少柔性结构以提供所需的可活化抗体结构的一个或多个部分。
[0188]
本公开还提供了包含可活化抗体的组合物和方法,所述可活化cd47抗体包含特异性结合cd47的抗体或抗体片段(ab),其中ab与降低ab结合其靶标的能力的掩蔽部分(mm)偶合。在一些实施方案中,可活化cd47抗体还包括作为蛋白酶的底物的可裂解部分(cm)。本文提供的组合物和方法使得能够将一种或多种剂附接到ab中的一个或多个半胱氨酸残基,而不损害可活化cd47抗体的活性(例如,掩蔽、活化或结合活性)。在一些实施方案中,本文提供的组合物和方法使得能够将一种或多种剂附接到ab中的一个或多个半胱氨酸残基,而不减少或以其他方式干扰mm中的一个或多个二硫键。本文提供的组合物和方法产生与一种或多种剂(例如,多种治疗剂、诊断剂和/或预防剂中的任一种)缀合的可活化cd47抗体,例如,在一些实施方案中,没有任何一种或多种剂与可活化cd47抗体的mm缀合。本文提供的组合物和方法产生缀合的可活化cd47抗体,其中mm保留有效且高效地掩蔽未裂解状态的可活化抗体的ab的能力。本文提供的组合物和方法产生缀合的可活化cd47抗体,其中可活化抗体在可裂解cm的蛋白酶存在下仍被活化,即被裂解。
[0189]
在一些实施方案中,可活化抗体包含seq id no:1的重链可变区氨基酸序列。在一些实施方案中,可活化抗体包含seq id no:2的轻链可变区氨基酸序列。
[0190]
在一些实施方案中,可活化抗体包含与seq id no:1的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的重链可变区氨基酸序列。在一些实施方案中,可活化抗体包含与seq id no:2的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的轻链可变区氨基酸序列。
[0191]
在一些实施方案中,可活化抗体包含与seq id no:1的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的重链可变区氨基酸序列和与seq id no:2的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的轻链可变区氨基酸序列。
[0192]
在一些实施方案中,可活化抗体包含以下的组合:可变重链互补决定区1(vh cdr1,在本文中也称为cdrh1)序列、可变重链互补决定区2(vh cdr2,在本文中也称为cdrh2)序列、可变重链互补决定区3(vh cdr3,在本文中也称为cdrh3)序列、可变轻链互补决定区1(vl cdr1,在本文中也称为cdrl1)序列、可变轻链互补决定区2(vl cdr2,在本文中也称为cdrl2)序列和可变轻链互补决定区3(vl cdr3,在本文中也称为cdrl3)序列,其中至少一个cdr序列选自由以下组成的组:包含氨基酸序列gytftny(seq id no:3)或氨基酸序
列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸序列ridpydvethyaqkfqg(seq id no:6)或氨基酸序列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
[0193]
在一些实施方案中,可活化抗体包含以下的组合:vh cdr1序列、vh cdr2序列、vh cdr3序列、vl cdr1序列、vl cdr2序列和vl cdr3序列,其中至少一个cdr序列选自由以下组成的组:包括与包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr1序列;包括与包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr2序列;包括与包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr3序列;包括与包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr1序列;包括与包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr2序列;以及包括与包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr3序列。
[0194]
在一些实施方案中,可活化抗体包含以下的组合:vh cdr1序列、vh cdr2序列、vh cdr3序列、vl cdr1序列、vl cdr2序列和vl cdr3序列,其中vh cdr1序列包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4);vh cdr2序列包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39);vh cdr3序列包含氨基酸序列ggvggmdy(seq id no:7);vl cdr1序列包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56);vl cdr2序列包含氨基酸序列rvskrfs(seq id no:9);并且vl cdr3序列包含氨基酸序列fqgshvprt(seq id no:10)。
[0195]
在一些实施方案中,可活化抗体包含以下的组合:vh cdr1序列、vh cdr2序列、vh cdr3序列、vl cdr1序列、vl cdr2序列和vl cdr3序列,其中包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包括与包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr2序列;包括与包含氨基酸序列
ggvggmdy(seq id no:7)的vh cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr3序列;包括与包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr1序列;包括与包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr2序列;以及包括与包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr3序列。
[0196]
在一些实施方案中,mm与ab的结合的解离常数大于ab与cd47的解离常数。
[0197]
在一些实施方案中,mm与ab的结合的解离常数不超过ab与cd47的解离常数。
[0198]
在一些实施方案中,mm与ab的结合的解离常数等于ab与cd47的解离常数。
[0199]
在一些实施方案中,mm与ab的结合的解离常数小于ab与cd47的解离常数。
[0200]
在一些实施方案中,mm针对ab的解离常数(kd)比ab针对所述cd47靶标的解离常数大不超过2、3、4、5、10、25、50、100、250、500、1,000、2,500、5,000、10,000、50,000、100,000、500,000、1,000,000、5,000,000、10,000,000、50,000,000倍或更多倍,或1-5、5-10、10-100、10-1,000、10-10,000、10-100,000、10-1,000,000、10-10,000,000、100-1,000、100-10,000、100-100,000、100-1,000,000、100-10,000,000、1,000-10,000、1,000-100,000、1,000-1,000,000、1000-10,000,000、10,000-100,000、10,000-1,000,000、10,000-10,000,000、100,000-1,000,000或100,000-10,000,000之间倍或更多倍。
[0201]
在一些实施方案中,当可活化抗体处于裂解状态时,mm不干扰ab结合至cd47或不与ab竞争结合至cd47。
[0202]
在一些实施方案中,mm是长度为约2至40个氨基酸的多肽。在一些实施方案中,mm是长度至多约40个氨基酸的多肽。
[0203]
在一些实施方案中,mm多肽序列与cd47的序列不同。在一些实施方案中,mm多肽序列与ab的任何天然结合配偶体不超过50%相同。在一些实施方案中,mm多肽序列与cd47的序列不同,并且与ab的任何天然结合配偶体至多40%、30%、25%、20%、15%或10%同一。
[0204]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少2倍。
[0205]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少5倍。
[0206]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少10倍。
[0207]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少20倍。
[0208]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少40倍。
[0209]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少100倍。
[0210]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少1000倍。
[0211]
在一些实施方案中,mm与ab的偶合降低所述ab结合cd47的能力,使得所述ab在偶合至所述mm时针对cd47的解离常数(kd)比所述ab未偶合至所述mm时针对cd47的kd大至少10,000倍。
[0212]
在一些实施方案中,在cd47存在下,当使用靶标置换测定,例如像pct公布号wo 2010/081173(其内容特此以引用的方式整体并入)中描述的测定在体外测定时,与cm裂解时相比,当所述cm未裂解时,mm使ab结合cd47的能力降低至少90%。
[0213]
在一些实施方案中,mm包含选自由seq id no:16-29组成的组的氨基酸序列。在一些实施方案中,mm包含seq id no:17的氨基酸序列。在一些实施方案中,mm包含seq id no:23的氨基酸序列。在一些实施方案中,mm包含seq id no:24的氨基酸序列。在一些实施方案中,mm包含seq id no:26的氨基酸序列。在一些实施方案中,mm包含seq id no:27的氨基酸序列。
[0214]
在一些实施方案中,裂解cm的蛋白酶在患病组织中具有活性,例如,上调或以其他方式不受调控,并且当可活化抗体暴露于所述蛋白酶时,所述蛋白酶裂解所述可活化抗体中的cm。
[0215]
在一些实施方案中,蛋白酶与cd47共定位在组织中,并且当可活化抗体暴露于蛋白酶时,蛋白酶使可活化抗体中的cm裂解。
[0216]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大至少2倍,而在裂解状态下(即,当可活化抗体处于裂解状态时),ab结合cd47。
[0217]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大至少5倍,而在裂解状态下(即,当可活化抗体处于裂解状态时),ab结合cd47。
[0218]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大至少10倍,而在裂解状态下(即,当可活化抗体处于裂解状态时),ab结合cd47。
[0219]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大至少20倍,而在裂解状态下(即,当可活化抗体处于裂解状态时),ab结合cd47。
[0220]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大
至少40倍,而在裂解状态下,ab结合cd47。
[0221]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大至少50倍,而在裂解状态下,ab结合cd47。
[0222]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大至少100倍,而在裂解状态下,ab结合cd47。
[0223]
在一些实施方案中,cm位于可活化抗体中,使得当可活化抗体处于未裂解状态时,可活化抗体与cd47的结合发生减少,其中解离常数比未修饰的ab与cd47结合的解离常数大至少200倍,而在裂解状态下,ab结合cd47。
[0224]
在一些实施方案中,cm是长度至多15个氨基酸的多肽。
[0225]
在一些实施方案中,cm是多肽,所述多肽包含作为至少一种基质金属蛋白酶(mmp)的底物的第一可裂解部分(cm1)和作为至少一种丝氨酸蛋白酶(sp)的底物的第二可裂解部分(cm2)。在一些实施方案中,cm1-cm2底物的cm1底物序列和cm2底物序列中的每一个独立地为长度至多15个氨基酸的多肽。
[0226]
在一些实施方案中,cm是至少一种蛋白酶的底物,所述至少一种蛋白酶被认为在癌症中上调或以其他方式不受调控。
[0227]
在一些实施方案中,cm是选自由以下组成的组的至少一种蛋白酶的底物:基质金属蛋白酶(mmp)、凝血酶、嗜中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、豆荚蛋白和丝氨酸蛋白酶如蛋白裂解酶(matriptase)(mt-sp1)和尿激酶(upa)。不受理论束缚,据信这些蛋白酶在至少一种癌症中被上调或以其他方式不受调控。
[0228]
示例性底物包括但不限于可被表a中所列的以下一种或多种酶或蛋白酶裂解的底物。
[0229]
在一些实施方案中,选择cm与特定蛋白酶一起使用,例如已知与可活化抗体的靶标共定位的蛋白酶。
[0230]
在一些实施方案中,cm是至少一种mmp的底物。mmp的实例包括表a中列出的mmp。在一些实施方案中,cm是选自mmp 9、mmp14、mmp1、mmp3、mmp13、mmp17、mmp11和mmp19的蛋白酶的底物。在一些实施方案中,cm是mmp9的底物。在一些实施方案中,cm是mmp14的底物。
[0231]
在一些实施方案中,cm是包括以下序列的底物:tgrgpswv(seq id no:356);sargpsrw(seq id no:357);targpsfk(seq id no:358);lsgrsdnh(seq id no:359);ggwhtgrn(seq id no:360);htgrsgal(seq id no:361);pltgrsgg(seq id no:362);aargpaih(seq id no:363);rgpafnpm(seq id no:364);ssrgpayl(seq id no:365);rgpatpim(seq id no:366);rgpa(seq id no:367);ggqpsgmwgw(seq id no:368);fprplgitgl(seq id no:369);vhmplgflgp(seq id no:370);spltgrsg(seq id no:371);sagfslpa(seq id no:372);laplglqrr(seq id no:373);sggplgvr(seq id no:374);plgl(seq id no:375);lsgrsgnh(seq id no:789);sgrsanprg(seq id no:790);lsgrsddh(seq id no:791);lsgrsdih(seq id no:792);lsgrsdqh(seq id no:793);lsgrsdth(seq id no:794);lsgrsdyh(seq id no:795);lsgrsdnp(seq id no:796);lsgrsanp(seq id no:797);lsgrsani(seq id no:798);lsgrsdni(seq id no:799);miapvayr(seq id no:800);
no:439)。
[0234]
在一些实施方案中,cm包含氨基酸序列issglss(seq id no:376)。在一些实施方案中,cm包含氨基酸序列qnqalrma(seq id no:377)。在一些实施方案中,cm包含氨基酸序列aqnllgmv(seq id no:378)。在一些实施方案中,cm包含氨基酸序列stfpfgmf(seq id no:379)。在一些实施方案中,cm包含氨基酸序列pvgytssl(seq id no:380)。在一些实施方案中,cm包含氨基酸序列dwlywpgi(seq id no:381)。在一些实施方案中,cm包含氨基酸序列issgllss(seq id no:382)。在一些实施方案中,cm包含氨基酸序列lkaaprwa(seq id no:383)。在一些实施方案中,cm包含氨基酸序列gpshlvlt(seq id no:384)。在一些实施方案中,cm包含氨基酸序列lpgglspw(seq id no:385)。在一些实施方案中,cm包含氨基酸序列mglfseag(seq id no:386)。在一些实施方案中,cm包含氨基酸序列splplrvp(seq id no:387)。在一些实施方案中,cm包含氨基酸序列rmhlrslg(seq id no:388)。在一些实施方案中,cm包含氨基酸序列laaplgll(seq id no:389)。在一些实施方案中,cm包含氨基酸序列avgllapp(seq id no:390)。在一些实施方案中,cm包含氨基酸序列llapshra(seq id no:391)。在一些实施方案中,cm包含氨基酸序列paglwldp(seq id no:392)。在一些实施方案中,cm包含氨基酸序列alahglf(seq id no:424)。在一些实施方案中,cm包含氨基酸序列dlahpll(seq id no:425)。在一些实施方案中,cm包含氨基酸序列afrhlr(seq id no:426)。在一些实施方案中,cm包含氨基酸序列phgffq(seq id no:427)。在一些实施方案中,cm包含氨基酸序列svhhli(seq id no:428)。在一些实施方案中,cm包含氨基酸序列rgpklyw(seq id no:429)。在一些实施方案中,cm包含氨基酸序列rfpygvw(seq id no:430)。在一些实施方案中,cm包含氨基酸序列hvprqv(seq id no:431)。在一些实施方案中,cm包含氨基酸序列snpfky(seq id no:432)。在一些实施方案中,cm包含氨基酸序列rfplkv(seq id no:433)。在一些实施方案中,cm包含氨基酸序列pfhlsr(seq id no:434)。在一些实施方案中,cm包含氨基酸序列stvfhm(seq id no:435)。在一些实施方案中,cm包含氨基酸序列mgpwfm(seq id no:436)。在一些实施方案中,cm包含氨基酸序列rhlakl(seq id no:437)。在一些实施方案中,cm包含氨基酸序列plgvrgk(seq id no:438)。在一些实施方案中,cm包含氨基酸序列qnqalria(seq id no:439)。
[0235]
在一些实施方案中,cm是凝血酶的底物。在一些实施方案中,cm是凝血酶的底物并且包括序列gprsfgl(seq id no:393)或gprsfg(seq id no:394)。在一些实施方案中,cm包含氨基酸序列gprsfgl(seq id no:393)。在一些实施方案中,cm包含氨基酸序列gprsfg(seq id no:394)。
[0236]
在一些实施方案中,cm包含选自由以下组成的组的氨基酸序列:ntlsgrsenhsg(seq id no:395);ntlsgrsgnhgs(seq id no:396);tstsgrsanprg(seq id no:397);tsgrsanp(seq id no:398);vagrsmrp(seq id no:399);vvpegrrs(seq id no:400);ilprspaf(seq id no:401);mvlgrsll(seq id no:402);qgraitfi(seq id no:403);sprsimla(seq id no:404);和smlrsmpl(seq id no:405)。
[0237]
在一些实施方案中,cm包含氨基酸序列ntlsgrsenhsg(seq id no:395)。在一些实施方案中,cm包含氨基酸序列ntlsgrsgnhgs(seq id no:396)。在一些实施方案中,cm包含氨基酸序列tstsgrsanprg(seq id no:397)。在一些实施方案中,cm包含氨基酸序列tsgrsanp(seq id no:398)。在一些实施方案中,cm包含氨基酸序列vagrsmrp(seq id no:
399)。在一些实施方案中,cm包含氨基酸序列vvpegrrs(seq id no:400)。在一些实施方案中,cm包含氨基酸序列ilprspaf(seq id no:401)。在一些实施方案中,cm包含氨基酸序列mvlgrsll(seq id no:402)。在一些实施方案中,cm包含氨基酸序列qgraitfi(seq id no:403)。在一些实施方案中,cm包含氨基酸序列sprsimla(seq id no:404)。在一些实施方案中,cm包含氨基酸序列smlrsmpl(seq id no:405)。
[0238]
在一些实施方案中,cm是嗜中性粒细胞弹性蛋白酶的底物。在一些实施方案中,cm是丝氨酸蛋白酶的底物。在一些实施方案中,cm是upa的底物。在一些实施方案中,cm是豆荚蛋白的底物。在一些实施方案中,cm是蛋白裂解酶的底物。在一些实施方案中,cm是半胱氨酸蛋白酶的底物。在一些实施方案中,cm是半胱氨酸蛋白酶如组织蛋白酶的底物。
[0239]
在一些实施方案中,cm是cm1-cm2底物并且包括序列issgllsgrsdnh(seq id no:406);issgllssggsggslsgrsdnh(seq id no:407);avgllappggtstsgrsanprg(seq id no:408);tstsgrsanprgggavgllapp(seq id no:409);vhmplgflgpggtstsgrsanprg(seq id no:410);tstsgrsanprgggvhmplgflgp(seq id no:411);avgllappgglsgrsdnh(seq id no:412);lsgrsdnhggavgllapp(seq id no:413);vhmplgflgpgglsgrsdnh(seq id no:414);lsgrsdnhggvhmplgflgp(seq id no:415);lsgrsdnhggsggsissgllss(seq id no:416);lsgrsgnhggsggsissgllss(seq id no:417);issgllssggsggslsgrsgnh(seq id no:418);lsgrsdnhggsggsqnqalrma(seq id no:419);qnqalrmaggsggslsgrsdnh(seq id no:420);lsgrsgnhggsggsqnqalrma(seq id no:421);qnqalrmaggsggslsgrsgnh(seq id no:422);issgllsgrsgnh(seq id no:423);issgllsgrsanprg(seq id no:680);avgllapptsgrsanprg(seq id no:681);avgllappsgrsanprg(seq id no:682);issgllsgrsddh(seq id no:683);issgllsgrsdih(seq id no:684);issgllsgrsdqh(seq id no:685);issgllsgrsdth(seq id no:686);issgllsgrsdyh(seq id no:687);issgllsgrsdnp(seq id no:688);issgllsgrsanp(seq id no:689);issgllsgrsani(seq id no:690);avgllappgglsgrsddh(seq id no:691);avgllappgglsgrsdih(seq id no:692);avgllappgglsgrsdqh(seq id no:693);avgllappgglsgrsdth(seq id no:694);avgllappgglsgrsdyh(seq id no:695);avgllappgglsgrsdnp(seq id no:696);avgllappgglsgrsanp(seq id no:697);avgllappgglsgrsani(seq id no:698)、issgllsgrsdni(seq id no:713);avgllappgglsgrsdni(seq id no:714);glsgrsdnhggavgllapp(seq id no:807);和/或glsgrsdnhggvhmplgflgp(seq id no:808)。
[0240]
在一些实施方案中,cm1-cm2底物包括序列issgllsgrsdnh(seq id no:406),其在本文中也称为底物2001。在一些实施方案中,cm1-cm2底物包括序列issgllssggsggslsgrsdnh(seq id no:407),其在本文中也称为底物1001/lp
′
/0001,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列avgllappggtstsgrsanprg(seq id no:408),其在本文中也称为底物2015和/或底物1004/lp
′
/0003,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列tstsgrsanprgggavgllapp(seq id no:409),其在本文中也称为底物0003/lp
′
/1004,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列vhmplgflgpggtstsgrsanprg(seq id no:410),其在本文中也称为底物1003/lp
′
/0003,其中如在此cm1-cm2底物中使用的lp
′
是氨基
酸序列gg。在一些实施方案中,cm1-cm2底物包括序列tstsgrsanprgggvhmplgflgp(seq id no:411),其在本文中也称为底物0003/lp
′
/1003,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsdnh(seq id no:412),其在本文中也称为底物3001和/或底物1004/lp
′
/0001,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列lsgrsdnhggavgllapp(seq id no:413),其在本文中也称为底物0001/lp
′
/1004,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列vhmplgflgpgglsgrsdnh(seq id no:414),其在本文中也称为底物1003/lp’/0001,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列lsgrsdnhggvhmplgflgp(seq id no:415),其在本文中也称为底物0001/lp
′
/1003,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列lsgrsdnhggsggsissgllss(seq id no:416),其在本文中也称为底物0001/lp
′
/1001,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列lsgrsgnhggsggsissgllss(seq id no:417),其在本文中也称为底物0002/lp
′
/1001,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列issgllssggsggslsgrsgnh(seq id no:418),其在本文中也称为底物1001/lp
′
/0002,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列lsgrsdnhggsggsqnqalrma(seq id no:419),其在本文中也称为底物0001/lp
′
/1002,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列qnqalrmaggsggslsgrsdnh(seq id no:420),其在本文中也称为底物1002/lp
′
/0001,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列lsgrsgnhggsggsqnqalrma(seq id no:421),其在本文中也称为底物0002/lp
′
/1002,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列qnqalrmaggsggslsgrsgnh(seq id no:422),其在本文中也称为底物1002/lp
′
/0002,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列ggsggs(seq id no:133)。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsgnh(seq id no:423),其在本文中也称为底物2002。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsanprg(seq id no:680),其在本文中也称为底物2003。在一些实施方案中,cm1-cm2底物包括序列avgllapptsgrsanprg(seq id no:681),其在本文中也称为底物2004。在一些实施方案中,cm1-cm2底物包括序列avgllappsgrsanprg(seq id no:682),其在本文中也称为底物2005。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsddh(seq id no:683),其在本文中也称为底物2006。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsdih(seq id no:684),其在本文中也称为底物2007。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsdqh(seq id no:685),其在本文中也称为底物2008。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsdth(seq id no:686),其在本文中也称为底物2009。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsdyh(seq id no:687),其在本文中也称为底物2010。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsdnp(seq id no:688),其在本文中也称为底物2011。在一些实
施方案中,cm1-cm2底物包括序列issgllsgrsanp(seq id no:689),其在本文中也称为底物2012。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsani(seq id no:690),其在本文中也称为底物2013。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsddh(seq id no:691),其在本文中也称为底物3006。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsdih(seq id no:692),其在本文中也称为底物3007。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsdqh(seq id no:693),其在本文中也称为底物3008。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsdth(seq id no:694),其在本文中也称为底物3009。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsdyh(seq id no:695),其在本文中也称为底物3010。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsdnp(seq id no:696),其在本文中也称为底物3011。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsanp(seq id no:697),其在本文中也称为底物3012。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsani(seq id no:698),其在本文中也称为底物3013。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsdni(seq id no:713),其在本文中也称为底物2014。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsdni(seq id no:714),其在本文中也称为底物3014。在一些实施方案中,cm1-cm2底物包括序列glsgrsdnhggavgllapp(seq id no:807),其在本文中也称为底物0001/lp
′
/1004,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。在一些实施方案中,cm1-cm2底物包括序列glsgrsdnhggvhmplgflgp(seq id no:808),其在本文中也称为底物0001/lp
′
/1003,其中如在此cm1-cm2底物中使用的lp
′
是氨基酸序列gg。
[0241]
在一些实施方案中,cm是cm1-cm2底物并且包括序列lsgrsalahglf(seq id no:440);alahglfsgrsan(seq id no:441);hvprqvlsgrs(seq id no:442);hvprqvlsgrsan(seq id no:443);targpalahglf(seq id no:444);targpvprqv(seq id no:445);aprsalahglf(seq id no:446);alahglfaprsf(seq id no:447);hvprqvaprsf(seq id no:448);alahglptfvhl(seq id no:449);glptfvhlprqv(seq id no:450);aanalahglf(seq id no:451);gptnalahglf(seq id no:452);issgllsgrsni(seq id no:453);avgllappgglsgrsni(seq id no:454);issgllsgrsnigs(seq id no:455);avgllappgglsgrsnigs(seq id no:456);issgllsgrsnig(seq id no:457);avgllappgglsgrsnig(seq id no:458)。
[0242]
在一些实施方案中,cm是cm1-cm2底物并且包括序列lsgrsalahglf(seq id no:440),其在本文中也称为底物5001。在一些实施方案中,cm是cm1-cm2底物并且包括序列alahglfsgrsan(seq id no:441),其在本文中也称为底物5002。在一些实施方案中,cm1-cm2底物包括序列hvprqvlsgrs(seq id no:442),其在本文中也称为底物5003。在一些实施方案中,cm1-cm2底物包括序列hvprqvlsgrsan(seq id no:443),其在本文中也称为底物5004。在一些实施方案中,cm1-cm2底物包括序列targpalahglf(seq id no:444),其在本文中也称为底物5005。在一些实施方案中,cm1-cm2底物包括序列targpvprqv(seq id no:445),其在本文中也称为底物5006。在一些实施方案中,cm1-cm2底物包括序列aprsalahglf(seq id no:446),其在本文中也称为底物5007。在一些实施方案中,cm1-cm2底物包括序列alahglfaprsf(seq id no:447),其在本文中也称为底物5008。在一些实施方案中,cm1-cm2底物包括序列hvprqvaprsf(seq id no:448),其在本文中也称为底物5009。在一些实施方
案中,cm1-cm2底物包括序列alahglptfvhl(seq id no:449),其在本文中也称为底物5010。在一些实施方案中,cm1-cm2底物包括序列glptfvhlprqv(seq id no:450),其在本文中也称为底物5011。在一些实施方案中,cm1-cm2底物包括序列aanalahglf(seq id no:451),其在本文中也称为底物5012。在一些实施方案中,cm1-cm2底物包括序列gptnalahglf(seq id no:452),其在本文中也称为底物5013。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsni(seq id no:453),其在本文中也称为底物5014。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsni(seq id no:454),其在本文中也称为底物5015。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsnigs(seq id no:455),其在本文中也称为底物5016。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsnigs(seq id no:456),其在本文中也称为底物5017。在一些实施方案中,cm1-cm2底物包括序列issgllsgrsnig(seq id no:457),其在本文中也称为底物5018。在一些实施方案中,cm1-cm2底物包括序列avgllappgglsgrsnig(seq id no:458),其在本文中也称为底物5019。
[0243]
在一些实施方案中,cm是至少两种蛋白酶的底物。在一些实施方案中,每种蛋白酶选自由表a所示的那些组成的组。在一些实施方案中,cm是至少两种蛋白酶的底物,其中一种蛋白酶选自由mmp、凝血酶、中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、upa、豆荚蛋白酶和蛋白裂解酶组成的组,并且另一种蛋白酶选自由表a所示的那些组成的组。在一些实施方案中,cm是选自由以下组成的组的至少两种蛋白酶的底物:mmp、凝血酶、中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、upa、豆荚蛋白酶和蛋白裂解酶。
[0244]
在一些实施方案中,可活化抗体包括至少第一cm和第二cm。在一些实施方案中,第一cm和第二cm各自是不超过15个氨基酸长的多肽。在一些实施方案中,处于未裂解状态的可活化抗体中的第一cm和第二cm从n末端到c末端具有如下结构排列:mm-cm1-cm2-ab或ab-cm2-cm1-mm。在一些实施方案中,第一cm和第二cm中的至少一者是多肽,所述多肽用作选自由以下组成的组的蛋白酶的底物:mmp、凝血酶、中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、upa、豆荚蛋白酶和蛋白裂解酶。在一些实施方案中,第一cm被靶组织中选自由mmp、凝血酶、中性弹性蛋白酶、半胱氨酸蛋白酶、upa、豆蔻蛋白酶和蛋白裂解酶组成的组的第一裂解剂裂解,并且第二cm被靶组织中的第二裂解剂裂解。在一些实施方案中,另一种蛋白酶选自由表a所示的那些组成的组。在一些实施方案中,第一裂解剂和第二裂解剂是选自由mmp、凝血酶、中性粒细胞弹性蛋白酶、半胱氨酸蛋白酶、upa、豆荚蛋白酶和蛋白裂解酶组成的组的相同蛋白酶,并且第一cm和第二cm是酶的不同底物。在一些实施方案中,第一裂解剂和第二裂解剂是选自由表a所示的那些组成的组的相同蛋白酶。在一些实施方案中,第一裂解剂和第二裂解剂是不同的蛋白酶。在一些实施方案中,第一裂解剂和第二裂解剂在靶组织中共定位。在一些实施方案中,第一cm和第二cm被靶组织中的至少一种裂解剂裂解。
[0245]
在一些实施方案中,使可活化抗体暴露于蛋白酶并被所述蛋白酶裂解,以使得在活化或裂解状态下,活化的抗体包含轻链氨基酸序列,所述轻链氨基酸序列在所述蛋白酶已经裂解cm后包含lp2和/或cm序列的至少一部分。
[0246]
本公开的合适的可活化cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含重链可变区氨基酸序列seq id no:1和轻链可变区氨基酸序列seq id no:2的cd47抗体结合至人cd47和/或食蟹猴cd47上的相同表位。
[0247]
本公开的合适的可活化cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗
原结合片段与包含以下的cd47抗体结合至人cd47和/或食蟹猴cd47上的相同表位:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
[0248]
本公开的合适的可活化cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含重链可变区氨基酸序列seq id no:1和轻链可变区氨基酸序列seq id no:2的cd47抗体交叉竞争结合至人cd47和/或食蟹猴cd47(抑制其结合cd47)。
[0249]
本公开的合适的可活化cd47抗体还包括抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含以下的cd47抗体交叉竞争结合至人cd47和/或食蟹猴cd47(抑制其结合cd47):包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。
[0250]
在一些实施方案中,可活化cd47抗体是在活化状态下结合cd47的可活化抗体,所述抗体包含:特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab),其中ab特异性结合人cd47和食蟹猴猴cd47;当可活化抗体处于未裂解状态时抑制ab与cd47的结合的掩蔽部分(mm);和偶合至ab的可裂解部分(cm),其中cm是用作蛋白酶的底物的多肽。
[0251]
在一些实施方案中,mm与ab的结合的解离常数大于ab与cd47的解离常数。在一些实施方案中,当可活化抗体处于裂解状态时,mm不干扰ab结合至cd47或不与ab竞争结合至cd47。在一些实施方案中,mm是长度不超过40个氨基酸的多肽。在一些实施方案中,mm多肽序列与人cd47的序列不同。在一些实施方案中,mm多肽序列与ab的任何天然结合配偶体不超过50%相同。在一些实施方案中,mm包含选自由seq id no:16-109组成的组的氨基酸序列。在一些实施方案中,mm包含选自由seq id no:107-109组成的组的氨基酸序列。
[0252]
在一些实施方案中,cm是在病变组织中具有活性的蛋白酶的底物。在一些实施方案中,cm包含选自由seq id no:356-458、680-698、713、714和789-808组成的组的氨基酸序列。在一些实施方案中,cm包含选自由seq id no:359、370、377、382、390、397、406-425、429、430、446、447、450、680-698、713、714和807-808组成的组的氨基酸序列。
[0253]
在一些实施方案中,可活化抗体包含其选自由以下组成的组的抗原结合片段:fab片段、f(ab’)2片段、scfv、scab、dab、单结构域重链抗体和单结构域轻链抗体。在一些实施方案中,可活化抗体的ab特异性结合人cd47。在一些实施方案中,所述ab包含:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系
列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,ab包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。
[0254]
在一些实施方案中,ab连接至cm。在一些实施方案中,ab直接连接至cm。在一些实施方案中,ab通过连接肽连接至cm。在一些实施方案中,mm连接至cm,使得处于未裂解状态的可活化抗体从n末端至c末端包含如下结构排列:mm-cm-ab或ab-cm-mm。在一些实施方案中,可活化抗体包含mm与cm之间的连接肽。在一些实施方案中,可活化抗体包含cm与ab之间的连接肽。在一些实施方案中,可活化抗体包含第一连接肽(lp1)和第二连接肽(lp2),并且其中处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:mm-lp1-cm-lp2-ab或ab-lp2-cm-lp1-mm。在一些实施方案中,两个连接肽不需要彼此相同。在一些实施方案中,lp1和lp2中的每一个是长度为约1至20个氨基酸的肽。
[0255]
在一些实施方案中,可活化抗体包含选自由seq id no:11-14组成的组的重链序列和包含选自由seq id no:15、41-54、61-74、81-94和16-114组成的组的氨基酸序列的轻链。
[0256]
在一些实施方案中,可活化抗体包含氨基酸序列的组合,其中氨基酸序列的组合选自表b中的单行,其中对于给定组合,(a)ab的重链包含对应于表b所列单行中的给定组合的vh cdr序列的氨基酸序列,(b)ab的轻链包含对应于表b所列单行中的给定组合的vl cdr序列的氨基酸序列,(c)mm包含对应于表b所列单行中的给定组合的掩蔽序列(mm)的氨基酸序列,并且(d)cm包含对应于表b所列单行中的给定组合的底物序列(cm)的氨基酸序列。
[0257]
在一些实施方案中,可活化抗体包含氨基酸序列的组合,其中对于给定的氨基酸序列组合,(a)ab的重链包含选自由表c的对应列中列出的vh序列或vh cdr序列组成的组的vh序列或vh cdr序列的氨基酸序列,(b)ab的轻链包含选自由表c的对应列中列出的vl序列或vl cdr序列组成的组的vl序列或vl cdr序列的氨基酸序列,(c)mm包含选自由表c的对应列中列出的mm序列组成的组的掩蔽序列(mm)的氨基酸序列,并且(d)cm包含选自由表c的对应列中列出的cm序列组成的组的底物序列(cm)的氨基酸序列。
[0258]
在一些实施方案中,可活化cd47抗体包含特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab)、mm和cm,其中可活化抗体包含:seq id no:11-14的重链序列;和包含选自由seq id no:15、41-54、61-74、81-94和16-114组成的组的氨基酸序列的轻链。在一些实施方案中,mm包含选自由seq id no:16-29组成的组的氨基酸序列,并且cm包含选自由seq id no:359、370、377、382、390、397、406-425、429、430、446、447、450、680-698、713、714和807-808组成的组的氨基酸序列。在一些实施方案中,所述ab包含:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:
56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,ab包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。
[0259]
在一些实施方案中,可活化cd47抗体包含特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab)、包含选自由seq id no:16-29组成的组的氨基酸序列的mm和包含选自由seq id no:356-458、680-698、713、714和789-808组成的组的氨基酸序列的cm。在一些实施方案中,mm包含选自由seq id no:16-29组成的组的氨基酸序列,并且cm包含选自由seq id no:359、370、377、382、390、397、406-425、429、430、446、447、450、680-698、713、714和807-808组成的组的氨基酸序列。在一些实施方案中,所述ab包含:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,ab包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。
[0260]
在一些实施方案中,可活化cd47抗体包含:特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab),其中ab与本公开的分离的抗体特异性结合至人cd47和/或食蟹猴猴cd47上的相同表位;当可活化抗体处于未裂解状态时抑制ab与cd47的结合的掩蔽部分(mm);和偶合至ab的可裂解部分(cm),其中cm是用作蛋白酶的底物的多肽。
[0261]
在一些实施方案中,本公开的cd47可活化抗体包含特异性结合至哺乳动物cd47的分离的抗体或其抗原结合片段(ab),其中ab特异性结合人cd47和食蟹猴cd47。在一些实施方案中,所述抗体或其抗原结合片段包含:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,ab包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。
[0262]
在一些实施方案中,可活化cd47抗体包含:特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab),其中ab与本公开的分离的抗体特异性交叉竞争结合至人cd47和/或食蟹猴猴cd47(抑制其结合cd47);当可活化抗体处于未裂解状态时抑制ab与cd47的结合的掩蔽部分(mm);和偶合至ab的可裂解部分(cm),其中cm是用作蛋白酶的底物的多肽。
[0263]
在一些实施方案中,本公开的cd47可活化抗体包含特异性结合至哺乳动物cd47的分离的抗体或其抗原结合片段(ab),其中ab特异性结合人cd47和食蟹猴cd47。在一些实施方案中,所述抗体或其抗原结合片段包含:包含氨基酸序列gytftny(seq id no:3)或氨基
酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,ab包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。
[0264]
在一些实施方案中,可活化抗体还包含缀合至ab的剂。在一些实施方案中,缀合至ab或可活化抗体的ab的剂为治疗剂。在一些实施方案中,剂为抗肿瘤剂。在一些实施方案中,剂为毒素或其片段。如本文所用,毒素的片段为保留毒素活性的片段。在一些实施方案中,剂通过可裂解的接头缀合至ab。在一些实施方案中,剂通过包含至少一个cm1-cm2底物序列的接头缀合至ab。在一些实施方案中,剂通过不可裂解的接头缀合至ab。在一些实施方案中,剂通过在细胞内或溶酶体环境中可裂解的接头缀合至ab。在一些实施方案中,剂为微管抑制剂。在一些实施方案中,剂为核酸损伤剂,诸如dna烷基化剂、dna裂解剂、dna交联剂、dna嵌入剂,或其他dna损伤剂。在一些实施方案中,剂为选自表e中列出的组的剂。在一些实施方案中,剂为多拉司他汀。在一些实施方案中,剂为澳瑞他汀或其衍生物。在一些实施方案中,剂为澳瑞他汀e或其衍生物。在一些实施方案中,剂为单甲基澳瑞他汀e(mmae)。在一些实施方案中,剂为单甲基澳瑞他汀d(mmad)。在一些实施方案中,剂为类美登素或类美登素衍生物。在一些实施方案中,剂为dm1或dm4。在一些实施方案中,剂为倍癌霉素或其衍生物。在一些实施方案中,剂为卡奇霉素(calicheamicin)或其衍生物。在一些实施方案中,剂为吡咯并苯并二氮杂在一些实施方案中,剂为吡咯并苯并二氮杂二聚体。
[0265]
在一些实施方案中,可活化抗体与一个或多个当量的剂缀合。在一些实施方案中,可活化抗体与一个当量的剂缀合。在一些实施方案中,可活化抗体与两个、三个、四个、五个、六个、七个、八个、九个、十个或大于十个当量的剂缀合。在一些实施方案中,可活化抗体是具有均一数目当量的缀合剂的可活化抗体混合物的一部分。在一些实施方案中,可活化抗体是具有非均一数目当量的缀合剂的可活化抗体混合物的一部分。在一些实施方案中,可活化抗体的混合物使得与每种可活化抗体缀合的剂的平均数目为零至一、一至二、二至三、三至四、四至五、五至六、六至七、七至八、八至九、九至十、十及以上。在一些实施方案中,可活化抗体的混合物使得与每种可活化抗体缀合的剂的平均数目为一、二、三、四、五、六、七、八、九、十或以上。
[0266]
在一些实施方案中,可活化抗体包含一种或多种位点特异性氨基酸序列修饰,使得赖氨酸和/或半胱氨酸残基的数目相对于可活化抗体的原始氨基酸序列增加或减少,因此在一些实施方案中,对应地增加或减少可与可活化抗体缀合的剂的数目,或在一些实施方案中,以位点特异性方式限制剂与可活化抗体的缀合。在一些实施方案中,修饰的可活化抗体以位点特异性方式经一种或多种非天然氨基酸修饰,因此在一些实施方案中,将剂的缀合限于仅非天然氨基酸的位点。
[0267]
在一些实施方案中,剂为抗炎剂。
[0268]
在一些实施方案中,可活化抗体还包含可检测部分。在一些实施方案中,可检测部
分为诊断剂。
[0269]
在一些实施方案中,可活化抗体还包含信号肽。在一些实施方案中,信号肽通过间隔区缀合至可活化抗体。在一些实施方案中,间隔区在不存在信号肽的情况下缀合至可活化抗体。在一些实施方案中,间隔区直接连接到可活化抗体的mm。在一些实施方案中,间隔区在间隔区-mm-cm-ab的n末端至c末端的结构排列中直接连接至可活化抗体的mm。直接连接至可活化抗体的mm的n末端的间隔区的实例是qgqsgq(seq id no:31)。直接连接至可活化抗体的mm的n末端的间隔区的其他实例包括qgqsgqg(seq id no:30)、qgqsg(seq id no:32)、qgqs(seq id no:33)、qgq、qg和q。直接连接至可活化抗体的mm的n末端的间隔区的其他实例包括gqsgqg(seq id no:34)、qsgqg(seq id no:35)、sgqg(seq id no:36)、gqg和g。在一些实施方案中,无间隔区连接至mm的n末端。在一些实施方案中,间隔区至少包含氨基酸序列qgqsgq(seq id no:31)。在一些实施方案中,间隔区至少包含氨基酸序列qgqsgqg(seq id no:30)。在一些实施方案中,间隔区至少包含氨基酸序列qgqsg(seq id no:32)。在一些实施方案中,间隔区至少包含氨基酸序列qgqs(seq id no:33)。在一些实施方案中,间隔区至少包含氨基酸序列qgq。在一些实施方案中,间隔区至少包含氨基酸序列qg。在一些实施方案中,间隔区至少包含氨基酸残基q。在一些实施方案中,间隔区至少包含氨基酸序列gqsgqg(seq id no:34)。在一些实施方案中,间隔区至少包含氨基酸序列qsgqg(seq id no:35)。在一些实施方案中,间隔区至少包含氨基酸序列sgqg(seq id no:36)。在一些实施方案中,间隔区至少包含氨基酸序列gqg。在一些实施方案中,间隔区至少包含氨基酸序列g。在一些实施方案中,不存在间隔区。
[0270]
在一些实施方案中,可活化抗体的ab天然含有一个或多个二硫键。在一些实施方案中,ab可被工程化为包含一个或多个二硫键。
[0271]
在一些实施方案中,可活化抗体或其抗原结合片段不缀合至剂。在一些实施方案中,可活化抗体包含抗体或其抗原结合片段,所述抗体或其抗原结合片段与包含以下的分离的抗体交叉竞争(抑制其结合):包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,可活化抗体包含与分离的抗体交叉竞争(抑制其结合)的抗体或其抗原结合片段,所述分离的抗体包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。在一些实施方案中,剂为毒素或其片段。在一些实施方案中,剂为微管抑制剂。在一些实施方案中,剂为核酸损伤剂。在一些实施方案中,剂选自由以下组成的组:多拉司他汀或其衍生物、澳瑞他汀或其衍生物、类美登素或其衍生物、倍癌霉素或其衍生物、卡奇霉素或其衍生物和吡咯并苯并二氮杂或其衍生物。在一些实施方案中,剂为澳瑞他汀e或其衍生物。在一些实施方案中,剂为单甲基澳瑞他汀e(mmae)。在一些实施方案中,剂为单甲基澳瑞他汀d(mmad)。在一些实施方案中,剂为选自由dm1和dm4组成的组的类美登素。在一些实施方案中,剂为类美登素dm4。在一些实施方
案中,剂为倍癌霉素。在一些实施方案中,剂通过接头缀合至ab。在一些实施方案中,剂缀合至ab所采用的接头包含spdb部分、vc部分或peg2-vc部分。在一些实施方案中,缀合至ab的接头和毒素包含spdb-dm4部分、vc-mmad部分、vc-mmae部分、vc-倍癌霉素或peg2-vc-mmad部分。在一些实施方案中,接头为可裂解的接头。在一些实施方案中,接头为不可裂解的接头。在一些实施方案中,剂为可检测部分。在一些实施方案中,可检测部分为诊断剂。
[0272]
在一些实施方案中,缀合的可活化抗体包含在活化状态下结合cd47的缀合的可活化抗体,所述抗体包含:特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab),其中ab特异性结合人cd47和食蟹猴猴cd47;当可活化抗体处于未裂解状态时抑制ab与cd47的结合的掩蔽部分(mm);偶合至ab的可裂解部分(cm),其中cm是用作蛋白酶的底物的多肽;和缀合至ab的剂。在一些实施方案中,剂选自由以下组成的组:多拉司他汀或其衍生物、澳瑞他汀或其衍生物、类美登素或其衍生物、倍癌霉素或其衍生物、卡奇霉素或其衍生物和吡咯并苯并二氮杂或其衍生物。在一些实施方案中,剂选自由以下组成的组:澳瑞他汀e、单甲基澳瑞他汀f(mmaf)、单甲基澳瑞他汀e(mmae)、单甲基澳瑞他汀d(mmad)、类美登素dm4、类美登素dm1、倍癌霉素、吡咯并苯并二氮杂和吡咯并苯并二氮杂二聚体。在一些实施方案中,剂通过接头缀合至ab。在一些实施方案中,剂缀合至ab所采用的接头包含spdb部分、vc部分或peg2-vc部分。在一些实施方案中,缀合至ab的接头和毒素包含spdb-dm4部分、vc-mmad部分、vc-mmae部分、vc-倍癌霉素或peg2-vc-mmad部分。在一些实施方案中,缀合的可活化抗体或其抗原结合片段的ab包含:包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列。在一些实施方案中,缀合的可活化抗体或其抗原结合片段的ab包含seq id no:1的重链可变区氨基酸序列和seq id no:2的轻链可变区氨基酸序列。在实施方案中,mm包含选自由seq id no:16-29组成的组的氨基酸序列。在一些实施方案中,mm包含选自由seq id no:17、23、24、25、27和28组成的组的氨基酸序列。在一些实施方案中,cm包含选自由seq id no:356-458、680-698、713、714和789-808组成的组的氨基酸序列。在一些实施方案中,cm包含选自由seq id no:359、370、377、382、390、397、406-425、429、430、446、447、450、680-698、713、714和807-808组成的组的氨基酸序列。在一些实施方案中,可活化抗体包含氨基酸序列的组合,其中氨基酸序列的组合选自表b中的单行,其中对于给定组合,(a)ab的重链包含对应于表b所列单行中的给定组合的vh cdr序列的氨基酸序列,(b)ab的轻链包含对应于表b所列单行中的给定组合的vl cdr序列的氨基酸序列,(c)mm包含对应于表b所列单行中的给定组合的掩蔽序列(mm)的氨基酸序列,并且(d)cm包含对应于表b所列单行中的给定组合的底物序列(cm)的氨基酸序列。在一些实施方案中,可活化抗体包含氨基酸序列的组合,其中对于给定的氨基酸序列组合,(a)ab的重链包含选自由表c的对应列中列出的vh序列或vh cdr序列组成的组的vh序列或vh cdr序列的氨基酸序列,(b)ab
的轻链包含选自由表c的对应列中列出的vl序列或vl cdr序列组成的组的vl序列或vl cdr序列的氨基酸序列,(c)mm包含选自由表c的对应列中列出的mm序列组成的组的掩蔽序列(mm)的氨基酸序列,并且(d)cm包含选自由表c的对应列中列出的cm序列组成的组的底物序列(cm)的氨基酸序列。在一些实施方案中,可活化抗体包含:包含选自由seq id no:1-4组成的组的氨基酸系列的重链和包含选自由seq id no:15、41-54、61-74、81-94和16-114组成的组的氨基酸序列的轻链。
[0273]
在一些实施方案中,缀合的可活化抗体包含在活化状态下结合至cd47的缀合的可活化抗体,所述抗体包含:特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab),其中ab特异性结合人cd47和食蟹猴cd47;当可活化抗体处于未裂解状态时抑制ab与cd47的结合的掩蔽部分(mm);偶合至ab的可裂解部分(cm),其中cm是用作蛋白酶的底物的多肽;和缀合至ab的剂,其中ab包含:(i)包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列,或(ii)包含氨基酸序列seq id no:1的重链可变区和包含氨基酸序列seq id no:2的轻链可变区,或(iii)包含选自由seq id no:11-14组成的组的氨基酸序列的重链和包含选自由seq id no:15、41-54、61-74、81-94和16-114组成的组的氨基酸序列的轻链;并且其中剂选自由以下组成的组:澳瑞他汀e、单甲基澳瑞他汀f(mmaf)、单甲基澳瑞他汀e(mmae)、单甲基澳瑞他汀d(mmad)、类美登素dm4、类美登素dm1、吡咯并苯并二氮杂吡咯并苯并二氮杂二聚体和倍癌霉素。在一些实施方案中,mm包含选自由seq id no:16-29组成的组的氨基酸序列。在一些实施方案中,mm包含选自由seq id no:17、23、24、25、27和28组成的组的氨基酸序列。在一些实施方案中,cm包含选自由seq id no:356-458、680-698、713、714和789-808组成的组的氨基酸序列。在一些实施方案中,cm包含选自由seq id no:359、370、377、382、390、397、406-425、429、430、446、447、450、680-698、713、714和807-808组成的组的氨基酸序列。在一些实施方案中,剂通过接头缀合至ab,并且其中剂缀合至ab的接头包含spdb部分、vc部分或peg2-vc部分。在一些实施方案中,缀合至ab的接头和毒素包含spdb-dm4部分、vc-mmad部分、vc-mmae部分、vc-倍癌霉素或peg2-vc-mmad部分。
[0274]
在一些实施方案中,缀合的可活化抗体包含如下缀合的可活化抗体,所述缀合的可活化抗体包含:在活化状态下结合cd47的抗体或其抗原结合片段(ab);和通过接头缀合至ab的毒素,其中缀合的可活化抗体包含选自表d中单行的氨基酸序列、接头和毒素,其中对于给定组合:(a)ab包含含有对应于表d所列单行中的给定组合的重链序列或重链可变结构域序列的氨基酸序列的重链;(b)ab包含含有对应于表d所列单行中的给定组合的轻链序列或轻链可变结构域序列的氨基酸序列的轻链;并且(c)接头和毒素包含对应于表d所列单行中的给定组合的接头和毒素。
[0275]
在一些实施方案中,可活化抗体由包含编码seq id no:1的重链可变区氨基酸序
列的核酸序列的核酸序列编码。在一些实施方案中,可活化抗体由包含编码seq id no:2的轻链可变区氨基酸序列的核酸序列的核酸序列编码。
[0276]
在一些实施方案中,可活化抗体由包含与编码seq id no:1的重链可变区氨基酸序列的核酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的核酸序列的核酸序列编码。在一些实施方案中,可活化抗体由包含与编码seq id no:2的轻链可变区氨基酸的核酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的核酸序列的核酸序列编码。
[0277]
本公开还提供了用于通过在导致可活化抗体表达的条件下培养细胞来产生本公开的可活化抗体的方法,其中所述细胞包含本公开的核酸分子或本公开的载体。
[0278]
本文还提供了制造在活化状态下结合cd47的可活化抗体的方法,所述方法包括:(a)在导致可活化抗体表达的条件下培养包含编码所述可活化抗体的核酸构建体的细胞,其中可活化抗体包含本公开的可活化抗体;以及(b)回收所述可活化抗体。
[0279]
在一些实施方案中,可活化抗体包括一种或多种多肽,其包括表b的给定行中的序列组合,或表c的掩蔽序列(mm)、底物序列(cm)、轻链可变结构域序列或轻链可变结构域cdr序列,和重链可变结构域序列或重链可变结构域cdr序列的任何组合。
[0280]
表b:cd47可活化抗体组合
[0281]
[0282]
[0283]
[0284]
[0285]
[0286]
[0287]
[0288]
[0289]
[0290]
[0291]
[0292]
[0293]
[0294]
[0295]
[0296]
[0297]
[0298]
[0299]
[0300]
[0301]
[0302]
[0303]
[0304]
[0305]
[0306]
[0307]
[0308]
[0309]
[0310]
[0311]
[0312]
[0313]
[0314]
[0315]
[0316][0317]
表c:cd47可活化抗体组分
[0318]
[0319]
[0320]
[0321]
[0322][0323]
在一些实施方案中,本公开的可活化抗体包括一种或多种多肽,其包括选自表b或表c的序列的组合,其中所述多肽包含以下的组合:选自表b或表c的标题为“掩蔽序列(mm)”的列的掩蔽序列,来自表b或表c的标题为“底物序列(cm)”的列的底物序列,来自表b或表c的标题为“vl或vl cdr”或“vl cdr seq id no”的列的轻链可变结构域或轻链cdr,和来自表b或表c的标题为“vh或vh cdr”或“vh cdr seq id no”的列的重链可变结构域或重链cdr。例如,本公开的可活化抗体可包括组合编号147的氨基酸序列,该组合包括seq id no:17的掩蔽序列、seq id no:412的底物序列、包括seq id no:15、16和18的vl cdr序列的轻链可变结构域,和包括11、12和13的vh cdr序列重链可变结构域。因此,本文描述了至少包括表b的任何给定行中的序列组合的可活化抗体。类似地,本文描述了表c的掩蔽序列(mm)、底物序列(cm)、轻链可变结构域序列或轻链可变结构域cdr序列,和重链可变结构域序列或重链可变结构域cdr序列的任何组合。本文还描述了至少包含选自表b或表c的对应列的掩蔽序列、底物序列、可变重链或可变重链cdr和可变轻链或可变轻链cdr的任何组合的可活化抗体。在一些实施方案中,包括表b的任何给定行中的序列组合或表c的掩蔽序列(mm)、底物序列(cm)、轻链可变结构域序列或轻链可变结构域cdr序列和重链可变结构域序列或重链可变结构域cdr序列的任何组合的可活化抗体可与一种或多种毒素组合,所述毒素包括多拉司他汀或其衍生物、澳瑞他汀或其衍生物、类美登素或其衍生物、倍癌霉素或其衍生物、卡奇霉素或其衍生物,或吡咯并苯并二氮杂或其衍生物。在一些实施方案中,包括表b的任何给定行中的序列组合或表c的掩蔽序列(mm)、底物序列(cm)、轻链可变结构域序列或轻链可变结构域cdr序列和重链可变结构域序列或重链可变结构域cdr序列的任何组合的可活化抗体可以一种或多种毒素组合,所述毒素包括澳瑞他汀e、单甲基澳瑞他汀f(mmaf)、单甲基澳瑞他汀e(mmae)、单甲基澳瑞他汀d(mmad)、类美登素dm4、类美登素dm1、吡咯并苯并二氮杂吡咯并苯并二氮杂二聚体和/或倍癌霉素。
[0324]
如上文所述的表b或表c中的任何组合可与人免疫球蛋白恒定区组合以产生完全人igg,包括igg1、igg2、igg4或突变的恒定区,从而产生具有改变的功能的人igg,诸如igg1 n297a、igg1 n297q或igg4 s228p。表b或表c中描述的组合不受任何给定行的特定组合的限制,因此可包括来自表b的第2列(或表c的第1列)的任何掩蔽序列与来自表b的第3列(或表c的第2列)的任何底物序列与来自表b的第4列(或表c的第3列)的任何vl序列或一组vl cdr序列与来自表b的第5列(或表c的第4列)的任何vh序列或一组vh cdr序列的组合。除表b的第2列或表c的第1列中公开的掩蔽序列之外,本文公开的任何掩蔽序列可组合使用。除表b的第3列或表c的第2列中公开的底物序列之外,本文公开的任何cm可组合使用。除表b的第4列或表c的第3列中公开的轻链可变区序列或轻链cdr序列之外,本文公开的任何轻链可变
区序列或轻链cdr序列可组合使用。除表b的第5列或表c的第4列中公开的重链可变区序列或重链cdr序列之外,本文公开的任何重链可变区序列或重链cdr序列可组合使用。
[0325]
在一些实施方案中,可活化抗体的血清半衰期长于相应抗体的血清半衰期,例如,可活化抗体的pk长于相应抗体的pk。在一些实施方案中,可活化抗体的血清半衰期与相应抗体的血清半衰期类似。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少15天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少12天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少11天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少10天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少9天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少8天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少7天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少6天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少5天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少4天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少3天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少2天。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少24小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少20小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少18小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少16小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少14小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少12小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少10小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少8小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少6小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少4小时。在一些实施方案中,当施用于生物体时,可活化抗体的血清半衰期为至少3小时。
[0326]
本公开还提供了通过在导致可活化cd47抗体多肽表达的条件下培养细胞来产生所述多肽的方法,其中所述细胞包含编码本文所述的抗体和/或可活化抗体的分离的核酸分子,和/或包括这些分离的核酸序列的载体。本公开提供了通过在导致抗体和/或可活化抗体表达的条件下培养细胞来产生所述抗体和/或可活化抗体的方法,其中所述细胞包含编码本文所述的抗体和/或可活化抗体的分离的核酸分子,和/或包括这些分离的核酸序列的载体。
[0327]
本发明还提供了一种制造在活化状态下结合cd47的可活化抗体的方法,所述方法通过以下进行:(a)在导致可活化抗体表达的条件下培养包含编码可活化抗体的核酸构建体的细胞,其中可活化抗体包含掩蔽部分(mm)、可裂解部分(cm)和特异性结合cd47的抗体或其抗原结合片段(ab),(i)其中cm为用作蛋白酶的底物的多肽;并且(ii)其中cm定位在可活化抗体中,使得当可活化抗体处于未裂解状态时,mm干扰ab与cd47的特异性结合,并且在裂解状态下,mm不干扰或竞争ab与cd47的特异性结合;以及(b)回收可活化抗体。适合的ab、mm和/或cm包括本文公开的任何ab、mm和/或cm。
[0328]
在一些实施方案中,处于未裂解状态的可活化抗体从n末端至c末端具有如下结构
排列:mm-cm-ab或ab-cm-mm。在一些实施方案中,可活化抗体包含mm与cm之间的连接肽。在一些实施方案中,可活化抗体包含cm与ab之间的连接肽。在一些实施方案中,可活化抗体包含第一连接肽(lp1)和第二连接肽(lp2),并且其中处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:mm-lp1-cm-lp2-ab或ab-lp2-cm-lp1-mm。在一些实施方案中,两个连接肽不需要彼此相同。在一些实施方案中,处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:间隔区-mm-lp1-cm-lp2-ab或ab-lp2-cm-lp1-mm-间隔区。
[0329]
在一些实施方案中,lp1或lp2中的至少一个包含选自由以下组成的组的氨基酸序列:(gs)n、(ggs)n、(gsggs)n(seq id no:116)和(gggs)n(seq id no:117),其中n为至少1的整数。
[0330]
在一些实施方案中,lp1或lp2中的至少一个包含选自由以下组成的组的氨基酸序列:ggsg(seq id no:118)、ggsgg(seq id no:119)、gsgsg(seq id no:120)、gsggg(seq id no:121)、gggsg(seq id no:122)、和gsssg(seq id no:123)。
[0331]
在一些实施方案中,lp1包含氨基酸序列gssggsggsggsg(seq id no:124)、gssggsggsgg(seq id no:125)、gssggsggsggs(seq id no:126)、gssggsggsggsgggs(seq id no:127)、gssggsggsg(seq id no:128)、gssggsggsgs(seq id no:129)或gggssggs(seq id no:134)。
[0332]
在一些实施方案中,lp2包含氨基酸序列gss、ggs、gggs(seq id no:130)、gssgt(seq id no:131)或gssg(seq id no:132)。
[0333]
在一些实施方案中,处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:间隔区-mm-lp1-cm-lp2-ab或ab-lp2-cm-lp1-mm-间隔区,其中lp1包含氨基酸序列gggssggs(seq id no:134)并且lp2包含氨基酸序列ggs。
[0334]
在一些实施方案中,处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:间隔区-mm-lp1-cm-lp2-ab或ab-lp2-cm-lp1-mm-间隔区,其中lp1包含氨基酸序列gggssggs(seq id no:134)并且lp2包含氨基酸序列gggs(seq id no:130)。
[0335]
缀合的cd47抗体和可活化抗体
[0336]
在一些实施方案中,本文所述的cd47抗体和可活化抗体还包含缀合至抗体/可活化抗体的剂。在一些实施方案中,缀合的剂为治疗剂,诸如抗炎剂和/或抗肿瘤剂。在此类实施方案中,剂与抗体/可活化抗体的碳水化合物部分缀合,例如,在一些实施方案中,其中碳水化合物部分位于可活化抗体的抗体或抗原结合片段的抗原结合区域之外。在一些实施方案中,剂与抗体/可活化抗体中抗体或抗原结合片段的巯基缀合。
[0337]
在一些实施方案中,剂为细胞毒性剂(诸如毒素(例如,细菌、真菌、植物或动物来源的酶活性毒素或其片段))或放射性同位素(即放射性缀合物)。
[0338]
在一些实施方案中,剂为可检测的部分,例如像标记或其他标志物。例如,剂是或包括放射性标记的氨基酸、可通过标志亲和素(例如,含有可通过光学或量热法检测的荧光标志物或酶活性的链霉亲和素)检测的一个或多个生物素部分、一种或多种放射性同位素或放射性核素、一种或多种荧光标记、一种或多种酶标记和/或一种或多种化学发光剂。在一些实施方案中,可检测的部分通过间隔区分子附接。
[0339]
本公开还涉及包含缀合至细胞毒性剂(诸如毒素(例如,细菌、真菌、植物或动物来源的酶活性毒素或其片段))或放射性同位素(即放射性缀合物)的抗体的免疫缀合物。合适
的细胞毒性剂包括例如多拉司他汀及其衍生物(例如,澳瑞他汀e、afp、mmaf、mmae、mmad、dmaf、dmae)。例如,剂为单甲基澳瑞他汀e(mmae)或单甲基澳瑞他汀d(mmad)。在一些实施方案中,剂为选自表e中列出的组的剂。在一些实施方案中,剂为多拉司他汀。在一些实施方案中,剂为澳瑞他汀或其衍生物。在一些实施方案中,剂为澳瑞他汀e或其衍生物。在一些实施方案中,剂为单甲基澳瑞他汀e(mmae)。在一些实施方案中,剂为单甲基澳瑞他汀d(mmad)。在一些实施方案中,剂为类美登素或类美登素衍生物。在一些实施方案中,剂为dm1或dm4。在一些实施方案中,剂为倍癌霉素或其衍生物。在一些实施方案中,剂为卡奇霉素(calicheamicin)或其衍生物。在一些实施方案中,剂为吡咯并苯并二氮杂在一些实施方案中,剂为吡咯并苯并二氮杂二聚体。
[0340]
可使用的酶活性毒素及其片段包括白喉a链、白喉毒素的非结合活性片段、外毒素a链(来自铜绿假单胞菌(pseudomonas aeruginosa))、蓖麻毒素(ricin)a链、相思豆毒素(abrin)a链、蒴莲根毒素(modeccin)a链、α-八叠球菌素(alpha-sarcin)、油桐(aleurites fordii)蛋白、香石竹毒(dianthin)蛋白、美洲商陆(phytolaca americana)蛋白(papi、papii和pap-s)、苦瓜(momordica charantia)抑制剂、麻风树毒蛋白(curcin)、巴豆毒素(crotin)、肥皂草(sapaonaria officinalis)抑制剂、白树毒素(gelonin)、米托菌素(mitogellin)、局限曲霉素(restrictocin)、酚霉素(phenomycin)、伊诺霉素(enomycin)和单端孢霉烯族毒素(tricothecene)。多种放射性核素可用于产生放射性缀合的抗体。实例包括
212
bi、
131
i、
131
in、
90
y和
186
re。
[0341]
在一些实施方案中,剂为毒素或其片段。在一些实施方案中,剂为微管抑制剂。在一些实施方案中,剂为核酸损伤剂。在一些实施方案中,剂选自由以下组成的组:多拉司他汀或其衍生物、澳瑞他汀或其衍生物、类美登素或其衍生物、倍癌霉素或其衍生物、卡奇霉素或其衍生物和吡咯并苯并二氮杂或其衍生物。在一些实施方案中,剂为澳瑞他汀e或其衍生物。在一些实施方案中,剂为单甲基澳瑞他汀e(mmae)。在一些实施方案中,剂为单甲基澳瑞他汀d(mmad)。在一些实施方案中,剂为选自由dm1和dm4组成的组的类美登素。在一些实施方案中,剂为类美登素dm4。在一些实施方案中,剂为倍癌霉素。在一些实施方案中,剂通过接头缀合至ab。在一些实施方案中,剂缀合至ab所采用的接头包含spdb部分、vc部分或peg2-vc部分。在一些实施方案中,缀合至ab的接头和毒素包含spdb-dm4部分、vc-mmad部分、vc-mmae部分、vc-倍癌霉素或peg2-vc-mmad部分。在一些实施方案中,接头为可裂解的接头。在一些实施方案中,接头为不可裂解的接头。在一些实施方案中,剂为可检测部分。在一些实施方案中,可检测部分为诊断剂。
[0342]
在一些实施方案中,缀合的可活化抗体包含抗体,所述抗体包含:(a)特异性结合至哺乳动物cd47的抗体或其抗原结合片段(ab),其中ab包含:(i)包含氨基酸序列gytftny(seq id no:3)或氨基酸序列nywmt(seq id no:4)的vh cdr1序列;包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列;包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列;包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列;包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列;和包含氨基酸
序列fqgshvprt(seq id no:10)的vl cdr3序列,或(ii)包含氨基酸序列seq id no:1的重链可变区和包含氨基酸序列seq id no:2的轻链可变区;(b)缀合至ab的剂,其中剂选自由以下组成的组:澳瑞他汀e、单甲基澳瑞他汀f(mmaf)、单甲基澳瑞他汀e(mmae)、单甲基澳瑞他汀d(mmad)、类美登素dm4、类美登素dm1、吡咯并苯并二氮杂吡咯并苯并二氮杂二聚体和倍癌霉素。
[0343]
本公开的cd47抗体和可活化抗体具有针对剂的至少一个缀合点,但是在本文提供的方法和组合物中,少于所有可能的缀合点可用于与剂缀合。在一些实施方案中,一个或多个缀合点是涉及二硫键的硫原子。在一些实施方案中,一个或多个缀合点是涉及链间二硫键的硫原子。在一些实施方案中,一个或多个缀合点是涉及链间二硫键的硫原子,而不是涉及链内二硫键的硫原子。在一些实施方案中,一个或多个缀合点是半胱氨酸或含有硫原子的其他氨基酸残基的硫原子。此类残基可天然存在于抗体结构中,或可通过定点诱变、化学转化或错误掺入非天然氨基酸而掺入抗体中。
[0344]
还提供了制备在ab中具有一个或多个链间二硫键且在mm中具有一个或多个链内二硫键的cd47抗体/cd47可活化抗体的缀合物的方法,并且提供了一种与游离硫醇反应的药物。所述方法通常包括用还原剂例如像tcep部分还原抗体/可活化抗体中的链间二硫键;以及使与游离硫醇反应的药物缀合至部分还原的可活化抗体。如本文所用,术语部分还原是指其中抗体/可活化抗体与还原剂接触并且少于所有二硫键(例如,少于所有可能的缀合位点)被还原的情况。在一些实施方案中,少于99%、98%、97%、96%、95%、90%、85%、80%、75%、70%、65%、60%、55%、50%、45%、40%、35%、30%、25%、20%、15%、10%或少于5%的所有可能的缀合位点被还原。
[0345]
在其他实施方案中,提供了一种将剂(例如药物)还原并缀合至cd47抗体/cd47可活化抗体从而导致剂具有布置的选择性的方法。所述方法通常包括用还原剂部分还原cd47抗体/cd47可活化抗体,使得cd47抗体/cd47可活化抗体的掩蔽部分或其他非ab部分中的任何缀合位点不被还原,以及将所述剂缀合至ab中的链间硫醇。选择一个或多个缀合位点以便允许所需剂布置,以允许在所需位点发生缀合。还原剂为例如tcep。还原反应条件(例如像还原剂与抗体/可活化抗体的比率、孵育时间、在孵育期间的温度、还原反应溶液的ph等)通过鉴别产生缀合的抗体/可活化抗体的条件例如产生缀合的可活化抗体的条件来确定,其中mm保留有效且高效地掩蔽未裂解状态下的可活化抗体的ab的能力。还原剂与抗体/可活化抗体的比率将根据抗体/可活化抗体而变化。在一些实施方案中,还原剂与抗体/可活化抗体的比率的范围将为约20:1至1:1、约10:1至1:1、约9:1至1:1、约8:1至1:1、约7:1至1:1、约6:1至1:1、约5:1至1:1、约4:1至1:1、约3:1至1:1、约2:1至1:1、约20:1至1:1.5、约10:1至1:1.5、约9:1至1:1.5、约8:1至1:1.5、约7:1至1:1.5、约6:1至1:1.5、约5:1至1:1.5、约4:1至1:1.5、约3:1至1:1.5、约2:1至1:1.5、约1.5:1至1:1.5或约1:1至1:1.5。在一些实施方案中,比率的范围为约5:1至1:1。在一些实施方案中,比率的范围为约5:1至1.5:1。在一些实施方案中,比率的范围为约4:1至1:1。在一些实施方案中,比率的范围为约4:1至1.5:1。在一些实施方案中,比率的范围为约8:1至约1:1。在一些实施方案中,比率的范围为约2.5:1至1:1。
[0346]
在一些实施方案中,cd47抗体首先经历缀合,然后进一步修饰以包括cm和mm(产生可活化抗体)。在一些实施方案中,cd47可活化抗体是缀合的。
[0347]
在一些实施方案中,提供了一种还原可活化cd47抗体的ab中的链间二硫键并使剂(例如,含有硫醇的剂诸如药物)缀合至所得链间硫醇以选择性地将一种或多种剂定位在ab上的方法。所述方法通常包括用还原剂部分还原ab以形成至少两种链间硫醇而不在可活化抗体中形成所有可能的链间硫醇;以及使所述剂与部分还原的ab的链间硫醇缀合。例如,将可活化抗体的ab在约37℃下以所需的还原剂:可活化抗体比率部分还原约1小时。在一些实施方案中,还原剂与可活化抗体的比率的范围将为约20:1至1:1、约10:1至1:1、约9:1至1:1、约8:1至1:1、约7:1至1:1、约6:1至1:1、约5:1至1:1、约4:1至1:1、约3:1至1:1、约2:1至1:1、约20:1至1:1.5、约10:1至1:1.5、约9:1至1:1.5、约8:1至1:1.5、约7:1至1:1.5、约6:1至1:1.5、约5:1至1:1.5、约4:1至1:1.5、约3:1至1:1.5、约2:1至1:1.5、约1.5:1至1:1.5或约1:1至1:1.5。在一些实施方案中,比率的范围为约5:1至1:1。在一些实施方案中,比率的范围为约5:1至1.5:1。在一些实施方案中,比率的范围为约4:1至1:1。在一些实施方案中,比率的范围为约4:1至1.5:1。在一些实施方案中,比率的范围为约8:1至约1:1。在一些实施方案中,比率的范围为约2.5:1至1:1。
[0348]
含有硫醇的试剂可为例如半胱氨酸或n-乙酰基半胱氨酸。还原剂可为例如tcep。在一些实施方案中,可在缀合之前使用例如柱色谱法、透析或透滤来纯化还原的可活化抗体。或者,在部分还原之后且在缀合之前不对还原的抗体进行纯化。
[0349]
本发明还提供了部分还原的抗体/可活化抗体,其中在不干扰抗体/可活化抗体中的任何链内二硫键的情况下,已用还原剂还原可活化抗体中的至少一个链间二硫键,其中可活化抗体包含特异性结合至cd47的抗体或其抗原结合片段(ab)、抑制未裂解状态的可活化抗体的ab与cd47的结合的掩蔽部分(mm)以及偶合至ab的可裂解部分(cm),其中cm为用作蛋白酶的底物的多肽。在一些实施方案中,mm通过cm偶合至ab。在一些实施方案中,抗体/可活化抗体的一个或多个链内二硫键不被还原剂干扰。在一些实施方案中,抗体/可活化抗体内的mm的一个或多个链内二硫键不被还原剂干扰。在一些实施方案中,处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:mm-cm-ab或ab-cm-mm。在一些实施方案中,还原剂为tcep。
[0350]
在其他实施方案中,一种通过提供具有限定数目和位置的赖氨酸和/或半胱氨酸残基的可活化cd47抗体,将剂(例如药物)还原并缀合至cd47抗体/cd47可活化抗体从而导致剂具有布置的选择性的方法。在一些实施方案中,限定数目的赖氨酸和/或半胱氨酸残基高于或低于亲本抗体或可活化抗体的氨基酸序列中对应残基的数目。在一些实施方案中,限定数目的赖氨酸和/或半胱氨酸残基可产生限定数目的可与抗cd47抗体或可活化抗cd47抗体缀合的剂当量。在一些实施方案中,限定数目的赖氨酸和/或半胱氨酸残基可产生限定数目的可以位点特异性方式与抗cd47抗体或可活化抗cd47抗体缀合的剂当量。在一些实施方案中,修饰的可活化抗体以位点特异性方式经一种或多种非天然氨基酸修饰,因此在一些实施方案中,将剂的缀合限于仅非天然氨基酸的位点。在一些实施方案中,可用如本文所论述的还原剂部分还原具有限定数目和位置的赖氨酸和/或半胱氨酸残基的抗cd47抗体或可活化抗cd47抗体,使得可活化抗体的掩蔽部分或其他非ab部分至的任何缀合位点不被还原,并且将剂缀合至ab中的链间硫醇。
[0351]
本公开还提供了部分还原的可活化抗体,其中在不干扰可活化抗体中的任何链内二硫键的情况下,已用还原剂还原可活化抗体中的至少一个链间二硫键,其中可活化抗体
包含特异性结合至靶标(例如cd47)的抗体或其抗原结合片段(ab)、抑制未裂解状态的可活化抗体的ab与靶标的结合的掩蔽部分(mm)以及偶合至ab的可裂解部分(cm),其中cm为用作至少一种蛋白酶的底物的多肽。在一些实施方案中,mm通过cm偶合至ab。在一些实施方案中,可活化抗体的一个或多个链内二硫键不被还原剂干扰。在一些实施方案中,可活化抗体内的mm的一个或多个链内二硫键不被还原剂干扰。在一些实施方案中,处于未裂解状态的可活化抗体从n末端至c末端具有如下结构排列:mm-cm-ab或ab-cm-mm。在一些实施方案中,还原剂为tcep。
[0352]
在一些实施方案中,使用马来酰亚胺己酰基-缬氨酸-瓜氨酸接头或马来酰亚胺peg-缬氨酸-瓜氨酸接头将剂连接到ab。在一些实施方案中,使用马来酰亚胺己酰基-缬氨酸-瓜氨酸接头将剂连接到ab。在一些实施方案中,使用马来酰亚胺peg-缬氨酸-瓜氨酸接头将剂连接到ab。在一些实施方案中,所述剂是使用马来酰亚胺peg-缬氨酸-瓜氨酸-对氨基苄氧基羰基接头连接到ab的单甲基澳瑞他汀d(mmad),并且此接头有效载荷构建体在本文中称为“vc-mmad”。在一些实施方案中,所述剂是使用马来酰亚胺peg-缬氨酸-瓜氨酸-对氨基苄氧基羰基接头连接到ab的单甲基澳瑞他汀e(mmae),并且此接头有效载荷构建体在本文中称为“vc-mmae”。在一些实施方案中,使用马来酰亚胺peg-缬氨酸-瓜氨酸接头将剂连接到ab。在一些实施方案中,所述剂是使用马来酰亚胺双-peg-缬氨酸-瓜氨酸-对氨基苄氧基羰基接头连接到ab的单甲基澳瑞他汀d(mmad),并且此接头有效载荷构建体在本文中称为“peg2-vc-mmad”。vc-mmad、vc-mmae和peg2-vc-mmad的结构如下所示:
[0353]
vc-mmad:
[0354][0355]
vc-mmae:
[0356][0357]
peg2-vc-mmad:
[0358]
[0359]
本公开还提供了缀合的可活化抗体,其包含连接到单甲基澳瑞他汀d(mmad)有效载荷的可活化抗体,其中可活化抗体包含特异性结合至靶标的抗体或其抗原结合片段(ab)、抑制未裂解状态的可活化抗体的ab与靶标的结合的掩蔽部分(mm)以及偶合至ab的可裂解部分(cm),并且cm为用作至少一种mmp蛋白酶的底物的多肽。
[0360]
在一些实施方案中,mmad缀合的可活化抗体可使用以下几种用于将剂附接到ab的方法中的任一种进行缀合:(a)附接到ab的碳水化合物部分,或(b)附接到ab的巯基,或(c)附接到ab的氨基,或(d)附接到ab的羧基。
[0361]
在一些实施方案中,mmad有效载荷通过接头缀合至ab。在一些实施方案中,mmad有效载荷通过接头缀合至ab中的半胱氨酸。在一些实施方案中,mmad有效载荷通过接头缀合至ab中的赖氨酸。在一些实施方案中,mmad有效载荷通过接头缀合至ab的另一个残基,诸如本文公开的那些残基。在一些实施方案中,接头为含硫醇的接头。在一些实施方案中,接头为可裂解的接头。在一些实施方案中,接头为不可裂解的接头。在一些实施方案中,接头选自由表7和表8中示出的接头组成的组。在一些实施方案中,可活化抗体和mmad有效载荷通过马来酰亚胺己酰基-缬氨酸-瓜氨酸接头连接。在一些实施方案中,可活化抗体和mmad有效载荷通过马来酰亚胺peg-缬氨酸-瓜氨酸接头连接。在一些实施方案中,可活化抗体和mmad有效载荷通过马来酰亚胺己酰基-缬氨酸-瓜氨酸-对氨基苄氧基羰基接头连接。在一些实施方案中,可活化抗体和mmad有效载荷通过马来酰亚胺peg-缬氨酸-瓜氨酸-对氨基苄氧基羰基接头连接。在一些实施方案中,使用本文公开的部分还原和缀合技术将mmad有效载荷缀合至ab。
[0362]
在一些实施方案中,本公开的接头的聚乙二醇(peg)组分由2个乙二醇单体、3个乙二醇单体、4个乙二醇单体、5个乙二醇单体、6个乙二醇单体、7个乙二醇单体、8个乙二醇单体、9个乙二醇单体或至少10个乙二醇单体形成。在本公开的一些实施方案中,peg组分是支化聚合物。在本公开的一些实施方案中,peg组分是非支化聚合物。在一些实施方案中,peg聚合物组分经氨基或其衍生物、羧基或其衍生物或氨基或其衍生物和羧基或其衍生物两者官能化。
[0363]
在一些实施方案中,本公开的接头的peg组分是氨基-四乙二醇-羧基或其衍生物。在一些实施方案中,本公开的接头的peg组分是氨基-三乙二醇-羧基或其衍生物。在一些实施方案中,本公开的接头的peg组分是氨基-二乙二醇-羧基或其衍生物。在一些实施方案中,氨基衍生物是在氨基与其所缀合的羧基之间的酰胺键的形成物。在一些实施方案中,羧基衍生物是在羧基与其所缀合的氨基之间的酰胺键的形成物。在一些实施方案中,羧基衍生物是在羧基与其所缀合的羟基之间的酯键的形成物。
[0364]
抗体和细胞毒性剂的缀合物使用多种双功能蛋白偶合剂制成,所述偶合剂诸如3-(2-吡啶基二巯基)丙酸n-琥珀酰亚胺酯(spdp)、亚氨基硫烷(iminothiolane,it)、亚氨酸酯的双功能衍生物(诸如己二酸二甲酯hcl)、活性酯(诸如辛二酸二琥珀酰亚胺酯)、醛(诸如戊二醛)、双叠氮基化合物(诸如双(对叠氮基苯甲酰基)己二胺)、双重氮衍生物(诸如双(对重氮苯甲酰基)-乙二胺)、二异氰酸酯(诸如甲苯2,6-二异氰酸酯)和双活性氟化合物(诸如1,5-二氟-2,4-二硝基苯)。例如,蓖麻毒素免疫毒素可如vitetta等人,science 238:1098(1987)中所述来制备。碳-14标记的1-异硫氰酸苄基-3-甲基二亚乙基三胺五乙酸(mx-dtpa)是用于将放射性核苷酸缀合至抗体的示例性螯合剂。(参见wo94/11026)。
[0365]
表e列出了可在本文描述的公开中采用的一些示例性药剂,但绝不意味着是详尽的列表。
[0366]
表e:用于缀合的示例性药剂
[0367]
细胞毒性剂
[0368]
[0369][0370]
抗病毒药
[0371][0372]
抗细菌药
[0373]
nhs(n-羟基磺基-琥珀酰亚胺:pierce chem.co.,目录号24510)。另外的接头包括但不限于smcc((4-(n-马来酰亚胺基甲基)环己烷-1-羧酸琥珀酰亚胺酯)、磺基-smcc(4-(n-马来酰亚胺基甲基)环己烷-1-羧酸磺基琥珀酰亚胺酯)、spdb(n-琥珀酰亚胺基-4-(2-吡啶基二硫代)丁酸酯)或磺基-spdb(n-琥珀酰亚胺基-4-(2-吡啶基二硫代)-2-磺基丁酸酯)。
[0379]
上文所述接头含有具有不同属性的组分,因此导致具有不同物理化学性质的缀合物。例如,羧酸烷基酯的磺基-nhs酯比羧酸芳基酯的磺基-nhs酯更稳定。含nhs酯的接头比磺基-nhs酯的溶解度低。此外,接头smpt含有空间位阻的二硫键,并且可形成具有提高的稳定性的缀合物。一般来说,二硫键联的稳定性低于其他键联,因为二硫键联在体外被裂解,从而导致可用的缀合物较少。磺基-nhs尤其可增强碳二亚胺偶合的稳定性。当与磺基-nhs结合使用时碳二亚胺偶合(诸如edc)形成的酯对水解的抵抗力大于单独的碳二亚胺偶合反应形成的酯对水解的抵抗力。
[0380]
在一些实施方案中,接头可裂解。在一些实施方案中,接头不可裂解。在一些实施方案中,存在两个或更多个接头。所述两个或更多个接头都是相同的,即,可裂解或不可裂解的,或者所述两个或更多个接头是不同的,即,至少一个可裂解和至少一个不可裂解。
[0381]
本公开利用以下几种用于将剂附接到ab的方法:(a)附接到ab的碳水化合物部分,或(b)附接到ab的巯基,或(c)附接到ab的氨基,或(d)附接到ab的羧基。根据本公开,ab可通过具有至少两个反应性基团的中间接头共价附接到剂,所述反应性基团中一个接头与ab反应并且一个接头与剂反应。可选择可以包括任何相容的有机化合物的接头,使得与ab(或剂)的反应不会不利地影响ab的反应性和选择性。此外,接头与剂的附接可能不破坏剂的活性。用于与氧化的抗体或氧化的抗体片段反应的合适的接头包括含有选自由以下组成的组的胺的那些接头:伯胺、仲胺、肼、酰肼、羟胺、苯肼、氨基脲和氨基硫脲基团。此类反应性官能团可作为接头结构的一部分存在,或可通过对不含此类基团的接头进行合适的化学修饰来引入。
[0382]
根据本公开,用于附接至还原的ab的合适的接头包括具有能够与还原的抗体或片段的巯基反应的某些反应性基团的那些接头。此类反应性基团包括但不限于:反应性卤代烷基(包括例如卤代乙酰基)、对汞基苯甲酸酯基团和能够进行迈克尔型(michael-type)加成反应的基团(包括例如马来酰亚胺以及由mitra和lawton,1979,j.amer.chem.soc.16:3097-3110所描述类型的基团)。
[0383]
根据本公开,用于附接至既不氧化也不还原的ab的合适的接头包括具有能够与ab中未修饰的赖氨酸残基中存在的伯氨基反应的某些官能团的那些接头。此类反应性基团包括但不限于nhs羧酸酯或碳酸酯、磺基-nhs羧酸酯或碳酸酯、4-硝基苯基羧酸酯或碳酸酯、五氟苯基羧酸酯或碳酸酯、酰基咪唑、异氰酸酯和异硫氰酸酯。
[0384]
根据本公开,用于附接至既不氧化也不还原的ab的合适的接头包括具有能够与ab中天冬氨酸残基或谷氨酸残基中存在的羧酸基团反应的某些官能团的那些接头,所述官能团已被合适的试剂活化。合适的活化试剂包括具有或不具有添加的nhs或磺基-nhs的edc,以及用于羧酰胺形成的其他脱水剂。在这些情况下,存在于合适的接头中的官能团将包含伯胺和仲胺、肼、羟胺和酰肼。
[0385]
可在将接头附接至ab之前或之后将剂附接至接头。在某些应用中,可能期望首先制备ab-接头中间体,其中所述接头不含缔合剂。根据特定应用,然后可将特定的剂共价附
接至接头。在一些实施方案中,出于缀合目的,首先将ab附接至mm、cm和缔合的接头,并且然后将其附接至接头。
[0386]
支链接头:在特定的实施方案中,利用具有用于附接剂的多个位点的支链接头。对于多位点接头,与ab的单共价附接将产生能够在许多位点处结合剂的ab接头中间体。所述位点可为可与醛或巯基或剂附接的任何化学位点。
[0387]
在一些实施方案中,可通过在ab上的多个位点处附接单个位点接头来实现更高的比活度(或更高的剂与ab的比率)。可通过两种方法中的任一种将所述多个位点引入ab中。首先,可在同一ab中产生多个醛基和/或巯基。第二,可将具有用于后续附接至接头的多个功能位点的“支化接头”附接至ab的醛或巯基。支化接头或多位点接头的功能位点可以是醛或巯基,或者可以是接头可附接的任何化学位点。可通过将这两种方法组合(即在ab上的多个位点处附接多位点接头)来获得更高的比活度。
[0388]
可裂解接头:易于被补体系统的酶裂解的肽接头可用于本公开的一个实施方案中,所述酶诸如但不限于u-纤溶酶原活化物、组织纤溶酶原活化物、胰蛋白酶、纤溶酶或具有蛋白水解活性的另一种酶。根据本公开的一种方法,剂通过易于被补体裂解的接头附接。抗体选自可活化补体的类别。因此,抗体-剂缀合物活化补体级联并在靶位点释放剂。根据本公开的另一种方法,剂通过易于被具有蛋白水解活性的酶裂解的接头附接,所述酶诸如u-纤溶酶原活化物、组织纤溶酶原活化物、纤溶酶或胰蛋白酶。这些可裂解接头可用于包括细胞外毒素的缀合的可活化抗体中,所述细胞外毒素以非限制性实例的方式例如表e中所示的任何细胞外毒素。
[0389]
表f提供可裂解接头序列的非限制性实例。
[0390]
表f:用于缀合的示例性接头序列
[0391][0392][0393]
另外,剂可通过二硫键(例如,半胱氨酸分子上的二硫键)附接至ab。由于许多肿瘤自然释放高水平的谷胱甘肽(一种还原剂),因此其可还原二硫键,随后在递送位点释放所述剂。在一些实施方案中,将修饰cm的还原剂还将修饰缀合的可活化抗体的接头。
[0394]
间隔区和可裂解元件:在一些实施方案中,可能有必要以优化所述剂与可活化抗
体的ab之间的间隔的方式构建接头。这可通过使用具有以下通用结构的接头来完成:
[0395]w–
(ch2)n
–q[0396]
其中
[0397]
w为
‑‑
nh
‑‑
ch2‑‑
或
‑‑
ch2‑‑
;
[0398]
q为氨基酸、肽;并且
[0399]
n为0至20的整数。
[0400]
在一些实施方案中,接头可包含间隔区元件和可裂解元件。间隔区元件用于将可裂解元件定位成远离ab的核心,以使得可裂解元件更易于接近负责裂解的酶。上文所述的某些支链接头可充当间隔区元件。
[0401]
在整个讨论中,应当理解,接头与剂的附接(或间隔区元件与可裂解元件的附接,或可裂解元件与剂的附接)不需要是特定的附接或反应模式。提供具有适当稳定性和生物相容性的产物的任何反应都是可接受的。
[0402]
血清补体以及接头的选择:根据本公开的一种方法,当需要释放剂时,使用作为可活化补体的一类抗体的ab。所得缀合物保留结合抗原补并活化补体级联两者的能力。因此,根据本公开的这一实施方案,剂连接至可裂解接头或可裂解元件的一端,并且接头基团的另一端附接至ab上的特异性位点。例如,如果剂具有羟基或氨基,则可分别通过酯或酰胺键将其附接至肽、氨基酸或其他合适选择的接头的羧基末端。例如,此类剂可通过碳二亚胺反应附接至接头肽。如果剂含有将干扰与接头的附接的官能团,那么可在附接之前封闭这些干扰官能团,并且一旦制得产物缀合物或中间体即加以去封闭。然后直接或在进一步修饰后使用接头的相反末端或氨基末端,以结合至能够活化补体的ab。
[0403]
接头(或接头的间隔区元件)可具有任何所需的长度,其一端可共价附接到可活化抗体的ab上的特异性位点。接头或间隔区元件的另一端可附接至氨基酸或肽接头。
[0404]
因此,当这些缀合物在补体存在下结合至抗原时,使剂附接至接头的酰胺或酯键将被裂解,从而导致所述剂以其活性形式释放。当施用于受试者时,这些缀合物将完成所述剂在靶位点处的递送和释放,并且特别有效于在体内递送如呈现于但不限于表e中的那些的药剂、抗生素、抗代谢物、抗增殖剂等。
[0405]
在无补体活化情况下释放的接头:在靶向递送的又一应用中,由于补体级联的活化将最终溶解靶细胞,因此需要在无补体活化的情况下释放所述剂。因此,当应在不杀死靶细胞的情况下完成剂的递送和释放时,此方法有用。当需要将细胞介体诸如激素、酶、皮质类固醇、神经递质、基因或酶递送至靶标细胞时,这就是目标。这些缀合物可通过经由适度易于被血清蛋白酶裂解的接头将剂附接到不能活化补体的ab而制备。当将这种缀合物施用于个体时,抗原-抗体复合物将快速形成,而剂的裂解将缓慢发生,从而导致化合物在靶位点处释放。
[0406]
生物化学交联剂:在一些实施方案中,可使用某些生物化学交联剂将可活化抗体缀合至一种或多种治疗剂。交联试剂形成将两个不同分子的官能团连结在一起的分子桥。为了以逐步方式连接两种不同的蛋白质,可使用消除不想要的均聚物形成的异双官能交联剂。
[0407]
可通过溶酶体蛋白酶裂解的肽基接头也是有用的,例如val-cit、val-ala或其他二肽。另外,可使用在溶酶体的低ph环境中可裂解的酸不稳定的接头,例如:双唾液酸醚。其
他合适的接头包括组织蛋白酶不稳定的底物,特别是在酸性ph下显示最佳功能的那些底物。
[0408]
表g中引用了示例性异双官能交联剂。
[0409]
表g:示例性异双官能交联剂
[0410]
[0411][0412]
不可裂解的接头或直接附接:在本公开的一些实施方案中,缀合物可被设计成使得剂被递送至靶标但未释放。这可通过将剂直接或经由不可裂解的接头附接至ab来完成。
[0413]
这些不可裂解的接头可包括氨基酸、肽、d-氨基酸或可被修饰以包含随后可通过本文所述的方法用于附接至ab的官能团的其他有机化合物。此种有机接头的通式可为
[0414]w–
(ch2)n
–q[0415]
其中
[0416]
w为
‑‑
nh
‑‑
ch2‑‑
或
‑‑
ch2‑‑
;
[0417]
q为氨基酸、肽;并且
[0418]
n为0至20的整数。
[0419]
不可裂解的缀合物:在一些实施方案中,化合物可附接至不活化补体的ab。当使用不能进行补体活化的ab时,可使用易于被活化的补体裂解的接头或使用不易于被活化的补体裂解的接头来完成这种附接。
[0420]
本文公开的抗体也可配制为免疫脂质体。含有抗体的脂质体通过本领域已知的方法制备,诸如以下所述的方法:epstein等人,proc.natl.acad.sci.usa,82:3688(1985);hwang等人,proc.natl acad.sci.usa,77:4030(1980);以及美国专利号4,485,045和4,544,545。循环时间增加的脂质体公开于美国专利号5,013,556中。
[0421]
特别有用的脂质体可通过反相蒸发法使用包含磷脂酰胆碱、胆固醇和peg-衍生的磷脂酰乙醇胺(peg-pe)的脂质组合物产生。通过具有限定的孔径的过滤器挤出脂质体,以产生具有所需直径的脂质体。本公开的抗体的fab'片段可通过二硫化物交换反应缀合至脂质体,如martin等人,j.biol.chem.,257:286-288(1982)中所述。
[0422]
cd47抗体药物缀合物和cd47可活化抗体药物缀合物
[0423]
在一些实施方案中,抗体药物缀合物(adc)和可活化抗体药物缀合物(aadc)可包括一种或多种多肽,其包括表d的给定行中的轻链序列或轻链可变结构域序列和重链序列或重链可变结构域序列、接头和毒素的组合,或表d的轻链序列或轻链可变结构域序列和重链序列或重链可变结构域序列、接头和毒素的任何组合。例如,组合编号1包含缀合至mmad毒素的seq id no.1的重链、seq id no.160的轻链、vc接头。
[0424]
表d:cd47可活化adc组合
[0425]
[0426]
[0427]
[0428][0429]
列出重链和轻链可变区的表d中的任何组合可与人免疫球蛋白恒定区组合以产生完全人igg,包括igg1、igg2、igg4或突变的恒定区,从而产生具有改变的功能的人igg,诸如igg1 n297a、igg1n297q或igg4 s228p。表d中描述的组合不受任何给定行中所示的特定组合的限制,因此可以包括来自表d的第2列的任何重链序列或重链可变区序列与来自表d的第3列的任何轻链序列或轻链可变区序列与来自第4列的任何接头与来自第5列的任何毒素的组合。除第2列中列出的重链序列或重链可变区序列之外,本文公开的任何重链序列或重链可变区序列可组合使用。除第3列中列出的轻链序列或轻链可变区序列之外,本文公开的任何轻链序列或轻链可变区序列可组合使用。除第4列中列出的接头之外,本文公开的任何接头可组合使用。除第5列中列出的毒素之外,本文公开的任何毒素可组合使用。
[0430]
多特异性抗体和可活化抗体
[0431]
在一些实施方案中,可活化cd47抗体和/或缀合的可活化cd47抗体为单特异性的。在一些实施方案中,可活化cd47抗体和/或缀合的可活化cd47抗体为多特异性的,例如,作为非限制性实例,为双特异性的或三功能的。
[0432]
在一些实施方案中,可活化cd47抗体和/或缀合的可活化cd47抗体被配制为pro-双特异性t细胞衔接蛋白(bite)分子的一部分。在一些实施方案中,可活化cd47抗体和/或缀合的可活化cd47抗体被配制为pro-嵌合抗原受体(car)修饰的t细胞或其他工程化受体的一部分。
[0433]
本公开还相应地提供了多特异性cd47抗体。本文提供的多特异性抗体是识别cd47和至少一种或多种不同抗原或表位的多特异性抗体。
[0434]
本公开还提供了多特异性cd47可活化抗体。本文提供的多特异性可活化抗体为多特异性抗体,其识别cd47和至少一种或更多种不同抗原或表位,并且包含至少一个掩蔽部分(mm),其与多特异性抗体的至少一个抗原或表位结合结构域连接,使得mm的偶合降低抗原或表位结合结构域结合其靶标的能力。在一些实施方案中,mm通过用作至少一种蛋白酶的底物的可裂解部分(cm)偶合至多特异性抗体的抗原或表位结合结构域。本文提供的可活化多特异性抗体在循环中稳定,在预期的治疗和/或诊断位点活化,但在正常组织(即健康组织)中不活化,并且在活化时表现出与相应的未修饰的多特异性抗体至少相当的与靶标的结合。
[0435]
在一些实施方案中,可活化抗体或其抗原结合片段并入多特异性可活化抗体或其抗原结合片段中,其中多特异性可活化抗体的至少一个臂特异性结合cd47。在一些实施方案中,可活化抗体或其抗原结合片段并入双特异性抗体或其抗原结合片段中,其中双特异性可活化抗体的至少一个臂特异性结合cd47。
[0436]
在一些实施方案中,抗体或其抗原结合片段并入多特异性抗体或其抗原结合片段中,其中多特异性抗体或其抗原结合片段的至少一个臂特异性结合cd47。在一些实施方案中,抗体或其抗原结合片段并入双特异性抗体或其抗原结合片段中,其中双特异性抗体或其抗原结合片段的至少一个臂特异性结合cd47。
[0437]
在一些实施方案中,多特异性抗体或其抗原结合片段,例如,双特异性抗体或其抗原结合片段的至少一个臂包含seq id no:1的重链可变区氨基酸序列。在一些实施方案中,多特异性抗体或其抗原结合片段,例如,双特异性抗体或其抗原结合片段的至少一个臂包含seq id no:2的轻链可变区氨基酸序列。
[0438]
在一些实施方案中,多特异性抗体或其抗原结合片段,例如,双特异性抗体或其抗原结合片段的至少一个臂包含与选自由seq id no:1-4组成的组的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的重链可变区氨基酸序列。在一些实施方案中,多特异性抗体或其抗原结合片段,例如,双特异性抗体或其抗原结合片段的至少一个臂包含与seq id no:1的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的重链可变区氨基酸序列。在一些实施方案中,多特异性抗体或其抗原结合片段,例如,双特异性抗体或其抗原结合片段的至少一个臂包含与seq id no:2的氨基酸序列至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一的轻链可变区氨基酸序列。
[0439]
在一些实施方案中,多特异性抗体或其抗原结合片段,例如,双特异性抗体或其抗
id no:10)。
[0442]
在一些实施方案中,多特异性抗体或其抗原结合片段,例如,双特异性抗体或其抗原结合片段的至少一个臂包含以下的组合:vh cdr1序列、vh cdr2序列、vh cdr3序列、vl cdr1序列、vl cdr2序列和vl cdr3序列,其中,包括与包含氨基酸序列gftfsnywmn(seq id no:37)或gftfsnywmd(seq id no:38)的vh cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr1序列;包括与包含氨基酸序列dpydve(seq id no:5)或氨基酸系列ridpydvethyaqkfqg(seq id no:6)或氨基酸系列ridpydvethynhk(seq id no:39)的vh cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr2序列;包括与包含氨基酸序列ggvggmdy(seq id no:7)的vh cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vh cdr3序列;包括与包含氨基酸序列rssqsivhsngntyle(seq id no:8)或rssqsivhssgntyle(seq id no:40)或rssqsivhssgqtyle(seq id no:55)或rssqsivhssgstyle(seq id no:56)的vl cdr1序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr1序列;包括与包含氨基酸序列rvskrfs(seq id no:9)的vl cdr2序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr2序列;以及包括与包含氨基酸序列fqgshvprt(seq id no:10)的vl cdr3序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高同一性的序列的vl cdr3序列。
[0443]
在一些实施方案中,多特异性抗体/可活化抗体被设计成衔接免疫效应细胞,在本文中也称为免疫效应细胞衔接性多特异性可活化抗体。在一些实施方案中,多特异性抗体/可活化抗体被设计成衔接白细胞,在本文中也称为白细胞衔接性多特异性可活化抗体。在一些实施方案中,多特异性抗体/可活化抗体被设计成衔接t细胞,在本文中也称为t细胞衔接性多特异性抗体/可活化抗体。在一些实施方案中,多特异性抗体/可活化抗体衔接白细胞上的表面抗原,诸如t细胞、自然杀伤(nk)细胞、髓样单核细胞、巨噬细胞和/或在另一种免疫效应细胞上的表面抗原。在一些实施方案中,免疫效应细胞为白细胞。在一些实施方案中,免疫效应细胞为t细胞。在一些实施方案中,免疫效应细胞为nk细胞。在一些实施方案中,免疫效应细胞为单核细胞,诸如髓样单核细胞。在一些实施方案中,多特异性可活化抗体被设计成与多于一个靶标和/或多于一个表位结合或以其他方式相互作用,在本文中也称为多抗原靶向可活化抗体。如本文所用,术语“靶标”和“抗原”可互换使用。
[0444]
在一些实施方案中,本公开的免疫效应细胞衔接的多特异性可活化抗体包含结合cd47的靶向抗体或其抗原结合片段和免疫效应细胞衔接性抗体或其抗原结合部分,其中靶向抗体或其抗原结合片段和/或免疫效应细胞衔接性抗体或其抗原结合部分中的至少一种被掩蔽。在一些实施方案中,免疫效应细胞衔接性抗体或其抗原结合片段包含结合第一免疫效应细胞衔接性靶标的第一抗体或其抗原结合片段(ab1),其中ab1附接至掩蔽部分(mm1),使得mm1的偶合降低ab1结合第一靶标的能力。在一些实施方案中,靶向抗体或其抗原结合片段包含第二抗体或其片段,所述第二抗体或其片段包含结合cd47的第二抗体或其抗原结合片段(ab2),其中ab2附接至掩蔽部分(mm2),使得mm2的偶合降低ab2结合cd47的能力。在一些实施方案中,接合免疫效应细胞的抗体或其抗原结合片段包含结合第一免疫效应细胞衔接性靶标的第一抗体或其抗原结合片段(ab1),其中ab1附接至掩蔽部分(mm1),使
得mm1的偶合降低ab1结合第一靶标的能力,并且靶向抗体或其抗原结合片段包含第二抗体或其片段,所述第二抗体或其片段包含结合cd47的第二抗体或其抗原结合片段(ab2),其中ab2附接至掩蔽部分(mm2),使得mm2的偶合降低ab2结合cd47的能力。在一些实施方案中,非免疫效应细胞衔接性抗体为靶向癌症的抗体。在一些实施方案中,非免疫细胞效应抗体为igg。在一些实施方案中,免疫效应细胞衔接性抗体为scfv。在一些实施方案中,靶向cd47的抗体(例如,非免疫细胞效应抗体)为igg,并且免疫效应细胞衔接性抗体为scfv。在一些实施方案中,免疫效应细胞为白细胞。在一些实施方案中,免疫效应细胞为t细胞。在一些实施方案中,免疫效应细胞为nk细胞。在一些实施方案中,免疫效应细胞为髓样单核细胞。
[0445]
在一些实施方案中,本公开的t细胞衔接性多特异性可活化抗体包含靶向cd47的抗体或其抗原结合片段和t细胞衔接性抗体或其抗原结合部分,其中靶向cd47的抗体或其抗原结合片段和/或t细胞衔接性抗体或其抗原结合部分中的至少一种被掩蔽。在一些实施方案中,t细胞衔接性抗体或其抗原结合片段包含结合第一t细胞衔接性靶标的第一抗体或其抗原结合片段(ab1),其中ab1附接至掩蔽部分(mm1),使得mm1的偶合降低ab1结合第一靶标的能力。在一些实施方案中,靶向抗体或其抗原结合片段包含第二抗体或其片段,所述第二抗体或其片段包含结合cd47的第二抗体或其抗原结合片段(ab2),其中ab2附接至掩蔽部分(mm2),使得mm2的偶合降低ab2结合cd47的能力。在一些实施方案中,t细胞衔接性抗体或其抗原结合片段包含结合第一t细胞衔接性靶标的第一抗体或其抗原结合片段(ab1),其中ab1附接至掩蔽部分(mm1),使得mm1的偶合降低ab1结合第一靶标的能力,并且靶向抗体或其抗原结合片段包含第二抗体或其片段,所述第二抗体或其片段包含结合cd47的第二抗体或其抗原结合片段(ab2),其中ab2附接至掩蔽部分(mm2),使得mm2的偶合降低ab2结合cd47的能力。
[0446]
在免疫效应细胞衔接性多特异性抗体/可活化抗体的一些实施方案中,一种抗原是cd47,并且另一种抗原通常是t细胞、自然杀伤(nk)细胞、髓样单核细胞、巨噬细胞和/或其他免疫效应细胞表面上存在的刺激性或抑制性受体,诸如但不限于b7-h4、btla、cd3、cd4、cd8、cd16a、cd25、cd27、cd28、cd32、cd56、cd137、ctla-4、gitr、hvem、icos、lag3、nkg2d、ox40、pd-1、tigit、tim3或vista。在一些实施方案中,抗原是t细胞或nk细胞表面上存在的刺激性受体;此类刺激性受体的实例包括但不限于cd3、cd27、cd28、cd137(也称为4-1bb)、gitr、hvem、icos、nkg2d和ox40。在一些实施方案中,抗原是t细胞表面上存在的抑制性受体;此类抑制性受体的实例包括但不限于btla、ctla-4、lag3、pd-1、tigit、tim3和nk表达的kir。赋予t细胞表面抗原特异性的抗体结构域也可被结合至t细胞受体、nk细胞受体、巨噬细胞受体和/或其他免疫效应细胞受体(诸如但不限于b7-1、b7-2、b7h3、pdl1、pdl2或tnfsf9)的配体或配体结构域取代。
[0447]
在一些实施方案中,t细胞衔接性多特异性可活化抗体包含抗cd3ε(cd3ε,在本文中也称为cd3e和cd3)scfv和靶向抗体或其抗原结合片段,其中抗cd3εscfv和/或靶向抗体或其抗原结合部分中的至少一种被掩蔽。在一些实施方案中,cd3εscfv包含结合cd3ε的第一抗体或其抗原结合片段(ab1),其中ab1附接至掩蔽部分(mm1),使得mm1的偶合降低ab1结合cd3ε的能力。在一些实施方案中,靶向抗体或其抗原结合片段包含第二抗体或其片段,所述第二抗体或其片段包含结合cd47的第二抗体或其抗原结合片段(ab2),其中ab2附接至掩蔽部分(mm2),使得mm2的偶合降低ab2结合cd47的能力。在一些实施方案中,cd3εscfv包含
vh*-l4-vh-ch1-ch2-ch3)2;(vl-cl)2:(mm-l1-cm-l2-vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2;(mm-l1-cm-l2-vl-cl)2:(vl*-l3-vh*-l4-vh-ch1-ch2-ch3)2;(mm-l1-cm-l2-vl-cl)2:(vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vh*-l3-vl*-l2-cm-l1-mm)2:(vh-ch1-ch2-ch3)2;(vl-cl-l4-vl*-l3-vh*-l2-cm-l1-mm)2:(vh-ch1-ch2-ch3)2;(mm-l1-cm-l2-vl*-l3-vh*-l4-vl-cl)2:(vh-ch1-ch2-ch3)2;(mm-l1-cm-l2-vh*-l3-vl*-l4-vl-cl)2:(vh-ch1-ch2-ch3)2;(vl-cl-l4-vh*-l3-vl*-l2-cm-l1-mm)2:(mm-l1-cm-l2-vl*-l3-vh*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vh*-l3-vl*-l2-cm-l1-mm)2:(mm-l1-cm-l2-vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vl*-l3-vh*-l2-cm-l1-mm)2:(mm-l1-cm-l2-vl*-l3-vh*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vl*-l3-vh*-l2-cm-l1-mm)2:(mm-l1-cm-l2-vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vh*-l3-vl*)2:(mm-l1-cm-l2-vl*-l3-vh*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vh*-l3-vl*)2:(mm-l1-cm-l2-vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vl*-l3-vh*)2:(mm-l1-cm-l2-vl*-l3-vh*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vl*-l3-vh*)2:(mm-l1-cm-l2-vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vh*-l3-vl*-l2-cm-l1-mm)2:(vl*-l3-vh*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vh*-l3-vl*-l2-cm-l1-mm)2:(vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2;(vl-cl-l4-vl*-l3-vh*-l2-cm-l1-mm)2:(vl*-l3-vh*-l4-vh-ch1-ch2-ch3)2;或(vl-cl-l4-vl*-l3-vh*-l2-cm-l1-mm)2:(vh*-l3-vl*-l4-vh-ch1-ch2-ch3)2,其中:vl和vh代表igg中包含的具有第一特异性的轻和重可变结构域;vl*和vh*代表scfv中包含的具有第二特异性的可变结构域;l1为连接掩蔽部分(mm)和可裂解部分(cm)的接头肽;l2为连接可裂解部分(cm)和抗体的连接肽;l3为连接scfv的可变结构域的接头肽;l4为将具有第一特异性的抗体连接至具有第二特异性的抗体的连接肽;cl为轻链恒定结构域;并且ch1、ch2、ch3为重链恒定结构域。所述第一特异性和第二特异性可针对任何抗原或表位。
[0452]
在t细胞衔接性多特异性抗体/可活化抗体的一些实施方案中,一种抗原是cd47,并且另一种抗原通常是t细胞、自然杀伤(nk)细胞、髓样单核细胞、巨噬细胞和/或其他免疫效应细胞表面上存在的刺激性(在本文中也称为活化)或抑制性受体,诸如但不限于b7-h4、btla、cd3、cd4、cd8、cd16a、cd25、cd27、cd28、cd32、cd56、cd137(也称为tnfrsf9)、ctla-4、gitr、hvem、icos、lag3、nkg2d、ox40、pd-1、tigit、tim3或vista。赋予t细胞表面抗原特异性的抗体结构域也可被结合至t细胞受体、nk细胞受体、巨噬细胞受体和/或其他免疫效应细胞受体的配体或配体结构域取代。
[0453]
在一些实施方案中,靶向抗体为本文公开的cd47抗体。在一些实施方案中,靶向抗体可以是呈可活化抗体的形式。在一些实施方案中,一个或多个scfv可以是呈pro-scfv的形式(参见例如wo2009/025846、wo 2010/081173)。
[0454]
在一些实施方案中,scfv对结合cd3ε具有特异性,并且包含或源自结合cd3ε的抗体或其片段,例如ch2527、fn18、h2c、okt3、2c11、ucht1或v9。在一些实施方案中,scfv对结合ctla-4(在本文中也称为ctla和ctla4)具有特异性。
[0455]
在一些实施方案中,抗ctla-4scfv包含以下氨基酸序列:
[0456]
gggsggggsgsgggsggggsgggeivltqspgtlslspgeratlscrasqsvsssylawyqqkpgqaprlliygassratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspltfgggtkveikrsggstitsynvyytklsssgtqvqlvqtgggvvqpgrslrlscaasgstfssyamswvrqapgkglewvsaisgsggstyyadsvkgr
ftisrdnskntlylqmnslraedtavyycatnslywyfdlwgrgtlvtvssas(seq id no:643)
[0457]
在一些实施方案中,抗ctla-4scfv包含与氨基酸序列seq id no:643至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多相同的氨基酸序列。
[0458]
在一些实施方案中,抗cd3εscfv包含以下氨基酸序列:
[0459]
gggsggggsgsgggsggggsgggqvqlqqsgaelarpgasvkmsckasgytftrytmhwvkqrpgqglewigyinpsrgytnynqkfkdkatlttdkssstaymqlssltsedsavyycaryyddhycldywgqgttltvssggggsggggsggggsqivltqspaimsaspgekvtmtcsasssvsymnwyqqksgtspkrwiydtsklasgvpahfrgsgsgtsysltisgmeaedaatyycqqwssnpftfgsgtkleinr(seq id no:644)
[0460]
在一些实施方案中,抗cd3εscfv包含与氨基酸序列seq id no:644至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多相同的氨基酸序列。
[0461]
在一些实施方案中,scfv对结合一种或多种t细胞、一种或多种nk细胞和/或一种或多种巨噬细胞具有特异性。在一些实施方案中,scfv对结合选自由以下组成的组的靶标具有特异性:b7-h4、btla、cd3、cd4、cd8、cd16a、cd25、cd27、cd28、cd32、cd56、cd137、ctla-4、gitr、hvem、icos、lag3、nkg2d、ox40、pd-1、tigit、tim3或vista。
[0462]
在一些实施方案中,多特异性抗体/可活化抗体还包含缀合至ab的剂。在一些实施方案中,剂为治疗剂。在一些实施方案中,剂为抗肿瘤剂。在一些实施方案中,剂为毒素或其片段。在一些实施方案中,剂通过接头缀合至多特异性抗体/可活化抗体。在一些实施方案中,剂通过可裂解的接头缀合至ab。在一些实施方案中,接头为不可裂解的接头。在一些实施方案中,剂为微管抑制剂。在一些实施方案中,剂为核酸损伤剂,诸如dna烷基化剂或dna嵌入剂,或其他dna损伤剂。在一些实施方案中,接头为可裂解的接头。在一些实施方案中,剂为选自表e中列出的组的剂。在一些实施方案中,剂为多拉司他汀。在一些实施方案中,剂为澳瑞他汀或其衍生物。在一些实施方案中,剂为澳瑞他汀e或其衍生物。在一些实施方案中,剂为单甲基澳瑞他汀e(mmae)。在一些实施方案中,剂为单甲基澳瑞他汀d(mmad)。在一些实施方案中,剂为类美登素或类美登素衍生物。在一些实施方案中,剂为dm1或dm4。在一些实施方案中,剂为倍癌霉素或其衍生物。在一些实施方案中,剂为卡奇霉素(calicheamicin)或其衍生物。在一些实施方案中,剂为吡咯并苯并二氮杂在一些实施方案中,剂为吡咯并苯并二氮杂二聚体。
[0463]
在一些实施方案中,多特异性抗体/可活化抗体还包含可检测部分。在一些实施方案中,可检测部分为诊断剂。
[0464]
在一些实施方案中,多特异性抗体/可活化抗体天然含有一个或多个二硫键。在一些实施方案中,多特异性可活化抗体可被工程化为包含一个或多个二硫键。
[0465]
本公开还提供了一种编码本文所述的多特异性抗体/可活化抗体的分离的核酸分子,以及包含这些分离的核酸序列的载体。本公开提供了产生多特异性抗体/可活化抗体的方法,其通过在导致所述抗体/可活化抗体表达的条件下培养细胞来进行,其中所述细胞包含此种核酸分子。在一些实施方案中,细胞包含此种载体。
[0466]
本公开还提供了一种制造本公开的多特异性cd47抗体的方法,其通过以下步骤进行:(a)在导致多特异性抗体表达的条件下培养包含编码多特异性抗体的核酸构建体的细胞。
[0467]
本公开还提供了一种制造本公开的多特异性可活化cd47抗体的方法,其通过以下
步骤进行:(a)在导致多特异性可活化抗体表达的条件下培养包含编码多特异性可活化抗体的核酸构建体的细胞,以及(b)回收多特异性可活化抗体。适合的ab、mm和/或cm包括本文公开的任何ab、mm和/或cm。
[0468]
本公开还提供了多特异性可活化抗体和/或多特异性可活化抗体组合物,其至少包含特异性结合第一靶标或第一表位的第一抗体或其抗原结合片段(ab1)和结合第二靶标或第二表位的第二抗体或其抗原结合片段(ab2),其中至少ab1偶合至或以其他方式附接至掩蔽部分(mm1),使得mm1的偶合降低ab1结合其靶标的能力。在一些实施方案中,mm1经由包含蛋白酶的底物的第一可裂解部分(cm1)序列偶合至ab1,所述蛋白酶例如是与ab1的靶标共定位在受试者的治疗部位或诊断部位的蛋白酶。本文提供的多特异性可活化抗体在循环中稳定,在预期的治疗和/或诊断位点活化,但在正常组织(即健康组织)中不活化,并且在活化时表现出与相应的未修饰的多特异性抗体至少相当的与ab1的靶标结合。适合的ab、mm和/或cm包括本文公开的任何ab、mm和/或cm。
[0469]
本公开还提供了包含多特异性可活化抗体的组合物和方法,所述多特异性可活化抗体至少包含特异性结合靶标的第一抗体或抗体片段(ab1)以及第二抗体或抗体片段(ab2),其中多特异性可活化抗体中的至少第一ab偶合至降低ab1结合其靶标的能力的掩蔽部分(mm1)。在一些实施方案中,每个ab偶合至mm,所述mm降低其相应的ab对每个靶标的能力。例如,在双特异性可活化抗体的实施方案中,ab1偶合至降低ab1结合其靶标的能力的第一掩蔽部分(mm1),并且ab2偶合至降低ab2结合其靶标的能力的第二掩蔽部分(mm2)。在一些实施方案中,多特异性可活化抗体包含多于两个ab区域;在此类实施方案中,ab1偶合至降低ab1结合其靶标的能力的第一掩蔽部分(mm1),ab2偶合至降低ab2结合其靶标的能力的第二掩蔽部分(mm2),ab3偶合至降低ab3结合其靶标的能力的第三掩蔽部分(mm3),对于多特异性可活化抗体中的每个ab,依此类推。适合的ab、mm和/或cm包括本文公开的任何ab、mm和/或cm。
[0470]
在一些实施方案中,多特异性可活化抗体还包含作为蛋白酶的底物的至少一种可裂解部分(cm),其中cm将mm连接至ab。例如,在一些实施方案中,多特异性可活化抗体至少包含特异性结合靶标的第一抗体或抗体片段(ab1)以及第二抗体或抗体片段(ab2),其中多特异性可活化抗体中的至少第一ab通过第一可裂解部分(cm1)偶合至降低ab1结合其靶标的能力的掩蔽部分(mm1)。在一些双特异性可活化抗体的实施方案中,ab1通过cm1偶合至mm1,并且ab2通过第二可裂解部分(cm2)偶合至降低ab2结合其靶标的能力的第二掩蔽部分(mm2)。在一些实施方案中,多特异性可活化抗体包含多于两个ab区域;在这些实施方案的一些中,ab1通过cm1偶合至mm1,ab2通过cm2偶合至mm2,并且ab3通过第三可裂解部分(cm3)偶合至降低ab3结合其靶标的能力的第三掩蔽部分(mm3),对于多特异性可活化抗体中的每个ab,依此类推。适合的ab、mm和/或cm包括本文公开的任何ab、mm和/或cm。
[0471]
具有非结合空间部分或非结合空间部分的结合配偶体的可活化抗体
[0472]
本公开还提供了可活化抗体,其包含非结合空间部分(nb)或非结合空间部分的结合配偶体(bp),其中bp募集或以其他方式将nb吸引至可活化抗体。本文提供的可活化抗体包括例如包含非结合空间部分(nb)、可裂解接头(cl)和结合靶标的抗体或抗体片段(ab)的可活化抗体;包含非结合空间部分的结合配偶体(bp)、cl和ab的可活化抗体;以及包含已募集nb的bp、cl和与靶标结合的ab的可活化抗体。其中nb共价连接至可活化抗体的cl和ab或
通过与共价连接至可活化抗体的cl底物和ab的bp相互作用而缔合的可活化抗体在本文中称为“含有nb的可活化抗体”。可活化的或可转换的意指当可活化抗体处于受抑制、掩蔽或未裂解状态(即第一构象)时,可活化抗体表现出与靶标的第一结合水平,并且当可活化抗体处于未受抑制、无掩蔽和/或裂解状态(即第二构象,即活化的抗体)时,可活化抗体表现出与靶标的第二结合水平,其中第二靶标结合水平大于第一靶标结合水平。与常规抗体治疗相比,可活化抗体组合物可表现出增加的生物利用度和更有利的生物分布。
[0473]
在一些实施方案中,如果ab未被掩蔽或以其他方式被抑制免于结合至非治疗位点和/或非诊断位点,则可活化抗体提供降低的另外可由这种位点的结合引起的毒性和/或不良副作用。
[0474]
可使用pct公布号wo 2013/192546中阐述的方法制备包括非结合空间部分(nb)的cd47可活化抗体,所述pct公布的内容特此以引用的方式整体并入本文。
[0475]
抗体和可活化抗体的治疗用途
[0476]
本发明提供了预防受试者的cd47介导的疾病、延迟所述疾病的进展、治疗所述疾病、缓解所述疾病的症状或以其他方式改善所述疾病的方法,所述方法通过向有需要的受试者施用治疗有效量的本文所述的cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体来进行。
[0477]
提供了用于预防cd47介导的疾病、延迟所述疾病的进展、治疗所述疾病、缓解所述疾病的症状或以其他方式改善所述疾病的cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体。
[0478]
本发明还提供了预防受试者的癌症、延迟所述癌症的进展、治疗所述癌症、缓解所述癌症的症状或以其他方式改善所述癌症的方法,所述方法通过向有需要的受试者施用治疗有效量的本文所述的cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体来进行。
[0479]
提供了用于预防癌症、延迟所述癌症的进展、治疗所述癌症、缓解所述癌症的症状或以其他方式改善所述癌症的cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体。
[0480]
本发明还提供了使用结合cd47的抗体/可活化抗体,特别是结合并中和或以其他方式抑制cd47的至少一种生物活性和/或cd47介导的信号传导的可活化抗体来治疗受试者中与cd47的异常表达和/或活性相关的症状、预防所述症状和/或延迟所述症状的发作或进展或缓解所述症状的方法。
[0481]
因此,提供了治疗与cd47的异常表达和/或活性相关的症状、预防所述症状和/或延迟所述症状的发作或进展、缓解或缓解所述症状的结合cd47的抗体/可活化抗体。
[0482]
本发明还提供了使用结合cd47的抗体/可活化抗体,特别是结合、靶向、中和、杀伤或以其他方式抑制正在表达或正在异常表达cd47的细胞的至少一种生物活性的可活化抗体来治疗受试者中与正在表达cd47或正在异常表达cd47的细胞的存在、生长、增殖、转移和/或活性相关的症状、预防所述症状和/或延迟所述症状的发作或进展或缓解所述症状的方法。
[0483]
本发明还提供了使用结合cd47的抗体/可活化抗体,特别是结合、靶向、中和、杀伤或以其他方式抑制正在表达cd47的细胞的至少一种生物活性的抗体/可活化抗体来治疗受
试者中与正在表达cd47的细胞的存在、生长、增殖、转移和/或活性相关的症状、预防所述症状和/或延迟所述症状的发作或进展或缓解所述症状的方法。
[0484]
本发明还提供了使用结合cd47的抗体/可活化抗体,特别是结合、靶向、中和、杀伤或以其他方式抑制正在异常表达cd47的细胞的至少一种生物活性的抗体/可活化抗体来治疗受试者中与正在异常表达cd47的细胞的存在、生长、增殖、转移和/或活性相关的症状、预防所述症状和/或延迟所述症状的发作或进展或缓解所述症状的方法。
[0485]
已知cd47在多种癌症中表达,如作为非限制性实例,腺癌、胆管(胆)癌、膀胱癌、乳腺癌,例如三阴性乳腺癌和her2阴性乳腺癌;类癌;宫颈癌;胆管癌;结肠直肠癌;子宫内膜癌;神经胶质瘤;头颈癌,例如头颈鳞状细胞癌;白血病;肝癌;肺癌,例如nsclc、sclc;淋巴瘤;黑素瘤;口咽癌;卵巢癌;胰腺癌;前列腺癌,例如转移性去势抵抗性前列腺癌;肾癌;皮肤癌;鳞状细胞癌,胃癌;睾丸癌;甲状腺癌;和尿路上皮癌。
[0486]
在一些实施方案中,癌症与表达cd47的肿瘤相关。在一些实施方案中,癌症归因于表达cd47的肿瘤。
[0487]
在这些方法和用途的任何实施方案中使用的cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体可在疾病的任何阶段施用。例如,可将此种cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体施用于患有从早期到转移的任何阶段的癌症的患者。术语受试者和患者在本文可互换使用。
[0488]
在一些实施方案中,受试者是哺乳动物,如人、非人灵长类动物、伴侣动物(例如猫、狗、马)、农场动物、工作动物或动物园动物。在一些实施方案中,受试者是人。在一些实施方案中,受试者为伴侣动物。在一些实施方案中,受试者为兽医护理的动物。
[0489]
将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体及其治疗性制剂施用于患有或易患与异常cd47表达和/或活性相关的疾病或病症的受试者。使用本领域已知的多种方法中的任一种来鉴别患有或易患与异常cd47表达和/或活性相关的疾病或病症的受试者。例如,使用多种临床和/或实验室测试(诸如身体检查和血液、尿液和/或粪便分析)中的任一种来鉴别患有癌症或其他赘生性疾患的受试者,以评估健康状况。例如,使用多种临床和/或实验室测试(诸如身体检查和/或体液分析,例如血液、尿液和/或粪便分析)中的任一种来鉴别患有炎症和/或炎性病症的受试者,以评估健康状况。
[0490]
如果实现了多种实验室或临床目标中任一种,则认为将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体施用于患有与异常cd47表达和/或活性相关的疾病或病症的患者是成功的。例如,如果与疾病或病症相关的一种或多种症状得到缓解、减轻、抑制或不进展到进一步(即,更糟)状态,则认为将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体施用于患有与异常cd47表达和/或活性相关的疾病或病症的患者是成功的。如果疾病或病症进入缓解期或不进展到进一步(即,更糟)状态,则认为将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体施用于患有与异常cd47表达和/或活性相关的疾病或病症的患者是成功的。
[0491]
在一些实施方案中,将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体及其治疗性制剂施用于患有或易患疾病或病症的受试者,诸如患有癌症或其他赘生性疾患的受试者,其中受试者的病变细胞正在表达cd47。在一些实施方案中,病变细胞与异常cd47表达和/或活性相关。在一些实施方案中,病变细胞与正常cd47表达和/或
活性相关。使用本领域中已知的多种方法中的任一种来鉴定患有或易患其中受试者的患病细胞表达cd47的疾病或病症的受试者。例如,使用多种临床和/或实验室测试(例如体格检查以及血液、尿液和/或粪便分析以评估健康状况)中的任一种来鉴定患有癌症或其他赘生性疾患的受试者。例如,使用多种临床和/或实验室测试(诸如身体检查和/或体液分析,例如血液、尿液和/或粪便分析)中的任一种来鉴别患有炎症和/或炎性病症的受试者,以评估健康状况。
[0492]
在一些实施方案中,将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体及其治疗性制剂施用于患有或易患与表达cd47的细胞或此类细胞的存在、生长、增殖、转移和/或活性相关的疾病或病症的受试者,诸如患有癌症或其他赘生性疾患的受试者。在一些实施方案中,细胞与异常cd47表达和/或活性相关。在一些实施方案中,细胞与正常cd47表达和/或活性相关。使用本领域中已知的多种方法中的任一种来鉴定与表达cd47的细胞相关的疾病或病症的受试者。例如,使用多种临床和/或实验室测试(例如体格检查以及血液、尿液和/或粪便分析以评估健康状况)中的任一种来鉴定患有癌症或其他赘生性疾患的受试者。例如,使用多种临床和/或实验室测试(诸如身体检查和/或体液分析,例如血液、尿液和/或粪便分析)中的任一种来鉴别患有炎症和/或炎性病症的受试者,以评估健康状况。
[0493]
如果实现了多种实验室或临床目标中任一种,则认为将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体施用于患有与表达d47的细胞相关的疾病或病症的患者是成功的。例如,如果与疾病或病症相关的一种或多种症状得到缓解、减轻、抑制或不进展到进一步(即,更糟)状态,则认为将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体施用于患有与表达d47的细胞相关的疾病或病症的患者是成功的。如果疾病或病症进入缓解期或不进展到进一步(即,更糟)状态,则认为将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体施用于患有与表达d47的细胞相关的疾病或病症的患者是成功的。
[0494]
在一些实施方案中,将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体在治疗期间和/或治疗后与一种或多种另外的剂(例如像化学治疗剂、抗炎剂和/或免疫抑制剂)组合施用。在一些实施方案中,同时施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及一种或多种另外的剂。例如,cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及一种或多种另外的剂可被配制成单一组合物或作为两种或更多种单独的组合物施用。在一些实施方案中,依序施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及一种或多种另外的剂。
[0495]
本公开还提供了治疗其中病变细胞表达cd47的病症或疾病、缓解所述病症或疾病的症状或延迟所述病症或疾病的进展的方法,所述方法包括向有需要的受试者施用治疗有效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,所述病症或疾病为癌症。
[0496]
本公开还提供了治疗与表达cd47的细胞相关的病症或疾病、缓解所述病症或疾病的症状或延迟所述病症或疾病的进展的方法,所述方法包括向有需要的受试者施用治疗有
效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,与表达cd47的细胞相关的病症或疾病是癌症。在一些实施方案中,癌症是腺癌、胆管(胆)癌、膀胱癌、骨癌、乳腺癌、三阴性乳腺癌、her2阴性乳腺癌、类癌、宫颈癌、胆管癌、结肠直肠癌、结肠癌、子宫内膜癌、食道癌、神经胶质瘤、头颈癌、头颈鳞状细胞癌、白血病、肝癌、肺癌、非小细胞肺癌、小细胞肺癌、淋巴瘤、黑素瘤、口咽癌、卵巢癌、胰腺癌、前列腺癌、转移性去势抵抗性前列腺癌、肾癌、肉瘤、皮肤癌、鳞状细胞癌、胃癌、睾丸癌、甲状腺癌、泌尿生殖系统癌或尿路上皮癌。在一些实施方案中,哺乳动物cd47的表达和/或活性是异常的。在一些实施方案中,所述方法包括施用另外的剂。在一些实施方案中,另外的剂为治疗剂。
[0497]
本公开还提供了抑制或减少表达哺乳动物cd47的细胞的生长、增殖或转移的方法,所述方法包括向有需要的受试者施用治疗有效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,哺乳动物cd47的表达和/或活性是异常的。在一些实施方案中,所述方法包括施用另外的剂。在一些实施方案中,另外的剂为治疗剂。
[0498]
本公开还提供了抑制、阻断或阻止天然配体与哺乳动物cd47结合的方法,所述方法包括向有需要的受试者施用治疗有效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,哺乳动物cd47的表达和/或活性是异常的。在一些实施方案中,所述方法包括施用另外的剂。在一些实施方案中,另外的剂为治疗剂。
[0499]
本公开还提供了治疗其中病变细胞表达cd47的病症或疾病、缓解所述病症或疾病的症状或延迟所述病症或疾病的进展的方法,所述方法包括向有需要的受试者施用治疗有效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,所述病症或疾病为癌症。
[0500]
本公开还提供了治疗与表达cd47的细胞相关的病症或疾病、缓解所述病症或疾病的症状或延迟所述病症或疾病的进展的方法,所述方法包括向有需要的受试者施用治疗有效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,与表达cd47的细胞相关的病症或疾病是癌症。在一些实施方案中,癌症是腺癌、胆管(胆)癌、膀胱癌、骨癌、乳腺癌、三阴性乳腺癌、her2阴性乳腺癌、类癌、宫颈癌、胆管癌、结肠直肠癌、结肠癌、子宫内膜癌、食道癌、神经胶质瘤、头颈癌、头颈鳞状细胞癌、白血病、肝癌、肺癌、非小细胞肺癌、小细胞肺癌、淋巴瘤、黑素瘤、口咽癌、卵巢癌、胰腺癌、前列腺癌、转移性去势抵抗性前列腺癌、肾癌、肉瘤、皮肤癌、鳞状细胞癌、胃癌、睾丸癌、甲状腺癌、泌尿生殖系统癌或尿路上皮癌。在一些实施方案中,哺乳动物cd47的表达和/或活性是异常的。在一些实施方案中,所述方法包括施用另外的剂。在一些实施方案中,另外的剂为治疗剂。
[0501]
本公开还提供了抑制或减少表达哺乳动物cd47的细胞的生长、增殖或转移的方法,所述方法包括向有需要的受试者施用治疗有效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,哺乳动物cd47的表达和/或活性是异常的。在一些实
施方案中,所述方法包括施用另外的剂。在一些实施方案中,另外的剂为治疗剂。
[0502]
本公开还提供了抑制、阻断或阻止天然配体与哺乳动物cd47结合的方法,所述方法包括向有需要的受试者施用治疗有效量的本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体或包含本公开的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的药物组合物。在一些实施方案中,哺乳动物cd47的表达和/或活性是异常的。在一些实施方案中,所述方法包括施用另外的剂。在一些实施方案中,另外的剂为治疗剂。
[0503]
制剂
[0504]
应当理解,根据本公开的治疗实体的施用将与并入制剂中以提供改善的转移、递送、耐受性等的合适的载体、赋形剂和其他剂一起施用。许多适当的制剂可见于所有药物化学家已知的处方集中:remington’s pharmaceutical sciences(第15版,mack publishing company,easton,pa(1975)),特别是其中blaug,seymour的第87章。这些制剂包括例如粉剂、糊剂、软膏剂、凝胶剂、蜡、油、脂质、含有脂质(阳离子或阴离子)的囊泡(诸如lipofectin
tm
)、dna缀合物、无水吸收糊剂、水包油和油包水乳剂、乳剂卡波蜡(carbowax)(各种分子量的聚乙二醇)、半固体凝胶和含有卡波蜡的半固体混合物。任一种上述混合物可适于根据本公开的治疗和疗法,条件是制剂中的活性成分不被制剂灭活,并且制剂在生理上相容且可耐受施用途径。也参见baldrick p.“pharmaceutical excipient development:the need for preclinical guidance.”regul.toxicol pharmacol.32(2):210-8(2000);wang w.“lyophilization and development of solid protein pharmaceuticals.”int.j.pharm.203(1-2):1-60(2000);charman wn“lipids,lipophilic drugs,and oral drug delivery-some emerging concepts.”j pharm sci.89(8):967-78(2000);powell等人“compendium of excipients for parenteral formulations”pda j pharm sci technol.52:238-311(1998)以及其中关于与药物化学家熟知的制剂、赋形剂和载体有关的另外的信息的引用。
[0505]
本公开的治疗性制剂(其包含cd47抗体和/或可活化cd47抗体,诸如作为非限制性实例,抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体)用于预防、治疗或以其他方式改善与异常靶标表达和/或活性相关的疾病或病症。例如,本公开的治疗性制剂(其包含缀合的抗体、可活化抗体和/或缀合的可活化抗体)用于治疗或以其他方式改善癌症或其他赘生性疾患、炎症、炎性病症和/或自身免疫疾病。在一些实施方案中,癌症是其中表达靶标的实体瘤或血液恶性肿瘤。在一些实施方案中,癌症是其中表达靶标的实体瘤。在一些实施方案中,癌症是其中表达靶标的血液恶性肿瘤。在一些实施方案中,靶标在实质(例如在癌症中,器官或组织的经常执行所述器官或组织的一种或多种功能的部分)上表达。在一些实施方案中,靶标在细胞、组织或器官上表达。在一些实施方案中,靶标在基质(即,细胞、组织或器官的结缔支持框架)上表达。在一些实施方案中,靶标在成骨细胞上表达。在一些实施方案中,靶标在内皮(脉管系统)上表达。在一些实施方案中,靶标在癌症干细胞上表达。在一些实施方案中,与抗体和/或可活化抗体缀合的剂为微管抑制剂。在一些实施方案中,与抗体和/或可活化抗体缀合的剂为核酸损伤剂。
[0506]
结合任何已知用于诊断或治疗与靶标表达和/或活性(例如像异常靶标表达和/或活性)相关的疾病或病症的方法来确定预防、改善或治疗的有效性。延长受试者的存活或以其他方式延迟受试者中与靶标表达和/或活性(例如异常靶标表达和/或活性)相关的疾病
或病症的进展表明,抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体赋予临床益处。
[0507]
抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体可以药物组合物的形式施用。涉及制备此类组合物的原理和考虑因素以及组分选择的指导提供于例如remington:the science and practice of pharmacy第19版(alfonso r.gennaro等人,编者)mack pub.co.,easton,pa.:1995;drug absorption enhancement:concepts,possibilities,limitations,and trends,harwood academic publishers,langhorne,pa.,1994;和peptide and protein drug delivery(advances in parenteral sciences,第4卷),1991,m.dekker,new york中。
[0508]
在使用抗体片段的一些实施方案中,选择特异性结合至靶蛋白的结合结构域的最小片段。例如,基于抗体的可变区序列,肽分子可被设计成保留结合靶蛋白序列的能力。此类肽可化学合成和/或通过重组dna技术产生。(参见例如marasco等人,proc.natl.acad.sci.usa,90:7889-7893(1993))。制剂还可含有正在治疗的特定适用症所必需的多于一种活性化合物,例如在一些实施方案中具有不会不利地互相影响的互补活性的那些化合物。在一些实施方案中,或另外,组合物可包含增强其功能的剂,例如像细胞毒性剂、细胞因子、化学治疗剂或生长抑制剂。此类分子以对于预期目的有效的量合适地组合存在。
[0509]
活性成分也可包埋在例如通过凝聚技术或通过界面聚合制备的微胶囊(例如分别为羟甲基纤维素或明胶-微胶囊和聚-(甲基丙烯酸甲酯)微胶囊)中、包埋在胶体药物递送系统(例如,脂质体、白蛋白微球、微乳剂、纳米颗粒和纳米胶囊)中或包埋在粗乳剂中。
[0510]
将用于体内施用的制剂必须是无菌的。这易于通过经由无菌过滤膜过滤来实现。
[0511]
可制备持续释放制剂。持续释放制备物的合适实例包括含有抗体的固体疏水性聚合物的半渗透性基质,所述基质呈成形物品,例如膜或微胶囊的形式。持续释放基质的实例包括聚酯、水凝胶(例如,聚(甲基丙烯酸-2-羟乙酯)或聚(乙烯醇))、聚丙交酯(美国专利号3,773,919)、l-谷氨酸和l-谷氨酸γ乙酯的共聚物、不可降解乙烯-乙酸乙烯酯、可降解乳酸-乙醇酸共聚物(诸如lupron depot
tm
(由乳酸-乙醇酸共聚物和醋酸亮丙瑞林组成的可注射微球))和聚-d-(-)-3-羟基丁酸。虽然诸如乙烯-乙酸乙烯酯和乳酸-乙醇酸的聚合物能够释放分子超过100天,但某些水凝胶释放蛋白质的时间较短。
[0512]
联合治疗
[0513]
在一些实施方案中,本文所述的cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体与一种或多种另外的剂或另外的剂的组合结合使用。合适的另外的剂包括用于预期应用诸如像癌症的当前药物和/或外科治疗。例如,可将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体与另外的化学治疗剂、抗肿瘤剂、抗炎剂、免疫抑制剂、烷基化剂、抗代谢物、抗微管剂、拓扑异构酶抑制剂、细胞毒性抗生素和/或任何其他核酸损伤剂结合施用。
[0514]
在一些实施方案中,一种或多种另外的剂为化学治疗剂,诸如选自由以下组成的组的化学治疗剂:多西他赛(docetaxel)、紫杉醇(paclitaxel)、abraxane(即,白蛋白缀合的紫杉醇)、多柔比星(doxorubicin)、奥沙利铂(oxaliplatin)、卡铂、顺铂、伊立替康(irinotecan)和吉西他滨(gemcitabine)。
[0515]
在一些实施方案中,一种或多种另外的剂为检查点抑制剂、激酶抑制剂、靶向肿瘤
微环境中的抑制剂的剂和/或t细胞或nk激动剂。在一些实施方案中,一种或多种另外的剂为单独的或与另外一种或多种另外的剂诸如化学治疗剂或抗肿瘤剂组合的放射疗法。在一些实施方案中,一种或多种另外的剂为疫苗、肿瘤病毒和/或dc活化剂,以非限制性实例的方式,诸如toll样受体(tlr)激动剂和/或α-cd40。在一些实施方案中,一种或多种另外的剂为被设计成通过adcc或通过与毒素直接缀合(例如,抗体药物缀合物(adc)来杀死肿瘤的肿瘤靶向抗体。
[0516]
在一些实施方案中,检查点抑制剂为选自由以下组成的组的靶标的抑制剂:ctla-4、lag-3、pd-1、cd47、tigit、tim-3、b7h4和vista。在一些实施方案中,激酶抑制剂选自由b-rafi、meki和btk抑制剂(诸如依鲁替尼(ibrutinib))组成的组。在一些实施方案中,激酶抑制剂为克唑替尼(crizotinib)。在一些实施方案中,肿瘤微环境抑制剂选自由以下组成的组:ido抑制剂、α-csf1r抑制剂、α-ccr4抑制剂、tgf-β、髓源性抑制细胞或t调节细胞。在一些实施方案中,激动剂选自由以下组成的组:ox40、gitr、cd137、icos、cd27和hvem。
[0517]
在一些实施方案中,抑制剂为ctla-4抑制剂。在一些实施方案中,抑制剂为lag-3抑制剂。在一些实施方案中,抑制剂为pd-1抑制剂。在一些实施方案中,抑制剂为cd47抑制剂。在一些实施方案中,抑制剂为tigit抑制剂。在一些实施方案中,抑制剂为tim-3抑制剂。在一些实施方案中,抑制剂为b7h4抑制剂。在一些实施方案中,抑制剂为vista抑制剂。在一些实施方案中,抑制剂为b-rafi抑制剂。在一些实施方案中,抑制剂为meki抑制剂。在一些实施方案中,抑制剂为btk抑制剂。在一些实施方案中,抑制剂为依布替尼(ibrutinib)。在一些实施方案中,抑制剂为克唑替尼(crizotinib)。在一些实施方案中,抑制剂为ido抑制剂。在一些实施方案中,抑制剂为α-csf1r抑制剂。在一些实施方案中,抑制剂为α-ccr4抑制剂。在一些实施方案中,抑制剂为tgf-β。在一些实施方案中,抑制剂为髓源性抑制细胞。在一些实施方案中,抑制剂为t调节细胞。
[0518]
在一些实施方案中,激动剂为ox40。在一些实施方案中,激动剂为gitr。在一些实施方案中,激动剂为cd137。在一些实施方案中,激动剂为icos。在一些实施方案中,激动剂为cd27。在一些实施方案中,激动剂为hvem。
[0519]
在一些实施方案中,将cd47抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体在治疗期间和/或治疗后与一种或多种另外的剂(例如像化学治疗剂、抗炎剂和/或免疫抑制剂)组合施用。在一些实施方案中,cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂被配制成单一治疗组合物,并且同时施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂。或者,cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂彼此分开,例如,将它们各自配制成单独的治疗组合物,并且同时施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂,或者在治疗方案中的不同时间施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂。例如,在施用另外的剂之前施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体,在施用另外的剂之后施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体,或以交替方式施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂。如本文所述,以单剂量或多剂量施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂。
[0520]
在一些实施方案中,同时施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及一种或多种另外的剂。例如,cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及一种或多种另外的剂可被配制成单一组合物或作为两种或更多种单独的组合物施用。在一些实施方案中,依次施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及一种或多种另外的剂,或在治疗方案中的不同时间施用cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体以及另外的剂。
[0521]
在一些实施方案中,将cd47抗体、缀合的cd47抗体、可活化cd47抗体和/或缀合的可活化cd47抗体在治疗期间和/或治疗后与一种或多种另外的剂组合施用,所述一种或多种另外的剂以非限制性实例的方式诸如化学治疗剂、抗炎剂和/或免疫抑制剂,诸如烷基化剂、抗代谢物、抗微管剂、拓扑异构酶抑制剂、细胞毒性抗生素和/或任何其他核酸损伤剂。在一些实施方案中,另外的剂为紫杉烷,诸如紫杉醇(例如)。在一些实施方案中,另外的剂为抗代谢物,诸如吉西他滨。在一些实施方案中,另外的剂为烷基化剂,诸如基于铂的化学治疗剂,诸如卡铂或顺铂。在一些实施方案中,另外的剂为靶向剂,诸如激酶抑制剂,例如索拉非尼(sorafenib)或埃罗替尼(erlotinib)。在一些实施方案中,另外的剂为靶向剂,诸如另一抗体,例如单克隆抗体(例如贝伐珠单抗(bevacizumab))、双特异性抗体或多特异性抗体。在一些实施方案中,另外的剂为蛋白酶体抑制剂,诸如硼替佐米(bortezomib)或卡非佐米(carfilzomib)。在一些实施方案中,另外的剂为免疫调节剂,诸如来那度胺(lenolidominde)或il-2。在一些实施方案中,另外的剂为辐射。在一些实施方案中,另外的剂为被本领域技术人员视为标准护理的剂。在一些实施方案中,另外的剂为本领域技术人员众所周知的化学治疗剂。
[0522]
在一些实施方案中,另外的剂为另一抗体或其抗原结合片段、另一缀合的抗体或其抗原结合片段、另一可活化抗体或其抗原结合片段和/或另一缀合的可活化抗体或其抗原结合片段。在一些实施方案中,另外的剂为与第一抗体或其抗原结合片段、第一缀合的抗体或其抗原结合片段、可活化抗体或其抗原结合片段和/或缀合的可活化抗体或其抗原结合片段针对相同的靶标,例如针对cd47的另一抗体或其抗原结合片段、另一缀合的抗体或其抗原结合片段、另一可活化抗体或其抗原结合片段和/或另一缀合的可活化抗体或其抗原结合片段。在一些实施方案中,另外的剂为与第一抗体或其抗原结合片段、第一缀合的抗体或其抗原结合片段、可活化抗体或其抗原结合片段和/或缀合的可活化抗体或其抗原结合片段针对不同的靶标的另一抗体或其抗原结合片段、另一缀合的抗体或其抗原结合片段、另一可活化抗体或其抗原结合片段和/或另一缀合的可活化抗体或其抗原结合片段。
[0523]
作为非限制性实例,抗体、抗原结合片段和/或(另外的剂的)可活化抗体的ab是表h中列出的任何靶标的结合配偶体。
[0524]
表h:示例性靶标
[0525]
[0526]
[0527][0528]
作为非限制性实例,抗体、抗原结合片段和/或(另外的剂的)可活化抗体的ab是或源自表j中列出的抗体。
[0529]
表j:ab的示例性来源
[0530]
[0531]
[0532][0533]
在一些实施方案中,另外的抗体或其抗原结合片段、缀合的抗体或其抗原结合片段、可活化抗体或其抗原结合片段和/或缀合的可活化抗体或其抗原结合片段为单克隆抗体、结构域抗体、单链、fab片段、f(ab’)2片段、scfv、scab、dab、单结构域重链抗体或单结构域轻链抗体。在一些实施方案中,另外的抗体或其抗原结合片段、缀合的抗体或其抗原结合片段、可活化抗体或其抗原结合片段和/或缀合的可活化抗体或其抗原结合片段为小鼠抗体、其他啮齿动物抗体、嵌合抗体、人源化抗体或完全人单克隆抗体。
[0534]
检测、诊断、成像、患者选择
[0535]
本发明还提供了用于在多种诊断性和/或预防性适应症中使用本文提供的抗体/缀合的抗体/可活化抗体/缀合的可活化抗体的方法和试剂盒。例如,本发明提供了检测受试者或样品中裂解剂和目标靶标的存在或不存在的方法和试剂盒,其通过以下步骤来进行:(i)使受试者或样品与cd47可活化抗体接触,其中cd47可活化抗体包含掩蔽部分(mm)、被裂解剂裂解的可裂解部分(cm)以及特异性结合目标靶标的抗原结合结构域或其片段(ab),其中处于未裂解的非活化状态的cd47可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与cd47结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列并且不是ab的天然结合配偶体的修饰形式;并且(b)其中当ab处于未裂解的非活化状态时,mm干扰ab与cd47的特异性结合,并且当ab处于裂解的活化状态时,mm不干扰或竞争ab与cd47的特异性结合;以及(ii)测量受试者或样品中活化的cd47可活化抗体的水平,其中受试者或样品中可检测水平的活化的cd47可活化抗体指示受试者或样品中存在裂解剂和cd47,并且其中受试者或样品中没有可检测水平的活化的cd47可活化抗体指示受试者或样品中不存在裂解剂、cd47或裂解剂和cd47两者。如本文所提供的,cd47可活化抗体可结合人cd47和食蟹猴cd47。
[0536]
在一些实施方案中,可活化cd47抗体为与治疗剂缀合的可活化cd47抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化cd47抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0537]
在这些方法和试剂盒的一些实施方案中,可活化cd47抗体包含可检测标记。在这些方法和试剂盒的一些实施方案中,可检测标记包括显像剂、造影剂、酶、荧光标记、发色团、染料、一种或多种金属离子或基于配体的标记。在这些方法和试剂盒的一些实施方案中,显像剂包括放射性同位素。在这些方法和试剂盒的一些实施方案中,放射性同位素为铟
或锝。在这些方法和试剂盒的一些实施方案中,造影剂包括碘、钆或铁氧化物。在这些方法和试剂盒的一些实施方案中,酶包括辣根过氧化物酶、碱性磷酸酶或β-半乳糖苷酶。在这些方法和试剂盒的一些实施方案中,荧光标记包括黄色荧光蛋白(yfp)、青色荧光蛋白(cfp)、绿色荧光蛋白(gfp)、修饰的红色荧光蛋白(mrfp)、红色荧光蛋白tdimer2(rfp tdimer2)、hcred或铕衍生物。在这些方法和试剂盒的一些实施方案中,发光标记包括n-甲基吖啶衍生物。在这些方法的一些实施方案中,标记包括alexa标记,诸如alex680或alexa750。在这些方法和试剂盒的一些实施方案中,基于配体的标记包括生物素、亲和素、链霉亲和素或一种或多种半抗原。
[0538]
在这些方法和试剂盒的一些实施方案中,受试者为哺乳动物。在这些方法的一些实施方案中,受试者为人。在一些实施方案中,受试者为非人哺乳动物,诸如非人灵长类动物、伴侣动物(例如,猫、狗、马)、农场动物、工作动物或动物园动物。在一些实施方案中,受试者为啮齿动物。
[0539]
在这些方法和试剂盒的一些实施方案中,方法为体内方法。在这些方法的一些实施方案中,方法为原位方法。在这些方法的一些实施方案中,方法为离体方法。在这些方法的一些实施方案中,方法为体外方法。
[0540]
在方法或试剂盒的一些实施方案中,所述方法用于鉴别或以其他方式细化适用于用本公开的cd47可活化抗体治疗的患者群体,随后通过向有需要的受试者施用此可活化cd47抗体和/或缀合的可活化cd47抗体来进行治疗。例如,对于靶标(例如cd47)和裂解正在这些方法中测试的cd47可活化抗体的可裂解部分(cm)中的底物的蛋白酶均测试为阳性的患者被鉴定为用包含此种cm的此种cd47可活化抗体治疗的合适候选者,并且然后向患者施用治疗有效量的经测试的可活化cd47抗体和/或缀合的可活化cd47抗体。同样,对于靶标(例如cd47)以及裂解正使用这些方法测试的可活化抗体的cm中的底物的蛋白酶中的一者或两者测试为阴性的患者可被鉴定为另一种治疗形式的合适候选者。在一些实施方案中,可用其他cd47可活化抗体测试此类患者,直到鉴别出用于治疗的合适的cd47可活化抗体(例如,包含在疾病位点被患者裂解的cm的cd47可活化抗体)。在一些实施方案中,然后向患者施用治疗有效量的对于患者测试为阳性的可活化cd47抗体和/或缀合的。适合的ab、mm和/或cm包括本文公开的任何ab、mm和/或cm。
[0541]
在一些实施方案中,抗体缀合的抗体、可活化抗体和/或缀合的可活化抗体含有可检测标记。使用完整的抗体或其片段(例如fab、scfv或f(ab)2)。关于探针或抗体的术语“标记的”旨在涵盖通过将可检测物质偶合(即物理连接)到探针或抗体来直接标记探针或抗体,以及通过与直接标记的另一种试剂反应来间接标记探针或抗体。间接标记的实例包括使用经荧光标记的二级抗体检测初级抗体,以及用生物素对dna探针进行末端标记,使得它可用经荧光标记的链霉亲和素来检测。术语“生物样品”旨在包括从受试者分离的组织、细胞和生物液体,以及存在于受试者内的组织、细胞和液体。因此,包括在术语“生物样品”的用法内的是血液以及血液的级分或组分,包括血清、血浆或淋巴液。也就是说,本公开的检测方法可用于在体外以及体内检测生物样品中的分析物mrna、蛋白质或基因组dna。例如,用于检测分析物mrna的体外技术包括northern杂交和原位杂交。用于检测分析物蛋白质的体外技术包括酶联免疫吸附测定(elisa)、蛋白质印迹、免疫沉淀、免疫化学染色和免疫荧光。用于检测分析物基因组dna的体外技术包括southern杂交。用于进行免疫测定的程序例
如描述于“elisa:theory and practice:methods in molecular biology”,第42卷,j.r.crowther(编)human press,totowa,nj,1995;“immunoassay”,e.diamandis和t.christopoulus,academic press,inc.,san diego,ca,1996;以及“practice and theory of enzyme immunoassays”,p.tijssen,elsevier science publishers,amsterdam,1985中。此外,用于检测分析物蛋白质的体内技术包括向受试者中引入标记的抗分析物蛋白质抗体。例如,抗体可用放射性标志物标记,所述放射性标志物在受试者中的存在和位置可通过标准成像技术检测。
[0542]
本公开的抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体也可用于多种诊断和预防制剂。在一个实施方案中,将抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体施用于处于发展一种或多种上述病症的风险下的患者。可使用基因型、血清学或生化标志物确定患者或器官对一种或多种上述病症的易感性。
[0543]
在本公开的一些实施方案中,将抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体施用于被诊断为患有与一种或多种上述病症相关的临床适应症的人个体。诊断后,施用抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体以减轻或逆转临床适应症的影响。
[0544]
本公开的抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体也可用于检测患者样品中的靶标,并因此可用作诊断剂。例如,本公开的抗体和/或可活化抗体及其缀合形式用于体外测定(例如elisa),以检测患者样品中的靶标水平。
[0545]
在一个实施方案中,将本公开的抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体固定在固体支持物(例如,微量滴定板的一个或多个孔)上。固定的抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体用作可存在于测试样品中的任何靶标的捕获抗体。在使固定的抗体和/或可活化抗体和/或其缀合的型式与患者样品接触之前,冲洗固体支持物并用封闭剂(诸如乳蛋白或白蛋白)处理以防止分析物的非特异性吸附。
[0546]
随后,用疑似含有抗原的测试样品或用含有标准量抗原的溶液处理孔。例如,此种样品是来自疑似具有被认为是对病理的诊断的循环抗原水平的受试者的血清样品。在冲洗掉测试样品或标准物之后,用以可检测方式标记的第二抗体处理固体载体。标记的第二抗体用作检测抗体。测量可检测标记的水平,并通过与由标准样品形成的标准曲线进行比较来确定测试样品中靶抗原的浓度。
[0547]
应当理解,基于使用本公开的抗体和可活化抗体及其缀合形式获得的结果,在体外诊断测定中,可以基于靶抗原的表达水平对受试者的疾病进行分期。对于给定的疾病,从被诊断为处于疾病进展的不同阶段和/或处于疾病治疗性治疗的不同时间点的受试者中抽取血液样品。使用为进展或治疗的每个阶段提供统计学上显著的结果的样品群体,指定了可被认为是每个阶段的特征的抗原浓度范围。
[0548]
抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体也可用于诊断和/或成像方法。在一些实施方案中,此类方法为体外方法。在一些实施方案中,此类方法为体内方法。在一些实施方案中,此类方法为原位方法。在一些实施方案中,此类方法为离体方法。例如,具有可酶裂解的cm的可活化抗体可用于检测能够裂解cm的酶的存在或不存在。此类可活化抗体可用于诊断中,其可包括通过在给定宿主生物体的给定细胞或组织中活化的抗体(即,由可活化抗体的裂解而产生的抗体)的测量的积累来在体内检测(例如,定性或定量)酶活
性(或在一些实施方案中,具有增加的还原电位的环境,诸如可提供二硫键还原的环境)。活化的抗体的这种积累不仅表明组织表达酶活性(或根据cm的性质而增加的还原电位),而且还表明组织表达活化的抗体结合的靶标。
[0549]
例如,可选择cm作为在肿瘤位点、生物限制位点的病毒或细菌感染位点(例如像脓肿、器官等)等处发现的至少一种蛋白酶的底物。ab可为结合靶抗原的ab。使用如本文所公开的方法,或在适当时使用本领域技术人员熟悉的方法,可将可检测标记(例如,荧光标记或放射性标记或放射性示踪剂)缀合至抗体和/或可活化抗体的ab或其他区域。在上述筛选方法的背景下讨论合适的可检测标记,并且下文提供了另外的具体实例。使用对疾病状态的蛋白质或肽具有特异性的ab以及在目标疾病组织中活性升高的至少一种蛋白酶,相对于其中cm特异性酶在可检测水平上不存在或以低于疾病组织中的水平存在或无活性(例如,呈酶原形式或呈与抑制剂的复合物)的组织,可活化抗体将表现出增加的与疾病组织的结合率。由于肾脏过滤系统迅速清除血液中的小蛋白质和多肽,并且由于对cm具有特异性的酶在可检测水平上不存在(或以较低水平存在于非疾病组织中或以无活性构象存在),相对于非疾病组织,活化的抗体在疾病组织中的积累增加。
[0550]
在另一个实例中,可活化抗体可用于检测样品中裂解剂的存在或不存在。例如,在可活化抗体含有易于被酶裂解的cm的情况下,可活化抗体可用于检测(定性或定量)样品中酶的存在。在另一个实例中,在可活化抗体含有易于被还原剂裂解的cm的情况下,可活化抗体可用于检测(定性或定量)样品中还原条件的存在。为了促进这些方法中的分析,可以可检测地标记可活化抗体,并且可将其结合至支持物(例如,固体支持物,诸如载玻片或珠)。可检测标记可定位在可活化抗体在裂解后不释放的一部分上,例如,可检测标记可为淬灭的荧光标记或在发生裂解前不可检测的其他标记。例如,可通过使固定的、可检测地标记的可活化抗体与疑似含有酶和/或还原剂的样品接触足以发生裂解的时间,然后洗涤以去除过量的样品和污染物来进行测定。然后通过在与样品接触之前可活化抗体的可检测信号的变化来评估样品中裂解剂(例如,酶或还原剂)的存在或不存在,例如,由于样品中的裂解剂裂解可活化抗体而导致可检测信号的存在和/或增加。
[0551]
此类检测方法可适于也提供对在裂解时能够结合可活化抗体的ab的靶标的存在或不存在的检测。因此,测定可适于评估裂解剂的存在或不存在以及目标靶标的存在或不存在。如上文所述,裂解剂的存在或不存在可通过可活化抗体的可检测标记的存在和/或增加来检测,并且靶标的存在或不存在可通过检测靶标-ab复合物(例如通过使用可检测地标记的抗靶抗体)来检测。
[0552]
可活化抗体也可用于原位成像,以验证例如通过蛋白酶裂解进行的可活化抗体活化和与特定靶标的结合。原位成像是能够在生物样品(诸如细胞培养物或组织切片)中定位蛋白水解活性和靶标的技术。使用此技术,可以基于可检测标记(例如,荧光标记)的存在来确认与给定靶标的结合和蛋白水解活性。
[0553]
这些技术可用于源自疾病位点(例如肿瘤组织)或健康组织的任何冷冻细胞或组织。这些技术也可用于新鲜的细胞或组织样品。
[0554]
在这些技术中,可活化抗体用可检测标记进行标记。可检测标记可为荧光染料(例如,荧光团、异硫氰酸荧光素(fitc)、异硫氰酸罗丹明(tritc)、alexa标记)、近红外(nir)染料(例如,纳米晶体)、胶体金属、半抗原、放射性标志物、生物素和扩增试剂
(诸如链霉亲和素)或酶(例如,辣根过氧化物酶或碱性磷酸酶)。
[0555]
在已与标记的可活化抗体一起孵育的样品中检测到标记表明,样品含有靶标并且含有对可活化抗体的cm具有特异性的蛋白酶。在一些实施方案中,可使用诸如本文所述的那些广谱蛋白酶抑制剂和/或通过使用对蛋白酶具有特异性的剂(例如,对蛋白酶蛋白裂解酶具有特异性并抑制蛋白裂解酶的蛋白水解活性的抗体,诸如a11)来确认蛋白酶的存在;参见例如2010年11月11日公布的国际公布号wo2010/129609。使用诸如本文所述的那些广谱蛋白酶抑制剂和/或通过使用更具选择性的抑制剂的相同方法可用于鉴别对可活化抗体的cm具有特异性的蛋白酶。在一些实施方案中,可使用对靶标具有特异性的剂(例如另一种抗体)来确认靶标的存在,或可检测标记可与未标记的靶标竞争。在一些实施方案中,可使用未标记的可活化抗体,其中通过标记的二级抗体或更复杂的检测系统进行检测。
[0556]
类似技术也可用于体内成像,其中在受试者(例如,哺乳动物,包括人)中检测到荧光信号指示疾病位点含有靶标并且含有对可活化抗体的cm具有特异性的蛋白酶。
[0557]
这些技术也可用于试剂盒中和/或用作试剂,以用于基于可活化抗体中的蛋白酶特异性cm来检测、鉴别或表征多种细胞、组织和生物体中的蛋白酶活性。
[0558]
本公开提供了在多种诊断性和/或预防性适应症中使用抗体和/或可活化抗体的方法。例如,本公开提供了检测受试者或样品中裂解剂和目标靶标的存在或不存在的方法,其通过以下步骤来进行:(i)使受试者或样品与可活化抗体接触,其中可活化抗体包含掩蔽部分(mm)、被裂解剂例如蛋白酶裂解的可裂解部分(cm)以及特异性结合目标靶标的抗原结合结构域或其片段(ab),其中处于未裂解的非活化状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与靶标结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列并且不是ab的天然结合配偶体的修饰形式;并且(b)其中在未裂解的非活化状态下,mm干扰ab与靶标的特异性结合,并且在裂解的活化状态下,mm不干扰或竞争ab与靶标的特异性结合;以及(ii)测量受试者或样品中活化的可活化抗体的水平,其中受试者或样品中可检测水平的活化的可活化抗体指示受试者或样品中存在裂解剂和靶标,并且其中受试者或样品中没有可检测水平的活化的可活化抗体指示受试者或样品中不存在和/或不充分存在裂解剂、靶标或裂解剂和靶标两者。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0559]
本公开还提供了检测受试者或样品中裂解剂的存在或不存在的方法,其通过以下步骤来进行:(i)在目标靶标(例如靶标)存在下,使受试者或样品与可活化抗体接触,其中可活化抗体包含掩蔽部分(mm)、被裂解剂例如蛋白酶裂解的可裂解部分(cm)以及特异性结合目标靶标的抗原结合结构域或其片段(ab),其中处于未裂解的非活化状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与靶标结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列并且不是ab的天然结合配偶体的修饰形式;并且(b)其中在未裂解的非活化状态下,mm干扰ab与靶标的特异性结合,并且在裂解的活化状态下,mm不干扰或竞争ab与靶标的特异性结合;以及(ii)测量受试
者或样品中活化的可活化抗体的水平,其中受试者或样品中可检测水平的活化的可活化抗体指示受试者或样品中存在裂解剂,并且其中受试者或样品中没有可检测水平的活化的可活化抗体指示受试者或样品中不存在和/或不充分存在裂解剂。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0560]
本公开还提供了用于在检测受试者或样品中裂解剂和靶标的存在或不存在的方法中使用的试剂盒,其中所述裂解剂包括至少一种可活化抗体,其包含掩蔽部分(mm)、被裂解剂例如蛋白酶裂解的可裂解部分(cm)以及特异性结合目标靶标的抗原结合结构域或其片段(ab),其中处于未裂解的非活化状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与靶标结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列并且不是ab的天然结合配偶体的修饰形式;并且(b)其中在未裂解的非活化状态下,mm干扰ab与靶标的特异性结合,并且在裂解的活化状态下,mm不干扰或竞争ab与靶标的特异性结合;以及(ii)测量受试者或样品中活化的可活化抗体的水平,其中受试者或样品中可检测水平的活化的可活化抗体指示受试者或样品中存在裂解剂,并且其中受试者或样品中没有可检测水平的活化的可活化抗体指示受试者或样品中不存在和/或不充分存在裂解剂。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0561]
本公开还提供了检测受试者或样品中裂解剂的存在或不存在的方法,其通过以下步骤来进行:(i)使受试者或样品与可活化抗体接触,其中可活化抗体包含掩蔽部分(mm)、被裂解剂例如蛋白酶裂解的可裂解部分(cm)、特异性结合靶标的抗原结合结构域(ab)以及可检测标记,其中处于未裂解的非活化状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;其中mm是抑制ab与靶标的结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列并且不是ab的天然结合配偶体的修饰形式;其中在未裂解的非活化状态下,mm干扰ab与靶标的特异性结合,并且在裂解的活化状态下,mm不干扰或竞争ab与靶标的特异性结合;并且其中可检测标记定位在可活化抗体的在cm裂解后释放的一部分上;以及(ii)测量受试者或样品中可检测标记的水平,其中受试者或样品中可检测水平的可检测标记指示受试者或样品中不存在和/或不充分存在裂解剂,并且其中受试者或样品中没有可检测水平的可检测标记指示受试者或样品中存在裂解剂。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0562]
本公开还提供了用于在检测受试者或样品中裂解剂和靶标的存在或不存在的方法中使用的试剂盒,其中试剂盒至少包括本文所述的用于接触受试者或生物样品的可活化抗体和/或缀合的可活化抗体(例如,与治疗剂缀合的可活化抗体)以及用于检测受试者或生物样品中活化的可活化抗体和/或缀合的可活化抗体的水平的装置,其中受试者或生物样品中可检测水平的活化的可活化抗体指示受试者或生物样品中存在裂解剂和靶标,并且其中受试者或生物样品中没有可检测水平的活化的可活化抗体指示受试者或生物样品中不存在和/或不充分存在裂解剂、靶标或裂解剂和靶标两者,使得在受试者或生物样品中不能检测到可活化抗体的靶标结合和/或蛋白酶裂解。
[0563]
本公开还提供了检测受试者或样品中裂解剂的存在或不存在的方法,其通过以下步骤来进行:(i)在靶标存在下使受试者或生物样品与可活化抗体接触;以及(ii)测量受试者或生物样品中活化的可活化抗体的水平,其中受试者或生物样品中可检测水平的活化的可活化抗体指示受试者或生物样品中存在裂解剂,并且其中受试者或生物样品中没有可检测水平的活化的可活化抗体指示受试者或生物样品中不存在和/或不充分存在可检测水平的裂解剂,使得在受试者或生物样品中不能检测到可活化抗体的蛋白酶裂解。此种可活化抗体包含掩蔽部分(mm)、被裂解剂例如蛋白酶裂解的可裂解部分(cm)以及特异性结合靶标的抗原结合结构域或其片段(ab),其中处于未裂解(即非活化)状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与靶标的结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列;并且(b)其中未裂解状态的可活化抗体的mm干扰ab与靶标的特异性结合,并且其中裂解(即活化)状态的可活化抗体的mm不干扰或竞争ab与靶标的特异性结合。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可检测标记附接到掩蔽部分。在一些实施方案中,可检测标记附接到蛋白酶裂解位点n末端的可裂解部分。在一些实施方案中,ab的单个抗原结合位点被掩蔽。在其中本公开的抗体具有至少两个抗原结合位点的一些实施方案中,至少一个抗原结合位点被掩蔽并且至少一个抗原结合位点不被掩蔽。在一些实施方案中,所有抗原结合位点均被掩蔽。在一些实施方案中,测量步骤包括使用包含可检测标记的二级试剂。
[0564]
本公开还提供了用于在检测受试者或样品中裂解剂和靶标的存在或不存在的方法中使用的试剂盒,其中试剂盒至少包括本文所述的用于在靶标存在下使受试者或生物样品与可活化抗体接触的可活化抗体和/或缀合的可活化抗体;以及测量受试者或生物样品中活化的可活化抗体的水平,其中受试者或生物样品中可检测水平的活化的可活化抗体指示受试者或生物样品中存在裂解剂,并且其中受试者或生物样品中没有可检测水平的活化的可活化抗体指示受试者或生物样品中不存在和/或不充分存在可检测水平的裂解剂,使得在受试者或生物样品中不能检测到可活化抗体的蛋白酶裂解。此种可活化抗体包含掩蔽部分(mm)、被裂解剂例如蛋白酶裂解的可裂解部分(cm)以及特异性结合靶标的抗原结合结构域或其片段(ab),其中处于未裂解(即非活化)状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与靶标的结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列;并且(b)其中未裂解状态的可活化抗体的mm干扰ab与靶标的特异性结合,并且其中裂解(即活化)状态的可活化抗体的mm不干扰或竞争ab与靶标的特异性结合。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。
在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可检测标记附接到掩蔽部分。在一些实施方案中,可检测标记附接到蛋白酶裂解位点n末端的可裂解部分。在一些实施方案中,ab的单个抗原结合位点被掩蔽。在其中本公开的抗体具有至少两个抗原结合位点的一些实施方案中,至少一个抗原结合位点被掩蔽并且至少一个抗原结合位点不被掩蔽。在一些实施方案中,所有抗原结合位点均被掩蔽。在一些实施方案中,测量步骤包括使用包含可检测标记的二级试剂。
[0565]
本公开还提供了用于在检测受试者或样品中裂解剂的存在或不存在的方法中使用的试剂盒,其中试剂盒至少包括本文所述的用于接触受试者或生物样品的可活化抗体和/或缀合的可活化抗体以及用于检测受试者或生物样品中活化的可活化抗体和/或缀合的可活化抗体的水平的装置,其中可活化抗体包含定位在可活化抗体的在cm裂解后释放的一部分上的可检测标记,其中受试者或生物样品中可检测水平的活化的可活化抗体指示受试者或生物样品中不存在和/或不充分存在裂解剂,使得在受试者或生物样品中不能检测到可活化抗体的靶标结合和/或蛋白酶裂解,并且其中受试者或生物样品中没有可检测水平的活化的可活化抗体指示受试者或生物样品中存在可检测水平的裂解剂。
[0566]
本公开提供了检测受试者或样品中裂解剂和靶标的存在或不存在的方法,其通过以下步骤来进行:(i)使受试者或生物样品与可活化抗体接触,其中可活化抗体包含定位在可活化抗体的在cm裂解后释放的一部分上的可检测标记;以及(ii)测量受试者或生物样品中活化的可活化抗体的水平,其中受试者或生物样品中可检测水平的活化的可活化抗体指示受试者或生物样品中不存在和/或不充分存在裂解剂、靶标或裂解剂和靶标两者,使得在受试者或生物样品中不能检测到可活化抗体的靶标结合和/或蛋白酶裂解,并且其中受试者或生物样品中降低的可检测水平的活化的可活化抗体指示受试者或生物样品中存在裂解剂和靶标。降低水平的可检测标记为例如降低约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%和/或约100%。此种可活化抗体包含掩蔽部分(mm)、被裂解剂裂解的可裂解部分(cm)以及特异性结合靶标的抗原结合结构域或其片段(ab),其中处于未裂解(即非活化)状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与靶标的结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列;并且(b)其中未裂解状态的可活化抗体的mm干扰ab与靶标的特异性结合,并且其中裂解(即活化)状态的可活化抗体的mm不干扰或竞争ab与靶标的特异性结合。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0567]
本公开还提供了用于在检测受试者或样品中裂解剂和靶标的存在或不存在的方法中使用的试剂盒,其中试剂盒至少包括本文所述的用于接触受试者或生物样品的可活化抗体和/或缀合的可活化抗体以及用于检测受试者或生物样品中活化的可活化抗体和/或缀合的可活化抗体的水平的装置,其中受试者或生物样品中可检测水平的活化的可活化抗体指示受试者或生物样品中不存在和/或不充分存在裂解剂、靶标或裂解剂和靶标两者,使
得在受试者或生物样品中不能检测到可活化抗体的靶标结合和/或蛋白酶裂解,并且其中受试者或生物样品中降低的可检测水平的活化的可活化抗体指示受试者或生物样品中存在裂解剂和靶标。降低水平的可检测标记为例如降低约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%和/或约100%。
[0568]
本公开还提供了检测受试者或样品中裂解剂的存在或不存在的方法,其通过以下步骤来进行:(i)使受试者或生物样品与可活化抗体接触,其中可活化抗体包含定位在可活化抗体的在cm裂解后释放的一部分上的可检测标记;以及(ii)测量受试者或生物样品中可检测标记的水平,其中受试者或生物样品中可检测水平的可检测标记指示受试者或生物样品中不存在和/或不充分存在可检测水平的裂解剂,使得在受试者或生物样品中不能检测到可活化抗体的蛋白酶裂解,并且其中受试者或生物样品中降低的可检测水平的可检测标记指示受试者或生物样品中存在裂解剂。降低水平的可检测标记为例如降低约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%和/或约100%。此种可活化抗体包含掩蔽部分(mm)、被裂解剂裂解的可裂解部分(cm)以及特异性结合靶标的抗原结合结构域或其片段(ab),其中处于未裂解(即非活化)状态的可活化抗体从n末端到c末端包含如下结构排列:mm-cm-ab或ab-cm-mm;(a)其中mm是抑制ab与靶标的结合的肽,并且其中mm不具有ab的天然存在的结合配偶体的氨基酸序列;并且(b)其中未裂解状态的可活化抗体的mm干扰ab与靶标的特异性结合,并且其中裂解(即活化)状态的可活化抗体的mm不干扰或竞争ab与靶标的特异性结合。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0569]
本公开还提供了用于在检测受试者或样品中目标裂解剂的存在或不存在的方法中使用的试剂盒,其中试剂盒至少包括本文所述的用于接触受试者或生物样品的可活化抗体和/或缀合的可活化抗体以及用于检测受试者或生物样品中活化的可活化抗体和/或缀合的可活化抗体的水平的装置,其中可活化抗体包含定位在可活化抗体的在cm裂解后释放的一部分上的可检测标记,其中受试者或生物样品中可检测水平的可检测标记指示受试者或生物样品中不存在和/或不充分存在裂解剂、靶标或裂解剂和靶标两者,使得在受试者或生物样品中不能检测到可活化抗体的靶标结合和/或蛋白酶裂解,并且其中受试者或生物样品中降低的可检测水平的可检测标记指示受试者或生物样品中存在裂解剂和靶标。降低水平的可检测标记为例如降低约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%和/或约100%。
[0570]
在这些方法和试剂盒的一些实施方案中,可活化抗体包含可检测标记。在这些方法和试剂盒的一些实施方案中,可检测标记包括显像剂、造影剂、酶、荧光标记、发色团、染料、一种或多种金属离子或基于配体的标记。在这些方法和试剂盒的一些实施方案中,显像剂包括放射性同位素。在这些方法和试剂盒的一些实施方案中,放射性同位素为铟或锝。在
这些方法和试剂盒的一些实施方案中,造影剂包括碘、钆或铁氧化物。在这些方法和试剂盒的一些实施方案中,酶包括辣根过氧化物酶、碱性磷酸酶或β-半乳糖苷酶。在这些方法和试剂盒的一些实施方案中,荧光标记包括黄色荧光蛋白(yfp)、青色荧光蛋白(cfp)、绿色荧光蛋白(gfp)、修饰的红色荧光蛋白(mrfp)、红色荧光蛋白tdimer2(rfp tdimer2)、hcred或铕衍生物。在这些方法和试剂盒的一些实施方案中,发光标记包括n-甲基吖啶衍生物。在这些方法的一些实施方案中,标记包括alexa标记,诸如alex680或alexa750。在这些方法和试剂盒的一些实施方案中,基于配体的标记包括生物素、亲和素、链霉亲和素或一种或多种半抗原。
[0571]
在这些方法的一些实施方案中,方法为体内方法。在这些方法的一些实施方案中,方法为原位方法。在这些方法的一些实施方案中,方法为离体方法。在这些方法的一些实施方案中,方法为体外方法。
[0572]
在一些实施方案中,原位成像和/或体内成像可用于鉴别要治疗的患者的方法。例如,在原位成像中,可活化抗体用于筛选患者样品,以鉴别在适当位置例如肿瘤位点具有适当的一种或多种蛋白酶和一种或多种靶标的那些患者。
[0573]
在一些实施方案中,原位成像用于鉴别或以其他方式细化适用于用本公开的可活化抗体治疗的患者群体。例如,对于靶标(例如靶标)和裂解正测试(例如,在疾病位点积聚活化的抗体)的可活化抗体的裂解部分(cm)中的底物的蛋白酶均测试为阳性的患者被鉴定为用包含此种cm的此种可活化抗体治疗的合适候选者。同样,对于靶标(例如靶标)以及裂解正使用这些方法测试的可活化抗体的cm中的底物的蛋白酶中的一者或两者测试为阴性的患者可被鉴定为另一种治疗形式的合适候选者。在一些实施方案中,可用包含不同cm的其他可活化抗体测试对于第一可活化抗体测试为阴性的此类患者,直到鉴别出用于治疗的合适的可活化抗体(例如,包含在疾病位点被患者裂解的cm的可活化抗体)。在一些实施方案中,然后向患者施用治疗有效量的对于患者测试为阳性的可活化抗体。
[0574]
在一些实施方案中,体内成像用于鉴别或以其他方式细化适用于用本公开的可活化抗体治疗的患者群体。例如,对于靶标(例如靶标)和裂解正测试(例如,在疾病位点积聚活化的抗体)的可活化抗体的裂解部分(cm)中的底物的蛋白酶均测试为阳性的患者被鉴定为用包含此种cm的此种可活化抗体治疗的合适候选者。同样,测试为阴性的患者可被鉴定为另一种治疗形式的合适候选者。在一些实施方案中,可用包含不同cm的其他可活化抗体测试对于第一可活化抗体测试为阴性的此类患者,直到鉴别出用于治疗的合适的可活化抗体(例如,包含在疾病位点被患者裂解的cm的可活化抗体)。在一些实施方案中,然后向患者施用治疗有效量的对于患者测试为阳性的可活化抗体。
[0575]
在方法和试剂盒的一些实施方案中,所述方法或试剂盒用于鉴别或以其他方式细化适用于用本公开的可活化抗体治疗的患者群体。例如,对于靶标(例如靶标)和裂解正在这些方法中测试的可活化抗体的可裂解部分(cm)中的底物的蛋白酶均测试为阳性的患者被鉴定为用包含此种cm的此种可活化抗体治疗的合适候选者。同样,对于靶标(例如靶标)和裂解正使用这些方法测试的可活化抗体的cm中的底物的蛋白酶均测试为阴性的患者可能被鉴定为另一种治疗形式的合适候选者。在一些实施方案中,可用其他可活化抗体测试此类患者,直到鉴别出用于治疗的合适的可活化抗体(例如,包含在疾病位点被患者裂解的cm的可活化抗体)。在一些实施方案中,对于任一靶标(例如,靶标)测试为阴性的患者被鉴
定为用包含此种cm的此种可活化抗体治疗的合适候选者。在一些实施方案中,对于任一靶标(例如,靶标)测试为阴性的患者被鉴定为不是用包含此种cm的此种可活化抗体治疗的合适候选者。在一些实施方案中,可用其他可活化抗体测试此类患者,直到鉴别出用于治疗的合适的可活化抗体(例如,包含在疾病位点被患者裂解的cm的可活化抗体)。在一些实施方案中,可活化抗体为与治疗剂缀合的可活化抗体。在一些实施方案中,可活化抗体不缀合至剂。在一些实施方案中,可活化抗体包含可检测标记。在一些实施方案中,可检测标记定位在ab上。在一些实施方案中,使用特异性结合至活化的抗体的二级试剂来完成测量受试者或样品中可活化抗体的水平,其中所述试剂包含可检测标记。在一些实施方案中,二级试剂为包含可检测标记的抗体。
[0576]
在一些实施方案中,方法或试剂盒用于鉴别或以其他方式细化适用于用本公开的抗靶可活化抗体和/或缀合的可活化抗体(例如,与治疗剂缀合的可活化抗体)治疗的患者群体,随后通过向有需要的受试者施用此可活化抗体和/或缀合的可活化抗体来进行治疗。例如,对于靶标(例如靶标)和裂解正在这些方法中测试的可活化抗体和/或缀合的可活化抗体的可裂解部分(cm)中的底物的蛋白酶均测试为阳性的患者被鉴定为用包含此种cm的此种抗体和/或此种缀合的可活化抗体治疗的合适候选者,并且然后向患者施用治疗有效量的经测试的可活化抗体和/或缀合的可活化抗体。同样,对于靶标(例如靶标)以及裂解正使用这些方法测试的可活化抗体的cm中的底物的蛋白酶中的一者或两者测试为阴性的患者可被鉴定为另一种治疗形式的合适候选者。在一些实施方案中,可用其他抗体和/或缀合的可活化抗体测试此类患者,直到鉴别出用于治疗的合适的抗体和/或缀合的可活化抗体(例如,包含在疾病位点被患者裂解的cm的可活化抗体和/或缀合的可活化抗体)。在一些实施方案中,然后向患者施用治疗有效量的对于患者测试为阳性的可活化抗体和/或缀合的可活化抗体。
[0577]
在这些方法和试剂盒的一些实施方案中,mm是长度为约4至40个氨基酸的肽。在这些方法和试剂盒的一些实施方案中,可活化抗体包含接头肽,其中接头肽定位在mm与cm之间。在这些方法和试剂盒的一些实施方案中,可活化抗体包含接头肽,其中接头肽定位在ab与cm之间。在这些方法和试剂盒的一些实施方案中,可活化抗体包含第一接头肽(l1)和第二接头肽(l2),其中第一接头肽定位在mm与cm之间,并且第二接头肽定位在ab与cm之间。在这些方法和试剂盒的一些实施方案中,l1和l2中的每一个是长度为约1至20个氨基酸的肽,并且其中l1和l2中的每一个不需要相同的接头。在这些方法和试剂盒的一些实施方案中,l1和l2中的一个或两个包含甘氨酸-丝氨酸聚合物。在这些方法和试剂盒的一些实施方案中,l1和l2中的至少一个包含选自由以下组成的组的氨基酸序列:(gs)n、(gsggs)n(seq id no:116)和(gggs)n(seq id no:117),其中n为至少1的整数。在这些方法和试剂盒的一些实施方案中,l1和l2中的至少一个包含具有式(ggs)n的氨基酸序列,其中n为至少1的整数。在这些方法和试剂盒的一些实施方案中,l1和l2中的至少一个包含选自由以下组成的组的氨基酸序列:gly-gly-ser-gly(seq id no:118)、gly-gly-ser-gly-gly(seq id no:119)、gly-ser-gly-ser-gly(seq id no:120)、gly-ser-gly-gly-gly(seq id no:121)、gly-gly-gly-ser-gly(seq id no:122)和gly-ser-ser-ser-gly(seq id no:123)。
[0578]
在这些方法和试剂盒的一些实施方案中,ab包含选自本文提出的交叉反应性抗体序列的抗体或抗体片段序列。在这些方法和试剂盒的一些实施方案中,ab包含fab片段、
scfv或单链抗体(scab)。
[0579]
在这些方法和试剂盒的一些实施方案中,裂解剂是与靶标共定位在受试者或样品中的蛋白酶,并且cm是用作蛋白酶的底物的多肽,其中当可活化抗体暴露于蛋白酶时,蛋白酶裂解可活化抗体中的cm。在这些方法和试剂盒的一些实施方案中,cm为长度至多15个氨基酸的多肽。在这些方法和试剂盒的一些实施方案中,cm偶合至ab的n末端。在这些方法和试剂盒的一些实施方案中,cm偶合至ab的c末端。在这些方法和试剂盒的一些实施方案中,cm偶合至ab的vl链的n末端。
[0580]
本公开的抗体、缀合抗体、可活化抗体和/或缀合的可活化抗体用于诊断性和预防性制剂中。在一个实施方案中,将可活化抗体施用于处于发展上述炎症、炎性病症、癌症或其他病症中的一种或多种的风险下的患者。
[0581]
可使用基因型、血清学或生化标志物确定患者或器官对一种或多种上述病症的易感性。
[0582]
在本公开的一些实施方案中,将抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体施用于被诊断为患有与一种或多种上述病症相关的临床适应症的人个体。诊断后,施用抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体以减轻或逆转临床适应症的影响。
[0583]
本公开的抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体也可用于检测患者样品中的靶标,并因此可用作诊断剂。例如,本公开的抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体用于体外测定(例如elisa),以检测患者样品中的靶标水平。
[0584]
在一个实施方案中,将本公开的抗体和/或可活化抗体固定在固体支持物(例如,微量滴定板的一个或多个孔)上。固定的抗体和/或可活化抗体用作可存在于测试样品中的任何靶标的捕获抗体。在使固定的抗体和/或可活化抗体与患者样品接触之前,冲洗固体支持物并用封闭剂(诸如乳蛋白或白蛋白)处理以防止分析物的非特异性吸附。
[0585]
随后,用疑似含有抗原的测试样品或用含有标准量抗原的溶液处理孔。例如,此种样品是来自疑似具有被认为是对病理的诊断的循环抗原水平的受试者的血清样品。在冲洗掉测试样品或标准物之后,用以可检测方式标记的第二抗体处理固体载体。标记的第二抗体用作检测抗体。测量可检测标记的水平,并通过与由标准样品形成的标准曲线进行比较来确定测试样品中靶抗原的浓度。
[0586]
应当理解,基于使用本公开的抗体和/或可活化抗体获得的结果,在体外诊断测定中,可以基于靶抗原的表达水平对受试者的疾病进行分期。对于给定的疾病,从被诊断为处于疾病进展的不同阶段和/或处于疾病治疗性治疗的不同时间点的受试者中抽取血液样品。使用为进展或治疗的每个阶段提供统计学上显著的结果的样品群体,指定了可被认为是每个阶段的特征的抗原浓度范围。
[0587]
抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体也可用于诊断和/或成像方法。在一些实施方案中,此类方法为体外方法。在一些实施方案中,此类方法为体内方法。在一些实施方案中,此类方法为原位方法。在一些实施方案中,此类方法为离体方法。例如,具有可酶裂解的cm的可活化抗体可用于检测能够裂解cm的酶的存在或不存在。此类可活化抗体可用于诊断中,其可包括通过在给定宿主生物体的给定细胞或组织中活化的抗体(即,由可活化抗体的裂解而产生的抗体)的测量的积累来在体内检测(例如,定性或定量)酶活
性(或在一些实施方案中,具有增加的还原电位的环境,诸如可提供二硫键还原的环境)。活化的抗体的这种积累不仅表明组织表达酶活性(或根据cm的性质而增加的还原电位),而且还表明组织表达活化的抗体结合的靶标。
[0588]
例如,可选择cm作为在肿瘤位点、生物限制位点的病毒或细菌感染位点(例如像脓肿、器官等)等处发现的蛋白酶的蛋白酶底物。ab可为结合靶抗原的ab。使用本领域技术人员熟悉的方法,可将可检测标记(例如,荧光标记或放射性标记或放射性示踪剂)缀合至可活化抗体的ab或其他区域。在上述筛选方法的背景下讨论合适的可检测标记,并且下文提供了另外的具体实例。使用对疾病状态的蛋白质或肽具有特异性的ab以及在目标疾病组织中活性升高的蛋白酶,相对于其中cm特异性酶在可检测水平上不存在或以低于疾病组织中的水平存在或无活性(例如,呈酶原形式或呈与抑制剂的复合物)的组织,可活化抗体将表现出增加的与疾病组织的结合率。由于肾脏过滤系统迅速清除血液中的小蛋白质和多肽,并且由于对cm具有特异性的酶在可检测水平上不存在(或以较低水平存在于非疾病组织中或以无活性构象存在),相对于非疾病组织,活化的抗体在疾病组织中的积累增加。
[0589]
在另一个实例中,可活化抗体可用于检测样品中裂解剂的存在或不存在。例如,在可活化抗体含有易于被酶裂解的cm的情况下,可活化抗体可用于检测(定性或定量)样品中酶的存在。在另一个实例中,在可活化抗体含有易于被还原剂裂解的cm的情况下,可活化抗体可用于检测(定性或定量)样品中还原条件的存在。为了促进这些方法中的分析,可以可检测地标记可活化抗体,并且可将其结合至支持物(例如,固体支持物,诸如载玻片或珠)。可检测标记可定位在可活化抗体在裂解后不释放的一部分上,例如,可检测标记可为淬灭的荧光标记或在发生裂解前不可检测的其他标记。例如,可通过使固定的、可检测地标记的可活化抗体与疑似含有酶和/或还原剂的样品接触足以发生裂解的时间,然后洗涤以去除过量的样品和污染物来进行测定。然后通过在与样品接触之前可活化抗体的可检测信号的变化来评估样品中裂解剂(例如,酶或还原剂)的存在或不存在,例如,由于样品中的裂解剂裂解可活化抗体而导致可检测信号的存在和/或增加。
[0590]
此类检测方法可适于也提供对在裂解时能够结合可活化抗体的ab的靶标的存在或不存在的检测。因此,测定可适于评估裂解剂的存在或不存在以及目标靶标的存在或不存在。如上文所述,裂解剂的存在或不存在可通过可活化抗体的可检测标记的存在和/或增加来检测,并且靶标的存在或不存在可通过检测靶标-ab复合物(例如通过使用可检测地标记的抗靶抗体)来检测。
[0591]
可活化抗体也可用于原位成像,以验证例如通过蛋白酶裂解进行的可活化抗体活化和与特定靶标的结合。原位成像是能够在生物样品(诸如细胞培养物或组织切片)中定位蛋白水解活性和靶标的技术。使用此技术,可以基于可检测标记(例如,荧光标记)的存在来确认与给定靶标的结合和蛋白水解活性。
[0592]
这些技术可用于源自疾病位点(例如肿瘤组织)或健康组织的任何冷冻细胞或组织。这些技术也可用于新鲜的细胞或组织样品。
[0593]
在这些技术中,可活化抗体用可检测标记进行标记。可检测标记可为荧光染料(例如,异硫氰酸荧光素(fitc)、异硫氰酸罗丹明(tritc))、近红外(nir)染料(例如,纳米晶体)、胶体金属、半抗原、放射性标志物、生物素和扩增剂(诸如链霉亲和素)或酶(例如,辣根过氧化物酶或碱性磷酸酶)。
[0594]
在已与标记的可活化抗体一起孵育的样品中检测到标记表明,样品含有靶标并且含有对可活化抗体的cm具有特异性的蛋白酶。在一些实施方案中,可使用诸如本文所述的那些广谱蛋白酶抑制剂和/或通过使用对蛋白酶具有特异性的剂(例如,对蛋白酶蛋白裂解酶具有特异性并抑制蛋白裂解酶的蛋白水解活性的抗体,诸如a11)来确认蛋白酶的存在;参见例如2010年11月11日公布的国际公布号wo2010/129609。使用诸如本文所述的那些广谱蛋白酶抑制剂和/或通过使用更具选择性的抑制剂的相同方法可用于鉴别对可活化抗体的cm具有特异性的一种蛋白酶或一类蛋白酶。在一些实施方案中,可使用对靶标具有特异性的剂(例如另一种抗体)来确认靶标的存在,或可检测标记可与未标记的靶标竞争。在一些实施方案中,可使用未标记的可活化抗体,其中通过标记的二级抗体或更复杂的检测系统进行检测。
[0595]
类似技术也可用于体内成像,其中在受试者(例如,哺乳动物,包括人)中检测到荧光信号指示疾病位点含有靶标并且含有对可活化抗体的cm具有特异性的蛋白酶。
[0596]
这些技术也可用于试剂盒中和/或用作试剂,以用于基于可活化抗体中的蛋白酶特异性cm来检测、鉴别或表征多种细胞、组织和生物体中的蛋白酶活性。
[0597]
在一些实施方案中,原位成像和/或体内成像可用于鉴别要治疗的患者的方法。例如,在原位成像中,可活化抗体用于筛选患者样品,以鉴别在适当位置例如肿瘤位点具有适当的一种或多种蛋白酶和一种或多种靶标的那些患者。
[0598]
在一些实施方案中,原位成像用于鉴别或以其他方式细化适用于用本公开的可活化抗体治疗的患者群体。例如,对于靶标和裂解正测试(例如,在疾病位点积聚活化的抗体)的可活化抗体的裂解部分(cm)中的底物的蛋白酶均测试为阳性的患者被鉴定为用包含此种cm的此种可活化抗体治疗的合适候选者。同样,对于靶标和裂解正使用这些方法测试的可活化抗体的cm中的底物的蛋白酶中的一者或两者测试为阴性的患者被鉴定为另一种治疗形式的合适候选者(即不适用于用所测试的可活化抗体进行治疗)。在一些实施方案中,可用包含不同cm的其他可活化抗体测试对于第一可活化抗体测试为阴性的此类患者,直到鉴别出用于治疗的合适的可活化抗体(例如,包含在疾病位点被患者裂解的cm的可活化抗体)。
[0599]
在一些实施方案中,体内成像用于鉴别或以其他方式细化适用于用本公开的可活化抗体治疗的患者群体。例如,对于靶标和裂解正测试(例如,在疾病位点积聚活化的抗体)的可活化抗体的裂解部分(cm)中的底物的蛋白酶均测试为阳性的患者被鉴定为用包含此种cm的此种可活化抗体治疗的合适候选者。同样,测试为阴性的患者被鉴定为另一种治疗形式的合适候选者(即不适用于用所测试的可活化抗体进行治疗)。在一些实施方案中,可用包含不同cm的其他可活化抗体测试对于第一可活化抗体测试为阴性的此类患者,直到鉴别出用于治疗的合适的可活化抗体(例如,包含在疾病位点被患者裂解的cm的可活化抗体)。
[0600]
药物组合物
[0601]
可将本公开的抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体(在本文中也称为“活性化合物”)及其衍生物、片段、类似物和同源物并入适用于施用的药物组合物中。此类组合物通常包含抗体、缀合的抗体、可活化抗体和/或缀合的可活化抗体以及药学上可接受的载体。如本文所用,术语“药学上可接受的载体”旨在包括可与药物施用相容的
任何和所有溶剂、分散介质、包衣、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂等。合适的载体描述于作为本领域中的标准参考教科书的最新版的remington’s pharmaceutical sciences中,所述教科书以引用的方式并入本文。此类载体或稀释剂的适合实例包括但不限于水、盐水、林格氏溶液(ringer’s solution)、右旋糖溶液和5%人血清白蛋白。还可使用脂质体和非水性媒介物诸如不挥发性油。用于药学活性物质的此类介质和试剂的用途是本领域熟知的。除非任何常规介质或试剂与活性化合物不相容,预期将其用于组合物中。补充性活性化合物也可并入组合物中。
[0602]
根据本发明的药物组合物可包括本发明的抗体/可活化抗体和载体。这些药物组合物可包括在试剂盒中,例如像诊断试剂盒。
[0603]
在一些实施方案中,药物组合物包含本公开的抗体、本公开的可活化抗体、本公开的缀合的抗体和/或本公开的缀合的可活化抗体以及载体。在一些实施方案中,药物组合物包含另外的剂。在一些实施方案中,另外的剂为治疗剂。
[0604]
将本公开的药物组合物配制成与其预期的施用途径相容。施用途径的实例包括肠胃外,例如静脉内、皮内、皮下、口服(例如吸入)、透皮(即局部)、透粘膜和直肠施用。用于肠胃外、皮内或皮下应用的溶液或悬浮液可包含以下组分:无菌稀释剂,诸如注射用水、盐溶液、不挥发性油、聚乙二醇、甘油、丙二醇或其他合成溶剂;抗细菌剂,诸如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂,诸如抗坏血酸或亚硫酸氢钠;螯合剂,诸如乙二胺四乙酸(edta);缓冲液,诸如乙酸盐、柠檬酸盐或磷酸盐,以及用于调节张力的剂,诸如氯化钠或葡萄糖。可用酸或碱(诸如盐酸或氢氧化钠)调节ph。肠胃外制剂可封装在由玻璃或塑料制成的安瓿、一次性注射器或多剂量小瓶中。
[0605]
适用于可注射用途的药物组合物包括无菌水溶液(其中可溶于水的)或分散体和用于临时制备无菌可注射溶液或分散体的无菌粉末。对于静脉内施用,合适的载体包括生理盐水、抑菌水、cremophor el
tm
(basf,parsippany,n.j.)或磷酸盐缓冲盐水(pbs)。在所有情况下,组合物必须为无菌的且应当为易于注射的流体。在制备和储存的条件下它必须稳定并且必须针对诸如细菌和真菌的微生物污染作用而防腐。载体可以是溶剂或分散介质,所述溶剂或分散介质含有例如水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇等)和其适合的混合物。例如,通过使用例如卵磷脂的包衣,在分散体的情况下通过保持所需的颗粒大小,和通过使用表面活性剂,可以保持适当的流动性。对微生物作用的预防可通过各种抗细菌剂和抗真菌剂(例如对羟基苯甲酸酯、氯丁醇、苯酚、抗坏血酸、硫柳汞等)来实现。在一些实施方案中,将期望在组合物中包含等渗剂,例如糖类、多元醇(诸如甘露醇、山梨醇)、氯化钠。可通过在组合物中包含延迟吸收的剂(例如单硬脂酸铝和明胶)来实现可注射组合物的延长吸收。
[0606]
可通过根据需要将所需量的活性化合物与一种上文列举的成分或其组合并入适当的溶剂中,随后进行过滤灭菌来制备无菌注射溶液。通常,通过将活性化合物并入无菌媒介物中来制备分散体,所述媒介物含有碱性分散介质和上文列举的所需要的其他成分。在用于制备无菌注射溶液的无菌粉剂的情况下,制备方法是真空干燥和冷冻干燥,所述冷冻干燥从其先前无菌过滤溶液中得到活性成分和任何另外所需成分的粉末。
[0607]
口服组合物通常包含惰性稀释剂或可食用载体。可将它们封装在明胶胶囊中或压成片剂。出于口服治疗性施用的目的,可将活性化合物与赋形剂合并,并且以片剂、锭剂或
胶囊形式使用。还可使用流体载体制备用作嗽口剂的口服组合物,其中化合物于流体载体中口服施加,并且漱口并吐出或吞咽。可包含药物相容性结合剂和/或佐剂材料作为组合物的一部分。片剂、丸剂、胶囊剂、含片等可含有以下成分中的任一种或具有类似性质的化合物:粘合剂,诸如微晶纤维素、黄蓍胶或明胶;赋形剂诸如淀粉或乳糖,崩解剂诸如海藻酸、primogel或玉米淀粉;润滑剂,诸如硬脂酸镁或sterotes;助流剂,诸如胶体二氧化硅;甜味剂,诸如蔗糖或糖精;或调味剂,诸如薄荷、水杨酸甲酯或橙子调味剂。
[0608]
对于通过吸入施用,将化合物以气溶胶喷雾的形式从含有合适的推进剂(例如,气体,诸如二氧化碳)的压力容器或分配器或者喷雾器中递送。
[0609]
全身施用也可通过透粘膜或透皮方式进行。对于透粘膜或透皮施用,在制剂中使用适于待渗透的屏障的渗透剂。此类渗透剂在本领域中是普遍已知的,并且对于经粘膜施用,包括例如清洁剂、胆汁盐和夫西地酸(fusidic acid)衍生物。可通过使用鼻用喷雾剂或栓剂实现经粘膜施用。对于透皮施用,将活性化合物配制成软膏、药膏、凝胶或乳膏,如本领域通常已知的。
[0610]
化合物还可被制备为栓剂(例如,具有常规栓剂基质诸如可可脂和其他甘油酯)或保留灌肠剂的形式,以用于直肠递送。
[0611]
在一个实施方案中,活性化合物与将保护化合物使其免于从体内快速消除的载体一起制备,诸如受控释放制剂,包括植入物和微囊化递送系统。可使用生物可降解的、生物相容的聚合物,诸如乙烯乙酸乙烯酯、聚酸酐、聚乙醇酸、胶原、聚原酯和聚乳酸。用于制备此类制剂的方法将为本领域技术人员显而易知。还可从alza corporation和nova pharmaceuticals,inc.商购获得材料。脂质体悬浮液(包括具有针对病毒抗原的单克隆抗体的靶向受感染细胞的脂质体)也可用作药学上可接受的载体。这些悬浮液可根据本领域技术人员已知的方法来制备,例如,如美国专利号4,522,811中所述。
[0612]
特别有利的是,将口服或肠胃外组合物配制成易于施用和均匀剂量的剂量单位形式。如本文所用,剂量单位形式指适合作为用于待治疗的受试者的单一剂量的物理离散单位;每个单位含有计算为与需要的药物载体结合以产生所需治疗效果的预定量的活性化合物。本公开的剂量单位形式的规格由以下规定并且直接取决于以下情况:活性化合物的独特特征和待实现的特定治疗效果,以及合成此类用于治疗个体的活性化合物的领域内的固有限制。
[0613]
药物组合物可与施用说明书一起包括在容器、包装或分配器中。
[0614]
本发明将在以下实施例中进一步描述,这些实施例不限制权利要求中所述的本发明的范围。
[0615]
实施例
[0616]
实施例1.抗人cd47抗体的表征
[0617]
本文提供的研究旨在评估本公开的抗人cd47抗体的结合。
[0618]
根据本领域已知的技术,使用小鼠杂交瘤技术获得本公开的抗人cd47单克隆抗体。用人cd47对小鼠进行免疫,随后通过elisa筛选杂交瘤与人cd47的结合,随后在背驮式测定中证实其具有细胞毒性,并通过facs证实可结合细胞表面。本公开的小鼠抗人cd47h4l2单克隆抗体包括seq id no:1的重链可变区(vh)和seq id no:2的轻链可变区(vl)。在本公开的一些实施方案中,本公开的示例性抗体包括具有seq id no:1的h4l2重链
可变区的重链和具有seq id no:2的h4l2轻链可变区的轻链。
[0619]
将小鼠抗人cd47单克隆抗体h4l2人源化以形成人源化抗人cd47重链和轻链。如表1所示,本公开的这些人源化抗体重链的示例性实施方案包括具有人igg1 fc结构域的h4l2-higg1重链(seq id no:11)、具有修饰的人igg1 fc结构域的h4l2-higg1增强的重链(seq id no:12)、具有人igg4 fc结构域的h4l2-higg4重链(seq id no:13)和具有修饰的人igg2 fc结构域的h4l2-higg2σ重链(seq id no:14)。本公开的这些人源化抗体轻链的示例性实施方案包括具有人轻链κ结构域的h4l2-h-κ轻链(seq id no:15)。本公开的这些示例性重链和轻链的氨基酸序列如下表1所示。
[0620]
在本公开的一些实施方案中,本公开的示例性抗体包括seq id no:11的重链h4l2-higg1和seq id no:15的轻链h4l2-h-κ。在本公开的一些实施方案中,本公开的示例性抗体包括seq id no:12的h4l2-higg1增强的重链和seq id no:15的轻链h4l2-h-κ。在本公开的一些实施方案中,本公开的示例性抗体包括seq id no:13的重链h4l2-higg4和seq id no:15的轻链h4l2-h-κ。在本公开的一些实施方案中,本公开的示例性抗体包括seq id no:14的重链h4l2-higg2σ和seq id no:15的轻链h4l2-h-κ。
[0621]
表1.抗人cd47小鼠和人源化抗体序列
[0622]
1.抗hucd47 h4l2-higg1 h4重链(氨基酸序列)
[0623]
qvqlvqsgaevkkpgssvklsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgratltvdkststaymelsslrsedtavyycarggvggmdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:11)
[0624]
2.抗hucd47 h4l2-higg1增强的h4重链(氨基酸序列)
[0625]
qvqlvqsgaevkkpgssvklsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgratltvdkststaymelsslrsedtavyycarggvggmdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellagpdvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapeektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:12)
[0626]
3.抗hucd47 h4l2-higg4 h4重链(氨基酸序列)
[0627]
qvqlvqsgaevkkpgssvklsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgratltvdkststaymelsslrsedtavyycarggvggmdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no:13)
[0628]
4.抗hucd47 h4l2-higg2σh4重链(氨基酸序列)
[0629]
qvqlvqsgaevkkpgssvklsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgratltvdkststaymelsslrsedtavyycarggvggmdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssnfgtqtytcnvdhkpsntkvdktverkccvecppcpappaaassvflfppkpkdtlmisrtpevtcvvvdvsaedpevqfnwyvdgvevhnaktkpreeqfnstfrvvsvltvlhqdwlngkeykckvsnkglpssiektisktkgqprepqvytlppsreemtknqvsltclvkgfypsdisvewesngqpennykttppmldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:14)
[0630]
5.抗hucd47 h4l2-hκl2轻链(氨基酸序列)
[0631]
dvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:15)
[0632]
6.抗hucd47 h4l2 h4 vh结构域(氨基酸序列)
[0633]
qvqlvqsgaevkkpgssvklsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgratltvdkststaymelsslrsedtavyycarggvggmdywgqgtlvtvss(seq id no:1)
[0634]
7.抗hucd47 h4l2 l2 vl结构域(氨基酸序列)
[0635]
dvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik(seq id no:2)
[0636]
8.抗hucd47亲本杂交瘤m1-vh1 vh结构域(氨基酸序列)
[0637]
qvqlqqpgaelvrpgasvklscrasgytftnywmtwvkqrpeqglewigridpydvethynhkfqdkailtvdkssstaymqlssltsedsavyycarggvggmdywgqgtsvtvss(seq id no:57)
[0638]
9.抗hucd47 h1 vh结构域(氨基酸序列)
[0639]
qvqlvqsgaevkkpgssvkvsckasgytftnywmtwvrqapgqglewmgridpydvethyaqkfqgrvtitadeststaymelsslrsedtavyycarggvggmdywgqgtlvtvss(seq id no:58)
[0640]
10.抗hucd47 h2 vh结构域(氨基酸序列)
[0641]
qvqlvqsgaevkkpgssvkvsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgrvtitvdeststaymelsslrsedtavyycarggvggmdywgqgtlvtvss(seq id no:59)
[0642]
11.抗hucd47 h3 vh结构域(氨基酸序列)
[0643]
qvqlvqsgaevkkpgssvklsckasgytftnywmtwvrqapgqglewigridpydvethyaqkfqgratltvdeststaymelsslrsedtavyycarggvggmdywgqgtlvtvss(seq id no:60)
[0644]
12.抗hucd47亲本杂交瘤m1-vk1 vl结构域(氨基酸序列)
[0645]
dvlmtqtplslpvslgdqasiscrssqsivhsngntylewylqkpghspnlliyrvskrfsgvpdrfsgsgsgtdftlkitrveaedlgvyycfqgshvprtfgggtkleik(seq id no:75)
[0646]
13.抗hucd47 l1 vl结构域(氨基酸序列)
[0647]
divmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltisslqaedvavyycfqgshvprtfgqgtkleik(seq id no:76)
[0648]
14.抗hucd47 l3 vh结构域(氨基酸序列)
[0649]
dvvmtqspdslavslgeratincrssqsivhssgntylewyqqkpgqppklliyrvskrfsgvpdrfs
gsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik(seq id no:77)
[0650]
15.抗hucd47 l4 vh结构域(氨基酸序列)
[0651]
dvvmtqspdslavslgeratincrssqsivhssgqtylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik(seq id no:78)
[0652]
16.抗hucd47 l5 vh结构域(氨基酸序列)
[0653]
dvvmtqspdslavslgeratincrssqsivhssgstylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik(seq id no:79)
[0654]
使用标准elisa方法测定本公开的示例性抗cd47抗体对人和食蟹猴cd47抗原的亲和力。将这些结合亲和力与抗cd47抗体b6h12-igg1和5f9-igg4进行比较。如表2所示,这些示例性结果证明本公开的示例性抗体以与5f9-igg4和b6h12-igg1抗cd47抗体相当或更好的亲和力结合至人cd47。这些示例性结果还显示本公开的示例性抗体以相当的亲和力结合至人和食蟹猴cd47。
[0655]
表2:人源化抗人cd47抗体对人和食蟹猴cd47抗原的平衡解离常数
[0656]
抗体抗原kd(nm)hu h4l2-igg1人cd470.4309hu h4l2-igg1食蟹猴cd470.18865f9-igg4人cd470.5287b6h12-igg1人cd470.6994
[0657]
还测定了本公开的抗-cd47抗体阻断cd47-sirpα相互作用的能力。在使用标准方案进行的该示例性微量滴定板测定中,在不存在或存在增加浓度的所指示抗cd47抗体的情况下,将磷酸盐缓冲盐水(pbs)中的sirpα/人fc融合蛋白与cd47/小鼠fc蛋白组合。随后洗涤板并将其与hrp缀合的抗小鼠fc二级抗体一起孵育,并用tmb底物显色。如表3所示,这些示例性结果证明本公开的示例性抗体以与5f9-igg4和b6h12-igg1抗cd47抗体相当或更好的ic50阻断cd47-sirpα相互作用。
[0658]
表3:人cd47-sirpα相互作用的阻断测定
[0659]
抗体ic50(nm)hu h4l2-igg11.5875f9-igg41.751b6h12-igg14.789
[0660]
实施例2.掩蔽物发现
[0661]
本文提供的研究旨在鉴定和表征用于本公开的可活化抗人cd47抗体中的掩蔽部分。
[0662]
使用与2010年7月15日公布的pct国际公布号wo 2010/081173中描述的方法类似的方法,将本公开的人源化抗人cd47 hu h4l2单克隆抗体(seq id no:1的vh和seq id no:2的vl)用于筛选总多样性为4x160的随机x
15
肽文库,其中x为任何氨基酸。筛选包括磁激活细胞分选(macs)和荧光激活细胞分选(facs)。经分离和测序的掩蔽肽(mm)的示例性单个克隆的氨基酸序列显示在表4中。
[0663]
表4.抗人cd47掩蔽肽(mm)
id no:697)、可裂解部分3013(avgllappgglsgrsani;seq id no:698)、或可裂解部分5007(aprsalahglf;seq id no:446)、可裂解部分5008(alahglfaprsf;seq id no:447)或可裂解部分5011(glptfvhlprqv;seq id no:450)。
[0667]
虽然以下所示的某些序列包含seq id no:645的间隔区序列,但是本领域普通技术人员应理解,本公开的可活化抗人cd47抗体可包含任何合适的间隔区序列,例如像选自由以下组成的组的间隔区序列:qgqsgqg(seq id no:30)、qgqsgq(seq id no:31)、qgqsg(seq id no:32)、qgqs(seq id no:33)、qgq、qg、gqsgqg(seqid no:34)、qsgqg(seq id no:35)、sgqg(seq id no:36)、gqg、g或q。在一些实施方案中,本公开的可活化抗人cd47抗体可不具有连接至其n末端的间隔区序列。
[0668]
表5.抗人cd47可活化抗体序列
[0669]
8.[间隔区(seq id no:30)][hucd47 h4l2-47.1-5007vl结构域(seq id no:41)]
[0670]
[qgqsgqg][lydcyalsksycmglgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:61)
[0671]
9.[间隔区(seq id no:30)][hucd47 h4l2-47.2-5007vl结构域(seq id no:42)]
[0672]
[qgqsgqg][gdctythskhycesvgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:62)
[0673]
10.[间隔区(seq id no:30)][hucd47 h4l2-47.3-5007vl结构域(seq id no:43)]
[0674]
[qgqsgqg][lecdpymgkamcinygggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:63)
[0675]
11.[间隔区(seq id no:30)][hucd47 h4l2-47.4-5007vl结构域(seq id no:44)]
[0676]
[qgqsgqg][drafcrfygtcwdtwgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:64)
[0677]
12.[间隔区(seq id no:30)][hucd47 h4l2-47.5-5007vl结构域(seq id no:45)]
[0678]
[qgqsgqg][eydhcqyklkcglytgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:65)
[0679]
13.[间隔区(seq id no:30)][hucd47 h4l2-47.6-5007vl结构域(seq id no:46)]
[0680]
[qgqsgqg][tdctyihsksycqnygggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:66)
[0681]
14.[间隔区(seq id no:30)][hucd47 h4l2-47.7-5007vl结构域(seq id no:
47)]
[0682]
[qgqsgqg][sscqygwrpevcplkgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:67)
[0683]
15.[间隔区(seq id no:30)][hucd47 h4l2-47.8-5007vl结构域(seq id no:48)]
[0684]
[qgqsgqg][kcsrpthpfknecqngggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:68)
[0685]
16.[间隔区(seq id no:30)][hucd47 h4l2-47.9-5007vl结构域(seq id no:49)]
[0686]
[qgqsgqg][gwdcysiskhicnpkgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:69)
[0687]
17.[间隔区(seq id no:30)][hucd47 h4l2-47.10-5007vl结构域(seq id no:50)]
[0688]
[qgqsgqg][sslrcinmlkcypatgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:70)
[0689]
18.[间隔区(seq id no:30)][hucd47 h4l2-47.11-5007vl结构域(seq id no:51)]
[0690]
[qgqsgqg][lscygpklkqectmlgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:71)
[0691]
19.[间隔区(seq id no:30)][hucd47 h4l2-47.12-5007vl结构域(seq id no:52)]
[0692]
[qgqsgqg][pnlctyprqtcpfktgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:72)
[0693]
20.[间隔区(seq id no:30)][hucd47 h4l2-47.13-5007 vl结构域(seq id no:53)]
[0694]
[qgqsgqg][srcygpylarqclshgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:73)
[0695]
21.[间隔区(seq id no:30)][hucd47 h4l2-47.14-5007vl结构域(seq id no:54)]
[0696]
[qgqsgqg][kclnhwnnpnhtcnkgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleik](seq id no:74)
[0697]
22.[间隔区(seq id no:30)][hucd47 h4l2-47.1-5007轻链(seq id no:81)]
[0698]
[qgqsgqg][lydcyalsksycmglgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec](seq id no:101)
[0699]
23.[间隔区(seq id no:30)][hucd47 h4l2-47.2-5007轻链(seq id no:82)]
[0700]
[qgqsgqg][gdctythskhycesvgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec](seq id no:102)
[0701]
24.[间隔区(seq id no:30)][hucd47 h4l2-47.3-5007轻链(seq id no:83)]
[0702]
[qgqsgqg][lecdpymgkamcinygggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec](seq id no:103)
[0703]
25.[间隔区(seq id no:30)][hucd47 h4l2-47.4-5007轻链(seq id no:84)]
[0704]
[qgqsgqg][drafcrfygtcwdtwgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec](seq id no:104)
[0705]
26.[间隔区(seq id no:30)][hucd47 h4l2-47.5-5007轻链(seq id no:85)]
[0706]
[qgqsgqg][eydhcqyklkcglytgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec](seq id no:105)
[0707]
27.[间隔区(seq id no:30)][hucd47 h4l2-47.6-5007轻链(seq id no:86)]
[0708]
[qgqsgqg][tdctyihsksycqnygggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec](seq id no:106)
[0709]
28.[间隔区(seq id no:30)][hucd47 h4l2-47.7-5007轻链(seq id no:87)]
[0710]
[qgqsgqg][sscqygwrpevcplkgggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec](seq id no:107)
[0711]
29.[间隔区(seq id no:30)][hucd47 h4l2-47.8-5007轻链(seq id no:88)]
[0712]
[qgqsgqg][kcsrpthpfknecqngggssggsaprsalahglfgggsdvvmtqspdslavslgeratincrssqsivhsngntylewyqqkpgqppklliyrvskrfsgvpdrfsgsgsgtdftltissvqaedvgvyycfqgshvprtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqd
h4l2-igg4 hc/h4l2-47.1-5007lc(seq id no:1的vh和seq id no:48的vl)、hu h4l2-igg4 hc/h4l2-47.1-5007lc(seq id no:1的vh和seq id no:49的vl)、hu h4l2-igg4 hc/h4l2-47.1-5007lc(seq id no:1的vh和seq id no:50的vl)、hu h4l2-igg4 hc/h4l2-47.1-5007lc(seq id no:1的vh和seq id no:51的vl)、hu h4l2-igg4 hc/h4l2-47.1-5007lc(seq id no:1的vh和seq id no:52的vl)、hu h4l2-igg4 hc/h4l2-47.1-5007lc(seq id no:1的vh和seq id no:53的vl)以及hu h4l2-igg4 hc/h4l2-47.1-5007lc(seq id no:1的vh和seq id no:54的vl)。本公开的人源化抗人cd47抗体hu h4l2-igg4 hc/h4l2 lc(seq id no:1的vh和seq id no:2的vl)用作对照。测定了本公开的这些掩蔽肽的掩蔽效率(即,可活化抗体的结合亲和力与亲本抗体的结合亲和力的比率)并显示在表6中。这些示例性结果表明所有示例性掩蔽肽表现出至少2个数量级的掩蔽效率,14个示例性掩蔽肽中有12个表现出超过三个数量级的掩蔽效率。
[0726]
表6:抗cd47可活化抗体的掩蔽效率
[0727]
可活化抗体的掩蔽肽掩蔽效率47.1》10347.2》10347.3》10347.4》10347.5》10347.6》10347.7》10347.8》10347.9》10347.1026047.11》10347.12》10347.13》10347.14186
[0728]
如图1b所示,将某些示例性抗cd47可活化抗体用蛋白酶蛋白裂解酶处理(在37℃下过夜),然后用elisa测定以确定它们与人cd47抗原的结合亲和力。如这些示例性结果所示,用可特异性裂解可裂解部分的蛋白酶裂解可活化抗体使可活化抗体的结合亲和力得以恢复,使得它们与亲本抗cd47抗体基本相同。这些示例性结果表明,当被蛋白裂解酶活化时,本公开的示例性抗cd47可活化抗体可以与亲本抗体相当的亲和力特异性结合至其cd47靶标。
[0729]
实施例3:掩蔽肽的抗体依赖性细胞吞噬作用(adcp)测定
[0730]
本文提供的研究旨在测定本公开的可活化抗人cd47抗体通过影响fcγriia受体途径诱导抗体依赖性细胞吞噬作用(adcp)。如这些示例性结果表明,与未掩蔽的亲本抗cd47抗体相比,含有本公开的掩蔽肽的完整可活化抗体通过fcγriia受体途径显示出较低的adcp活化。
[0731]
在该测定(fcγriia-h adcp reporter bioassay,promega)中,将表达靶抗原的
靶细胞与具有fcγriia-h受体的工程化效应细胞系共培养。在存在通过抗原结合结构域结合靶抗原同时通过fc效应结构域结合效应细胞上的fcγriia的抗体的情况下,抗体结合导致来自效应细胞系的fcγriia受体聚集、细胞内信号传导和nfat-re介导的荧光素酶活性。测量由荧光素酶活性产生的发光强度作为adcp的指标。
[0732]
参考表7和图2,显示了如在fcγriia介导的adcp测定中测定的本公开的所示抗cd47可活化抗体(如本文实施例1所定义)的ec50和掩蔽效率。将指示的测试物品的量添加到细胞共培养物中并测量发光。这些示例性结果表明,与亲本抗体(ab)相比,所有示例性抗cd47可活化抗体都显示出掩蔽。使用具有掩蔽肽47.11和47.12的本公开的抗cd47可活化抗体观测到最高的观测掩蔽效率。
[0733]
表7:cd47可活化抗体在fcγriia adcp测定中的掩蔽效率
[0734][0735][0736]
实施例4:fc效应结构域的抗体依赖性细胞吞噬作用(adcp)测定
[0737]
本文提供的研究旨在测定本公开的可活化抗人cd47抗体通过影响fcγriia受体途径诱导抗体依赖性细胞吞噬作用(adcp)。如这些示例性结果表明,与未掩蔽的亲本抗cd47抗体相比,含有本公开的掩蔽肽的完整可活化抗体通过fcγriia受体途径显示出较低的adcp活化。这些示例性结果还表明,具有igg1 fc效应结构域的本公开的抗体和可活化抗体显示出比具有igg4 fc效应结构域的那些抗体更高水平的adcp。
[0738]
参考表8和图3a-3d,本公开的所指示抗cd47可活化抗体的ic50和掩蔽效率如实施例3中所述在fcγriia介导的adcp测定中测定。测定的测试制品为hu抗cd47 h4l2-higg1(“h4l2-igg1”;seq id no:11的hc,seq id no:1 5的lc)、hu抗cd47 h4l2-higg1增强的(“h4l2-igg1-en”;seq id no:12的hc,seq id no:15的lc)、hu抗cd47 h4l2-higg4(“h4l2-igg4”;seq id no:13的hc,seq id no:15的lc)、hu抗cd47 h4l2-higg1-47.3-5007(“h4l2-igg1”;seq id no:11的hc,seq id no:83的vl)、hu抗cd47 h4l2-higg1-47.10-5007
(“h4l2-igg1”;seq id no:11的hc,seq id no:90的vl)和hu抗cd47 h4l2-higg1-47.14-5007(“h4l2-igg1”;seq id no:11的hc,seq id no:94的vl)。相对于抗cd47抗体5f9-igg4测试了本公开的这些抗体。在这些测定中测试的靶细胞是nci h82细胞(图3a和图3b)和jurkat细胞(图3c和图3d)。
[0739]
表8:cd47抗体和可活化抗体的fcγriia介导的adcp测定
[0740][0741]
这些示例性结果表明,与具有igg4结构域的抗体相比,基于igg1效应fc结构域的示例性抗cd47抗体显示出更高的adcp活性。这些示例性结果表明,与未掩蔽的亲本抗体(ab)相比,完整的示例性抗cd47可活化抗体显示出更低的adcp活性。
[0742]
实施例5:fc效应结构域的抗体依赖性细胞吞噬作用(adcp)测定
[0743]
本文提供的研究旨在测定本公开的可活化抗人cd47抗体以测量它们诱导抗体依赖性细胞吞噬作用(adcp)的能力。这些示例性结果还表明,具有igg1 fc效应结构域的本公开的抗体和可活化抗体显示出比具有igg2σfc效应结构域的那些抗体更高水平的adcp。
[0744]
在该测定中,使用ficoll histopaque溶液从3个供体中分离出新鲜的外周血单核细胞(pbmc)。使用抗cd14微磁珠对pbmc进行分选和纯化,并用抗cd14 apc抗体和facs分析进行验证。将纯化的细胞培养14天,并使用cd11b pe抗体验证分化的巨噬细胞,然后进行facs分析。将每孔约25,000个巨噬细胞接种到96孔板中。将每个测试物品在pbs中以指定浓度制备并添加到板中。洗涤大约1x106个靶细胞并用荧光染料标记并添加到含有巨噬细胞的96孔板中。使用incucyte s3以10倍成像每30分钟扫描板,并如图所示测量强度。
[0745]
参考图4a至图4c,所测定的测试制品是hu抗cd47 h4l2-higg1(“h4l2-igg1”;seq id no:11的hc,seq id no:15的lc)、h4l2-higg1增强的hu抗cd47(“h4l2-igg1-en”;seq id no:12的hc,seq id no:15的lc)和hu抗cd47 h4l2-higg2σ(“h4l2-igg2σ”;seq id no:14的hc,seq id no:15的lc)。在这些测定中测试的靶细胞是daudi细胞,该细胞源自人b淋巴母细胞。
[0746]
这些示例性结果表明,用本公开的h4l2-igg1和h4l2-igg1-en抗cd47抗体观察到adcp效应,该效应大于用本公开的h4l2-igg2σ观察到的效应。
[0747]
实施例6:h82和raji异种移植模型中的抗人cd47-aadc体内功效
[0748]
该实施例显示,与媒介物对照相比,本公开的抗人cd47可活化抗体在小鼠异种移植模型中是有效的。这些示例性结果表明,与媒介物对照相比,本公开的这些抗cd47抗体在该模型中显示出体内功效。
[0749]
图5a和图5b显示出本公开的抗人cd47抗体的功效:hu抗cd47h4l2-higg1(“h4l2-igg1”;seq id no:11的hc,seq id no:15的lc)、h4l2-higg1增强的hu抗cd47(“h4l2-igg1 en”;seq id no:12的hc,seq id no:15的lc),hu抗cd47 h4l2-higg4(“h4l2-igg4”;seq id no:13的hc,seq id no:15的lc)和hu抗cd47 h4l2-higg2σ(“h4l2-igg2σ”;seq id no:14的hc,seq id no:15的lc)。相对于pbs缓冲液媒介物对照和抗cd47抗体5f9-igg4测试了本公开的这些抗体。每隔一天以10mg/kg的剂量向具有h82细胞系异种移植物(源自人小细胞肺癌)的nod/scid小鼠给予指定的测试物品,持续4周,并在指定的天数测量肿瘤大小。参考图5a,这些示例性结果表明本公开的抗cd47抗体显示出与5f9抗体相当的抗肿瘤活性。
[0750]
参考图5b,测试了本公开的所指示抗cd47抗体在具有表达cd20的raji细胞异种移植物(源自人b细胞淋巴瘤)的nod/scid小鼠中的体内功效。相对于pbs缓冲液媒介物对照和抗cd20抗体利妥昔单抗测试了本公开的这些抗体。每隔一天以10mg/kg的剂量给予测试物品,持续4周,并在指定的天数测量肿瘤大小。还将测试制品与单独的或与本公开的h4l2-igg4抗体组合的利妥昔单抗进行比较。图5b中所示的示例性结果表明,本公开的抗cd47抗体显示出高于媒介物对照和利妥昔单抗的抗肿瘤活性,其中h4l2-igg4/利妥昔单抗组合显示出最高的相对功效。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1