用于在临床诊断过程中进行虚拟交叉研究的系统和方法与流程
背景技术:
1、本发明总体上涉及临床诊断过程,更具体地说,涉及在该过程中使用临床诊断分析仪和系统以及包括这种分析仪的同等组(peer group)进行虚拟交叉(cross over)研究的系统和方法。
2、临床诊断实验室使用各种质控方案来确保所采用的临床诊断过程和用于分析患者样本或其他测试样本的临床诊断分析仪提供准确的诊断结果。一种常见的质控方案涉及使用用于测试患者样本的相同分析仪和过程来测试具有已知特性的质控(qc)材料。用具有已知特性的材料运行这种质控测试确保了用于执行测试的临床诊断分析仪提供预期的和准确的结果,或者提供预定范围或规格内的结果,并且同样确保了与分析仪结合使用的试剂和过程提供预期的结果。
3、虽然使用具有已知特性的质控材料进行质控测试通常是有用的,但是当必须补充质控材料时,会出现统计控制问题。因为质控材料有效期有限,并且因为使用质控材料的qc测试消耗该材料,所以实验室必须定期处理新批次的质控材料的获得和使用,因此要求实验室交叉并开始使用新批次的qc材料。交叉到新的qc材料对实验室来说是一项艰巨的任务,因为在依靠新的质控材料进行进一步测试之前,必须确保新质控材料的可靠性和准确性。即使新批次的qc材料具有与先前批次相似的特性,批次之间的差异也会影响检测的准确性,尤其是在可以对新质控材料进行足够数量的检测之前。而且,即使另一个实验室已经改用新批次的质控材料,来自该另一个实验室的数据也不能简单地被另一个实验室使用,因为如果使用来自另一个实验室的数据,每个实验室的测试方法和设备中隐含的偏差会导致不准确。
4、因此,实验室必须进行交叉研究,以验证新材料的准确性,然后才能确保测试的预期准确性。对于质控材料的任何变化,都必须进行此类交叉研究,因为即使质控材料具有插入范围,即经过分析的质控材料,插入范围也仅供实验室用于快速确定其是否处于控制状态,而不是用于性能监控。
5、交叉研究通常涉及确定新批次的质控材料的统计行为,即计算或估计新材料的平均值和标准差(sd)。为了获得平均值和sd测量值,交叉研究的一般方法是随着时间的推移评估样品并收集新质控材料的数据,直到收集到足够的数据并根据收集的数据计算平均值和标准差,然后,一旦计算完成,就使用新质控材料在将来的质控测试中使用和分配所计算的平均值和标准差。
6、在《定量测量程序的统计质控:原理和定义;批准指南——第三版》(statisticalquality control for quantitative measurement procedures:principles anddefinitions;approved guideline–third edition)中描述了一种普遍接受的进行初始评估的方法,要求在不同的日期对每个质控水平的质控材料进行至少二十次不同的测量。因此,这种普遍接受的方法需要在20天的时间内,针对每个质控水平收集至少20个数据点。因此,例如,对于包含30种不同分析物的三级质控材料,必须进行90次单独的研究,并为每次单独测试收集数据点。然后,收集的数据用于估计新批次材料的平均值和sd。除了所需的时间之外,这种研究还会给实验室带来费用,在测试过程中收集的每个分子数据点都会产生单独的费用。这种研究也是劳动密集型的。由于没有进行此类交叉研究的标准化系统,大多数实验室通常使用电子表格手动处理收集的数据,并手动输入数据来计算新质控材料的平均值和sd。
7、即使按照普遍推荐的程序进行交叉研究花费了时间、费用,且效率低下,这些研究的结果也没有达到实验室期望或要求的准确度。例如,虽然20个数据点足以确定新材料的平均值,但是收集该数量的数据点不是必要的,因此效率低下,因为仅使用10个数据点就可以确定平均值。因此,普遍推荐的交叉研究方法在确定平均值时会导致不必要的测试和费用。此外,20个数据点不足以确定期望精度水平的sd,要实现这一点,通常需要80个数据点。因此,使用通常推荐的方法通常会导致估计的sd具有较高的误差容限。
8、认识到上述局限性后,业界提出了一种替代方法来确定新质控材料的标准差,该方法仅使用10个数据点,通过合并旧材料的平均值和标准差、使用公式sdnew=(meannew*cvold)/100来确定新质控材料的标准差,其中cvold=100*(sdold/meanold)。然而,尽管该替代测定需要的数据点更少,因此花费的时间更少,但是使用该方法的结果仍然会导致平均值计算中潜在的不准确性(参见,例如,《定量测量程序的c24统计质控:原理和定义,第4版》(c24 statistical quality control for quantitative measurement procedures:principles and definitions,4th edition))。
9、不考虑所使用的计算,进行交叉研究的已知方法要求每个单独的实验室对新批次的质控材料进行分析,并且在例如患者样本的测试可以开始之前完成交叉研究。
10、因此,很明显,在本领域中仍然需要进行交叉研究的系统和方法,以加速该过程并克服本领域中已知方法的不足。
技术实现思路
1、本发明涉及一种用于在使用临床诊断分析仪的临床诊断过程以及在使用临床诊断分析仪的系统、系统组和系统同等组中进行虚拟交叉研究的系统和方法。
2、在示例性实施例中,本发明的系统和方法使用一个或多个临床诊断分析仪,通过依靠从已经在使用新批次的质控材料并且已经从该新批次的材料收集了数据的类似实验室的同等组中收集的与新批次的材料相关联的数据,来对新批次的质控材料进行虚拟交叉研究。使用比较数据来关联来自先前或旧批次的质控材料的数据,以考虑单独实验室中的偏差,在评估或分析任何新批次的材料之前,计算新批次的质控材料的预测的平均值和标准差。使用贝叶斯(bayesian)方法,在实验室对新批次的质控材料进行评估之前,使用来自新批次的质控材料的同等统计来生成新批次的质控材料的实验室平均值的估计值。新批次的质控材料的实验室数据以加权方式纳入,以更新新批次的质控材料的实验室平均值的估计值,该值进一步用于估计新批次的质控材料的sd。
3、在一个方面,通过使用来自同等组的关于质控材料的先前批次号(lot number)和关于由同等组收集的新批次号的数据,可以对新批次的质控材料发起虚拟交叉研究。根据同等组数据来计算估计的或预测的平均值和标准差(sd)值,实验室的交叉研究可以在对新批次的质控材料进行任何新分析之前开始。随着测试的继续和对新批次的质控材料进行新的分析,实际数据被整合到预测值的计算中,直到至少已经收集了所需目标数量的新数据点——通常至少10个——此时,仅使用实际收集的数据就可以继续计算平均值和标准差。在另一方面,在计算中对来自已完成分析的数据进行加权,以在收集实际数据时给予实际数据更多的优先权。
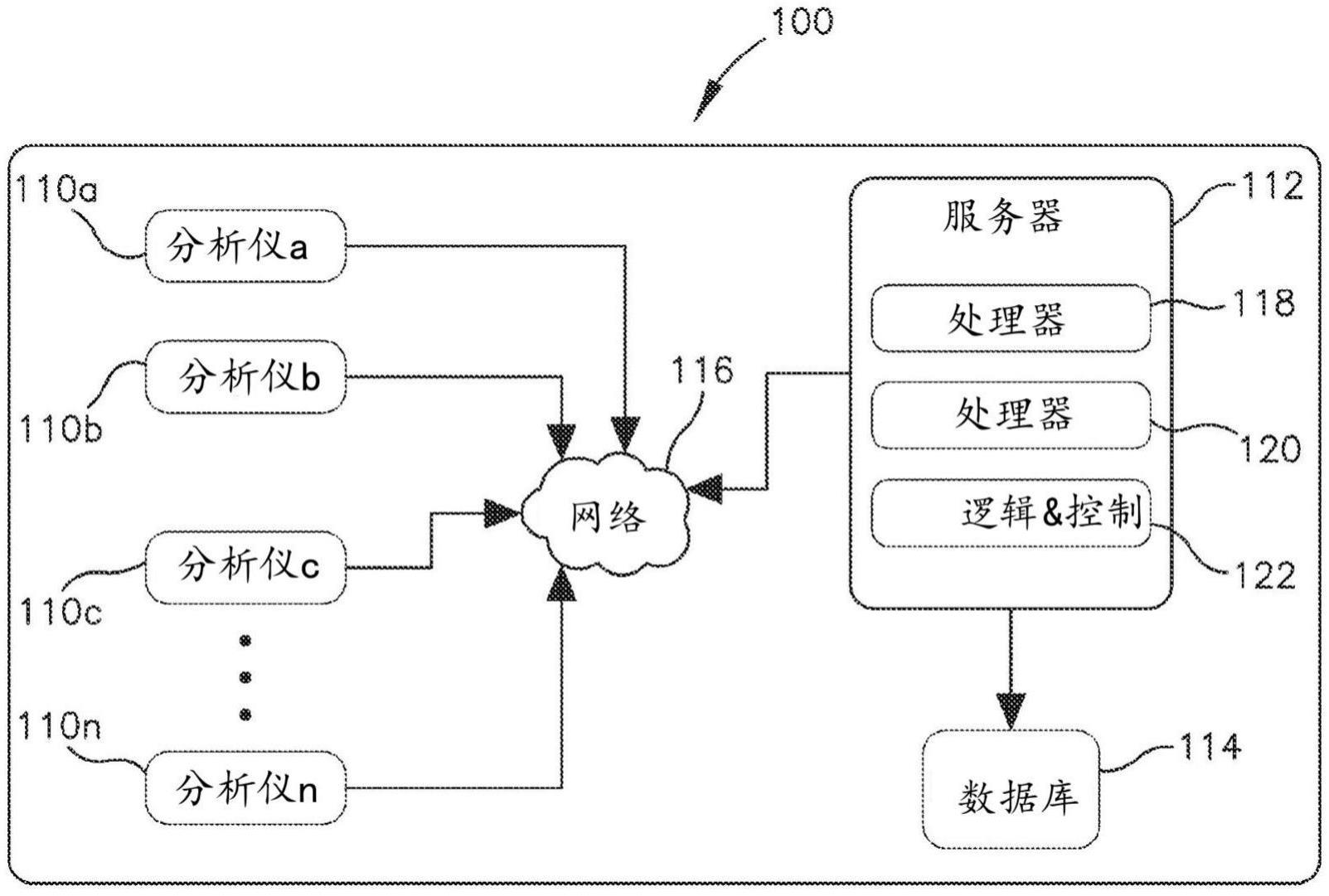
4、在另一方面,用于执行虚拟交叉研究的临床诊断分析仪包括处理器、存储器、测量硬件和输入面板/显示器。分析仪提示用户开始虚拟交叉研究,并访问来自同等组的关于新批次和旧批次的qc材料的数据。分析仪计算新批次的qc材料的估计平均值和标准差,并且进一步提示用户装载或自动装载来自新批次的材料的qc样本,并且发起测试和分析以确定新材料的平均值和标准差。
5、在另一方面,一组实验室,每个实验室包括一个或多个临床诊断分析仪,在同等组配置中相互通信,其中在同等组的成员之间共享信息和数据。共享信息可以包括与所执行的分析相关的数据以及与实验室中使用的质控材料相关的信息。
6、另一方面,当新批次的质控材料的分析仍在进行中时,同等组估计的平均值和标准差值使得实验室能够继续进行交叉研究,就像交叉研究已经完成一样——使用预测的平均值和标准差值。因此,交叉研究对实验室操作的影响被最小化。
7、参考说明书的剩余部分,包括附图和权利要求,将会认识到本发明的其他特征和优点。本发明的其他特征和优点,以及本发明的各种实施例的结构和操作,将在下面参照附图和权利要求进行详细描述。在附图中,相同的附图标记表示相同或功能相似的元件。
- 还没有人留言评论。精彩留言会获得点赞!