苯甲酸酯类化合物在制备缓解或治疗类风湿性关节炎的药物的应用
1.本发明涉及苯甲酸酯类化合物的应用,特别涉及苯甲酸酯类化合物在治疗类风湿性关节炎疾病中的应用,属于生物医药技术领域。
背景技术:
2.类风湿性关节炎(ra)是一种慢性进行性的自身免疫性疾病,以关节滑膜炎及对称性、破坏性的关节病变为主要特征,在工业化国家中,类风湿性关节炎影响着0.5
‑
1%的成年人,这种疾病最常见于女性和老年人。不受控制的活动性类风湿关节炎会导致关节损伤、残疾、生活质量下降以及心血管疾病和其他合并症。该病的诊断是包括放射成像,血液和血清学标志物评估的组合方法,其发病机制尚未明确。
3.传统治疗药物如抗风湿药、非甾体抗炎药和糖皮质激素等具有不可预期的不良反应。当关节炎不受控制或抗风湿药产生毒性作用时可使用生物制剂,但感染和高昂费用限制了生物制剂的应用。中草药治疗ra的历史悠久,其较少的不良反应和适中的治疗效果使其在关节炎治疗中作为补充和替代的治疗手段。
4.有报道显示苯甲酸钠在实验性脑脊髓膜炎(eae)中具有治疗效果。苯甲酸衍生酚酸物质,如没食子酸对ra的患者的滑膜组织分离的成纤维细胞样滑膜细胞(ra
‑
fls)细胞具有抗炎作用;原儿茶酸通过减低脂质过氧化物的表达和反应性自由基一氧化氮的水平以及增加抗氧化酶表达(sod、过氧化氢酶、gsh等)显着减少了大鼠佐剂诱导的关节炎(aia)中的爪肿胀,抗关节炎活性与双氯芬酸钠相当。芍药苷可能通过肠道菌群中的羧酸酯酶代谢生成苯甲酸发挥其药效作用如抗抑郁、免疫调节,苯甲酸可能是芍药苷发挥抗关节炎的活性代谢物。
5.但类风湿性关节炎疾病作为一种慢性疾病,其理想药物的药代动力学性质为存在持久的体内暴露,而苯甲酸吸收和分布迅速、消除速度快不利于其抗炎免疫药效的发挥。
技术实现要素:
6.发明目的:本发明的目的是提供一种苯甲酸酯类化合物在制备缓解或治疗类风湿性关节炎的药物的应用。
7.技术方案:本发明公开了所述苯甲酸酯类化合物在制备缓解或治疗类风湿性关节炎的药物的应用,如式i所示,其中n1=1,2,3,4,5,6,7,n2=1,2,3,4,5,6。
[0008][0009]
优选的,所述苯甲酸酯类化合物为式v所示苯甲酸
‑
十八碳烯醇酯化合物,其中n1=7,n2=6,分子式:c
25
h
40
o2,分子量:372.303。
[0010][0011]
优选的,所述药物剂型为片剂、胶囊剂、口服溶液剂、丸剂、颗粒剂或散剂。
[0012]
优选的,所述药物剂型还包括凝胶剂、涂剂、贴剂、外用溶液剂、气雾剂或注射剂。
[0013]
优选的,所述的苯甲酸酯类化合物包括其衍生物和药物载体。
[0014]
本发明公开的苯甲酸酯类化合物药物持续时间长、浓度波动较小,具有更优药代动力学特点,在制备缓解或治疗类风湿性关节炎的药物的应用的有效性更好,作用更明显,具有潜在的制药应用前景;以cia小鼠作为模型动物,通过灌胃给予苯甲酸
‑
十八碳烯醇酯、苯甲酸钠治疗,测定足爪肿胀程度、关节病理评分进行苯甲酸
‑
十八碳烯醇酯治疗类风湿性关节炎的评价。药效学实验结果表明,本发明苯甲酸酯类化合物对类风湿性关节炎具有较好的药理作用,给药后缓解cia小鼠关节肿胀度,改善cia小鼠关节组织病理学变化;体内代谢研究结果表明,本发明苯甲酸酯类化合物能够表现出更好的药代动力学行为,增加其活性产物苯甲酸的体内暴露量。苯甲酸
‑
十八碳烯醇酯化合物提高了药物的脂溶性和被动的膜渗透能力,提高药物的口服吸收度,口服后在肠道中被肠道菌群的羧酸酯酶水解后再释放原药苯甲酸,延长了药物的作用时间。
[0015]
有益效果:与现有技术相比,本发明具有如下显著优点:苯甲酸酯类化合物在体内药物持续时间长、浓度波动较小,具有更优药代动力学特点,应用于慢性疾病类风湿性关节炎疾病,持久的体内暴露可缓慢释放苯甲酸,苯甲酸在体内浓度更为持久稳定,抗关节炎药效良好。苯甲酸酯类化合物应用在制备缓解或治疗类风湿性关节炎的药物中,能有效缓解治疗类风湿性关节炎。
附图说明
[0016]
图1为苯甲酸
‑
十八碳烯醇酯化合物的制备反应式;
[0017]
图2为苯甲酸
‑
十八碳烯醇酯化合物的核磁共振氢谱图;
[0018]
图3为苯甲酸
‑
十八碳烯醇酯化合物的核磁共振碳谱图;
[0019]
图4为关节炎临床评分平均值随时间变化图,其中control组为对照组,cia为模型组,nab为模型动物苯甲酸钠给药组,lef为模型动物来氟米特阳性药组,ob为模型动物苯甲酸
‑
十八碳烯醇酯给药组;
[0020]
图5为足爪厚度平均值随时间变化图,其中control组为对照组,cia为模型组,nab为模型动物苯甲酸钠给药组,lef为模型动物来氟米特阳性药组,ob为模型动物苯甲酸
‑
十八碳烯醇酯给药组;
[0021]
图6为小鼠体重平均值随时间变化图,其中control组为对照组,cia为模型组,nab为模型动物苯甲酸钠给药组,lef为模型动物来氟米特阳性药组,ob为模型动物苯甲酸
‑
十八碳烯醇酯给药组;
[0022]
图7为每组代表性小鼠初次免疫的第48天处死前左后足拍照,其中control组为对照组,cia为模型组,nab为模型动物苯甲酸钠给药组,lef为模型动物来氟米特阳性药组,ob为模型动物苯甲酸
‑
十八碳烯醇酯给药组;
[0023]
图8为每组代表性小鼠的关节部位病理切片h&e染色,其中control组为对照组,cia组为模型组,nab为模型动物苯甲酸钠给药组,lef为模型动物来氟米特阳性药组,ob为模型动物苯甲酸
‑
十八碳烯醇酯给药组;
[0024]
图9为各组小鼠的h&e染色病理评分结果均值,其中control组为对照组,model组为模型组,nab为模型动物苯甲酸钠给药组,lef为模型动物来氟米特阳性药组,ob为模型动物苯甲酸
‑
十八碳烯醇酯给药组;
[0025]
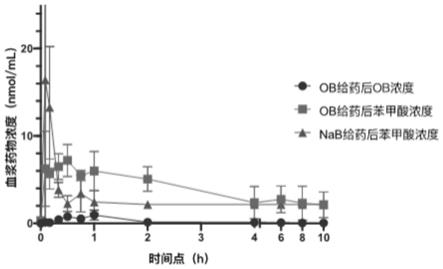
图10为苯甲酸酯前药及苯甲酸单次给药后血浆中苯甲酸药物浓度
‑
时间曲线,其中nab为苯甲酸钠给药组,ob为苯甲酸
‑
十八碳烯醇酯给药组。
具体实施方式
[0026]
下面结合附图对本发明的技术方案作进一步说明。
[0027]
为了评价苯甲酸
‑
十八碳烯醇酯对类风湿性关节炎ra的治疗作用。本发明以cia小鼠作为模型动物,通过灌胃给予苯甲酸及其酯类前药治疗,测定关节炎临床指标(足爪肿胀评分、足爪肿胀厚度及关节部位的he病理切片)进行苯甲酸及其酯类前药治疗关节炎的药效评价。
[0028]
本发明所采用的苯甲酸
‑
十八碳烯醇酯化合物,如图1所示,为苯甲酸
‑
十八碳烯醇酯化合物的制备反应式;所述化合物的制备方法具体包括以下步骤:
[0029]
(1)室温下,取1mmol苯甲酰氯140.6mg、1mmol油醇268.5mg,溶于4ml无水二氯甲烷溶液,室温下搅拌过夜;
[0030]
(2)tlc追踪直至反应完全后,加入10ml1m的nahco3过夜搅拌以除去未反应的苯甲酰氯,二氯甲烷萃取两次,饱和食盐水洗一次,无水硫酸钠干燥,浓缩,柱层析纯化,得苯甲酸
‑
十八碳烯醇酯化合物。
[0031]
如图2所示,为制备而得的苯甲酸
‑
十八碳烯醇酯化合物的核磁共振氢谱图;如图3所示,为制备而得的苯甲酸
‑
十八碳烯醇酯化合物的核磁共振碳谱图。
[0032]
药效评价实验材料如下,来氟米特购自中国食品药品检定研究所;苯甲酸
‑
十八碳烯醇酯的化学结构如图1中所示,由中国药科大学药物化学实验室合成;完全弗氏佐剂试剂购自sigma
‑
aldrich(usa);牛ii型胶原、不完全弗氏佐剂购自chondrex(usa);健康6
‑
7周龄的spf级dba/1j小鼠(雄性),购自常州卡文斯实验动物有限公司。动物在无特定病原体(spf)的条件下(温度22
±
2℃,湿度40
‑
70%,12小时明/暗交替环境),小鼠自由摄食饲养一周适应环境。
[0033]
随后进行类风湿性关节炎小鼠造模,cia模型小鼠的初次免疫:取一定量的完全弗氏试剂与注射器中,然后缓慢滴加等体积的牛ii型胶原(使用前提前3h置于4℃溶化),同时使用电动匀浆机(1000~3000rpm)进行混合,注意热量会使胶原变性从而无法诱发关节炎,在整个混合的过程中应在冰水浴上以冷却乳液,继续以高转速(3000~5000rpm)混合乳液2分钟,完成乳液制备后通过将一滴乳液加入烧杯中来测试乳液的稳定性,如果乳液是稳定的,则乳白色的液滴会漂浮在水面上不会消散开。如果乳液在水表面消散,则表示乳液不稳定,加入几滴完全弗氏佐剂再次混合,然后重新进行测试。充分乳化后的乳液应排尽空气确保注射准确量的乳液,并在制备后的1小时内注射乳液进行造模,保持在4℃直至使用前。针尖斜面的一面朝上并保持与小鼠尾部平行,在小鼠尾根部2cm的距离插入针头,直到针尖到
达距离尾根部0.5cm的位置皮下注射0.1ml乳剂进行初次免疫;初次免疫21天后进行加强免疫,使用电动匀浆机以同样的方法将牛ii型胶原与不完全弗氏佐剂等体积混合,充分乳化后,于模型小鼠尾根部3cm处进针,直到针尖到达尾根部1.5cm处注射0.1ml乳剂(加强免疫应与初次免疫注射在不同的位置)。
[0034]
将dba/1j小鼠分成随机分为6组,设正常小鼠为对照组,将造模后的小鼠随机分为模型组、来氟米特组(阳性药组)、苯甲酸
‑
十八碳烯醇组、苯甲酸钠低剂量组、苯甲酸钠中剂量组,每组共6只小鼠;各组给药剂量见下表1。
[0035]
表1小鼠分组与给药情况
[0036][0037][0038]
各用药组于初次免疫后21天开始进行给药干预,给药溶液配制方法如下,精密称取来氟米特25.0mg,在研钵中少量多次加入0.5%cmc
‑
na溶液共50ml混悬至来氟米特浓度为0.5mg/ml;精密称取苯甲酸
‑
十八碳烯醇酯258.5mg加入50ul吐温80助溶,加入少量0.5%cmc
‑
na超声5min充分溶解后补充溶剂至50ml使其成为均匀的混悬液,浓度为5.17mg/ml;分别精密称取苯甲酸钠50.0mg、100.0mg,分别少量多次加入50ml0.5%cmc
‑
na溶液,使其成为均匀的混悬液,浓度分别为1mg/ml、2mg/ml。给药组均按照0.1ml/10g灌胃给药,一共给药4周。
[0039]
实验期间,每日观察各组小鼠饮食、活动度及皮毛状态,并于初次免疫后27、30、33、36、39、42、45、48天对小鼠进行称重,并根据小鼠关节炎发病情况按0
‑
4分进行关节炎临床评分(polyarthritis index,pi)。0分:无关节炎症(无红肿);1分:小趾关节轻度红肿;2分:小趾关节和足跖肿胀;3分:踝关节以下的足爪肿胀;4分:包括踝关节在内的全部足爪、关节肿胀。根据可个关节的病变程度累计积分,即为每只小鼠的pi,最高16分。用数显游标卡尺测量足垫厚度(小鼠的鼠爪太小因此无法通过体积测量器来确定鼠爪的肿胀情况),初次免疫48天后,将实验小鼠处死,采集踝关节置于4%多聚甲醛中固定,经常规脱钙、脱水、石蜡包埋、切片和h&e染色后,在光镜下观察组织病理学改变。检查指标包括关节软骨破坏程度,滑膜增生、关节腔狭窄,以及间质炎细胞浸润和纤维组织增生程度,根据病变程度进行评分,累计分数算出每组平均分。
[0040]
各组小鼠关节炎评分结果如表2和图4所示,结果表明,正常组小鼠关节无病变症状,模型组小鼠临床评分平均数最高,关节病变程度最严重,来氟米特阳性药组显著降低造模小鼠的关节病变程度,与模型组相比,苯甲酸钠低剂量组、苯甲酸钠中剂量组及苯甲酸
‑
十八碳烯醇酯给药组临床评分也显著降低,说明其具有类似的抗关节炎治疗效果。
[0041]
表2、各组小鼠关节炎临床评分
[0042][0043][0044]
各组小鼠足爪厚度结果如表3和图5所示,踝关节外观病变程度如图6所示,正常组小鼠足爪无肿胀,踝关节、指尖均无红肿,模型组小鼠踝关节、足跖及指节部位均出现明显的红肿,与模型组小鼠相比来氟米特阳性药组显著缓解小鼠足爪部位肿胀的程度、足爪厚度下降,说明阳性药对关节炎有抑制作用,与模型组小鼠相比,苯甲酸钠给药组及其等摩尔酯类前药给药也显著改善关节炎小鼠的疾病进程和关节炎病理特征。
[0045]
表3、各组小鼠足爪厚度平均值
[0046][0047]
各组小鼠体重变化如表4与图7所示,初次免疫造模后随着时间的增加疾病程度加重,小鼠体重会逐渐下降,与正常组小鼠相比,模型组小鼠体重下降明显,各给药组小鼠体重下降程度均低于模型组,其中来氟米特组较模型组体重下降情况明显改善,苯甲酸钠给药组体重下降程度具有一定的剂量依赖性,苯甲酸
‑
十八碳烯醇酯给药组较苯甲酸钠给药组体重下降情况有一定的改善。
[0048]
表4、各组小鼠体重平均值
[0049][0050]
各组小鼠踝关节病理切片结果如表5与图8、图9所示。control组h&e染色结果显示踝关节组织结构正常完整,与control组相比,cia模型组踝关节可见关节软骨破坏、关节滑膜增生、间质炎细胞浸润、纤维组织增生等病理变化;与模型组相比,各给药组可见于模型组相似的病理变化,苯甲酸
‑
十八碳烯醇酯组、苯甲酸钠中剂量组踝关节病变程度较模型组明显降低。
[0051]
表5、各组小鼠h&e染色组织学损伤程度平均值
[0052][0053]
苯甲酸酯类化合物的血浆药代动力学实验:
[0054]
类风湿性关节炎疾病作为一种慢性疾病,其理想药物的药代动力学性质为存在持久的体内暴露,而苯甲酸吸收和分布迅速、消除速度快不利于其抗炎免疫药效的发挥,为此合成苯甲酸
‑
十八碳烯醇酯前药以改善其药代动力学。
[0055]
通过建立gc
‑
ms/ms检测方法,应用于苯甲酸及苯甲酸
‑
十八碳烯醇酯的血浆药代动力学实验,药代动力学实验材料如下,苯甲酸钠标准品购自上海甄准生物科技有限公司;d5‑
苯甲酸同位素标准品购自cambridge isotope laboratories,inc.(cambridge,usa),苯甲酸
‑
十八碳烯醇酯由中国药科大学药物化学实验室合成;内标1,2
‑
13
c2‑
肉蔻酸、衍生化试剂(mstfa+1%tmcs)均购于sigma
‑
aldrich(st.louis,usa),色谱纯的甲醇、庚烷购自merk公司。健康6
‑
7周龄的spf级sd大鼠,购自维通利华实验动物技术有限公司。动物在温度22
±
2℃,湿度40
‑
70%,12小时明/暗交替环境下自由摄食饲养一周适应环境。
[0056]
给药溶液的配置,精密称取苯甲酸
‑
十八碳烯醇酯258.5mg加入50ul吐温80助溶,加入少量0.5%cmc
‑
na超声5min充分溶解后补充溶剂至50ml使其成为均匀的混悬液,浓度为5.17mg/ml;分别精密称取苯甲酸钠100.0mg,少量多次加入50ml0.5%cmc
‑
na溶液,使其
成为均匀的混悬液,浓度为2mg/ml。每只大鼠给药剂量均为1ml/100g。
[0057]
sd大鼠苯甲酸及苯甲酸
‑
十八碳烯醇酯等摩尔剂量单次给药后,对大鼠进行眼眶静脉丛采血,8000rpm x 10min离心取上层血浆于
‑
70℃保存。血浆样品复溶,振荡30s,取50ul血浆,加入200ul含内标甲醇溶液,涡旋振荡3min。(内标为同位素标记的肉蔻酸,母液为5mg/ml,稀释1000倍至5ug/ml)4℃下20000g x10min,离心取上清150ul至gc进样小瓶内插管中,减压挥干后加入60ul衍生化试剂复溶(mstfa:庚烷=1:1),涡旋器振荡3min复溶,室温静置1h进行衍生化反应,gc
‑
ms/ms 1ul进样分析,通过gc
‑
ms/ms方法同时检测血浆中苯甲酸
‑
十八碳烯醇酯前药及苯甲酸的含量。
[0058]
两组大鼠给药后血浆药物浓度随时间变化如图10所示,结果显示苯甲酸钠给药后吸收迅速,没有监测到药物吸收相,给药后苯甲酸浓度高,约为酯类前药给药后苯甲酸cmax的两倍,并在30min内迅速代谢,而前药给药后缓慢释放苯甲酸,代谢时间较苯甲酸直接给药延长,说明合成的前药能够表现出更好的药代动力学行为,增加其活性产物苯甲酸的体内暴露量。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1