一种高纯镁带线锚钉及其植入装置的制作方法
1.本发明涉及医疗器械技术领域,特别涉及一种高纯镁带线锚钉及其植入装置。
背景技术:
2.关节软组织损伤主要是指肌腱、韧带、关节囊等受到直接或间接暴力,或受到长期慢性劳损所引起的一大类创伤综合征,属于运动医学学科的常见疾病,例如,肩袖损伤、膝关节交叉韧带断裂、跟腱断裂等。
3.对于轻度的软组织损伤,一般经过专业医生的正确处理即可较快缓解;而对于严重的软组织损伤,如肌腱撕脱、韧带撕裂或断裂等,则需要进行手术治疗。
4.临床上,对于肩袖撕裂、膝关节副韧带损伤以及踝关节、肘关节软组织损伤等,通常通过植入带线锚钉进行修复治疗。手术时,先使用打孔器在骨面上打出骨隧道,再通过锚钉插入器将锚钉置入皮质骨下,然后使用缝线将撕脱或撕裂的软组织固定在骨表面上,以促进软组织与骨的愈合,达到修复作用。
5.带线锚钉通过将线穿过软组织,并打结将软组织固定在骨表面,已经成为骨科手术中不可或缺的器械之一。经过30多年的发展,不同材料与设计的带线锚钉广泛应用于临床,但都遵循一些共同的原则:一、最大限度地提高拔出强度;二、最大限度地减少急性医源性损伤;三、最大限度地减少长期应用中发生关节炎的可能性。
6.带线锚钉的材料主要有惰性金属(钛及其合金)、peek和高分子可降解材料(如聚乙醇酸、聚乳酸的立体异构体等)。惰性金属在体内不能被降解吸收,而且其弹性模量远大于人骨,会产生应力遮挡效应,造成骨质疏松甚至内固定失败的风险,且长期植入可能释放各种有害离子,引发炎症、过敏的风险,所以多需要在骨愈合后再次手术取出,这不但提高了医疗支出、给患者带来二次伤害并且还增加了患者心理负担。peek材料在人体不能降解,且其强度低、脆性大等,限制了其临床应用。高分子可降解材料也存在诸多问题,如力学性能较低、应用范围局限、降解过程中会产生大量酸性小分子或低聚体从而对周围组织产生刺激导致比较严重的炎性反应,甚至积液、囊肿等,影响手术预后并降低患者的满意度。因此,为了克服以上材料在应用中的各种局限,采用新的材料制备带线锚钉是必要的。镁及镁合金具有良好的生物相容性、力学性能和生物可降解性,而且其无害的降解产物可通过人体新陈代谢排出体外,是一种理想的带线锚钉制备材料。
7.常规的带线锚钉,其在锚钉末端设置穿线孔,固定时,锚钉末端会露出在骨表面,会阻碍肌腱、韧带与骨表面的紧密接触,固定的不牢固,不利于肌腱、韧带与骨表面的粘附结合;还有部分锚钉或结构复杂,或设置不合理导致固定不稳固。
8.常规可吸收带线锚钉钉体材料多采用高分子材料,力学强度不足,钉体的几何结构设计受限,镁的力学强度接近人体皮质骨,用其设计更为优化适合固定腱骨和外科医生操作的类似于我们的锚钉。现有技术中有采用镁合金材料制作,镁合金中添加稀土元素,稀土元素可有效提高镁合金的力学强度,并可通过稳定表面腐蚀产物膜以调控其降解速率,但该类镁合金在长期的安全性方面存在隐患。
技术实现要素:
9.本发明的目的在于提供一种高纯镁带线锚钉及其植入装置,具有良好的生物相容性、力学性能和生物可降解性,在保证腱骨愈合的同时具有更高的力学强度,外科医生的操作更简单,能将肌腱、韧带与骨表面牢固结合,降解机制上相较于高分子材料对人体更为无害。
10.本发明解决其技术问题所采用的技术方案是:一种高纯镁带线锚钉,包括锚钉本体,所述锚钉本体上设有在宽度方向上贯穿锚钉本体的贯通孔,所述锚钉本体后端的中心处设有安装孔,所述安装孔的底部设有穿线孔,所述穿线孔包括左穿线孔和右穿线孔,所述安装孔通过左穿线孔和右穿线孔与贯通孔连通。
11.所述锚钉本体的外表面设有螺纹,所述贯通孔位于靠近锚钉本体后端处,且位于螺纹槽内。本发明的贯通孔位于螺纹槽内,这样不会影响螺纹而导致螺纹被破坏,螺纹保持完整性在骨内的固定更稳定,结合力更好,同时,本发明的穿线孔位于安装孔的底部,这样直接隐藏在了锚钉内部,这样锚钉固定后能与骨表面完全齐平,肌腱、韧带与骨表面的粘附结合紧密,固定牢固,利于恢复。
12.高纯镁的纯度在99.98wt%以上。本发明锚钉材料选择纯度在99.98wt%以上高纯镁,而非常见的镁合金材料,主要基于以下几点考虑:镁合金的制作难度大,成本较高;镁合金由于存在较多其它金属,虽然能够提高合金的强度,但是同时也加快其降解速度,而对于腱骨愈合而言,需要3周左右初步愈合,镁合金由于降解速度快,可能在3周不到的时候已经开始降解,降解会破坏锚钉的完整性,使得固定在骨上的把持力降低,导致腱骨未愈合锚钉已经脱出,影响恢复,即普通的镁合金的降解与腱骨愈合的恢复不适配。而本发明通过研究发现,选择高纯镁,强度可以达到要求,关键的在于在3周左右能维持锚钉的完整性,基本不降解,而是在一个月之后才开始降解,直到一年左右降解完成,非常符合腱骨愈合的周期。同时,镁合金含有的金属如锌、钙之类,非人体需要的大量元素,降解后容易造成潜在的隐患,还会使得锚钉周边的骨溶降。镁本身是人体存在的大量元素,采用高纯镁杂质少,降解后的安全性好。
13.所述锚钉本体的外表面设有螺纹,所述贯通孔位于靠近锚钉本体后端处,且位于螺纹槽内。
14.所述安装孔为正方形孔或内六角孔;所述穿线孔的形状为圆形或方形。安装孔为正方形孔或内六角孔,这样方便转动装配。
15.制备方法包括如下步骤:(1)将铸态高纯镁锭通过超声波探伤确定内部缺陷,并通过机械切割去除缺陷部位;(2)在200
±
5℃条件下将高纯镁锭热挤压成初级高纯镁棒,然后利用三滚轧机在室温条件下通过二次冷轧制成次级高纯镁棒,最后将次级高纯镁棒在160
±
5℃热处理20
±
1min得高纯镁棒成品;(3)将高纯镁棒成品使用数控机床加工出高纯镁锚钉的结构,通过磷酸
‑
乙二醇体系溶液在40
±
2℃下化学抛光去除高纯镁锚钉表面毛刺和氧化皮,通过碱溶液和纯化水清洗表面残留的抛光液,干燥后使用铝箔袋真空包装,最后辐照灭菌。
16.一种高纯镁带线锚钉配套的植入装置,包括连杆和手柄,所述连杆的前端设有与安装孔相配的适配头,所述连杆的后端与手柄连接;所述连杆的轴线上设有贯穿连杆的穿线通道,所述手柄的轴线上设有贯穿手柄的穿线通道,连杆的穿线通道与手柄的穿线通道连通。植入装置整体类似螺丝刀,能与锚钉相适配,操作简单。
17.所述手柄的外表面上设有绕线部。
18.所述手柄的外表面上还设有防滑纹。
19.所述适配头呈正方形或内六角形;所述适配头的轴线上也设有贯穿适配头的穿线通道,适配头的穿线通道与连杆的穿线通道连通。
20.所述连杆呈圆柱形。
21.本发明的有益效果是:具有良好的生物相容性、力学性能和生物可降解性,在保证腱骨愈合的同时具有更高的力学强度,外科医生的操作更简单,能将肌腱、韧带与骨表面牢固结合,降解机制上相较于高分子材料对人体更为无害。
附图说明
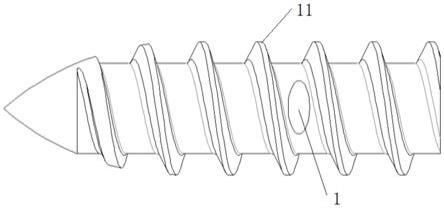
22.图1是本发明的高纯镁带线锚钉一种结构示意图;图2是本发明高纯镁带线锚钉后端的第一种横截面示意图;图3是本发明高纯镁带线锚钉后端的第二种横截面示意图;图4是本发明高纯镁带线锚钉后端的第三种横截面示意图;图5是本发明装配后的一种结构示意图;图6是本发明装配后的另一种结构示意图。
23.图7是高纯镁带线锚钉组和高分子带线锚钉组的植入物周围肩袖组织的显微变化视图。
24.图8是高纯镁带线锚钉组和高分子带线锚钉组的动物脏器的组织学显微变化视图。
25.图9是高纯镁带线锚钉组和高分子带线锚钉组的肩关节ct图。
26.图10是高纯镁带线锚钉组和高分子带线锚钉组术后血清镁离子浓度变化图。
27.图中:1、贯通孔,2、安装孔,3、左穿线孔,4、右穿线孔,5、连杆,6、手柄,7、适配头,8、绕线部,9、防滑纹,10、穿线通道,11、螺纹,12、缝线,13、锚钉本体。
具体实施方式
28.下面通过具体实施例,对本发明的技术方案作进一步的具体说明。
29.本发明中,若非特指,所采用的原料和设备等均可从市场购得或是本领域常用的。下述实施例中的方法,如无特别说明,均为本领域的常规方法。
30.实施例1:一种高纯镁带线锚钉(图1),包括锚钉本体13,所述锚钉本体上设有在宽度方向上贯穿锚钉本体的贯通孔1,所述锚钉本体后端的中心处设有安装孔2,所述安装孔的底部设有穿线孔,所述穿线孔包括左穿线孔3和右穿线孔4,所述安装孔通过左穿线孔和右穿线孔与贯通孔连通,所述安装孔为正方形孔;所述穿线孔的形状为长方形(图2)。所述锚钉本体的外表面设有螺纹11,所述贯通孔位于靠近锚钉本体后端处,且位于螺纹槽内。高纯镁的纯
度在99.98wt%以上。
31.一种与所述的高纯镁带线锚钉配套的植入装置(图5),包括连杆5和手柄6,所述连杆呈圆柱形。所述手柄的外表面上设有绕线部8,所述手柄的外表面上还设有防滑纹9;所述连杆的前端设有与安装孔相配的适配头7,所述适配头呈正方形;所述连杆的后端与手柄连接;所述连杆的轴线上设有贯穿连杆的穿线通道10,所述手柄的轴线上设有贯穿手柄的穿线通道,连杆的穿线通道与手柄的穿线通道连通。所述适配头的轴线上也设有贯穿适配头的穿线通道,适配头的穿线通道与连杆的穿线通道连通。
32.实施例2:一种高纯镁带线锚钉(图1),包括锚钉本体13,所述锚钉本体上设有在宽度方向上贯穿锚钉本体的贯通孔1,所述锚钉本体后端的中心处设有安装孔2,所述安装孔的底部设有穿线孔,所述穿线孔包括左穿线孔3和右穿线孔4,所述安装孔通过左穿线孔和右穿线孔与贯通孔连通,所述安装孔为内六角孔;所述穿线孔的形状为长方形(图3)。所述锚钉本体的外表面设有螺纹11,所述贯通孔位于靠近锚钉本体后端处,且位于螺纹槽内。高纯镁的纯度在99.98wt%以上。
33.一种与所述的高纯镁带线锚钉配套的植入装置(图5),包括连杆5和手柄6,所述连杆呈圆柱形。所述手柄的外表面上设有绕线部8,所述手柄的外表面上还设有防滑纹9;所述连杆的前端设有与安装孔相配的适配头7,所述适配头呈内六角形;所述连杆的后端与手柄连接;所述连杆的轴线上设有贯穿连杆的穿线通道10,所述手柄的轴线上设有贯穿手柄的穿线通道,连杆的穿线通道与手柄的穿线通道连通。所述适配头的轴线上也设有贯穿适配头的穿线通道,适配头的穿线通道与连杆的穿线通道连通。
34.实施例3:一种高纯镁带线锚钉(图1),包括锚钉本体13,所述锚钉本体上设有在宽度方向上贯穿锚钉本体的贯通孔1,所述锚钉本体后端的中心处设有安装孔2,所述安装孔的底部设有穿线孔,所述穿线孔包括左穿线孔3和右穿线孔4,所述安装孔通过左穿线孔和右穿线孔与贯通孔连通,所述安装孔为正方形孔;所述穿线孔的形状为圆形(图4)。所述锚钉本体的外表面设有螺纹11,所述贯通孔位于靠近锚钉本体后端处,且位于螺纹槽内。高纯镁的纯度在99.98wt%以上。
35.一种与所述的高纯镁带线锚钉配套的植入装置(图5),包括连杆5和手柄6,所述连杆呈圆柱形。所述手柄的外表面上设有绕线部8,所述手柄的外表面上还设有防滑纹9;所述连杆的前端设有与安装孔相配的适配头7,所述适配头呈正方形;所述连杆的后端与手柄连接;所述连杆的轴线上设有贯穿连杆的穿线通道10,所述手柄的轴线上设有贯穿手柄的穿线通道,连杆的穿线通道与手柄的穿线通道连通。所述适配头的轴线上也设有贯穿适配头的穿线通道,适配头的穿线通道与连杆的穿线通道连通。
36.本发明的装配及使用方法为:缝线12从手柄端头的穿线通道进入(图6),缝线穿过手柄、连杆和适配头,从锚钉本体后端的安装孔进入左穿线孔再到贯通孔,再穿出右穿线孔,再从安装孔穿出,依次经过适配头、连杆和手柄的穿线通道后重新穿出手柄端头,活动线头绕线暂时固定在手柄一侧面的绕线部上。
37.使用时,首先需要在骨头上钻孔形成骨孔,然后植入装置的适配头插入至锚钉本体的安装孔内,拧动手柄,从而将高纯镁带线锚钉钻入骨头内,转动的过程中缝线不受到影
响,高纯镁带线锚钉,然后松开手柄绕线部的缝线端头,拔出植入装置,缝线端头穿过肌腱或韧带,将肌腱或韧带于骨表面拉紧贴合,然后打结,剪除多余线头。
38.实施例4:一种高纯镁带线锚钉的制备方法包括如下步骤:(1)将铸态高纯镁锭通过超声波探伤确定内部缺陷,并通过机械切割去除缺陷部位;(2)在200
±
5℃条件下将高纯镁锭热挤压成初级高纯镁棒,然后利用三滚轧机在室温条件下通过二次冷轧制成次级高纯镁棒,最后将次级高纯镁棒在160
±
5℃热处理20
±
1min得高纯镁棒成品;(3)将高纯镁棒成品使用数控机床加工出高纯镁锚钉的结构,通过磷酸
‑
乙二醇体系溶液在40
±
2℃下化学抛光去除高纯镁锚钉表面毛刺和氧化皮,通过碱溶液和纯化水清洗表面残留的抛光液,干燥后使用铝箔袋真空包装,最后辐照灭菌。
39.具体实施方案:将铸态高纯镁锭(镁 99.98wt.% ;锶0.002 wt.% ;铁0.0015 wt.% ;铝0.0008 wt.% ;锰0.0008 wt.% ;镍0.0002 wt.% ;铜0.0003 wt.% )通过超声波探伤确定内部缺陷,并通过机械切割去除缺陷部位;在200℃条件下将高纯镁锭热挤压成直径8.2mm高纯镁棒,然后利用三滚轧机在室温条件下通过二次冷轧制成直径8.0mm的高纯镁棒,最后将高纯镁棒在160℃热处理20min,释放材料内部的残余应力。
40.高纯镁棒使用数控机床加工出高纯镁锚钉的结构,通过磷酸
‑
乙二醇体系溶液(磷酸与乙二醇体积比1:1,磷酸浓度≥85%,乙二醇浓度99.9%)在40℃下化学抛光去除高纯镁锚钉表面毛刺和氧化皮,通过碱溶液(浓度为1mol/l的碳酸钠溶液)和纯化水清洗表面残留的抛光液,干燥后使用铝箔袋真空包装,最后辐照灭菌制成实验所用的高纯镁锚钉。
41.制备完成后首先进行体外研究,包括形貌表征、降解实验、拔出强度及扭矩测试。
42.以成年母绵羊为实验动物,通过构建冈下肌肌腱损伤修补模型比较不同材料带线锚钉在动物体内的有效性及生物安全性。共选取年龄及体重相近的6只绵羊,其中年龄24
‑
30月,体重72
‑
78kg。将实验动物分为2组,每组3只,实验组采用高纯镁带线锚钉,对照组采用高分子带线锚钉。
43.本研究以绵羊右侧冈下肌肌腱构建动物模型,将该肌腱从远端完全离断,并向近端锐性分离腱骨结合部分,随后在足印区用丝锥开孔植入带线锚钉,用mason
‑
allen法修补肌腱。造模后定期对实验动物进行影像学检查、血清学检查,组织标本取样后组织学研究。
44.结果分析 :体外研究:形貌表征,将本发明镁钉样品在pbs液中浸泡3周,降解3周后的样品表面结构平整,未见明显的裂隙,表面降解均匀。降解实验:共用3个镁钉样本在pbs液中浸泡进行降解实验,降解3周后,平均重量变化为0.019
±
0.0088 g,平均失重率为13.35
±
6.15 %。
45.拔出强度测试:用丝攻在人工骨内预置孔道,将镁钉样本拧入孔道内,人工骨固定于下方夹具,镁钉尾端缝线固定于上方夹具,固定完毕后沿垂直方向施加应力直至镁钉从人工骨拔出或缝线断裂。
46.共用3个镁钉样本进行测试,结局都为镁钉未拔出,缝线断裂,平均断裂强度为
297.667
±
24.007n。
47.扭矩测试:共用3个镁钉样本进行测试,平均扭矩为0.253
±
0.012nm。
48.动物体内研究:分别对高纯镁带线锚钉组和高分子带线锚钉组的植入物周围肩袖组织进行组织学研究,两组肩袖组织和骨组织之间无明显间隙,结合紧密,表明在动物模型中两组腱骨愈合程度相当,组织修复良好(图7)。
49.分别对高纯镁带线锚钉组和高分子带线锚钉组的动物脏器进行组织学研究,两组动物的心脏、肝脏及肾脏组织均呈现正常的组织结构,无病理性改变,表明两组植入物均对动物的脏器无毒副作用,生物安全性良好(图8)。
50.分别对高纯镁带线锚钉组和高分子带线锚钉组动物的肩关节进行mri检查。术后两组植入物情况同ct结果一致。两组肌腱情况亦表现相近,在术后1天,肌腱远端均有少许游离,系缝线固定远端未完全贴合骨表面所致,术后4周开始,肌腱形状正常,远端已与骨表面愈合良好,表明两组肌腱在4周或更短的时间内进行了良好的腱骨愈合(图9)。
51.术后定期检测实验动物血清镁离子浓度,两组动物(1
‑
3实验组,4
‑
6对照组)的指标变化趋势相近,表明与高分子带线锚钉相比,高纯镁带线锚钉降解过程中对于动物血清中镁离子的浓度影响无差异(图10)。
52.结论制备的高纯镁带线锚钉在体外能实现均匀降解。
53.制备的高纯镁带线锚钉具有良好的力学性能。
54.制备的高纯镁带线锚钉在实验动物体内能缓慢降解,在腱骨愈合完成前发挥可靠的固定作用,且对动物脏器无毒副作用。
55.制备的高纯镁带线锚钉在实验动物体内降解过程中会在植入物周围产生少许空洞,12周的观察时间内未发现此现象对植入物固定情况及腱骨愈合产生负面影响。
56.以上所述的实施例只是本发明的一种较佳的方案,并非对本发明作任何形式上的限制,在不超出权利要求所记载的技术方案的前提下还有其它的变体及改型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1