一种妇科用温敏凝胶及其制备方法与流程
1.本发明涉及妇科用药技术领域,具体涉及一种妇科用温敏凝胶及其制备方法。
背景技术:
2.妇科炎症已成为女性常见的多发病,其临床表现多种多样,病因复杂且常伴有多种严重并发病,对女性的生活和工作有很大影响。目前的一些药物制剂在疗效方面不能完全满足临床和市场的需要,有些化学药品虽然有消炎、抗菌作用,但是没有考虑到对皮肤刺激性问题。当前妇科炎症或术后修复中使用的主要产品为壳聚糖类,主要剂型包含栓剂、凝胶、粉末、液体等,产品具有抑菌和修复作用,但这类产品的抑菌性较弱,治疗作用不明显,甚至还会破坏女性生殖系统的酸碱平衡,对女性生殖道造成污染。而常用的一些冲洗液的原料包含中药和消毒剂,此类产品在使用时容易污染患者衣物,且沾染后清洗不便。
技术实现要素:
3.本发明的目的在于:为解决上述问题,提供一种杀菌效果好且无刺激、作用时间长的妇科用温敏凝胶及其制备方法。
4.本发明采用的技术方案如下:
5.一种妇科用温敏凝胶,包括以下重量份的原料:
6.次氯酸盐:0.1~1份;
7.ph调节剂:0.01~1份;
8.卡波姆:0.01~0.5份;
9.泊洛沙姆:0.01~1份;
10.水:100份。
11.进一步地,所述凝胶还包括甘草酸,其重量份为0.01~0.3;甘草酸具有抗发炎的作用,可防止皮肤的敏感反应。
12.进一步地,所述凝胶还包括葡萄寡糖,其重量份为0.01~1;葡萄寡糖可被皮肤的有益菌所分解吸收营养,有助于皮肤的生物平衡。
13.进一步地,所述次氯酸盐包括次氯酸钠、次氯酸钙、次氯酸钾中的至少一种。
14.进一步地,所述ph调节剂包括盐酸、磷酸、硫酸中的至少一种。
15.上述一种妇科用温敏凝胶的制备方法,包括以下步骤:
16.步骤1:将次氯酸盐加入适量水中溶解,再加入ph调节剂,将溶液ph值调节至3~6之间,得到溶液一;
17.步骤2:在剩余水中加入卡波姆,搅拌至其溶解,再加入泊洛沙姆搅拌均匀,放置,直至溶液澄清,得到溶液二;
18.步骤3:将溶液一缓慢加入溶液二中,缓慢搅拌至混合均匀,即得。
19.进一步地,所述步骤2的制备环境为2℃~6℃。
20.进一步地,所述步骤2中,放置时间为6~24小时。
21.进一步地,所述步骤2中,在加入泊洛沙姆时,还加入有甘草酸。
22.进一步地,所述步骤3中,将溶液一和溶液二混合时,还加入有葡萄寡糖。
23.综上所述,由于采用了上述技术方案,本发明的有益效果是:
24.本发明的温敏凝胶的主要有效成分为次氯酸、卡波姆和泊洛沙姆,次氯酸具有高效的杀菌作用,无毒、无刺激、无残留且安全,可快速杀灭创面细菌,对细菌、霉菌、芽孢均有杀灭作用,在杀菌的同时还能促进伤口愈合;卡波姆具有消炎杀菌、降粘稠度、中和以及保护作用,可减少对皮肤的刺激和伤害;泊洛沙姆具有促进吸收、固体分散以及稳定的作用;使用本发明的温敏凝胶时,对患者病患部位无刺激,药物与患者病患部位接触时间和作用时间长达24小时,且不会对患者病患部位以及衣物造成污染,舒适度高。
具体实施方式
25.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。
26.实施例一
27.本实施例提供了一种妇科用温敏凝胶,包括以下重量份的原料:次氯酸盐0.1份;ph调节剂0.01份;卡波姆0.01份;泊洛沙姆0.01份;水100份。其中,次氯酸盐采用次氯酸钠,ph调节剂采用盐酸。
28.按照上述各原料的重量份数,本实施例的妇科用温敏凝胶的制备方法包括以下步骤:
29.步骤1:在常温环境下,将0.1%次氯酸钠加入60份水中进行溶解,再加入盐酸,将溶液ph值调节至3,得到溶液一。
30.步骤2:在4℃时,在剩余水中加入0.02%~0.2%的卡波姆,不断搅拌至其溶解,再加入0.05%~2%的泊洛沙姆407进行搅拌,搅拌均匀后,在4℃放置6小时至溶液澄清,得到溶液二。
31.步骤3:在常温环境下,将溶液一缓慢加入溶液二中,缓慢搅拌至混合均匀,即得。
32.实施例二
33.本实施例提供了一种妇科用温敏凝胶,包括以下重量份的原料:次氯酸盐0.5份;ph调节剂0.4份;卡波姆0.3份;泊洛沙姆0.45份;甘草酸0.01份;水100份。其中,次氯酸盐采用次氯酸钙,ph调节剂采用磷酸。
34.按照上述各原料的重量份数,本实施例的妇科用温敏凝胶的制备方法包括以下步骤:
35.步骤1:在常温环境下,将0.1%次氯酸钙加入65份水中进行溶解,再加入磷酸,将溶液ph值调节至4.5,得到溶液一。
36.步骤2:在2℃时,在剩余水中加入0.02%~0.2%的卡波姆,不断搅拌至其溶解,再加入0.05%~2%的泊洛沙姆407和甘草酸进行搅拌,搅拌均匀后,在2℃放置8小时至溶液澄清,得到溶液二。
37.步骤3:在常温环境下,将溶液一缓慢加入溶液二中,缓慢搅拌至混合均匀,即得。
38.实施例三
39.本实施例提供了一种妇科用温敏凝胶,包括以下重量份的原料:次氯酸盐0.75份;
ph调节剂0.6份;卡波姆0.4份;泊洛沙姆0.6份;葡萄寡糖0.01份;水100份。其中,次氯酸盐采用次氯酸钠和次氯酸钾,次氯酸钠、次氯酸钾的加入量分别为0.45份、0.3份,ph调节剂采用盐酸和磷酸,盐酸、磷酸的加入量分别为0.3份、0.3份。
40.按照上述各原料的重量份数,本实施例的妇科用温敏凝胶的制备方法包括以下步骤:
41.步骤1:在常温环境下,将0.1%次氯酸钠、次氯酸钾加入65份水中进行溶解,再加入盐酸和磷酸,将溶液ph值调节至5,得到溶液一。
42.步骤2:在2℃时,在剩余水中加入0.02%~0.2%的卡波姆,不断搅拌至其溶解,再加入0.05%~2%的泊洛沙姆407进行搅拌,搅拌均匀后,在2℃放置12小时至溶液澄清,得到溶液二。
43.步骤3:在常温环境下,将溶液一缓慢加入溶液二中,并加入葡萄寡糖,缓慢搅拌至混合均匀,即得。
44.实施例四
45.本实施例提供了一种妇科用温敏凝胶,包括以下重量份的原料:次氯酸盐1份;ph调节剂1份;卡波姆0.5份;泊洛沙姆1份;甘草酸0.3份;葡萄寡糖1份;水100份。其中,次氯酸盐采用次氯酸钠、次氯酸钙和次氯酸钾,次氯酸钠、次氯酸钙、次氯酸钾的加入量分别为0.5份、0.3份、0.2份,ph调节剂采用盐酸和硫酸,盐酸、硫酸的加入量分别为0.7份、0.3份。
46.按照上述各原料的重量份数,本实施例的妇科用温敏凝胶的制备方法包括以下步骤:
47.步骤1:在常温环境下,将0.1%次氯酸钠、次氯酸钙和次氯酸钾加入70份水中进行溶解,再加入盐酸和硫酸,将溶液ph值调节至6,得到溶液一。
48.步骤2:在6℃时,在剩余水中加入0.02%~0.2%的卡波姆,不断搅拌至其溶解,再加入0.05%~2%的泊洛沙姆407和甘草酸进行搅拌,搅拌均匀后,在6℃放置24小时至溶液澄清,得到溶液二。
49.步骤3:在常温环境下,将溶液一缓慢加入溶液二中,并加入葡萄寡糖,缓慢搅拌至混合均匀,即得。
50.以下为将实施例四制备的凝胶作为样品进行有关杀菌试验和毒性试验:
51.一、阴道黏膜刺激试验
52.试验准备:
53.实验动物:普通级新西兰白色家兔6只,雌性,体重2.0kg~2.5kg,购自广州市花都区花东信华实验动物养殖场。
54.试验方法:
55.(1)检验依据:《消毒技术规范》(2002年版)和《一次性使用卫生用品卫生标准gb15979
‑
2002》。
56.(2)检验方法:
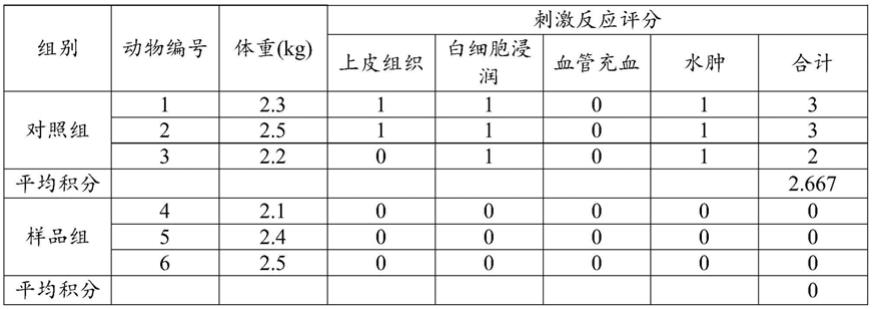
57.将6只动物分为样品组和对照组各3只,使动物仰面固定,暴露出会阴和阴道口。将连有钝头软管的注射器吸好受试液后轻柔地插入家兔阴道4~5cm,并缓慢地注入2ml受试液,完成染毒。对照组动物用生理盐水做同样处理。24小时后采用气栓法处死动物,剖腹取出完整的阴道,纵向切开,肉眼观察是否有充血、水肿等表现,供病理取材时参考,然后将阴
道放入10%福尔马林溶液中固定24h以上,选取阴道的两端和中央三个部位的组织制片,he染色后再显微镜下进行组织病理学检查,根据阴道黏膜反应评分标准进行评分。
58.试验结果如下表所示,经病理学检测,根据《消毒技术规范》(2002年版)中“阴道黏膜刺激强度分级”评定,该试验阴道黏膜刺激指数为0,属无刺激性。
[0059][0060]
二、对金黄色葡萄球菌、大肠杆菌的灭杀试验
[0061]
试验准备:
[0062]
(1)试验菌株:金黄色葡萄球菌atcc 6538、大肠杆菌8099。以上菌种代数均为第4代,并用0.03mol/lpbs配制菌液。
[0063]
(2)中和剂:0.5%卵磷脂,1%吐温80的pbs溶液。
[0064]
(3)刻度吸管(0.1ml、1.0ml、5.0ml、10.0ml)等。
[0065]
试验方法:
[0066]
(1)检测依据:《一次性使用卫生用品卫生标准gb15979
‑
2002》附录c中产品杀菌性能、抑菌性能与稳定性测试方法。
[0067]
(2)中和剂鉴定试验:试验菌为金黄色葡萄球菌。试验分组为:
①
、消毒剂+菌悬液;
②
、(消毒剂+菌悬液)+中和剂;
③
、中和剂+菌悬液;
④
、(消毒剂+中和剂)+菌悬液;
⑤
、pbs溶液+菌悬液;
⑥
、同批次pbs溶液;
⑦
、同批次中和剂;
⑧
、同批次培养基。稀释剂+中和剂+培养基。样品作用5min。试验重复3次。试验环境温度20℃。
[0068]
(3)灭杀性能测试:样品作用时间5min、10min、15min、20min,试验重复3次。试验环境温度20℃。
[0069]
试验结果如下:
[0070]
1、中和剂鉴定试验
[0071]
3次重复试验证明,第1组平均生长菌落数为无菌生长,第2组平均生长菌落数为1.04
×
102cfu/ml,第3、4、5组平均生长菌落数相近,第6、7、8组无菌生长,结果如下表:
[0072][0073]
注:阴性对照无菌生长。
[0074]
2、对金黄色葡萄球菌、大肠杆菌的灭杀效果
[0075]
经3次重复试验证明,样品作用5min,对金黄色葡萄球菌、大肠杆菌的杀灭率可达90%,结果如下表:
[0076][0077]
注:阴性对照无菌生长。
[0078]
三、对白色念珠菌的灭杀试验
[0079]
检验样品对白色念珠菌的杀灭效果的试验准备和试验方法中,除试验菌株与检测依据与上述检验样品对金黄色葡萄球菌、大肠杆菌的灭杀效果有所不同以外,其余均相同,相同之处不再赘述。检验样品对白色念珠菌的杀灭效果的试验菌株为白色念珠菌atcc10231。
[0080]
1、中和剂鉴定试验
[0081]
3次重复试验证明,第1组平均生长菌落数为无菌生长,第2组平均生长菌落数为1.05
×
102cfu/ml,第3、4、5组平均生长菌落数相近,第6、7、8组无菌生长,结果如下表:
[0082][0083]
注:阴性对照无菌生长。
[0084]
2、对白色念珠菌的灭杀效果
[0085]
经3次重复试验证明,样品作用5min,对白色念珠菌的杀菌率可达90%,结果如下表:
[0086][0087]
注:阴性对照无菌生长。
[0088]
四、稳定性试验
[0089]
检测条件:将样品置37℃恒温箱内3个月,保持相对湿度78%,进行杀菌性能试验。试验重复次数:2次,结果如下表:
[0090][0091]
检测结论如下:
[0092]
1、阴道黏膜刺激试验:样品对家兔阴道黏膜刺激试验结果为无刺激性,符合《消毒技术规范》(2002年版)的要求。
[0093]
2、以含0.5%卵磷脂,1%吐温80的pbs溶液为中和剂,样品原液作用5min后,对金黄色葡萄球菌、大肠杆菌和铜绿假单胞菌的杀菌率可达90%,符合《一次性使用卫生用品卫生标准gb15979
‑
2002》的要求。
[0094]
3、以含0.5%卵磷脂,1%吐温80的pbs溶液为中和剂,样品原液作用5min后,对白色念珠菌的杀菌率可达90%,符合《一次性使用卫生用品卫生标准gb15979
‑
2002》的要求。
[0095]
4、样品经37℃保存90天后,杀菌率可达90%以上,符合《一次性使用卫生用品卫生标准gb15979
‑
2002》的要求。
[0096]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1