一种具有组织光愈合功能的高分子水凝胶及其制备和应用
本发明涉及高分子水凝胶技术领域,具体涉及一种组织光愈合高分子水凝胶及其制备方法和应用。
背景技术:
日常生活中人们总会受到各种程度的皮肤组织创伤,进而带来一系列健康隐患,如伤口愈合慢、创面感染等问题,严重时还会导致伤口化脓扩大,降低病人的机体素质,最终导致组织坏死,所以伤口护理及其产品的选择就显得尤为重要。日常生活中,根据创伤大小和严重程度的不同,人们所选择的伤口护理产品也不尽相同,如碘伏、消炎药膏、消炎喷雾、创口贴、医用创伤敷料等……其中一次性医用敷料是用量巨大的伤口护理用品,可用于覆盖不同程度的创口,具有阻隔外界环境、防止创伤感染、减少伤口疼痛以及伤口的止血消炎促修复等功能。
1962年,英国皇家医学会winter博士提出“湿性伤口愈合理论”,即伤口在湿润的环境下比在干燥的环境下愈合得更快,使得人们对伤口愈合过程的认识有了突破性的进展。从只能覆盖伤口而起不到促进愈合作用的传统敷料,到可促进愈合功能多样的新型创伤敷料,如今的创伤敷料相较于以前已经发生了革命性的变化。
作为新型创伤敷料的一种,高分子水凝胶类敷料具有极高的含水量和组织相容性,有利于创造湿润环境促进伤口愈合。除此之外,水凝胶类敷料容易更换、吸收渗液能力强、在伤口愈合的过程中不会粘连伤口、还可以负载各种药物进一步促进伤口愈合,是一种理想型的创伤敷料,在生物医用领域得到了广泛的研究和应用。
岳婉晴等将高分子纤维束与多肽水凝胶相结合,利用微流控纺织技术制备海藻酸钠纤维束,并将多肽快速自组装包裹在纤维束外,提供一种可包含两种促进伤口愈合药物的纤维束/多肽复合水凝胶体系,实现对抗炎药物的快速释放和促进伤口修复药物的缓慢释放,同时为创口提供合适的湿润度以及透气环境,能够促进慢性创口愈合。kaorumurakami等开发了一种可为伤口快速愈合持续创造湿润环境的海藻酸、甲壳素/壳聚糖和褐藻多糖复合功能创面敷料,具有易于涂抹和去除、黏附性好等特点。gong等设计了一种以载药胶束包载姜黄素的温敏性水凝胶可降解释药系统,应用于皮肤创面修复,姜黄素具有较高的疏水性,具有较高的载药量和包封效率,以此为基础设计的温敏性水凝胶可降解释药系统具有良好的组织粘附性,能在较长时间内释放姜黄素。
虽然水凝胶型敷料具有较好的性能,但目前的水凝胶创伤敷料降解速度较慢、不易调节降解速率或很难完全降解成小分子,导致其药物释放缓慢和不可控、治愈周期长,并且具有诱发耐药性的风险。此外还存在着药物包载能力低、难以负载疏水性药物、缺乏功能性等问题。如果创伤敷料的治愈效率不能进一步提升,将会增加伤口二次感染、炎症复发及愈后留疤的风险,使患者饱受痛苦。所以新型水凝胶敷料的设计仍是一个巨大的挑战,改善水凝胶敷料的降解和释药性能对防止伤口感染、促进创面愈合、提升患者使用舒适度等具有重要意义。
技术实现要素:
针对上述缺陷,本发明提供一种组织光愈合高分子水凝胶,所得水凝胶能够在光照刺激下原位将高分子还原降解为生物活性小分子,实现光照凝胶瞬间消融,因此在作为水凝胶敷料使用时,在换料过程中免揭除,避免二次创伤,同时实现光控超快可控释放药物,协同加速伤口愈合。
本发明的技术方案:
本发明要解决的第一个技术问题是提供一种高分子水凝胶,所述高分子水凝胶的原料包括光还原自降解高分子材料和上转换纳米粒子,其中,所述光还原自降解高分子材料的分子结构的主链含有还原敏感基团,支链含有光敏感基团,并且其分子结构中还含有还原剂残基;所述光还原自降解高分子材料在外部光刺激的作用下由于光敏感基团的脱除从而激活了还原剂残基,还原剂残基进一步与主链上的还原敏感基团发生反应使得所述高分子材料的主链断裂,进而实现了所述高分子材料的还原降解。
进一步,所述光还原自降解高分子材料与上转换纳米粒子的质量比为5:1~1:2。
进一步,所述上转换纳米粒子为:(naerf4@nagdf4);((biaerbybc)ta7o19);(nayf4:yb,er);(nayf4:tm,yb@nayf4);(nayf4:yb,er@nayf4:yb);(nagdf4:yb,tm@nagdf4:tb@nayf4);或(nayf4:yb,tm@nayf4:yb,er@nayf4:yb,tm)。
进一步,所述高分子水凝胶的原料还包括:亲水组分、生物活性因子、水溶性药物或疏水性药物中的至少一种。
进一步,所述亲水组分为聚乙二醇。
进一步,所述生物活性因子为壳聚糖、透明质酸、海藻酸盐或明胶。
进一步,所述水溶性药物为:阿莫西林、盐酸四环素、盐酸米诺环素、左氧氟沙星、夫西地酸钠、积雪草苷、多粘菌素b、两性霉素b、环丙沙星、莫匹罗星、酚磺乙胺、氨甲环酸、亚胺培南、西司他汀或胰岛素。
进一步,所述疏水性药物为:甲硝唑、苯妥英、磺胺嘧啶银、氢化可的松、姜黄素或肉桂醛。
进一步,所述光还原自降解高分子材料中光敏感基团选自下述结构式中一种:
式中,r1为氢原子或任意取代基,r2和r3为氢原子或烷氧基,r2和r3可以相同,也可以不同;虚线表示和还原剂残基的连接位置。
进一步,所述还原剂残基指:还原剂在参与光还原自降解高分子材料分子结构的形成过程中,除参与反应的基团外,还原剂的剩余结构即为还原剂残基。
进一步,所述还原剂残基中的还原剂为二硫苏糖醇(dtt)、二硫赤藓醇(dte)或谷胱甘肽(gsh)。
进一步,所述光还原自降解高分子材料中还原敏感基团为二硫基或二硒基。
进一步,所述光还原自降解高分子材料采用下述制备方法制得:先将还原剂与含光敏感基团的物质反应得中间体,所得中间体及其衍生物(中间体或中间体衍生物)再与含还原敏感基团的物质反应即得光还原自降解高分子材料。
进一步,上述方法中,所述还原剂为二硫苏糖醇(dtt)、二硫赤藓醇(dte)或谷胱甘肽(gsh)。
进一步,上述方法中,所述含光敏感基团的物质选自下述化合物中的一种:
式中,r1为氢原子或任意取代基,r2和r3为氢原子或烷氧基,其中r2和r3可以相同,也可以不同;x为卤原子。
进一步,上述方法中,所述含还原敏感基团的物质为:含二硫基或二硒基的二元醇、二元胺、二元酸、二异氰酸酯或二酰卤化合物。
更进一步,所述含有还原性敏感基团的物质为:二硫二乙醇、二硫二丙醇、二硫二乙酸、二硫二丙酸、胱胺、二硫二丙胺、二硫代二苯胺、胱胺二异氰酸酯、二硫二丙基二异氰酸酯、胱氨酸二甲酯二异氰酸酯、胱氨酸二乙酯二异氰酸酯、高胱氨酸二甲酯二异氰酸酯、高胱氨酸二乙酯二异氰酸酯、胱氨酸二甲酯、胱氨酸二乙酯、高胱氨酸二甲酯、高胱氨酸二乙酯、二叔丁氧羰基胱氨酸、二硫二苯甲酰氯、二硫二乙酰氯、二硒二乙醇、二硒二丙醇、二硒二乙酸、二硒二丙酸、硒代胱胺、二硒二丙胺、二硒代二苯胺、硒代胱胺二异氰酸酯、二硒二丙基二异氰酸酯、硒代胱氨酸二甲酯二异氰酸酯、硒代胱氨酸二乙酯二异氰酸酯、硒代高胱氨酸二甲酯二异氰酸酯、硒代高胱氨酸二乙酯二异氰酸酯、硒代胱氨酸二甲酯、硒代胱氨酸二乙酯、硒代高胱氨酸二甲酯、硒代高胱氨酸二乙酯、二叔丁氧羰基硒代胱氨酸、二硫二苯甲酰氯或二硒二乙酰氯中的一种。
进一步,上述方法中,还原剂与含光敏感基团的物质通过取代反应得中间体。
进一步,上述方法中,中间体及其衍生物再与含还原敏感基团的物质通过加聚、缩聚或偶联反应得光还原自降解高分子材料。
进一步,所述高分子水凝胶具有组织光愈合功能。所述具有组织光愈合功能是指高分子水凝胶具有下述功能:1、光照瞬间消融(作为敷料换料时免揭除,从而避免二次创伤);2、若引入药物,光照超快可控释放药物(从而加速愈合,减少耐药性);3、光降解产物具有抗氧化和消炎功效(从而促进伤口愈合);4、水凝胶中聚合物快速光降解为小分子(易于代谢吸收);5、光愈合与传统近红外理疗可结合使用(协同加速组织愈合)。
本发明要解决的第二个技术问题是提供上述组织光愈合高分子水凝胶的制备方法,所述制备方法为:在合成所述光还原自降解高分子材料的过程中加入上转换纳米粒子,混匀后于30~50℃静置制得高分子水凝胶。
进一步,所述高分子水凝胶的制备方法为:先将还原剂与含光敏感基团的物质反应得中间体,所得中间体及其衍生物(中间体或中间体衍生物)再与含还原敏感基团的物质反应,反应结束后加入上转换纳米粒子搅拌分散均匀得到产物;然后将所得产物的水溶液加热到50~70℃,之后迅速放入冰浴保持5~10min,然后于30~50℃静置制得组织光愈合高分子水凝胶。
进一步,上述高分子水凝胶的制备方法中,还引入水溶性药物、疏水性药物、亲水活性组分或生物活性因子中的至少一种。
本发明要解决的第三个技术问题是指出上述高分子水凝胶用于皮肤创伤或手术创面的敷料。
本发明的有益效果:
本发明与已有技术相比,具有以下优点:
(1)本发明提供一种组织光愈合高分子水凝胶,其在光照刺激下原位将高分子还原降解为小分子,实现光照凝胶瞬间消融;因此可以作为水凝胶敷料,换料过程免揭除,避免二次创伤。
(2)所得高分子水凝胶在光照下凝胶内部原位产生刺激源,克服浓度和位阻障碍,实现药物超快、按需和可控释放,减少耐药性。
(3)所得高分子水凝胶的降解产物具备抗菌、消炎、抗氧化和促组织修复愈合等多种功能。
(4)本发明的水凝胶可以和近红外理疗仪搭配使用,协同加速伤口愈合。
(5)本发明所得高分子水凝胶具有较高的生物相容性,易于被生物体清除和代谢;
(6)本发明所得高分子水凝胶可以广泛应用于皮肤创伤、手术创面、肿瘤切除术后化疗和免疫治疗等领域。
附图说明
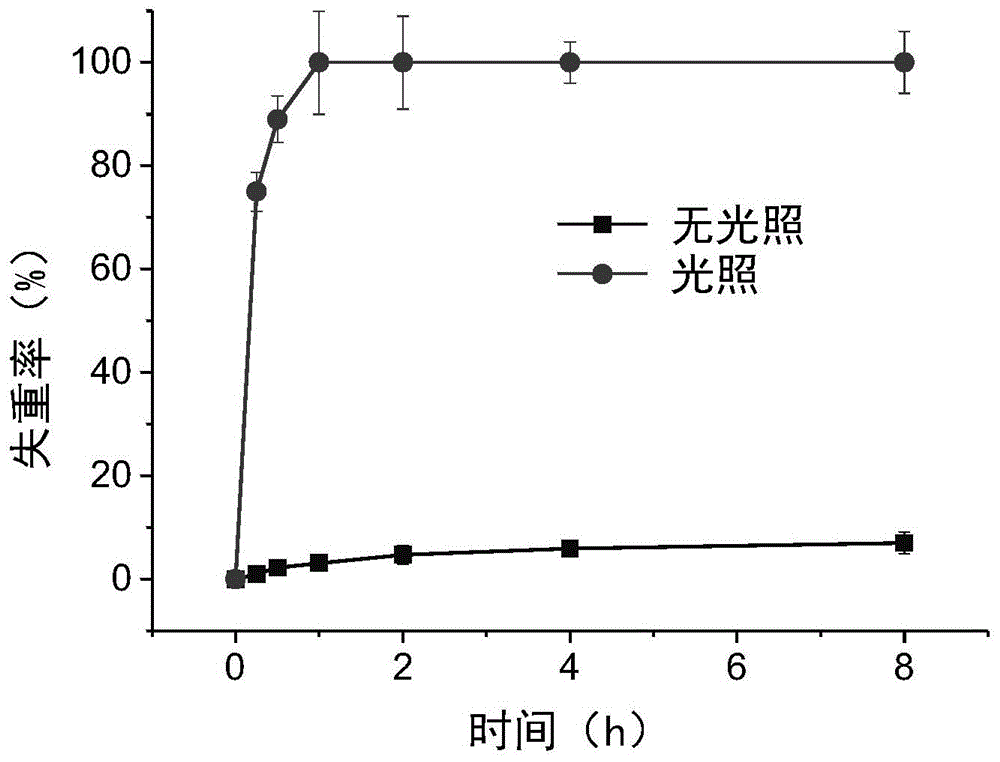
图1为本发明实施例所得组织光愈合高分子水凝胶敷料1在光照和无光照条件下的失重率曲线,*表示凝胶已经没有残留,完全分散于溶液中。
图2为实施例5所得组织光愈合高分子水凝胶敷料5在光照和非光照条件下的释药曲线。
图3a为3t3成纤维细胞与不同浓度实施例1所得组织光愈合高分子水凝胶敷料1的浸提液培养24h的照片;图3b为3t3成纤维细胞与不同浓度实施例2所得组织光愈合高分子水凝胶敷料2的浸提液培养24h的照片;图3c为阴性对照组、实施例1和实施例2的细胞成活率。
图4a为大鼠皮下植入实施例1所得组织光愈合高分子水凝胶敷料1的组织切片;图4b为大鼠皮下植入实施例2所得组织光愈合高分子水凝胶敷料2的组织切片。
图5为大鼠背部创伤未治疗组、以及采用实施例5所得组织光愈合高分子水凝胶敷料5非光照处理和光照处理后不同时间点的创面愈合率。
具体实施方式
下面给出实施例以对本发明进行具体描述,但值得指出的是以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,该领域的普通专业人员根据上述发明的内容对本发明所作出的一些非本质的改进和调整,仍属于本发明的保护范围。
实施例1
取dtt-onb1(2.5mmol)加入反应瓶,注入无水dmf(20ml),然后滴加胱氨酸二甲酯二异氰酸酯(5mmol)的dmf溶液(5ml)及1滴辛酸亚锡,升温至60℃反应2h,加入peg(2.5mmol),反应2h后,加入7.7g上转换纳米粒子nayf4:tm,yb@nayf4,继续搅拌分散1h,得到产物1。将产物1的水溶液加热到60℃,迅速放入冰浴保持5min,然后静置于37℃孵育4h得到光愈合高分子水凝胶敷料1。
实施例中dtt-onb1采用下述方法制得:取二硫苏糖醇(3.08g)溶于naoh的乙醇溶液(40ml),冰浴冷却;滴加2-硝基苄溴(10.3g)的乙醇溶液(40ml),自然恢复至室温反应6小时,将生成的沉淀抽滤,冻干,避光保存,得到中间体dtt-onb1。
实施例2
取dtt-onb1(5mmol)加入反应瓶,注入无水dmf(20ml),然后滴加胱氨酸二甲酯二异氰酸酯(12mmol)的dmf溶液(5ml)及1滴辛酸亚锡,升温至60℃反应2h,加入peg(5mmol),反应2h,降至室温,加入15.3g上转换纳米粒子nayf4:tm,yb@nayf4和1ml壳聚糖的水溶液(5%),室温反应2h,得到产物2。将产物2的水溶液加热到60℃,迅速放入冰浴保持5min,然后静置于37℃孵育3h得到光愈合高分子水凝胶敷料2。
实施例3
取dtt-onb1(5mmol)加入反应瓶,注入无水dmf(20ml),然后滴加胱氨酸二甲酯二异氰酸酯(12mmol)的dmf溶液(5ml)及1滴辛酸亚锡,升温至60℃反应2h,加入peg(5mmol),反应2h,加入3.1g上转换纳米粒子naerf4@nagdf4和1ml胶原的水溶液(8%),室温反应2h,得到产物3。将产物3的水溶液加热到60℃,迅速放入冰浴保持5min,加入夫西地酸钠的水溶液混合均匀,然后静置于37℃孵育2h得到光愈合高分子水凝胶敷料3。
实施例4
取dtt-onb1(2.5mmol)加入反应瓶,注入无水dmf(20ml),然后滴加胱氨酸二甲酯二异氰酸酯(6mmol)的dmf溶液(5ml)及1滴辛酸亚锡,升温至60℃反应2h,加入peg(2.5mmol),反应2h,加入15.3g上转换纳米粒子(biaerbybc)ta7o19和1ml壳聚糖的水溶液(5%),室温反应2h,加入两性霉素b的dmf溶液搅拌1h后对水透析,得到产物5。将产物5的水溶液加热到60℃,迅速放入冰浴保持5min,然后静置于37℃孵育3h得到光愈合高分子水凝胶敷料4。
实施例5
取dtt-onb1(5mmol)加入反应瓶,注入无水dmf(20ml),然后滴加胱氨酸二甲酯二异氰酸酯(12mmol)的dmf溶液(5ml)及1滴辛酸亚锡,升温至60℃反应2h,加入peg(5mmol),反应2h,加入7.7g上转换纳米粒子nayf4:tm,yb@nayf4和1ml壳聚糖的水溶液(5%),室温反应2h,加入姜黄素的dmf溶液搅拌1h后对水透析,得到产物5。将产物5的水溶液加热到60℃,迅速放入冰浴保持5min,加入莫匹罗星的水溶液混合均匀,然后静置于37℃孵育3h得到光愈合高分子水凝胶敷料5。
对比例1
取dtt-onb1(5mmol)加入反应瓶,注入无水dmf(20ml),然后滴加胱氨酸二甲酯二异氰酸酯(12mmol)的dmf溶液(5ml)及1滴辛酸亚锡,升温至60℃反应2h,加入peg(5mmol),反应2h得到对比产物1。将对比产物1的水溶液加热到60℃,迅速放入冰浴保持5min,加入积雪草苷的水溶液混合均匀,然后静置于37℃孵育4h得到高分子水乳液1;由此可知,本发明如果不引入上转换粒子,并不能得到水凝胶,也就无法得到水凝胶敷料。
应用例1
将实施例1制取的光愈合高分子水凝胶敷料1放置于37℃的pbs缓冲液中,用近红外光照射10min,然后于不同时间点取出样品用蒸馏水润洗数次后进行称重,计算水凝胶敷料的失重率,没有接受近红外光照射的水凝胶敷料作为对照;结果如图1所示,由图1可知,没有光照的水凝胶敷料在缓冲液中较为稳定,失重率很低,而近红外光照的水凝胶失重率急剧增加,表明光照触发了光愈合高分子水凝胶敷料的降解。
应用例2
称取1g实施例5制取的光愈合高分子水凝胶敷料5置于透析袋中,以37℃的pbs缓冲液为介质,于156r/min的恒温振荡器中进行释放。对于光照组,打开透析袋使用近红外光照射样品溶液30min。在释放过程中,于不同时间点取出释放介质2ml,同时补充2ml新鲜pbs。每组平行取样三次,使用高效液相色谱和紫外分光光度计测定释放介质中药物的含量,利用药物标准曲线计算累积释放率,结果如图2所示;由图2可知,未光照组药物释放均非常缓慢,6h累积释放率不超过20%;光照后样品释放速率急剧增加,1h之内亲水药物莫匹罗星和疏水药物姜黄素的释放率分别超过80%和70%,说明本发明所得水凝胶中聚合物的光还原降解从内部破坏凝胶的结构,从而实现药物的超快和可控释放。
应用例3
将实施例1和实施例2制备的光愈合高分子水凝胶敷料1和2以100mg/ml的浓度放置于37℃的细胞培养基中浸提24h,采用空白的细胞培养基作为阴性对照。浸提液经过0.22μm滤器过滤除菌,然后在无菌条件下用培养基稀释2,5,10,20,50和100倍。将不同浓度的浸提液与3t3小鼠成纤维细胞共培养24h,用倒置相差显微镜(olympusltd,japan)观测细胞生长形态后,吸去上层清液,每孔加入20μlmtt溶液(5mg/ml,pbs),继续培养4h,轻轻吸去上清液,每孔加入110μl二甲基亚砜(dmso),震荡摇匀10min,使用酶标仪测定各孔在492nm的吸光度(od值),计算细胞成活率。图3为3t3成纤维细胞与不同浓度光愈合高分子水凝胶敷料1(a)和2(b)的浸提液培养24h的照片和细胞成活率(c);由图3可知,3t3小鼠成纤维细胞与不同浓度浸提液培养后细胞形态良好,其细胞成活率均在90%以上,表明光愈合高分子水凝胶敷料具有良好的细胞相容性。
应用例4
使用水合氯醛将sd大鼠进行全身麻醉,俯卧位固定于手术创伤,背部两侧手术区域脱毛(2×2cm),用碘伏消毒后,切出1cm切口。将实施例1和实施例2制备的光愈合高分子水凝胶敷料用γ射线辐照消毒灭菌后植入背部皮下,然后缝合,消毒棉球覆盖。整个手术过程中,未对大鼠进行任何抗生素注射,于术后第6周处死大鼠。取样品周围约0.5cm范围内的组织样品,置于4%多聚甲醛溶液中固定,依次经过乙醇梯度脱水,石蜡包埋切片,然后进行苏木精-伊红染色,显微镜下观察;结果如图4所示,由图4可知,样品植入42d后周围组织炎性细胞含量非常少,并且没有明显的纤维囊泡形成,表明光愈合高分子水凝胶敷料具有良好的组织相容性。
应用例5
使用水合氯醛将sd大鼠进行全身麻醉,俯卧位固定于手术创伤,背部手术区域脱毛(2×2cm),用碘伏消毒后,用剪刀制造0.8cm开放性全层皮肤缺损的圆形创面,至肌筋膜深层,创建全层皮肤创伤模型。将实施例5制取的光愈合高分子水凝胶敷料5贴附于创面,并每2d换料一次,观察不同时间点的创伤愈合情况。其中光照组贴附敷料24h后近红外光照10min,并于换料时直接贴附新的水凝胶敷料;非光照组不接受光照,换料时先揭除旧的凝胶敷料,再进行换料操作;未治疗组不接受任何治疗和换料的操作。大鼠背部创伤进行水凝胶敷料处理后不同时间点的创面愈合率结果如图5所示,由图5可知,各组创伤面积在7和14d均显著减小,愈合率逐渐提高;光照组在同一时间的创面愈合率优于非光照组和未治疗组。其中,光照组14d的创面愈合率达到99.1±5.2%,显著高于非光照组(58.6±6.2%)和未治疗组(46.9±4.8%)。此结果说明光照组具有更高效和完全的药物释放速率、避免换料带来的二次创伤,可以显著加快伤口愈合。
- 还没有人留言评论。精彩留言会获得点赞!