用于增强螺钉稳定性和诱导骨再生的纤维膜及其制备方法与流程
1.本发明属于生物材料技术领域,具体涉及一种用于增强螺钉稳定性和诱导骨再生的纤维膜及其制备方法。
背景技术:
2.骨折时人类常见的损伤,是指由于外伤或病理等原因致使骨质部分或完全断裂的一种疾病。在目前骨折内固定治疗中,对于骨折的患者,在行手术切开复位和钢板螺钉内固定时,目前临床上使用的螺钉有时不能满足固定所有骨折块的要求,骨折内固定手术过程中可因螺钉多次进出、更换螺钉或骨质疏松导致螺钉部分松动或完全松动,进而引起内固定失效而引发一系列并发症,影响内固定的强度和效果,可能会造成内固定手术的失败,目前尚无良好解决办法。受安全套启发,如果在螺钉上也戴上“安全套”再拧入松动的孔道,也许会即刻增加螺钉固定的稳定性。
3.静电纺织技术一种高效低耗的纳米纤维制备技术,其原理是在装有聚合物溶液的喷头和接收装置之间施加高压静电,使溶液在高压电场作用下产生与表面张力相反的电场力,驱使溶液在喷头末端拉伸成一个泰勒锥,当电场力足够大时泰勒锥处液滴可克服表面张力而产生喷射流,在高速震荡中喷射流被迅速拉细,溶剂也快速挥发,最终形成纳微米直径的超细纤维,理论上任何可溶解或熔融的材料均可进行电纺加工。电纺纤维直径通常介于数十纳米至数微米之间,在微观结构上具有交错的网格结构,具有可控的力学性能和高摩擦性,同时高孔隙率和孔径的纤维排列可模拟细胞外基质的结构,进而促进细胞粘附、生长和分化。
4.聚3
‑
羟基丁酸酯/4
‑
羟基丁酸酯共聚物(poly(3
‑
hydroxybutyrate
‑
co
‑4‑
hydroxybutyrate), p34hb),除了具有良好的生物相容性、生物降解性和可纺性,还具有良好的力学性能,p34hb 电纺纤维材料可部分修复在sd大鼠颅骨缺损,但其亲水性较差,限制了其在生物医学方面的应用。氧化石墨烯(graphene oxide,go)由于其特殊的sp2键合和六角形碳结构而具有较佳的机械强度和亲水性,能够有效调控细胞行为,为细胞提供定位点和诱导骨髓间充质干细胞成骨分化,并可作为涂层材料改善钛合金内固定与骨组织之间的相容性,另外,石墨烯基的材料具有良好抗菌性能,能使内固定植入物感染风险进一步降低,但go本身不具备可纺性,需要和其它材料复合才能静电纺丝成为纳微米纤维而发挥作用。聚乙二醇(polyethylene glycol,peg)是亲水性生物材料,具备良好的生物相容性和可纺性而在生物制药领域广泛应用,与p34hb的复合纤维材料已证明了可促进骨再生,并且聚乙二醇作为粘结剂使氧化铝粉末形成固体,表明具有良好金属粘附性能。
技术实现要素:
5.为克服以上技术问题,本发明提供了一种用于增强螺钉稳定性和诱导骨再生的纤维膜及其制备方法。该方法制备的纤维可成膜状、圆柱体状、以及螺钉套状,以解决现有骨科手术技术中螺钉固定不牢固和骨折愈合延迟或不愈合的技术问题。该纤维膜可以按需要
growth peptide, ogp)、甲状旁腺激素相关肽(pthrp
‑
1)、qk肽、prominin
‑
1衍生肽(prominin
‑
1derivedpeptide,pr1p);槲皮素、葛根素、白藜芦醇、姜黄素、表没食子儿茶素没食子酸酯(egcg)、和小檗碱中的任一种或多种。
24.优选地,步骤(3)中,所述注射器的规格为5ml。
25.优选地,步骤(3)中,所述正电压为15kv,负电压为5kv,所述温度为37℃,所述推注速度为0.5/0.1mm/min,所述接收距离15
‑
20cm;接收装置转速为2000r/min。
26.优选地,步骤(3)中,所述干燥后放置于真空干燥机中干燥48小时,使残余有机溶剂蒸发。
27.本发明的另一目的在于提供一种所述的制备方法制备的纳/微米纤维膜。
28.优选地,所述的纳/微米纤维成膜状或成空心或实心的圆柱体状或成螺钉套状。
29.优选地,所述纳/微米纤维具有中空多孔的微观结构。
30.本发明的另一目的在于提供一种功能型可吸收的骨科螺钉套,所述骨科螺钉套由所述纤维素膜或纳/微米纤维制备而成。
31.本发明的另一目的在于所述功能型可吸收的骨科螺钉套的制备方法,包括以下步骤:
32.根据临床骨科螺钉直径、长度需要,利用智能滚轴将同一厚度的纤维膜做成不同直径、不同长度的套状,与螺钉本体形成一体。
33.螺钉套与临床上骨科螺钉直径、长度相匹配,紧密结合于螺钉体表面,可有效增加术中螺钉的初试稳定性和抗拔出力。
34.优选地,所述功能型可吸收的骨科螺钉套的制备还可以将骨科金属螺钉与电纺接收器相连,一次成型获得螺钉与螺钉套的一体结构。
35.与现有技术比,本发明的技术优势在于:
36.(1)本发明提供的纤维膜以具有生物相容性的可降解聚羟基脂肪酸酯及氧化石墨烯为主要材料,通过静电纺丝技术制备。其纤维具有中空多孔或取向结构,该方法制备的纤维膜具有良好的力学性能,与骨科螺钉结合后,可有效增强螺钉的初始稳定性和轴向抗拔出力,解决了术中螺钉松动的临床问题。
37.(2)本发明的通过同轴静电纺丝技术,结合氧化石墨烯、聚羟基脂肪酸酯和聚乙二醇三种材料的优点,构建具有控制缓释成分的中空多孔纤维膜,增加螺钉术中即刻和维持术后螺钉稳定性和轴向抗拔出力,并且促进骨折愈合,为临床螺钉松动提供有效的解决方案。
38.(3)同时在具有中空多孔微观结构的纤维中添加成骨诱导成分,在增加生物稳定性的同时诱导新生骨的生成,避免目前临床上螺钉固定不牢固、骨折愈合延迟,畸形愈合或骨折不愈合的技术问题;其在骨修复过程中缓慢释放,促进骨折愈合,在生物医药尤其骨科领域有着广泛的应用前景。
39.(4)本发明中所述螺钉套,是将生物可吸收材料聚羟基脂肪酸酯、聚乙二醇、和氧化石墨烯配置成溶液,利用静电纺织技术,在高压电场下,将材料纺织为纳米级的膜装、三维套状、以及与螺钉一体。所采用的聚羟基脂肪酸酯、聚乙二醇、和氧化石墨烯材料,具有可完全降解的同时,无酸性代谢产物的产生,有效避免目前临床上内固定材料所产生的无菌性炎症反应并发症的发生,同时氧化石墨烯具有良好的生物活性和生物力学性能。使螺钉
具有更好的早期生物稳定性,防止术后常见的螺钉松动问题。
40.进一步,所述的功能型螺钉套,是在聚羟基脂肪酸酯、聚乙二醇、和氧化石墨烯的溶液中在添加成骨活性肽或天然小分子化合物,利用静电纺织技术,在高压电场下,将材料纺织为纳微米级的纤维膜状、空心或实心的圆柱体状、和螺钉套状。在材料吸收过程中,成骨活性肽或天然小分子化合物具有成骨诱导作用,促进骨折愈合和骨再生。
41.(5)本发明制备的中空多孔纤维,可以调控纤维丝上孔的大小,以控制成骨成分释放的速度。
附图说明
42.图1:实施例1制成的纤维膜;
43.图2:实施例1纤维膜的电镜图;
44.图3:实施例2制成的纤维膜;
45.图4:实施例2纤维膜的微观孔径结构图;其中,(4
‑
1)为纤维中空结构图;(4
‑
2)为纤维表面多孔结构图。
46.图5:实施例3制成的纤维膜;
47.图6:实施例3纤维膜的纤维排列微观结构图;其中,(6
‑
1)为纤维取向排列图;(6
‑
2) 为纤维无序
‑
有序排列图。
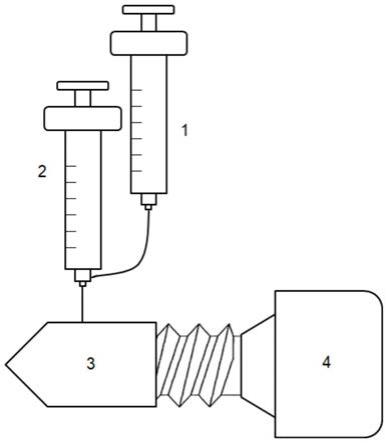
48.图7:实施例4的制备示意图;其中,1为溶液a,2为溶液b,3为纤维膜,4为螺钉。
49.图8:实施例4的螺钉套形状;
50.图9:实施例5中纤维膜的力学性能图;其中,a为应力
‑
位移图;b为弹性模量图;c为伸长率图;d为最大抗拉伸强度图;
51.图10:实施例5的拔出曲线与拔出力对比图;其中,a为螺钉在体外标准试件中初次轴向拔出力、第二次轴向拔出力、完全松动情况下的拔出力曲线;b为部分松动情况下,将各组安全套螺钉结合后拧入原钉道进行拔出力测试,所得到的拔出力曲线;c为完全松动情况下,将各组安全套与螺钉结合后拧入钉道,进行拔出力测试,所得到的拔出力曲线;d为标准试件中初次轴向拔出力、第二次轴向拔出力、完全松动情况下的拔出力大小对比;e为部分松动情况下,各组安全套与螺钉结合后的轴向拔出力大小对比;f为完全松动情况下,各组安全套与螺钉结合后的轴向拔出力大小对比;
52.图11:体外抗拔出试验结果,其中,a为手术示意图;b为箭头钉道和骨折线位置示意图;c为常规组螺钉使用示意图;d为实验组螺钉使用示意图;e为无松动组骨折示意图;f 为无松动组愈合后示意图;g为无松动组cbct检查结果示意图;h为安全套组骨折示意图; i为安全套组愈合后示意图;j为安全套组cbct检查结果示意图;k为完全松动组骨折示意图;l为完全松动组愈合后示意图;m为完全松动组cbct检查结果示意图。
53.现结合附图和实施例对本发明作进一步说明:
具体实施方式
54.下面通过具体实施例对本发明进行说明,以使本发明技术方案更易于理解、掌握,但本发明并不局限于此。下述实施例中所述实验方法,如无特殊说明,均为常规方法;所述试剂和材料,如无特殊说明,均可从商业途径获得。
溶液,利用同轴喷头,将溶液a作为壳层,溶液b作为芯层,设置正电压约15kv,负电压5kv,温度37℃,推注速度分别0.5/0.1mm/min,接收距离15
‑
20cm,获得螺钉
‑
螺钉套一体后,真空干燥机中干燥48小时,使残余有机溶剂蒸发;双面紫外照射4h除菌。工艺图见图 7。
70.制成的螺钉套直观图如图8,该螺钉套为功能型可吸收骨科螺钉套,包括螺钉本身和由生物可吸收材料制成的螺钉套。所述的螺钉套,类似安全套一样套在螺钉钉体部位。螺钉套是将聚羟基脂肪酸酯、聚乙二醇、氧化石墨烯配置成溶液,同时溶液中添加成骨活性肽,利用静电纺织技术,在高压电场下,使用同轴喷头,将材料纺织为纳米级的三维套状。在材料吸收过程中,成骨活性肽的释放具有成骨诱导作用,可在增加生物稳定性的同时诱导新生骨的生成,避免目前临床上螺钉固定不牢固、骨折愈合延迟,畸形愈合或骨折不愈合的技术问题。
71.实施例5
72.参照实施例1的方法,在实验步骤不变的前提下,分别使用原料:p34hb和peg并加入不同比例(0.5
‑
2.5)氧化石墨烯,制成10mm
×
15mm
×
0.14mm大小、有效拉伸长度10mm的薄膜(n=5for each group);其中,单纯p34hb为(p),peg加入后为(p
‑
p),加入氧化石墨烯后为(p
‑
p
‑
g);制得产品:p、p
‑
p、p
‑
p
‑
g0.5、p
‑
p
‑
g1、p
‑
p
‑
g1.5、p
‑
p
‑
g2、p
‑
p
‑
g2.5。
73.效果评价:
74.1、力学性能测试
75.实验方法:测试实施例5中产品的力学性能,包括应力
‑
位移关系、弹性模量、伸长率、最大抗拉伸强度。
76.经万能力学试验机(倾技科技有限公司,中国)进行拉伸测试(100n传感器,拉伸速度 1mm/min);得到拉伸强度、杨氏模量。
77.结果如图9,经力学测试仪测得各组薄膜材料应力
‑
位移关系,取各自平均水平曲线表示各组应力
‑
位移(a),由力学测试仪得出各组弹性模量(b),伸长率(c),最大抗拉伸强度(d)(n=5for each group)*p<0.05(one
‑
way anova)(图中“*”表示p<0.05)。
78.2、松动模型测试
79.方法:硬质聚氨酯泡沫材料在材料性能、均匀性和可用性等方面差异小,因此被用作骨性材料的替代品。根据美国测试材料协会(astm:f1839
‑
08)规范选择第20级(0.32g/cm3)标准硬质聚氨酯泡沫作为骨模型替代的标准试件。
80.样品:实施例5中产品。
81.部分松动模型测试:直径1.0mm的钻头在试件(上海超群橡塑有限公司,中国)上钻孔,拧入直径1.5mm的自攻螺钉(广州华创医疗,中国),经力学测试仪轴向拔出测得空白组螺钉轴向拔出力;拧入螺钉后拧出,再次沿原钉道拧入,测出第二次轴向抗拔出力;同时将薄膜包覆螺钉再拧入,检测轴向抗拔出力。
82.完全松动模型测试:直径1.5mm钻头钻孔,造成完全松动的钉道,拧入1.5mm的自攻螺钉,薄膜包覆螺钉再拧入,检测轴向拔出力;所有测试重复5次。
83.结果如图10,a为螺钉在体外标准试件中初次轴向拔出力、第二次轴向拔出力、完全松动情况下的拔出力曲线。b为部分松动情况下,将各组安全套螺钉结合后拧入原钉道进行拔出力测试,所得到的拔出力曲线。c为完全松动情况下,将各组安全套与螺钉结合后拧入钉道,进行拔出力测试,所得到的拔出力曲线。d为标准试件中初次轴向拔出力、第二次轴
向拔出力、完全松动情况下的拔出力大小对比。e为部分松动情况下,各组安全套与螺钉结合后的轴向拔出力大小对比。f为完全松动情况下,各组安全套与螺钉结合后的轴向拔出力大小对比。(n=5for each group),*p<0.05,(one
‑
way anova)。
84.3、体内完全松动模型试验
85.根据膜力学测试、细胞相容性测试和体外抗拔出试验的结果,选取实施例2的制成的膜进行体内完全松动模型试验。
86.新西兰白兔9只(雄性,平均2
‑
2.5kg)。10%的水合氯醛,按3.5ml/kg腹腔注射麻醉后,双侧髋关节备皮,消毒铺敷,于股骨大转子处切开皮肤约3cm,逐层进入显露骨组织,电锯制备转子间不全性骨折,分为三组:1.5mm直径的电钻垂直于骨折线钻孔,分别用直径1.5mm 自攻螺钉拧入(完全松动组),包覆材料后行螺钉拧入(安全套组);无松动组以1.0mm直径钻头钻孔后直径1.5mm的自攻金属螺钉拧入。关闭切口后双下肢肌肉注射青霉素8万单位,持续3日,预防感染。结果见图11,其中,a为手术示意图;b为箭头钉道和骨折线位置示意图;c为常规组螺钉使用示意图;d为实验组螺钉使用示意图;
87.影像学检查:术后第一天(day 1)及第四周(day 28),并于术后4周cbct检查,结果见图11,其中,e为无松动组(control)骨折示意图;f为无松动组愈合后示意图;g为无松动组cbct检查结果示意图;h为安全套组(ms
‑
cl)骨折示意图;i为安全套组愈合后示意图;j为安全套组cbct检查结果示意图;k为完全松动组(ns
‑
cl)骨折示意图;l为完全松动组愈合后示意图;m为完全松动组cbct检查结果示意图。
88.上述详细说明是针对本发明其中之一可行实施例的具体说明,该实施例并非用以限制本发明的专利范围,凡未脱离本发明所为的等效实施或变更,均应包含于本发明技术方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1