硫康唑和/或硫康唑的盐在制备治疗食管鳞状细胞癌药物中的应用
本发明涉及生物医药领域,特别是涉及硫康唑和/或硫康唑的盐在制备治疗食管鳞状细胞癌药物中的应用。
背景技术:
食管癌(esophagealcancer)是由食管鳞状上皮或腺上皮的异常增生所形成的恶性病变。食管癌主要分为食管鳞状细胞癌(esophagealsquamouscellcarcinoma,escc)和食管腺癌(esophagealadenocarcinoma,eac)两种主要病理类型。
食管癌发生涉及多因素、多阶段、多基因变异积累及与环境因素相互作用的复杂过程,包括在分子水平上涉及众多原癌基因、抑癌基因以及蛋白质的改变,以及长期不良的生活或饮食习惯的影响(进食含亚硝胺类较多的食物、如喜欢腌制酸菜或霉变食品、长期喜进烫食、吸烟、饮酒或其他不良嗜好等)。食管癌发病隐匿,早期无症状或症状很不典型,发现时已是临床晚期,普遍预后不佳(5年生存率约为13%)。目前,食管癌的治疗方法仍以化疗药物为主,副作用比较大。
技术实现要素:
为了解决上述问题,本发明提供了硫康唑和/或硫康唑的盐在制备治疗食管鳞状细胞癌药物中的应用。硫康唑和/或硫康唑的盐的副作用较化疗药更清楚,该药物药物安全性已被证明,可用作治疗食管鳞状细胞癌,而且还能显著抑制食管鳞状细胞癌细胞和裸鼠移植瘤的增殖以及抑制细胞中食管鳞状细胞癌细胞转移水平。
为了实现上述目的,本发明提供如下技术方案:
本发明提供了硫康唑和/或硫康唑的盐在制备治疗食管鳞状细胞癌药物中的应用。
优选的,所述硫康唑的盐包括硝酸硫康唑。
本发明提供了一种治疗食管鳞状细胞癌的药物,所述药物的有效成分包括硫康唑和/或硫康唑的盐。
优选的,所述药物还包括药学上可接受的辅料。
优选的,所述药物的剂型包括注射剂。
本发明提供了硫康唑和/或硫康唑的盐在制备促进食管鳞状细胞癌凋亡及抑制食管鳞状细胞增殖、转移和葡萄糖的吸收药物中的应用。
本发明提供了一种促进食管鳞状细胞癌凋亡及抑制食管鳞状细胞增殖、转移和葡萄糖的吸收药物,所述药物的有效成分包括硫康唑和/或硫康唑的盐。
优选的,所述药物还包括药学上可接受的辅料。
优选的,所述药物的剂型包括注射剂。
有益效果:
本发明提供了硫康唑和/或硫康唑的盐在制备治疗食管鳞状细胞癌药物中的应用。本发明所述硫康唑和/或硫康唑的盐的药物安全性已被证明,其副作用较化疗药更清楚,可用作治疗食管鳞状细胞癌。本发明具体实施例采用食管鳞状细胞癌的细胞和荷瘤裸鼠动物模型试验证明:硫康唑和/或硫康唑的盐能显著抑制食管鳞状细胞癌细胞和裸鼠移植瘤的增殖以及细胞中食管鳞状细胞癌细胞转移水平,并限制抑制了食管鳞状细胞癌细胞对葡萄糖的吸收;硫康唑和/或硫康唑的盐能显著促进了食管鳞状细胞癌细胞凋亡。
附图说明
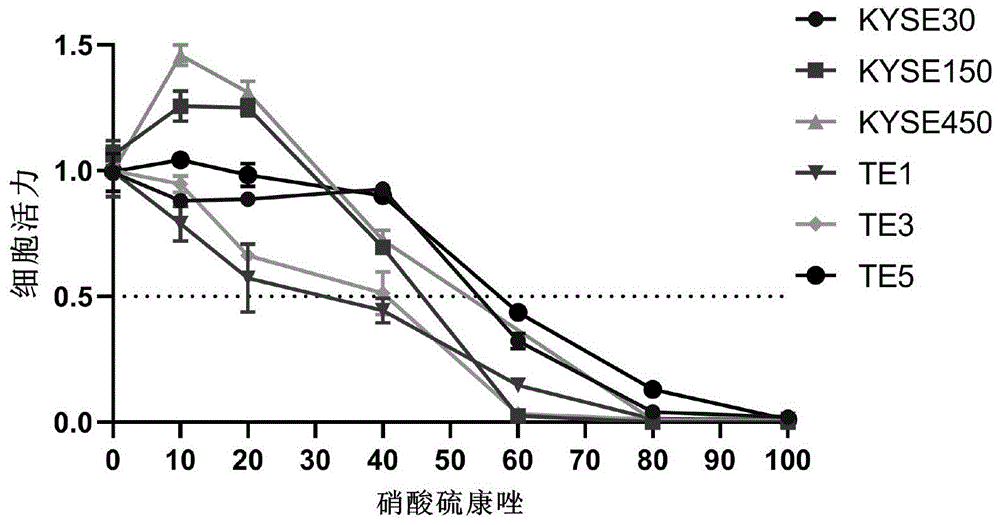
图1为不同药物浓度下的细胞活力典型图;
图2为细胞克隆数量示意图,其中a为培养kyse30细胞用0μm和20μm的硝酸硫康唑处理后的克隆数量统计柱状图,b为培养kyse150细胞用0μm和20μm的硝酸硫康唑处理后的克隆数量统计柱状图,c为a图数据来源情况的细胞真实克隆情况典型图片,d为b图数据来源情况的细胞真实克隆情况典型图片;
图3为划痕愈合面积示意图,其中a为0μm和20μm的硝酸硫康唑在分别处理kyse30细胞0小时和24小时的愈合变化统计柱状图,b为0μm和20μm的硝酸硫康唑在分别处理kyse150细胞0小时和24小时的愈合变化统计柱状图,c为0μm和20μm的硝酸硫康唑在分别处理kyse30细胞0小时和24小时的愈合变化的真实细胞图片,d为0μm和20μm的硝酸硫康唑在分别处理kyse150细胞0小时和24小时的愈合变化的真实细胞图片;
图4为细胞转移实验图,其中a为二甲亚砜和30μm的硝酸硫康唑处理kyse30细胞48小时后,转移细胞柱状统计图;b为二甲亚砜和30μm的硝酸硫康唑处理kyse150细胞48小时后,转移细胞柱状统计图;c为二甲亚砜和30μm的硝酸硫康唑处理kyse30细胞48小时后,转移细胞的真实细胞图片;d为二甲亚砜和30μm的硝酸硫康唑处理kyse150细胞48小时后,转移细胞的真实细胞图片;
图5为流式细胞术实验图,其中a为细胞凋亡检测结果图,b为统计凋亡的比例定量图;
图6为葡萄糖摄取测定实验图,其中a为食管癌细胞kyse30的葡萄糖摄取变化柱状图,b为食管癌细胞kyse150的葡萄糖摄取变化柱状图;
图7为裸鼠接种kyse30和kyse150后,按每3天分别腹腔注射药物溶解剂二甲亚砜和硝酸硫康唑(10mg/kg),30天后的肿瘤体积和重量变化示意图,其中a为kyse30形成的肿瘤的体积和重量的实物图,b为kyse30形成的肿瘤的体积变化图,c为kyse30形成的肿瘤的重量变化图,d为kyse150形成的肿瘤的体积和重量的实物图,e为kyse150形成的肿瘤的体积变化图,f为kyse150形成的肿瘤的重量变化图。
具体实施方式
本发明提供了硫康唑(sulconazole)和/或硫康唑的盐在制备治疗食管鳞状细胞癌药物中的应用,所述所述硫康唑的盐优选包括硝酸硫康唑(sulconazolenitrate)。sulconazole的药物安全性已被证明,其副作用较化疗药更清楚,可用作治疗食管鳞状细胞癌细胞;本发明对所述硫康唑和/或硫康唑的盐的来源没有特殊限定,本领域技术人员常规购买即可;在本发明具体实施例中,所述硝酸硫康唑优选购买于medchemexpress,货号为hy-b1460a;所述硝酸硫康唑的化学式优选如式i所示:
本发明具体实施例采用食管鳞状细胞癌的细胞和荷瘤裸鼠动物模型试验证明:硝酸硫康唑能显著抑制食管鳞状细胞癌细胞和裸鼠移植瘤的增殖和转移水平,可见硝酸硫康唑能够用于制备治疗食管鳞状细胞癌药物。
本发明提供了一种治疗食管鳞状细胞癌的药物,所述药物的有效成分包括硫康唑和/或硫康唑的盐,所述硫康唑的盐优选包括硝酸硫康唑。在本发明中,所述药物优选还包括药学上可接受的辅料;所述药物的剂型优选包括注射剂。本发明所述硝酸硫康唑在进行细胞活力试验时,浓度为20μm,进行裸鼠异种移植实验时的用量是10mg/kg,就能够达到抑制癌细胞生长的效果。
本发明提供了硫康唑和/或硫康唑的盐在制备促进食管鳞状细胞癌凋亡及抑制食管鳞状细胞增殖、转移和葡萄糖的吸收药物中的应用,所述硫康唑的盐优选包括硝酸硫康唑。
本发明提供了一种促进食管鳞状细胞癌凋亡及抑制食管鳞状细胞增殖、转移和葡萄糖的吸收药物,所述药物的有效成分包括硫康唑和/或硫康唑的盐,所述硫康唑的盐优选包括硝酸硫康唑。在本发明中,所述药物优选还包括药学上可接受的辅料;所述药物的剂型优选包括注射剂。本发明所述硝酸硫康唑在进行细胞活力试验时,浓度为20μm,进行裸鼠异种移植实验时的用量是10mg/kg,就能够达到抑制癌细胞生长的效果;进行细胞划痕愈合实验时的浓度是20μm,就能够达到抑制食管鳞状细胞癌细胞在细胞培养皿中的转移效果;进行流式细胞术实验时的浓度为50μm就能够达到促进癌细胞的死亡率;进行葡萄糖摄取测定实验时,30μm和50μm的硝酸硫康唑显著抑制了kyse30和kyse150两种细胞的葡萄糖的摄取。
本发明在进行细胞活力试验时,采用的细胞系优选包括kyse30、kyse150、kyse450、te1、te3和te5;本发明对所述kyse30、kyse150、kyse450、te1、te3和te5的来源没有特殊要求,采用本领域技术人员常规购买所得,kyse30、kyse150、kyse450来自于日本细胞库japanesecollectionofresearchbioresourcescellbank;te1、te3和te5来自于japanesecellresourcecenterforbiomedicalresearch。
为了进一步说明本发明,下面结合附图和实施例对本发明提供的硫康唑和/或硫康唑的盐在制备治疗食管鳞状细胞癌药物中的应用进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
实施例1
细胞活力试验(mts试验)
为了测量不同细胞系(kyse30、kyse150、kyse450来自于日本细胞库japanesecollectionofresearchbioresourcescellbank;te1、te3和te5来自于japanesecellresourcecenterforbiomedicalresearch)对药物硝酸硫康唑的敏感性,细胞被消化并在含有10%血清的rpmimedium1640培养基(购买厂家:英潍捷基(上海)贸易有限公司,货号:11875119,品牌:gibco)中培养,形成单个细胞悬液,计数细胞,接种于96孔板,每孔10000个细胞。每孔介质体积为100μl。将细胞培养12小时贴壁,然后换成分别含有0μm、10μm、20μm、40μm、60μm、80μm和100μm的硝酸硫康唑的rpmimedium1640培养基(购买厂家:英潍捷基(上海)贸易有限公司,货号:11875119,品牌:gibco)。连续培养24小时后,每孔加入mts(货号:g3581,公司:promega)20μl,孵育2小时。采用thermoscientific公司的mk3酶标仪在波长为492nm处测量各孔的吸光度值。具体步骤参考《slc52a3expressionisactivatedbynf-kappabp65/rel-bandservesasaprognosticbiomarkerinesophagealcancer》(long,l.etal.cellmollifesci75,2643-2661,doi:10.1007/s00018-018-2757-4(2018)),计算不同药物浓度下的细胞活力,结果见表1,然后使用graphpadprism7软件进行绘图,结果见图1。
表1不同药物浓度下的细胞活力比值
由表1和图1记载的可知,随着药物浓度的增加硝酸硫康唑逐渐显著地抑制了食管鳞状细胞系kyse30,kyse150,kyse450,te1,te3和te5这些癌细胞的存活。
实施例2
细胞克隆形成实验
在12孔板中,每孔接种500~1,000个kyse30或kyse150细胞。待细胞贴壁后,在rpmimedium1640细胞培养液(购买厂家:英潍捷基(上海)贸易有限公司,货号:11875119,品牌:gibco)中加入浓度为20μm的硝酸硫康唑药物,培养12小时。用rpmimedium1640培养基(购买厂家:英潍捷基(上海)贸易有限公司,货号:11875119,品牌:gibco)替换含有药物的rpmimedium1640细胞培养液再继续培养细胞2周,以二甲亚砜(dmso,全称为dimethylsulfoxide,购买厂家:sigma,货号:d4540-1l,品牌:sigma)为阴性对照。4℃预冷pbs洗涤后,用4℃预冷甲醇和冰醋酸3:1固定20分钟,并用紫结晶染色15分钟,具体步骤参考《riboflavindepletionpromotestumorigenesisinhek293tandnih3t3cellsbysustainingcellproliferationandregulatingcellcycle-relatedgenetranscription》(long,l.,etal.jnutr,2018.148(6):p.834-843)。用chemidoctouch(bio-rad)对菌落拍照,用imagej软件(美国国立卫生研究院,bethesda,md,usa)计算克隆数量,每个实验重复3次,结果见表2、表3和图2。
表2kyse30细胞克隆数量示意表
表3kyse150细胞克隆数量示意表
由表2、表3和图2记载的可知,20μm的硝酸硫康唑显著抑制了kyse30和kyse150两种细胞形成的细胞克隆数目。
实施例3
划痕愈合实验
将kyse30或kyse150细胞(来自于日本细胞库japanesecollectionofresearchbioresourcescellbank)接种到6孔板中,在无血清的rpmimedium1640培养基中培养12小时。用无菌移液管尖端画一条直线。用pbs清洗细胞,然后在2%胎牛血清的rpmimedium1640培养基中培养。分别用含有0μm和20μm的硝酸硫康唑药物的rpmimedium1640培养基分别于培养kyse30或kyse150细胞的细胞皿中加入该含药的rpmimedium1640培养基的0小时和24小时后用显微镜对指定区域进行显微观察,以二甲亚砜为阴性对照,具体步骤参考《rac1inhibitionreversescisplatinresistanceinesophagealsquamouscellcarcinomaandinducesdownregulationofglycolyticenzymes》(zeng,r.j.,etal.moloncol,2019.13(9):p.2010-2030.)。采用imagej软件(美国国立卫生研究院,bethesda,md,usa)计算划痕愈合面积,结果见表4、表5和图3。
表4kyse30的划痕愈合面积
表5kyse150的划痕愈合面积
由表4、表5和图3记载的可知,20μm的硝酸硫康唑显著抑制了kyse30和kyse150两种细胞在细胞培养板中的移动速度。
实施例4
细胞转移实验
为了测量药物硝酸硫康唑对细胞系移动能力的影响,食管癌细胞kyse30和kyse150用无血清的rpmimedium1640培养基饥饿12小时后,以每孔5万个细胞分解接种到transwell小室内,分别以二甲亚砜(对照组)和30μm硝酸硫康唑处理48小时后,对transwell小室进行固定、染色和成像,每个小室随机统计十个视野细胞数,结果见表6和图4。
表6kyse30和kyse150细胞转移个数统计表
由表6和图4记载的可知,30μm的硝酸硫康唑显著抑制了kyse30和kyse150两种细胞在transwell小室中的转移程度。
实施例5
流式细胞术实验
以二甲亚砜处理为对照组,食管癌细胞kyse30和kyse150分别用50μm硝酸硫康唑处理24小时后(每组三个样本),按细胞凋亡试剂盒(公司:碧云天,货号:c1062s)说明书处理细胞,用流式细胞仪检测细胞凋亡水平。结果见表7和图5,其中图5中a为细胞凋亡检测结果图。图5中b为统计凋亡的比例定量图。
表7kyse30和kyse150细胞死亡率统计表
由表7和图5记载的可知,50μm的硝酸硫康唑显著促进了kyse30和kyse150两种细胞的死亡率。
实施例6
葡萄糖摄取测定实验
食管癌细胞kyse30和kyse150分别用0μm、30μm、50μm硝酸硫康唑处理24小时后(每组三个样本),试剂盒(glucose-uptakeglotmassay,货号:j1342,公司:promega)检测细胞葡萄糖的摄取变化。结果见表8和图6。
表8kyse30和kyse150细胞葡萄糖摄取情况统计表
由表8和图6记载的可知,30μm和50μm的硝酸硫康唑显著抑制了kyse30和kyse150两种细胞的葡萄糖的摄取,进而达到抑制食管癌细胞的效果。
实施例7
裸鼠异种移植实验
动物实验按照汕头大学医学院医学实验动物伦理委员会批准的方案进行,具体步骤参考《rac1inhibitionreversescisplatinresistanceinesophagealsquamouscellcarcinomaandinducesdownregulationofglycolyticenzymes》(zeng,r.j.,etal.moloncol,2019.13(9):p.2010-2030)。3~5周龄裸鼠(中国北京vitalriver实验动物技术有限公司)随机分为4组(1组为kyse30二甲亚砜组、2组为kyse30硝酸硫康唑组、3组为kyse150二甲亚砜组和4组为kyse150硝酸硫康唑组),每组5只,分别将kyse30(2×106个)和kyse150(1×106个)细胞注入小鼠腋窝。当肿瘤平均体积达到50mm3时开始注射药物,其中2组和4组每3天腹腔注射硝酸硫康唑(10mg/kg),1组和3组每3天注射二甲亚砜(150μl)。每3天测量肿瘤体积,按下式(宽2×长)/2计算。接种后30天,用二氧化碳对小鼠实施安乐死,切除肿瘤并称重,结果见表9~表12和图7。
表9kyse30细胞裸鼠移植瘤体积统计表(mm3)
表10kyse150细胞裸鼠移植瘤体积统计表(mm3)
表11kyse30细胞裸鼠移植瘤重量统计表(g)
表12kyse150细胞裸鼠移植瘤重量统计表(g)
由表9~表12和图7记载的可知,在裸鼠异种移植实验中,硝酸硫康唑(10mg/kg)分别显著抑制了kyse30和kyse150细胞在裸鼠皮下形成移植瘤的体积和重量。
虽然本发明已以较佳的实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可以做各种改动和修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
- 还没有人留言评论。精彩留言会获得点赞!