一种用于关节腔注射的医用几丁糖及其制备方法与流程
1.本发明属于生物医用材料领域,具体涉及一种用于关节腔注射的医用几丁糖及其制备方法,预期应用于骨关节炎、软骨损伤等骨科领域。
背景技术:
2.目前临床上骨关节炎的治疗包括非药物保守治疗、药物治疗和手术治疗等方式,需要根据患者所处的疾病阶段和全身情况选择个体化治疗方案。关节腔内注射药物或生物制剂具有操作简单、局部生物利用度高、全身不良反应少等优点,已经作为治疗骨关节相关疾病的常规干预手段之一,被广泛应用于临床。现用于关节腔内注射的制剂包括:透明质酸、糖皮质激素、富血小板血浆、医用几丁糖等。各种关节腔内注射物具有各自的特点:糖皮质激素具有起效快、短期疗效显著的特点,但其长期疗效欠佳,且可能存在软骨损伤作用,使正常的软骨退变,发生类固醇诱导的骨关节病,更适用于骨关节炎的短期疼痛缓解;透明质酸钠是关节液及软骨基质的主要成分,可以防止软骨基质丢失,阻止蛋白多糖从软骨中溢出。此外,还可促进关节软骨的愈合与再生,能有效缓解疼痛、肿胀与改善关节功能,增加其润滑能力。透明质酸钠对疼痛的缓解作用持续时间可达6个月以上。
3.医用几丁糖是一种经提纯加工后主要成分为聚氨基葡萄糖的高分子化合物,在理化性质上与关节内构成软骨及软骨基质的氨基多糖相似,具有抑制关节炎进展的作用。
4.氨基葡萄糖是一种天然的氨基单糖,是软骨基质和滑液中聚氨基葡萄糖的成分。外源性的氨基葡萄糖可以刺激软骨细胞合成蛋白多糖,补充软骨基质的丢失成分,并可抑制基质金属蛋白酶的表达,从而促进软骨的修复。氨基葡萄糖可以抑制因免疫而造成的蛋白多糖降解,达到修复受损的关节软骨的作用;研究表明,氨基葡萄糖可抑制弹性蛋白酶、溶酶体酶等水解酶的释放,减少其对软骨基质的水解破坏,从而阻碍因免疫反应的恶性循环对关节软骨的不断破坏。
5.将医用几丁糖注射剂应用于膝关节病变,能够润滑关节,改善关节内环境,减轻患者的疼痛,通过保护患者关节软骨,延缓软骨组织被破坏及磨损的进程,从而进一步改善患者的生活质量。
6.目前,医用几丁糖注射剂普遍存在以下技术难点:
7.1)过滤除菌工艺是通过除菌过滤器,将料液中的微生物除去而得到无菌滤液的生产工艺。终端湿热灭菌是指在最终容器中,用饱和水蒸汽、沸水或流通蒸汽进行灭菌的方法。与过滤除菌相比,终端湿热灭菌的无菌保证水平更高。在1980~2000年间,几乎所有非无菌或缺乏无菌性保证而召回的药品,都是通过无菌工艺生产的。因此2004版fda无菌工艺指南明确指出:使用无菌工艺生产的无菌药品与可最终灭菌的无菌药品有着本质区别,只有在最终灭菌不可行的条件下,则使用无菌工艺生产无菌药品。此外,《中国药典》明确规定,根据无菌保证水平(sterility assurance level,sal)的高低和风险的大小,注射剂首选最终端灭菌工艺,对于不能耐受最终端灭菌工艺的药物,即对热不稳定的一些药物品种,可选择用无菌生产工艺制备。由于羧甲基甲壳质对热不稳定,因此目前市面上产品以及临
床均为过滤除菌,无菌保证水平较低,影响患者的使用安全性;因此如何同时保证无菌水平而不影响产品性能是目前技术的一大难点;
8.2)羧甲基壳聚糖制备工艺需要在碱性条件下将氯乙酸与壳聚糖反应,最终得到羧甲基壳聚糖。在此过程中,氯乙酸自身会反应生成少量的二甘醇酸(dga)查阅毒理数据库显示dga具有刺激性、食入毒性和细胞毒性。医药级壳聚糖类产品会直接与体液及血液接触,存在潜在危害性,因此对羧甲基壳聚糖中的dga残留量进行控制是目前技术的难点;
9.3)真空干燥技术也被称为解析干燥技术,工作时将物料置于真空负压条件下,并通过适当提高温度的方式达到物料在负压状态下的沸点或者通过降低温度的方式达到物料在负压状态下的熔点,以达到干燥物料的目的。此外,采用真空干燥技术可以隔绝空气,防止物料发生氧化等化学变化,避免物料失去原有的特性溶剂,但干燥速度慢。鼓风干燥速度快,对有机溶剂的干燥效果好。几丁糖注射剂在醇沉的过程中会用到大量的乙醇,若含有残留的乙醇,可能会对患者产生刺激作用,影响使用过程中的安全性。因此采用鼓风干燥和真空干燥相结合的干燥工艺,可以较好地去除材料中的水以及乙醇残留。
技术实现要素:
10.本发明的目的是为了克服现有技术的不足,提供一种用于关节腔注射的医用几丁糖。
11.根据本发明的第一个方面,本发明提供了一种用于关节腔注射的医用几丁糖,其特征在于所述医用几丁糖的组分包括羧甲基甲壳质和平衡液。进一步地,是由由羧甲基甲壳质和平衡液配制灌装而成。
12.进一步地,所采用的羧甲基甲壳质的分子量分布为200-1500kda。
13.进一步地,平衡液的ph在6.5-7.5之间,渗透压在200-250mosm/kg之间。
14.进一步地,几丁糖的浓度在5mg/ml-50mg/ml。
15.本发明的一个突出之处是找到了一种非常适合用于关节腔注射的医用几丁糖的产品形式和灭菌方式组合方案,所述医用几丁糖制成后被直接灌装到注射器中,然后进行终端灭菌,所述终端灭菌采用终端高温湿热灭菌。
16.进一步地,灌装量为匹配一次注射量的容量。
17.进一步地,对于所述终端高温湿热灭菌的方式,其中,灭菌温度121.0℃,满载fo=6.5,半载fo=6.7,灭菌时间为6min。
18.根据本发明的第二个方面,本发明提供一种用于关节腔注射的医用几丁糖的制备方法,其特征在于包括以下步骤:
19.1)羧甲基甲壳质制备:将块状甲壳质粉碎机粉碎后,使用异丙醇膨化,氢氧化钠溶液碱化,氯乙酸羧化。
20.醇沉:将羧化后的羧甲基甲壳质静置分层后倒去上清液后,转移至2#砂芯漏斗真空抽滤,抽滤后制品分别用80%酒精、95酒精和无水乙醇洗涤三次,最后用2#砂芯漏斗抽滤干净。
21.干燥:将滤干后制品先鼓风干燥后真空干燥。
22.2)将氯化钠,磷酸二氢钠,磷酸氢二钠分别配制成一定的浓度加入到注射用水中,以一定的比例混合搅拌后,配制成平衡液;
23.3)将羧甲基甲壳质以一定的比例加入到配制好的平衡液当中,搅拌一段时间,直至溶液完全溶解,得到医用几丁糖配制液;
24.然后进行灌装和终端灭菌,终端灭菌完成后用泡罩包装一体机进行包装。
25.进一步地,所述灌装和终端灭菌包括以下步骤:
26.4)采用灌装设备对配制液进行灌装,灌装至预灌封注射器中,灌装量为匹配一次注射量的容量;
27.5)灌装完成的注射器进行高温湿热灭菌,灭菌完成后用泡罩包装一体机进行包装。
28.优选地,步骤1)中,将羧化后的羧甲基甲壳质静置分层后倒去上清液后,转移至2#砂芯漏斗真空抽滤,抽滤后制品分别用80%酒精洗涤三次,将第三次洗涤且真空抽滤的制品溶于注射用水中,用盐酸调ph在5.9-6.1。调节ph后用2#砂芯漏斗过滤,随后用95%酒精洗涤;静置分层倒去上清液,将多次静置的沉淀用无水乙醇脱水两次,第一次直接倒去上清液,第二次无水乙醇脱水后用2#砂芯漏斗抽滤,滤干后的制品用70%酒精超声波清洗机超声10-30min;此步骤重复两次。最后用无水乙醇脱水两次,用2#砂芯漏斗抽滤干净。
29.优选地,步骤1)中,干燥方式为先鼓风干燥后真空干燥。滤干后制品先在20-30℃鼓风干燥10h以上,然后40-60℃鼓风干燥2-6h,最后置于真空干燥箱在50-70℃下真空干燥4-8h。
30.优选地,步骤2)中,氯化钠,磷酸二氢钠,磷酸氢二钠三者的质量比为(500-1000):(10-20):(20-50)。
31.优选地,步骤2)中,平衡液的ph在6.5-7.5之间,渗透压在200-250mosm/kg之间;
32.优选地,步骤5)中,采用终端高温湿热灭菌的方式,规格:灭菌温度121.0℃,满载fo=6.5,半载fo=6.7,灭菌时间设置为6min。优选地,制备后的用于关节腔注射的医用几丁糖中,几丁糖的浓度在5mg/ml-50mg/ml。
33.本发明是以虾壳或蟹壳处理之后的甲壳质为主要原料,通过对其进行碱化、羧化等步骤制得羧甲基壳聚糖,并在一定条件下对羧甲基壳聚糖进行配制及灌装,高温湿热灭菌后获得的医用几丁糖注射剂。其外观为无色、透明粘稠状液体,主要成分为聚氨基葡萄糖,具有粘弹性,缓吸收性,所得关节腔注射剂具有良好的生物相容性和安全性,不具有细胞毒性,对骨关节炎有一定的治疗作用,并且对免疫功能无明显影响。
34.本发明涉及的医用几丁糖具有润滑作用和生物屏障作用,与透明质酸钠相比,具有更加优异的润滑效果,因此本品可作为骨关节内的润滑剂用于关节润滑、保护关节软骨、辅助骨关节病的治疗。有望应用于临床骨关节病的预防和治疗,改善关节功能,有利于病理性关节软骨修复。
35.本发明采用终端灭菌工艺在控制微生物污染量的基础上,在灌封后,通过高温湿热灭菌方式除菌。本方法成本低,无菌保证水平高,适宜于大容量注射剂的灭菌。采用超声清洗工艺降低二甘醇酸含量,改进干燥方式降低乙醇残留,进一步提高产品的使用安全性。
附图说明
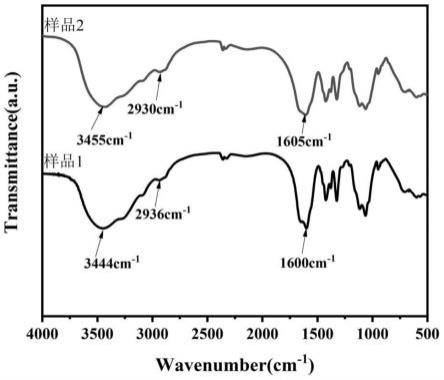
36.图1为样品1和样品2的医用几丁糖的红外吸收图。
37.图2为骨关节炎模型中阴性对照组和模型对照组的大体观察图以及组织he染色
图。(a)阴性对照组:大体观察关节面光滑,色泽与未手术侧(左侧)一致,0分;(b)阴性对照组:关节组织结构正常,透明软骨层结构完整(he染色,100x);(c)模型对照组:软骨增生,多处深处破损软骨溃疡3分;(d)模型对照组:关节软骨变薄,镜下见明显软骨层溃疡面(he染色,100x)。
38.图3为骨关节炎模型上市对照组与供试品组(样品1)的大体观察图以及组织he染色图。(a)上市对照组:关节面少量糜烂,软骨发生浅层片状缺损2分;(b)上市产品组:关节软骨变薄,形成凹陷的溃疡面(he染色,100x);(c)供试品组:关节面糜烂,软骨发生浅层片状缺损2分;(d)供试品组:关节软骨变薄,镜下见较小的软骨层溃疡面(he染色,100x)。
具体实施方式
39.为了进一步理解本发明,下面结合实施例对本发明提供的一种用于关节腔注射的医用几丁糖进行具体描述,但本发明并不限于这些实施例,该领域技术人员在本发明核心指导思想下做出的非本质改进和调整,仍然属于本发明的保护范围。
40.(一)、一种用于关节腔注射的医用几丁糖的制备
41.实施例1
42.1)羧甲基甲壳质制备:将块状甲壳质粉碎机粉碎后,经50目筛网过筛;称取过筛后甲壳质200g溶于200ml异丙醇中搅拌膨化溶胀,搅拌2.0-2.5h,将50%氢氧化钠溶液(称取400
±
0.2g氢氧化钠,再将氢氧化钠溶于400ml注射用水中)冰水浴冷却至15℃以下后缓慢加入到上述甲壳质溶液中;挪去冰水浴,将氯乙酸溶液(准确称取氯乙酸440溶于1000ml异丙醇中)缓慢加入到上述碱化甲壳质溶液中,加完后继续搅拌3.5-4.0h,搅拌结束后静置10h以上;
43.醇沉:将羧化后的羧甲基甲壳质静置分层后倒去上清液后,转移至2#砂芯漏斗真空抽滤,抽滤后制品分别用80%酒精洗涤三次,将第三次洗涤且真空抽滤的制品溶于注射用水中,用盐酸调ph在5.9-6.1。调节ph后用2#砂芯漏斗过滤,随后用95%酒精洗涤;静置分层倒去上清液,将多次静置的沉淀用无水乙醇脱水两次,第一次直接倒去上清液,第二次无水乙醇脱水后用2#砂芯漏斗抽滤,滤干后的制品用70%酒精超声波清洗机超声10-30min;此步骤重复两次。最后用无水乙醇脱水两次,用2#砂芯漏斗抽滤干净。
44.干燥:将滤干后制品在25℃鼓风干燥10h以上,然后45℃鼓风干燥2h,最后置于真空干燥箱在60
±
5℃下真空干燥4h。
45.2)用注射用水配制平衡液,其中各组分的浓度为:氯化钠6.8g/l,磷酸二氢钠0.25g/l,磷酸氢二钠0.33g/l;
46.3)称取1000g羧甲基甲壳质,加入到100l配制好的平衡液当中,搅拌15h至溶液完全溶解,得到医用几丁糖配制液;
47.4)采用灌装设备对配制液进行灌装,灌装至2ml预灌封注射器中;
48.5)灌装完成的注射器进行高温湿热灭菌,规格:灭菌温度121.0℃,满载fo=6.5,半载fo=6.7,灭菌时间设置为6min。灭菌完成后用泡罩包装一体机进行包装,得到浓度为10mg/ml的医用几丁糖(以下称为样品1)
49.实施例2
50.1)羧甲基甲壳质制备:将块状甲壳质粉碎机粉碎后,经50目筛网过筛;称取过筛后
甲壳质200g溶于200ml异丙醇中搅拌膨化溶胀,搅拌2.0-2.5h,将50%氢氧化钠溶液(称取400
±
0.2g氢氧化钠,再将氢氧化钠溶于400ml注射用水中)冰水浴冷却至15℃以下后缓慢加入到上述甲壳质溶液中;挪去冰水浴,将氯乙酸溶液(准确称取氯乙酸440溶于1000ml异丙醇中)缓慢加入到上述碱化甲壳质溶液中,加完后继续搅拌3.5-4.0h,搅拌结束后静置10h以上;
51.醇沉:将羧化后的羧甲基甲壳质静置分层后倒去上清液后,转移至2#砂芯漏斗真空抽滤,抽滤后制品分别用80%酒精洗涤三次,将第三次洗涤且真空抽滤的制品溶于注射用水中,用盐酸调ph在5.9-6.1。调节ph后用2#砂芯漏斗过滤,随后用95%酒精洗涤;静置分层倒去上清液,将多次静置的沉淀用无水乙醇脱水两次,第一次直接倒去上清液,第二次无水乙醇脱水后用2#砂芯漏斗抽滤,滤干后的制品用70%酒精超声波清洗机超声10-30min;此步骤重复两次。最后用无水乙醇脱水两次,用2#砂芯漏斗抽滤干净。
52.干燥:将滤干后制品在25℃鼓风干燥10h以上,然后45℃鼓风干燥2h,最后置于真空干燥箱在60
±
5℃下真空干燥4h。
53.2)用注射用水配制平衡液,其中各组分的浓度为:氯化钠7.2g/l,磷酸二氢钠0.2g/l,磷酸氢二钠0.28g/l;
54.3)称取2000g羧甲基甲壳质,加入到100l配制好的平衡液当中,搅拌15h至溶液完全溶解,得到医用几丁糖配制液;
55.4)采用灌装设备对配制液进行灌装,灌装至2ml预灌封注射器中;
56.5)灌装完成的注射器进行高温湿热灭菌,规格:灭菌温度121.0℃,满载fo=6.5,半载fo=6.7,灭菌时间设置为6min。灭菌完成后用泡罩包装一体机进行包装,得到浓度为20mg/ml的医用几丁糖(以下称为样品2)。
57.(二)、测定医用几丁糖的ph、渗透压和动力粘度
58.对实施例1和实施例2中的医用几丁糖进行ph、渗透压和动力粘度的检测,结果如表1所示。
59.表1医用几丁糖的ph、渗透压和动力粘度
60.样品编号ph渗透压动力粘度样品17.1280mosm/kg1158mpa
·
s样品26.9320mosm/kg1526mpa
·s61.(三)、测定医用几丁糖的红外吸收峰
62.方法:取样品1和样品2各3g,置于含适量无水乙醇的烧杯中,用玻璃棒轻轻搅拌,至样品全部变成白色絮状沉淀,取出白色沉淀至称量瓶中,置于60℃烘箱中烘干。采用kbr压片法制样,按傅里叶红外光谱仪的操作方法进样检测。结果如图1所示。
63.如图1所示,结果表明,医用几丁糖的傅里叶红外光谱在3250-3450cm-1
、2910-2950cm-1
、1600cm-1
具有特征吸收峰。
64.(四)、测定医用几丁糖的二甘醇酸残留
65.供试品溶液的制备:精密称取样品1g,用流动相溶解定容至10ml,同法制备另一份样品作为平行样。
66.标准溶液的制备:精密称取二甘醇酸标准品0.1g,置100ml容量瓶中,用流动相溶解并稀释至刻度,摇匀,得到1mg/ml的二甘醇酸标准储备液。临用前,再用流动相稀释成10μ
g/ml的对照品溶液。
67.测定方法:精确量取20μl对照品和供试品进注入液相色谱仪,记录二甘醇酸的峰面积。根据对照品溶液峰面积按外标法计算出供试品中二甘醇酸的浓度,结果如表2所示:
68.表2医用几丁糖的二甘醇酸
69.样品编号二甘醇酸对照品1100μg/g对照品2110μg/g样品150μg/g样品261μg/g
70.与对照组相比:p》0.05
71.对照品1和对照品2除未超声,其它工艺均不变
72.(五)、测定医用几丁糖的溶剂残留
73.精密称取乙醇0.1g置100ml容量瓶中,加纯化水溶解并稀释至刻度,摇匀,得乙醇浓度均约为1mg/ml的标准储备液。再用纯化水稀释成约200μg/ml的对照品溶液。取样品1g,精密称定,置20ml顶空瓶中,准确加入纯化水1.0ml,混合均匀。另精密量取乙醇对照品溶液1.0ml,置20ml顶空瓶中,准确加入纯化水1.0ml,混合均匀。在80℃的顶空箱中加热30min,抽取顶空气体,在规定的色谱分析条件下,注入气相色谱仪,待乙醇色谱峰流出后,量取乙醇峰的面积,以峰面积作为外标的定量标准,结果如表3所示:
74.表3医用几丁糖的乙醇残留
75.样品编号乙醇残留对照品11.9%对照品22.1%样品10.01%样品20.02%
76.与对照组相比:p》0.05
77.对照品1和对照品2除干燥工艺(只鼓风干燥),其它工艺均不变
78.(六)、测定医用几丁糖的细胞相容性
79.采用小鼠成纤维细胞l-929来评价材料的细胞毒性。取样本1和样本2各1ml,加细胞培养液29ml稀释制备样本供试液。将细胞消化后,用细胞液培养配制成一定浓度的细胞悬液供试验用。在12孔细胞培养板中分别加入每孔细胞悬液3ml,置二氧化氮培养箱培养至单层细胞形成。弃去原培养液,分组加液2.5ml。阴性对照组3孔用不锈钢材料浸提液交换,阳性对照组3孔用10%dmso溶液交换,样品1和样品2各3孔用样本材料浸提后在二氧化碳培养箱中继续培养24h。
80.结果如表4所示,表明医用几丁糖具有较好的生物相容性,不具有细胞毒性。
81.表4医用几丁糖的细胞毒性
82.样品编号细胞毒性结果阳性组细胞呈圆缩,脱落死亡,重度细胞毒性阴性组细胞形态正常,生长良好,无细胞毒性
样品1细胞形态正常,生长良好,与阴性对照组无明显差异,无细胞毒性样品2细胞形态正常,生长良好,与阴性对照组无明显差异,无细胞毒性
83.(七)、动物实验评估医用几丁糖用于关节腔注射治疗骨关节炎的有效性
84.采用兔前交叉韧带切断术建立骨关节炎模型,术后5周将动物分成4组,分别为阴性对照组、模型对照组、上市对照组、供试品组,模型建立后,供试品组和上市对照组实验兔手术侧关节腔注射分别注射样品1及某上市产品,每两周注射1次,0.5ml/次,二次一个疗程;阴性对照组和模型组关节腔注射0.9%的氯化钠溶液。
85.术后40天处死动物,收集血液检测血常规和血生化,收集关节液检测no含量,大体观察动物手术关节活动角度,关节软骨面磨损情况与he病理检测。观察免疫器官功能与重量变化,以判断骨关节炎模型与治疗对免疫功能的影响。
86.结果显示,骨关节炎模型能够明显增高关节液no的含量,样品1和已上市对照能在一定程度上回调这一升高的现象。经治疗后动物活动能力均得到一定程度的恢复。两组产品均能在一定程度上改善关节损伤,降低损伤评分。
87.表5医用几丁糖对兔关节炎的治疗作用研究关节液no含量检测
88.组别关节液no含量(μmol/l)阳性对照组32.707
±
20.398模型对照组64.507
±
28.634**上市对照组55.546
±
30.022供试品组(样品1)51.477
±
26.095
89.与阴性对照组对比:**p《0.01
90.通过称取实验兔体重、胸腺、淋巴结与脾脏,计算其胸腺指数、淋巴结指数、脾脏指数,进而评价骨关节炎模型组与上市对照组、供试品组对兔免疫功能的影响。结果显示,模型对照组与阴性对照组相比并无显著变化。与模型对照组相比,上市对照组与供试品组无显著变化。试验结果说明,骨关节炎造模未对兔免疫功能产生明显的影响。(见表6)
91.表6医用几丁糖对家兔关节炎的治疗作用研究(脏器指数)
[0092][0093][0094]
与阴性对照相比:p》0.05。
[0095]
通过量取实验兔膝关节活动角度及数据统计分析可见,模型对照组较阴性对照组活动角度显著减少。与模型对照组相比,注射医用几丁糖后,活动角度显著增大,说明
[0096]
骨关节炎模型建立能显著减少兔后肢踝关节活动能力,而医用几丁糖注射后能使其活动能力得到一定程度的恢复,结果如表7,图2和图3为动物试验照片。
[0097]
表7医用几丁糖对兔关节炎的治疗作用研究膝关节活动角度检测
[0098]
组别膝关节活动角度(
°
)模型对照组127
±
3.1阴性对照组113
±
3.0*上市对照组127
±
3.1供试品组(样品1)125
±
3.1
[0099]
与阴性对照组对比:*p《0.05;与模型对照相比:
#
p《0.05,
##
p《0.05。
[0100]
以上结果表明,本发明方法制备的用于关节腔注射的医用几丁糖产品,具有良好的生物相容性,对骨关节炎具有一定的治疗作用,有望早日应用于临床骨科领域。
[0101]
(八)、评估医用几丁糖对猪关节软骨的润滑效果
[0102]
首先剥离猪关节软骨,厚度约1.8mm,使用cetr umt疲劳磨损试验机在往复频率1hz和5n载荷下,测量了在不同润滑剂下(包括干摩擦组、生理盐水组、玻璃酸钠组和医用几丁糖组)猪关节软骨与抛光不锈钢球形头(直径22mm)之间的摩擦力,分别计算出在不同润滑剂下的摩擦学系数,结果如下表:
[0103]
表8对猪关节软骨润滑效果影响
[0104][0105][0106]
与生理盐水组相比:p》0.05。
[0107]
由结果可知,在摩擦损耗试验机上,猪关节软骨在医用几丁糖下的润滑效果优于玻璃酸钠,因此本品可作为骨关节内的润滑剂用于关节润滑、保护关节软骨、辅助骨关节病的治疗。
[0108]
上述实施例仅为说明本发明的原理,而非限制本发明。在本发明权利要求所限定的精神和范围内可对其进行许多改变,修改,但都将在本发明的保护之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1