用于评估患者眼睛中疾病或病症的活动水平的计算机实施的系统和方法与流程
1.本发明涉及一种用于自动评估患者眼睛中的疾病或病症的活动水平的计算机实施的方法,例如其中,所述疾病是导致眼睛的视网膜的和/或视网膜附近的新生血管形成的新生血管性眼部疾病。
2.基于所述评估,所述方法可以因此自动输出关于疾病活动水平的信息、与这种疾病活动有关的特征、和/或对眼睛进行医疗干预的最佳时机,诸如治疗疾病或病症的药物注射的最佳时机。所述信息可以包括按照所批准的药物剂量学的给药频率、患者就诊以执行下一次干预的时机等。
3.具体地,根据本发明的计算机实施的方法基于所述评估生成并输出与疾病的活动水平相对应的疾病活动分数,其中,所述疾病活动分数还可以与有效地将用于治疗患者眼睛疾病的药物的当前给药方案切换为其不同的给药方案的概率或适当性相关。
4.本发明还涉及一种被设计为执行所述方法的计算系统,其中,所述计算系统包括计算设备,所述计算设备包括一个或多个处理器;一个或多个输入元件;存储器;以及存储在存储器中的包括用于实施所述方法的指令的一个或多个程序。
5.本发明进一步涉及一种非暂态计算机可读存储介质,其存储有一个或多个程序,所述一个或多个程序被配置成由具有一个或多个输入元件的电子设备的一个或多个处理器执行,所述一个或多个程序包括用于执行上述计算机实施的方法的指令。
6.根据本发明的计算机实施的方法适用于训练机器学习算法,以评估受眼睛视网膜的和/或视网膜附近的新生血管形成的影响、特别是受年龄相关性黄斑变性的影响、并且尤其是受湿性年龄相关性黄斑变性(也可称为w-amd)影响的患者的疾病活动。在下面的
背景技术:
部分给出了本发明意义上的新生血管性眼部疾病的定义。
7.基于所述评估,根据本发明的计算机实施的方法所依据的算法支持实现临床决策的给药系统,所述系统向治疗这种影响视网膜疾病(特别是通过抗血管内皮生长因子(抗vegf)药物治疗湿性年龄相关性黄斑变性(w-amd))的医疗保健提供者或医师提供了精确且智能的疾病活动评估以及给药频率指导。
背景技术
8.通常,视网膜病变包括几种视网膜血管疾病,这些疾病最终可能会导致视力障碍。特别地,以下解决了对导致眼睛的视网膜的和/或视网膜附近的新生血管形成的新生血管性眼部疾病的治疗。其中,新生血管性年龄相关性黄斑变性(或namd)也称为“渗出性”或“湿性(wet)”amd(也由w-amd表示),是一种慢性眼睛障碍,其特征是新脉络膜血管的异常形成并在视网膜色素上皮(rpe)下或视网膜下空间中生长,从而影响了眼睛中视网膜的中央区域,所述中央区域称为黄斑,负责中心视力和看到细节。这会导致视力模糊、波浪线、颜色暗淡、盲点、并最终导致严重的视力丧失。
9.以非详尽示例的方式,其他视网膜病变也包括糖尿病性视网膜病变(dr);糖尿病
性黄斑水肿(dme);近视脉络膜新生血管形成(mcnv);视网膜静脉阻塞(rvo)后黄斑水肿;早产儿视网膜病变(rop)。
10.如本文所使用的,术语“新生血管性眼部疾病”是指与眼部新生血管形成相关的病症、疾病、或障碍。可以使用本披露内容的方法治疗的“新生血管性眼部疾病”包括与眼部新生血管形成相关的病症、疾病、或障碍,其包括但不限于:异常血管生成、脉络膜新生血管形成(cnv)、与w-amd相关的脉络膜新生血管形成(cnv)、视网膜血管通透性、视网膜水肿、糖尿病性视网膜病变(特别是增生性糖尿病性视网膜病变(pdr)和非增生性糖尿病性视网膜病变(npdr))、黄斑水肿(me)、糖尿病性黄斑水肿(dme)、新生血管性(渗出性)年龄相关性黄斑变性(w-amd)、与视网膜缺血相关的后遗症、视网膜静脉阻塞(rvo)、视网膜中央静脉阻塞(crvo)、视网膜分支静脉阻塞(brvo)、视网膜静脉阻塞后黄斑水肿、和后段新生血管形成。
11.如今尤其是通过在受影响的眼睛中注射抗血管内皮细胞生长因子或抗vegf药物(也称为vegf抑制剂)来治疗受上述视网膜病变影响的患者。抗血管内皮细胞生长因子药物包括例如雷珠单抗、阿柏西普和布洛赛珠单抗-dbll,后者特别适合于治疗湿性年龄相关性黄斑变性或w-amd。
12.接受抗vegf疗法以治疗上述视网膜病变的患者需要定期拜访医疗保健专业人员,以进行疾病监测和再治疗。进一步地,很难在患者水平上预测如w-amd疾病活动等疾病活动的模式以及通过注射对抗vegf药物的所需相关施用的模式。
13.一些起作用的抗vegf剂是长效的,由此使得对接受治疗的患者的监测变得困难。此外,难以预测从当前给药方案切换为不同给药方案的效果如何。
14.在许多情况下,这些问题会导致对患者的如w-amd等视网膜病变的治疗不足和/或增加患者的负担,例如以不必要的注射和/或多余的医疗保健专业人员就诊的形式。
15.迄今为止,在现实世界的实践中,对w-amd患者或受上述视网膜病变之一影响的患者进行管理存在许多挑战。在定期就诊期间眼科医生为这些患者提供咨询的时间有限,并且经常需要在不完全知情的情况下快速做出给药决策。辅助临床医生做出给药决策的信息通常不容易获得,例如由于图像分割和视网膜液体的体积测定是有限的和/或没有对疾病活动进行量化。总而言之,疾病活动评估和给药决策可能是复杂的,并且在不同的眼科医生之间可能存在关于在个体病例中最佳给药的构成内容的差异并且在患者间可能存在表型差异。
16.目前没有成熟合理的基于计算机的全自动程序来管理受w-amd或其他视网膜病变影响的患者的治疗,改进他们的治疗,同时还减轻重复就诊带来的对患者独立性和生活质量的影响的相关负担。
17.因此,需要可靠且准确地评估w-amd的和/或其他视网膜病变的疾病活动并提供如定制化的给药频率模型等患者特定的抗vegf治疗方案模型的方法。
技术实现要素:
18.根据本发明,该需求通过一种用于对患者的至少一只眼睛中疾病或病症的活动水平、包括疾病或病症的存在或不存在进行评估的计算机实施的方法来解决,其中,所述疾病是新生血管性眼部疾病。
19.这种疾病活动水平的评估由计算机实施的系统通过使用非暂态计算机可读存储
介质来自动执行。前述各项均由一个或多个所附权利要求限定。
20.根据本发明的方法允许通过施用所开的药物(例如,通过注射在患者的受影响的眼睛中)来最佳地个体化治疗间隔,以更好地保护患者的视力并同时促进患者的独立性和更好的生活质量。
21.通过易于使用的专家系统模拟经验丰富的视网膜专家的决策制定来随时随地优化决策,可以以最低的患者和医疗保健专业人员负担来高效地保护患者的视力。还可以有利地集中所有用于指导疾病活动评估和给药决策的相关信息。
22.如所提到的,所述方法可以在包括一个或多个处理器、存储器、一个或多个输入元件和/或输出元件的一个或多个计算设备上实施。
23.所述方法的以及由其实施生成的模型的主要输出是与待治疗的疾病的活动水平相对应的疾病活动分数。这种疾病活动分数或da分数用于评估疾病活动水平,所述疾病活动水平可以进一步分为高或中等或低。
24.疾病活动分数可以被认为是衡量待治疗疾病的潜在可逆方面在患者中存在的程度的指数,所述程度可基于如患者的一个或多个解剖变量和功能变量的值等输入患者数据检测到。
25.疾病活动分数可以进一步与将用于治疗患者的眼睛疾病的药物的当前给药方案切换为其不同的给药方案的适当性相关。因此,就通过给药方案切换分别实现较低或较高的疾病活动分数而言,疾病活动分数也可以与这种给药方案切换的预期成功或失败相关联。
26.因此,根据本发明的方法不仅可以产生与当前疾病活动相关的分数,而且可以产生由于从用于治疗患者眼睛疾病的药物的当前给药方案改变到其不同的给药方案而产生的疾病活动变化的预测,即,在相对于当前给药方案而言在更频繁或更不频繁的给药方案下的疾病活动的预测。
27.疾病活动分数可以由本发明的方法的实施例输出为表征疾病活动水平的数值,例如以供由被提供疾病活动分数的参考清单的医疗专业人员进行解释;或者输出为针对医疗保健专业人员的或者替代性地说明需要审查当前给药方案的警告消息;或者输出为仅当所计算的水平超过预设阈值时才会触发并发出的警报。例如,疾病活动分数以及可能地与其相关联的置信度或不确定性统计值可以在连接到实施本方法的计算机系统的设备的显示屏上进行可视化,优选地借助于直观地传达疾病活动水平并指导由医疗保健专业人员做出的给药决策的图形用户界面。
28.根据本发明的方法包括经由一个或多个输入元件接收与患者相对应的输入患者数据集的步骤。输入患者数据集包括患者的至少一个或多个视网膜图像、优选地患者眼睛的光学相干断层扫描(oct)图像。
29.上述输入患者数据集包括需要对其与上述给定视网膜病变之一相关的疾病活动水平进行评估的特定患者的真实世界数据。除了视网膜图像之外,在本发明的实施例中,输入患者数据集可以进一步包括非成像导出的临床输入患者数据,诸如:纵向患者眼睛数据,例如最佳矫正视敏度;和/或患者病史信息和/或捕获特定患者的不一定与眼睛病症直接相关的一些生理特性的患者纵向数据;和/或基线人口统计数据,诸如被检查患者的年龄、体重、性别、种族等。与患者相关的纵向数据可以是在例如从治疗开始后的第0周到目标第16
周或20周的一段时间内以例如2周或4周间隔收集的被监测患者的数据。
30.通常,输入患者数据集将反映适合描述患者健康状况的多个输入变量或特征或参数,这些变量或特征或参数体现或存储在通过根据本发明的用于对患者双眼的至少一只眼睛中疾病的活动水平、包括疾病的存在或不存在进行评估的方法实施的算法中。
31.在本发明的实施例中,输入患者数据集可以至少包括在初级或二级护理服务处、在评估日期前的第一索引日期作出的对影响患者眼睛的视网膜的疾病或病症的诊断。这样的疾病或病症可以是以下列出的疾病或病症中的一种或多种:湿性年龄相关性黄斑变性,也可称为w-amd;糖尿病性视网膜病变,也可称为dr;糖尿病性黄斑水肿,也可称为dme;近视脉络膜新生血管形成,也可称为mcnv;视网膜静脉阻塞(也可称为rvo)后黄斑水肿;早产儿视网膜病变,也可称为rop。
32.纵向患者数据输入类型的示例包括:最佳矫正视敏度(bcva);中心子区中央凹厚度(csft);玻璃疣面积和/或体积;玻璃疣概率;视网膜前膜厚度;视网膜前膜概率;纤维色素上皮脱离概率;地图状萎缩面积和/或体积;地图状萎缩概率;健康概率(未检测到异常或生物标志物);高反射灶和硬渗出物概率;外层视网膜萎缩面积和/或体积;外层视网膜萎缩概率;网状假玻璃膜疣面积和/或体积;网状假玻璃膜疣的概率;在预定区域(例如,1mm、3mm和/或6mm区域)中的神经节细胞层和内丛状层体积;在预定区域(例如,1mm、3mm和/或6mm区域)中的内核层和外丛状层体积;在预定区域(例如,1mm、3mm和/或6mm区域)中的视网膜内液和囊肿体积;在预定区域(例如,1mm、3mm和/或6mm区域)中的外核层体积;在预定区域(例如,1mm、3mm和/或6mm区域)中的色素上皮脱离体积;在预定区域(例如,1mm、3mm和/或6mm区域)中的光感受器和视网膜色素上皮体积;在预定区域(例如,1mm、3mm和/或6mm区域)中的视网膜神经纤维层体积;以及在预定区域(例如,1mm、3mm和/或6mm区域)中的视网膜下液体积。
33.如所提到的,在本发明的实施例中,可以例如在目标评估日期之前的预设时间段内根据时间顺序来构造输入患者数据。例如,在对受治疗患者进行监测期间,可以考虑这样的时间段,即,0周、4周、8周、12周、一直到固定为从患者治疗开始的例如16周的目标评估日期。这样的预设时间段可以捕获并解释治疗期间可能的模式和依赖性。
34.在一些实施例中,上述患者数据输入中的一个或多个数据输入的值是从一个或多个其他数据输入值中确定或导出的。在一些示例中,上述一个或多个数据输入的一个或多个值基于所接收的oct图像,例如,基于在oct图像中捕获的解剖特征的尺寸。
35.oct图像也可以由位于临床医生办公室或患者家中的oct设备生成。在各个实施例中,作为对标准oct的增强,可以例如通过光谱域光学相干断层扫描(sd-oct)成像设备来生成图像。
36.根据本发明的方法进一步包括将用于成像数据分析的第一算法应用于作为输入患者数据集的一部分接收的一个或多个视网膜图像的步骤。
37.在一些实施例中,第一算法可以是用于图像分割的机器学习模型或制品,其例如通过将机器学习算法应用于历史患者图像数据集而生成。但是,第一算法还可以替代性地是在没有机器学习辅助的情况下开发的明确编码的常规算法。
38.根据本发明的方法进一步包括基于接收到的患者的视网膜图像来识别患者眼睛的一个或多个解剖变量或特征的值的步骤。
39.以示例的方式,这种解剖变量的值可以是以下各项的任意组合:中央视网膜厚度和/或体积的值;视网膜间液体积的值;视网膜下液体积的值;色素上皮脱离(也表示为ped)的值;玻璃疣、纤维血管或浆液性ped的值;高反射灶的值;椭圆体区缺陷的值;外界膜带缺陷的值;视网膜色素上皮萎缩的值。
40.可以识别其值以在本方法的实施方式中考虑的其他解剖变量可以是:中心子区中央凹厚度(csft);神经节细胞层和内丛状层;内核层和外丛状层体积;囊肿体积;外核层体积;色素上皮脱离体积;光感受器和视网膜色素体积;视网膜神经纤维层体积。
41.在一些示例中,液体是w-amd中疾病活动的有用生物标志物,因此,原则上,在一些示例中,液体可以作为诊断和管理建议的基础。示例包括视网膜内液(irf)、视网膜下液(srf)和/或视网膜下色素上皮(rpe)液。在本发明的实施例中,液体可以是在评估疾病活动水平并做出是维持固定的治疗方案还是转向治疗并延长给药时间表的决策时要考虑的变量或特征。
42.在一些实施例中,视网膜液体、疾病活动评估和治疗频率表现出相关性。
43.在一些实施例中,视网膜厚度——尤其是厚或异常薄的视网膜——可以是疾病活动评估和治疗考虑以及结果确定中的因素。视网膜厚度可能是非常重要的变量或特征,对最终算法输出有相当大的影响。
44.根据本发明的方法进一步包括将第二算法应用于识别的一个或多个解剖变量的值以及包括在输入患者数据集中的非图像导出的不同临床输入患者数据的步骤。以上已经提供了非图像导出的不同临床输入患者数据的示例。
45.对于给定患者,第二算法的应用允许相对于当前评估之前同一患者的就诊来考虑所识别的解剖变量的和/或非图像导出的不同患者数据的水平和变化。
46.因此,第二算法的应用可以实现估计视敏度损失或增益;视网膜厚度损失或增益的速率;视网膜内液体积损失或增益的速率。
47.第二算法也可以是通过在历史患者数据集上训练一个或多个机器学习算法而生成的机器学习模型或制品,所述历史患者数据集至少包括例如从临床试验中导出的一个或多个识别的解剖变量的值。如所提到的,一个或多个识别的解剖变量的值优选地用历史患者数据的值来补充,所述历史患者数据诸如是患者人口统计和/或病史和/或伴随用药和/或合并症和/或不良事件和/或严重不良事件。
48.相应地,在一些实施例中,所述第二算法是由包括多个输入变量的一个或多个机器学习算法生成的疾病活动评估模型,所述多个输入变量与所述一个或多个识别的解剖变量以及所述非图像导出的不同临床输入患者数据相对应。一个或多个机器学习算法是在来自被诊断患有被评估的疾病的多个历史患者的历史患者数据集上训练的。
49.在这种情况下,历史患者数据集包括:一个或多个识别的解剖变量的输入值,这些输入值是从登记在专门执行例如以用于确认抗vegf药物的作用的临床试验中的多个历史患者中的每一个的视网膜图像中识别和量化的;和/或包括与多个历史患者中的每一个的上述非图像导出的临床输入患者数据相关的值,所述非图像导出的临床输入患者数据包括历史患者的人口统计和/或病史和/或伴随用药和/或合并症和/或不良事件和/或严重不良事件。临床试验可以以传统方式运行和/或经由收集患者数据的设备和/或传感器来远程运行。
dbll),针对将当前治疗方案切换为施用频率为8周间隔的第二给药方案的情况,预测疾病活动变化;反之亦然。
60.在其中确定疾病活动变化的预测的各个实施例中,疾病活动分数可以与在不同给药方案之间切换的概率或适当性相关、或与同所述切换相关的疾病活动变化的概率预测相关。此外,确定疾病活动变化的预测可以基于预测一个或多个识别的解剖变量之一在一段时间(此时已经从当前第一给药方案改变到第二给药方案)内的生理变化,所述生理变化例如一段时间内视网膜厚度和/或体积损失或增益的量;和/或一段时间内视敏度损失或增益的速率;和/或一段时间内视网膜内液体积损失或增益的速率。
61.在其中给药方案包括用一定剂量的药物治疗患者的药物施用频率的各个实施例中,根据本发明的方法可以进一步包括使用第三算法生成药物施用频率建议的步骤。药物施用频率建议可以基于识别的一个或多个解剖变量的值和/或总的疾病活动分数。所述第三算法可以与第二算法基本一致或包括在第二算法中;或者它可以是不同于第二算法的附加算法。
62.在各个实施例中,所述药物施用频率建议包括选自由以下各项组成的组中的参数:
[0063]-给药频率间隔,例如,随后的注射之间经过了多少周;
[0064]-下一次给药日期;
[0065]-下一次药剂量;
[0066]-下一次视网膜成像日期;
[0067]-用于医疗保健提供者对所述患者进行监测的下一次就诊日期;和/或
[0068]-其组合。
[0069]
在一些实施例中,生成上述药物施用频率建议可以包括以下步骤:使用第三算法生成不同的给药方案的治疗结果的一个或多个概率模拟;以及基于治疗结果的这种概率模拟最终生成药物施用频率建议。例如,模拟的治疗结果可以是视敏度增益和/或对一个或多个识别的解剖变量(比如视网膜内液体积损失)的治疗效果。这些概率模拟可以考虑先前生成并输出的疾病活动分数和/或药物施用频率建议。
[0070]
第三算法还可以用于基于所生成的药物施用频率建议来预测时间依赖性视敏度增益。因此,可以预测,如果根据所生成的药物施用频率建议进行治疗,患者的视敏度在给定一段时间内将改善多少。
[0071]
在各个实施例中,例如馈送到第二算法的输入患者数据集进一步包括选自由以下各项组成的组中的数据:关于视敏度的患者纵向数据,例如当前和先前的斯内伦视力表测量结果;关于生理特性的患者纵向数据,例如当前和先前的年龄、体重等;既往疾病活动分数;既往药物施用频率建议;和/或其组合。
[0072]
优选地,用于根据本发明治疗患者的眼睛疾病的药物是抗血管内皮生长因子药物,也可称为抗vegf药物,所述药物包括具有多种作用模式的药物,其中至少一种模式是抗vegf(例如,包括抗vegf活性的双特异性抗体)。
[0073]
在一些实施例中,用于训练本发明方法的机器学习算法的历史数据集的临床试验数据部分包括与一种或多种抗vegf药物及其对一个或多个识别的解剖变量中的至少一个的效果相关联的数据。
[0074]
在各个实施例中,患者的眼睛疾病是以下各项之一:
[0075]-湿性年龄相关性黄斑变性,也可称为w-amd;
[0076]-糖尿病性视网膜病变,也可称为dr,包括增生性糖尿病性视网膜病变(pdr)和非增生性糖尿病性视网膜病变(npdr);和/或
[0077]-糖尿病性黄斑水肿,也可称为dme;和/或
[0078]-近视脉络膜新生血管形成,也可称为mcnv;和/或
[0079]-视网膜静脉阻塞(也可称为rvo)后黄斑水肿,包括视网膜中央静脉阻塞(crvo)和视网膜分支静脉阻塞(brvo);和/或
[0080]-早产儿视网膜病变,也可称为rop。
[0081]
本发明还涉及一种包括计算设备的系统,所述计算设备包括:一个或多个处理器;一个或多个输入元件和/或输出元件;存储器;以及存储在所述存储器中的一个或多个程序。所述一个或多个程序包括用于执行上述方法的指令。
[0082]
此外,本发明还涉及一种非暂态计算机可读存储介质,其存储有一个或多个程序,所述一个或多个程序被配置成由计算系统的一个或多个处理器执行,其中,所述一个或多个程序包括用于执行上述方法的指令。
[0083]
在一些实施例中,可以对根据本发明的方法进行修改,以将一种算法同时应用于一个或多个视网膜图像数据分量和非图像数据分量二者,以便对所述患者的所述至少一只眼睛中所述疾病的所述活动水平和/或所述疾病相对于先前为所述患者确定的活动水平而言的进展或消退来作出评估。这种情况可以尤其应用于其中未指定分割视网膜结构或评估疾病活动或提供给药建议的确切步骤的采用单个神经网络架构的方法。在这种实例中,深度学习功能不是被指派来识别软件开发人员预定义的特征,而是它是特征不可知的并且自主地搜索特征,以最终实现量化疾病活动和告知医疗干预(包括给药频率)的最佳时机的目标。
[0084]
在机器学习算法用于产生用于疾病活动评估和给药建议的人工智能引擎的情况下,在通过将例如第二机器学习算法应用于历史患者数据集来对其进行训练时,根据本发明的方法可以包括在整个算法中或者在算法的一个或多个步骤中选择性地使用或不使用包括在第二机器学习算法中的输入变量的步骤。
[0085]
因此,每个输入变量对预测的贡献程度不同,并存储在相应的模型中。这可以通过重要性矩阵来表征,其中,机器学习算法中实际使用的每个变量都与通过采用给定重要性指标的计算得出的相应的“重要性”值或权重相关联。
[0086]
在各个实施例中,第一算法和/或第二算法和/或第三算法是机器学习生成的模型,包括如lightgbm算法或xgboost算法等梯度提升决策树算法;和/或决策树的聚合,诸如贝叶斯加性回归树(bart);和/或循环神经网络(rnn)算法。
[0087]
xgboost是基于决策树的集成机器学习算法,其使用梯度提升框架。xgboost是并行化的树学习算法。每个树都由多个分支组成,其中,数据集对应于所选变量和拆分值进行拆分。在这个变量上添加拆分后,将创建两个新分支。拆分的数量常规上设置为较小的数字(如3至10),这限制了单个树准确地拟合函数的能力。但是如果将许多树(集成)进行组合,就可以设计出非常准确的分类器。在提升算法中,每个树都旨在与先前树所执行的相比更好地适应实例。
[0088]
lightgbm也是梯度提升框架,其使用基于树的学习算法。light gbm垂直生长树,而其他算法水平生长树,这意味着light gbm逐叶(leaf-wise)生长树,而其他算法逐层(level-wise)生长。它将选择具有最大增量损失(delta loss)的叶来生长。当生长相同的叶时,逐叶增长算法可以比逐层增长算法减少更多的损失。lightgbm的优势在于更高的处理速度,并专注于针对更大数据集的准确性。
[0089]
贝叶斯加性回归树(bart)模型整合了多个决策树,其中,每个树都被正则化先验约束为弱学习者,并且拟合和推理是经由从后验生成样本的迭代贝叶斯反向拟合mcmc算法完成的。实际上,bart是使用维度自适应随机基元的非参数化贝叶斯回归方法。类似于通常的集成方法、并且特别是提升算法,bart是由整合了先验和似然两者的统计模型定义的。这种方法实现完整的后验推理,其包括未知回归函数的点和区间估计以及潜在预测因子的边际效应。
[0090]
可以使用适当的k折叠交叉验证方法来优化模型超参数(例如,将数据分成k=4部分并训练4个模型,每次在的数据上进行训练并评估剩余的性能),同时确保来自同一患者的数据总是在训练或验证折叠中。
[0091]
通过根据本发明的方法实施的适用于评估患者眼睛的疾病活动水平的上述梯度提升决策树算法有效地从加权输入变量中找到最佳拆分点。以示例的方式,相对变量重要性度量可以基于变量被选择进行分裂的次数,通过每次拆分对模型产生的改进来加权,并且对所有树进行平均。
[0092]
在根据本发明的方法的各个实施例中,采用指标“增益”来建立相对变量重要性。增益可以定义为变量的属性,并且它表明对应的变量对模型的相对贡献,通过取每个变量对模型中每个树的贡献来计算得出。与不同的第二变量相比,给定第一变量的这个指标的值越高,表明第一变量对于生成评估或预测越重要。“增益”实质上是由变量为其所在的树分枝带来的准确性的提高。在一些实施例中,增益被实施为夏普利值(例如参见表1)。在一些实施例中,增益被实施为其他方法,例如,夏普利加性解释(shapley additive explanations,shap)。
[0093]
循环神经网络(rnn)是一类使用顺序数据或时间序列数据的人工神经网络。它们具有能够捕获按顺序存储的所有信息的内部存储器,从而从先前的输入中获取信息以影响当前的输入和输出。因此,rnn足够强大,可以利用相对较长的序列中的信息,因为它们可以对序列中的每个数据输入执行相同的任务,而当前输入的输出取决于先前的计算。
附图说明
[0094]
下面通过示例性实施例并参考附图在本文中更详细地描述根据本发明的方法和系统,在附图中:
[0095]
图1展示了用于生成并利用机器学习模型的示例性系统,其对导致患者眼睛的视网膜和/或视网膜附近的新生血管形成的疾病的活动水平、包括疾病的存在或不存在进行评估;
[0096]
图2展示了根据一些实施例的示例性机器学习系统;
[0097]
图3展示了根据一些实施例的示例性电子设备;
[0098]
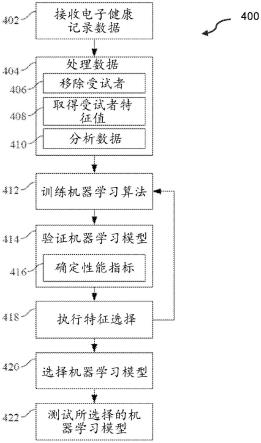
图4展示了对用于对患者眼睛疾病的活动水平进行评估的一个或多个机器学习模
型进行训练、验证并测试的示例性过程;
[0099]
图5展示了信息流的高级图,从患者获取输入患者数据集以及随后通过实施根据本发明的方法的基于ai的临床决策支持软件对这种数据进行细化,从而向医疗保健提供者或医师输出治疗建议;
[0100]
图6展示了用于训练图5的基于ai的临床决策支持软件的示例性历史数据集的代表性部分,包括与第一8周负荷阶段内的以及随后另外8周治疗阶段(直至目标第16周,其中由蒙面研究人员进行第一疾病活动评估)内的患者就诊有关的给定患者的匿名电子健康记录;
[0101]
图7示出了图5的基于ai的临床决策支持软件的第一方法和第二方法的示意性表示;
[0102]
图8示出了用于图7的基于ai的临床决策支持软件的第二方法的示例工作流;
[0103]
图9展示了通过图5的基于ai的临床决策支持软件得到的示例性输出数据集的代表性部分,所述输出数据与由数字2至9标识的对应8名匿名患者在目标治疗第16周的疾病活动分数相关;
[0104]
图10展示了例如在医疗保健专业人员的或眼科医生的前端处的图形用户界面的一部分,显示了由图5的基于ai的临床决策支持软件输出的数据,其中,所显示的数据提供了患者的当前疾病活动分数的视觉再现;
[0105]
图11展示了与图10类似的图形用户界面的一部分,其中,所显示的数据针对被检查患者提供了合适给药方案的指导,尤其示出了可以预测患者眼睛的疾病活动水平会如何由于将注射到所述患者眼睛中的抗vegf药物的两种不同的给药方案之间的变化而发生变化;
[0106]
图12展示了图11的图形用户界面的另一部分,其中,呈现了影响患者的疾病活动评估的解剖特征和功能特征的相对重要性,以作为对眼科医生的另一解释性指导;
[0107]
图13展示了图10的图形用户界面的另一部分,其中,跨治疗的负荷阶段以及随后的维持阶段随时间示出了被检查患者的疾病活动分数。
具体实施方式
[0108]
在以下描述中,某些术语是出于方便的原因而被使用,而不旨在限制本发明。术语“右”、“左”、“上”、“下”、“下面”和“上方”指的是图中的方向。术语包括明确提及的术语以及它们的派生词和具有相似含义的术语。另外,可以在本文中使用如“之下”、“下方”、“下部”、“上方”、“上部”、“近端”、“远端”等空间相对术语,以描述如附图中所展示的一个元件或特征相对于另一元件或特征的关系。这些空间相对术语意在涵盖设备在使用或者操作中除附图中所示的位置和取向之外的不同位置和取向。例如,如果倒转附图中的设备,那么被描述为在其他元件或特征“下方”或“之下”的元件则在其他元件或特征的“上方”或“之上”。因此,示例性术语“下方”可以涵盖在上方和下方两种位置和取向。设备可以被以其他方式定向(旋转90度或者其他取向),并且本文中使用的空间相对的描述词被相应地解释。
[0109]
同样,对沿着和围绕各种轴的运动的描述包括各种特殊的设备位置和取向。
[0110]
为了避免在附图和对各个方面以及说明性实施例的描述中的重复,应当理解许多特征对于许多方面和实施例是共同的。从描述或附图中省略一方面并不意味着所述方面从
包含该方面的实施例中缺失。相反,为了清楚起见并避免冗长的描述,所述方面可能已经被省略。在这种上下文下,以下内容适用于本说明书的其余部分:如果为了阐明附图,一个图包含未在说明书的直接相关部分中解释的附图标记,则参考之前或之后的描述部分。进一步地,为了清晰起见,如果在一个附图中没有为零件的所有特征提供附图标记,则参考示出相同零件的其他附图。在两个或更多个图中的相似的数字表示相同或相似的要素。
[0111]
以下描述阐述了示例性系统、设备、方法、参数等。然而,应当认识到,这种描述并非旨在限制本披露内容的范围,而是作为示例性实施例的描述来提供。例如,参考了附图,在所述附图中,通过图示的方式示出特定示例实施例。应当理解,在不脱离本披露内容的范围的情况下,可以对这种示例实施例作出改变。
[0112]
如本文所使用的,术语“受试者(subject)”或“受试者(subjects)”等同于术语“患者”,并且是指哺乳动物有机体(优选地,人类),其可能被诊断患有所关注的病症(例如,疾病或障碍)并且可能从针对所述病症的治疗中在生物学、医学或生活质量上受益。
[0113]
现在将注意力集中到根据一些实施例的用于执行本文描述的技术的电子设备和系统的示例。参考图1,示出了电子设备(如电子设备300)的示例性系统100。系统100包括客户端系统102。在一些示例中,客户端系统102包括一个或多个电子设备(例如,300)。例如,客户端系统102可以表示医疗保健提供者(hcp)的计算系统(例如,比如大型主机或个人计算机等任何形式的一个或多个计算机),并且可以用于由hcp输入、收集和/或处理受试者数据并且用于输出受试者数据分析(例如,预后信息)。进一步例如,客户端系统102可以表示连接到一个或多个hcp电子设备和/或系统108并且用于输入和收集受试者数据的受试者设备(例如,家用医疗设备;比如智能电话、平板计算机、台式计算机或膝上型计算机等个人电子设备)。在一些示例中,客户端系统102包括(例如,经由局域网)联网在一起的一个或多个电子设备(例如,300)。在一些示例中,客户端系统102包括用于接收受试者数据和/或与一个或多个远程系统(例如,112、126)通信以处理这种受试者数据的计算机程序或应用程序(包括可由一个或多个处理器执行的指令)。
[0114]
客户端系统102经由连接104连接到网络106。连接104可以用于从一个或多个其他电子设备或系统(例如,112、126)传输和/或接收数据。网络106可以包括允许发送和接收通信信号的任何类型的网络,比如无线电信网络、蜂窝电话网络、时分多址(tdma)网络、码分多址(cdma)网络、全球移动通信系统(gsm)、第三代(3g)网络、第四代(4g)网络、第五代(5g)网络、卫星通信网络和其他通信网络。网络106可以包括广域网(wan)(例如,互联网)、局域网(lan)和个域网(pan)中的一个或多个。在一些示例中,网络106包括数据网络的组合、电信网络以及数据网络和电信网络的组合。系统和资源102、112和/或126通过经由网络106发送和接收信号(有线或无线)来彼此通信。在一些示例中,网络106提供对云计算资源(例如,系统112)的访问,所述云计算资源可以是可通过网络106获得的弹性/按需计算和/或存储资源。术语“云”服务通常是指不在用户的设备上本地执行而是从可经由一个或多个网络访问的一个或多个远程设备传递的服务。
[0115]
云计算系统112经由连接108连接到网络106。连接108可以用于从一个或多个其他电子设备或系统传输和/或接收数据,并且可以是任何适合类型的数据连接(例如,有线、无线或有线和无线的任何组合)。在一些示例中,云计算系统112是具有可扩展/弹性计算资源的分布式系统(例如,远程环境)。在一些示例中,计算资源包括一个或多个计算资源114(例
如,数据处理硬件)。在一些示例中,这种资源包括一个或多个存储资源116(例如,存储器硬件)。云计算系统112可以执行对(例如,从客户端系统102接收的)受试者数据的处理(例如,应用一个或多个机器学习模型、应用一个或多个算法)。在一些示例中,云计算系统112托管用于接收和处理受试者数据(例如,来自一个或多个远程客户端系统,比如102)的服务(例如,包括可由一个或多个处理器执行的指令的计算机程序或应用程序)。以这种方式,云计算系统112可以(例如,经由网络106)向多个医疗保健提供者提供受试者数据分析服务。服务可以为客户端系统102提供可在客户端系统102上执行的客户端应用程序(例如,移动应用程序、网站应用程序或包括指令集的可下载程序),或以其他方式使所述客户端应用程序可用。在一些示例中,客户端系统(例如,102)使用应用程序编程接口与云计算系统(例如,112)上的服务器侧应用程序(例如,服务)通信。
[0116]
在一些示例中,云计算系统112包括数据库120。在一些示例中,数据库120在云计算系统112外部(例如,远离其)。在一些示例中,数据库120用于存储受试者数据、算法、机器学习模型或由云计算系统112使用的任何其他信息中的一个或多个。
[0117]
在一些示例中,系统100包括云计算资源126。在一些示例中,云计算资源126向云计算系统112提供外部数据处理和/或数据存储服务。例如,云计算资源126可以如云计算系统112所指导的执行资源密集型处理任务,比如机器学习模型训练。在一些示例中,云计算资源126经由连接124连接到网络106。连接124可以用于从一个或多个其他电子设备或系统传输和/或接收数据,并且可以是任何适合类型的数据连接(例如,有线、无线或有线和无线的任何组合)。例如,云计算系统112和云计算资源126可以经由网络106以及连接108和124进行通信。在一些示例中,云计算资源126经由连接122连接到云计算系统112。连接122可以用于从一个或多个其他电子设备或系统传输和/或接收数据,并且可以是任何适合类型的数据连接(例如,有线、无线或有线和无线的任何组合)。例如,云计算系统112和云计算资源126可以经由连接122进行通信,所述连接是私有连接。
[0118]
在一些示例中,云计算资源126是具有可扩展/弹性计算资源的分布式系统(例如,远程环境)。在一些示例中,计算资源包括一个或多个计算资源128(例如,数据处理硬件)。在一些示例中,这种资源包括一个或多个存储资源130(例如,存储器硬件)。云计算资源126可以执行对(例如,从客户端系统102或云计算系统112接收的)受试者数据的处理(例如,应用一种或多种机器学习模型、应用一种或多种算法)。在一些示例中,云计算系统(例如,112)使用应用程序编程接口与云计算资源(例如,126)通信。
[0119]
在一些示例中,云计算资源126包括数据库134。在一些示例中,数据库134在云计算资源126外部(例如,远离其)。在一些示例中,数据库134用于存储受试者数据、算法、机器学习模型或由云计算资源126使用的任何其他信息中的一个或多个。
[0120]
图2展示了根据一些实施例的示例性机器学习系统200。在一些实施例中,机器学习系统(例如,200)包括一个或多个电子设备(例如,300)。在一些实施例中,机器学习系统包括用于执行与以下中的一个或多个有关的任务的一个或多个模块:训练一种或多种机器学习算法、应用一种或多种机器学习模型以及输出和/或操纵机器学习模型输出的结果。机器学习系统200包括若干示例性模块。在一些实施例中,模块在硬件(例如,专用电路)中、软件(例如,包括由一个或多个处理器执行的指令的计算机程序)中或硬件和软件两者的某种组合中实施。在一些实施例中,下文关于机器学习系统200的模块所描述的功能由本地、远
程或两者的某种组合连接的两个或更多个电子设备执行。例如,下文关于机器学习系统200的模块所描述的功能可以由远离彼此的电子设备执行(例如,系统112内的设备执行数据调控,并且系统126内的设备执行机器学习训练)。
[0121]
在一些实施例中,机器学习系统200包括数据检索模块210。数据检索模块210可以提供与获取和/或接收输入数据以用于使用机器学习算法和/或机器学习模型进行处理有关的功能。例如,数据检索模块210可以与客户端系统(例如,102)或服务器系统(例如,112)接口连接以接收将被处理的数据,包括经由一种或多种通信协议建立通信并管理数据的传送。
[0122]
在一些实施例中,机器学习系统200包括数据调控模块212。数据调控模块212可以提供与准备输入数据以用于处理有关的功能。例如,数据调控可以包括使多个图像大小一致(例如,裁剪、调整大小)、增强数据(例如,获得单个图像并创建稍微不同的变化(例如,通过像素重调、剪切、缩放、旋转/翻转)、外推、变量工程化、过滤和/或清理数据、对从数据库检索的变量的映射和结构化、合并来自不同来源或临床研究点的数据集、按患者分离数据、构建观察性研究文件等。
[0123]
在一些实施例中,机器学习系统200包括机器学习训练模块214。机器学习训练模块214可以提供与训练一种或多种机器学习算法有关的功能,以创建一个或多个经训练机器学习模型。
[0124]“机器学习”的概念通常是指使用一个或多个电子设备来执行一个或多个任务,而无需被明确编程成执行这种任务。机器学习算法可以被“训练”成通过将算法应用于训练数据集来执行一个或多个任务(例如,将输入数据分类为一个或多个类别、对输入数据内的变量进行识别和分类、基于输入数据来预测值),以创建“机器学习模型”(例如,所述机器学习模型可以应用于非训练数据以执行任务)。“机器学习模型”(在本文中也被称为“机器学习模型制品”或“机器学习制品”)是指通过训练机器学习算法的过程创建的制品。机器学习模型可以是输入可以应用于其以获得输出的数学表示(例如,数学表达式)。如本文所指,“应用”机器学习模型可以指使用机器学习模型来处理输入数据(例如,使用输入数据执行数学计算)以获得某种输出。
[0125]
机器学习算法的训练可以包括“监督式”或“非监督式”学习。总体而言,监督式机器学习算法通过处理包括输入数据和期望输出两者的训练数据来构建机器学习模型(例如,对于每个输入数据来说,是对机器学习模型要执行的处理任务的正确回答(也被称为“目标”或“目标属性”))。监督式训练可用于开发将被用于基于输入数据作出预测的模型。非监督式机器学习算法通过处理仅包括输入数据(无输出)的训练数据来构建机器学习模型。非监督式训练可用于确定输入数据内的结构。替代性地,也可以采用半监督式和/或强化机器学习算法。还设想了将上述机器学习算法中的所有或一些进行组合以执行根据本发明的方法。机器学习算法可以使用各种各样的技术来实施,包括使用梯度提升树、人工神经网络、深度神经网络、transformer或长短期记忆循环神经网络等中的一种或多种。
[0126]
再次参考图2,在一些示例中,机器学习训练模块214包括将被训练的一个或多个机器学习算法216。在一些示例中,机器学习训练模块214包括一个或多个机器学习参数218。例如,训练机器学习算法可以涉及使用一个或多个参数218,所述一个或多个参数可以(例如,由用户或者由超参数优化)定义为影响所得机器学习模型的性能。机器学习系统200
可以接收(例如,经由电子设备处的用户输入)并存储这种参数以用于在训练期间使用。示例性参数包括步幅、池化层设置、内核大小、过滤器数量、学习率、最大树深度、子采样比率等,然而该列表并不旨在是详尽的。
[0127]
在一些示例中,机器学习系统200包括机器学习模型输出模块220。机器学习模型输出模块220可以提供与例如基于对训练数据的处理来输出机器学习模型有关的功能。输出机器学习模型可以包括将机器学习模型传输到一个或多个远程设备。例如,在云计算资源126的电子设备上实施的机器学习系统200可以将机器学习模型传输到云计算系统112,以用于处理在客户端系统102与系统112之间发送的受试者数据。
[0128]
图3展示了根据一些示例可以使用的示例性电子设备300。电子设备300可以表示例如pc、智能电话、服务器、工作站计算机、医疗设备等。在一些示例中,电子设备300包括连接输入/输出(i/o)部分302、一个或多个处理器304以及存储器306的总线308。在一些示例中,电子设备300包括一个或多个网络接口设备310(例如,网络接口卡、天线)。在一些示例中,i/o部分302连接到一个或多个网络接口设备310。在一些示例中,电子设备300包括一个或多个人类输入设备312(例如,键盘、鼠标、触敏表面)。在一些示例中,i/o部分302连接到所述一个或多个人类输入设备312。在一些示例中,电子设备300包括一个或多个显示设备314(例如,计算机监视器、液晶显示器(lcd)、发光二极管(led)显示器)。在一些示例中,i/o部分302连接到所述一个或多个显示设备314。在一些示例中,i/o部分302连接到一个或多个外部显示设备。在一些示例中,电子设备300包括一个或多个成像设备316(例如,相机、用于捕获医学图像的设备)。在一些示例中,i/o部分302连接到成像设备316(例如,包括计算机可读介质的设备、与计算机可读介质接口连接的设备)。
[0129]
在一些示例中,存储器306包括一个或多个计算机可读介质,所述一个或多个计算机可读介质存储(例如,有形地体现)用于根据一些示例执行本文所描述技术的一个或多个计算机程序(例如,包括计算机可执行指令)和/或数据。在一些示例中,存储器306的计算机可读介质是非暂态计算机可读介质。可以将基于本文所描述技术的结果的至少一些值保存到比如存储器306等存储器中,以供后续使用。在一些示例中,将计算机程序作为软件应用程序下载到存储器306中。在一些示例中,一个或多个处理器304包括用于执行上文描述的技术的一个或多个专用芯片组。
[0130]
图5示出了实施根据本发明的方法的实施例的基于人工智能或ai的临床决策支持软件的高级图。在图5中,展示了从与给定患者有关的输入到被输出到医疗保健专业人员的定制化临床决策支持建议的信息流。这种基于ai的临床决策支持软件包括若干个ai模型或制品,即,基于机器学习算法的图像分割模型、疾病活动评估模型以及给药频率建议模型。
[0131]
最终,基于ai的临床决策支持软件致力于基于从患者的oct图像以及其他非成像患者特征中自动提取的特征来评估患者眼睛中的疾病活动水平,并向医疗保健提供者提供个人化的给药频率建议。
[0132]
如已经解释的,疾病活动评估模型是由包括多个输入变量的一个或多个机器学习算法生成的。输入变量对应于从oct图像中识别的解剖变量以及非图像导出的不同临床输入患者数据。
[0133]
一个或多个机器学习算法是在来自被诊断患有眼睛或眼部疾病的多个历史患者的历史患者数据集上训练的。
[0134]
虽然下文是针对受新生血管性年龄相关性黄斑变性(w-amd或namd)影响的患者来解释本发明的方法,但进行适当的修改后,所述方法可以应用于评估受选自由以下各项组成的列表中的眼部疾病影响的患者的疾病活动:异常血管生成、脉络膜新生血管形成(cnv)、视网膜血管通透性、视网膜水肿、糖尿病性视网膜病变(特别是增生性糖尿病性视网膜病变(pdr)和非增生性糖尿病性视网膜病变(npdr))、黄斑水肿(me)、糖尿病性黄斑水肿(dme)、新生血管性(渗出性)年龄相关性黄斑变性(namd)、与namd相关的脉络膜新生血管形成(cnv)、与视网膜缺血相关的后遗症、视网膜静脉阻塞(rvo)、视网膜中央静脉阻塞(crvo)、视网膜分支静脉阻塞(brvo)、视网膜静脉阻塞后黄斑水肿、和后段新生血管形成。
[0135]
以下实施例中提及的示例性疾病是新生血管性年龄相关性黄斑变性,特别是w-amd;并且用于治疗的示例性药物是抗血管内皮生长因子药,也可称为抗vegf药,比如布洛赛珠单抗,也称为rth258并且商业上称为
[0136]
由本发明的基于ai的临床决策支持软件所获得的给予医疗保健提供者的个人化给药频率建议无论如何都包括在经批准的给药频率的范围内,如标明用于治疗w-amd的布洛赛珠单抗中所述。这对应于以下方案:前三剂每月(约每25天至31天)一次玻璃体内注射,然后每8-12周一次玻璃体内注射6mg(0.05ml)。借助于根据本发明的方法,可以早在治疗的第一个16周后(即,8周的负荷阶段结束后的8周)确定给药频率建议。
[0137]
历史患者数据集包括从历史患者的视网膜图像中导出的所识别解剖变量的输入值。历史患者数据集还包括与非图像导出的临床输入患者数据相关的值,所述非图像导出的临床输入患者数据包括历史患者的人口统计和病史。
[0138]
图4展示了对用于对新生血管性眼部疾病的活动水平、包括疾病的存在或不存在进行评估的一个或多个机器学习模型进行训练、验证并测试的示例性过程。
[0139]
过程400仅仅是示例性的。因此,方法400中的一些操作可选地被组合,一些操作的顺序可选地改变,并且一些操作可选地被省略。在一些示例中,过程400由具有图1所示的系统100的和/或图2所示的系统200的一个或多个特征的系统执行。例如,过程400的一个或多个框可以由客户端系统102、云计算系统112和/或云计算资源126执行。
[0140]
参考示例性应用程序来描述过程400,所述示例性应用程序使用在两个已完成的诺华临床试验过程中收集的真实世界数据作为用于模型开发的历史患者数据集。在称为hawk和harrier的两项关键的第3期诺华研究中,已经在患有namd或w-amd的患者中测试了布洛赛珠单抗的功效和安全性。
[0141]
hawk和harrier是两年的随机双盲研究,用于评估在患有namd的患者中玻璃体内注射6mg布洛赛珠单抗(hawk和harrier)和3mg布洛赛珠单抗(仅hawk)与注射2mg阿柏西普相比的功效和安全性。分别有1082名患者和743名患者登记执行hawk和harrier临床研究。将参考在这些临床试验的第3期收集的数据,这些数据也分别以clinicaltrials.gov的标识符编号nct02307682和nct02434328为人所知。
[0142]
在hawk和harrier临床试验的背景下,疾病活动(da)评估是医师确定哪些布洛赛珠单抗患者适合12周给药间隔而哪些患者应该调整为8周间隔的步骤。在所有患者中,无论治疗方式如何,疾病活动均由蒙面研究人员进行评估。在接受布洛赛珠单抗的患者中,如果蒙面研究人员确定存在疾病活动,则给药间隔调整为q8w给药,并且他们在剩余的研究中保持为q8w或8周的给药间隔。
[0143]
在hawk和harrier试验中,如以上已经提到的,通过测量多个关键变量来评估namd或w-amd的严重性。这些变量的示例至少包括:
[0144]-最佳矫正视敏度(bcva),使用称为etdrs图表(早期治疗糖尿病性视网膜病变研究图表)的标准视敏度测试图表来测量通过矫正(例如,眼镜)可以达到的最佳视力;
[0145]-中心子区厚度(cst或csft),其中,cst的增加可能指示中央凹中的异常液体积聚(称为黄斑水肿),所述中央凹是负责锐度的中央视觉的部分;
[0146]-视网膜下液(srf)和视网膜内液(irf),其指示可能会损害细胞和周围组织的异常液袋的积聚;以及
[0147]-视网膜下色素上皮(rpe)液,即,在视网膜下色素上皮下部液体的积聚(其可能导致视敏度下降)。
[0148]
下面将阐明前述变量和另外的变量如何有助于开发实施本发明的方法的疾病评估模型。
[0149]
来自hawk和harrier临床试验的受治疗的随机患者的数据被包括用于模型训练。因此,在hawk和harrier临床试验期间治疗的共计1817名患者被插入到其数据构成历史患者数据集的多个患者中。合格性由已公布的相应临床试验方案的包括和排除标准来定义。
[0150]
来自hawk和harrier的可用数据被划分为两个不重叠的子集:用于模型开发和选择的训练集(80%的数据),以及为测试最终模型性能而保留的验证集(20%的数据)。
[0151]
在本发明的实施例中,用于最终获得本发明的疾病评估模型的机器学习算法可以附加地通过专家裁决过程来改进,包括使用蒙面评估研究人员做出的治疗决策进一步训练模型。在这种情况下,可以由在w-amd治疗和视网膜成像方面经验丰富的视网膜专家组成的独立专家组来评审自动输出的疾病活动评估。因此,可以动态地使用在所收集的在先前的迭代期间由裁决专家组进行的疾病活动评估上再训练的经更新的模型,按照能够调整病例选择和专家组成员之间的分配的迭代过程,在多个步骤中选择和评审裁决病例。因此,对于裁决过程的每次迭代,病例选择可以基于已经用先前迭代期间生成的数据进一步训练的疾病活动评估模型。
[0152]
在框402处,计算系统(例如,客户端系统102、云计算系统112和/或云计算资源126、电子设备300)接收数据集(例如,经由数据检索模块210),所述数据集包括来自外部来源(例如,数据库120或数据库134)的与眼睛健康相关的电子健康记录。所述数据集包括:借助于对已确认诊断为w-amd的多个患者的视网膜图像的分割而识别的若干解剖变量的值,如图5所示;以及非图像导出的临床输入患者数据(比如相同患者的纵向假名电子健康记录)的值。
[0153]
图6示出了包括在示例性历史数据集中的给定患者或受试者(表示为“2”)的匿名电子健康记录的示例,所述匿名电子健康记录涉及该患者在第一8周负荷阶段内的以及随后另一8周治疗阶段(直至目标第16周,此时由蒙面研究人员进行第一疾病活动评估)内的就诊。在某些情况下,变量值以存在概率的形式进行量化或归为二元的存在/不存在系数。
[0154]
在一些示例中,计算系统从一个或多个来源接收包括与视网膜病变相关的匿名电子健康记录的多于一个历史数据集。在一些示例中,框402进一步包括计算系统将多个接收到的历史数据集组合成单个组合历史数据集。
[0155]
在为发展本发明的一个实施例而进行的特定研究中,所处理的所有患者层面的数
据都是假名的,而没有任何识别患者身份的可能。
[0156]
在一些示例中,与示例性数据集中包括的相比,在框402处接收的历史数据集包括给定受试者的相应更多输入变量的更多值。
[0157]
在一些示例中,与示例性数据集中包括的相比,在框402处接收的数据集包括给定受试者的更少的数据输入。应当理解,上面的受试者变量或特征的列表并不是详尽的,并且在某些示例中,计算系统还接收包括在框402处接收的数据集中的多个受试者中的一个或多个受试者的描述性数据(例如,其他受试者诊断、受试者用药等)。
[0158]
返回到图4,在框404处,计算系统(例如,经由数据调控模块212)对在框402处接收的数据集进行处理。在计算系统在框402处接收多于一个数据集的上述示例中,计算系统对单个组合数据集进行处理。如图4所示,在框404处对数据集进行处理可以包括计算系统在框406处从数据集中排除受试者,在框408处导出数据集的受试者特征值,以及在框410处对数据集中包括的受试者数据进行分析。
[0159]
在框406处,在一些实施例中,计算系统基于一组预定的包括和/或排除标准来从数据集中移除一个或多个受试者。例如,可以在分析中丢弃缺少了一次或多次计划就诊的受试者;可以丢弃在他/她的历史中缺少一个或多个测量结果的受试者。在一些实施例中,计算系统不移除任何受试者。
[0160]
在框408处,计算系统导出数据集中包括的多个变量的患者输入变量值。计算系统导出包括在该受试者的历史数据集中的、与患者相对应的输入变量的输入值。
[0161]
在某些示例中,计算系统基于受试者特征的先前(例如,较旧的)值来导出一个或多个受试者的受试者变量或特征值(例如,使用时间窗口方法)。例如,监督式机器学习算法可以实施预处理步骤,即,计算在评估日期之前的预设时间段(例如,在评估日期之前的0、4、8、12周)记录的多个输入变量的值。在某些情况下,可以使用线性插值或外推;可以使用基于样条的方法。
[0162]
如果患者在评估日期之前没有任何测量结果,则保留该患者,并且可以将没有测量结果的时期视为null。也可以保留没有任何测量结果的患者,并且其所有评估日期都为null。
[0163]
参考图4的框410和图2的框212,计算系统对包括在数据集中的受试者数据进行分析。具体地,计算系统在框410处例如使用一种或多种统计测试和/或技术来分析数据集中包括的一个或多个患者的输入变量值或受试者特征值。执行该步骤以确定一个或多个输入变量与疾病活动之间的统计关联(例如,以确定单独的输入变量是否具有解释能力来区分具有较高疾病活动的患者与具有较低疾病活动的患者)。在实施xgboost机器学习算法的情况下,该步骤可能尤其合适并且具有优势。
[0164]
在一些示例中,框404不包括框406、框408、框410之一。
[0165]
在一些示例中,在框404处理数据集进一步包括计算系统从数据集中移除重复的、无意义的或不必要的受试者特征(及其对应的值)和/或统一用于数据集中包括的受试者特征值的测量单位。
[0166]
在一些示例中,在框404处理数据集进一步包括计算系统为数据集中包括的多个受试者中的一个或多个受试者的分类(即,非数字)受试者特征值进行独热编码或创建嵌入。
[0167]
在框412处,计算系统通过(例如,经由机器学习训练模块214)将多个机器学习算法中的每一个分别应用于在经处理的数据集中包括的患者历史数据来训练(例如,包括在机器学习算法216中的)多个机器学习算法。例如,计算系统分别应用多个监督式机器学习算法,包括(但不限于)逻辑回归算法;梯度提升树算法,如lightgbm或xgboost算法;循环神经网络(rnn);以及随机森林算法。在一些示例中,计算系统可以将一个或多个非监督式或半监督式机器学习算法应用于在经处理的数据集中包括的受试者数据。
[0168]
在其中对基于树的算法进行训练的一些实施例中,计算系统开始先识别作为可以产生良好预测性能的一个或多个根变量的特征,然后搜索其到根变量的附连可以提高预测性能的附加叶变量层;搜索是递归实施的(即,通过寻找其到前一叶变量层的添加可以提高预测性能的新叶变量层),直到预测性能无法提高为止。在某些情况下,当已学习的基于树的算法看到一个或多个新样本时,所述算法可以适配其树结构。
[0169]
在其中对基于rnn的算法进行训练的一些实施例中,计算系统包括能够分析纵向数据的神经网络。神经网络可以将输入数据变换为预测分数和一组不可知特征。不可知特征被进一步反馈给神经网络,以作为用于下一个时间点的输入的一部分;这意味着,用于下一个时间点的输入包括患者数据和从前一时间点导出的不可知特征。在数学上,不可知特征捕获历史中的可以帮助算法在未来做出更好预测的重要信息。对神经网络进行训练,直到预测性能无法提高为止。
[0170]
将机器学习算法应用于在经处理的数据集中包括的患者数据包括计算系统将经处理的数据集划分为第一部分(本文称为“训练集”)和第二部分(本文称为“验证集”)。在一些实施例中,计算系统进一步将经处理的数据集划分为第三部分(本文称为“测试集”)。训练集用于训练机器学习算法并基于所述训练生成机器学习模型。验证集用于评估所生成的机器学习模型并更新机器学习模型超参数,以获得更好的性能。代替单个验证集,可以使用交叉验证。即,可以随机创建多个训练数据集和验证数据集,其中,每个记录在验证集中存在一次。交叉验证(cv)可以以这样的方式实施,即,来自特定患者的记录始终都在相同的训练集或验证集中,从而避免信息泄露。测试集用于评估经训练的机器学习模型在未见过的数据上的表现,并且当应用于新的受试者数据集(例如,未包括在经处理的数据集中的受试者数据)时,还用于估计机器学习模型的性能。
[0171]
例如,在下面披露的一个优选实施例中,如已经提到的,将历史数据集中80%的数据用作模型开发和选择的训练集,同时将20%的数据用作验证集。然而,计算系统可以替代性地划分经处理的数据集,将经处理的数据集中包括的不同百分比的受试者(及其对应的受试者特征值)分配为训练集、验证集或测试集。在各个实施例中,百分比可以是100%与0%、95%与5%、90%与10%、85%与15%、或75%与25%。
[0172]
例如,在一些实施例中,如果采用监督式机器学习技术,则将机器学习算法应用于在经处理的数据集中包括的受试者数据进一步包括计算系统将疾病活动水平标记为目标属性并且随后使用训练集来训练机器学习算法。如以上讨论的,目标属性表示机器学习算法被训练来预测的“正确回答”。因此,在这种情况下,使用训练集(例如,训练集的受试者特征值)来训练多个机器学习算法中的每一个,使得机器学习算法学习在被提供与训练集类似的数据(例如,包括多个受试者特征的受试者数据)时输出与有效地将用于治疗患者眼睛疾病的药物的当前给药方案切换为不同的给药方案的概率或适当性相关的疾病活动。
[0173]
在分别训练多个机器学习算法之后,计算系统(例如,经由机器学习模型输出模块220)生成与被训练的每个机器学习算法相对应的机器学习模型。例如,计算系统分别生成与经训练的逻辑回归算法相对应的机器学习模型、与经训练的xgboost算法相对应的机器学习模型、与经训练的lightgbm算法相对应的机器学习模型、与经训练的随机森林算法相对应的机器学习模型。生成机器学习模型包括计算系统基于对机器学习算法的训练来确定一个或多个模式,所述一个或多个模式将训练集中包括的受试者特征的值映射到患者的对应疾病活动水平(例如,目标属性)。此后,计算系统生成表示所述一个或多个模式的机器学习模型。在被提供与训练集类似的数据(例如,包括训练集中包括的患者输入变量中的一个或多个的输入值的特定患者数据)时,计算系统使用(例如,多个生成的机器学习模型中的)生成的机器学习模型来输出疾病活动分数和/或预测由于给药方案之间的变化而产生的疾病活动变化。
[0174]
在框414处,计算系统使用经处理的数据集中的验证集来验证在框412处生成的机器学习模型。验证机器学习模型是对机器学习模型的以下能力进行评估,即,当被提供与用于训练生成机器学习模型的机器学习算法的数据类似的数据时所述机器学习模型准确地评估或预测目标属性(在这种情况下,疾病活动水平,尤其是在w-amd的情况下)的能力。如图4所示,在框414处验证机器学习模型包括计算系统在框416处确定性能指标。
[0175]
在框416处,计算系统为在框412处生成的一个或多个机器学习模型确定一个或多个性能指标。例如,计算系统为逻辑回归机器学习模型、xgboost机器学习模型、light gbm机器学习模型和随机森林机器学习模型中的每一个确定一个或多个性能指标。一个或多个性能指标包括(但不限于)召回率、精确率、召回率-精确率曲线下面积(auprc);接受者操作特性曲线下面积(auroc)。
[0176]
召回率也称为灵敏度,等于正确预测的事件的比例;精确率,也称为阳性预测值,等于实际发生的预测事件的比例;auprc等同于精确率-召回率曲线下面积,并衡量不同阈值的预测性能。auroc曲线是绘制真阳性率和假阳性两个参数的曲线图,表示模型对随机正例的排名高于随机负例的概率,并示出分类模型在所有可能的分类阈值上的性能。
[0177]
在框418处,计算系统基于在框412处生成的机器学习模型和经处理的数据集中包括的受试者变量或特征来执行特征选择。这个步骤针对在框412处生成的每个机器学习模型单独执行。计算系统优选地为在训练集和/或验证集中包括的每个受试者变量或特征确定性能指标。具体地,计算系统可以优选地使用增益指标来缩减在准确并可靠地对视网膜病变、特别是在w-amd的情况下的疾病活动水平进行评估方面最重要的受试者特征(例如,在训练集中和/或验证集中包括的)。替代性地,为此目的,可以采用递归特征消除(rfe),其是迭代特征选择技术,例如从而为每个受试者特征确定auc性能指标。基于所确定的性能指标,计算系统确定每个受试者特征的相对重要性百分比。然后,计算系统(基于所确定的相对重要性百分比)为每个机器学习模型移除最不重要的受试者特征。因此,产生了减少的训练集和减少的验证集,这有助于避免使机器学习模型过拟合(原因是在连续几轮特征选择中的每一轮之后会存在较少的冗余数据),提高预测性能,并减少机器学习模型生成预测所需的时间量。
[0178]
在计算系统生成减少的训练集和减少的验证集之后,计算系统针对先前使用的相同机器学习算法(例如,逻辑回归算法、xgboost算法和随机森林算法)中的每一个,使用减
少的训练集和减少的验证集(而不是包括所有受试者特征的原始训练集/验证集)来重复在框412至418处执行的动作。进一步地,对于框412至418的每次迭代,计算系统为减少的训练集/减少的验证集中包括的每个受试者特征确定性能指标(例如,在框418处),使得计算系统可以再次确定并移除在减少的训练集/减少的验证集中包括的最不重要的受试者特征。以示例的方式,在产生用于本发明的实施例的数据的研究中,当采用分割输出时,最初创建了多于100个输入变量或特征以进行探索,以便识别被视为w-amd的生物标志物或预测因子的因素;而当使用原始图像数据作为输入(即,没有进行分割步骤)时,最初创建了多于2,500,000个输入变量或特征进行探索,以用于生物标志物的识别。
[0179]
计算系统将迭代地执行框412至418的动作,从而在框416处基于使用减少的训练集/减少的验证集训练/验证的机器学习模型来确定性能指标。以这种方式,计算系统(1)为所使用的机器学习算法中的每一个生成多个机器学习模型,(2)为多个生成的机器学习模型中的每一个确定一个或多个性能指标,以及(3)为用于训练每个机器学习模型的每个受试者特征生成相对特征重要性百分比。
[0180]
在框420处,计算系统基于验证集上的结果或来自交叉验证的结果来选择机器学习模型和所选择的特征集。具体地,计算系统基于为在递归特征消除期间生成的各个模型确定的一个或多个性能指标来选择机器学习模型。在这种情况下,考虑到验证集上的主要目标或基于交叉验证,计算系统(在针对所使用的每个机器学习算法生成的所有机器学习模型中)选择具有最高性能的机器学习模型。
[0181]
在框422处,计算系统使用未见过的受试者数据的数据集来测试所选择的机器学习模型。在框422处测试所选择的机器学习模型包括计算系统基于将所选择的机器学习模型应用于未见过的受试者数据的数据集来确定一个或多个性能指标。在计算系统进一步将经处理的数据划分为训练集、验证集和测试集的示例中(例如,在框412处),使用测试集来测试所选择的机器学习模型。
[0182]
参考图7,呈现了用于生成对患者眼睛中视网膜病变(即,在该特定情况下为w-amd)的活动水平、包括视网膜病变的存在或不存在进行评估的相应ai驱动模型700a、700b的两种可能方法。更准确地说,模型700a、700b基于循环神经网络(rnn),即,允许将先前的输出用作输入同时具有隐藏状态的一类神经网络。模型700a、700b最终允许对疾病活动进行个人化评估,以及相应地给出最佳给药方案的建议,如框703'所示。
[0183]
图7中由“深度学习#1”指定的路径基本上是基于特征的。首先将深度学习算法700a应用于原始oct图像701,以检测和/或因此测量相关的解剖变量或特征,诸如视网膜内液(irf)的、视网膜下液(srf)的以及色素上皮脱离(ped)的生物标志物。检测和体积量化是通过对原始oct图像701的基于ai的分割来执行的。给定图像701,分割神经网络识别详细的视网膜结构的边界并测量视网膜结构的尺寸(例如,厚度、面积或体积),如框702所示。更广泛的结构信息的示例包括:中心子区中央凹厚度(csft);高反射灶、神经节细胞层和内丛状层;内核层和外丛状层体积;视网膜内液和囊肿体积;外核层体积;色素上皮脱离体积;光感受器和视网膜色素体积;视网膜神经纤维层体积;视网膜下液体积;视网膜厚度。
[0184]
同时,分割神经网络还可以评估以下异常中的一种或多种的概率:视网膜前膜概率;纤维色素上皮脱离概率;地图状萎缩概率;健康概率(未检测到异常或生物标志物);硬渗出物概率;外层视网膜萎缩概率;网状假玻璃膜疣的概率;玻璃疣概率。
[0185]
更一般地,如已经提到的,上述数据然后与如bcva、人口统计(性别、年龄)以及疾病特性等对应的非成像数据相组合,如框702'所示。
[0186]
然后,将循环神经网络(rnn)机器学习算法应用于在框702'中如此组合的数据,以最终构建用于疾病评估和给药方案优化的预测模型,如框703所示。将上述所识别的解剖变量的测量尺寸的值和概率的值同非成像附加信息相结合,以形成在时间“t”处的输入数据集,其可以表示为d(t)。d(t)成为上述介绍的rnn的输入,以用于输出疾病评估分数和给药方案建议。
[0187]
假设在参考临床试验中药物负荷周为0周、4周和8周;而非负荷周从第16周开始并持续到20周、24周、28周等直到96周,针对这种情况通过应用rnn来生成评估模型所依据的数学过程可以总结为以下一系列步骤。
[0188]
对于在非负荷周“t”处的给定数据样本,根据本发明的方法将d(t)作为第一输入数据集。
[0189]
进一步地,采用第二输入数据集,表示为d(0),其包括在基线负荷期“0”处的上述识别的解剖变量的值、概率和非成像附加信息。
[0190]
在第一神经网络中,d(t)被追加到d(0)。将产生的聚合数据作为对第一神经网络的输入,并将其变换为第一向量空间f1(t)。
[0191]
第二神经网络计算d(t)与d(0)之间的差异(表示为d(t)-d(0)),并将d(t)-d(0)变换为第二向量空间f2(t)。
[0192]
第三神经网络将f2(t)追加到f1(t),将f1(t)和f2(t)的聚合数据作为其输入,并将该输入变换为第三向量空间f3(t)。
[0193]
第四神经网络将f3(t)变换为0与1之间的概率分数。如已经介绍的,这样的概率分数可以被视为疾病活动分数。
[0194]
随后,如果概率分数大于给定的阈值或基准,则基于阈值或基于基准的算子将数据样本确定为1类。在这种情况下,系统输出将低频给药方案切换为高频给药方案的建议,例如,从12周给药方案切换为8周给药方案。否则,基于阈值的算子将样本确定为0类,即,系统输出保持当前给药方案频率并且不切换给药方案的建议。
[0195]
相对于上述基于rnn的模型的性能,已经建立了0.835的auroc度量。
[0196]
经过适当的修改,上述d(t)也可以有资格作为如先前所介绍的根据本发明的基于树的机器学习方法的输入。在这种情况下,对于d(t)中的每个特征{xi},机器学习算法会寻找函数f(xi)来预测疾病活动水平和/或给药频率,其可以表示为y。在数学上,函数f(xi)需要近似或预测地面真值y,其中,取决于特征{xi}是高于或低于阈值,y等于1或0。从图形上看,该预测采用二叉树的形式:给定每个函数f(xi),指派对应的权重wi。对基于树的机器学习算法进行训练旨在找到实现最准确预测的最佳权重集。在数学上,要求真实回答y(0或1)尽可能接近每个函数f(xi)的加权和,如通过公式y~∑wi f(xi)所表示的。在迭代过程中,所述方法在当前树集之间随机选择一个树;将所选择的树变为给定集中另一个树的子代分支;评估当前树设置的预测的加权和;并重复上述步骤,直到算法性能得到优化为止。然后,将这种树的最佳集及其相应的权重作为生成的最终模型的一部分。
[0197]
由根据本发明的基于树的机器学习算法生成的疾病活动评估模型识别了20个最重要的变量或特征,以用于输出例如在患者的治疗开始后的目标第16周处的活动疾病分数
和相关的给药方案建议,如表1所示。在一些实施例中,变量排名越高,权重就越多或它们对预测性能的贡献就越重要。
[0198]
表1
[0199][0200]
在表1中,对20个最重要的变量按夏普利值(标记为“shap”值)进行排序,该值衡量每个特征对根据本发明的基于树的模型的性能的贡献。
[0201]
整体基于树的模型性能如曲线图1所示,其中,表示了roc曲线。测试数据集的roc曲线下面积等于0.88
±
0.012;而训练数据集的roc曲线下面积等于0.93
±
0.003。
[0202]
曲线图1
[0203]
[0204]
根据本发明的基于树的疾病活动评估模型可以选择排名靠前的变量,以形成如表2所示的减少的或简化的预测变量集,其中,项“idx”表示在运行模型和进行疾病活动评估时(即,患者就诊时)的索引日期的变量值。
[0205]
表2
[0206][0207]
可以在曲线图2中对依赖于表2中减少的变量集的基于树的模型的性能进行例示,其中,表示了roc曲线。测试数据集的roc曲线下面积等于0.86
±
0.001;而训练数据集的roc曲线下面积等于0.9
±
0.002。
[0208]
曲线图2
[0209][0210]
参考图8,还示出了根据本发明的生成基于ai的临床决策支持软件模型700b的第
二方法的工作流。本方法遵循由图7中的“深度学习#2”指定的路径。
[0211]
这种第二方法可以定义为“特征不可知的”,因为人类用户不会预先确定用于分类和/或预测的确切变量或特征。而是,计算模型700b自动从原始数据中选择变量,甚至可能在机器学习过程中自动导出变量本身。
[0212]
因此,根据这种第二方法的模型700b通过将机器学习算法应用于原始oct图像701和非成像数据两者来执行疾病活动的端到端评估和预测在修改的给药方案下的疾病活动变化。
[0213]
简而言之,参考图8,在由神经网络机器800分析oct图像801之后,在框802处自动识别多个特征;然后,在框803处重建oct图像;在框804处,评估oct图像重建的准确性,并且在框806处,基于神经网络识别的特征,系统进行疾病活动评估和/或给药方案切换的预测。
[0214]
为此目的,采用包括多个神经网络的单个神经网络架构800,即,在图8中例示的特定实施例中的四个神经网络。
[0215]
在框802处,指定为特征识别神经网络的第一神经网络将原始oct图像801作为输入并生成多个变量或特征。人类用户可以指定要生成的特征的数量,诸如100个、200个、240个等。
[0216]
在框803处,指定为原始图像重建神经网络的第二神经网络将所生成的特征作为输入,并尽可能准确地将这些特征变换回原始oct图像801。
[0217]
在框804处,指定为评估神经网络的第三神经网络评估原始oct图像801与所重建的oct图像之间的相似性。如果图像不相似,则该神经网络要求前两个神经网络进行训练;否则,前两个神经网络被认为已经经过适当的训练。一旦对第一神经网络和第二神经网络(即,特征识别神经网络和原始图像重建神经网络)进行了训练,就认为特征识别神经网络可以自动识别特征。
[0218]
在框805处,指定为疾病活动预测神经网络的第四神经网络同时将自动识别的特征和其他非图像信息(比如性别、年龄和最佳矫正视敏度)作为输入,并进行疾病活动评估。在框807处,疾病活动预测神经网络还基于所计算的疾病活动来输出对给药频率切换的合适度的后续决策。实际上,所述系统向眼科医生输出关于从低频给药方案切换为高频给药方案(例如,从12周给药方案切换为8周给药方案)是否合适的建议;反之亦然。
[0219]
在图9中,示出了从根据本发明的计算机实施的方法的应用而产生的示例性输出数据集。特别地,实施这种方法的基于ai的临床决策支持软件可以在目标治疗的第16周为由数字“2”至“9”标识的对应8名匿名患者输出如所示的数据,从而产生疾病活动分数。每个活动分数与所计算的疾病活动分数值可能与其“真实值”的相差程度的相应统计最佳估计(即,与所计算的分数值相关的不确定性)相关联。根据由模型输出的疾病活动分数的值,显而易见的是,患者6在索引日期或就诊时间具有最低的疾病活动水平;而患者3在就诊时间具有最高的疾病活动水平。
[0220]
参考图5的高级图,如上所述开发的模型500最终允许基于与例如被诊断患有w-amd的给定患者10相关的输入患者数据集的获取,向医疗保健提供者或医师20输出患者10的疾病活动的评估和随之而来的定制化治疗建议。输入患者数据集包括借助于对患者10的视网膜图像501的分割502而识别的解剖变量;以及非图像导出的临床输入患者数据(诸如,同一患者10的纵向假名电子医疗记录或健康记录505)的值。如所解释的,患者特定数据
501、505由实施根据本发明的方法的基于ai的临床决策支持软件500来细化,以计算疾病活动和适当的给药频率,如框503所示。为方便起见,输出可以显示在医疗保健专业人员界面504上,如将在下面更详细地讨论的。
[0221]
图10至图13示出了实施根据本发明的方法的软件的图形用户界面的各部分的示例,所述软件特别是被设想为指导医疗保健提供者(诸如,眼科医生)的给药决策。
[0222]
设想软件的图形用户界面将提供若干个级别的信息,以在任何就诊期间指导眼科医生评估疾病活动,即,w-amd疾病活动。
[0223]
模型将生成疾病活动或da的分数,以允许区分da的水平。取决于由软件生成并由眼科医生读取的信息,具有高da的患者可以切换为更频繁的给药;具有低da的患者可以维持在当前给药方案下或切换为较低频率的给药(例如,q8w患者控制良好并且可能被认为有资格进行q12w再考验)。
[0224]
为了进一步指导眼科医生做出决策,将显示影响对da的评估的解剖特征和功能特征(例如,视网膜液的存在和位置)的相对重要性。
[0225]
最后,以通过分割提取的相关解剖变量标注的oct图像将有助于立即验证患者的情况。
[0226]
特别地,图10示出了在医疗保健专业人员或眼科医生的前端(例如,在他的计算机屏幕上)的图形用户界面的一部分,显示了由根据本发明的基于ai的临床决策支持软件输出的数据。所显示的数据提供了分别在两个不同的评估时间(例如,治疗中的两个连续时间)的患者的当前疾病活动分数的视觉再现。
[0227]
疾病活动的水平和对应分数的水平可以进一步分类并标记为高或中等或低。
[0228]
在图10中,被评估的患者示出疾病活动,所述疾病活动包括在评定量表的中间分数区域中、在其较高端与较低端之间。在疾病活动评定量表上示出了界限,其界定了诸如中等疾病活动水平的中间区域或范围。在这种中等疾病活动水平的范围内,眼科医生对病例的判断可能更加模糊。在图10中例示的情况下,对于以12周间隔用抗vegf药物(如布洛赛珠单抗-dbll)治疗的患者,眼科医生可能仍然决定不让患者从12周间隔或q12w的当前方案切换为更频繁的8周间隔或q8w给药方案。例如,这可能归因于他/她自己的一般方法,例如,他/她对某种残留的疾病活动水平感到满意;或者因为这种患者可能不太适合更频繁的给药,例如,因为患者对更密集治疗有低依从性的风险。替代性地,鉴于不同专家对所治疗的受试者的考虑,眼科医生可能希望考虑切换为更频繁的8周间隔给药方案,例如,如果他/她认为根据本发明的模型量化的残留疾病活动水平风险太高。
[0229]
在图11中,显示的数据提供了针对被检查患者的合适给药方案的指导。事实上,所述数据示出了可以预测患者眼睛的疾病活动水平会如何由于将注射到所述患者眼睛中的抗vegf药物的两种不同的给药方案之间的变化而发生变化。软件可以预测,对患者“无名氏”进行更频繁治疗的效果可能会产生对于疾病活动的更好控制。与当前的12周药物注射间隔方案相比,针对布洛赛珠单抗-dbll的注射之间的8周药物间隔的更频繁给药方案来自动进行疾病活动变化的预测(即,下降)。
[0230]
图12展示了解剖特征和功能特征的相对重要性如何影响对图11患者的疾病活动的评估。所呈现和量化的主要风险因素有:相对于基线的最佳矫正视敏度(bcva);自上次就诊以来的中央视网膜厚度(crt);视网膜内液(irf);自上次就诊以来的视网膜下液(srf);
以及就诊时的色素上皮脱离(ped)。
[0231]
在一些实施例中,对在hawk和harrier临床试验中登记的患者的sd-oct图像的液体体积进行的基于ai的分析证实了在维持期间irf、srf和ped的较低水平都独立地与在bcva反应方面的更好视觉结果相关联,这表明所有上述三个液体空间都是与w-amd中的视觉功能同等且独立相关的疾病活动标志物。
[0232]
图13展示了实施根据本发明的方法的软件的图形用户界面的不同部分,其中,随时间示出了被检查患者的疾病活动分数,即,从治疗前水平到治疗的各个阶段,跨越以12周给药间隔进行的负荷阶段以及随后以8周给药间隔进行的维持阶段。
[0233]
基于由根据本发明的方法输出的疾病活动分数,可以设计和规定各种各样的个体化治疗方案。事实上,基于这样的疾病活动分数,医疗保健提供者可以调整他/她的决策,例如立即注射药物,或指派下一次监测就诊,或切换为另一种治疗。
[0234]
以下提及根据本发明的方法的应用的另外的示例。
[0235]
在以布洛赛珠单抗或另一抗vegf药物进行q12w/q8w治疗的当前标签下,医疗保健提供者可以使用当前患者就诊时的疾病活动分数以及关于自上次注射以来的时间的信息来决定是否将患者从“默认”的q12w给药方案治疗(每12周一次)切换为q8w给药方案治疗(即,每8周注射一次)。
[0236]
在“治疗-结束-延长”治疗方案下,医疗保健提供者可以使用当前患者就诊时的疾病活动分数来决定是让患者保持在当前治疗间隔,还是以其他方式延长或缩短治疗间隔。
[0237]
在“视情况而定(pro-re-nata)”或“按需”治疗方案下,疾病活动分数可以用于区分是在当前就诊时注射抗vegf,还是将其推迟到下一次监测就诊,其中,就诊通常是每月一次。
[0238]
总体上,通过实施根据本发明的方法实现的对患者(诸如,湿性amd患者)的眼部新生血管疾病活动的算法评估不仅可以用于调整用抗vefg药物进行的治疗,而且还用于调整用旨在维持血管稳定性(例如通过抑制血管通透性)和/或抑制血管生成的其他药物(包括抑制vegf和血管生成素-2(ang-2)两者的双特异性抗体)进行的治疗;或者甚至用于已建立的激光治疗方案。
[0239]
此外,本发明还涉及在治疗患者新生血管性年龄相关性黄斑变性(namd)中使用的vegf拮抗剂,其中,所述使用包括以4周间隔向患者施用三次单独剂量的vegf拮抗剂,此后每4周、8周或12周向患者施用额外的剂量。如果患者的疾病活动恶化,则可以将12周的治疗间隔切换为8周的治疗间隔。否则,如果患者的疾病基本稳定或改善,则可以维持或延长12周的治疗间隔。患者的疾病的恶化、改善或稳定状态可以有利地基于上述用于对疾病活动水平、包括疾病的存在或不存在进行评估的计算机实施的方法来确定。
[0240]
展示本发明的各方面和实施例的本说明书和附图不应被视为限制,而是权利要求定义了受保护的发明。换言之,虽然已经在附图和前述描述中详细说明和描述了本发明,但是这样的说明和描述被认为是说明性的或示例性的,而不是限制性的。在不脱离本说明书和权利要求的精神和范围的情况下,可以进行各种机械的、组成的、结构的、电气的和操作上的改变。在某些情况下,未详细示出公知的电路、结构和技术,以免模糊本发明。因此,应当理解,普通技术人员可以在所附权利要求的范围和精神内做出改变和修改。特别地,本发明涵盖具有来自上文和下文所描述的不同实施例的特征的任何组合的另外实施例。
[0241]
本披露内容还覆盖了图中单独示出的所有另外的特征,尽管在前面或后面的描述中可能没有对这些特征进行描述。此外,在这些图和说明书中描述的实施例的单个替代方案及其特征的单个替代方案可以从本发明的主题或从所披露的主题中放弃。本披露内容包括由权利要求或示例性实施例中定义的特征组成的主题以及包括所述特征的主题。
[0242]
此外,在权利要求中,“包括”不排除其他元素或步骤,并且不定冠词“一个”(“a”或“an”)不排除多个。单个单元或步骤可以实现权利要求中叙述的若干特征的功能。仅仅在彼此不同的从属权利要求中叙述某些措施这一事实不表明这些措施的组合不能被有利地使用。特别地,与属性或值相关的术语“基本上”、“大约”、“约”等也分别确切地定义了所述属性或确切地定义了所述值。在给定数值或范围的上下文中,术语“大约”是指例如在给定值或范围的20%内、10%内、5%内或2%内的值或范围。被描述为耦合或连接的部件可以以电的方式或以机械的方式直接耦合,或者它们可以经由一个或多个中间部件间接耦合。权利要求中的任何附图标记不应被解释为限制范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1