抗体的皮下吸收和生物利用度的制作方法
抗体的皮下吸收和生物利用度
发明领域
1.本公开涉及选择适于皮下施用的抗体的方法;用于改善抗体的皮下吸收和生物利用度的方法;以及将抗体皮下施用于受试者的方法。
2.背景
3.在过去几十年中,由于其靶结合特异性、二价相互作用特性、具有天然的效应子功能的潜能及其体外和体内生化稳定性,人或人源化单克隆抗体(mab)药物已经成功用作多种人类疾病中的治疗方式(kaplon h和reichert jm.mabs2018;10:183-203;kaplon等,mabs.2020年1月-12月;12(1):1703531)。抗体工程化方法的进展,如实现理想药效学(pd)的人源化、效价和特异性优化,以及药物性能(如药代动力学(pk))的改善,对基于mab的治疗的成功至关重要。
4.相对于静脉内(iv)途径,由于增加的患者便利性和依从性,对于临床环境中的治疗性抗体,sc给药通常是优选的(matucci a等,respir res 2018;19:154;viola m等,j control release 2018;286:301-14)。经常,这一努力的障碍包括与减少全身暴露的sc注射相关的生物利用度限制。难以预测sc给药后单克隆抗体的生物利用度,其值可能是可变的和部分的,约为50至100%(lobo ed等,j pharm sci 2004;93:2645-68;turner mr和balu-iyer sv.j pharm sci 2018;107:1247-60;wang w等,clin pharmacol ther 2008;84:548-58)。目前,已上市mab在人体中的平均sc生物利用度约为60-80%(viola m等,j control release 2018;286:301-14;turner mr和balu iyer sv.j pharm sci 2018;107:1247-60;richter wf和jacobsen b.drug metabolism and disposition:the biological fate of chemicals 2014;42:1881-9)。虽然对一些mab的不完全生物利用度的相关机制尚不清楚,但普遍认为sc给药后mab的pk去向和吸收情况需要了解sc空间/解剖结构和组成。
5.已经大范围地综述了sc基质或皮下组织(viola m等,j control release 2018;286:301-14;turner mr和balu-iyer sv.j pharm sci 2018;107:1247-60;richter wf和jacobsen b.drug metabolism and disposition:the biological fate of chemicals 2014;42:1881-9)。sc给药后,mab必须通过间质分流以到达这些毛细血管。考虑到细胞(脂肪细胞、巨噬细胞和成纤维细胞)和基质(脂肪、糖胺聚糖(gag)、蛋白聚糖、弹性蛋白和胶原蛋白)的混合物,pk去向、吸收谱和用于改善mab sc动力学的工程化策略可能需要了解分子的物理化学性质与sc空间和解剖结构的相互作用。
6.有趣的是,虽然基于mab的生物疗法的数量已经增加,但是关于物理化学特征与其对mab pk的影响之间的相对平衡仍然存在相当多的争论和信息的匮乏。这导致对这些参数如何影响施用于sc空间的mab的吸收过程的理解不足。已经研究了一些有限的物理化学要素,如分子量和fcrn结合能力。此外,已经用具有混合发现的基于电荷的mab变体进行了一些研究。在khawli等的研究中,用iggl电荷变体没有报道sc吸收的显著差异;然而,在该报告中,这些iggl分子的pi变化轻微(在0.1pi单位内),因此可能没有不同到足以影响sc吸收(khawli la等,mabs 2010;2:613-24)。相比之下,在另一篇报道中,pi具有更宽范围(1个单位差异)的mab显示出与递增的mab pi和递减的sc生物利用度相关的中等趋势(zheng y等,
mabs 2012;4:24 3-55)。与后来的发现一致,mach及其合作者报道了带正电荷的mab在体外与sc组织相互作用,可能是通过静电相互作用介导的(mach h等,ther deliv 2011;2:727-36)。总之,这些少数研究为内在mab物理化学特征对sc吸收的速率和程度的作用奠定了一些基础。关于诸如sc注射后mab的疏水性、热稳定性和聚集潜力等因素以及这些因素与电荷、等电点和fcrn结合作用的相互影响的数据缺乏。
7.需要选择适于皮下施用的mab并改善mab的皮下吸收和生物利用度。
8.发明详述
9.本文提供了选择适于皮下施用的抗体(例如mab)的方法;用于改善抗体(例如mab)的皮下吸收和生物利用度的方法;以及向受试者皮下施用抗体(例如mab)的方法。
10.在一个方面中,本文提供了选择适于皮下施用的抗体(例如mab)的方法,此类方法包括测量结合相同靶标的第一和第二抗体的t
agg
(聚集起始的温度)、测量第一和第二抗体的t
m起始
(解折叠起始的温度),比较第一和第二抗体的t
agg
和/或t
m起始
;和选择具有更高t
agg
和/或t
m起始
的第一或第二抗体用于皮下施用。在一些实施方案中,此类方法进一步包括测量第一和第二抗体的hpnip(heparin binding interaction potential,肝素结合相互作用势)和/或hip(hydrophobic interaction potential,疏水相互作用势)。在一些实施方案中,此类方法进一步包括选择具有较低hpnip和/或hip的第一或第二抗体。在一些实施方案中,此类方法进一步包括测量第一和第二抗体的皮下吸收速率(ka)和/或皮下生物利用度(%f)。
11.在一些实施方案中,此类方法进一步包括测量第一和第二抗体的一个或多个pk参数,其中pk参数选自c
max
(maximal observed serum concentration,最大观察血清浓度),t
max
(time of maximal observed serum concentration,最大观察血清浓度的时间),auc
0-inf
(area under the serum concentration curve from time zero extrapolated to infinite time,从时间零外推至无限时间的血清浓度曲线下面积),cl/f(sc施用后的清除率),和t
1/2
(消除半衰期)。
12.在一些实施方案中,第一抗体和第二抗体都是单克隆抗体,例如人源化mab。在一些实施方案中,第一抗体和第二抗体具有iggl或igg4同种型。在一些实施方案中,第一抗体和第二抗体均包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区(hcdr)hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区(lcdr)lcdr1、lcdr2和lcdr3。
13.在一些实施方案中,此类方法进一步包括评估第一和第二抗体是否包含一个或多个以下氨基酸残基:
14.lcdr1的24位的氨基酸残基是赖氨酸;
15.lcdr2的54位的氨基酸残基是亮氨酸;
16.lcdr2的55位的氨基酸残基是天冬氨酸或谷氨酸;
17.lcdr2的56位的氨基酸残基是丝氨酸或苏氨酸;
18.lcdr3的96位的氨基酸残基是苯丙氨酸;或
19.hcdr2的61位的氨基酸残基是谷氨酸;
20.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。基于实施例中的观察结果,在特定cdr中包含一个或多个特定氨基酸表明抗体可具有有利的皮下吸收和生物利用度特征。
21.在一些实施方案中,此类方法包括选择包含一个或多个以下氨基酸残基的第一或第二抗体:
22.lcdr1的24位的氨基酸残基是赖氨酸;
23.lcdr2的54位的氨基酸残基是亮氨酸;
24.lcdr2的55位的氨基酸残基是天冬氨酸或谷氨酸;
25.lcdr2的56位的氨基酸残基是丝氨酸或苏氨酸;
26.lcdr3的96位的氨基酸残基是苯丙氨酸;或
27.hcdr2的61位的氨基酸残基是谷氨酸;
28.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
29.在一些实施方案中,此类方法进一步包括评估第一和第二抗体是否包含一个或多个以下氨基酸残基:
30.lcdr1的25位的氨基酸残基是丙氨酸或丝氨酸;
31.lcdr1的26位的氨基酸残基是丝氨酸;
32.lcdr2的52位的氨基酸残基是丝氨酸或苏氨酸;
33.lcdr3的89位的氨基酸残基是谷氨酰胺或缬氨酸;
34.lcdr3的90位的氨基酸残基是谷氨酰胺;
35.lcdr3的95位的氨基酸残基是脯氨酸;
36.lcdr3的97位的氨基酸残基是苏氨酸;
37.hcdr1的26位的氨基酸残基是甘氨酸;
38.hcdr1的27位的氨基酸残基是酪氨酸;
39.hcdr1的29位的氨基酸残基是苯丙氨酸;
40.hcdr1的30位的氨基酸残基是苏氨酸;
41.hcdr2的62位的氨基酸残基是赖氨酸;或
42.hcdr2的65位的氨基酸残基是甘氨酸;
43.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
44.在一些实施方案中,此类方法进一步包括选择包含一个或多个以下氨基酸残基的第一或第二抗体:
45.lcdr1的25位的氨基酸残基是丙氨酸或丝氨酸;
46.lcdr1的26位的氨基酸残基是丝氨酸;
47.lcdr2的52位的氨基酸残基是丝氨酸或苏氨酸;
48.lcdr3的89位的氨基酸残基是谷氨酰胺或缬氨酸;
49.lcdr3的90位的氨基酸残基是谷氨酰胺;
50.lcdr3的95位的氨基酸残基是脯氨酸;
51.lcdr3的97位的氨基酸残基是苏氨酸;
52.hcdr1的26位的氨基酸残基是甘氨酸;
53.hcdr1的27位的氨基酸残基是酪氨酸;
54.hcdr1的29位的氨基酸残基是苯丙氨酸;
55.hcdr1的30位的氨基酸残基是苏氨酸;
56.hcdr2的62位的氨基酸残基是赖氨酸;或
57.hcdr2的65位的氨基酸残基是甘氨酸;
58.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
59.本文还提供了通过本文所述的任何方法选择的用于皮下施用的抗体。在一些实施方案中,抗体是单克隆抗体,例如人源化mab。在一些实施方案中,抗体具有iggl或igg4同种型。
60.在另一个方面中,本文提供了产生与亲本抗体(例如mab)相比具有改善的皮下吸收和生物利用度的变体抗体的方法,此类方法包括产生亲本抗体的变体抗体,其中变体抗体具有高于亲本抗体的t
agg
和/或t
m起始
。在一些实施方案中,其中变体抗体具有低于亲本抗体的hpnip和/或hip。在一些实施方案中,此类方法还包括测量亲本抗体和变体抗体的ka和/或%f。在一些实施方案中,此类方法还包括测量亲本抗体和变体抗体的一个或多个pk参数,其中pk参数选自c
max
、t
max
、auc
0-inf
、cl/f和t
1/2
。
61.在一些实施方案中,亲本抗体和变体抗体都是单克隆抗体,例如人源化mab。在一些实施方案中,亲本抗体和变体抗体具有iggl或igg4同种型。在一些实施方案中,亲本抗体和变体抗体均包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区(hcdr)hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区(lcdr)lcdr1、lcdr2和lcdr3。
62.在一些实施方案中,此类方法还包括产生包含一个或多个以下氨基酸残基的变体抗体:
63.lcdr1的24位的氨基酸残基是赖氨酸;
64.lcdr2的54位的氨基酸残基是亮氨酸;
65.lcdr2的55位的氨基酸残基是天冬氨酸或谷氨酸;
66.lcdr2的56位的氨基酸残基是丝氨酸或苏氨酸;
67.lcdr3的96位的氨基酸残基是苯丙氨酸;或
68.hcdr2的61位的氨基酸残基是谷氨酸;
69.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
70.在一些实施方案中,产生变体抗体的方法还包括:
71.用赖氨酸替换亲本抗体的lcdr1的24位的氨基酸残基;
72.用亮氨酸替换亲本抗体的lcdr2的54位的氨基酸残基;
73.用天冬氨酸或谷氨酸替换亲本抗体的lcdr2的55位的氨基酸残基;
74.用丝氨酸或苏氨酸替换亲本抗体的lcdr2的56位的氨基酸残基;
75.用苯丙氨酸替换亲本抗体的lcdr3的96位的氨基酸残基;或
76.用谷氨酸替换亲本抗体的hcdr2的61位的氨基酸残基;
77.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
78.在一些实施方案中,此类方法还包括产生包含一个或多个以下氨基酸残基的变体抗体:
79.lcdr1的25位的氨基酸残基是丙氨酸或丝氨酸;
80.lcdr1的26位的氨基酸残基是丝氨酸;
81.lcdr2的52位的氨基酸残基是丝氨酸或苏氨酸;
82.lcdr3的89位的氨基酸残基是谷氨酰胺或缬氨酸;
83.lcdr3的90位的氨基酸残基是谷氨酰胺;
84.lcdr3的95位的氨基酸残基是脯氨酸;
85.lcdr3的97位的氨基酸残基是苏氨酸;
86.hcdr1的26位的氨基酸残基是甘氨酸;
87.hcdr1的27位的氨基酸残基是酪氨酸;
88.hcdr1的29位的氨基酸残基是苯丙氨酸;
89.hcdr1的30位的氨基酸残基是苏氨酸;
90.hcdr2的62位的氨基酸残基是赖氨酸;或
91.hcdr2的65位的氨基酸残基是甘氨酸;
92.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
93.在一些实施方案中,产生变体抗体的方法还包括:
94.用丙氨酸或丝氨酸替换亲本抗体的lcdr1的25位的氨基酸残基;
95.用丝氨酸替换亲本抗体的lcdr1的26位的氨基酸残基;
96.用丝氨酸或苏氨酸替换亲本抗体的lcdr2的52位的氨基酸残基;
97.用谷氨酰胺或缬氨酸替换亲本抗体的lcdr3的89位的氨基酸残基;
98.用谷氨酰胺替换亲本抗体的lcdr3的90位的氨基酸残基;
99.用脯氨酸替换亲本抗体的lcdr3的95位的氨基酸残基;
100.用苏氨酸替换亲本抗体的lcdr3的97位的氨基酸残基;
101.用甘氨酸替换亲本抗体的hcdr1的26位的氨基酸残基;
102.用酪氨酸替换亲本抗体的hcdr1的27位的氨基酸残基;
103.用苯丙氨酸替换亲本抗体的hcdr1的29位的氨基酸残基;
104.用苏氨酸替换亲本抗体的hcdr1的30位的氨基酸残基;
105.用赖氨酸替换亲本抗体的hcdr2的62位的氨基酸残基;或
106.用甘氨酸替换亲本抗体的hcdr2的65位的氨基酸残基;
107.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
108.本文还提供了通过上述任何方法产生的变体抗体。在一些实施方案中,变体抗体是单克隆抗体,例如人源化mab。在一些实施方案中,变体抗体具有iggl或igg4同种型。
109.在另一个方面中,本文提供了选择适于皮下施用的抗体的方法,所述方法包括选择包含一个或多个以下氨基酸残基的抗体:
110.lcdr1的24位的氨基酸残基是赖氨酸;
111.lcdr2的54位的氨基酸残基是亮氨酸;
112.lcdr2的55位的氨基酸残基是天冬氨酸或谷氨酸;
113.lcdr2的56位的氨基酸残基是丝氨酸或苏氨酸;
114.lcdr3的96位的氨基酸残基是苯丙氨酸;或
115.hcdr2的61位的氨基酸残基是谷氨酸;
116.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
117.在一些实施方案中,此类方法还包括选择包含一个或多个以下氨基酸残基的抗体:
118.lcdr1的25位的氨基酸残基是丙氨酸或丝氨酸;
119.lcdr1的26位的氨基酸残基是丝氨酸;
120.lcdr2的52位的氨基酸残基是丝氨酸或苏氨酸;
121.lcdr3的89位的氨基酸残基是谷氨酰胺或缬氨酸;
122.lcdr3的90位的氨基酸残基是谷氨酰胺;
123.lcdr3的95位的氨基酸残基是脯氨酸;
124.lcdr3的97位的氨基酸残基是苏氨酸;
125.hcdr1的26位的氨基酸残基是甘氨酸;
126.hcdr1的27位的氨基酸残基是酪氨酸;
127.hcdr1的29位的氨基酸残基是苯丙氨酸;
128.hcdr1的30位的氨基酸残基是苏氨酸;
129.hcdr2的62位的氨基酸残基是赖氨酸;或
130.hcdr2的65位的氨基酸残基是甘氨酸;
131.其中所有位置根据kabat编号进行编号,并且cdr由kabat和chothia的混合方式定义。
132.在一些实施方案中,此类方法还包括测量抗体的t
agg
和t
m起始
。在一些实施方案中,此类方法还包括测量抗体的hpnip和/或hip。在一些实施方案中,此类方法进一步包括测量抗体的ka和/或%f。在一些实施方案中,此类方法还包括测量抗体的一个或多个pk参数,其中pk参数选自c
max
、t
max
、auc
0-inf
、cl/f和t
1/2
。
133.在另一个方面中,本文提供了向受试者皮下施用抗体(例如mab,例如人源化mab)的方法;此类方法包括:测量抗体的t
agg
和t
m起始
,并确定抗体适于皮下施用,并将抗体皮下施用于受试者。在一些实施方案中,此类方法还包括测量抗体的hpnip和/或hip。在一些实施方案中,此类方法进一步包括测量抗体的ka和/或%f。在一些实施方案中,此类方法还包括测量抗体的一个或多个pk参数,其中pk参数选自c
max
、t
max
、auc
0-inf
、cl/f和t
1/2
。
134.如本文所用,除非本文另有说明或与上下文明显矛盾,否则在本公开的上下文中(特别是在权利要求的上下文中)使用的术语“一个(a)”、“一个(an)”、“该(the)”和类似术语应被解释为涵盖单数和复数。
135.如本文所用,术语“抗体”是指结合抗原的免疫球蛋白分子。抗体的实施方案包括单克隆抗体、多克隆抗体、人抗体、人源化抗体、嵌合抗体或缀合抗体。抗体可以是任何类别(例如igg、ige、igm、igd、iga)和任何亚类(例如iggl、igg2、igg3、igg4)。
136.示例性抗体是由四条多肽链组成的免疫球蛋白g(igg)型抗体:通过链间二硫键交联的两条重链(hc)和两条轻链(lc)。四条多肽链中的每一条的氨基末端部分包括主要负责抗原识别的约100-125个或更多个氨基酸的可变区。四条多肽链中的每一条的羧基末端部
分含有主要负责效应子功能的恒定区。每条重链由重链可变区(vh)和重链恒定区组成。每条轻链由轻链可变区(vl)和轻链恒定区组成。igg同种型可以进一步分为亚类(例如iggl、igg2、igg3和igg4)。
137.vh和vl区可以进一步细分为高变区,称为互补决定区(cdr),其散布有更保守的区域,称为框架区(fr)。cdr暴露在蛋白质的表面上,并且是抗体针对抗原结合特异性的重要区域。每个vh和vl由三个cdr和四个fr组成,从氨基末端到羧基末端按以下顺序排列:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。在本文中,重链的三个cdr称为“hcdr1、hcdr2和hcdr3”,轻链的三个cdr称为“lcdr1、lcdr2和lcdr3”。cdr含有大多数与抗原形成特异性相互作用的残基。氨基酸残基到cdr的分配可以根据众所周知的方案进行,包括kabat(kabat等,“sequences of proteins of immunological interest,”national institutes of health,bethesda,md.(1991))、chothia(chothia等,“canonical structures for the hypervariable regions of immunoglobulins”,journal of molecular biology,196,901-917(1987);al-lazikani等,“standard conformations for the canonical structures of immunoglobulins”,journal of molecular biology,273,927-948(1997))、north(north等,“a new clustering of antibody cdr loop conformations”,journal of molecular biology,406,228-256(2011))或imgt(可在www.imgt.org上获得的国际immunogenetics数据库;参见lefranc等,nucleic acids res.1999;27:209-212)中描述的那些。本文使用的cdr定义是kabat和chothia的混合。
138.本公开的抗体的示例性实施方案还包括抗体片段或抗原结合片段,其包含抗体的保留与抗原特异性相互作用的能力的至少一个部分,如fab、fab'、f(ab')2、fv片段、scfv、scfab、二硫键连接的fv(sdfv)、fd片段和线性抗体。
139.除非另有说明,否则如本文所用的术语“结合(bind和binds)”旨在意指蛋白质或分子与另一个蛋白质或分子形成化学键或吸引相互作用的能力,其导致两个蛋白质或分子的接近,如通过本领域已知的常用方法所确定的。
140.如本文所用,术语“受试者”是指哺乳动物,包括但不限于人、黑猩猩、猿、猴、牛、马、绵羊、山羊、猪、兔、狗、猫、大鼠、小鼠、豚鼠等。优选,受试者是人。
141.如本文所用,术语“治疗有效量”是指将引发受试者的生物学或医学反应的蛋白质或核酸或载体或组合物的量,所述反应例如为降低或抑制酶或蛋白质活性,或改善症状、缓解病症、减缓或延迟疾病进展,或预防疾病等。在非限制性实施方案中,术语“治疗有效量”是指蛋白质或核酸或载体或组合物施用于受试者时有效地至少部分缓解、抑制、预防和/或改善病症或障碍或疾病的量。
142.如本文所用,“治疗(treatment)”或“治疗(treating)”是指其中可以减缓、控制、延迟或停止本文公开的病症或疾病的进展或改善病症或疾病症状的所有过程,但不一定指示所有病症或疾病症状的完全消除。治疗包括施用蛋白质或核酸或载体或组合物以治疗患者,特别是人的疾病或病症。
实施例
143.材料和方法
144.六个mab的构建、表达和纯化
145.使用标准分子生物学方法将fab区克隆到mab表达载体中以与人κ轻链和人igg1或igg4重链的恒定区融合,并通过dna测序确认。使用cho表达系统表达所有igg。按照先前描述的(datta-mannan a等,mabs 2015;7:48 3-93)使用标准的蛋白-a琼脂糖(ge healthcare)亲和层析,然后是尺寸排阻层析方法,从培养物上清液中纯化mab。
146.食蟹猴fcrn结合亲和力的评估
147.按照之前所述的(datta-mannan a等,drug metabolism and disposition:the biological fate of chemicals 2007;35:86-94;datta-mannan a等,the journal of biological chemistry 2007;282:1709-17),在用编码αfcrn的可溶性部分和β
2-微球蛋白的质粒转染的293ebna细胞中表达的重组可溶性食蟹猴(cfcrn),并纯化蛋白质。按照之前所述的(datta-mannan a等,drug metabolism and disposition:the biological fate of chemicals 2007;35:86-94;datta-mannan a等,the journal of biological chemistry 2007;282:1709-17),使用biacore 3000仪器(ge healthcare)通过spr检测监测igg1和igg4分子与重组的、固定的cfcrn的相互作用。简言之,使用胺偶联化学(ge healthcare)将重组可溶性cfcrn固定于cm5传感器芯片的流动池2。cfcrn固定化表面密度为约300ru。第一流动池用作缺乏cfcrn的空白对照表面。所有结合实验均用溶解于含有0.005%tween 20,ph6的运行缓冲液磷酸盐缓冲盐水(pbs)或含有0.005%tween 20,ph7.4的pbs中的化合物进行,样品以100μl/min的流速运行30秒,解离时间为10分钟。pbs(ph 7.4)用作解离缓冲液。使用含有0.005%tween 20,ph6的pbs作为运行缓冲液用于进行确定igg对cfcrn的亲和力的实验。使用每种igg的0.00316μm至3.16μm的浓度范围来估算缔合和解离常数。通过从流动池2减去流动池1(未与fcrn偶联的空白流动池)的信号获得结合数据。然后将动力学(缔合和解离)数据同时拟合至igg-cfcrn相互作用的异质结合模型(biaevaluation,ver.4.1)。在ph6.0下igg的传感图的结合和解离相的数据曲线具有低残留和低χ2值。报告了kd的平均值,其说明了来自两个独立实验的最大结合分数的值。
148.mab等电点(pi)的评估
149.将毛细管等电聚焦(cief)方法用于测量所有mab的pi。用ph6的10mm柠檬酸盐将所有蛋白质样品稀释至1mg/ml。通过cief主溶液将最终蛋白质浓度稀释至0.25mg/ml,所述cief主溶液包括4%ph 3-10pharmalyte和4m尿素。使用(protein simple,san jose,ca)进行数据采集和分析,其通过compass for ice software(版本:1.1.5build id:0920)来实现。在数据采集期间,使用4.1和9.5的标志物,并通过施加1500伏1分钟,然后施加3000伏9分钟来分离各种带电物质。采集后,通过校正标志物位置来处理原始数据。色谱图内具有最高强度和面积的峰被指定为蛋白质的pi值。
150.用(malvern instruments ltd.,uk)仪器通过电泳光散射测量在10mm ph6组氨酸或10mm ph5乙酸盐中的1mg/ml mab溶液的ζ电位。在25℃下,将颗粒折射率设定为1.003。使用zetasizer软件基于溶液组分计算溶液折射率、粘度和介电常数。
151.评估融解温度或温度转变中点(midpoint of temperature transition,tm)和三级结构解折叠的起始温度
152.使用microcal vp-毛细管差示扫描量热法(dsc)系统(malvern instruments ltd.,malvern uk)进行温度转变中点(tm)的测量。在测量前将样品稀释至1mg/ml。通过以1℃/min的速率从20℃至105℃扫描温度来产生热谱图,并且在测量期间施加60psi恒定压
力。在蛋白质样品前运行四个安慰剂对以生成纯基线。使用microcal vp-毛细管dsc自动化分析软件2.0进行数据分析。t
m起始
定义为比热(c
p
)达到最大峰值的2%时的温度。还将每个蛋白质样品手动拟合至非-2状态(non-2state)模型以计算tm值。在模型拟合期间,肉眼选择峰并拟合直至卡方值不改变。
153.使用与静态光散射耦合的荧光来评估三级结构解折叠的起始温度。使用(unchained labs,pleasanton,ca)系统同时测量荧光和静态光散射。在测量期间,将1mg/ml的~8.8μl蛋白质样品加载到比色皿中;将样品在20℃下保持120s,然后以0.3℃/min的速率升温至95℃。在266nm激发后收集荧光和静态光散射(266nm)。测量后,将数据加载到分析软件中,提取原始荧光信号并用excel进一步处理。将三级结构解折叠起始(t
起始
)定义为荧光发射光谱的质心(bcm)(λm=∑
λfλ
λ/∑
λfλ
)与初始值(头5个点的平均值)相比增加0.4%时的温度。通过分析软件,分析了原始sls(静态光散射)数据,其中聚集的起始(t
agg
)被定义为一阶导数大于0的第一温度。
154.肝素柱结合和疏水相互作用柱结合
155.具有1ml容量的hitrap肝素hp sepharose(ge healthcare)和agilent 1100(santa clara,ca)系统用于评估mab的相对肝素结合亲和力。在实验中,将40μg蛋白质注射到柱中,并使用磷酸钾为20mm的ph 7.0的0至1m nacl的线性梯度洗脱,用214nm uv检测仪检测,且流速为1ml/min。
156.使用tosho npr butyl柱(san francisco,ca)和agilent 1100(santa clara,ca)系统来评估mab的相对疏水相互作用势。用50mm磷酸钾,ph 6.7,1m硫酸铵将每种mab的储存溶液稀释至0.5mg/ml。在实验中,将5μg蛋白质注射到柱中,并使用磷酸钾为50mm的ph 6.7的1至0m硫酸铵的线性梯度洗脱,用214nm uv检测仪检测,且流速为0.5ml/min。
157.记录每个样品的洗脱时间以评估相对肝素相互作用势(hpnip%)或疏水性相互作用势(hip%):
[0158][0159]
其中ti是样品的洗脱时间,to是梯度前的柱平衡时间,te是梯度结束的时间。
[0160]
sprague dawley大鼠药代动力学研究
[0161]
sprague dawley大鼠获自the jackson laboratory(bar harbor,me)。所有大鼠均为8至11周龄的未处理雄性,平均体重为0.3kg(+/-0.05kg)。pk研究在covance(madison,wi)进行,并根据动物使用方案(aup)和遵守covance institutional animal care and use committee(iacuc)法规进行设计和执行。以1mg/kg通过iv和sc给药mab,剂量体积为1ml/kg(剂量制备在pbs ph7.4中)。选择1mg/kg的剂量,因为对于任何抗体,在啮齿动物中预期没有靶标介导的药物处置(tmdd)。在剂量施用后0.083、1、6、12、24、48、72、96、120、168、240和336小时,从颈静脉收集血液样品,对于每种mab,重复2次或3次。使血样在环境温度下凝结,然后离心以获得血清。
[0162]
食蟹猴药代动力学研究
[0163]
所有猴的年龄在2至3岁之间,平均体重为3kg(+/-0.5kg)。pk研究在covance(madison,wi)进行,并根据动物使用方案(aup)和遵守covance iacuc规定进行设计和执
行。平台1和3mab以1或5mg/kg通过iv和sc给药,剂量体积为1ml/kg(剂量制备在pbs ph7.4中)。选择这些剂量是因为对于任何抗体在猴中预期没有tmdd,并且对于两个平台预期在线性pk范围内,从而允许跨剂量和途径的非靶标介导的pk参数估算。在剂量施用后1、6、12、24、48、72、96、168、240、336、432、504、600和672小时从股静脉收集血样,每种mab重复2次。使血样在环境温度下凝结,然后离心以获得血清。由于预期的将影响pk的tmdd,在食蟹猴中未评估平台2。
[0164]
生物分析测定和药代动力学数据分析
[0165]
对于每个分子,使用抗人igg或抗人κelisa测定sprague dawley大鼠或食蟹猴血清中的mab浓度。简言之,用羊抗人igg(jackson immunoresearch laboratories,inc.,west grove,pa)或羊抗人κ抗体(southern biotech,birmingham,al)包被微量滴定板的每个孔。在1:10最小所需稀释的样品预处理、洗涤和封闭后,将所有标准品、对照样品和研究样品加入板中,然后在室温下孵育1小时。洗涤后,经由用于比色响应的tmb microwell peroxidase substrate system(kpl,gaithersburg,md)用辣根过氧化物酶偶联的小鼠抗人igg(fc)抗体(southern biotech,birmingham,al)检测结合的分子。在450-493nm处读取板,参考标准为630nm。用在测量的样品中给药的抗体的已知量制备标准曲线,从中确定来自血浆或血清样品的浓度。使用watson lims软件版本7.4(thermo scientific inc.waltham,ma usa),用1/y2响应加权,使用4/5-参数逻辑曲线拟合,通过从标准曲线内插来确定来自每个mab的研究样品的浓度。平台1mab的标准曲线范围为8至500ng/ml,并且定量下限(lloq)定义为15ng/ml。平台2和3mab的标准曲线范围为4至384ng/ml,并且定量下限(lloq)定义为8ng/ml。
[0166]
使用winnonlin professional(版本3.2)软件包(pharsight corporation,mountain view,ca)计算药代动力学参数。使用基于统计矩理论的模型无关方法计算血清浓度-时间数据。计算的参数包括最大血清浓度(c
max
)、曲线下面积(auc
0-∞
)、清除率(cl)、消除半衰期(t
1/2
)和吸收速率(ka)。
[0167]
125
i-mab制备和食蟹猴中皮下组织结合定量
[0168]
用
125
i放射性标记平台1和平台3的一个子集的mab,以监测食蟹猴中皮下注射部位的损失百分比。使用琥珀酰亚胺基碘苯甲酸酯(sib)碘化方法进行用于皮下组织结合百分比计算的mab的放射性碘化(
125
i)。简言之,将2-3mci的na 125
i(perkin-elmer,billerica,ma)与5-8μg n-琥珀酰亚胺基-3-(三-n-丁基甲锡烷基)苯甲酸酯(american advanced scientific,college station,tx)反应以产生
125
i sib,其进而与1-2mg的每种测试mab反应,基本上如所述。通过在od-10脱盐柱(ge healthcare,pscataway,nj)上的凝胶过滤来纯化标记的蛋白质,以除去未缀合的
125
i sib,并通过uv光谱验证蛋白质浓度。通过将未标记的mab与相应的
125
i-mab在缓冲液中混合至终浓度为1mg/ml来制备给药溶液。使用组织穿刺取样方法,给药溶液的放射性比活性平均为0.1mci/mg。通过三氯乙酸(tca;sigma-aldrich,s.louis,mo)沉淀和使用agilent bio sec-3柱(gilent tchnologies,santa clara,xa)的尺寸排阻hplc来表征给药溶液的放射化学纯度。在所有给药溶液制剂中游离
125
i的百分比小于1%。
[0169]
所有食蟹猴均为治疗雄性,年龄为2至3岁,平均体重为3kg(+/-0.5kg)。研究在covance(madison,wi)进行,并在aup的范围内和遵守covance iacuc法规进行设计和执行。
由于预期的tmdd,未评估平台2mab。
125
i标记的平台1和3mab以0.1mg/kg/部位在胸部区域sc施用,剂量体积为每个注射部位300μl(剂量在pbs ph7.4中制备)。将
125
i标记的mabs 1p和1re或
125
i标记的mab 3p和3re1各自在抗体的预定和明显分离的注射部位施用至两组四只猴,每只动物多达六个施用部位。
[0170]
为了量化sc组织施用部位的mab损失,
125
i标记的mab施用的每个部位在指定的给药后时间进行8mm的皮肤穿刺活检。一个皮肤穿刺活检代表在给药后1和6小时的预定给药后时间的一个给药部位。收集后将皮肤活检穿刺物直接称重。使用γ计数器(wallac wizard 1480,perkin elmer,waltham,ma)测量每个皮肤穿刺计数,并计算与sc组织结合的百分比。出于数据归一化目的,每个mab的给药后1小时时间点皮肤穿刺放射性计数被认为是100%结合。比较给药后6小时收集的放射性数据,报告为相对于给药后1小时时间点的百分比结合的分数,用于计算、数据处理和随时间报告的sc部位的mab损失。
[0171]
结果
[0172]
igg分子的描述
[0173]
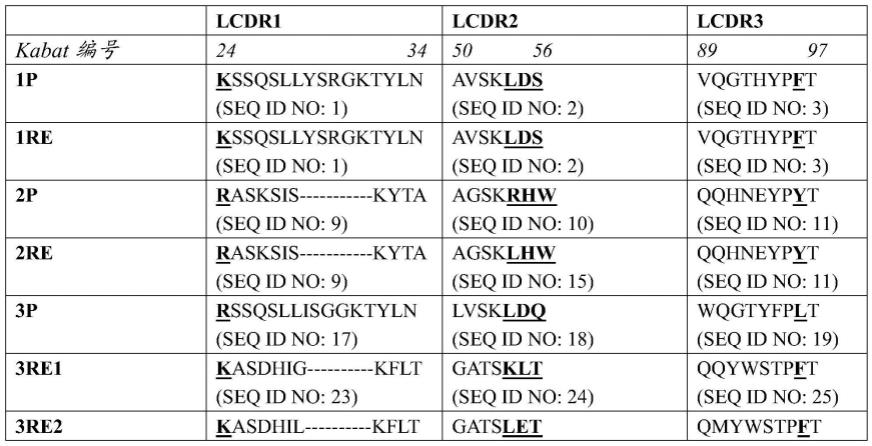
在本评估中,测试了跨越三个平台的几种人源化igg分子,以表征mab物理化学性质和sc施用后的pk参数之间的联结度(connectivity)。针对不同的未披露的目标开发每种抗体平台。在每个平台内,表征了两种或三种mab;亲本分子和一个或两个被设计为具有不同于亲本的物理化学性质的重新工程化的mab。平台1由两个人源化igg1分子组成,包括亲本(p)mab 1p,其包含分别具有seq id no:1、2、3中的序列的三个lcdr和分别具有seq id no:4、5、6中的序列的三个hcdr;和重新工程化的(re)mab 1re,其包含分别具有seq id no:1、2、3中的序列的三个lcdr和分别具有seq id no:7、5、8中的序列的三个hcdr。平台2和3各自由人源化igg4构建体组成。平台2中的分子是亲本mab 2p,其包含分别具有seq id no:9、10、11中的序列的三个lcdr和分别具有seq id no:12、13、14中的序列的三个hcdr;和重新工程化的mab 2re,其包含分别具有seq id no:9、15、11中的序列的三个lcdr和分别具有seq id no:12、16、14中的序列的三个hcdr。平台3由以下组成:亲本mab 3p,其包含分别具有seq id no:17、18、19中的序列的三个lcdr和分别具有seq id no:20、21、22中的序列的三个hcdr;重新工程化的mab 3re1,其包含分别具有seq id no:23、24、25中的序列的三个lcdr和分别具有seq id no:26、27、28中的序列的三个hcdr;和重新工程化的mab 3re2,其包含分别具有seq id no:29、30、31中的序列的三个lcdr和分别具有seq id no:32、33、28中的序列的三个hcdr(参见表1和2)。
[0174]
基于kabat编号比对cdr序列;并且cdr由kabat和chothia的混合方式定义。mab的关键重新工程化cdr残基用粗体字和下划线表示,其包括以下氨基酸残基中的一个或多个:lcdr1的24位的赖氨酸(k);lcdr2的54位的亮氨酸(l);lcdr2的55位的天冬氨酸(d)或谷氨酸(e);lcdr2的56位的丝氨酸(s)或苏氨酸(t);lcdr3的96位的苯丙氨酸(f);和hcdr2的61位的谷氨酸(e)(所有残基基于kabat编号来编号)。
[0175]
对重新工程化的mab的cdr序列的分析显示它们包含一个或多个以下的共同残基:lcdr1的25位的丙氨酸(a)或丝氨酸(s);lcdr1的26位的丝氨酸(s);lcdr2的52位的丝氨酸(s)或苏氨酸(t);lcdr3的89位的谷氨酰胺(q)或缬氨酸(v);lcdr3的90位的谷氨酰胺(q);lcdr3的95位的脯氨酸(p);lcdr3的97位的苏氨酸(t);hcdr1的26位的甘氨酸(g);hcdr1的27位的酪氨酸(y);hcdr1的29位的苯丙氨酸(f);hcdr1的30位的苏氨酸(t);hcdr2的62位的
赖氨酸(k);以及hcdr2的65位的甘氨酸(g)。
[0176]
表1.mab的轻链cdr序列
[0177][0178][0179]
表2.mab的重链cdr序列
[0180][0181]
总之,利用三个平台来剖析sc施用后电荷和疏水性在mab动力学中的作用。利用平台1分子来理解电荷的作用;平台2分子具有电荷和疏水性的组分;平台3分子主要受疏水性差异的影响。表3列出了构建体及其定性生物物理性质的高水平总结。
[0182]
表3:mab的一般描述*
[0183][0184][0185]
*所有分子都是人源化igg。“+”和
“‑”
符号分别表示特征的存在和不存在。基于电荷的和疏水性的相互作用势栏内的“+”符号的数量旨在提供mab跨平台和平台内的每个特征的相对优势的定性视角。基于电荷的和疏水性的相互作用势的定量值在表2中。*t
agg
是聚集起始的温度。^tmdd=靶标介导的药物处置
[0186]
mab的物理化学性质的表征
[0187]
表4通过旨在理解与sc施用后的pk和吸收相关的物理化学特征的一组分析总结了每个平台中mab的物理化学属性。使用多种正交方法评估由疏水性和基于电荷的机制控制的分子相互作用。此外,还评估了分子的总体热稳定性以及它们的聚集潜力。
[0188]
使用基于层析hic(疏水相互作用柱)的方法测定整体分子疏水性。数据表示为每种mab的相对疏水性相互作用百分比,以允许在三个mab平台内和跨三个mab平台进行比较;较大的疏水性相互作用百分比(hip)值表示对hic基质的亲和力增加。平台1分子显示相似且相对低的hip值;mab 1p和mab 1re的hip分别为1.3%和0.7%。相比之下,平台2和3分子都显示出比平台1mab高~10至~100倍的hip值(表4)。平台2构建体显示出mab 2p和mab 2re的相似hip值分别为约16%和约20%。平台3mab具有最广泛的hip多样性,mab 3p、3re1和3re2分别显示出~100%、~12%和~17%的值。
[0189]
表4:mab的生物物理和fcrn结合特性*
[0190][0191][0192]
*fcrn kd表示在ph6下的食蟹猴fcrn结合亲和力。hpnip是相对肝素结合相互作用势。hip是相对疏水相互作用势。pi是等电点。t
agg
是聚集起始的温度。t
m起始
是三级结构解折叠的起始。
[0193]
使用多种正交方法评估mab的电荷。通过测定pi和ζ电位评估整体mab表面电荷,而通过肝素结合相互作用确定局部表面电荷。使用毛细管等电泳测定pi值。结果表明了在每个平台内和跨每个平台进行比较时,分子的pi存在一些细微差异(《0.2个单位)(表4)。平台1mab ip和1re的pi值分别为8.8和9.1;平台2mab 2p和mab 2re分子的pi值分别为9.2和9.0;平台3mab 3p、3re1和3re2构建体分别具有8.3、8.5和8.5的pi值(表4)。使用电泳光散射测定mab的ζ电位。分子的ζ电位倾向于相似,除了分别观察到mab 1p和2p的不显著更低和更高的电位(表4)。使用填充到柱中的肝素包被的基质评估mab与肝素的相互作用。选择肝素是因为发现其在sc毛细血管上丰富。之前,报道了使用肝素包被的平板的分子与肝素的相互作用(datta-mannan a等,mabs 2015;7:483-93;datta-mannan a等,mabs 2015;7:1084-93)。该方法依赖于使用基于抗体的检测来检测肝素结合的mab。mab与检测抗体的交叉反应性的差异在分子间肝素结合的定量比较中产生了挑战(数据未显示)。因此,使用肝素柱和基于uv-vis的检测评估所有三个mab平台,以允许充分比较分子间的肝素相互作用。数据表示为每种mab的相对肝素相互作用百分比(hpnip),以允许在三个mab平台内和跨三个mab平台进行比较;较大的肝素相互作用百分比(hpnip)值表示对肝素基质的亲和力增加。平台1分子显示出~1.9倍差异的hpnip值;mab ip和mab 1re的hpnip分别为~52%和~28%。平台2分子显示出~1.7倍差异,其中mab 2p和mab 2re分别显示出~100%和~58%hpnip值。平台3mab的hpnip值分别为mab 3p、3re1和3re2的~32%、~19%和~46%。
[0194]
使用差示扫描量热法(dsc)测定mab的tm。在三个平台内,对于mab 1re相对于1p、mab 2re相对于2p以及mab 3re1和3re2各自相对于3p,观察到更高的融解温度起始(t
m起始
)(表4)。在平台3内的fab区、平台1分子的ch2结构域和平台2mab的ch3中观察到tm值的差异(表4)。除了dsc之外,还使用同时的静态光散射(sls)和荧光光谱来监测聚集(t
agg
)和三级结构解折叠(t
m起始
)的起始温度。蛋白质解折叠自由能依赖于温度的抛物线性质决定了在高温下蛋白质将容易解折叠。在从中等温度升温期间,蛋白质将在某一点部分解折叠,因此将进一步驱动分子间相互作用并最终聚集。sls对痕量聚集物敏感,并且非常适合于测量聚集
起始。同时,由于芳香族氨基酸(在这种情况下为色氨酸)的暴露,解折叠事件将触发荧光光谱的红移。因此,同时sls和荧光光谱法能够在热升温期间同时捕获聚集倾向和构象稳定性。结果报告于表4中。平台1mab 1p和mab 1re的聚集起始温度(t
agg
)分别为64.2℃和64.5℃。平台2mab中的t
agg
,从mab 2p的52.4℃提高至mab 2re的59.6℃。在平台3的情况下,t
agg
从mab 3p的55.6℃提高至mab 3re1的63.9℃和mab 3re2的61.4℃。同时,在重新工程化后,平台2mab的解折叠起始(t
m起始
)从57.6℃提高至62.0℃,尊敬地对应于mab 2p和2re,以及对于平台3mab,从对应于mab 3p的58.9℃至62.2℃和62.0℃,尊敬地对应于mab 3e1和3re2(表4)。
[0195]
使用先前报道的表面等离子体共振方法测量mab与固定的cfcrn的结合亲和力(datta-mannan a,drug metabolism and disposition:the biological fate of chemicals 2012;40:1545-55)。在ph 6.0下,mab对cfcrn的结合亲和力(kd)在三个mab平台上的范围为~93至121nm。对于任何mab,在ph7.4下未检测到与cfcrn的直接结合(数据未显示)。
[0196]
大鼠中mab的药代动力学评估
[0197]
由于在体内研究的持续时间内连续提取个体动物样品的能力,在向大鼠单次iv或sc施用后评估构建体的pk。此外,在大鼠中,由于低内源性抗原浓度或缺乏抗体与大鼠抗原的交叉反应性,没有一种分子具有靶标介导的组分清除(即靶标介导的药物处置或tmdd);因此,可以在不存在与tmdd相关的动力学复杂性的情况下评估mab的物理化学参数对pk的固有影响。
[0198]
单次1mg/kg iv或sc施用mab后的pk参数报告于表5中。总体而言,相对于各自的亲本mab(分别为1p、2p和3p),每个平台(1re、2re和3re1和3re2)中重新工程化的mab的表观清除率(cl/f)(和iv施用情况下的内在清除率)、sc吸收速率(ka)和sc生物利用度得到改善(表5)。
[0199]
表5:mab的大鼠药代动力学参数
[0200][0201]cmax
,最大观察血清浓度;t
max
,最大观察血清浓度的时间;auc
0-inf
,从时间零外推至无限时间的血清浓度曲线下面积;cl,iv施用后的清除率;cl/f,作为sc施用后生物利用度函数的表观清除率;t
1/2
,消除半衰期;ka,sc吸收速率;%f,sc生物利用度。na=不适用。^^^所有报告的auc。
[0202]
除非另有说明,否则^n=3/时间点,连续取样。仅对于%f报告,
#
n=2(标准偏差仅用于说明目的)。
[0203]a由两室药代动力学分析确定
[0204]
平台1和3变体mab在食蟹猴中的药代动力学
[0205]
sc空间在组成上跨物种变化;因此,作为理解大鼠中的sc pk发现在另一物种中是否有意义的手段,在食蟹猴中评估了分子子集的pk,因为该物种通常用于预测人抗体pk。在
单次1mg/kg iv或sc施用平台1和3mab后评估食蟹猴中的pk。未评估平台2分子,因为该组中的分子与食蟹猴靶标的已知交叉反应性导致iv施用后的非线性清除(数据未显示),因此可能混淆sc pk的解释。表6中报告了单次1mg/kg iv或sc施用平台1和3mab后的pk参数。总体而言,相对于它们各自的亲本mab(分别为1p和3p),每个平台(1re和3re1和3re2)中重新工程化的mab的表观清除率(cl/f)(和iv施用情况下的内在清除率)、sc吸收速率(ka)和sc生物利用度得到改善(表6)。
[0206]
表6:mab的食蟹猴药代动力学参数
[0207][0208][0209]cmax
,最大观察血清浓度;t
max
,最大观察血清浓度的时间;auc
0-inf
,从时间零外推至无限时间的血清浓度曲线下面积;cl,iv施用后的清除率;cl/f,作为sc施用后生物利用度函数的表观清除率;t
1/2
,消除半衰期;ka,sc吸收速率;%f,sc生物利用度。na=不适用。^n=3只食蟹猴/时间点。仅对于%f报告,#n=2(标准偏差仅用于说明目的)。除非另有说明,否则所有pk参数均由非隔室药代动力学分析确定。假设剂量比例,
^^
剂量从5mg/kg归一化至1mg/kg。^^^所有报告的auc。
[0210]a由两室药代动力学分析确定
[0211]
评估食蟹猴中平台1和3变体mab的相对sc组织缔合
[0212]
pk研究表明,相对于其重新工程化的对应物mab 1re和3re1,在sc施用后吸收到体循环中的亲本mab 1p和3p的量分别减少。作为开始剖析亲本mab的较低吸收程度和速率是
否是由于sc注射部位内的停留时间增加所致的手段,在食蟹猴中评估了平台1和3分子在施用后6小时注射部位处sc组织缔合的暴露。平台1mab的组织缔合显示,在给药后6小时,相对于重新工程化的mab 1re,sc组织内亲本mab 1p的保留增加~30%。在平台3的情况下,与重新工程化的mab 3re1相比,亲本mab 3p在sc施用后6小时具有~2倍增加的保留/缔合。相对于重新工程化的mab 1re和3re1,对应的亲本mab 1p和3p尊敬地显示出减少的sc生物利用度和降低的ka值。与sc组织缔合的发现一并地,数据表明了在注射部位增加的sc组织缔合减少了mab暴露。
[0213]
在大鼠和食蟹猴中测试多种mab物理化学因素(电荷、疏水性、聚集潜力和热稳定性)对人源化mab的sc吸收速率和程度的影响。这些测试的mab的清除不是靶标相互作用(tmdd)的结果,因为在物种(大鼠、食蟹猴或两者)中评估mab的动力学,其中存在的影响清除的抗原浓度不显著。pk也与异常fcrn结合无关,因为mab在ph6下显示出受体结合亲和力,其在针对具有良好表现的动力学的分子所报道的范围内,而在中性ph下没有直接的fcrn相互作用(表4)。因此,焦点在于理解上述物理化学参数在sc空间/解剖结构和组成的背景下的作用。重要的是,使用这种方法,发现几种物理化学性质对于其对sc施用后mab动力学的影响是至关重要的,并且发现这些中的一些(例如,t
m起始
和t
agg
)关于跨物种地sc相对于iv施用具有增加的联结度的独特性。
[0214]
在本文中,大鼠和食蟹猴中,相对于它们的重新工程化的对应物,三个平台中降低的sc生物利用度、减慢的sc吸收速率和增加的亲本mab清除率指向考虑固有的mab电荷、疏水性、聚集潜力和热稳定性,作为工程化这些分子以改善体内sc吸收速率和生物利用度的手段。这些因素中的每一个的相对贡献是抗体的基本体内特征的基础,并且严重影响旨在优化mab的pk性质的策略(chaparro-riggers j等,the journal of biological chemistry 2012;287:11090-7;datta-mannan a和wroblewski vj.drug metabolism and disposition:the biological fate of chemicals 2014;42:1867-72;igawa t等,nature biotechnology 2010;28:1203-7;yeung ya等,cancer res 2010;70:3269-77)。在这个研究中,高局部正电荷(如通过肝素相互作用测量的)、增加的疏水性相互作用势和导致增加的聚集潜力的低热稳定性的组合对sc吸收速率、表观清除率和生物利用度具有最大的负面影响,正如如与平台内和平台间的其他抗体相比,大鼠中mab 2p的pk发现所证明的。因此,建议考虑这些因素用于改善sc施用后的体内性能。考虑到sc施用对患者的增加的依从性和便利性益处,剖析影响mab的sc处置的因素将进一步扩展基于mab的治疗剂的药物能力并改善患者结果和体验。
[0215]
从关于全局(pi和ζ电位)和局部表面电荷(hpnip值)评估的mab的物理化学表征的比较中获得了相当大的见解。在这个比较中观察到跨三个平台的局部和全局电荷发现的灵敏度的一些相似性和许多差异。在mab表面电荷的全局评估研究中,mab的pi值范围为8.2至9.4;然而,在平台内,pi值是相似的,并且显示出不超过边缘0.3pi单位偏移。即使对于每个平台中的分子对也是如此,其显示出hpnip值的》2倍差异,这给出了对局部表面电荷的评估的额外见解,其是比pi更敏感的基于电势电荷的相互作用的量度。值得注意的是,考虑到mab的总体大分子量、平台内mab间改变的少数残基和抗体的有序三级结构,在给定平台内电荷的全局测量(如pi)的轻微变化并不令人惊讶。与pi观察类似,跨分子的ζ电位(其也是电荷的全局量度)的变化也是轻微的,且因此表明mab的相似的总体或全局表面净电荷。表
面电荷的这些全局评估难以完全解释sc pk发现/与其关联。先前的报告已经提出了关于评估pi或mab表面电荷的其他全局测量值及其与mab动力学的连接的一些复杂的发现(igawa t等,protein eng des sel 2010;23:385-92;li b等,mab 2014;6:12 55-64;sampei z等,plos one 2013;8:e57479;datta-mannan a等,mabs 2015;7:483-93)。在目前的研究中,用hpnip观察到mab平台内和跨mab平台的基于电荷的相互作用的最大差异,与全局表面电荷评估(即pi或ζ电位测量)相比,hpnip在检测局部电荷补丁方面更灵敏。所有分子在肝素柱相互作用测定中显示出一定水平的基于电荷的相互作用,表明对带负电荷的体内基质(如sc空间)具有非特异性结合(nsb)的潜力。所报道的发现表明,电荷显示的局部位置(即,在溶剂可及区域中,如cdr)是一个有影响的方面,考虑用于pk联结度属性的mab工程化方法时,在总体pi或ζ电位测定中可能表示不足,并且通过hpnip更好地表征。
[0216]
此外,对于影响pk的基于电荷驱动的nsb电位的组分,三个mab平台的物理化学表征表明疏水性相互作用也影响动力学。这些在sc空间内的体内相互作用的背景下可能更重要,其中在组成上存在可能有利于非共价疏水性相互作用的脂肪小叶、脂肪细胞、胶原蛋白和其他结缔组织。平台2和3(hip范围为~16-100%)具有比平台1(hip值为~1%)大得多的固有hip,表明电荷相关相互作用和疏水性相关相互作用的组合可能不同程度地影响这些分子的体内性能。有趣的是,基于疏水性的相互作用的固有差异显示出与三个mab平台上热诱导的三级结构解折叠和聚集潜能的起始的一些联结度。这个观察结果的起源是跨本文的三个平台的聚集起始(t
agg
)。在平台1mab的情况下,mab 1p(具有降低的sc%f的亲本)和mab 1re(具有较高sc%f的重新工程化的mab)的t
agg
;与基于疏水性的相互作用相比,这些mab主要显示出电荷的差异。相比之下,对于平台2mab 2p和mab 2re(分别从52.4℃至59.6℃)和平台3mab 3p、3re1和3re2(分别从55.6℃至63.9℃和61.4℃),t
agg
均得到改善;然而,与平台1mab不同,与基于电荷的相互作用相比,平台2和3分子在其疏水性方面显示出增加的差异。在平台2中观察到的相对于mab 2p的mab 2re改善的t
agg
,以及平台3中组合的mab 3re1》mab 3re2》mab 3p的t
agg
改善的相对等级顺序表明了具有增加的hip的分子对解折叠更敏感。这可能是由于试图通过更大的倾向掩埋溶剂可及的疏水区域以经由解折叠来改变构象,从而导致聚集增加的倾向。表面疏水性的降低导致聚集倾向降低,如通过t
agg
测量的。平台1mab的可比的t
agg
,其主要受基于电荷的相互作用(如在hpnip中观察到的)的影响,其通常在自缔合或聚集方面以排斥的方式表现,也支持这种假设。
[0217]
平台1mab是主要研究局部电荷相关的nsb对sc吸收和生物利用度的影响的合理替代物,因为这些分子在体外显示出强的基于电荷的结合信号和很少/没有疏水性相互作用势(在个位数百分比范围内的值)。由于sc空间由带负电荷的gag和其他蛋白聚糖的环境组成,大鼠和食蟹猴中,更多溶剂暴露的正电荷的亲本mab 1p具有减低的ka和sc生物利用度,表明了一种机制,其中mab 1p在sc空间内具有增强的驻留,与重新工程化的较低hpnip mab 1re相比,这降低了mab 1p被吸收到血液循环中的速率和程度。这个假设也得到了在食蟹猴中观察到的相对于mab 1re的mab 1p的sc组织缔合增加的支持。可能的是,相对于mab 1p,降低局部电荷相关的hpnip降低了mab 1re的nsb sc组织基质相互作用,这改善了mab 1re的体内pk。在本研究中利用的条件下,两种mab出现热不稳定性和聚集起始的温度略微不同,其中mab 1re(重新工程化的分子)在两个方面显示出比mab 1p略低的值。数据表明,对于具有很少/没有疏水性相互作用势但局部电荷相关的物理化学方面高的分子,热不稳定
性和聚集不是区别因素。与mab 1p相比,mab 1re改善的sc吸收和生物利用度可能与减少的非特异性组织摄取和随后的分解代谢有关,这得到了显示增强的nsb驱动的细胞缔合/结合导致mab降解的早期研究的支持(datta-mannan a等,mabs 2015;7:48 3-93)。有趣的是,虽然mab 1re和mab 1p的sc pk的相对等级顺序在食蟹猴和大鼠中是相同的,但观察到了跨物种的ka和生物利用度的量级的差异。这可能与跨物种的sc组织基质内组分的组成优势的已知差异有关;跨物种的这些sc组织组成差异也可能影响跨物种的相关性分析。尽管如此,虽然由于sc组织结构的差异,效应的规模可能在物种间不是完全可预测的,但是基于电荷的相互作用的非特异性性质强烈表明在人类中将预期类似的发现。
[0218]
与平台1相反,平台2和3促进了不同水平的电荷相关的nsb和疏水性相关的相互作用两者对sc吸收和生物利用度的影响的剖析/联结度。平台2mab对作为一组合理的分子来剖析基于电荷的相互作用的作用(mab 2p)显示出比具有基础的类似疏水性相互作用组分(mab 2p和2re分别具有~16%和~20%的hip值)的mab 2re高~2倍的hpnip。在大鼠中,与mab 2p相比,电荷重新工程化使mab 2re的动力学(即清除率)和sc吸收/生物利用度分别提高~4.5倍和~3倍。因此,类似于平台1的发现,平台2的数据也支持基于正电荷的相互作用可能通过增加的与sc组织基质的组分的结合/缔合而对sc吸收/生物利用度产生负面影响。然而,重要的是注意到尽管电荷再平衡显著改善了pk,但mab 2re在大鼠中仍然显示出分别为~1ml/hr/kg和~60%的相对清除率和sc生物利用度。工程化的mab 2re实际上在动力学上差于电荷不平衡的亲本mab 1p(cl/f和sc%f分别为~0.8ml/hg/kg和~70%),即使mab 1p和mab 2re具有相似的hpnip值。mab 1p和mab 2re变体之间的主要差异在于它们的hip值,其显示出mab 2re具有比mab 1p高~20倍的疏水性相互作用势。总之,数据表明平台2mab的疏水性相互作用势是影响mab 2p和2re清除率、sc吸收和生物利用度的nsb的重要组分。数据表明,进一步工程化以减少mab 2p和2re的hip将可能通过减少与sc组织基质的相互作用来改善它们的sc吸收。
[0219]
与平台2类似,平台3mab对于剖析疏水性相互作用对mab sc吸收的速率和程度以及生物利用度的作用也是有洞察力的。平台3与平台2相比的独特之处在于,平台3中的mab在其疏水性相互作用方面显示出更大的差异(平台3mab的hip差异~6-9倍,而平台2mab具有相当的hip值)以及在更小范围内的一些基于电荷的相互作用(mabs 3p、3re1和3re2的hpnip值为~20-46%,相比之下mab 2p和mab 2re的hpnip值》58%)。因此,虽然关于hip和hpnip不是完全无缝的,但平台3中电荷的影响比其他两个平台更轻微,确实定向地促进疏水性的询问。分别地,与mab 3re1相比,mab 3p高~9倍的hip值与食蟹猴中mab 3p比mab 3re1尊敬地快~1.6倍的清除率和低~2倍的生物利用度相关,以及与大鼠中mab 3p与mab 3re1相比尊敬地快~2.3倍的清除率和低~1.7倍的生物利用度相关。分别地,与mab 3re2相比,mab 3p高~6倍的hip值与食蟹猴中mab 3p与mab 3re2相比快~2倍的清除率和~相当的生物利用度相关,以及与大鼠中mab 3p与mab 3re2相比快~2.2倍的清除率和低~2倍的生物利用度相关。因此,从平台3显而易见的是,降低疏水性相互作用对pk是有益的;然而,与对平台2观察到的pk增强(清除率和sc生物利用度分别改善~4.5倍和~3倍)相比时,平台3改善更轻微。发现表明,对于本文的分子,存在电荷和疏水性相互作用两者时,减少基于电荷的相互作用可能比减少疏水性相互作用对增强动力学具有更大的影响。值得注意的是,缓慢的清除率(或sc途径的cl/f)与降低的hip之间的跨平台高度相关性,以及对于iv和
sc施用两者,降低的hpnip确实表明减少基于疏水性相互作用或电荷的缔合将跨物种地改善两种肠胃外途径的pk;因此,重要的是针对这两种性质优化分子。此外,跨平台的c
max
的剖析表明sc途径特定的与t
agg
和t
m起始
的高相关性。这可能与热稳定性在吸收到血液循环中前在sc组织基质内起到的作用增大有关。在大鼠和食蟹猴之间,通常不能始终观察到跨平台的ka或sc生物利用度和大多数物理化学性质(除了t
m起始
和ka)之间的高度相关性。虽然这可能部分是由于检查的mab的数量引起的,尽管实例有限,但这些参数中的一些的合理联结度表明,有必要用另外的分子进行进一步研究,以更好地描绘物种内和跨物种的这些关系。
[0220]
该发现表明具有增加的sc吸收速率和mab生物利用度的mab变体具有潜在降低的局部正电荷、较低的疏水性基质相互作用、较高的热稳定性和降低的热诱导聚集潜力。这些观察结果有助于假设结果可能与几种机制有关:1)由于与sc环境的负电荷组分(包括ecm的组分,包括gag)的电荷排斥而减少的sc组织基质相互作用;2)由于与脂肪组织的基于较差疏水性的范德华相互作用而减少的sc组织组分相互作用;和3)由于生理相关温度而减少的局部和全局解折叠的可能性,这可能导致sc空间中基于巨噬细胞的宿主防御机制的识别增加。mab 1re、2re和3re1和3re2降低的清除率(分别相对于mab 1p、2p和3p)可能是这些机制的结果,但程度不同。特别地,mab 1p和3p降低的sc吸收和生物利用度分别与高度的局部sc组织缔合和随后的降解(分别由于增加的基于电荷或疏水的相互作用的组合)良好相关。尽管由于食蟹猴中的tmdd,没有评估平台2分子的组织结合数据,但对于mab 2p,数据的优势表明由于电荷和疏水性相互作用两者,局部sc组织结合的程度可能增加。从概念的角度来看,与没有这些性质的分子相比,sc施用的动力学上较差的mab可能更大程度地非特异性地结合gag、脂肪小叶和细胞(脂肪细胞和内皮细胞)。因此,与sc组织组分的更大程度/强度的缔合不允许mab进入淋巴系统以随后释放到外周循环中。此外,增加内皮细胞与膜组分的缔合可能导致mab的细胞摄取增加,但缺乏从胞内降解中有效补救的能力。由于相互作用的非特异性性质,这可以将具有溶剂暴露电荷和增加的疏水潜力性质的mab分配远离再循环途径并朝向溶酶体降解。最后,局部组织相互作用和对体内较高生理温度的敏感性可能促进一些分子的三级结构的一些损失,这导致一些增加的聚集潜力。这些聚集物对于系统可能看起来是“外来的”,并且促进sc巨噬细胞的应答增加以促进mab的去除(即降解),使得这些不再可用于吸收。如果考虑如上所述的潜在细胞和sc组织基质相互作用的背景下的优势物理化学发现,这似乎是有意义的。
[0221]
总之,本文显示的数据表明,利用抗体工程化或筛选方法来改善mab生物治疗剂的sc生物利用度/药物能力时,有许多基于mab和sc基质中心的因素要考虑。应用基于理性的方法以整合这些因素的复杂性影响了mab的体内性能。由于mab和制剂的其他特征(化学稳定性、fcrn结合、溶解度、浓缩能力)可以影响sc处置和消除,因此研究这些其他机制对最终设计、工程化和筛选具有增加的治疗潜力的分子的相对作用将是有影响的。
[0222]
序列表
[0223]
seq id no:1
[0224]
kssqsllysrgktyln
[0225]
seq id no:2
[0226]
avsklds
[0227]
seq id no:3
[0228]
vqgthypft
[0229]
seq id no:4
[0230]
gytftryyin
[0231]
seq id no:5
[0232]
inpgsgntkynekfkg
[0233]
seq id no:6
[0234]
egttvy
[0235]
seq id no:7
[0236]
gytftdyyin
[0237]
seq id no:8
[0238]
egetvy
[0239]
seq id no:9
[0240]
rasksiskyta
[0241]
seq id no:10
[0242]
agskrhw
[0243]
seq id no:11
[0244]
qqhneypyt
[0245]
seq id no:12
[0246]
gyaftsflie
[0247]
seq id no:13
[0248]
snprtgrtkykskfrg
[0249]
seq id no:14
[0250]
effdy
[0251]
seq id no:15
[0252]
agsklhw
[0253]
seq id no:16
[0254]
snprtggrkykekfrg
[0255]
seq id no:17
[0256]
rssqsllisggktyln
[0257]
seq id no:18
[0258]
lvskldq
[0259]
seq id no:19
[0260]
wqgtyfplt
[0261]
seq id no:20
[0262]
gktfwsygin
[0263]
seq id no:21
[0264]
iyigtgytepnpkykg
[0265]
seq id no:22
[0266]
iggyygnfdq
[0267]
seq id no:23
[0268]
kasdhigkflt
[0269]
seq id no:24
[0270]
gatsklt
[0271]
seq id no:25
[0272]
qqywstpft
[0273]
seq id no:26
[0274]
gykftryvmh
[0275]
seq id no:27
[0276]
inpyndgvnynekfkg
[0277]
seq id no:28
[0278]
nwdtgl
[0279]
seq id no:29
[0280]
kasdhilkflt
[0281]
seq id no:30
[0282]
gatslet
[0283]
seq id no:31
[0284]
qmywstpft
[0285]
seq id no:32
[0286]
gykftryvmh
[0287]
seq id no:33
[0288]
inpyndgtnynekfkg
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1