抑制针对载体递送的治疗性蛋白质的免疫应答的方法与流程
本公开一般涉及包含用于基因治疗、基因编辑或其他应用的多核苷酸的载体。关于序列表的声明与本技术相关的序列表以文本格式提供,而不是纸质副本,并通过引用并入说明书。包含序列表的文本文件的名称为sctb_010_01wo_st25.txt。该文本文件为约20kb,创建于2021 10月18日,通过efs-web以电子方式提交。
背景技术:
0、发明背景
1、各种类型的载体,包括但不限于病毒载体,可用于在体内将目标多核苷酸序列递送至受试者的细胞。当向受试者施用这种载体时,受试者可能对由载体编码的治疗性蛋白质产生免疫应答。这种免疫应答可能会降低载体的效力。本领域需要与抑制针对由载体编码的治疗性蛋白质的免疫应答和/或用载体治疗受试者有关的组合物和方法。
技术实现思路
1、本公开的一个方面涉及一种用于在有需要的受试者中抑制针对包含编码治疗性蛋白质的多核苷酸的载体的免疫应答、用于在有需要的受试者中表达治疗性蛋白质和/或用于在有需要的受试者中治疗与治疗性蛋白质的表达减少相关的疾病或病症的方法,所述方法包括:a)选择受试者作为需要用载体进行治疗的受试者,和然后b)向受试者施用包含治疗性蛋白质或者其同源物或功能性变体、任选地其免疫相关变体的组合物。
2、在一些实施方案中,所述方法包括向受试者施用载体,所述载体包含编码治疗性蛋白质的多核苷酸。
3、在一些实施方案中,所述方法包括向受试者施用包含治疗性蛋白质的组合物,以及向受试者施用包含编码治疗性蛋白质的多核苷酸的载体。
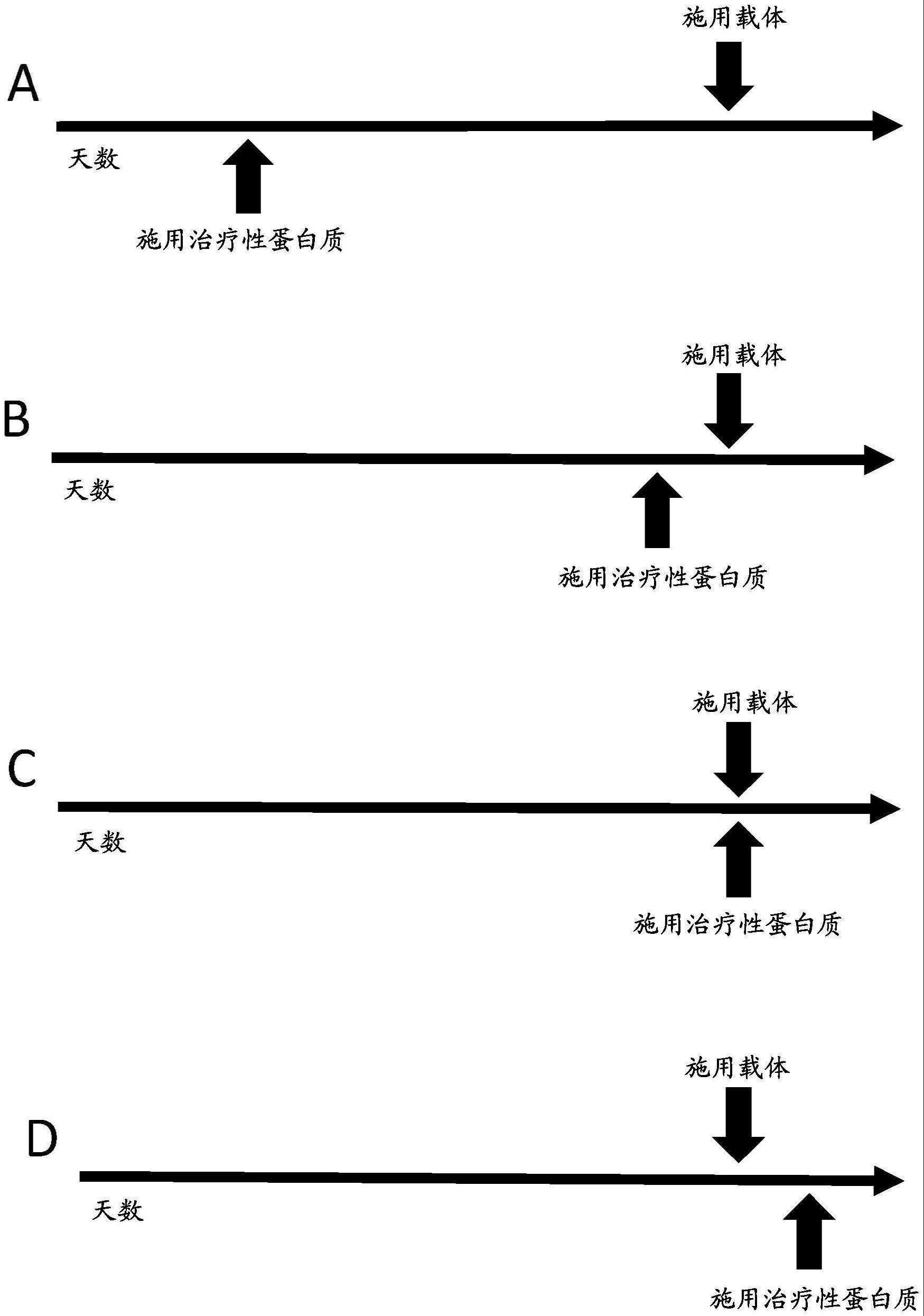
4、在一些实施方案中,在施用载体之前施用治疗性蛋白质。
5、在一些实施方案中,在施用载体之后施用治疗性蛋白质。
6、在一些实施方案中,在施用载体的大约同时施用治疗性蛋白质。
7、在一些实施方案中,施用的治疗性蛋白质与由载体编码的治疗性蛋白质相同。
8、在一些实施方案中,施用的治疗性蛋白质与由载体编码的治疗性蛋白质相似但不相同。
9、在一些实施方案中,载体是病毒载体。
10、在一些实施方案中,病毒载体是腺相关病毒(aav)载体。
11、在一些实施方案中,aav载体是aav1载体。
12、在一些实施方案中,以1x107至1x1015 gc/kg的剂量施用载体。
13、在一些实施方案中,以1x109至1x1013 gc/kg的剂量施用载体。
14、在一些实施方案中,以2.5x1011 gc/kg的剂量施用载体。
15、在一些实施方案中,肌肉内施用治疗性蛋白质。
16、在一些实施方案中,静脉内施用治疗性蛋白质。
17、在一些实施方案中,治疗性蛋白质或者其同源物或功能性变体与受试者的内源性蛋白质或者内源性蛋白质的功能性片段具有至少95%的同一性。
18、在一些实施方案中,治疗性蛋白质被免疫系统识别为自身抗原。
19、在一些实施方案中,以有效抑制针对由载体编码的治疗性蛋白质的免疫应答的剂量向受试者施用组合物。
20、在一些实施方案中,治疗性蛋白质包括抗体或其抗原结合片段。
21、在一些实施方案中,治疗性蛋白质是单克隆抗体。
22、在一些实施方案中,单克隆抗体是特异性结合神经生长因子(ngf)的单克隆抗体。
23、在一些实施方案中,单克隆抗体是特异性结合红细胞生成素(epo)、il-31、血管内皮生长因子(vegf)、cd20、人表皮生长因子受体2(her 2)、肿瘤坏死因子(tnf)、免疫球蛋白e(ige)、il-2、il-33、cd52、cd3、cd19、il-6、il-4、il-4r、il-4r trap、il-13、il-13r、il-5、il-5r、il-5r trap、il-33r、st2受体、il-1ra、α4β7整合素、il-12、il-23、粒细胞-巨噬细胞集落刺激因子(gm-csf)、gm-csf受体、程序性细胞死亡蛋白1(pd-1)、程序性死亡配体1(pd-l1)、细胞毒性t淋巴细胞相关蛋白4(ctla-4)、b7-1(cd80)或b7-2(cd86)的单克隆抗体。
24、在一些实施方案中,治疗性蛋白质是双特异性抗体。双特异性抗体可以特异性结合cd3(“bite”)。在一些实施方案中,治疗性蛋白质是与免疫效应细胞(例如,t细胞、nk细胞)和目标抗原结合以促进细胞杀伤的抗体样分子。
25、在一些实施方案中,治疗性蛋白质是胰高血糖素样肽1(glp-1)、胰岛素、促性腺激素释放激素(gnrh)或米勒抑制物质(mis)/抗米勒激素(amh)。
26、在一些实施方案中,治疗性蛋白质是glp-1、胰岛素、gnrh或mis/amh的激动剂或拮抗剂。
27、在一些实施方案中,受试者是猫类。
28、在一些实施方案中,受试者是犬类。
29、在一些实施方案中,受试者是人类。
30、在一些实施方案中,治疗性蛋白质是猫类单克隆抗体或猫源化单克隆抗体。
31、在一些实施方案中,受试者是幼年的或成年的。
32、在一些实施方案中,以小于约50mg/kg、小于约25mg/kg、小于约10mg/kg、小于约5mg/kg、小于约1mg/kg或小于约0.5mg/kg的剂量施用治疗性蛋白质。
33、在一些实施方案中,以至少约0.01mg/kg、至少约0.05mg/kg、至少约0.1mg/kg、至少约1mg/kg、至少约2mg/kg、至少约5mg/kg、至少约10mg/kg的剂量或至少约15mg/kg的剂量施用治疗性蛋白质。
34、在一些实施方案中,以约0.1mg/kg至约50mg/kg、约1mg/kg至约50mg/kg、约0.1mg/kg至约25mg/kg、约1mg/kg至约25mg/kg或约5mg/kg至约10mg/kg的剂量施用治疗性蛋白质。
35、在一些实施方案中,以约0.1mg/kg、约1mg/kg、约2mg/kg、约5mg/kg、约10mg/kg或约15mg/kg的剂量施用治疗性蛋白质。
36、在一些实施方案中,以对于治疗性蛋白质的亚治疗剂量施用治疗性蛋白质。
37、在一些实施方案中,在施用载体之前少于6周、少于5周、少于4周、少于3周、少于2周、少于1周、少于5天、少于3天或少于一天,向受试者施用治疗性蛋白质。
38、在一些实施方案中,免疫应答是响应受试者中用载体转导的细胞的治疗性蛋白质的表达,受试者针对治疗性蛋白质的基于抗体的免疫应答。
39、在一些实施方案中,所述方法将宿主抗体应答减少至少约20%。
40、在一些实施方案中,所述方法将宿主抗体应答减少至少约50%。
41、在一些实施方案中,所述方法将宿主抗体应答减少至少约75%。
42、在一些实施方案中,所述方法将宿主抗体应答减少至少约90%。
43、在一些实施方案中,在施用载体之后1天、之后2天、之后5天、之后7天、之后10天或之后20天,施用治疗性蛋白质。
44、在一些实施方案中,受试者对于治疗性蛋白质是未接受过治疗的。
45、在一些实施方案中,在允许在施用载体时存在可测量水平的治疗性蛋白质的时间,施用治疗性蛋白质。
46、在一些实施方案中,在预期治疗性蛋白质由载体表达之前,施用治疗性蛋白质。
47、根据以下对本发明的详细描述,本发明的其他方面和优点将显而易见。
- 还没有人留言评论。精彩留言会获得点赞!