药代动力学被改善的含CD1d配体化合物的脂质体制剂的制作方法
本发明涉及药代动力学被改善的含cd1d配体化合物的脂质体制剂。更详细而言,本发明涉及通过均匀地调整粒径从而改善药代动力学的含cd1d配体化合物的脂质体制剂。
背景技术:
1、移植物抗宿主病(gvhd)是与同种异体造血干细胞移植相伴的并发症之一,是来源于供体的淋巴细胞将接受者的器官视为异物而攻击的疾病。在由移植引起的、供血者的免疫系统攻击并破坏受血者的全身组织的疾病中,有移植前期的急性gvhd和移植后期的慢性gvhd。另外,已知gvhd也会因输血而发病。
2、cd4+cd25+foxp3+调节性t细胞(treg)被认为是维持中枢及末梢的免疫耐受的关键角色。动物实验显示,该细胞通过恢复对自身抗原以及对同种异体抗原的免疫耐受,从而预防或改善自身免疫疾病、移植物排斥等t细胞介导疾病。在人及小鼠两种试验中,验证了tregs在gvhd控制中的极重要作用。然而,由于该细胞群的数量少,因此以treg为基础的治疗方式的开发受到阻碍。在生物体内有效地增加功能性tregs的分子的发现能够有助于用于治疗gvhd以及其他免疫疾病的新疗法的开发。在原位(in situ)使tregs活化、增加的多种策略正在出现。
3、α-半乳糖神经酰胺(α-galcer)作为在抗原呈递细胞上表达的cd1d分子的配体发挥功能。cd1d分子是具有用于脂质抗原呈递的抗原结合性沟的、非多态性肿瘤组织相容性复合体(mhc)i类抗原呈递分子。当α-galcer呈递给表达于树突状细胞(dcs)、巨噬细胞、及b细胞等多种细胞种上的cd1d分子时,其被表达于恒定nkt(inkt)细胞上的恒定t细胞(tcr)识别,以cd1d限制性方式将inkt细胞活化。cd1d限制性inkt细胞活化会带来th1及th2细胞因子两者快速且大量的释放,其将inkt细胞与以往的t细胞区分开,是表明天然免疫及获得性免疫两者中的重要免疫控制功能的独特特征。krn7000((2s,3s,4r)-1-o-(α-d-吡喃半乳糖基)-2-(n-二十六烷酰基氨基)-1,3,4-十八烷三醇,(2s,3s,4r)-1-o-(α-d-galactopyranosyl)-2-(n-hexacosanoylamino)-1,3,4-octadecanetriol)是最初从海绵中发现的α-galcer的合成衍生物。
4、显示krn7000在水性形态中作为免疫刺激剂发挥作用,但发现krn7000的脂质体制剂会诱导抗原特异性免疫抑制或耐受(专利文献1、非专利文献1、2)。以前的试验表明,利用脂质体化krn7000靶向不同的细胞时会带来不同的免疫调节性反应。即,水性的krn7000主要呈递给dcs,结果,在由dcs分泌的il-12的存在下刺激inkt细胞。与此相对,脂质体化krn7000主要呈递至b细胞上,通过与inkt细胞的相互作用,诱导从inkt细胞及b细胞两者产生il-10,引起免疫耐受性的dcs的增殖(非专利文献1)。然后,在作为模型抗原的卵白蛋白的存在下观察到抗原特异性cd4+cd25+foxp3+细胞的产生诱导(非专利文献1、2)。认为脂质体的脂质组成增强了b细胞对脂质体化krn7000的摄取,结果,免疫反应偏向耐受性的方向。
5、本技术的发明人揭示,脂质体化krn7000(rgi-2001)能够通过诱导treg来诱导同种异体抗原特异性耐受(非专利文献3)。在小鼠急性gvhd模型中,通过单次施予rgi-2001,小鼠的生存显著地延长。已知来自供体的cd4+foxp3+tregs经强化的增殖是关键机理。骨髓移植(bmt)后,早期诱导宿主同种异体抗原特异性免疫抑制,但对第三方的同种异体抗原、白细胞的响应未被抑制。此外,rgi-2001在小鼠慢性gvhd模型中也确认到减轻症状的效果,因此根据这些结果表明,rgi-2001能够成为预防急性gvhd和慢性gvhd两者的新型治疗法(非专利文献4)。
6、在人的临床试验中也确认了rgi-2001向gvhd的可应用性(非专利文献5)。在接受了同种异体造血干细胞移植的29名患者的治疗中,于第0天进行单次静脉内施予rgi-2001的第1/2a期临床试验。经rgi-2001治疗的一些患者在移植后1~3周内tregs(cd4+cd25+cd127lofoxp3+)的数目显著上升。在伴随tregs数目的增加具有响应的患者中,与非响应者相比,gvhd更显著地降低。
7、rgi-2001适用于器官移植的可能性已在小鼠心脏移植模型中得到确认(非专利文献6、7)。对受体小鼠照射亚致死量的放射线后,移植供体小鼠的脾脏细胞和骨髓细胞时,通过同时施予rgi-2001和cd40-cd40l阻断抗体,受体小鼠产生骨髓嵌合体,长期维持抑制源自供体的心脏、皮肤的排斥。
8、专利文献2中公开了脂质体制造技术,其在使用中空纤维透析柱进行透析的工序中,通过简单地控制透析后的被透析液(例如,脂质体液)的浓度,能够得到具有所期望浓度的被透析液(例如,脂质体液)。
9、专利文献3公开了脂质粒子的制造技术,其以脂质粒子不稳定化的醇浓度对溶解有脂质的含醇溶液进行1次稀释后,进而进行2次稀释,由此得到稳定化的粒子,此处,通过调整从1次稀释至2次稀释为止的保持时间,能够在保持均匀的粒度分布的状态下控制脂质粒子的粒径。
10、非专利文献8公开了使用pet技术来分析各种粒径的脂质体的药代动力学的结果。
11、现有技术文献
12、专利文献
13、专利文献1:wo2005/120574a1
14、专利文献2:wo2016/024510a1
15、专利文献3:wo2019/088193a1
16、非专利文献
17、非专利文献1:tamura y等人,biochem biophys res commun369:485-492,2008
18、非专利文献2:ishii y等人,front biosci 13:6214-6228,2008
19、非专利文献3:duramad o等人,biol blood marrow transplant 17:1154-1168,2011
20、非专利文献4:du jing等人,blood 129:3121-3125,2017
21、非专利文献5:chen yb等人,biol blood marrow transplant 23:625-634,2017
22、非专利文献6:hirai等人,am j transplant 14:1154-1168,2014
23、非专利文献7:hirai等人,am j transplant 16:426-439,2016
24、非专利文献8:oku,n等人,biochim.biophys.acta,1238:86-90,1995
技术实现思路
1、发明所要解决的课题
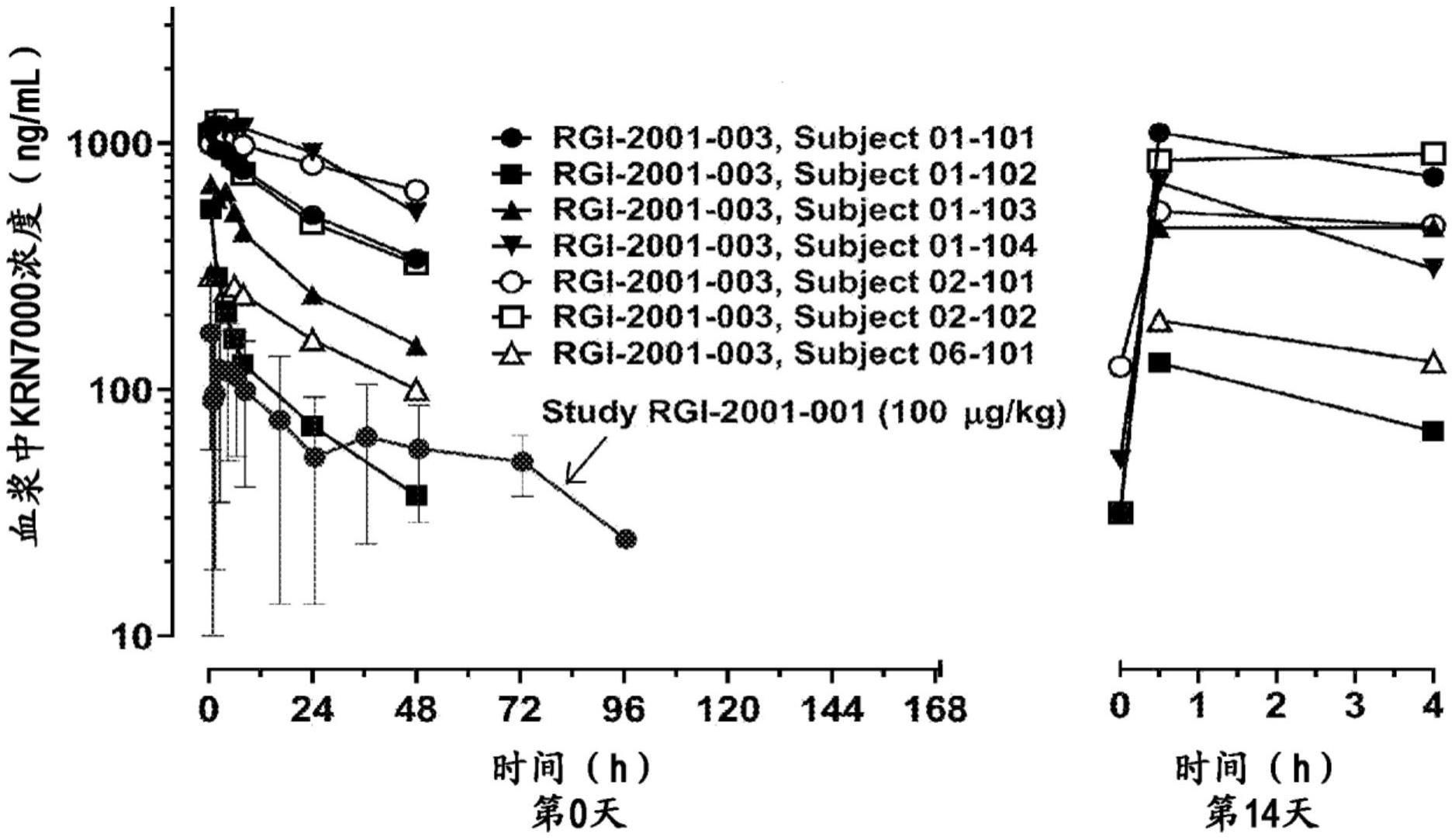
2、如上文所述,在以预防gvhd为目的的脂质体化krn7000的第1/2a期临床试验中,观察到显示显著的治疗响应的患者,另一方面也观察到未发现充分响应的患者。因此,对其原因进行研究,结果可知药物动力学不稳定,血浆中krn7000浓度在刚施予后为低值,之后暂时上升,但又再次下降。根据该结果表明,为了充分发挥脂质体化krn7000的药效,从刚施予后起长时间在血中滞留是重要的,第1/2a期临床试验中使用的制剂(rgi-2001-001)可能并不满足该条件。
3、本发明的目的在于提供能够在血中长期滞留、能够长时间维持高的血中cd1d配体浓度的含cd1d配体的脂质体。
4、用于解决课题的手段
5、本技术的发明人为解决上述课题而进行了深入研究,结果查明,血中动力学不稳定性的主要原因在于第1/2a期临床试验中使用的脂质体的粒径。第1/2a期临床试验中使用的脂质体化krn7000制剂(rgi-2001-001)中的脂质体的平均粒径为约120nm,但是不从rgi-2001-001改变krn7000含量及脂质组成,重新制备平均粒径收敛于100nm左右的脂质体制剂(rgi-2001-003),并在造血干细胞移植后对患者进行静脉内施予时,令人惊奇地,成功改善了药物动力学,使krn7000的最大血药浓度上升,延长血液半衰期(the blood half-life)。向小鼠静脉内施予这些制剂,测定血浆中的ifn-γ及il-4浓度,结果,就il-4而言,rgi-2001-003施予组高于rgi-2001-001施予组,但就ifn-γ而言,rgi-2001-003施予组反而低于rgi-2001-001施予组,表明rgi-2001-003可能具有更有效地诱导treg的特性。本技术的发明人基于上述见解进一步进行研究,完成了本发明。
6、即,本发明涉及以下的方案。
7、[1]脂质体制剂,其是包含含有cd1d配体化合物的脂质体群的脂质体制剂,该脂质体群的平均粒径为90~110nm,粒径分布的多分散度为0.2以下。
8、[2]如[1]所述的脂质体制剂,其中,平均粒径为92.9~101.0nm。
9、[3]如[1]或[2]所述的脂质体制剂,其中,粒径分布的多分散度为0.133以下。
10、[4]如[1]~[3]中任一项所述的脂质体制剂,其中,粒径小于50nm的脂质体的数目为该脂质体群的整体的10%以下。
11、[5]如[1]~[4]中任一项所述的脂质体制剂,其中,粒径超过450nm的脂质体的数目为该脂质体群的整体的10%以下。
12、[6]如[1]~[5]中任一项所述的脂质体制剂,其中,在温度25℃、相对湿度60%rh的条件下,平均粒径以90~110nm维持至少1个月。
13、[7]如[1]~[6]中任一项所述的脂质体制剂,其中,cd1d配体化合物为α-半乳糖神经酰胺。
14、[8]如[7]所述的脂质体制剂,其中,α-半乳糖神经酰胺为(2s,3s,4r)-1-o-(α-d-吡喃半乳糖基)-2-(n-二十六烷酰基氨基)-1,3,4-十八烷三醇。
15、[9]如[1]~[8]中任一项所述的脂质体制剂,其中,该脂质体群以脂质体悬浮液的形式被包含。
16、[10]如[9]所述的脂质体制剂,其中,脂质体悬浮液的ph为5.8~6.8。
17、[11]如[1]~[8]中任一项所述的脂质体制剂,其中,该脂质体群以冷冻干燥物的形式被包含。
18、[12]如[1]~[11]中任一项所述的脂质体制剂,其用于注射施予。
19、[13]如[1]~[12]中任一项所述的脂质体制剂,其用于移植物抗宿主病的预防或治疗。
20、[14]如[13]所述的脂质体制剂,其中,移植物抗宿主病是由同种异体造血干细胞移植引起的。
21、[15]如[1]~[12]中任一项所述的脂质体制剂,其用于器官移植排斥的预防或治疗。
22、[16]如[15]所述的脂质体制剂,其中,器官移植为同种异体器官或细胞的移植。
23、[17]如[15]所述的脂质体制剂,其中,器官移植为异种器官或细胞的移植。
24、[18]降低对象的移植物抗宿主病的发病风险的方法,其包括向具有移植物抗宿主病的发病风险的该对象施予有效量的[1]~[12]中任一项所述的脂质体制剂。
25、[19]如[18]所述的方法,其中,具有移植物抗宿主病的发病风险的对象为接受了同种异体的组织或细胞的移植的对象、或者预定接受同种异体的组织或细胞的移植的对象。
26、[20]对象的移植物抗宿主病的治疗方法,其包括向罹患移植物抗宿主病的该对象施予有效量的[1]~[12]中任一项所述的脂质体制剂。
27、[21]如[18]~[20]中任一项所述的方法,其中,移植物抗宿主病是由同种异体造血干细胞移植引起的。
28、[22]降低对象的器官移植排斥的发病风险的方法,其包括向具有器官移植排斥的发病风险的该对象施予有效量的[1]~[12]中任一项所述的脂质体制剂。
29、[23]如[22]所述的方法,其中,具有器官移植排斥的发病风险的对象为接受了同种异体或异种的器官或细胞的移植的对象、或者预定接受同种异体或异种的器官或细胞的移植的对象。
30、[24]对象的器官移植排斥的治疗方法,其包括向罹患器官移植排斥的该对象施予有效量的[1]~[12]中任一项所述的脂质体制剂。
31、[25]如[22]~[24]中任一项所述的方法,其中,器官移植为同种异体器官或细胞的移植。
32、[26]如[22]~[24]中任一项所述的方法,其中,器官移植为异种器官或细胞的移植。
33、[27]如[1]~[12]中任一项所述的脂质体制剂,其用于移植物抗宿主病的预防或治疗。
34、[28]如[27]所述的脂质体制剂,其中,移植物抗宿主病是由同种异体造血干细胞移植引起的。
35、[29]如[1]~[12]中任一项所述的脂质体制剂,其用于器官移植排斥的预防或治疗。
36、[30]如[29]所述的脂质体制剂,其中,器官移植为同种异体器官或细胞的移植。
37、[31]如[29]所述的脂质体制剂,其中,器官移植为异种器官或细胞的移植。
38、[32][1]~[12]中任一项所述的脂质体制剂在移植物抗宿主病的预防或治疗用医药的制造中的用途。
39、[33]如[32]所述的用途,其中,移植物抗宿主病是由同种异体造血干细胞移植引起的。
40、[34][1]~[12]中任一项所述的脂质体制剂在器官移植排斥的预防或治疗用医药的制造中的用途。
41、[35]如[34]所述的用途,其中,器官移植为同种异体器官或细胞的移植。
42、[36]如[34]所述的用途,其中,器官移植为异种器官或细胞的移植。
43、发明的效果
44、通过本发明,提供能够在血中长期滞留且能够长时间维持高的血中cd1d配体浓度的含cd1d配体的脂质体制剂。本发明的脂质体制剂能够有效地诱导treg,因此可期待对gvhd、器官移植排斥、自身免疫疾病等的优异的预防或治疗效果。
- 还没有人留言评论。精彩留言会获得点赞!