防治骨质疏松的中药组合物及其制备方法与流程
1.本技术属于药物技术领域,尤其涉及一种防治骨质疏松的中药组合物及其制备方法。
背景技术:
2.骨质疏松症(osteoporosis,op)是一种以骨量下降,骨微结构损坏,导致骨骼脆性增加,易发生骨折为特征的全身性骨病。骨质疏松症分为原发性和继发性两大类,原发性骨质疏松症包括绝经后骨质疏松症(ⅰ型)、老年骨质疏松症(ⅱ型)和特发性骨质疏松症(包括青少年型)。原发性骨质疏松症多见于绝经后妇女和老年男性。初期通常没有明显的临床表现,随着病情进展,骨量不断丢失,患者会出现疼痛、脊柱变形,严重者可发生骨质疏松性骨折。部分患者出现肌容量和肌力下降,容易跌倒,导致骨折风险增加,生活质量下降。骨质疏松性骨折的危害巨大,是老年患者致残和致死的主要原因之一。老年性骨质疏松症的发病因素和发病机理是多方面的,增龄造成的器官功能减退是主要因素。除内分泌因素外,多种细胞因子也影响骨代谢,降低成骨活性。例如:钙和维生素d的摄入不足,会导致皮肤中维生素d原向维生素d的转化不足,肾功减退,维生素d的羟化不足。骨髓间充质干细胞成骨分化能力下降。肌肉衰退,对骨骼的应力剌激減少,对骨代谢调节障碍。凡此种种,都影响骨代谢,使得成骨不足,破骨有余,骨丢失,骨结构损害,形成骨质疏松。然而,必须强调骨质疏松症可防、可治。
3.目前,西药治疗骨质疏松的原理有两点:1.抑制破骨细胞,减少骨吸收;2.促进成骨细胞,增加骨形成。西药在一定程度上对治疗骨质疏松起到有效作用,但是随着用药疗程的延长,药效减弱、药物安全性以及药物对机体的不良反应渐渐引起人们的关注,例如长期服用雌激素可增加女性患子宫内膜癌、乳腺癌等风险。
技术实现要素:
4.本技术的目的在于提供一种防治骨质疏松的中药组合物及其制备方法,旨在一定程度上解决现有治疗骨质疏松的药物疗效差,药物安全性差,容易对机体产生不良反应的问题。
5.为实现上述申请目的,本技术采用的技术方案如下:
6.第一方面,本技术提供一种防治骨质疏松的中药组合物,包括以下重量份的原料药:
7.淫羊藿
ꢀꢀꢀꢀꢀꢀꢀꢀ
300~500份,
8.骨碎补
ꢀꢀꢀꢀꢀꢀꢀꢀ
300~400份,
9.尿石素a
ꢀꢀꢀꢀꢀꢀꢀ
400~600份。
10.进一步地,所述防治骨质疏松的中药组合物,包括如下重量份的原料:
11.淫羊藿
ꢀꢀꢀꢀꢀꢀꢀꢀ
350~450份,
12.骨碎补
ꢀꢀꢀꢀꢀꢀꢀꢀ
300~350份,
13.尿石素a
ꢀꢀꢀꢀꢀꢀꢀ
450~550份。
14.进一步地,所述防治骨质疏松的中药组合物,包括重量份的原料:淫羊藿400量份,骨碎补300份,尿石素a 500份。
15.进一步地,所述防治骨质疏松的中药组合物,包括重量份的原料:淫羊藿370量份,骨碎补350份,尿石素a 450份。
16.进一步地,所述防治骨质疏松的中药组合物,包括重量份的原料:淫羊藿420量份,骨碎补320份,尿石素a 530份。
17.进一步地,所述防治骨质疏松的中药组合物中还包括药学上可接收的辅料。进一步地,所述防治骨质疏松的中药组合物的剂型包括胶囊、片剂、颗粒剂、冲剂、咀嚼片中的至少一种。
18.进一步地,所述药学上可接受的辅料包括:二氧化硅、甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、滑石粉、纤维素、葡萄糖、明胶、蔗糖、碳酸镁中的至少一种。
19.第二方面,本技术提供一种防治骨质疏松的中药组合物的制备方法,其特征在于,包括以下步骤:
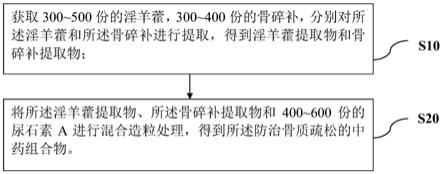
20.获取300~500份的淫羊藿,300~400份的骨碎补,分别对所述淫羊藿和所述骨碎补进行提取,得到淫羊藿提取物和骨碎补提取物;
21.将所述淫羊藿提取物、所述骨碎补提取物和400~600份的尿石素a进行混合造粒处理,得到所述防治骨质疏松的中药组合物。
22.进一步地,对所述淫羊藿进行醇提,得到所述淫羊藿提取物。
23.进一步地,对所述骨碎补进行醇提,得到所述骨碎补提取物。
24.进一步地,所述淫羊藿提取物中,总黄酮的质量百分含量以淫羊藿苷计不低于30%。
25.进一步地,所述骨碎补提取物中,总黄酮的质量百分含量不低于30%。
26.进一步地,所述混合造粒处理的步骤包括:采用湿法制粒或者干法制粒,将所述淫羊藿提取物、所述骨碎补提取物和所述尿石素a与药学上可接受的辅料制成口服制剂。
27.进一步地,所述口服制剂包括胶囊、片剂、颗粒剂、冲剂、咀嚼片中的至少一种。
28.进一步地,所述药学上可接受的辅料包括:二氧化硅、甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、滑石粉、纤维素、葡萄糖、明胶、蔗糖、碳酸镁中的至少一种。
29.本技术第一方面提供的防治骨质疏松的中药组合物中,尿石素a,一方面,能够显著抑制破骨细胞的活化,明显减少破骨细胞生成的数量以及大小,对骨吸收功能以及破骨相关基因的表达均具有显著的抑制作用,能够显著抑制破骨细胞的增殖和活性,减缓软骨退化,起到促进骨质健康的功效。另一方面,尿石素a能够调节骨骼肌线粒体的表达,提升骨骼肌的细胞呼吸强度,进而增加骨骼肌的强度,间接促进骨代谢的正常调节。淫羊藿与骨碎补均具有促进骨髓间充质干细胞的成骨性分化作用。通过三种原料药的协同复配作用,能够协同调节骨代谢,抑制骨吸收,促进骨形成,进而增加骨密度,共同起到防治中老年人骨质疏松,促进中老年人骨质健康的作用。若尿石素a配比过低,则中药组合物对破骨细胞活化的抑制效果不佳;若淫羊藿与骨碎补配比过低,则对骨髓间充质干细胞的成骨性分化的促进效果不佳。
30.本技术第二方面提供的防治骨质疏松的中药组合物的制备方法,分别对配方量的淫羊藿和骨碎补进行提取,获得淫羊藿提取物和骨碎补提取物后,与配方量的尿石素a进行
混合造粒处理,便可得到防治骨质疏松的中药组合物。制备工艺简单,适用于工业化大规模生产和应用。制备的防治骨质疏松的中药组合物,通过三种原料药的协同复配作用,能够协同调节骨代谢,抑制骨吸收,促进骨形成,进而增加骨密度,共同起到防治中老年人骨质疏松,促进中老年人骨质健康的作用。
附图说明
31.为了更清楚地说明本技术实施例中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本技术的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
32.图1是本技术实施例提供的防治骨质疏松的中药组合物的制备方法的流程示意图。
具体实施方式
33.为了使本技术要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本技术进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本技术,并不用于限定本技术。
34.本技术中,术语“和/或”,描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b的情况。其中a,b可以是单数或者复数。字符“/”一般表示前后关联对象是一种“或”的关系。
35.本技术中,“至少一个”是指一个或者多个,“多个”是指两个或两个以上。“以下至少一项(个)”或其类似表达,是指的这些项中的任意组合,包括单项(个)或复数项(个)的任意组合。例如,“a,b或c中的至少一项(个)”,或,“a,b和c中的至少一项(个)”,均可以表示:a,b,c,a-b(即a和b),a-c,b-c,或a-b-c,其中a,b,c分别可以是单个,也可以是多个。
36.应理解,在本技术的各种实施例中,上述各过程的序号的大小并不意味着执行顺序的先后,部分或全部步骤可以并行执行或先后执行,各过程的执行顺序应以其功能和内在逻辑确定,而不应对本技术实施例的实施过程构成任何限定。
37.在本技术实施例中使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本技术。在本技术实施例和所附权利要求书中所使用的单数形式的“一种”和“该”也旨在包括多数形式,除非上下文清楚地表示其他含义。
38.本技术实施例说明书中所提到的相关成分的重量不仅仅可以指代各组分的具体含量,也可以表示各组分间重量的比例关系,因此,只要是按照本技术实施例说明书相关组分的含量按比例放大或缩小均在本技术实施例说明书公开的范围之内。具体地,本技术实施例说明书中的质量可以是μg、mg、g、kg等化工领域公知的质量单位。
39.术语“第一”、“第二”仅用于描述目的,用来将目的如物质彼此区分开,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。例如,在不脱离本技术实施例范围的情况下,第一xx也可以被称为第二xx,类似地,第二xx也可以被称为第一xx。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。
40.本技术实施例第一方面提供一种防治骨质疏松的中药组合物,包括以下重量份的原料药:
41.淫羊藿
ꢀꢀꢀꢀꢀꢀꢀꢀ
300~500份,
42.骨碎补
ꢀꢀꢀꢀꢀꢀꢀꢀ
300~400份,
43.尿石素a
ꢀꢀꢀꢀꢀꢀꢀ
400~600份。
44.本技术实施例第一方面提供的防治骨质疏松的中药组合物,其原料药包括300~500份的淫羊藿,300~400份的骨碎补和400~600份的尿石素a(urolithin-a)。其中,尿石素a,一方面,能够显著抑制破骨细胞的活化,明显减少破骨细胞生成的数量以及大小,对骨吸收功能以及破骨相关基因的表达均具有显著的抑制作用,能够显著抑制破骨细胞的增殖和活性,减缓软骨退化,起到促进骨质健康的功效。另一方面,尿石素a能够调节骨骼肌线粒体的表达,提升骨骼肌的细胞呼吸强度,进而增加骨骼肌的强度,间接促进骨代谢的正常调节。淫羊藿与骨碎补均具有促进骨髓间充质干细胞的成骨性分化作用。本技术实施例防治骨质疏松的中药组合物,通过三种原料药的协同复配作用,能够协同调节骨代谢,抑制骨吸收,促进骨形成,进而增加骨密度,共同起到防治中老年人骨质疏松,促进中老年人骨质健康的作用。若尿石素a配比过低,则中药组合物对破骨细胞活化的抑制效果不佳;若淫羊藿与骨碎补配比过低,则对骨髓间充质干细胞的成骨性分化的促进效果不佳。
45.本技术实施例防治骨质疏松的中药组合物中,淫羊藿,抗骨质疏松的主要有效成分是以淫羊藿苷为代表的黄酮类化合物,除淫羊藿苷外,还含有朝藿定a、朝藿定b、朝藿定c和宝藿苷
‑ⅰ
等,它们合起来的活性基团更多,作用靶点也更为丰富,因而应具有较淫羊藿苷单体更强的抗骨质疏松活性。淫羊藿抗骨质疏松的作用机制是促进骨髓间充质干细胞的成骨性分化,并具有促进骨形成和抑制骨吸收的双重活性。淫羊藿总黄酮能够有效预防切除卵巢大鼠发生骨质疏松症,且其作用机制不同于雌激素,既具有预防绝经后骨质疏松的作用,同时又不会引发生殖系统肿瘤等潜在的不良反应。骨碎补,具有续伤止痛、补肾壮骨的功效,骨碎补的核心化合物是柚皮苷、圣草酚、山奈酚等黄酮类化合物,具有类雌激素类化合物的生物学作用,具有从抗炎、内分泌系统等途径发挥抗骨质疏松的作用机制。骨碎补通过多种途径,多种信号通路作用于多种靶点发挥抗骨质疏松的生物学效用。淫羊藿和骨碎补复配,促进老年人群骨质健康的应用领域中依然存在很大的研究和提升空间。介于此,本技术实施例防治骨质疏松的中药组合物中,添加尿石素a进行复配,尿石素a旨在发挥其增强细胞机能,抑制破骨细胞,增加肌肉强度的功效,共同起到对抗中老年人骨质疏松的目的。尿石素a具有抗炎、抗氧化等生物活性的主要功效物质,通过促进线粒体自噬,提高线粒体机能达到减少有害炎症,增强细胞健康的功效。尿石素a具有减轻增龄造成的肌肉、关节退化,起到增强肌肉强度,增强机体细胞活性,延缓老年人群的肌肉衰老,减轻软骨退化和膝关节炎症的功效,减轻因增龄造成的全身性器官功能衰退,包括肾脏和骨骼,进而改善老年人群的骨代谢,促进成骨,减缓破骨。并且,能够抑制破骨细胞活性,减少破骨细胞生成的数量以及大小,抑制破骨相关基因的表达。进而维持对骨骼的应力刺激和正常骨代谢调节机制。因此,本技术实施例通过添加尿石素a进行复配,其功效优于淫羊藿或骨碎补单方增加骨密度的功效。
46.在一些实施例中,防治骨质疏松的中药组合物,包括如下重量份的原料:
47.淫羊藿
ꢀꢀꢀꢀꢀꢀꢀꢀ
350~450份,
48.骨碎补
ꢀꢀꢀꢀꢀꢀꢀꢀ
300~350份,
49.尿石素a
ꢀꢀꢀꢀꢀꢀꢀ
450~550份。
50.本技术实施例防治骨质疏松的中药组合物中,三种原料药的配比为350~450份的淫羊藿,300~350份的骨碎补和450~550份的尿石素a时,三种原料药有更好的复配作用,使得中药组合物对破骨细胞活化有更好的抑制效果;同时能够更好的促进骨髓间充质干细胞的成骨性分化。
51.在一些具体实施例中,防治骨质疏松的中药组合物,包括重量份的原料:淫羊藿400量份,骨碎补300份,尿石素a 500份。在一些具体实施例中,防治骨质疏松的中药组合物,包括重量份的原料:淫羊藿370量份,骨碎补350份,尿石素a 450份。在一些具体实施例中,防治骨质疏松的中药组合物,包括重量份的原料:淫羊藿420量份,骨碎补320份,尿石素a 530份。本技术上述具体实施例防治骨质疏松的中药组合物,通过实验研究表明能够有效预防、改善、治疗中老年人骨质疏松,提高骨质疏松症患者的骨密度,可明显抑制骨吸收,减少骨量的丢失,从而治疗骨质疏松症,促进中老年人骨质健康。
52.在一些实施例中,防治骨质疏松的中药组合物中还包括药学上可接收的辅料。本技术实施例防治骨质疏松的中药组合物还可以包含药学上可接收的辅料,例如,通过辅料改善防治骨质疏松的中药组合物的口感,提高患者顺应性;也可以通过辅料提高防治骨质疏松的中药组合物的赋形效果,使防治骨质疏松的中药组合物方便制作成不同剂型,提高其使用灵活性。
53.在一些实施例中,药学上可接受的辅料包括:二氧化硅、甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、滑石粉、纤维素、葡萄糖、明胶、蔗糖、碳酸镁中的至少一种,这些辅料可以提高防治骨质疏松的中药组合物的赋形效果,也能够改善防治骨质疏松的中药组合物的口感,提高患者顺应性。
54.在一些实施例中,防治骨质疏松的中药组合物的剂型包括胶囊、片剂、颗粒剂、冲剂、咀嚼片中的至少一种固体口服制剂。在实际应用中可将防治骨质疏松的中药组合物制成不同剂型,其中胶囊具有质量稳定,生物利用度高,方便服用等特点,为优选剂型。
55.在一些实施例中,防治骨质疏松的中药组合物中,淫羊藿的每日有效剂量以总黄酮含量为计150~450mg,以淫羊藿苷含量计为15~45mg;骨碎补的每日有效剂量以总黄酮摄入量计为250~300mg,以柚皮苷摄入量计为80~120mg;尿石素a的每日有效剂量500~1000mg。各原料药在此剂量范围内,能显著调节骨骼肌线粒体基因的表达,增加骨骼肌的强度。在一些实施例中,防治骨质疏松的中药组合物的服用量优选为2~3个月。
56.本技术实施例防治骨质疏松的中药组合物可通过以下实施例方法制得。
57.如附图1所示,本技术实施例第二方面提供一种防治骨质疏松的中药组合物的制备方法,包括以下步骤:
58.s10.获取300~500份的淫羊藿,300~400份的骨碎补,分别对淫羊藿和骨碎补进行提取,得到淫羊藿提取物和骨碎补提取物;
59.s20.将淫羊藿提取物、骨碎补提取物和400~600份的尿石素a进行混合造粒处理,得到防治骨质疏松的中药组合物。
60.本技术实施例第二方面提供的防治骨质疏松的中药组合物的制备方法,分别对配方量的淫羊藿和骨碎补进行提取,获得淫羊藿提取物和骨碎补提取物后,与配方量的尿石素a进行混合造粒处理,便可得到防治骨质疏松的中药组合物。制备工艺简单,适用于工业化大规模生产和应用。制备的防治骨质疏松的中药组合物,通过三种原料药的协同复配作
用,能够协同调节骨代谢,抑制骨吸收,促进骨形成,进而增加骨密度,共同起到防治中老年人骨质疏松,促进中老年人骨质健康的作用。
61.在一些实施例中,上述步骤s10中,对骨碎补进行醇提,得到骨碎补提取物。在一些具体实施例中,对骨碎补进行醇提的步骤包括:
62.s11.将骨碎补药材与乙醇溶液(浓度约70%)按1:(6~10)倍混合,加热回流提取物1~3小时后过滤,得到滤液提取液和药渣;
63.s12.药渣先后加5~7倍乙醇溶液(浓度约70%),加热回流提取2~3次,每次1~3h;过滤收集提取液;
64.s13.将所有提取液浓缩成小体积,加入原料量约0~10%的麦芽糊精等辅料,继续浓缩至密度为1.25~1.5g/ml。
65.s14.将上述浓缩物放入真空干燥箱内,于70℃左右真空干燥,干燥物经粉碎后过80目以上筛,即得骨碎补提取物。
66.在一些实施例中,上述步骤s10中,对淫羊藿进行醇提,得到淫羊藿提取物。在一些具体实施例中,对淫羊藿进行醇提的步骤包括:
67.s15.将淫羊藿药材与乙醇溶液(浓度约60%)按1:(8~12)倍混合,加热回流提取物1~3h后过滤,得到滤液提取液和药渣;
68.s16.药渣先后加8~12倍乙醇溶液(浓度约60%),加热回流2~3次,每次1~3h,过滤收集提取液;
69.s17.将所有提取液浓缩成小体积,加入原料量约0~10%的麦芽糊精等辅料,继续浓缩至密度1.25~1.5g/ml;
70.s18.将上述浓缩物放入真空干燥箱内,于60℃左右真空干燥,干燥物经粉碎后过80目以上筛,即得淫羊藿提取物。
71.在一些实施例中,淫羊藿提取物中,总黄酮的质量百分含量以淫羊藿苷计不低于30%。本技术实施例淫羊藿抗骨质疏松的主要有效成分是以淫羊藿苷为代表的黄酮类化合物,淫羊藿提取物的活性成分以总黄酮含量计,不低于30wt%,可有效确保淫羊藿提取物中淫羊藿苷等活性成分的含量,使其具有丰富的活性基团和作用靶点,从而确保淫羊藿提取物以及中药组合物对抗骨质疏松的作用。
72.在一些实施例中,骨碎补提取物中,总黄酮的质量百分含量不低于30%。本技术实施例骨碎补的核心化合物是柚皮苷、圣草酚、山奈酚等黄酮类化合物,以柚皮苷为主,具有类雌激素类化合物的生物学作用,具有从抗炎、内分泌系统等途径发挥抗骨质疏松的作用机制。通过对骨碎补提取物中柚皮苷,以及总黄酮含量的限定,有效确保了骨碎补的活性成分,从而确保了中药组合物对抗骨质诉讼的作用。在另一些实施例中,骨碎补提取物中,柚皮苷的质量百分含量占总黄酮含量的30%以上。
73.在一些实施例中,上述步骤s20中,混合造粒处理的步骤包括:采用湿法制粒或者干法制粒,将淫羊藿提取物、骨碎补提取物和尿石素a与药学上可接受的辅料制成口服制剂。通过药学上可接受的辅料料改善防治骨质疏松的中药组合物的口感,提高患者顺应性;提高防治骨质疏松的中药组合物的赋形效果。
74.在一些实施例中,药学上可接受的辅料包括:二氧化硅、甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、滑石粉、纤维素、葡萄糖、明胶、蔗糖、碳酸镁中的至少一种,这些辅料可以提
高防治骨质疏松的中药组合物的赋形效果,也能够改善防治骨质疏松的中药组合物的口感,提高患者顺应性。
75.在一些实施例中,口服制剂包括胶囊、片剂、颗粒剂、冲剂、咀嚼片中的至少一种;可将防治骨质疏松的中药组合物制成不同剂型,其中胶囊具有质量稳定,生物利用度高,方便服用等特点,为优选剂型。
76.在一些实施例中,湿法制粒的步骤包括:在药物粉末中加入黏合剂,靠黏合剂的桥架或黏结作用使粉末聚结在一起而制成固体口服制剂。包括但不限于挤压制粒、转动制粒、流化制粒和搅拌制粒等。湿法制成的颗粒经过表面润湿,具有颗粒质量好,外形美观、耐磨性较强、压缩成型性好等优点。
77.在一些实施例中,干法制粒的步骤包括:将松散的粉末压缩团聚,然后将压实的粉末粉碎制粒使粉末的流动性得到改善,适用于工艺生产如压片胶囊灌装等。与湿法制粒相比,干法制粒的优点是在整个工艺过程中无需水或其它机溶剂的参与,对湿、热敏感的药物尤为合适。包括但不限于,辊压干法制粒,容易实现自动化控制,效率高、工艺简单且更加环保。粉末压缩方式有辊压与非辊压方式,辊压是制药行业的主流,其主要优势是工艺过程连续具有更大的生产能力、粉末对润滑剂的依赖性小等。一般干法制粒辊压工艺主要变量有三个:压力大小、进料螺杆的转速及辊筒转速。混合粉末中对辊压影响较大的辅料主要有两种:粘合剂与润滑剂。
78.为使本技术上述实施细节和操作能清楚地被本领域技术人员理解,以及本技术实施例防治骨质疏松的中药组合物及其制备方法的进步性能显著的体现,以下通过多个实施例来举例说明上述技术方案。
79.实施例1
80.一种防治骨质疏松的中药硬胶囊制剂,其原料包括:
81.淫羊藿400g,骨碎补300g,尿石素a 500g,辅料为微晶纤维素,二氧化硅,硬脂酸镁。
82.其制备包括以下步骤:
83.①
对淫羊藿进行提取:将淫羊藿药材与乙醇溶液(浓度60%)按1:10倍混合,加热回流提取物2h后过滤,得到滤液提取液和药渣;药渣先后加10倍乙醇溶液(浓度60%),加热回流2次,每次2h,过滤收集提取液;将所有提取液浓缩成小体积,加入原料量约10%的麦芽糊精等辅料,继续浓缩至密度1.25g/ml;将上述浓缩物放入真空干燥箱内,于60℃真空干燥,干燥物经粉碎后过80目筛,即得淫羊藿提取物。
84.②
对骨碎补进行提取:将骨碎补药材与乙醇溶液(浓度70%)按1:8倍混合,加热回流提取物2小时后过滤,得到滤液提取液和药渣;药渣先后加6倍乙醇溶液(浓度70%),加热回流提取2次,每次2h;过滤收集提取液;将所有提取液浓缩成小体积,加入原料量约10%的麦芽糊精等辅料,继续浓缩至密度为1.25g/ml;将上述浓缩物放入真空干燥箱内,于70℃真空干燥,干燥物经粉碎后过80目筛,即得骨碎补提取物。
85.③
将淫羊藿提取物、骨碎补提取物、尿石素a过60目筛;取该混合粉,以80%乙醇溶液作为粘合剂,采用手工混合制软材,用20目筛制粒,干燥,再用30目筛整粒。
86.④
取干颗粒,加入适量微晶纤维素、二氧化硅、硬脂酸镁,手工过30目筛,混合均匀,用0号胶囊填充,装量为0.50g/粒,得到防治骨质疏松的中药硬胶囊制剂。按此方法制得
的胶囊,每粒中含淫羊藿提取物160mg,骨碎补提取物120mg,尿石素a 200mg。
87.实施例2
88.一种防治骨质疏松的中药片剂,其原料包括:
89.淫羊藿370g,骨碎补350g,尿石素a 450g,辅料为微晶纤维素,二氧化硅,硬脂酸镁。
90.其制备包括以下步骤:
91.①
对淫羊藿进行提取:将淫羊藿药材与乙醇溶液(浓度60%)按1:10倍混合,加热回流提取物2h后过滤,得到滤液提取液和药渣;药渣先后加10倍乙醇溶液(浓度60%),加热回流2次,每次2h,过滤收集提取液;将所有提取液浓缩成小体积,加入原料量约10%的麦芽糊精等辅料,继续浓缩至密度1.25g/ml;将上述浓缩物放入真空干燥箱内,于60℃真空干燥,干燥物经粉碎后过80目筛,即得淫羊藿提取物。
92.②
对骨碎补进行提取:将骨碎补药材与乙醇溶液(浓度70%)按1:8倍混合,加热回流提取物2小时后过滤,得到滤液提取液和药渣;药渣先后加6倍乙醇溶液(浓度70%),加热回流提取2次,每次2h;过滤收集提取液;将所有提取液浓缩成小体积,加入原料量约10%的麦芽糊精等辅料,继续浓缩至密度为1.25g/ml;将上述浓缩物放入真空干燥箱内,于70℃真空干燥,干燥物经粉碎后过80目筛,即得骨碎补提取物。
93.③
将淫羊藿提取物、骨碎补提取物、尿石素a过60目筛;取该混合粉,以50%乙醇溶液作为粘合剂,采用手工混合制软材,用20目筛制粒,干燥,再用30目筛整粒。
94.④
取干颗粒,加入适量微晶纤维素、二氧化硅、硬脂酸镁,手工过20目筛混合均匀。采用压片机按操作规程进行压片,调整装量为0.75g/片,并采用包衣机按操作规程进行包衣至增重3-5%,得到防治骨质疏松的中药片剂。按此方法制得的片剂,每片中含淫羊藿提取物185mg,骨碎补提取物175mg,尿石素a 225mg。
95.实施例3
96.一种防治骨质疏松的中药片剂,其原料包括:
97.淫羊藿420量份,骨碎补320份,尿石素a 530份,辅料为微晶纤维素,二氧化硅,硬脂酸镁。
98.其制备包括以下步骤:
99.①
对淫羊藿进行提取:将淫羊藿药材与乙醇溶液(浓度60%)按1:10倍混合,加热回流提取物2h后过滤,得到滤液提取液和药渣;药渣先后加10倍乙醇溶液(浓度60%),加热回流2次,每次2h,过滤收集提取液;将所有提取液浓缩成小体积,加入原料量约10%的麦芽糊精等辅料,继续浓缩至密度1.25g/ml;将上述浓缩物放入真空干燥箱内,于60℃真空干燥,干燥物经粉碎后过80目筛,即得淫羊藿提取物。
100.②
对骨碎补进行提取:将骨碎补药材与乙醇溶液(浓度70%)按1:8倍混合,加热回流提取物2小时后过滤,得到滤液提取液和药渣;药渣先后加6倍乙醇溶液(浓度70%),加热回流提取2次,每次2h;过滤收集提取液;将所有提取液浓缩成小体积,加入原料量约10%的麦芽糊精等辅料,继续浓缩至密度为1.25g/ml;将上述浓缩物放入真空干燥箱内,于70℃真空干燥,干燥物经粉碎后过80目筛,即得骨碎补提取物。
101.③
将淫羊藿提取物、骨碎补提取物、尿石素a过60目筛;取该混合粉,以50%乙醇溶液作为粘合剂,采用手工混合制软材,用20目筛制粒,干燥,再用30目筛整粒。
102.④
取干颗粒,加入适量微晶纤维素、二氧化硅、硬脂酸镁,手工过20目筛混合均匀。采用压片机按操作规程进行压片,调整装量为0.75g/片,并采用包衣机按操作规程进行包衣至增重3-5%,得到防治骨质疏松的中药片剂。按此方法制得的片剂,每片中含淫羊藿提取物210mg,骨碎补提取物160mg,尿石素a 265mg。
103.进一步的,为了验证本技术实施例的进步性,通过建立大鼠骨质疏松模型,观察本实施例制备的防治骨质疏松的中药组合物在调节骨代谢、增加骨密度功能及骨钙含量等方面的效果,从而评价受试品改善抗骨质疏松的作用。
104.1、待试药:
105.以实施例1制备的防治骨质疏松的中药硬胶囊制剂为实验对象,分别设置高剂量组、低剂量组,以及骨碎补提取物组,淫羊藿提取物组,雌激素组。
106.2、采用70只,雌性3月龄的wistar大,经去势手术构建骨质疏松动物模型。动物自由饮水和给予饲料,饲料配方见表1。
107.表1
108.成分质量分数%酪蛋白23dl-蛋氨酸0.3玉米淀粉32蔗糖30纤维5玉米油5混合矿物盐3.5混合维生素1二酒石酸胆碱0.2
109.注:
①
混合矿物盐,每千克饲料含有各组分成分如下:mnso
4 110mg,cuso
4 0.8mg,feso
4 1.2mg,ki 18mg,znso
4 2960mg,cahpo
4 2890mg,mgso
4 1.25*104mg;
②
混合维生素,每千克饲料含有各组分成分如下:维生素a 1.4*104iu,维生素d 1500iu,维生素e 120mg,维生素k 3mg,维生素b1 12mg,维生素b2 20mg,维生素b6 12mg,维生素b12 0.03mg,烟酸60mg,泛酸24mg,叶酸6mg,生物素0.54mg。
110.3、试剂及仪器:
111.仪器:原子吸收分光光度计、单光子骨密度仪或双能x线骨密度仪或其他相关仪器、精密卡尺、动物解剖器械、动物天平、105℃烘箱。
112.试剂:硝酸(优级纯)、高氯酸(优级纯)、氧化镧、钙标准溶液。
113.4、实验分组和试验剂量:
114.手术后大鼠经适应性饲养3-5d后分组,按体重随机分成7组,每组10只。在手术后第5周开始,按照表1方案给予灌胃给药,每日1次。
115.根据说明书推荐人群用量进行剂量设定。说明书规定人群服用量为1.5g/d/人。本实验设定大鼠生物等效给药量为人临床用药量的10倍,人标准体重按50kg计,大鼠的等效剂量为1.5g
÷
50kg*10=0.30g/kg/d。喂养时间为12周,实验过程中每周测定体重,并根据体重调整给药量。具体如下表2所示:
116.表2
[0117][0118]
5、检测指标
[0119]
实验结束后,处死动物,腹部主动脉釆血静置1h后离心后取血清,进行检测血清骨代谢生化指标:
[0120]
①
血清骨钙素(osteocalcin,oc):骨形成标志物,含量越高表明骨形成活动越强。
[0121]
②
骨碱性磷酸酶(alkaline phosphatase,alp):骨形成标志物,含量越高表明骨形成活动越强。
[0122]
③ⅰ
型胶原氨基端交联肽(n-terminal cross-linked telopeptide of typeⅰcollagen,ntx):骨吸收标志物,含量越高表明骨吸收活性越强。
[0123]
④
抗酒石酸酸性磷酸酶(tracp-5b):骨吸收标志物,含量越高表明骨吸收活动越强。
[0124]
取大鼠双侧完整股骨(或也包括肱骨)和腰椎,分离干净上面的肌肉组织,进行检测骨钙及骨密度:
[0125]
①
骨钙含量:取右侧股骨进行测定。
[0126]
②
骨密度(bone mineral density,bmd):左侧股骨和第2-4腰椎进行测定。根据以上实验数据获得本发明专利组合物的药效评价。
[0127]
6、数据分析
[0128]
实验数据以“平均值
±
标准差(x
±
sd)”标示。数据采用方差分析,先进性方差齐性检验。方差齐,计算f值,f值《f
0.05
,则各组均数间无显著性差异;f值》f
0.05
且p≤0.05,用多个试验组和一个对照组间均数的两两比较法进行统计。
[0129]
7、实验结果:
[0130]
(1)各组大鼠骨代谢生化指标变化情况见表3所示:
[0131]
表3
[0132][0133]
由上述表3实验结果表明,模型组血清骨钙素以及骨碱性磷酸酶水平显著降低,与假手术组有显著性差异(p《0.01)。而本技术实施例1防治骨质疏松的中药组合物组的血清骨钙素以及骨碱性磷酸酶水平显著高于模型组,说明本技术实施例防治骨质疏松的中药组合物具有促进骨形成的功效。另外,模型组ntx以及tracp-5b水平显著高于假手术组(p《0.01)。而本技术实施例防治骨质疏松的中药组合物组ntx以及tracp-5b水平显著低于模型组(p《0.01),说明本技术实施例防治骨质疏松的中药组合物具有抑制骨吸收的功效。
[0134]
(2)各组大鼠股骨及腰椎骨密度变化情况见表4
[0135]
表4
[0136][0137]
由上述表4实验结果表明,模型构建组大鼠骨密度显著低于假手术组(p《0.01)。与
模型组比较,本技术实施例1胶囊高剂量组和低剂量组均可显著增加模型大鼠的骨密度(p《0.01)。说明本技术实施例防治骨质疏松的中药组合物能够有效改善去势大鼠的骨密度。另外,本技术实施例高剂量组大鼠骨密度显著高于骨碎补提取物大鼠组以及淫羊藿提取物大鼠组(p《0.01),说明本技术实施例防治骨质疏松的中药组合物增加骨密度的功效优于骨碎补单方或淫羊藿单方。
[0138]
(3)各组大鼠股骨钙含量如下表5所示:
[0139]
表5
[0140]
组别例数骨钙含量(mg/g)假手术组10322.32
±
15.70模型组10220.50
±
40.46实施例1高剂量组10295.12
±
22.51实施例1低剂量组10276.76
±
18.91骨碎补提取物组10245.93
±
14.34淫羊藿提取物组10250.73
±
24.13阳性对照组(戊酸雌二醇)10307.28
±
18.10
[0141]
由上述表5测试结果显示,模型组股骨钙含量显著降低(p《0.001)。本技术实施例1高、低剂量组均可显著升高模型大鼠股骨骨钙含量,与模型组有显著性差异(p《0.01)。且本技术实施例1高剂量组明显高于骨碎补组以及淫羊藿组(p《0.01)。
[0142]
由上述测试结果表明,与假手术组比较,模型组大鼠股骨和腰椎bmd、骨钙含量明显降低,血清oc、alp水平明显降低,ntx、tracp-5b水平明显升高,差异均有统计学意义(p《0.05)。与模型组比较,本技术实施例1胶囊低、高剂量组大鼠股骨和腰椎bmd、骨钙含量、血清oc和alp水平均升高,血清ntx、tracp-5b水平明显降低,差异均有统计学意义(p《0.05)。与骨碎补或淫羊藿单方组比较,本技术实施例1胶囊高剂量组大鼠股骨和腰椎bmd、骨钙含量、血清oc和alp水平较高,血清ntx、tracp-5b水平较低,差异均有统计学意义(p《0.05)。
[0143]
结论:本技术实施例防治骨质疏松的中药组合物能够治疗去卵巢所致骨质疏松大鼠,能够通过调节血清oc、alp、ntx、tracp-5b水平,改善骨代谢,提高bmd。说明本技术实施例防治骨质疏松的中药组合物能够提高骨质疏松症患者的骨密度,可明显抑制骨吸收,减少骨量的丢失,从而治疗骨质疏松症。
[0144]
以上所述仅为本技术的较佳实施例而已,并不用以限制本技术,凡在本技术的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本技术的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1