一种传染性造血器官坏死病佐剂疫苗及其制备方法与流程
1.本发明涉及生物技术领域,具体涉及一种传染性造血器官坏死病佐剂疫苗及其制备方法。
背景技术:
2.鲑鳟鱼(salmon and trout)是指以鲑科鱼类为主要代表的一批优质冷水性鱼类,主要包括大西洋鲑(salmo salar)、虹鳟(oncorhynchus mykiss)、王鲑(oncorhynchus tshawytscha)等。我国鲑鳟鱼主养品种为虹鳟,养殖区域广泛分布在中国东北、西北、西南等冷水资源较发达的地区,在带动当地经济发展、促进渔民增收方面发挥了积极的作用。但是目前我国鲑鳟鱼养殖业正面临重大病害难题,产业发展严重受阻。其中危害最大的为传染性造血器官坏死病(infectious hematopoietic necrosis,ihn)。根据环境、宿主、毒株等不同,ihn最高可造成虹鳟、大西洋鲑等幼鱼90%以上的死亡率,是我国鲑鳟鱼产业发展必须解决的首要病害难题。
3.目前全球范围内,仅加拿大上市了一种针对北美基因型的ihn核酸疫苗,我国尚无有效的ihn防控药物。由于毒株存在变异及存在生物安全隐患等问题,国外商业化疫苗无法直接引进应用,因此我国鲑鳟鱼病害难题只能通过疫苗的自主研发来解决。课题组在前期开展了ihn灭活疫苗的研制工作,通过利用甲醛和bpl进行灭活,制备了ihn灭活疫苗,利用该疫苗直接对虹鳟进行免疫,结果发现所制备的灭活疫苗具有较理想的早期免疫保护效力(参见中国专利cn113144185a和cn113122510a),但是随着时间的延长,在免疫后60天时,疫苗免疫保护效率显著下降,不能维持较长的保护期,无法满足市场需求,因此极有必要对现有的ihn灭活疫苗进行优化。
技术实现要素:
4.本发明的目的是提供一种传染性造血器官坏死病佐剂疫苗及其制备方法。
5.第一方面,本发明要求保护一种传染性造血器官坏死病疫苗。
6.本发明要求保护的传染性造血器官坏死病疫苗,由传染性造血器官坏死病毒灭活液和montanide
tm gel 02 pr佐剂组成。
7.进一步地,在所述传染性造血器官坏死病疫苗中,montanide
tm gel 02 pr佐剂的体积百分含量为10%-20%(即所述传染性造血器官坏死病毒灭活液的体积百分含量为80-90%)。
8.更进一步地,所述传染性造血器官坏死病毒灭活液和montanide
tm gel 02 pr佐剂的体积比可为9:1。
9.进一步地,所述传染性造血器官坏死病毒灭活液可为传染性造血器官坏死病毒经甲醛灭活后所得。
10.进一步地,所述传染性造血器官坏死病毒灭活液在灭活前的病毒滴度可为107tcid
50
/0.1ml。
11.进一步地,所述传染性造血器官坏死病疫苗可按照如下第二方面所述方法制备得到。
12.第二方面,本发明要求保护一种制备传染性造血器官坏死病疫苗的方法。
13.本发明所要求保护的制备传染性造血器官坏死病疫苗的方法,可包括如下步骤:
14.(a)制备传染性造血器官坏死病毒灭活液;
15.(b)将所述传染性造血器官坏死病毒灭活液和montanide
tm gel 02p r佐剂混合,制备得到传染性造血器官坏死病疫苗。
16.进一步地,在所述传染性造血器官坏死病疫苗中,montanide
tm gel 02 pr佐剂的体积百分含量为10%-20%(即所述传染性造血器官坏死病毒灭活液的体积百分含量为80-90%)。
17.更进一步地,在所述传染性造血器官坏死病疫苗中,所述传染性造血器官坏死病毒灭活液和montanide
tm gel 02 pr佐剂的体积比可为9:1。
18.进一步地,所述传染性造血器官坏死病毒灭活液可为传染性造血器官坏死病毒经甲醛灭活后所得。
19.进一步地,所述传染性造血器官坏死病毒灭活液在灭活前的病毒滴度可为107tcid50/0.1ml。
20.在步骤(a)中,所述制备传染性造血器官坏死病毒灭活液可按照如下进行:取病毒滴度为107tcid
50
/0.1ml的传染性造血器官坏死病毒液,加入甲醛使其终浓度为5mm,迅速混匀;将加完甲醛的病毒液置于摇床,24℃条件下,100r/min灭活24h,用终浓度为1mm的亚硫酸氢钠溶液终止灭活,即得传染性造血器官坏死病毒灭活液。
21.在步骤(b)中,将所述传染性造血器官坏死病毒灭活液和montanide
tm gel 02 pr佐剂混合前,还可包括将montanide
tm gel 02 pr佐剂进行灭菌的步骤。如高温高压灭菌锅(116℃)灭菌20min。
22.第三方面,本发明要求保护传染性造血器官坏死病毒灭活液和montanide
tm gel 02 pr佐剂在制备传染性造血器官坏死病疫苗中的应用。
23.进一步地,在所述传染性造血器官坏死病疫苗中,montanide
tm gel 02 pr佐剂的体积百分含量为10%-20%(即所述传染性造血器官坏死病毒灭活液的体积百分含量为80-90%)。
24.更进一步地,所述传染性造血器官坏死病毒灭活液和montanide
tm gel 02 pr佐剂的体积比为9:1。
25.进一步地,所述传染性造血器官坏死病毒灭活液为传染性造血器官坏死病毒经甲醛灭活后所得。
26.进一步地,所述传染性造血器官坏死病毒灭活液在灭活前的病毒滴度为107tcid
50
/0.1ml。
27.在上述各方面中,本发明所述疫苗可用于预防ihnv宿主感染传染性造血器官坏死病毒,用于预防和/或治疗ihnv宿主因感染传染性造血器官坏死病毒所致疾病。
28.本发明还要求保护所述疫苗在预防和/或治疗ihnv宿主因感染传染性造血器官坏死病毒所致疾病中的应用。
29.本发明还要求保护一种预防和/或治疗ihnv宿主因感染传染性造血器官坏死病毒
and evolution,2019,131:19-28.”一文,按照国家生物安全的有关规定公众可从申请人处获得,仅可用于重复本发明试验使用,不得他用。
51.2、灭活佐剂疫苗的制备
52.甲醛灭活液的制备:取新鲜的ihnv病毒液(107tcid
50
/0.1ml),加入甲醛(终浓度为5mm),迅速混匀。将加完甲醛的病毒液置于摇床,24℃条件下,100r/min灭活24h,加入亚硫酸氢钠溶液(终浓度为1mm)终止灭活,获得ihn甲醛灭活疫苗。
53.bpl灭活液制备:取新鲜的ihnv病毒液(107tcid
50
/0.1ml),加入β-丙内酯(bpl),使bpl的终浓度为3mm,混匀后置于24℃摇床,100r/min进行灭活24h,加入硫代硫酸钠溶液(终浓度为20mm)终止灭活,获得ihn bpl灭活疫苗。
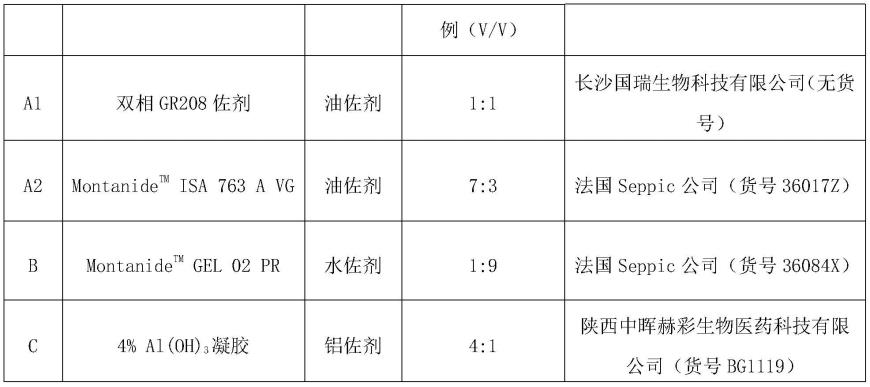
54.佐剂灭活疫苗的制备:各佐剂(表1)经高温高压灭菌锅(116℃)灭菌20min,分别与ihnv甲醛灭活液和bpl灭活液按照配比(表1),进行混匀,形成均质溶液,获得甲醛灭活佐剂疫苗和bpl灭活佐剂疫苗。
55.表1、佐剂信息
[0056][0057][0058]
3、最佳疫苗及最佳免疫剂量的确定
[0059]
虹鳟(平均体重5
±
1g)来自辽宁本溪艾格莫林实业有限公司。pbs注射组作为阴性对照组。疫苗组包括:添加佐剂的灭活疫苗和不加佐剂的灭活疫苗(裸苗)。灭活疫苗:包括甲醛灭活疫苗和bpl灭活疫苗。佐剂为四种(表1):双相gr208佐剂(标记为a1)、montanide
tm isa 763 a vg(标记为a2)、montanide
tm gel 02 pr(标记为b)、4%al(oh)3凝胶(标记为c)。采用的剂量分别为10μl、50μl和100μl每尾。采用的免疫方式为腹腔注射免疫。免疫后将虹鳟置于室内循环水系统(水温13
±
1℃)养殖。在免疫后30d,对虹鳟进行腹腔注射攻毒,攻毒剂量为50μl 100 tcid
50
的ihnv病毒原液,每种处理60尾,连续观察21d,统计各组虹鳟累积死亡数,计算各组疫苗相对免疫保护率。计算公式为:相对免疫保护率=[1-(免疫组死亡率/对照组死亡率)]
×
100%。根据相对保护率结果,确定最佳疫苗及其最佳免疫剂量。
[0060]
4、最佳疫苗的长期免疫保护效力分析
[0061]
选择最佳佐剂疫苗及其裸苗,采用10μl和50μl的剂量,对平均体重为10
±
1g的虹鳟进行腹腔注射免疫。以pbs注射的虹鳟为阴性对照。免疫后将虹鳟置于室内流水养殖圆缸
(2米直径,水深80cm,水温14
±
1℃)养殖。于免疫后不同时间对虹鳟进行攻毒试验(同步骤3),每种处理60尾虹鳟,置于室内循环水系统(水温13
±
1℃)养殖。记录各组虹鳟死亡情况,计算疫苗的相对免疫保护率(同步骤3),确定疫苗的长效保护作用。
[0062]
5、佐剂灭活疫苗的安全性检验
[0063]
选择最佳佐剂疫苗,采用一次单剂量(50μl)、二次单剂量(间隔7天,每次50μl)、一次超剂量(250μl)佐剂疫苗,对虹鳟(平均体重10
±
1g)进行腹腔注射免疫,每个处理20尾。以pbs注射的虹鳟为阴性对照。免疫后每天观察虹鳟精神状态及接种部位有无异常,摄食是否正常,是否出现死亡等症状。于末次免疫后7d和14d分别从各组中随机挑选5尾虹鳟,进行解剖及肉眼观察,同时取肝、脾、肾脏,制作he染色石蜡切片,利用显微镜观察组织切片。
[0064]
二、结果与分析
[0065]
1、最佳疫苗及最佳免疫剂量
[0066]
将甲醛灭活疫苗和bpl灭活疫苗,分别与4种佐剂进行配伍,制备出佐剂灭活疫苗,采用不同的免疫剂量对虹鳟进行腹腔注射免疫,于免疫后30d进行攻毒,测定各组相对免疫保护率。在操作过程中发现,油佐剂a2制备以后粘稠度过高,颗粒过大,无法进行注射操作,因此利用剩余三种佐剂疫苗进行了免疫。结果显示:在免疫后30d,添加佐剂b的灭活疫苗的相对免疫保护率显著高于其他佐剂疫苗及裸苗(p《0.05),其中甲醛灭活的佐剂b疫苗的相对免疫保护率均显著高于bpl灭活的佐剂b疫苗(p《0.05)。10μl、50μl、100μl的免疫剂量的甲醛灭活的佐剂b疫苗的相对免疫保护率均可达88%以上。参见图1。
[0067]
2、最佳佐剂疫苗的免疫保护期
[0068]
对效果最好的甲醛灭活的佐剂b疫苗进行保护期研究,同时以不加佐剂的甲醛灭活裸苗进行对比研究。结果发现,不加佐剂的裸苗的相对免疫保护率大大低于加了佐剂b的甲醛灭活疫苗。并且随着时间的增加,裸苗的免疫保护效果急剧下降,而佐剂b甲醛灭活疫苗的相对保护率一直维持在较高水平,在免疫后120天相对免疫保护率仍然高达90%以上,而相同剂量的裸苗随着免疫后时间的增加,相对免疫保护率急剧降低,到免疫后120天时,相对免疫保护效率降到20%以下。该结果说明佐剂b显著延长了疫苗的保护期,可使疫苗保护效力维持在较高水平长达数月。参见图2。
[0069]
3、最佳佐剂疫苗的安全性
[0070]
对效果最好的甲醛灭活的佐剂b疫苗进行了免疫动物安全性研究。采用不同剂量对虹鳟进行免疫,然后对虹鳟的行为状态及组织生理变化进行了观察。通过观察发现,各组免疫虹鳟均摄食正常,精神状态正常,无任何不良反应,无任何死亡情况(图3)。于免疫后第7d和14d分别从各组中随机挑选5尾虹鳟,解剖观察状态。如图所示,一次单剂量、多次单剂量和一次超剂量方式免疫虹鳟,免疫后第7d和14d,虹鳟的各器官均正常,没有明显的损伤(图4和图5)。对各时期的肝、脾、肾组织进行石蜡切片he染色观察,结果发现与对照组相比,各剂量组的虹鳟组织均无病理变化(图6至图11)。该结果表明,该佐剂灭活疫苗对虹鳟具有理想的安全性。
[0071]
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本申
请中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1